Внебольничная инфекция что это такое
С момента открытия Alexander Fleming пенициллина до настоящего времени бета-лактамные антибиотики остаются одними из самых востребованных препаратов для лечения инфекций дыхательных путей.
Идея о том, что бета-лактамные структуры могут ингибировать продуцируемые микроорганизмами бета-лактамазы, воплотилась в жизнь в начале 70-х годов прошлого века, когда был получен первый ингибитор бета-лактамаз — клавулановая кислота [2]. В настоящее время в клинической практике доступны препараты, содержащие в своей структуре следующие ингибиторы бета-лактамаз: клавулановая кислота, сульбактам и тазобактам. Клавулановая кислота по своей структуре является производной Streptomyces clavuligeris, а сульбактам и тазобактам — полусинтетические производные пенициллановой кислоты (сульфоны) (рис.). Все ингибиторы бета-лактамаз имеют в своей структуре бета-лактамное кольцо, что обусловливает возможность образования стабильного комплекса между ингибитором и бета-лактамазой бактерий; это приводит к необратимому подавлению активности фермента и тем самым предотвращает инактивацию антибиотика.
В целом клавуланат, тазобактам и сульбактам имеют сходный спектр ингибирующей активности, однако установлено, что сульбактам имеет ряд преимуществ перед другими ингибиторами. Во-первых, сульбактам в меньшей степени индуцирует продукцию хромосомных бета-лактамаз, характеризуясь низкими темпами роста резистентности микроорганизмов [3]. Во-вторых, сульбактам обладает природной бактерицидной активностью в отношении Acinetobacter spp., Bacteroides fragilis и Neisseria gonorrhoeae [4, 5], в отношении других инфекционных агентов собственная активность ингибиторов бета-лактамаз минимальна и сопоставима между собой (табл. 1). В-третьих, сульбактам обладает значительно большей, чем клавуланат или тазобактам, устойчивостью к изменениям рН раствора. С практической точки зрения это означает, что в условиях актуального инфекционно-воспалительного процесса, протекающего со значительными вариациями кислотности среды, сульбактам активнее проникает в ткани [6]. В-четвертых, сульбактам обладает высокой степенью абсорбции в желудочно-кишечном тракте (биодоступность сульбактам пивоксила при приеме внутрь составляет 85%); в отличие от клавулановой кислоты устойчив к метаболизму и выводится преимущественно в неизмененном виде, что определяет минимальную вероятность возникновения нежелательных реакций со стороны печени и желчевыводящих путей; устойчив в водных растворах (возможность длительного хранения).
До 2005 г. в арсенале российского врача присутствовал только один препарат, содержащий сульбактам, — ампициллин/сульбактам. Однако фармакокинетические недостатки ампициллина (низкая биодоступность при приеме внутрь и др.) оказались свойственны и комбинированному препарату, что значительно ограничило применение его пероральной формы.
Амоксициллин/сульбактам демонстрирует хороший профиль безопасности — по данным метаанализа (30 исследований по оценке эффективности и безопасности антибиотика) прием препарата сопровождался развитием нежелательных явлений (НЯ) в 9,8% случаев. Чаще всего наблюдались нарушения со стороны желудочно-кишечного тракта (диарея, тошнота, рвота), гиперчувствительность и кожная сыпь, при этом большинство НЯ носили транзиторный характер и не требовали отмены препарата [11]. Несомненным преимуществом препарата является меньшая, по сравнению с амоксициллином/клавуланатом, вероятность возникновения гепатотоксических реакций, ассоциированных с приемом антибиотика.
Высокая клиническая эффективность амоксициллина/сульбактама при различных инфекциях доказана в ходе контролированных клинических исследованиях и более чем 20-летней клинической практикой. Одним из основных показаний для назначения антибиотика являются инфекции дыхательных путей (ИДП).
Антибактериальная терапия внебольничных ИДП
Острый тонзиллофарингит (ОТФ). ОТФ в большинстве случаев (30–60% у взрослых, 15–40% у детей) имеет вирусную этиологию и не требует назначения антибиотиков [12, 13]. Среди же бактериальных возбудителей ОТФ ведущая роль принадлежит бета-гемолитическому стрептококку группы А (БГСА), реже (≤ 5%) ОТФ вызывают стрептококки групп C и G, а также другие микроорганизмы [14–17]. Наибольшую опасность при стрептококковом ОТФ представляют возможные осложнения, которые подразделяются на ранние (отит, синусит, паратонзиллярный абсцесс) и поздние (острый гломерулонефрит, острая ревматическая лихорадка), что, безусловно, требует назначения антибактериальной терапии (АБТ). Клиническими маркерами бактериальной инфекции являются: передний шейный лимфаденит, лихорадка, гиперемия и экссудат на задней стенке глотки и миндалинах. Показанием для назначения АБТ служит наличие всех четырех вышеуказанных критериев. Антибиотики показаны и в том случае, если присутствуют два или три из них в сочетании с положительным результатом тестирования на наличие стрептококкового антигена. Отсутствие этих критериев или наличие одного из них делают антибиотикотерапию тонзиллофарингита недостаточно обоснованной [15, 16].
Острый синусит (ОС). ОС — воспаление слизистой оболочки носовой полости и околоносовых пазух носа, развивающееся чаще всего как осложнение острой респираторной вирусной инфекции. В большинстве случаев этиология заболевания вирусная [20]. В случае же сохранения симптомов (гнойные выделения из носа и/или в ротоглотку, лихорадка, головная боль, боль и болезненность при пальпации в проекции синусов) более 7 дней можно предположить бактериальную природу синусита. Чаще всего возбудителями являются S. pneumoniae (20–43%) и H. influenzae (22–35%), реже встречаются M. catarrhalis, БГСА, S. aureus и другие микроорганизмы [20, 21].
При легком течении ОС (если клинические симптомы сохраняются более 10 дней без улучшения или прогрессируют) у пациентов, не получавших антибиотики в предшествующие 4 недели, препаратом выбора является амоксициллин. В качестве альтернативы могут использоваться ингибиторозащищенные аминопенициллины или цефуроксим аксетил [22].
Острый средний отит (ОСО). ОСО — воспаление среднего уха, обычно возникающее как осложнение вирусных инфекций дыхательных путей. О распространенности заболевания говорят следующие данные — только в США с развитием ОСО у взрослых пациентов ежегодно связаны около 31 млн обращений за медицинской помощью и 20–25% назначений антибиотиков [24]. Чаще всего ОСО имеет бактериальную этиологию, основные возбудители — S. pneumoniae и H. influenzae (60–80% всех случаев заболевания). Редкими возбудителями ОСО являются M. catarrhalis, БГСА, S. aureus [25]. До настоящего времени тактика ведения пациентов с ОСО остается неоднозначной, так как заболевание имеет склонность к самоизлечению без проведения антибиотикотерапии, в особенности если возбудителем является M. catarrhalis или H. influenzae. Однако саморазрешение ОСО, вызванного S. pneumoniae, отмечается менее чем в 20% случаев, при этом пневмококковая инфекция обусловливает ряд серьезных осложнений заболевания, таких как бактериальный менингит, абсцесс мозга, тромбоз сигмовидного синуса, лабиринтит, парез лицевого нерва, сепсис. В этой связи целесообразность назначения антибиотиков при ОСО требует тщательного анализа степени тяжести и длительности сохранения клинических симптомов заболевания. При появлении первых признаков болезни рекомендована выжидательная тактика: назначение симптоматической терапии и динамическое наблюдение за состоянием пациента в течение ближайших 24 ч. Абсолютными показаниями к применению антибиотиков считаются возраст до 2 лет, тяжелые формы ОСО, сопровождающиеся выраженным болевым синдромом, температурой тела выше 38°C и сохранением симптомов более одних суток. Препаратом выбора при ОСО является амоксициллин. В случае отсутствия положительного эффекта (сохранение клинических симптомов и отоскопической картины ОСО) по прошествии 3 дней терапии рекомендуется отмена амоксициллина и назначение ингибиторозащищенных аминопенициллинов или цефуроксима аксетила внутрь либо 3-дневное назначение цефтриаксона в/м. В качестве альтернативы амоксициллину (особенно у детей, часто получающих АБТ) предлагается использование амоксициллина/сульбактама либо клавуланата, цефуроксима аксетила или цефтриаксона в качестве препаратов первого ряда. Продолжительность антибактериальной терапии при ОСО составляет 7–10 дней [26, 27].
Эпиглоттит — быстро прогрессирующее воспаление надгортанника и окружающих тканей, которое может привести к полной обструкции дыхательных путей. Чаще всего встречается у мальчиков 2–4 лет. Клиническими симптомами заболевания являются: боль в горле, лихорадка, дисфония и дисфагия при отсутствии видимых изменений со стороны ротоглотки. Основной возбудитель эпиглоттита — H. influenzae типа В, реже (у взрослых пациентов) — S. pneumoniae, БГСА, S. aureus и анаэробы [27, 28]. Лечение эпиглоттита направлено на поддержание проходимости дыхательных путей (трахеостомия, интубация эндотрахеальной или назотрахеальной трубками) и эрадикацию H. influenzae. Препаратами выбора являются ингибиторозащищенные пенициллины, цефалоспорины II (цефуроксим), III (цефотаксим, цефтриаксон) или IV поколений (цефепим). Рекомендован внутривенный путь введения (возможна ступенчатая терапия), длительность антибиотикотерапии составляет 7–10 дней [28].
Обострение хронической обструктивной болезни легких (ХОБЛ). По современным представлениям до 75–80% обострений ХОБЛ имеют инфекционную природу и наиболее вероятными возбудителями обострения заболевания являются H. influenzae, S. pneumoniae и M. catarrhalis, удельный вес которых, по данным различных исследователей, составляет 13–46%, 7–26% и 9–20% соответственно. Реже выделяются H. parainfluenzae, S. aureus, P. aeruginosa и представители семейства Enterobacteriaceae [29].
Классическими признаками, характеризующими обострение заболевания, являются: появление или усиление одышки; увеличение объема отделяемой мокроты; усиление гнойности мокроты. Наличие всех трех вышеуказанных критериев описывается как I тип, двух из них — как II тип, одного — как III тип обострения заболевания [30]. Показаниями для назначения АБТ являются: обострение ХОБЛ I типа; обострение ХОБЛ II типа при наличии гнойной мокроты; тяжелое обострение ХОБЛ, требующее проведения респираторной поддержки.
Важнейшее значение имеет разделение на простое (неосложненное) и осложненное обострение ХОБЛ. В первом случае у пациентов отсутствуют факторы риска неэффективности антибиотикотерапии и для этой категории больных наиболее вероятными возбудителями являются H. influenzae, M. сatarrhalis, H. parainfluenzae, S. pneumoniae с природным уровнем чувствительности к антибиотикам. В качестве препаратов выбора рекомендуются амоксициллин или современные макролиды (азитромицин, кларитромицин). Альтернативой им является применение ингибиторозащищенных пенициллинов (амоксициллин/клавуланат) и респираторных фторхинолонов.
Внебольничная пневмония (ВП). В настоящее время ингибиторозащищенные аминопенициллины являются препаратами выбора в лечении нетяжелой ВП у амбулаторных больных в возрасте старше 60 лет и/или при наличии сопутствующих заболеваний (хронический бронхит/ХОБЛ, сахарный диабет, застойная сердечная недостаточность, хроническая почечная недостаточность, заболевания печени, дистрофия) [31]. Именно у такого рода пациентов заболевание возникает в результате влияния пенициллинорезистентных S. pneumoniae, а также H. influenzae, S. aureus и грамотрицательных бактерий семейства Enterobacteriaceae.
Ингибиторозащищенные аминопенициллины являются препаратами первого ряда у пациентов, злоупотребляющих алкоголем, страдающих сахарным диабетом. Кроме того, амоксициллин/сульбактам либо клавуланат применяются в режиме монотерапии или в комбинации с макролидом для лечения пневмонии у лиц, проживающих в домах престарелых [32].
Эффективность амоксициллина/сульбактама при лечении взрослых и детей с ВП продемонстрирована в ходе многих клинических исследований. Так, например, согласно результатам многоцентрового исследования, участниками которого стали 84 пациента с ВП, клиническая эффективность ингибиторозащищенного аминопенициллина, применявшегося в дозе 1000 мг (875 мг амоксициллина и 125 мг сульбактама) 2 раза в сутки в течение 7 дней составила 97,4%. Следует отметить, что у 6,5% пациентов, включенных в исследование, была диагностирована пневмококковая бактериемия [33].
Российские врачи также обладают опытом применения препарата при ВП. В собственном исследовании изучалась эффективность и безопасность амоксициллина/сульбактама при лечении нетяжелой ВП у пациентов старше 60 лет и/или у больных с сопутствующими заболеваниями (хронический бронхит, сахарный диабет, застойная сердечная недостаточность и др.). В исследование было включено 27 больных ВП, средний возраст которых составил 61,7 ± 5,1 года. По данным исследования амоксициллин/сульбактам продемонстрировал высокую клиническую (92,6%) и бактериологическую эффективность (88,9%), наряду с хорошим профилем безопасности — частота НЯ составила 14,8% [34].
Абсцесс легкого. Более чем в половине случаев возникновение заболевания обусловлено анаэробными микроорганизмами — Fusobacterium nucleatum, Peptostreptococcus spp., Bacteroides spp., в остальных случаях выделяют ассоциации анаэробных и аэробных микроорганизмов (в первую очередь — K. pneumoniae и K. оxytoca, существенно меньшее значение имеют S. aureus, H. influenzae и S. pneumoniae). Общепринятым стандартом в лечении абсцесса легкого до настоящего времени остается применение бензилпенициллина по 2 млн ЕД внутривенно с интервалом 4 часа в комбинации с метронидазолом; в последующем, при достижении отчетливого клинико-рентгенологического улучшения, осуществляется переход на пероральную терапию амоксициллином и метронидазолом внутрь [35]. Однако слабой стороной такой терапии является тот факт, что 15–20% штаммов потенциальных возбудителей абсцесса легкого оказываются резистентными к бензилпенициллину (прежде всего, это фузобактерии и бактероиды). Кроме того, на сегодняшний день доказанным является преимущество линкосамидов (клиндамицин по 600 мг в/в с интервалом 6–8 ч с последующим переходом на прием антибиотика внутрь по 300 мг с интервалом 6 ч) по сравнению с традиционной терапией бензилпенициллином. В связи с этим российские эксперты в качестве препаратов выбора для эмпирической терапии абсцесса легкого рекомендуют ингибиторозащищенные аминопенициллины (амоксициллин/клавуланат, ампициллин/сульбактам) либо цефоперазон/сульбактам. При отсутствии этих антибиотиков либо их неэффективности могут использоваться карбапенемы, другие ингибиторозащищенные пенициллины (тикарциллин/клавуланат, пиперациллин/тазобактам) либо комбинации клиндамицина с аминогликозидами [36].
Эмпиема плевры. В этиологии заболевания ведущую роль занимают грамотрицательные бактерии (15–32%) и анаэробы (5–19%) — так называемая подострая/хроническая эмпиема плевры. На долю S. aureus приходится от 7 до 15% случаев, S. pneumoniae выделяется у 5–7% больных, еще реже встречается H. influenzae — острая, постпневмоническая эмпиема. В 20–25% случаев обнаруживают микробные ассоциации, прежде всего, анаэробов и аэробов, представленных грамотрицательными бактериями [37]. В большинстве случаев проводится именно целенаправленная антибактериальная терапия с учетом данных микробиологического исследования содержимого плевральной полости. Однако если гнойный выпот оказывается стерильным, назначаются антибиотики, активные в отношении вероятных возбудителей острой постпневмонической эмпиемы плевры, это, прежде всего, S. pneumoniae, S. pyogenes, S. aureus и H. influenzae. В данной клинической ситуации целесообразно применение цефалоспоринов II–IV поколения (цефотаксим, цефтриаксон, цефепим).
По вопросам литературы обращайтесь в редакцию.
А. А. Зайцев, кандидат медицинских наук
Е. В. Колобанова
А. И. Синопальников, доктор медицинских наук, профессор
ГИУВ МО РФ, Москва
В США, по оценкам Центров контроля и профилактики заболеваний, около 1,7 миллиона случаев внутрибольничных инфекций, вызванных всеми типами микроорганизмов, приводят или сопутствуют 99 000 смертям ежегодно.
В Европе, по результатам проведенных госпитальных исследований, смертность от внутрибольничных инфекций составляет 25 000 случаев в год, из них две трети вызваны грам-отрицательными микроорганизмами.
В России фиксируется около 30 тысяч случаев ежегодно, что свидетельствует о недостатках статистики. [3]
Внутрибольничными агентами могут вызываться тяжёлые пневмонии, инфекции мочевыводящих путей, крови и других органов.
Для ВБИ характерны свои особенности эпидемиологии, отличающие ее от классических инфекций. К ним относятся: своеобразие механизмов и факторов передачи, особенности течения эпидемиологического и инфекционного процессов, важная роль медицинского персонала ЛПУ в возникновении, поддержании и распространении очагов ВБИ.
Многие типы инфекций трудно поддаются лечению по причине антибиотикорезистентности, которая постепенно начинает распространяться и среди грам-отрицательных бактерий, опасных для людей во внебольничной среде [4] .
Для возникновения ВБИ необходимо наличие следующих звеньев инфекционного процесса:
- источник инфекции (хозяин, пациент, медработник);
- возбудитель (микроорганизм);
- факторы передачи [5]
- восприимчивый организм
Источниками в большинстве случаев служат:
- медицинский персонал;
- носители скрытыми формами инфекции;
- больные с острой, стёртой или хронической формой инфекционных заболеваний, включая раневую инфекцию;
Посетители стационаров очень редко бывают источниками ВБИ [1] .
Факторами передачи чаще всего выступают пыль, вода, продукты питания, оборудование и медицинские инструменты.
Ведущими путями заражения в условиях ЛПУ являются контактно-бытовой, воздушно-капельный и воздушно-пылевой. Также возможен парентеральный путь (характерно для гепатитов В, С, D и др.)
Механизмы передачи инфекции: аэрозольный, фекально-оральный, контактный, гемоконтактный [5] .
К факторам внутрибольничной среды, способствующим распространению ВБИ относятся:
- недооценка эпидемической опасности внутрибольничных источников инфекции и риска заражения при контакте с пациентом;
- перегрузка ЛПУ;
- наличие невыявленных носителей внутрибольничных штаммов среди медперсонала и пациентов;
- нарушение медперсоналом правил асептики и антисептики, личной гигиены;
- несвоевременное проведение текущей и заключительной дезинфекции, нарушение режима уборки;
- недостаточное оснащение ЛПУ дезинфекционными средствами;
- нарушение режима дезинфекции и стерилизации медицинских инструментов, аппаратов, приборов и т. д.;
- устаревшее оборудование;
- неудовлетворительное состояние пищеблоков, водоснабжения;
- отсутствие фильтрационной вентиляции.
Лица с повышенным риском заражения ВБИ:
- Больные:
- без определенного места жительства, мигрирующее население,
- с длительными не долеченными хроническими соматическими и инфекционными заболеваниями,
- не имеющие возможность получать специальную медицинскую помощь;
- Лица, которым:
- назначена терапия, подавляющая иммунную систему (облучение, иммунодепрессанты);
- проводятся обширные хирургические вмешательства с последующей кровезаместительной терапией, программный гемодиализ, инфузионная терапия;
- Родильницы и новорождённые, особенно недоношенные и переношенные;
- Дети с врождёнными аномалиями развития, родовой травмой;
- Медперсонал ЛПУ.
Этиология
Всего насчитывается более 200 агентов, которые могут быть причиной ВБИ. До появления антибиотиков основными из них были стрептококки и анаэробные палочки. Однако после начала клинического применения антибиотиков возбудителями основных ВБИ стали ранее непатогенные (или условно-патогенные) микроорганизмы: St. aureus, St. epidermidis, St. saprophiticus, Escherichia coli, Enterococcus faecalis, Enterococcus durans, Klebsiella sp., Proteus mirabilis, Providencia spp, Acinetobacter, Citobacter, Serratia marcescens.
Так же установлено, что внутрибольничное инфицирование может быть связано с распространением ротавирусной, цитомегаловирусной инфекции, кампилобактера, вирусов гепатита В, С и D, а также ВИЧ-инфекции.
В результате циркуляции микроорганимов в отделении происходит их естественный отбор и мутация с образованием наиболее устойчивого госпитального штамма, являющегося непосредственной причиной ВБИ.
Основные черты приспособления — это устойчивость к одному или нескольким антибиотикам широкого спектра действия, устойчивость в условиях внешней среды, снижение чувствительности к антисептикам. [6] . Госпитальные штаммы очень разнообразны, в каждой больнице или отделении возможно появление своего характерного штамма со свойственным только ему набором биологических свойств.
Классификация
- В зависимости от путей и факторов передачи ВБИ классифицируют:
- Воздушно-капельные (аэрозольные)
- Вводно-алиментарные
- Контактно-бытовые
- Контактно-инструментальные
- Постинъекционные
- Постоперационные
- Послеродовые
- Посттрансфузионные
- Постэндоскопические
- Посттрансплантационные
- Постдиализные
- Постгемосорбционные
- Посттравматические инфекции
- Другие формы.
- От характера и длительности течения:
- Острые
- Подострые
- Хронические.
- По степени тяжести:
- Тяжелые
- Средне-тяжелые
- Легкие формы клинического течения.
- В зависимости от степени распространения инфекции:
- Генерализованные инфекции: бактериемия (виремия, микемия), септицемия, септикопиемия, токсико-септическая инфекция (бактериальный шок и др.).
- Локализованные инфекции
- Инфекции кожи и подкожной клетчатки (ожоговых, операционных, травматический ран, Постинъекционные абсцессы, омфалит,рожа, пиодермия, абсцесс и флегмона подкожной клетчатки, парапроктит, мастит, дерматомикозы и др.);
- Респираторные инфекции (бронхит, пневмония, легочный абсцесс и гангрена, плеврит, эмпиема и др.);
- Инфекции глаза (конъюнктивит, кератит, блефарит и др.);
- ЛОР-инфекции (отиты, синуситы, ринит, мастоидит, ангина, ларингит, фарингит, эпиглоттит и др.);
- Стоматологические инфекции (стоматит, абсцесс, др.);
- Инфекции пищеварительной системы (гастроэнтероколит, энтерит, колит, холецистит, гепатиты, перитонит, абсцессы брюшины и др.);
- Урологические инфекции (бактериурия, пиелонефрит, цистит, уретрит, др.);
- Инфекции половой системы (сальпингоофорит, эндометрит, др.);
- Инфекции костей и суставов (остеомиелит, инфекция сустава или суставной сумки, инфекция межпозвоночных дисков);
- Инфекции ЦНС (менингит, абсцесс мозга, вентрикулит и др.);
- Инфекции сердечно-сосудистой системы (инфекции артерий и вен, эндокардит, миокардит, перикардит, постоперационный медиастинит).
Профилактика
Профилактика внутрибольничных инфекций является сложным и комплексным процессом, который должен включать три составляющие:
- минимизация возможности заноса инфекции извне;
- исключение распространение инфекции между больными внутри учреждения;
- исключение выноса инфекции за пределы ЛПУ.
Лечение
Примечания
Wikimedia Foundation . 2010 .
ВНУТРИБОЛЬНИЧНЫЕ ИНФЕКЦИИ — ВНУТРИБОЛЬНИЧНЫЕ ИНФЕКЦИИ, заразные заболевания, к рые возникают среди б ных в больничных учреждениях. Наиболее частым источником В. и. являются б ные, поступающие в б цу в инкубационном периоде. Особенно это относится к б ным со смешанными… … Большая медицинская энциклопедия
ВНУТРИБОЛЬНИЧНЫЕ ИНФЕКЦИИ — (син: нозокомиальные инфекции) – инфекционные болезни и раневые инфекции, присоединившиеся в стационаре к основному заболеванию, а также заболевания медработников, возникшие в связи с лечением и уходом за инфекционными больными. Источником… … Энциклопедический словарь по психологии и педагогике
инфекции нозокомиальные — (лат. nosocomialis больничный) см. Инфекции внутрибольничные … Большой медицинский словарь
Инфекции внутрибольничные послеоперационные — 2.6. К внутрибольничным послеоперационным инфекциям относятся заболевания, возникающие в течение 30 дней после оперативного вмешательства, а при наличии имплантата в месте операции до года. Источник: Постановление Главного государственного… … Официальная терминология
Ятрогенные инфекции — (внутрибольничные инфекции, госпитальные инфекции, нозокомиальные инфекции) любые инфекц. и паразитарные заболевания пациентов и мед работников, заражение к рыми происходит в процессе оказания мед. помощи в больничных стационарах, амбулаторно… … Словарь микробиологии
Стафилококковые инфекции — острые и хронические, локализованные и генерализованные инфекции, обусловленные стафилококками. Большинство случаев С.и. вызывается S. aureus, но их возбудителями могут быть также S. epidermidis, S. saprophiticus и др виды коагулазоотрицательных… … Словарь микробиологии
Пневмония — I Пневмония (pneumonia; греч. pneumon легкое) инфекционное воспаление легочной ткани, поражающее все структуры легких с обязательным вовлечением альвеол. Неинфекционные воспалительные процессы в легочной ткани, возникающие под влиянием вредных… … Медицинская энциклопедия
Внутрибольни́чные инфе́кции — (синоним нозокомиальные инфекции) инфекционные болезни, связанные с пребыванием, лечением, обследованием и обращением за медицинской помощью в лечебно профилактическое учреждение. Присоединяясь к основному заболеванию, В. и. ухудшает течение и… … Медицинская энциклопедия

Общие сведения
Частота регистрации ИСМП в разных странах варьирует в широких пределах. Так, в РФ этот показатель составляет 1-1,5% (40-60 тыс. случаев/год), США — 3-5 % (2,5 млн. случаев/год), Великобритании — 5-6 %, Германии —3,5 %, Китае — 7-8 %. Однако, эти показатели, особенно в странах СНГ и, в частности, России не отражают реальную эпидемиологическую ситуацию. Результаты научных исследований ведущих специалистов-эпидемиологов РФ свидетельствуют, что реальное количество ИСМП составляет в среднем около 10% и находится на уровне 2-2,5 миллионов случаев/год. Присоединение ИСМП к основному заболеванию увеличивает продолжительности лечения (пребывания в стационаре) пациента на 7-10 дней, а прямые затраты лечебных учреждений на 65-85 млрд рублей в год. Летальность при различных нозологических формах ИСМП варьирует в пределах 3,5-35%.
Наибольший удельный вес ИСМП приходится на хирургические и акушерские стационары (отделения травматологии, урологии, реанимации, абдоминальной хирургии, гинекологии, ожоговой травмы, стоматологии, отоларингологии, онкологии). Наиболее драматичны проявления ИСМП в отделениях интенсивной терапии и реанимации, где они в различных нозологических формах регистрируются в 25-30% случаев.
Патогенез
Патогенез внутрибольничных инфекций существенно различается и определяется видом заболевания, этиологическим фактором (видом возбудителя, факторами его вирулентности), механизмом и путями передачи инфекции.
Классификация
Прежде всего, различают две больших группы ИСМП (рис. ниже):
- Экзогенная инфекция — обусловлена заражением пациента инфекционным агентом в условиях посещения/нахождения в ЛПУ.
- Эндогенная инфекция — инфекции, вызванных условно-патогенными микроорганизмами, вегетирующими в пищеварительном тракте, на кожных и слизистых покровах, которые при неблагоприятных условиях становятся патогенными. В структуре ВБИ роль эндогенной инфекции незначительна.
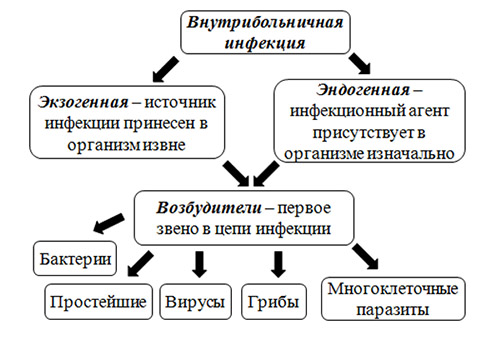
Группы и этиологический фактор ИСМП
В основу классификации ВБИ положены различные факторы. В зависимости от путей/факторов передачи различают воздушно-капельные, контактно-бытовые, контактно-инструментальные, постоперационные, постинфекционные, постэндоскопические, послеродовые, посттрансфузионные, постдиализные, посттравматические, постгемосорбционные и другие инфекции.
В зависимости от степени распространения инфекции различают:
- Генерализованные: бактериемия, септицемия, септикопиемия, токсико-септическая инфекция.
- Локализованные инфекции, включающие:
- Респираторные инфекции (ОРЗ, бронхит, плеврит, пневмония, легочный абсцесс и др.).
- Инфекции подкожной клетчатки/кожи (послеожоговые, послеоперационные, послетравматические), дерматомикозы, постинъекционные — абсцессы/флегмоны подкожной.
- Стоматологические инфекции (абсцесс, стоматит).
- ЛОР-инфекции (ринит, отиты, синуситы, ангина, ларингит, фарингит).
- Урологические инфекции.
- Инфекции пищеварительного тракта (энтерит, колит, гастроэнтероколит, холецистит, гепатиты др.).
- Постоперационные инфекции (перитонит, абсцессы брюшины).
- Инфекции глаза (конъюнктивит).
- Инфекции урологической и половой системы (пиелонефрит, уретрит, цистит, бактериурия, эндометрит, сальпингоофорит).
- Инфекции костно-cуставного аппарата (остеомиелит, бурсит, артрит).
- Инфекции сердечно-сосудистой системы (миокардит, эндокардит, перикардит, инфекции артерий и вен).
- Инфекции ЦНС (менингит).
- По характеру течения: острые, подострые, хронические. По тяжести течения: легкие, тяжёлые и среднетяжелые.
Причины
Этиологическим фактором ИСМП может быть чрезвычайно широкий спектр микроорганизмов (около 250 видов), принадлежащих к разным таксономическим группам: бактерии, вирусы, простейшие, грибы. При этом, инфекционным агентом могут быть патогенные, условно-патогенные микроорганизмы, а в ряде случаев и сапрофитная микрофлора. Наибольшей удельный вес в этиологической структуре ИСМП принадлежит возбудителям гнойно-септических инфекций (80-85%), кишечных инфекций (8-10%), вирусам гепатитов В, С, D (6-7%), инфекции дыхательных путей (2-3%). В целом, структура ВБИ изменчива и зависит преимущественно от профиля отделения/вида стационара и микробного пейзажа конкретного лечебного отделения (рисунок ниже).
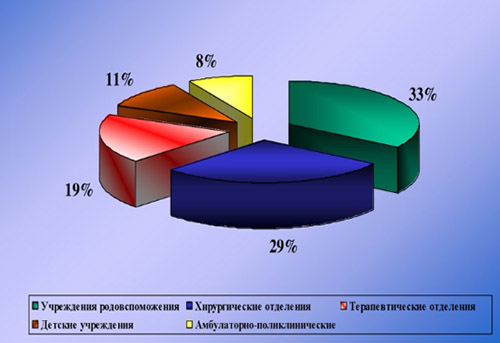
К возбудителям ВБИ, имеющими наибольшее значение относятся:
- грамположительная флора: стафилококки (золотистый, эпидермальный), стрептококки (пневмококк, энтерококк, пиогенный стрептококк);
- грамотрицательная флора: энтеробактерии (эшерихия, сальмонелла, шигелла, синегнойная палочка, клебсиелла, протей, иерсиния).
- вирусы (аденовирусной инфекции, простого герпеса, кори, ветряной оспы, гриппа, парагриппа, респираторно-синцитиальной инфекции, эпидпаротита, ротавирусы, риновирусы, энтеровирусы, возбудители вирусных гепатитов);
- грибы (рода Candida, аспергиллы).
Значимость различных видов ИСМП во многом определяется профилем ЛУ. Так, в гинекологических и родильных отделениях ведущую роль играет стафилококковая инфекция (золотистый стафилококк), кишечная палочка, энтерококки, диплоидный грибок (молочница); в ожоговых стационарах — синегнойная инфекция; в урологических отделениях — грамотрицательная микрофлора: кишечная, синегнойная палочка; в детских отделениях — вирусы краснухи, кори, эпидемического паротита, ветряной оспы.
Формирование госпитального штамма (с приобретенной устойчивостью) обеспечивается за счет их преимущества (доминирования) перед другими представителями микробной популяции. Основными отличиями госпитального штамма микроорганизма от стандартного являются: повышенная вирулентность (патогенность), формирующаяся за счет многократного пассажа через организм больных ЛПУ, высокая устойчивость к воздействию неблагоприятных факторов (дезинфектантам, антисептикам, химиопрепаратам, применяемым в конкретном мед. учреждении) и способность к длительному выживанию, постоянная циркуляция в среде больничного стационара среди больных и персонала.
Основную массу всех форм ВБИ (около 80%) составляют:
- инфекции мочевыделительной системы;
- ОРЗ и вентилятор-ассоциированные пневмонии;
- послеоперационные раневые гнойно-септические инфекции;
- кожные инфекции;
- интраабдоминальные инфекции;
- ангиогенные катетер-ассоциированные инфекции.
Любая нозологическая форма ВБИ развивается только при наличии всех звеньев эпидемического процесса: источника инфекции, механизма (факторов) передачи и восприимчивого организма человека.
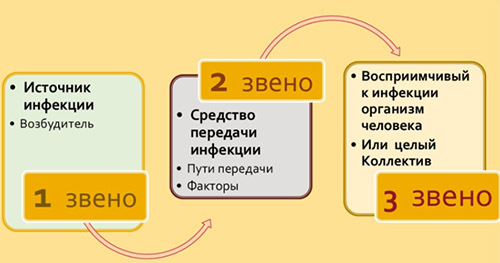
Основные источники внутрибольничной инфекции:
- больные и носители, находящиеся в стационаре;
- персонал лечебных учреждений;
- лица, ухаживающие за больными и посетители стационаров (студенты, лица, навещающие пациентов).
Аэрогенный — процесс заражения осуществляется через воздушную среду. Выделяют:
- воздушно-капельный путь (этим путем возбудитель передается при большинстве ОРЗ, пневмониях) при разговоре, кашле;
- воздушно-пылевой путь (передаются заболевания, возбудитель которых устойчив во внешней среде — кишечные инфекции, туберкулез, зоонозы).
- Контактно-бытовой путь – инфекционный агент передается через грязные рук, предметы личной гигиены, игрушки, посуду.
- Пищевой (реализуется через зараженные продукты питания при нарушениях технологии приготовления или хранения готовых блюд и пищевых продуктов).
- Водный (через воду).
- Прямой — передача возбудителя непосредственно через физический контакт между резервуаром инфекции (инфицированный индивидуум/контаминированный предмет) с кожей, слизистой или раневой поверхностью восприимчивого организма человека.
- Непрямой — посредством механического переноса инфекционного агента через руки медицинского персонала, предметы обихода, инструменты и оборудование лечебного учреждения. Непрямой контакт является наиболее часто задействованным путем распространения. Этот путь передачи часто называют артифициальным (искусственным) или парентеральным путем передачи возбудителя, который реализуется путем проведения различных инвазивных манипуляций (инъекции, забор крови, инструментальные манипуляции, вакцинацию, местные/общие операции) или использовании специальной аппаратуры при проведении гемодиализа, ИВЛ.
- Гемоконтактный — передается через кровь при обширных хирургические вмешательствах, инфузионной терапии, программном гемодиализе.
Заболеваемость ИСМП носит преимущественно эндемический характер и обусловлена индивидуальными факторами риска и клиническими процедурами. Значительно реже ИСМП протекают в виде локальных эпидемий. Развитию эпидемических вспышек способствует несвоевременная диагностика стертых форм заболевания и выявление носителей инфекционных агентов, как среди поступающих пациентов, так и среди медицинского персонала, контаминация предметов общего пользования, систематическое нарушение методов асептики при выполнении инструментальных процедур.
Специфичны для каждого вида инфекционного возбудителя. Однако, в целом для большинства нозологических форм ИСМП определяющими факторами являются параметры, характеризующие организм хозяина:
- возраст (пожилой/старческий, дети — новорожденные и раннего возраста, особенно недоношенные, со сниженной сопротивляемостью организма и перенесшие родовую травму);
- пациенты, страдающие тяжелыми хроническими заболеваниями, с алиментарной дистрофией;
- длительно находящиеся в стационаре и особенно на постельном режиме;
- беременные/роженицы;
- пациенты, получающие лучевую/иммуносупрессивную терапию;
- имунноскомпрометированные лица;
- больные после обширных хирургических операций, получающие кровезаместительную/инфузионную терапию, с программным гемодиализом, находящиеся на ИВЛ.
Факторы риска ИСМП, связанные с предметами окружающей среды (загрязнение поверхностей, воздуха, воды в распространении инфекции) имеют меньшую значимость.
Возникновению и распространению ИСМП способствуют:
Симптомы
Симптоматика внутрибольничных инфекций определяется конкретной нозологической формой и симптомами основного заболевания, формой и тяжестью их течения, вирулентностью инфекционного агента и состоянием организма больного.
Анализы и диагностика
К ВБИ относятся случаи, отвечающие следующим критериям:
- Повторное поступление пациента в стационар с установленной инфекцией (с клиническими признаками, данными инструментальных и лабораторных методов исследовани — микробиологических, серологических и методов экспресс-диагностики), являющееся следствием предыдущей госпитализации.
- Период развития клинической симптоматики заболевания ВБИ после поступления в лечебный стационар должен составлять не менее 48 часов и более.
- Выявляется четкая взаимосвязь между симптоматикой заболевания и проведенными вмешательства инвазивного типа (после ингаляции, инъекций, перевязки и т.д.) или в ряде случаев — с выявленным источником инфекционного агента (поступивший больной со стертой формой заболевания/носитель) и фактором ее распространения.
Для точной диагностики заболевания и определения конкретного штамма возбудителя инфекции, требуется проведение лабораторных—бактериологических/серологических исследований различных биоматериалов (мазок из зева, мокрота, кровь, моча, кал, раневое отделяемое).
Лечение
Проблема лечения госпитальных инфекций представляет значительную трудность, что обусловлено неэффективностью большинства широко применяемых антибиотиков, в частности цефалоспоринов. Для лечения таких инфекций применяются карбапенемы (Меропенем, Дорипенем), имеющие широкий спектр антимикробной активности, в частности к микроорганизмам, устойчивым к пенициллинам/цефалоспоринам или в ряде случаев комбинированные лекарственные препараты пенициллинов с ингибиторами бета-лактамаз (Пиперациллин + Тазобактам, Тикарциллин, Амоксициллин-Клавуланат и др.).
Карбапенемы используются для лечения тяжелых нозокомиальных пневмоний и других инфекций верхних дыхательных путей; инфекций органов малого таза, гинекологических, абдоминальных, мочеполовых инфекций; кожи и мягких тканей; сепсиса. Однако, препараты этой группы могут вызывать побочные реакции в виде крапивницы, сыпи, диспепсических расстройств, поражения печени и почек, дисбактериоза.
При выявлении метициллинрезистентных штаммов золотистого стафилококка, являющегося частым возбудителем внутрибольничных резистентных стафилококковых инфекций для лечения, используются гликопептидные антибиотики (Ванкадицин, Тейкопланин-Тева, Ликованум, Таргоцид и др.), которые высокоактивны по отношению к грамположительным аэробным/анаэробным инфекционным агентам — стафилококкам, стрептококкам, пневмококкам, энтерококкам, клостридиям, листериям, коринебактериям и другим. Показаниями к назначению являются тяжелые инфекции, вызванные энтерококками, инфекционный эндокардит, ассоциированный с зеленящими стрептококками, менингит и пневмонии, вызванные пневмококком, катетер-ассоциированный сепсис, перитонит, антибиотик-ассоциированная диарея и других инфекций, угрожающих жизни. В ряде случае гликопептидные антибиотики сочетаются с цефалоспоринами 3 поколения (Цефтибутен, Цефиксим, Цефотаксим, Цефоперазон, Цефтазидим и др.) или фторхинолонами (Офлоксацин, Ципрофлоксацин, Пефлоксацин, Норфлоксацин, Левофлоксацин и другие).
Необходимо отметить, что спектр возбудителей внутригоспитальных осложнений, а также их антибиотикорезистентность существенно различаются в отделениях различного профиля, поэтому при выборе антибиотика следует ориентироваться на чувствительность выделенной микрофлоры к ним, в также учитывать эпидемиологическую ситуацию в каждом конкретном лечебном учреждении.
Кроме антибиотикотерапии назначается специфическое лечение при той или иной конкретной нозологической форме ВБИ с учетом клинических проявлений, тяжести течения, риска развития осложнений. В индивидуальном порядке проводится симптоматическое лечение. В качестве дополнительной терапии назначают иммуностимуляторы: интерферон; бактериофаги, витаминно- минеральные комплексы.
В настоящее время для борьбы с тяжелыми проявлениями ВБИ разработана стратегия деэскалационной терапии, базирующаяся на нескольких принципах:
- Безотлагательное начало проведения антибактериальной терапии.
- Выбор антимикробных препаратов (АМП) с учетом чувствительности микроорганизмов и способности проникать в ткани, при отсутствии таких данных — использование антибиотиков широкого спектра действия.
- Назначение высоких доз антибиотиков, подбираемых индивидуально.
Эта стратегия предполагает безотлагательное назначение стартового антибиотика широкого спектра действия (комбинации антибиотиков) с целью максимально полного охвата спектра вероятных возбудителей с последующим переходом на антибиотик, к которому отсутствует устойчивость согласно данным микробиологического исследования. Именно своевременная и адекватная антимикробная терапия является ключевым условием и благоприятным прогностическим фактором, увеличивающей вероятность благоприятного исхода заболевания.
Читайте также:
- Инфекция комаровский 6 месяцев
- Значение иммунитета при инфекционных заболеваниях
- Скарлатина предупреждение внутрибольничный инфекций
- Профилактика инфекций дыхательных путей у детей
- Инфекция на стенках аквариума
 Пожалуйста, не занимайтесь самолечением!При симпотмах заболевания - обратитесь к врачу.
Пожалуйста, не занимайтесь самолечением!При симпотмах заболевания - обратитесь к врачу.

