Что такое активная репликация вируса
Комплексное исследование при подтвержденном вирусном гепатите В (HBV). Анализ маркеров инфекции позволяет установить клиническую стадию заболевания, иммунологический статус обследуемого, а также оценить эффективность лечения. Включает в себя определение белков вируса (антигенов), основных классов специфических антител, а также обнаружение ДНК вируса в крови.
Какой биоматериал можно использовать для исследования?
Как правильно подготовиться к исследованию?
- Исключить из рациона жирную пищу в течение 24 часов до исследования.
- Не курить за 30 минут до исследования.
Общая информация об исследовании
Вирусный гепатит B (HBV) – инфекционное заболевание, которое является причиной серьёзных поражений печени. Зачастую гепатит B переходит в хроническую форму, его течение становится затяжным и провоцирует возникновение цирроза и рака печени.
Вирус гепатита B (Hepadnaviridae) содержит двухцепочечную ДНК, окруженную нуклеокапсидом размером 27 нм, в состав которого входит антиген HBcAg, и внешней оболочкой, содержащей антиген HBsAg. Этот антиген обнаруживается в крови за 6 недель до появления симптомов заболевания и может выявляться длительное время как при их наличии, так и в при их отсутствии (при хроническом гепатите и носительстве). На ранних стадиях заболевания присутствует у 90-95 % больных.
Особенностью вируса гепатита B является то, что он поступает непосредственно в кровь и циркулирует в ней на протяжении всего периода заболевания. У некоторых пациентов вирус в крови сохраняется всю жизнь. По этой причине источником заражения могут стать не только те, кто болен гепатитом в его острой форме, но также те, кто уже перенес данное заболевание, а также люди, у которых заболевание не проявляется, однако они являются носителями вируса.
Полное выздоровление регистрируется у 92-95 % больных острым гепатитом В, и лишь у 5-8 % из них отмечается переход заболевания в хроническую форму.
Гепатит B лечится исключительно в условиях стационара. Это заболевание в случае длительного течения является фактором риска развития первичной гепатоцеллюлярной карциномы (рак печени).
В жизнедеятельности вируса гепатита В различают две фазы: фазу репликации и фазу интеграции. В фазе репликации происходит воспроизведение (размножение) вируса. ДНК вируса проникает в ядро гепатоцита, где с помощью ДНК-полимеразы синтезируется нуклеокапсид, содержащий ДНК вируса, антигены HBcAg, HBeAg, которые являются основной мишенью иммунной системы. Затем нуклеокапсид мигрирует из ядра в цитоплазму, где реплицируются белки внешней оболочки (HBsAg), и, таким образом, происходит сборка полного вириона. При этом избыток HBsAg, не использованный для сборки вируса, через межклеточное пространство попадает в кровь. Полная сборка (репликация) вируса заканчивается презентацией его растворимого нуклеокапсидного антигена – HBeAg на мембране гепатоцита, где происходит его "узнавание" иммуноцитами. Антиген HBcAg серологическими методами не определяется, потому что отсутствует в крови в свободном виде. Определяется наличие в крови антител (anti-HBc) к этому антигену, вырабатывающихся вследствие его высокой иммуногенности.
Маркерами фазы репликации вируса гепатита В являются:
- выявление в крови антигенов HBeAg и anti-HBc (Ig M).
У 7-12 % больных хроническим вирусным гепатитом В возможен спонтанный переход фазы репликации в нерепликативную фазу (при этом из крови исчезает HBeAg и появляются anti-HBe). Именно фаза репликации обусловливает тяжесть поражения печени и контагиозность больного.
В фазе интеграции происходит интегрирование (встраивание) фрагмента вируса гепатита В, несущего ген HBsAg, в геном (ДНК) гепатоцита с последующим образованием преимущественно HBsAg. При этом репликация вируса прекращается, однако генетический аппарат гепатоцита продолжает синтезировать HBsAg в большом количестве.
Вирусная ДНК может быть интегрирована не только в гепатоциты, но и в клетки поджелудочной железы, слюнных желез, лейкоциты, сперматозоиды, клетки почек.
Фаза интеграции сопровождается становлением клинико-морфологической ремиссии. В этой фазе в большинстве случаев формируется состояние иммунологической толерантности к вирусу, что приводит к купированию активности процесса и носительству HBsAg. Интеграция делает вирус недосягаемым для иммунного контроля.
Серологические маркеры фазы интеграции:
- наличие в крови только HBsAg или в сочетании с anti-HBc (IgG);
- отсутствие в крови ДНК-вируса;
- сероконверсия HBeAg в anti-HBe (т.е. исчезновение из крови HBeAg и появление anti-HBe).
Пациенты, перенесшие инфекцию и имеющие антитела к вирусу, не могут повторно заразиться гепатитом B. В некоторых случаях полное выздоровление не наступает и человек становится хроническим вирусоносителем. Вирусоносительство может протекать бессимптомно, но в некоторых случаях развивается хронический активный гепатит B. Ключевым фактором риска активного вирусоносительства является возраст, когда человек был заражен: для грудных детей уровень риска превышает 50 %, в то время как для взрослых остается на уровне 5-10 %. Исследования показывают, что мужчины чаще становятся носителями, чем женщины.
HBsAg – поверхностный антиген вируса гепатита В
Поверхностный антиген вируса гепатита В (HВsAg) является белком, который присутствует на поверхности вируса. Обнаруживается в крови при остром и хроническом гепатите В. Самый ранний маркер. Достигает максимума к 4-6-й неделе заболевания. Сохраняется до 6 месяцев при остром гепатите, свыше 6 месяцев – при переходе заболевания в хроническую форму.
HBeAg – ядерный 'е’-антиген вируса гепатита В
Антиген, находящийся в ядре вируса. Появляется в крови одновременно с HBsAg и сохраняется в течение 3-6 недель. HBeAg появляется в крови больного острым гепатитом В одновременно с HBsAg или вслед за ним и сохраняется в крови 3-6 недель. Указывает на активное размножение и высокий риск передачи вируса при половом контакте, а также перинатально. Инфекционность HBeAg-положительной сыворотки в 3-5 раз выше, чем HBsAg-положительной. Выявление HBeAg в крови более 8-10 недель свидетельствует о переходе заболевания в хроническую форму. При отсутствии репликативной активности вируса во время хронической инфекции HBeAg не выявляется. Его появление же свидетельствует о реактивации вируса, что чаще происходит на фоне иммуносупрессии.
При лечении вирусного гепатита В исчезновение HBeAg и появление антител к HBe-антигену свидетельствует об эффективности терапии.
anti-HBc (Ig M) – специфические антитела класса IgМ к ядерному 'core' антигену вируса
Начинают вырабатываться еще до клинических проявлений, указывают на активную репликацию вируса.
Появляются в крови через 3-5 недель, сохраняются в течение 2-5 месяцев и исчезают в период выздоровления.
anti-HBc – суммарные антитела (IgM+IgG) к ядерному ‘core' антигену вируса гепатита В
Важный диагностический маркер, особенно при отрицательном значении HBsAg. Антитела класса IgM вырабатываются через 3-5 недель. Антитела класса IgG начинают вырабатываться с 4-6-го месяца и могут сохраняться пожизненно. Подтверждают контакт организма с вирусом.
anti-HBs – суммарные антитела к поверхностному антигену вируса гепатита В
Появляются медленно, достигая максимума через 6-12 месяцев. Указывают на перенесенную инфекцию или наличие поствакцинальных антител. Выявление этих антител свидетельствует о выздоровлении и развитии иммунитета. Обнаружение антител в высоком титре в первые недели заболевания может быть связано с развитием гипериммунного варианта фульминантного гепатита В.
anti-HBe – антитела к 'е’-антигену вируса гепатита В
Появляются на 8-16-й неделе после инфицирования у 90 % больных. Свидетельствуют о завершении острого периода болезни и начале периода реконвалесценции. Могут сохраняться до 5 лет после перенесенного заболевания.
HBV (ДНК) – ДНК вируса гепатита В
Маркер наличия и репликации вируса. Методом ПЦР можно определить ДНК вируса качественно или количественно. Благодаря качественному методу подтверждается присутствие вируса гепатита В в организме и его активное размножение. Это особенно важно в сложных диагностических случаях. При инфицировании мутантными штаммами вируса результаты теста на специфические антигены HBsAg и HBeAg могут быть отрицательными, но при этом риск распространения вируса и развития заболевания у зараженного человека сохраняется.
Качественное определение ДНК вируса играет важную роль в раннем выявлении гепатита В у людей с высоким риском инфицирования. Генетический материал вируса обнаруживается в крови на несколько недель раньше, чем HBsAg. Положительный результат ПЦР за период более 6 месяцев указывает на хроническую инфекцию. Определение вирусной нагрузки (количество ДНК вируса в крови) позволяет оценить вероятность перехода заболевания в хроническую форму.
Повышенные уровни печеночных трансаминаз при положительном результате ПЦР являются показателями необходимости проведения терапии. Во время лечения вирусного гепатита В исчезновение ДНК вируса свидетельствует об эффективности лечения.
Для чего используется исследование?
- Для оценки серологического профиля;
- для выяснения стадии заболевания и степени контагиозности;
- для подтверждения заболевания и уточнения его формы (острая, хроническая, носительство);
- для наблюдения за течением хронического гепатита В;
- для оценки эффективности противовирусной терапии.
Когда назначается исследование?
- При выявлении у пациента поверхностного антигена вируса гепатита В (HBsAg);
- при подозрении на инфицирование вирусом гепатита В и сомнительных результатах серологических тестов;
- при микст-гепатитах (сочетанные вирусные гепатиты В и С);
- при динамическом наблюдении за больным гепатитом В (определение стадии процесса при совместном исследовании на другие специфические маркеры инфекции).
Что означают результаты?
Для каждого показателя, входящего в состав комплекса:
Острый гепатит В. Выделяют "дикий" штамм (естественный) и "мутантный" штамм (вид) вируса. Определение штамма вируса имеет определенное значение при выборе противовирусного лечения. Мутантные штаммы вируса несколько хуже поддаются лечению в сравнении с "диким".
Хронический гепатит В (ХВГВ). Выделяют три серологических варианта:
- ХВГВ с минимальной активностью (ранее использовали термин "носительство HBsAg");
- НВе-негативный ХВГВ;
- НВе-позитивный ХВГВ.
Интерпретация сочетаний серологических маркеров гепатита В

Репликация гепатита С — это период размножения вирусных частиц в клетках печени. Часто этот процесс протекает без видимых симптомов, а само заболевание постепенно переходит в хроническую форму. Только человек с сильным иммунитетом способен самостоятельно победить болезнь. Репликативная фаза может продолжаться долго. Инфицированный чувствует себя хорошо, в то время как вирус продолжает размножаться, постоянно мутируя и поражая новые клетки печени. Распознать гепатит С можно только посредством лабораторных анализов.
Что такое репликация вируса гепатита
Фаза репликации гепатита С — это активное распространение вируса в гепатоцитах. Каждый день инфицированной клеткой производится около 50 вирионов (вирусных частиц). В общей сложности в клетках печени их может быть более одного триллиона. Также вирус поражает иммунные клетки, что приводит к нарушению в работе всех систем и органов человека при хроническом гепатите С.
РНК вируса включает больше 9 тысяч нуклеотидов (фрагментов). Из них примерно 30% постоянно мутирует. Из-за быстрой скорости мутации возникает множество вариантов вируса, которые являются квазивидами, а не обычными видами вирусного гепатита. Чтобы иммунитет начал вырабатывать антитела к новым квазивидам, должно пройти некоторое время, за которое вирус снова мутирует.
За 7 дней HCV успевает полностью изменить антигенную структуру, вследствие чего иммунная система перестает вообще его распознавать.
Интенсивность репликации HCV не такая высокая, в отличие от других видов гепатита. Активность распространения патогенов зависит от генотипа болезни. Самая низкая репликация у 1b генотипа, вследствие чего он не замечается человеком и вскоре приобретает хроническую форму.
Активная фаза репликации начинается в течение 2 недель после инфицирования, когда все вирусные частицы достигают клеток печени. Эта фаза продолжается до 3 месяцев. При сильном иммунитете патогенные клетки могут быть полностью подавлены.
Возможна репликация двух и более вирусов (В, А или D). В этом случае диагностируется микст-гепатит.
Как проявляется стадия репликации ВГС
Чаще всего (в 80% случаев) фаза репликации при гепатите С протекает бессимптомно. Инфицированный чувствует себя хорошо, к врачу не обращается. Однако в это время растет количество зараженных клеток, вследствие чего повышается вирусная нагрузка.
У 10-20% больных стадия репликации сопровождается острой симптоматикой. Первые признаки могут проявляться уже на 2 неделе после инфицирования. Наблюдается:
- повышенная утомляемость, слабость;
- головные боли;
- снижение умственной и физической активности;
- мышечные, суставные боли;
- дискомфорт в области правого подреберья;
- пожелтение кожи и склер глаз (в редких случаях);
- повышение температуры тела до 37,5°C.
При остром гепатите С на стадии репликации также могут появиться следующие жалобы:
- тошнота и рвота;
- ухудшение аппетита;
- обесцвечивание кала и потемнение мочи.
Во время осмотра больного врач диагностирует увеличение размеров печени и селезенки. Биохимия крови показывает повышение уровня печеночных ферментов (АЛТ, АСТ, билирубина). Если сразу же не начать лечение, из фазы репликации спустя полгода разовьется хронический гепатит.
Наличие вируса в организме в стадии репликации выявляется посредством ИФА (иммуноферментного анализа). С его помощью определяется ответ иммунной системы на появление в организме HCV.
Если в крови обнаружен анти-HCV IgM, значит, человек инфицировался недавно, то есть в данный момент происходит активная репликация вирусных частиц и болезнь еще не стала хронической. Анти-HCV IgG свидетельствуют о хронизации гепатита С.
Как протекает гепатит С вне репликации
После стадии репликации начинается хроническая (латентная или скрытая) фаза. Продолжаться она может до 15-20 лет. Больной является хроническим носителем HCV и иногда даже не подозревает, что болен. Симптомы могут быть слабыми или отсутствовать полностью. Лишь иногда после активных физических нагрузок или переедания чувствуется тяжесть в правом подреберье. Вирусная нагрузка стихает, но патогенные клетки все равно продолжают постепенно разрушать гепатоциты.
Хронический вирусный гепатит может резко обостриться. Это называется фазой реактивации, когда заболевание вспыхивает с новой силой. Это может произойти спустя 12-15 лет после репликации вируса, при циррозе печени — через 15-20 лет, а в случае рака печени — спустя 25-28 лет. Клетки печени полностью перестают нормально работать, в процессе обследования диагностируется высокая вирусная нагрузка.
Подбор лечения для разных фаз
Вирус HCV врачи лечат лекарственными средствами, называемыми ингибиторами протеазы и полимеразы. Такие препараты предотвращают самокопирование (репликацию) патогенных микроорганизмов. Подобная терапия проводится:
При помощи этих медикаментов достигается прямое действие на вирус HCV, в отличие от интерферона, который только стимулирует иммунитет на борьбу с возбудителем.
Благодаря ингибиторам протеазы и полимеразы вирусные частицы не могут расщепляться и строить новые РНК. Также для устранения патогенов могут прописываться интерфероны совместно с Рибавирином. Но от такой терапии в последнее время стараются отказаться вследствие невысокой эффективности (до 70%) и большого количества побочных действий.


ДЕШЕВЫЕ ЛЕКАРСТВА ОТ ГЕПАТИТА С Сотни поставщиков везут лекарства от гепатита С из Индии в Россию, но только компания IMMCO поможет вам купить софосбувир и даклатасвир (а так же велпатасвир и ледипасвир) из Индии по самой выгодной цене и с индивидуальным подходом к каждому пациенту!

Вирусный гепатит С (HCV, ВГС) до недавнего времени во многих случаях оставался неизлечимой болезнью. Несмотря на то, что сам вирус не является смертельным, его склонность к ускользанию от иммунной системы позволяет ему разрушать печень на протяжении десятилетий, приводя к необратимым изменениям этого жизненноважного органа.
Сегодня в разработке препаратов для лечения вирусного гепатита С достигнуты приемлемые результаты. Современные лекарственные средства позволяют получить устойчивый вирусологический ответ (УВО) в 98% случаев даже при вирусе 1 и 4 типов.
Что такое вирусный гепатит С?

Вирус гепатита С является РНК-содержащей частицей, которая, как и все другие вирусы, использует чужие живые клетки для собственной репликации (размножения). Вид клеток, в которых вирусы могут размножаться ограничен.
Для гепатита С это могут быть клетки печени (гепатоциты), а также клетки иммунной системы (лимфоциты), причем не любого живого существа, а только человека. Гепатиты — это исключительно антропонозные вирусы.
Что же такое РНК вируса гепатита С? Макромолекула рибонуклеиновой кислоты (РНК) находится внутри вириона (вирусной частицы). Она представляет собой нить сцепленных друг с другом нуклеотидов, последовательность которых кодирует генетическую информацию вируса.
РНК гепатита С содержит более 9000 нуклеотидов.
Такое огромное количество нуклеотидов кодирует всего 10 вирусных белков — 3 структурных протеина и 7 не структурных.

Период размножения вируса гепатита С в клетках печени называют репликативной фазой заболевания. Интенсивность репликации вируса не слишком высокая (по сравнению с другими гепатитами).
По этой причине в большинстве случаев заболевание протекает бессимптомно и даже такие общие признаки, как интоксикация, повышение температуры, не свойственны течению этого заболевания. Заболевший чувствует себя хорошо, к врачу не обращается. Тем не менее количество вирусных частиц в организме растет, увеличивается вирусная нагрузка. Все большее количество гепатоцитов переключается со своих естественных функций на копирование чужеродных белков.
Фаза репликации при гепатите С может длиться сколько угодно долго. Несмотря на то, что иммунная система распознает вторжение вируса сразу после попадания его в кровь, лишь в редких случаях, которые могут быть отнесены к исключительным, ей удается подавить инфекционный процесс. В большинстве же случаев вялотекущая репликативная фаза продолжается, переводя заболевание в хроническую форму.
Почему же, несмотря на все усилия, иммунная система не в состоянии справиться с вирусом?
Причина в том, что вирусный гепатит С характеризуется изменчивостью, обусловленной, говоря научным языком, высокой гетерогенностью генома на уровне последовательности нуклеотидов.
В большинстве случаев иммунная система никогда не успевает за появлением новых квазивидов вируса, что и является причиной хронического вирусного гепатита С.

Изменения в печени при вирусном гепатите С
Как передается вирус?
Гепатит С передается через кожный покров, целостность которого нарушена. Это может происходить:
- при инъекциях и других медицинских манипуляциях;
- при нанесении татуировок, при маникюре и других манипуляциях немедицинского характера;
- при незащищенном половом акте (крайне редко);
- от матери — к ребенку при родах.
Тем же способом, при тех же ситуациях передается и хронический вирусный гепатит С.
Чего боится вирус гепатита С и можно ли его убить?
Вирусные частицы, находящиеся в окружающей среде, проявляют достаточно высокую степень устойчивости. Вирус сохраняет свои патогенные свойства:
- при комнатной температуре — до нескольких месяцев;
- при отрицательных температурах — в течение лет.
Вирус сохраняется, в том числе в высохших пятнах крови, на бритвенных лезвиях, на иглах от шприцов, от тату-машинок и прочих инструментах и предметах, проконтактировавших с кровью человека.
Возникает закономерный вопрос: можно ли убить вирус гепатита С? Безусловно, можно. Оболочка вириона не абсолютно устойчива и разрушается под действием химических веществ и экстремальных условий окружающей среды.
Таблица. Чего боится вирус гепатита С
| Что убивает вирус гепатита С | Время воздействия |
|---|---|
| Антисептические препараты (спирт, хлоргексидин, мирамистин, перекись водорода) | мгновенно |
| Кипячение | 5 минут |
| Воздействие ультрафиолетом (вирус должен быть доступен для ультрафиолетовых лучей) | 1 час |
Таким образом, термическая стерилизация инструментов и обработка их антисептиками способна убить вирус достаточно быстро.
Лечение
Вирусные протеазы — это ферменты, расщепляющие вирусные белки NS3 и NS4A. Расщепление является одной из фаз репликации, без которой невозможно построение копий вирусов. Полимеразы — другой вид ферментов, связанных с вирусными белками NS5A и NS5B, которые участвует в построении вирусной РНК.
Ингибирование протеазы и полимеразы препятствует процессам расщепления вирусных белков и построения новых РНК. Таким образом достигается прямое противовирусное воздействие препаратов.
К ингибиторам протеазы неструктурных белков NS3/NS4A относятся:
К ингибиторам полимеразы неструктурных белков NS5A/NS5B относятся:
Схемы лечения вирусного гепатита С могут включать:
- комплекс из двух ингибиторов полимеразы (напр., софосбувир + даклатасвир);
- ингибитор протеазы + ингибитор полимеразы (напр., симепревир + софосбувир);
- ингибитор протеазы/полимеразы + пегинтерферон альфа + рибавирин;
- ингибитор полимеразы + рибавирин.
Излечим ли вирусный гепатит С?
Разработка и внедрение в терапевтическую практику ингибиторов вирусной протеазы и полимеразы позволили сделать гепатит С, даже 1 типа, излечимым в 90 и более процентах случаев.
Профилактика

В связи со способностью такого вируса, как гепатит С, к трансформации своей генной структуры, вакцины против него не существует.
Единственно возможная профилактика вирусного гепатита С заключается в соблюдении мер предосторожности:
- все медицинские и немедицинские манипуляции, связанные с нарушением целостности кожного покрова должны проводиться стерильными (желательно одноразовыми) инструментами;
- нестерильные инструменты необходимо подвергать термической стерилизации и/или обрабатывать антисептиками;
- при любом виде полового контакта необходимо пользоваться презервативом;
- предметы личной гигиены (бритвы, зубные щетки) должны быть строго индивидуального использования.
Полезное видео
В следующем видео вы можете получить дополнительную информацию о том, что такое вирусный гепатит С:

Вирусы — это микроскопические патогены, заражающие клетки живых организмов для самовоспроизводства. Они состоят из одного вида нуклеиновой кислоты (или ДНК или РНК, но не обе вместе), которая защищена оболочкой, содержащей белки, липиды, углеводы или их комбинацию. Размер типичного вируса варьируется от 15 до 350 нм, поэтому его можно увидеть только с помощью электронного микроскопа.
В 1892 году русский ученый Д.И. Ивановский впервые доказал существование ранее неизвестного типа возбудителя болезней, это был вирус мозаичной болезни табака. А в 1898 году Фридрих Лоффлер и Пол Фрош нашли доказательства того, что причиной ящура у домашнего скота была инфекционная частица, которая меньше, чем любая бактерия. Это были первые шаги к изучению природы вирусов, генетических образований, которые лежат где-то в серой зоне между живыми и неживыми состояниями материи. На текущий момент описано около 6 тыс. вирусов, но их существует несколько миллионов.
Строение вирусов
Вне клеток-хозяев вирусы существуют в виде белковой оболочки (капсида), иногда заключенного в белково-липидную мембрану. Капсид обволакивает собой либо ДНК, либо РНК, которая кодирует элементы вируса. Находясь в такой форме вне клетки, вирус метаболически инертен и называется вирионом.
Простая структура, отсутствие органелл и собственного метаболизма позволяет некоторым вирусам кристаллизоваться, т.е. они могут вести себя подобно химическим веществам. С появлением электронных микроскопов было установлено, что их кристаллы состоят из тесно прижатых друг к другу нескольких сотен миллиардов частиц. В одном кристалле вируса полиомиелита столько частиц, что ими можно заразить не по одному разу всех жителей Земли.
Формы вирусов
Вирусы встречаются в трех основных формах. Они бывают:
- Сферическими (кубическими или полигидральными). Вирусы герпеса, типулы, полиомы и т.д.
- Спиральными (цилиндрическими или стержнеобразными). Вирусы табачной мозаики, гриппа, эпидемического паротита и др.
- Сложными. Например, бактериофаги.
Проникновение вирусов в клетку-хозяина
Капсид в основном защищает нуклеиновую кислоту от действия клеточного нуклеазного фермента. Но некоторые белки капсида способствуют связыванию вируса с поверхностью клеток-хозяев, и работают, как ключики, вставляемые в нужные замочки. Другие поверхностные белки действуют как ферменты, они растворяют поверхностный слой клетки-хозяина и таким образом помогают проникновению нуклеиновой кислоты вируса в клетку-хозяина.
Жизненный цикл вирусов сильно отличается у разных видов, но существует шесть основных этапов жизненного цикла вирусов:
Присоединение к клетке-хозяину представляет собой специфическое связывание между вирусными капсидными белками и рецепторами на клеточной поверхности. Эта специфика определяет хозяина вируса.
Проникновение следует за прикреплением: вирионы проникают в клетку-хозяина через рецептор-опосредованный эндоцитоз или слияние мембран. Это часто называют вирусной записью.
Проникновение вирусов в клетку достигается за счет:
Размножение вирусов
После того, как вирусный геном освобождается от капсида, начинается его транскрипция или трансляция. Именно эта стадия вирусной репликации сильно различается между ДНК- и РНК-вирусами и вирусами с противоположной полярностью нуклеиновой кислоты. Этот процесс завершается синтезом новых вирусных белков и генома (точных копий внедрённых).
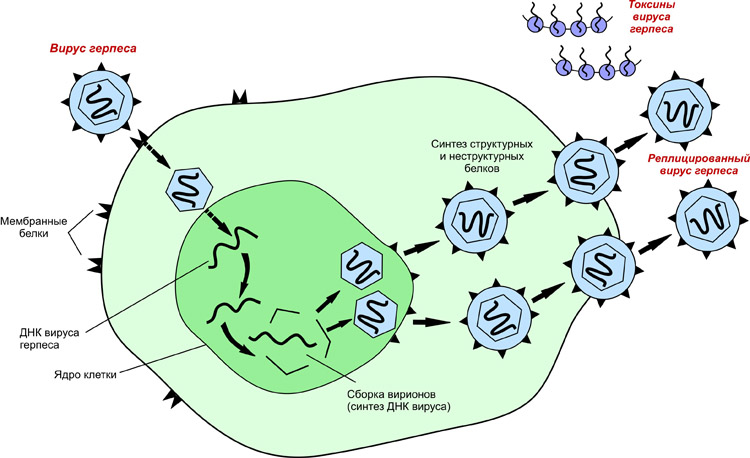
Механизм репликации зависит от вирусного генома.
- ДНК-вирусы обычно используют белки и ферменты клетки-хозяина для получения дополнительной ДНК, она транскрибируется в РНК-мессенджер (мРНК), которая затем используется для управления синтезом белка.
- РНК-вирусы обычно используют ядро РНК в качестве матрицы для синтеза вирусной геномной РНК и мРНК. Вирусная мРНК направляет клетку-хозяина на синтез вирусных ферментов и капсидных белков и сборку новых вирионов. Конечно, есть исключения из этого шаблона. Если клетка-хозяин не обеспечивает ферменты, необходимые для репликации вируса, вирусные гены предоставляют информацию для прямого синтеза отсутствующих белков.
Чтобы преобразовать РНК в ДНК, вирусы должны содержать гены, которые кодируют вирус-специфический фермент обратной транскриптазы. Она транскрибирует матрицу РНК в ДНК. Обратная транскрипция никогда не происходит в неинфицированных клетках. Необходимый фермент, обратная транскриптаза, происходит только от экспрессии вирусных генов в инфицированных клетках.
Вироиды
Вироиды заражают только растения. Одни вызывают экономически важные заболевания сельскохозяйственных культур, в то время как другие являются доброкачественными. Двумя примерами экономически важных вироидов являются кокосный cadang-cadang (он вызывает массовую гибель кокосовых пальм) и вироид рубцовой кожицы яблок, который безнадежно портит товарный вид яблок.
30 известных вироидов были классифицированы в две семьи.
- Члены семейства Pospiviroidae, названные по имени вироида клубневого веретена картофеля, имеют палочковидную вторичную структуру с небольшими одноцепочечными областями, имеет центральную консервативную область, и реплицируются в ядре клетки.
- Avsunviroidae, названный в честь вироида авокадо, имеет как палочковидную, так и разветвленную области, но не имеет центральной консервативной области и реплицируется в хлоропластах растительной клетки.
В отличие от вирусов, которые являются паразитами механизма трансляции хозяина, вироиды являются паразитами клеточных транскрипционных белков.
Бактериофаги

Существуют тысячи разновидностей фагов, каждый из которых может заразить только один тип или несколько близких типов бактерий или архей. Фаги классифицируются по ряду семейств вирусов; например:
Как и все вирусы, фаги являются простыми организмами, которые состоят из ядра генетического материала (нуклеиновой кислоты), окруженного капсидом белка. Нуклеиновая кислота может представлять собой либо ДНК, либо РНК, и может быть двухцепочечной или одноцепочечной.
Существует три основных структурных формы фага:
- Икосаэдрическая (20-сторонняя) головка с хвостом
- Икосаэдрическая головка без хвоста
- Нитевидная форма
Во время заражения фаг прикрепляется к бактерии и вставляет в нее свой генетический материал. После этого фаг обычно следует одному из двух жизненных циклов: литическому (вирулентному) или лизогенному (умеренному).
Литические, или вирулентные, фаги захватывают механизм клетки, чтобы скопировать компоненты фага. Затем они разрушают или лизируют клетку, высвобождая новые частицы фага.
Лизогенные, или умеренные, фаги включают свою нуклеиновую кислоту в хромосому клетки-хозяина и реплицируются с ней как единое целое, не разрушая клетку. При определенных условиях лизогенные фаги могут индуцироваться в соответствии с литическим циклом.
Существуют и другие жизненные циклы, в т.ч. псевдолизогенез и хроническая инфекция. При псевдолизогении бактериофаг проникает в клетку, но не использует механизм репликации клеток и не интегрируется в геном хозяина, просто как бы прячется внутри бактерии, не нанося ей никакого вреда. Псевдолизогенез возникает, когда клетка-хозяин сталкивается с неблагоприятными условиями роста и, по-видимому, играет важную роль в выживании фага, обеспечивая сохранение генома фага до тех пор, пока условия роста хозяина снова не станут благоприятными.
При хронической инфекции новые фаговые частицы образуются непрерывно и длительно, но без явного уничтожения клеток.
Вскоре после открытия фаги начали использовать для лечения бактериальных заболеваний человека, таких как бубонная чума и холера. Но фаговая терапия тогда не была успешной, и после открытия антибиотиков в 1940-х годах она была практически заброшена. Однако с появлением устойчивых к антибиотикам бактерий терапевтическому потенциалу фагов уделяется все больше внимания.
Наше время с антибиотиками заканчивается. В 2016 году женщина в штате Невада умерла от бактериальной инфекции, вызванной Klebsiella pneumoniae, которая была устойчивой ко всем известным антибиотикам. Бактерии, устойчивые к колистину, антибиотику последней инстанции, были обнаружены на свинофермах в Китае. В настоящее время бактерии приспосабливаются к антибиотикам быстрее, чем когда-либо.
Покажите ножницы которыми вирусы разрезают молекулу РНК что бы встроиться для мутации.Может что нибудь придумаете другое.К примеру деление цепочка аминокислот получив энергию из вне как одноименные заряды распадается на две. К каждой соединятся только те какие были ранее (другие проскочат мимо),казалось бы копии,но внутренняя энергия разная(уменьшается увеличивается) поэтому распад и создание. Вся химия углерода на этом построена 1000 орган соединений создает у других хим элементов этого свойства нет. Иммунная система делает накладку(интерференция)с помощью энергии интерферонов пытаясь разрушить цепочку РНК вируса.Надо помочь организму но не вакциной(вирус быстро мутирует)
Читайте также:


