Эндогенная интоксикация клинические рекомендации
В настоящее время одной из наиболее сложных проблем интенсивной терапии является синдром эндогенной интоксикации (СЭИ), сопровождающий значительное количество патологических состояний (шок, перитонит, панкреатит и др.), которые по мере своего развития могут приводить к летальному исходу.
Прогрессирование эндотоксикоза обусловлено накоплением в крови различных по происхождению, химической структуре и биологическому воздействию веществ, именуемых эндотоксинами. Эндотоксины способствуют развитию острой почечно-печеночной недостаточности, сердечно-сосудистой недостаточности, острого респираторного дистресс-синдрома, приводя в конечном итоге к появлению крайне тяжелого состояния - синдрома мультиорганной дисфункции.
Эндогенная интоксикация - клинический синдром, возникающий при различных по этиологии патологических состояниях, обусловленных накоплением в тканях и биологических жидкостях организма продуктов нарушенного обмена веществ, метаболитов, деструктивных клеточных и тканевых структур, разрушенных белковых молекул, pi сопровождающийся функциональными и морфологическими поражениями органов и систем организма.
Выделяют три основных звена, которые определяют тяжесть состояния больных и выраженность клинической симптоматики: токсемия, нарушение микроциркуляции, угнетение функций собственных детоксицирующих и защитных систем организма.
Основным звеном патогенеза синдрома эндогенной интоксикации является токсемия. К сожалению, четкая дифференциация токсических веществ эндогенного происхождения практически невозможна. Однако в каждом конкретном случае можно выделить "первичные" и "вторичные" эндотоксины. Так, при ожогах, синдроме длительного раздавливания, облитерирующих сосудистых заболеваниях "первичными" являются продукты белковой деградации, "вторичными" - продукты естественного метаболизма, накопление которых в организме является следствием угнетения функций естественной детоксикации и экскреции.
Эндотоксемия, нарушая тонус периферических сосудов, реологию крови, кинетические и механические свойства форменных элементов крови, приводит к тканевой гипоксии, которая является одним из важных звеньев патогенеза СЭИ, течение которого усугубляется снижением функции органов естественной детоксикации и экскреции. Токсины блокируют места связывания молекул альбумина, что ведет к снижению эффективности проводимого медикаментозного лечения, поскольку этот белок является транспортным агентом для многих фармакологических препаратов.
Сопоставление экспериментальных и клинических исследований позволило выявить следующие стадии развития синдрома эндогенной интоксикации.
I стадия синдрома эндогенной интоксикации. Реактивно-токсическая возникает в ответ на формирование первичного деструктивного очага или травматического повреждения. Лабораторными признаками этой стадии являются повышение в крови уровней молекул средней массы (МСМ), продуктов перекисного окисления липидов (ДК и МДА), возрастание ЛИИ.
II стадия синдрома эндогенной интоксикации - стадия выраженной токсемии развивается после прорыва гастогематического барьера, когда в циркулирующую кровь попадают эндотоксины, образовавшиеся в первичном очаге интоксикации, с последующим распространением и накоплением в организме. В зависимости от состояния организма, его резистентности и исходного уровня детоксицирующих и иммунных систем выделяют компенсированную и декомпенсированную стадии выраженной токсемии.
III стадия синдрома эндогенной интоксикации - мультиорганной дисфункции (СМОД) наблюдается при дальнейшем прогрессировашш патологического процесса как следствие тяжелого повреждения эндотоксинами различных органов и систем с развитием их функциональной декомпенсацш!. Клинически эта стадия Проявляется нарушением сознания, гипоксией, выраженной сердечной Недостаточностью, олигурией, паралитической непроходимостью кишечника. В крови определяется высокая концентрация креатинина, мочевины, билирубина.
Интоксикация - патологическое состояние, возникающее в результате действия на организм токсических (ядовитых) веществ эндогенного или экзогенного происхождения. Соответственно и различают эндогенные и экзогенные интоксикации.
Эндогенные интоксикаций классифицируются в зависимости от:
· заболевания, послужившего источником их возникновения (травматическая, радиационная, инфекционная, гормональная).
· от расстройства физиологической системы, которое привело к накоплению в организме токсических продуктов (кишечная, почечная, печеночная).
Интоксикация обычно наступает в результате действия циркулирующих в крови токсических веществ; циркуляция в крови эндогенных ядов чаще обозначается как токсемия, а циркуляция токсинов - как токсинемия.
Часто используются термины, указывающие вещество, находящееся в крови, например - азотемия.
По механизму развития можно различать следующие виды:
Ретенционные - вследствие затрудненного выведения и задержки выделений, например, при нарушениях выделительной способности почек, при накоплении углекислоты и обеднении кислородом крови и тканей в связи с расстройством дыхания.
Резорбционные - вследствие образования ядовитых веществ в полостях тела при гниении и брожении с последующим всасыванием продуктов распада, например, при гнойных процессах в полости плевры, мочевого пузыря либо в кишечнике при непроходимости, кишок, кишечных, инфекциях, или при длительном запоре.
Обменные - вследствие нарушения обмена веществ и изменения состава тканей, крови и лимфы, в результате чего происходит избыточное накопление в организме ядовито действующих веществ:
1. фенольных соединений,
2. азотистых оснований типа бетаина,
3. аммонийных веществ,
4. кислых продуктов промежуточного углеводного обмена ( молочная и др.).
Сюда можно отнести азотемии при эндокринных заболеваниях (диабете, микседеме, базедовой и аддисоновой болезнях, паратиреоидной тетании), при авитаминозах, злокачественных новообразованиях, при заболевании печени, когда интоксикация может наступить вследствие потери печенью способности обезвреживать ядовитые продукты.
Инфекционные - вследствие накопления бактериальных токсинов и др. продуктов жизнедеятельности микробов, а также продуктов распада тканей при инфекционных заболеваниях.
Может иметь место сочетание нескольких факторов. Так при уремии задержка ядовитых продуктов вследствие недостаточности функции почек сочетается с нарушениями обмена веществ. При патологии беременности аутоинтоксикация возникает вследствие задержки ядовитых продуктов обмена в материнском организме и одновременно вследствие нарушения обмена веществ и совершающихся процессов распада в организме плода.
Особое место занимает кишечная аутоинтоксикация, которой И.И.Мечников придавал большое значение в патологии человека. В кишечнике и в норме проходят процессы брожения и гниения. Эксперимент этого является действие экстрактов содержимого кишечника.
При внутривенном введении их экспериментальному животному наблюдались судорога, центральные параличи, остановка дыхания и коллапс. В нормальных условиях всасывающиеся ядовитые вещества легко обезвреживаются печенью, но в патологических условиях пищеварения в кишечнике усиливаются процессы гниения и брожения, вследствие чего накапливаются ядовитые вещества. Всасываясь в увеличенном количестве, они могут оказывать токсическое действие. Среди этих ядовитых веществ следует отметить некоторые ароматические соединения (фенол, крезол, скатол, индол), образующиеся из аминокислот в результате превращения боковой цепи, а также продукты декарбоксилирования аминокислот - путресцин, кадаверин.
Кишечная аутоинтоксикация наиболее выражена в случаях, когда усиленные процессы гниения и брожения в кишечнике сочетаются с ослаблением барьерной функции кишечника, печени и выделительной деятельности почек.
При различных экстремальных воздействиях (механическая травма, обширный ожог, массивная кровопотеря) аутоинтоксикация может развиваться в результате поступления в кровь эндотоксииа Escherichia coli, вызывающего функциональные нарушения в системе кровообращения. Плазма, полученная от животных с необратимым постгеморрагическим шоком, вызывает некроз слизистой оболочки тонкого кишечника, пирогенную реакцию и лейкопению у здоровых животных. Существует концепция, объясняющая механизм эндотоксемии при экстремальных состояниях различного происхождения. Известно, что всем видам шока присуща недостаточность кровообращения внутренних органов с последующим развитием тканевой гипоксии, неизбежно приводящей к повышению активности клеток ретикулоэндотелиальной системы (РЭС). В результате РЭС утрачивает способность нейтрализовать эндотоксин, непрерывно поступающий из кишечника в кровь через воротную вену. Количество циркулирующего постоянно эндотоксина увеличивается, что отражается на функции кровообращения; возникает порочный круг при котором накопление эндоксииа усугубляет нарушение кровообращения и прежде всего микроциркуляцию.
Биофизические механизмы, аутоинтоксикации.
В основе биофизических механизмов аутоинтоксикации лежат нарушения физико-химических процессов в организме. Известно, что в клетке существуют как ферментативные, так и неферментативные системы, инициирующие процессы перикисного окисления липидов клеточных мембран. В результате этих физико-химических процессов образуются продукты окисления липидов- гидроперикиси, перикиси, альдегиды и кетоны ненасыщенных жирных кислот. Эти продукты обладают значительной реактивной способностью они взаимодействуют с аминокислотами белков, нуклеиновыми кислотами и другими молекулами клетки, что приводит к инактивации ферментов, разобщению окислительного фосфорилирования, возникновению хромосомных аберраций. Образование перекисей ненасыщенных жирных кислот в фосфолипидах мембран способствует изменению проницаемости этих мембран. Ряд экстремальных факторов стимулируют ПОЛ и в первую очередь к ним относятся отравление ядами, действие ионизирующей радиации, стрессовые воздействия.
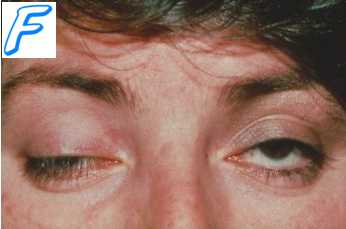
Клинические проявления аутоинтоксикации имеют свои особенности. Течение эндогенной интоксикации в значительной степени определяется характером основного заболевания. Так, например, для диффузного и токсического зоба характерны стойкая тахикардия, похудание, экзофтальм, симптомы токсического действия избыточного количества тиреоидных гормонов (тиреотоксикоз).
При хронической уремии отмечаются явления в местах выделения азотистых шлаков: в гортани, в глотке, желудочно-кишечном тракте, на коже обнаруживаются скопления кристаллов мочевины.
При хронической эндогенной интоксикации больные отмечают недомогание, раздражительность, разбитость, головную боль, головокружение, тошноту; наступает истощение, снижается резистентность организма. В ряде случаев аутоинтоксикация может протекать в форме тяжелого острого отравления (рвота, ступор, коматозное состояние). Такое течение характерно для острой почечной недостаточности, гепатаргии, острой ожоговой токсемии.
Возникновение аутоинтоксикации раньше представляли себе только как результат непосредственного воздействия эндотоксина на ткани и органы. Однако ядовитые продукты обмена, как и всякие другие биологически активные вещества, оказывают воздействия на органы и через центральную нервную систему. Возможно так же раздражение ими обширного поля рецепторных образований с последующим рефлекторным влиянием на разнообразные функции организма.
Таким образом, аутоинтоксикация (autos - сам + интоксикация) - самоотравление ядовитыми веществами, которые вырабатываются организмом как при некоторых нарушениях нормальной жизнедеятельности так и при различных заболеваниях. В основном вещества, вызывающие аутоинтоксикацию, представляют собой продукты обмена веществ или тканевого распада.
В нормальных условиях естественные метаболиты выделяются из организма (через почки с мочой, через толстую кишку с калом, через кожу с потом, через легкие с воздухом или различными секретами), либо подвергаются обезвреживанию в результате химического превращения в процессах промежуточного обмена веществ. Аутоинтоксикация возникает при патологических состояниях, когда защитные приспособления оказываются недостаточными, например, при нарушении функции выделительных органов или при расстройствах обмена веществ, а также при ненормальных процессах всасывания из различных полостей.
Основные принципы лечения:
1. При хирургической патологии - радикальное хирургическое вмешательство с удалением пораженного органа и эффективным дренированием. В некоторых случаях (например, при деструктивном холецистите, аппендиците), это удается сделать достаточно успешно, тем самым прерывается дальнейшее прогрессирование эндотоксикоза. В других случаях, например, при осложнении ЖКБ механической желтухой, радикальной операции может оказаться недостаточно, так как уже развились явления печеночной и печеночно-почечной недостаточности. Повышение эффективности лечения больных с механической желтухой может быть достигнуто с помощью патогенетически обоснованной коррекции нарушений гемостаза.
2. Устранение основного заболевания, которое послужило источником образования и накопления в организме эндогенных токсических веществ, например, при эндокринной недостаточности необходимо восполнение недостающего гормона, при уремии - восстановление функции почек, при инфекционной аутоинтоксикации - применение антибиотиков.
3. Устранение ядовитых веществ, например, при аутоинтоксикации углекислотой удаление ее избытка с помощью стимуляции дыхания, при аутоинтоксикации из полостей (кишок, матки, мочевого пузыря, плевральной, брюшной полостей) удаление содержимого промыванием или выведением его с помощью дренажа.
4. Обезвреживание ядовитых веществ прибавлением к промывающим жидкостям обеззараживающих средств либо введением их peros или внутривенно.
5. Усиление выделительной способности организма с помощью мочегонных, слабительных, патогенных средств.
6. Понижение концентрации ядовитых веществ введением в организм физиологических растворов, форсированный диурез, а при сильной аутоинтоксикации – плазмоферез, гемодиализ, гемосорбция.
Дезинтоксикационная терапия - лечебные меры, направленные на прекращение или снижение интенсивности действия на организм токсических веществ.
Имеющиеся в организме механизмы преодоления интоксикации антитоксическая функция печени и ретикулоцитарной системы, элиминация токсических веществ почками, органами желудочно-кишечного тракта и др.
При эндогенной интоксикации дезинтоксикационную терапию проводят в следующих направлениях.
1. Гемодилюция с целью снижения концентрации токсических веществ, циркулирующих в крови. С этой целью применяют обильное питье, па-рэнтералыюе введение изотонических растворов солей, глюкозы.
2. Улучшение кровоснабжения тканей и органов для ускорения вымывания токсических веществ. Этой цели служат внутривенное капельное введение реологически активных препаратов - низкомолекулярных декстранов (реополиглюкин, гемодез), обладающих также способностью связывать токсины и содействию выведения их с мочой.
3. Ускорение выведения токсических веществ с мочой, предпринимаемое, как правило, вслед за гемодилюцией и введения реологически активных препаратов и осуществляемое формированием диуреза с помощью значительных доз быстродействующих диуретических средств (фуросемид) при условии сохранения функции почек и при отсутствии артериальной гипертонии.
Методы внепочечного кровеочищения занимают особое место. К числу таких методов относятся плазмоферрез, перитонельный диализ, в/в лазерное, УФО облучение крови.
Проведение дезинтоксикационной терапии нуждается в систематическом клинико-лабораторном контроле, во избежание отрицательных для состояния больного ее последствий, которые могут быть обусловлены нарушением состава электролитов в организме и водного обмена. Основными осложнениями могут быть - гиперволемия и гипергидратация, ведущие к декомпенсации кровообращения с развитием анасарки, отека легких, головного мозга.
Более редкие побочные эффекты терапии - снижение толерантности миокарда к сердечным гликозидам, снижением эффективности антибиотиков и других препаратов, миграция конкрементов в желче- и мочевыводящих путях, аллергические реакции на вводимые препараты.
Водно-электролитные нарушения у хирургических больных и принципы инфузионной терапии. Показания, опасности и осложнения. Растворы для инфузионной терапии. Лечение осложнений инфузионной терапии.
Водно - солевой состав организмаВодно-солевой обмен (ВСО)- это совокупность процессов поступления воды и солей (электролитов) в организм, распределение их во внутренней среде и выведение. Системы регуляции ВСО обеспечивают постоянство суммарной концентрации растворенных частиц, ионного состава и КЩР, а также объема и качественного состава жидкостей организма.
Организм человека состоит в среднем на 65% из воды, которая находится в 3-х жидкостных фазах - внутриклеточной, внеклеточной и трансцеллюлярной. Наибольшее количество воды (40-45%) находится внутри клеток.
Внеклеточная жидкость включает (в процентах от массы тела) плазму крови (5%), межклеточную жидкость (16%) и лимфу (2%).
Трансцеллюлярная жидкость (1-3%) изолирована от сосудов слоем эпителия и по своему составу близка к внеклеточной. Это - спинномозговая и внутриглазная жидкости, а также жидкости брюшной полости, плевры, перикарда, суставных сумок и желудочно-кишечного тракта.
Вода свободно проходит через клеточные мембраны, выравнивая осмотическое давление внутриклеточной и внеклеточной жидкостей.
Измеряя осмолярность одного пространства (например, плазмы), мы оцениваем осмолярность всех жидкостных пространств организма.
Водный и электролитный балансы у человека рассчитываются по суточному потреблению и выделению воды и электролитов из организма.
Вода поступает в организм в виде питья - примерно 1,2 л и с пищей -примерно 1 л. Около 0,3 л воды образуется в процессе обмена веществ (из 100г жиров; 100 г углеводов и 100 г белков образуется 107, 55 и 41 мл воды соответственно).
Не нашли то, что искали? Воспользуйтесь поиском:
опубликовано 19.04.2006 (Московское время 19:06) -->
I. ПАТОГЕНЕЗ И КЛИНИЧЕСКАЯ ДИАГНОСТИКА СИНДРОМА ЭНДОГЕННОЙ ИНТОКСИКАЦИИ
Вопрос о том, что может являться такими токсическими субстанциями и обусловливать тяжесть состояния пациентов, сложен и противоречив, так как многие вещества в зависимости от их концентрации могут оказывать и благоприятное, и неблагоприятное функциональное воздействие, а большинство из них вообще не идентифицированы. Можно классифицировать их в зависимости от этиологии и механизма выведения.
2.1. ПРИЧИНЫ И МЕХАНИЗМЫ ЭНДОГЕННОЙ ИНТОКСИКАЦИИ
Эндогенная И может быть вызвана токсическими продуктами, образующимися в организме при различных заболеваниях (аллергических болезнях, ожоговой болезни) и экстремальных состояниях. К эндогенной И. относится отравление продуктами жизнедеятельности бактерий, находящихся в организме. В ряде случаев И. становится ведущим патогенетическим фактором, определяющим развитие клинической картины (уремия, токсикоинфекции, тиреотоксикоз, токсическая дифтерия, токсическая диспепсия и др).
В механизмах как эндогенной, так и экзогенной И. имеется много общего, т. к. в том и другом случае повреждающим фактором является токсический агент. Кроме того, И, вызванная экзогенным фактором, может реализоваться эндогенным путем; например, отравление антихолинэстеразными ядами типа физостигмина или фосфакола в основном сводится к аутоинтоксикации ацетилхолином, который накапливается в синаптических образованиях вследствие прекращения его ферментативного гидролиза.
К числу веществ, накапливающихся в организме при различных заболеваниях и вызывающих эндогенную И., относятся химические соединения различной природы: продукты превращения аминокислот (фенол, крезол, индол, скатол, путресцин, кадаверин), жиров (γ-оксимасляная кислота, ацетоуксусная кислота и ацетон). Имеют значение также активные белки, аденилнуклеотиды, гистамин, серотонин, кинины и другие физиологически активные вещества, выделяющиеся в значительных количествах при повреждении клеток и тканей. При инфекционных заболеваниях происходит накопление бактериальных токсинов и других продуктов жизнедеятельности микробов, а также продуктов распада тканей.
Основной причиной И в условиях трансплантации является реакция трансплантат против хозяина. При возникновении И в различных экстремальных состояниях, например, при ожоговой болезни, травме, патогенетическое значение имеет подавление детоксицирующей способности ретикулоэндотелиальной системы, в связи с чем в организме происходит накопление эндотоксина Е. coli. вызывающего расстройства микроциркуляции. Имеет место также стимулирование неферментативного перекисного окисления липидов клеточных мембран, в результате чего в организме накапливаются токсичные продукты, что вызывает изменение проницаемости этих мембран. При лучевом поражении, кроме того, происходит накопление липидных и хиноноподобных токсинов, повреждающее действие которых на клетки приводит к накоплению в организме гистамина и других физиологически активных продуктов белкового распада. Снижение содержания в тканях естественного ингибитора цепных окислительных реакций токоферола имеет значение для развития И при авитаминозе Е и новообразованиях.
2.2. ИСТОЧНИКИ ЭНДОТОКСИНЕМИИ
- продукты нормального обмена веществ в высоких концентрациях (лактат, пируват, мочевая кислота, мочевина, креатинин, билирубина глюкуронид и др.);
- вещества, избыточно образующиеся при извращенном метаболизме (кетоны, альдегиды, спирты, карбоновые кислоты, аммиак и др.);
- продукты распада клеток и тканей из очагов тканевой деструкции и/или из ЖКТ при нарушении барьерных функций мембран (липазы, лизосомальные ферменты, катионные белки, миоглобин, индол, скатол, фенол и др.);
-компоненты и эффекторы регуляторных систем организма в патологических концентрациях: активированные ферменты (лизосомальные, протеолитические, продукты активации калликреинкининового каскада, системы свертывания крови и фибринолиза);
- медиаторы воспаления, биогенные амины, цитокины, простагландины, лейкотриены, белки острой фазы и другие биологически активные вещества;
- активные соединения, образующиеся при перекисном окислении липидов;
- микробные токсины (экзо- и эндотоксины) и другие факторы патогенности микроорганизмов (патогенных, условно-патогенных, непатогенных);
- иммуночужеродные продукты клеточного распада, антигены и иммунные комплексы-агрессоры.
2.3. ПУТИ ЭЛИМИНАЦИИ ЭНДОГЕННЫХ ТОКСИНОВ
- газообразные вещества – выделяются через легкие;
- гидрофильные низко- и среднемолекулярные вещества – удаляются почками, через кожу, ЖКТ в виде растворов;
- гидрофобные низко- и среднемолекулярные вещества – транспортируются белками и/или клетками крови в печень и легкие, где и биотрансформируются при участии монооксигеназной системы или
претерпевают изменения в реакциях связывания с последующим удалением через почки, кожу, ЖКТ;
- гидрофобные низко- и среднемолекулярные вещества – связываются с белками плазмы крови, приобретают свойства гаптенов и поглощаются клетками иммунной системы;
- высокомолекулярные соединения – транспортируются по лимфатическим сосудам, элиминируются моноцитарно-макрофагальной системой (до 80% макрофагов организма находится в печени).
2.4. СТАДИИ ЭНДОГЕННОЙ ИНТОКСИКАЦИИ
Острый эндотоксикоз протекает как каскадный процесс. Развитие и прогрессирование его связано с несоответствием между образованием (поступлением и т.д.) токсических субстанций, в том числе образующихся в результате последующей токсической аутоагрессии, и способностью органов, входящих в функциональную систему детоксикации (легкие, печень, почки, ЖКТ, кожа, система иммунологического надзора), их трансформировать, нейтрализовать и элиминировать. Существенное значение могут иметь нарушения соотношений между веществами антагонистами в гуморальных регуляторных системах (ферменты-антиферменты, оксиданты-антиоксиданты, цитокины-антицитокины и т.д.).
Исходя из взаимоотношений эндогенной интоксикации и возможностей функциональной системы детоксикации (ФСД) можно выделить 4 стадии развития эндотоксикоза: компенсации, напряжения, субкомпенсации и декомпенсации.
3. ПАТОГЕНЕЗ ЭНДОГЕННОЙ ИНТОКСИКАЦИИ
Механизм И в основном заключается в повреждающем действии эндогенного или экзогенного токсического агента на те или иные клеточные структуры и нарушении метаболических процессов в организме. При некоторых видах И повреждение клеток может иметь характер некроза (напр., при воздействии четыреххлористого углерода на печень), однако, в большинстве случаев происходят обратимые изменения на различных уровнях организма от субклеточного до системного, которые приводят к сдвигам гомеостаза в связи с нарушением метаболизма. Так, в основе мембранотоксического действия афлатоксинов, некоторых бактериальных токсинов, сапонинов лежит нарушение структуры фосфолипидов и образование промежуточных продуктов гидролиза. В механизмах И имеет значение не только непосредственное действие токсических веществ на определенные функции, но и нейрогуморальные и рефлекторные влияния, а также вовлечение в патологический процесс серотонина, кининов и других физиологически активных веществ, выделяющихся в значительных количествах при повреждении клеток и тканей.
В механизмах И имеют значение не только непосредственное действие токсических веществ на определенные функции, но и нейрогуморальные и рефлекторные влияния, а также вовлечение в патологический процесс различных органов и систем. При хронических И некоторыми химическими соединениями, алкилирующими фосфатные группы нуклеиновых кислот (нитрозоэтилмочевина, этилметан-сульфонат и др.), может проявиться их мутагенное действие; при И некоторыми циклическими углеводородами (3,4-бензпирен и др.) – канцерогенное действие.
Развитию И противостоят детоксицирующие системы организма, обеспечивающие химическое превращение токсичных веществ в менее токсичные или растворимые вещества, поддающиеся выведению из организма (окисление, гидролиз, метилирование, восстановление и образование парных соединений и другие процессы). Эти процессы происходят с участием ферментных систем организма, обеспечивающих обезвреживание и метаболические превращения ядовитых веществ. Яды, поступающие в кровь, через воротную вену попадают в печень, являющуюся мощным детоксицирующим барьером, и частично в ней нейтрализуются. И развивается при поступлении в организм токсичных веществ в количестве, превышающем возможности детоксицирующих систем или при их неполноценности.
4. КЛИНИКА ЭНДОГЕНОЙ ИНТОКСИКАЦИИ
5. КЛИНИЧЕСКОЕ ОБСЛЕДОВАНИЕ ПАЦИЕНТОВ С СИНДРОМОМ ЭНДОГЕННОЙ ИНТОКСИКАЦИИ. УРОВНИ ДИАГНОСТИКИ
Диагностика ЭИ разработана главным образом на биохимическом уровне.
В том случае, если состояние не является критическим, для его диагностики целесообразно использовать тот же принцип, что и заложенный в основу распознавания дистресса, т.к., по-видимому, эндогенная интоксикация во многом пересекается с реакцией общего адаптационного синдрома. Мы предлагаем оценивать такие признаки дистресса, главным образом субъективные, которые составляют основу ряда вопросников для диагностики дистресса (табл. 1).
Шкала для диагностики хронической эндогенной интоксикации .
Синдром эндогенной интоксикации (эндотоксемия) - это накопление в крови и тканях организма эндотоксинов.
Эндотоксины – это вещества, которые оказывают отравляющее воздействие на организм. Они, в свою очередь, могут быть продуктами жизнедеятельности самого организма, либо могут попадать в него извне.
Синдром эндогенной интоксикации является одной из острейших проблем в интенсивной терапии, так как сопутствует большому количеству патологических состояний, среди которых: шок, панкреатит, перитонит и пр. Выраженный синдром эндогенной интоксикации способен приводить к гибели человека.
Причины синдрома эндогенной интоксикации

Причины синдрома эндогенной интоксикации могут быть самыми разнообразными. Тем не менее, этот процесс всегда развивается при поступлении эндотоксинов из мест их образования в кровоток. По крови эндотоксины распространяются в органы и системы органов, а также во все ткани организма. Когда количество агрессивных компонентов и эндотоксинов превышает естественные возможности организма в их биотрансформации, наступает синдром эндогенной интоксикации.
Различают следующие причины синдрома эндогенной интоксикации:
Болезни, протекающие с гнойно-воспалительной реакцией в организме. Сюда можно отнести холецистит, острую пневмонию, перитонит, панкреатит и пр.
Тяжелые и сложные травмы: краш-синдром.
Некоторые хронические болезни в стадии обострения, например, сахарный диабет, тиреотоксический зоб.
Первичные механизмы возникновения синдрома эндогенной интоксикации следующие:
Резорбционный механизм. При этом происходит рассасывание токсических веществ (некротических масс, воспалительного экссудата) из ограниченного очага инфекции по всему организму. Этот процесс может быть запущен при кишечной непроходимости, при абсцессах, при флегмоне мягких тканей и пр.
Обменный механизм развития синдрома эндогенной интоксикации. Он обуславливается чрезмерной выработкой токсических веществ. Этот механизм развития характерен для пневмонии, острого панкреатита, разлитого перитонита.
Ретенционный механизм. По такому типу синдром эндогенной интоксикации развивается в том случае, если страдает непосредственно сам процесс выведения токсинов из организма, то есть нарушается работа органов детоксикации.
Реперфузионный механизм. Проникновение эндотоксинов в кровь происходит из тканей, которые продолжительное время находились в состоянии ишемии, при этом антиоксидантный барьер организма утратил состоятельность. Это может происходить при шоковых состояниях, при проведении оперативного вмешательства с использованием АИК и пр.
Механизм вторичной токсической агрессии, при которой ткани отвечают токсической реакцией на воздействие эндотоксинов.
Инфекционный механизм, при котором в качестве эндотоксинов выступают патогенные микроорганизмы из очагов инвазивной инфекции.
Классификация эндотоксинов
Эндотоксины – это те вещества, которые приводят к формированию эндотоксемии и к синдрому эндогенной интоксикации.
Выделяют следующие эндотоксины, в зависимости от механизма их образования:
Ферменты, которые после активации тем или иным патологическим процессом, начинают повреждать ткани. Это могут быть протеолитические и лизосомные ферменты, а также продукты активации калликреин-кининовой системы.
Продукты естественной жизнедеятельности организма могут выступать в качестве эндотоксинов при условии накопления их в высоких концентрациях. Сюда можно отнести мочевину, билирубин и пр.
Все биологически активные вещества, которые имеются в организме человека. Это могут быть медиаторы воспаления, цитокины, простагландины и пр.
Агрессоры, которые возникают при распаде чужеродных антигенов и иммунных комплексов.
Токсины, выделяемые микробами или иными патологическими агентами.
Среднемолекулярные вещества (вирусы, аллергены, холестерин и пр.).
Продукты, которые возникают при перекисном окислении липидов.
Продукты, которые появляются в результате распада клеток при повреждении их мембран деструктивными процессами. Это могут быть белки, миоглобин, липазы, фенол и пр.
Высокие концентрации компонентов регуляторных систем.
Эндотоксины способны оказывать на организм прямое и опосредованное воздействие, они способны повлиять на микроциркуляцию, на процессы синтеза и метаболизма в тканях.
Симптомы синдрома эндогенной интоксикации

Одним из ведущих симптомов эндотоксемии является угнетение сознания. Возможна его полная потеря, либо частичное снижение. Параллельно у больного возникают выраженные головные боли, появляется мышечная слабость, характерна миалгия.
По мере прогрессирования интоксикации организма, присоединяется тошнота и рвота. Так как организм больного теряет жидкость, слизистые оболочки становятся сухими.
Развивается тахикардия или брадикардия. Температура тела может и повышаться, и, напротив, понижаться.
Так как эндогенная интоксикация часто возникает на фоне шокового состояния, то на первый план выходят симптомы эндотоксического шока. В крови при тяжелых состояниях человека однозначно будут присутствовать те или иные эндотоксины бактериальной природы, даже на фоне отсутствия бактериемии. Это не зависит от того, что спровоцировало синдром эндогенной интоксикации: травма, ожог, ишемия тканей и др. Важна лишь степень тяжести состояния человека.
Степени эндогенной интоксикации
Врачи различают три степени тяжести синдрома эндогенной интоксикации, для каждой из которых имеются свои критерии:
Реакция организма возникает в ответ на формирование очага деструкции, либо на полученную травму:

Пульс не превышает 110 ударов в минуту.
Сознание человека сильно не затуманено, он находится в легкой эйфории.
Кожные покровы не изменены, их цвет обычный.
Перистальтика кишечника нарушена и определяется как вялая.
Частота дыхания не превышает 22 вдохов-выдохов в минуту.
Объемы выделяемой в сутки мочи превышает 1000 мл.
Для второй степени эндогенной интоксикации характерно попадание в кровь эндотоксинов, которые поступают в нее из источника интоксикации. С током крови они распространяются по организму и накапливаются во всех тканях:

Пульс учащается и может достигать 130 ударов в минуту.
Сознание больного заторможено, либо, напротив, наблюдается психомоторное возбуждение. Этот параметр зависит от причины возникновения синдрома эндотоксического шока.
Усиливается частота дыхания, количество вдохов-выдохов в минуту составляет от 23 до 30.
Кожные покровы больного бледные.
Суточный объем мочи уменьшается и составляет от 800 до 1000 мл.
Перистальтика кишечника отсутствует.
Эта степень эндотоксикации характеризуется нарушением работы всех органов. Патологический процесс прогрессирует вплоть до развития функциональной мультиорганной дисфункции:

Пульс больного превышает 130 ударов в минуту.
Сознание больного нарушено, начиная от помраченного сознания и заканчивая комой. Это состояние называется интоксикационным делирием.
Дыхание значительно усиливается и превышает 30 вдохов-выдохов в минуту.
Кожные покровы могут иметь цианотичный, либо землянистый оттенок. Не исключена гиперемия дермы.
Суточный объем мочи не превышает800 мл.
Кишечник не функционирует, перистальтика отсутствует.
Диагностика синдрома эндогенной интоксикации

Диагностика синдрома эндогенной интоксикации выстраивается на основе оценки степени тяжести состояния человека по характерным симптомам (оттенок кожных покровов, частота дыхания и сердцебиения и пр.). Кроме того, необходимо проведение анализов крови.
Полученные результаты обрабатываются, и по ним будет наблюдаться изменение таких показателей как:
Значительное увеличение количества лейкоцитов в венозной крови.
Превышение лейкоцитарного и ядерного индекса интоксикации. Хотя иногда эти показатели могут быть заниженными, что свидетельствует о несостоятельности системы кроветворения и о детоксикации организма.
Увеличение индекса интоксикации. Если он превышает отметку в 45, то это однозначно указывает на неминуемый летальный исход.
Необходима оценка концентрации общего белка в плазме крови.
Увеличение уровня билирубина.
Увеличение уровня креатинина и мочевины.
Увеличение концентрации молочной кислоты.
Увеличение коэффициента клеток неспецифической защиты относительно клеток специфической защиты. О тяжелом состоянии больного говорит коэффициент, превышающий 2,0.
Наиболее чувствительным признаком эндотоксикации является увеличение уровня молекулы средней массы.
Лечение синдрома эндогенной интоксикации

Лечение синдрома эндогенной интоксикации предполагает удаление токсических компонентов из организма и из крови с первоначальным снижением их концентрации. Активную детоксикацию назначают при установлении 2 или 3 степени тяжести патологического синдрома.
Биологическая интоксикация всегда базируется на следующих механизмах:
Биологическая трансформация эндотоксических компонентов в печени. Для запуска данного механизма выполняют гемоксигенацию, химическое окисление крови (непрямое), ее фотомодификацию. Возможно проведение перфузии через клеточные взвеси или ксеноорганы.
Связывание и разведение эндотоксических компонентов. С этой целью возможно выполнение сорбционных мероприятий, направленных на выведение эндотоксических компонентов из крови, из плазмы, из лимфы, из ликвора.
Удаление эндотоксических компонентов. Для реализации данного механизма задействуют печень, почки, желудочно-кишечный тракт, кожу и легкие. Пациенту проводят кишечный диализ, гемодиализ, энтеросорбцию, плазмаферез, гемо- и ультрафильтрацию, замещение крови, форсируется диурез.
В период острой интоксикации общий суточный объем воды, которую вводят через капельницу, должен быть на уровне 4-5 литров. Причем 2,5-3 литра должны составлять кристаллоидные растворы, а оставшаяся часть - коллоидные и белковые препараты крови: плазму, альбумин, протеин.
Форсированный диурез считается простым и часто используемым способом лечения эндоинтоксикации, который базируется на применении естественного процесса удаления токсинов из организма.
Прогноз при синдроме эндогенной интоксикации напрямую зависит от тяжести состояния больного и от первопричины, приведшей к развитию патологии.

О враче: С 2010 по 2016 гг. практикующий врач терапевтического стационара центральной медико-санитарной части №21, город электросталь. С 2016 года работает в диагностическом центре №3.
Читайте также:


