Вакцина пневмококковая полисахаридная для профилактики пневмококковых инфекций
Что такое пневмококковая инфекция
Почти полное исчезновение 13 серотипов пневмококка, включ.
Профилактика пневмококковой инфекции
- конъюгированная вакцина, которая рекомендуется для всех детей младше 5 лет
- полисахаридная вакцина, которая рекомендуется для всех взрослых с 65 лет и старше, а также для пациентов старше двух лет, имеющих определенные сопутствующие заболевания, увеличивающие риск пневмококковой инфекции.
Симптомы пневмококковой инфекции
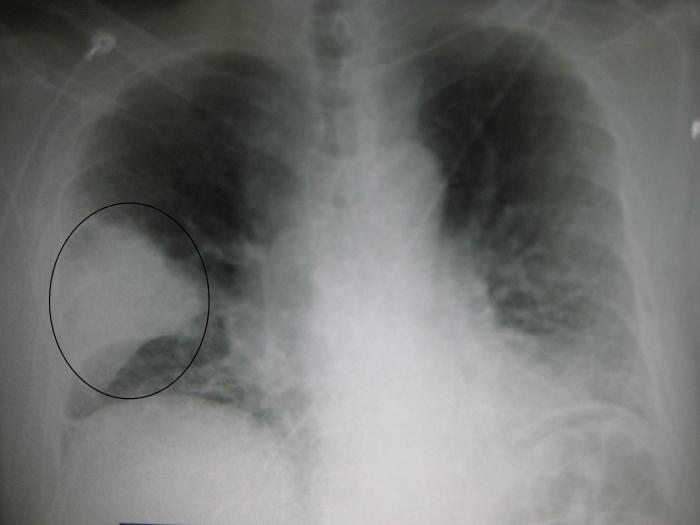
- Легкие (пневмония)
- Среднее ухо (средний отит)
- Придаточные пазухи носа (синусит)
- Кровь (септикопиемия)
- Оболочки головного и спинного мозга (менингит).
Консультативный комитет по практике иммунизации (Advisory Co.
- головную боль,
- ригидность затылочных мышц (невозможность наклонить голову вперед, усиление головной боли при попытках кивания),
- лихорадку,
- спутанность сознания и дезориентацию,
- светобоязнь (резкий дискомфорт от яркого света).
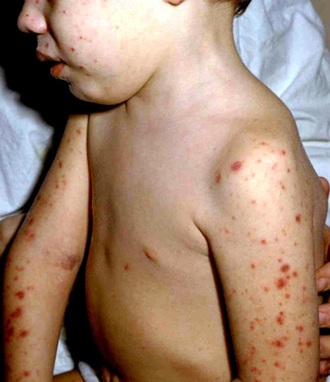
Показания к вакцинации от пневмококковой инфекции
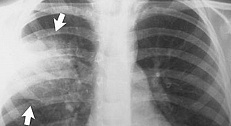
Выводы авторов исследования, которые изучали структуру детск.
- Всех лиц в возрасте 65 лет и старше
- Всех лиц, старше 2 лет, имеющих хронические заболевания, такие как сахарный диабет, болезни сердца, почек, печени или хронические заболевания легких (кроме пациентов с бронхиальной астмой*); а также всех лиц, страдающих от алкоголизма
- Также к группе высокого риска пневмококковой инфекции относятся пациенты с кохлеарным имплантатом, со спинно-мозговым шунтом; а также пациенты, подвергающиеся вдыханию паров металла на работе (например, сварщики).
- Лиц с ослабленным иммунитетом, например ВИЧ-инфицированных, или пациентов со злокачественными новообразованиями
- Лиц с удаленной селезенкой, и/или с серповидно-клеточной анемией
- Детей старше 2 месяцев - 3 дозы с промежутком не менее 1 месяца между ними (по российскому нацкалендарю – в 2 и 4,5 месяца), с последующей ревакцинацией в возрасте 12-15 месяцев (по российскому нацкалендарю – в 15 месяцев). Следует отметить, что российская интерпретация графика вакцинации связана с экономическими причинами и отличается от рекомендаций производителя.
- Детей в возрасте 24-59 месяцев, которые подвергаются высокому риску пневмококковой инфекции.
- Детям в возрасте от 2 до 6 месяцев: 3 дозы вакцины по 0.5 мл каждая, с интервалом между дозами не менее 1 месяца, первая доза обычно вводится в возрасте 2 месяцев. Четвертую дозу (т.е. ревакцинацию) рекомендуется вводить на 2 году жизни, оптимально в 12-15 месяцев.
- Если вакцинация не была начата в первом полугодии жизни, назначение Превенара проводится по следующим схемам.
- Детям в возрасте от 7 до 11 месяцев: 2 дозы по 0.5 мл каждая, с интервалом не менее 1 месяца между введениями. Третья доза (т.е. ревакцинация) рекомендуется на втором году жизни.
- Детям в возрасте от 12 до 23 месяцев: 2 дозы по 0.5 мл каждая, с интервалом между введениями не менее 2 месяцев.
- Детям в возрасте от 2 до 5 лет: 1 доза 0.5 мл однократно.
Безопасность вакцинации
Основные факты о пневмококковой инфекции
- Пневмококковая инфекция вызывается бактериями Streptococcus pneumoniae. Эти бактерии могут проникать в легкие, кровь, ткани и жидкости, окружающие головной и спинной мозг, и вызывать ряд заболеваний, включая пневмонию и менингит.
- Каждый год только в Соединенных Штатах Америки по оценкам экспертов насчитывается 175 000 случаев госпитализации по поводу пневмококковой пневмонии, 34 500 случаев сепсиса и 2200 случаев менингита. Пневмококковая инфекция приводит, приблизительно, к 4800 смертям в США ежегодно.
Использование PCV13 (13-валентной пневмококковой конъюгирова.
- Имеющиеся в настоящее время вакцины против пневмококка безопасны и эффективны, а возрастающее число серотипов, включаемых в эти вакцины, по сравнению с первой лицензированной вакциной PCV7 (Превенар 7), представляет собой значительный прогресс в борьбе с заболеваемостью и смертностью от пневмококковой инфекции в перспективе, особенно в развивающихся странах
- Пневмококковую инфекцию можно предотвратить у взрослых и детей, с помощью введения двух видов безопасных и эффективных вакцин: конъюгированной вакцины для детей в возрасте до 5 лет, или полисахаридной вакцины для детей старше 2 лет, и взрослых.
- Вы не можете заразиться пневмококковой инфекцией при введении вакцины.
- Вакцины от пневмококковой инфекции могут быть введены в любое время года и могут вводиться одновременно с любыми другими вакцинами.
- Разовая доза вакцины рекомендуется для всех людей в возрасте 65 лет или старше. Некоторым людям, которые уже получали вакцинацию против пневмококковой инфекции в возрасте моложе 65 лет, по достижении 65 лет может потребоваться повторение вакцинации.
- Около 20% взрослого населения планеты находится в группе высокого риска пневмококковой инфекции и должны получить вакцину для снижения этого риска.
Читайте также




мион (myonum, LNH; греч. mys, myos мышца) - поперечнополосатое мышечное волокно в совокупности с его базальной оболочкой, кровеносными и лимфатическими капиллярами и нервным аппаратом. [[Категория:Нек.
магнитная запись - фиксирование на ферромагнитном материале последовательности электрических сигналов с целью их последующего воспроизведения; широко применяется для накопления диагностической.
лихорадка денге классическая (f. dengue classica; син.: лихорадка "жирафов", лихорадка костоломная, лихорадка суставная) - клиническая форма лихорадка денге, характеризующаяся двухфазной лих.
[youtube.player]Краткая информация
Заболевания пневмококковой этиологии являются актуальной проблемой практического здравоохранения, что обусловлено ведущей ролью Streptococcus pneumoniae в структуре инфекций дыхательных путей. По мнению экспертов Всемирной организации здравоохранения (ВОЗ), это наиболее часто возникающие бактериальные инфекции у взрослого населения в мире. S. pneumoniae по-прежнему остается основной причиной серьезных заболеваний, в т. ч. бактериемии, менингита и пневмонии.
Представляя серьезную медико-социальную проблему для многих стран, пневмококковые инфекции (ПИ) актуальны и для России. Вместе с тем проблеме ПИ в нашей стране уделяется явно недостаточное внимание, несмотря на имеющиеся достижения в данной области, главное из которых – создание эффективных способов профилактики данных инфекций, направленных на снижение затрат на лечение заболеваний, вызываемых пневмококком, и смертности по этой причине. Доказанная в многочисленных исследованиях эффективность вакцинации против ПИ позволила рассматривать это мероприятие в качестве перспективного и рекомендуемого для внесения в Календарь профилактических прививок.
Определение
Пневмококковая инфекция – группа повсеместно распространенных антропонозных болезней, обусловленных наличием передаваемых воздушно-капельным путем бактерий S. pneumoniae, способных проникать в обычно стерильные среды организма человека, вызывая серьезную патологию с высокой летальностью. Различают 2 формы ПИ – инвазивные (иПИ) (менингит, пневмония с бактериемий, септицемия, септический артрит, остеомиелит, перикардит, эндокардит) и неинвазивные (пневмония без бактериемии, острый средний отит, синусит и т. п.) формы.
Эпидемиология и особенности клинических форм
По данным ВОЗ, самой опасной из всех предупреждаемых вакцинопрофилактикой (ВП) болезней признана ПИ; при этом до внедрения универсальной вакцинации ПИ ежегодно являлась причиной смерти 1,6 млн человек, из которых от 0,7 до 1 млн составляли дети.
Показатель летальности при иПИ может быть высоким – от 20 % при септицемии до 50 % – при менингите в развивающихся странах. Показатели смертности наиболее высоки у детей раннего возраста и лиц старше 65 лет.
Пневмококк играет первостепенную роль в качестве возбудителя пневмонии. По данным зарубежных и отечественных авторов, этот возбудитель является причиной 25–35 % всех внебольничных и 3–5 % госпитальных пневмоний.
Наиболее тяжело внебольничная пневмония протекает у лиц пожилого возраста (с возрастом человек становится более подверженным развитию тяжелых инфекций), а также на фоне сопутствующих заболеваний (хронические бронхообструктивные, онкогематологические сердечно-сосудистые заболевания, вирусные инфекции, сахарный диабет (СД), болезни почек и печени, инфекция вирусом иммунодефици- та человека (ВИЧ), алкоголизм и т. п.) Так, риск развития иПИ увеличивается при бронхиальной астме (БА) в 2 раза, хронической обструктивной болезни легких (ХОБЛ) – в 4 раза, легочном фиброзе – в 5 раз, саркоидозе и бронхоэктазах – в 2–7 раз. Установлена прямая связь частоты иПИ с возрастом, курением и лечением системными или ингаляционными глюкокортикостероидами. У пожилых больных отмечается в 3–5 раз более высокий риск развития летального исхода от пневмонии и ее осложнений по сравнению с лицами молодого возраста
У работников промышленных предприятий с профессиональным контактом с парами металлов, минеральной или любой другой пылью или газообразными веществами отмечается быстрое распространение респираторных инфекций и тяжелое течение этих заболеваний. Загрязнение рабочей зоны аэрозольными частицами вносит существенный вклад в развитие и распространение не только спорадических случаев ПИ, но и групповых заболеваний.
Пациенты с ХОБЛ составляют 20,5–25,7 % госпитализированных с внебольничной пневмонией, при этом 30-дневная летальность составляет примерно 9,6 % случаев. Среди пациентов, поступающих в стационары по поводу пневмонии, у 15,8 % отмечается ишемическая болезнь сердца (ИБС), у 14,3 % – хроническая сердечная недостаточность, у 9,6 % – СД, при этом летальность составляет 15–30 %. Доказан патогенез развития кардиальных осложнений при пневмококковой пневмонии, которые могут при- вести к летальному исходу. Пневмония, вызванная S. pneumoniae, чаще других осложняется эмпиемой легких и приводит к летальному исходу (до ⅔ случаев для эмпиемы). Жизнеугрожающей формой ПИ является пневмококковый сепсис с развитием тяжелого шокового повреждения органов. От пневмококкового менингита в РФ умирают 60 % заболевших взрослых в возрасте старше 65 лет.
Механизм передачи пневмококков – аэрозольный, путь передачи – воздушно-капельный. Возбудитель передается от источника к восприимчивым лицам при тесном общении, кашле, чихании и т. д.
Большинство случаев ПИ являются спорадическими. Вспышки ПИ характерны для лиц, находящихся в т. н. организованных (закрытых) коллективах (дома ребенка, детские сады, школы, студенческие общежития, воинские коллективы, учреждения уголовно-исполнительной (пенитенциарной) системы, стационары длительного пребывания, интернаты, дома для престарелых лиц и т. п.). В этих же коллективах определяется наиболее высокий уровень носительства пневмококка.
Распределение заболеваемости ПИ по месяцам неравномерно, максимальный уровень заболеваемости регистрируется в холодный период времени (ноябрь–февраль), минимальный – в теплые месяцы (июль–август). Внутригодовая динамика заболеваемости ПИ коррелирует с таковой при гриппе и острых респираторных заболеваниях.
Основным средством сдерживания распространения ПИ на сегодняшний день остается вакцинопрофилактика
Характеристика вакцин для профилактики пневмококковой инфекции
В настоящее время с целью специфической профилактики заболеваний, вызванных пневмококком, у взрослых применяются вакцины 2 типов: полисахаридная 23-валентная (ППВ-23) и полисахаридная конъюгированная адсорбированная 13-валентная (ПКВ-13).
Полисахаридные вакцины содержат высокоочищенные капсульные полисахариды (по 25 мкг каждого) в качестве антигенов, которые активируют В-лимфоциты, запуская продукцию иммуноглобулинов (Ig) классов М и G. Основу действия ППВ составляет Т-независимый иммунный ответ. Иммунитет приобретается через 10–15 дней после однократной вакцинации и со храняется в течение ≥ 5 лет.
Показания к применению – заболевания и состояния, предрасполагающие к развитию ПИ у лиц старше 2 лет. Способ введения – подкожное или внутримышечное (преимущественно) введение в область дельтовидной мышцы плеча.
В основе действия конъюгированных вакцин лежит Т-зависимый ответ. В результате конъюгации полисахаридов с белком-носителем формируется качественно другой по сравнению с ППВ иммунный ответ. Антигенпрезентирующая клетка распознает полисахаридный антиген, захватывая белок-носитель, одновременно обрабатывая и презентуя его Т-клеткам в составе с молекулами комплекса гистосовместимости.
Т-клетки, в свою очередь, обеспечивают необходимые процессы для переключения классов антител преимущественно с IgM- и IgG2- на IgG1-типы, связанные с более высоким уровнем бактерицидной активности сыворотки, а также для родственного созревания
и выработки В-клеток памяти. Кроме того, происходит прайминг для последующей ревакцинации, что выражается в очень быстром нарастании титра антител с высокой активностью при последующей вакцинации ПКВ. ПКВ-13 содержит полисахариды 13 серотипов пневмококка. Вакцина не содержит консерванта. Показания к применению – профилактика ПИ, вызванной серотипами, включенными в состав вакцины у детей старше 2 мес. жизни, и взрослых. Способ введения – внутримышечно. Рекомендуемые места введения – переднебоковая поверхность бедра (у детей первых 2 лет жизни) или дельтовидная мышца плеча (у детей старше 2 лет и взрослых).
Вводится однократно, необходимость ревакцинации не установлена. Возможно подкожное введение ПКВ-13 пациентам с нарушениями в системе свертывания крови (гемофилия, тромбоцитопения, лечение антикоагулянтами). Пациентам, ранее иммунизированным ППВ-23, по показаниям следует вводить ПКВ-13, но не рранее чем через 1 год после последней дозы ППВ-23.
Специфическая вакцинопрофилактика пневмококковой инфекции
Вакцинация признана наиболее эффективным методом предупреждения ПИ. Согласно позиции ВОЗ, вакцинация – единственный способ существенно повлиять на заболеваемость и смертность от ПИ и снижение уровня резистентности к АБП. Имея подтверждение безопасности и эффективности пневмококковых вакцин, специалисты ВОЗ и UNICEF считают необходимым включать пневмококковые вакцины с подтвержденным профилем безопасности и эффективности во все национальные программы иммунизации.
При проведении ВП ПИ необходимо руководствоваться действующими нормативными и методическими документами по организации иммунизации, прежде всего – Национальным календарем профилактических прививок и Календарем профилактических прививок по эпидемическим показаниям, а также инструкциями по применению иммунобиологических препаратов.
В Российской Федерации вакцинация против ПИ всех взрослых лиц, достигших возраста 50 лет, и пациентов групп риска (в т. ч. ВИЧ-инфицированных) в настоящее время включается в качестве обязательного мероприятия в клинические рекомендации и стандарты оказания медицинской помощи по терапии, кардиологии, неврологии, онкологии, онкогематологии, нефрологии, пульмонологии, аллергологии, иммунологии, эндокринологии и трансплантологии.
Вакцинация против ПИ направлена на предупреждение возникновения генерализованных форм пневмококковой инфекции (иПИ), пневмоний, снижение заболеваемости, инвалидизации и смертности населения от этих инфекций. Согласно данным ВОЗ по разным странам, убедительно показано, что специфическая ВП является наиболее доступным и экономичным способом профилактики ПИ. Это подтверждается также результатами отечественных исследований..
Группы риска по развитию пневмококковой инфекции у взрослых
Вакцинация пневмококковой вакциной рекомендуется лицам с высоким риском развития иПИ. Таких пациентов можно разделить на 2 группы: иммунокомпетентные и иммунокомпрометированные.
К группе иммунокомпетентных относятся следующие пациенты:
- с хроническими бронхолегочными заболевания- ми (ХОБЛ, БА) с сопутствующей патологией в виде хронического бронхита, эмфиземы, при частых рецидивах респираторной патологии;
- с сердечно-сосудистыми заболеваниями (ИБС, сердечная недостаточность, кардиомиопатия, хроническая сердечная недостаточность и т. п.);
- с хроническими заболеваниями печени (включая цирроз);
- с СД и ожирением;
- направляемые и находящиеся в специальных условиях пребывания: организованные коллективы (военнослужащие и призывники, лица, работающие вахтовым методом, пребывающие в местах заключения, социальных учреждениях – домах инвалидов, домах сестринского ухода, интернатах и т. д.);
- страдающие алкоголизмом;
- курильщики;
- работники вредных для дыхательной системы производств (с повышенным пылеобразованием, мукомольные и т. п.), сварщики;
- медицинские работники;
- в возрасте 65 лет и старше;
- реконвалесценты острого среднего отита, менингита, пневмонии;
К группе иммунокомпрометированных относятся следующие пациенты:
- с врожденными и приобретенными иммунодефицитами (в т. ч. ВИЧ-инфекцией и ятрогенными иммунодефицитами);
- получающие иммуносупрессивную терапию, включающую иммунобиологические препараты, системные глюкокортикостероиды (≥ 20 мг преднизолона в день), противоопухолевые препараты;
- страдающие нефротическим синдромом / хронической почечной недостаточностью, при которой требуется диализ;
- с кохлеарными имплантами (или подлежащие кохлеарной имплантации);
- с подтеканием спинномозговой жидкости;
- страдающие гемобластозами, получающие иммуносупрессивную терапию;
- с врожденной или приобретенной (анатомической или функциональной) аспленией;
- страдающие гемоглобинопатиями (в т. ч. серповидноклеточной анемией);
- состоящие в листе ожидания на трансплантацию органов или после таковой.
Вакцинация лиц, причисленных к группам риска
Иммунизация против ПИ проводится в течение всего года. Если планируется организация программы массовой вакцинации против гриппа, то удобно провести эту вакцинацию одновременно с иммунизацией против ПИ перед началом сезона острых респираторных заболеваний и гриппа, что соответствует рекомендациям ВОЗ.
Иммунизация против ПИ необходима лицам любого возраста из групп риска развития иПИ. У пациентов с нарушениями иммунологической реактивности или в связи с использованием иммуносупрессивной терапии, генетическими дефектами, ВИЧ-инфекцией или в силу других причин может отмечаться сниженный гуморальный иммунный ответ на вакцинацию.
- У иммунокомпрометированных пациентов любого возраста первоначально рекомендуется однократная вакцинация ПКВ-13, а затем (не ранее чем через 8 нед.) – ППВ-23, через 5 лет необходимо повторное введение ППВ-23.
Противопоказания к проведению вакцинации
Основными противопоказаниями для вакцинации против ПИ являются следующие:
- выраженные, тяжелые системные реакции на предыдущее введение вакцины (анафилактические реакции);
- гиперчувствительность к любому компоненту вакцины;
- острые инфекционные заболевания или обострение хронического процесса (основного заболевания).
Вакцинацию можно проводить через 1–2 нед. после достижения ремиссии или выздоровления от острого инфекционного заболевания. Перенесенная ранее ПИ не является противопоказанием к проведению иммунизации.
В целом частота серьезных нежелательных явлений, зарегистрированных в течение 1 мес. после введения вакцины, составила
[youtube.player]Инструкция
Превенар 13® (вакцина пневмококковая полисахаридная конъюгированная адсорбированная инактивированная, жидкая)
Международное непатентованное (группировочное) название:
Суспензия для внутримышечного введения 0.5мл/доза
Вакцина Превенар 13® представляет собой капсулярные полисахариды 13 серотипов пневмококка: 1, 3, 4, 5, 6A, 6B, 7F, 9V, 14, 18C, 19A, 19F и 23F, индивидуально конъюгированные с дифтерийным белком CRM197 и адсорбированные на алюминия фосфате.
Один шприц (0.5 мл) содержит
активные вещества: пневмококковые конъюгаты (полисахарид + CRM197)
полисахарид серотипа 1
полисахарид серотипа 3
полисахарид серотипа 4
полисахарид серотипа 5
полисахарид серотипа 6А
полисахарид серотипа 6В
полисахарид серотипа 7F
полисахарид серотипа 9V
полисахарид серотипа 14
олигосахарид серотипа 18C
полисахарид серотипа 19A
полисахарид серотипа 19F
полисахарид серотипа 23F
вспомогательные вещества: алюминия фосфат (эквивалентно Al+3), натрия хлорид, кислота янтарная, полисорбат 80, вода для инъекций.
Гомогенная суспензия белого цвета. Допускается наличие белого мутного осадка.
Противобактериальные вакцины. Противопневмококковые вакцины. Пневмококковый очищенный полисахаридный антиген конъюгированный.
Код АТХ J07AL02
Фармакокинетика
Фармакодинамика (иммунологические свойства)
Вакцина Превенар 13® содержит пневмококковые капсульные полисахариды: 7 серотипов, общих с пневмококковой 7-валентной конъюгированной вакциной (4, 6B, 9V, 14, 18C, 19F, 23F), и 6 дополнительных серотипов (1, 3, 5, 6A, 7F, 19A), индивидуально конъюгированные с белком-носителем CRM197.
Введение вакцины Превенар 13® вызывает выработку антител к капсулярным полисахаридам Streptococcus pneumoniae, обеспечивая тем самым специфическую защиту от инфекций, вызываемых включенными в вакцину 1, 3, 4, 5, 6A, 6B, 7F, 9V, 14, 18C, 19A, 19F и 23F серотипами пневмококка.
Согласно рекомендациям ВОЗ для новых конъюгированных пневмококковых вакцин, проведена оценка эквивалентности иммунного ответа при использовании вакцин Превенар 13® и Превенар® по совокупности трёх независимых критериев: процент пациентов, достигших концентрации специфических антител IgG≤0,35 мкг/мл; средние геометрические концентрации иммуноглобулинов (IgG СГК), опсонофагоцитарная активность бактерицидных антител (ОФА титр ≤1:8) и среднегеометрические титры серотип-специфических бактерицидных антител при анализе опсоно-фагоцитирующей активности (СГТ ОФА).
Для оценки эффективности новых пневмококковых конъюгированных вакцин в отношении инвазивных пневмококковых инфекций (ИПИ) у детей ВОЗ рекомендует использовать в качестве эталонной концентрацию полисахаридных капсульных серотип-специфических антител в сыворотке, равную 0.35 мкг/мл, измеренную через один месяц после первичной серии вакцинации. Данная рекомендация основана на выявленной взаимосвязи между иммуногенностью и эффективностью пневмококковой 7-валентной конъюгированной вакцины и экспериментальной 9-валентной конъюгированной полисахаридной вакцины CRM197. Указанная эталонная концентрация применима только в масштабах популяции, ее нельзя использовать для прогнозирования уровня защищенности от ИПИ в индивидуальных случаях.
В клинических исследованиях Превенар 13® вызывал иммунный ответ против всех тринадцати серотипов, входящих в состав вакцины. Иммунный ответ на серотип 3 после бустерной дозы не превышал уровни, наблюдаемые после серии первичной вакцинации; клиническая значимость этого наблюдения в отношении индукции иммунной памяти к серотипу 3 неизвестна.
Для взрослых лиц не определен защитный уровень противопневмококковых антител и используется серотип-специфические СГТ ОФА.
Введение Превенар 13® вызывает выработку иммунного ответа на все 13 вакцинальных серотипов, эквивалентного по вышеуказанным критериям вакцине Превенар®.
Несмотря на то, что идентифицировано более 90 различных серотипов S.pneumoniae, заболевания у людей вызываются относительно небольшой группой серотипов. По результатам оценки наблюдения за серотипами в Европе, проведенной до внедрения Превенара®, Превенар 13® в разных странах охватывает 73–100 % серотипов, вызывающих инвазивные пневмококковые инфекции (ИПИ) у детей в возрасте младше 5 лет и как минимум 50–76 % ИПИ у взрослых. Бактериемическая пневмония (приблизительно 80 % всех случаев ИПИ у взрослых), бактериемия без очага инфекции и менингит являются наиболее частыми проявлениями ИПИ у взрослых. Согласно оценкам, Превенар 13® охватывает более 90 % серотипов, вызывающих антибиотикорезистентную ИПИ.
Острый средний отит (ОСО) является распространенным детским заболеванием с различной этиологией. Бактерии могут обуславливать 60–70 % клинических эпизодов ОСО. S. pneumoniae является одной из наиболее распространенных причин бактериального ОСО по всему миру.
Пневмония является наиболее частым клиническим проявлением пневмококковой инфекции у взрослых. Частота внебольничной пневмонии (ВБП) и ИПИ повышается у пациентов, начиная с возраста 50 лет, и является наибольшей у лиц в возрасте ≥ 65 лет. S. pneumoniae является наиболее частой причиной ВБП и, согласно расчетам, обуславливает приблизительно 30 % всех требующих госпитализации случаев ВБП среди взрослого населения развитых стран.
Риск ВБП и ИПИ также повышается при наличии хронических фоновых заболеваний, в частности анатомической или функциональной асплении, сахарного диабета, бронхиальной астмы, хронической сердечно-сосудистой патологии, заболеваний легких, почек или печени, а наиболее высок он у пациентов с иммунодепрессией, например, при злокачественных гематологических заболеваниях или ВИЧ-инфекции.
Наблюдения, проведенные в США с момента внедрения 7-валентной конъюгированной вакцины Превенар®, позволяют предположить, что наиболее тяжелые случаи инвазивной пневмонии связаны с действием серотипов, включенных в Превенар 13® (1, 3, 7F и 19А), в частности, серотип 3 непосредственно связан с заболеванием некротизирующей пневмонией.
Согласно мета-анализу результатов лечения пациентов с серотип-специфичной пневмонией, серотипы 3, 6A, 6B, 9N и 19F статистически связаны с повышенным уровнем смертности по сравнению с серотипом 14, использованным как эталон. Для серотипов 19A и 23F выявлена тенденция к повышенной смертности, но она не достигает статистической значимости. Несмотря на определенные отличия в уровнях заболеваемости и смертности, данные наблюдения оказались достаточно точной характеристикой серотипов и не зависели от резистентности к антибиотикам.
Резистентность серотипов S.pneumoniae осложняет подбор эффективного антибиотика для лечения. Несмотря на значительную географическую вариабельность распределения серотипов и наличия резистентности к антибиотикам, серотипы 6A, 6B, 9V, 14, 15A, 19F, 19A и 23F наиболее склонны проявлять резистентность к пенициллину и макролидам.
Эффективность Превенар 13®
Инвазивная пневмококковая инфекция (ИПИ)
Через четыре года после внедрения препарата Превенар® с применением двух доз при первичной вакцинации и ревакцинацией на втором году жизни и при охвате вакцинацией 94 % в Англии и Уэльсе сообщалось о снижении на 98 % (95 % ДИ: 95; 99) частоты заболевания, вызванного 7 серотипами вакцины. Впоследствии через четыре года после перехода на Превенар 13® дополнительное снижение частоты возникновения ИПИ в связи с 6 дополнительными серотипами в составе Превенара 13® колебалось от 76 % у детей в возрасте младше 2 лет до 91 % у детей в возрасте 5–14 лет. Не наблюдалось случаев ИПИ, вызванных серотипом 5.
Снижение частоты возникновения ИПИ, вызванных конкретным серотипом, для каждого из дополнительных серотипов в Превенар 13® по возрастным группам приводится в таблице 1; оно колебалось от 68 % (серотип 3) до 100 % (серотип 6А) у детей в возрасте младше 5 лет. Значимое снижение частоты возникновения также наблюдалось в более старших возрастных группах, не получавших вакцинацию Превенар 13® (популяционный эффект).
Таблица 1. Количество серотип-специфичных случаев и снижение частоты возникновения ИПИ в 2013/2014 г. по сравнению с периодом с 2008/2009 г. по 2009/2010 г. (2008/2010 г.) в Англии и Уэльсе с распределением по возрасту
[youtube.player]Аннотация научной статьи по наукам о здоровье, автор научной работы — Рулева Анна Александровна, Перова А. Л.
Пневмококковая инфекция , помимо тяжелых инвазивных форм, способна вызывать менее тяжелые, но широко распространенные неинвазивные заболевания респираторного тракта и служить причиной повторных острых респираторных инфекций (ОРИ) и их осложненного течения. В настоящей статье проанализирован опыт применения пневмококковой полисахаридной вакцины Пневмо 23. Изучалась (на основании записей в медицинской документации) заболеваемость ОРИ в течение 6-12 мес до и после прививки у детей в возрасте 2-14 лет с различной патологией. Продемонстрирована высокая эффективность вакцинации часто болеющих детей и пациентов с аллергическими заболеваниями.
Похожие темы научных работ по наукам о здоровье , автор научной работы — Рулева Анна Александровна, Перова А. Л.
Experience of prophylaxis of acute respiratory infections in children with pneumococcal polysaccharide vaccine
Pneumococcal infection induces both severe invasive diseases and widespread non-invasive disorders of respiratory tract; it can cause recurrent acute respiratory infections (ARI) and their complications. Present article analyzes experience of treatment with pneumococcal polysaccharide vaccine Pneumo 23. Authors studied morbidity with ARI (according to medical documentation) during 6-12 months after vaccination in children 2-14 years old with different pathologies. The study showed high efficacy of vaccination in frequently ailing children and patients with allergic diseases.
А.А. Рулева, А.Л. Перова
НИИ детских инфекций, Санкт-Петербург
Опыт применения пневмококковой полисахаридной вакцины для профилактики острых респираторных инфекций у детей
Пневмококковая инфекция, помимо тяжелых инвазивных форм, способна вызывать менее тяжелые, но широко распространенные неинвазивные заболевания респираторного тракта и служить причиной повторных острых респираторных инфекций (ОРИ) и их осложненного течения. В настоящей статье проанализирован опыт применения пневмококковой полисахаридной вакцины Пневмо 23. Изучалась (на основании записей в медицинской документации) заболеваемость ОРИ в течение 6-12 мес до и после прививки у детей в возрасте 2-14 лет с различной патологией. Продемонстрирована высокая эффективность вакцинации часто болеющих детей и пациентов с аллергическими заболеваниями.
Ключевые слова: дети, пневмококковая инфекция, вакцинация, эффективность.
В настоящее время Россия, как и большинство стран мира, обладает большим нереализованным потенциалом в сфере вакцинопрофилактики — дети все еще страдают от инфекций, распространение которых можно предотвратить. В их числе — пневмококковая инфекция — по-прежнему одна из ведущих причин заболеваемости и смертности. По данным ВОЗ, пневмококковая инфекция является причиной смерти от 1,5 до 2 млн людей в год по всему миру; около 40% случаев смерти приходится на детей в возрасте до 5 лет [1].
Пневмококк (Streptococcus pneumoniae) был открыт примерно 130 лет назад. Сегодня ученым известно более
90 серотипов этого микроорганизма, однако причиной тяжелых заболеваний могут быть лишь некоторые из них (около 30). Пневмококковая инфекция объединяет группу инвазивных и неинвазивных заболеваний. К первой группе относятся пневмония, менингит и бактериемия (септицемия). Согласно международным и российским данным, на внебольничную пневмококковую пневмонию приходится до 76% этиологически расшифрованных случаев болезни среди взрослых пациентов и до 94% — у детей [2]. В структуре возбудителей, вызывающих развитие менингита, пневмококк занимает третье место (после менингококка и гемофильной палочки типа Ь)
A.A. Ruleva, A.L. Perova
Scientific Center of Children's Infections, St.-Petersburg
Experience of prophylaxis of acute respiratory infections in children with pneumococcal polysaccharide vaccine
Pneumococcal infection induces both severe invasive diseases and widespread non-invasive disorders of respiratory tract; it can cause recurrent acute respiratory infections (ARI) and their complications. Present article analyzes experience of treatment with pneumococcal polysaccharide vaccine Pneumo 23. Authors studied morbidity with ARI (according to medical documentation) during 6-12 months after vaccination in children 2-14 years old with different pathologies. The study showed high efficacy of vaccination in frequently ailing children and patients with allergic diseases.
Key words: children, pneumococcal infection, vaccination, efficacy.
(5-20%) [3]. При этом летальность от пневмококкового менингита, по некоторым данным (Санкт-Петербург, 2000-2004 гг.), составляет 7,8%, а полное выздоровление наступает только в 61% случаев [4]. Однако наиболее угрожающей жизни формой пневмококковой инфекции является бактериемия, летальность при которой составляет около 20% [5].
Помимо тяжелых инвазивных форм, регистрируются неинвазивные, менее тяжелые, но более распространенные формы пневмококковой инфекции (средний отит, бронхит, фарингит, синусит). S. pneumoniae является одной из наиболее частых причин развития среднего отита у детей раннего возраста. В посевах содержимого, полученного при пункции у детей с острым средним отитом, пневмококк высевается в 27-52% случаев [6], при остром синусите — в 60% случаев [7]. Пневмококк считается обитателем слизистой оболочки верхних дыхательных путей человека. Его массивная колонизация сдерживается механизмами местной иммунной защиты. Именно носители пневмококка являются резервуаром инфекции и способствуют распространению пневмококковых заболеваний в коллективе и популяции в целом. Частота носительства пневмококка в организованных детских коллективах достигает примерно 50% [8]. Носительство одного серотипа пневмококка может продлиться от 1 до нескольких месяцев, затем микроорганизм элиминируется, что, однако, не препятствует колонизации слизистой оболочки верхних дыхательных путей другим серотипом. Пневмококк может служить причиной повторных острых респираторных инфекций (ОРИ). Согласно данным российских исследований, пневмококки и гемофильная палочка типа b вызывают до 60% всех случаев бактериальных ОРИ [9]. Кроме того, пневмококк является ведущим агентом, вызывающим осложнения при респираторных вирусных инфекциях. Риск развития пневмококкового заболевания особенно повышают гриппозные вирусы, нейраминидаза которых, разрушая сиаловые кислоты, облегчает адгезию пневмококков к клеткам эпителия бронхов.
охватывает 80% серотипов пневмококка, полученных у здоровых носителей и больных ОРИ, и 92% серотипов, полученных у больных острыми бронхитами и пневмониями [11]. В регистрационных испытаниях в Национальном органе контроля иммунобиологических препаратов — ГИСК им. Л. А. Тарасевича — была показана хорошая переносимость вакцины: лишь у 5% привитых регистрировались слабые местные реакции [12].
В настоящее время не только за рубежом, но и в России накоплен значительный опыт применения Пневмо 23. Вакцинация против пневмококковой инфекции может проводиться круглогодично и сочетаться с любыми другими вакцинами. Единственное противопоказание к введению пневмококковой полисахаридной вакцины — гиперчувствительность к любому из компонентов, входящих в состав вакцины или выраженная аллергическая реакция на предшествовавшее введение пневмококковой вакцины.
Ниже представлены результаты влияния вакцины Пневмо 23 на заболеваемость ОРИ у детей с различной патологией.
В ходе наблюдения изучены данные анамнеза и катам-неза 134 детей в возрасте 2-14 лет (средний возраст 3,1 ± 1,9 года), привитых указанной вакциной в Домах ребенка, поликлиниках и НИИ детских инфекций (Санкт-Петребург). В возрасте 2-3 лет было 80 (59,7%) детей, 4-5 лет — 22 (16,4%), старше 5 лет — 32 (23,8%) ребенка. В числе находившихся под наблюдением было 44 часто и длительно болеющих ребенка (ЧБД) с хронической патологией ЛОР-органов (возраст 4,9 ± 1,5 года), 39 детей с патологией ЦНС (резидуально-органическое поражение ЦНС, микроцефалия, детский церебральный паралич, эпилепсия; возраст 4,8 ± 1,7), 19 инфицированных ВИЧ (3,4 ± 0,7 года), 18 — с аллергопатологией (бронхиальная астма, атопический дерматит, пищевая аллергия; 5,4 ± 3,4 года), 9 — с патологией сердечно-сосудистой системы (врожденные пороки сердца, миокардиоди-строфия; 3,6 ± 1,4), 1 — с лимфобластным лейкозом и 4 здоровых ребенка. Иммунизация проводилась только вакциной Пневмо 23 (п = 92) или в сочетании с вакцинами против гемофильной инфекции типа Ь (Акт-ХИБ, Хиберикс; п = 30) или противогриппозными вакцинами (Гриппол, Ваксигрип, Инфлювак; п = 12) по рекомендациям педиатра и при желании родителей (табл. 1). Большинство привитых перенесли вакцинацию бессимптомно, в единичных случаях регистрировались обычные поствакцинальные реакции, которые сохранялись в течение 1-3 суток и купировались самостоятельно. Общие реакции в виде повышения температуры зарегистрированы у 4 (3%) детей, все соответствовали реакциям средней силы (37,6-38,5°С). Местные реакции отмечались у 2 (1,5%) детей в виде уплотнения размером до 5 см и болезненности кожи в месте введения вакцины.
У всех детей проведена оценка заболеваемости ОРИ в течение 6-12 мес до и после вакцинации. Случаи ОРИ фиксировались на основании записи в медицинской документации (форма 112/у), а также после опроса родителя ребенка по телефону.
Для оценки эффективности иммунизации Пневмо 23 все дети были разделены на несколько групп в зависимости от динамики частоты заболеваний в поствакци-нальном периоде:
1) снижение частоты заболеваний (болеет реже);
2) снижение тяжести заболеваний, отсутствие осложнений (болеет легче);
Группа Пневмо 23, абс. Пневмо 23 + Акт-ХИБ / Хиберикс, абс. Пневмо 23 + ПГВ, абс.
Патология ЦНС 38 1 -
Аллергопатология 11 7 -
Кардиопатология 8 - 1
ВИЧ инфицированные 9 10 -
Примечание. ПГВ — противогриппозные вакцины (Гриппол, Ваксигрип, Инфлювак). В таблице не учтены здоровые дети (п = 4) и ребенок с лимфобластным лейкозом (п = 1).
3) редко болеющие ОРИ как до, так и после прививки (болеет редко);
4) без динамики — болеющие ОРИ так же часто, с осложнениями, как и до вакцинации (болеет часто);
5) увеличение частоты заболеваний после вакцинации (болеет чаще).
Эффективность вакцинации (положительная динамика) в общей группе привитых детей составила 63,4% (табл. 2). Факт отрицательной динамики заболеваемости
у 2 детей можно объяснить началом посещения ими детского дошкольного учреждения сразу после иммунизации. При оценке частоты заболеваемости в группах детей с различной патологией выявлено, что наиболее эффективной (болеют реже, болеют легче), как и следовало ожидать, вакцинация оказалась в группе часто болеющих (35 из 44 детей или 79,6%) и у детей с аллергией (14 из 18 детей или 77,7%) (рис. 1). В группе инфицированных ВИЧ, с патологией ЦНС и сердечно-сосудистой
полноценная защита от пневмококковой инфекции
sanofi aventi s
Больше, чем вакцина против пневмонии
^Надежная защита от 23-х серотипов Streptococcus pneumoniae1
при однократном введении.
Длительность защиты до 5 лет2
Безопасность и хорошая переносимость3
^Рекомендована взрослым и детям старше 2-х лет 4
^Доверие во всем мире.
23-летний опыт применения.
100 стран, 65 млн доз.
Для получения дополнительной информации обращайтесь по адресу:
1. Иммунизация полисахаридной поливалентной вакциной для профилактики пневмококковой инфекции. Методические рекомендации, Роспотребнадзор, 2008. 2. Геппе НМ, Малахов АБ, Пневмококковая инфекция респираторной системы в детском возрасте.
Практическое руководство для врачей, М, 2005.3. Опыт применения вакцин "Пневмо 23" и “Вакси грип”у инфицированных микобактериями туберкулеза детей из групп риска. И.Е Костяная с соавт. Вакцинация №1(19), 2002 4. Инструкция по применению Пневмо 23.
Таблица 2. Динамика заболеваемости ОРИ после вакцинации Пневмо 23 (n = 134)
Динамика заболеваемости Вариант динамики Число детей, абс. (%)
Положительная Болеют реже 61 (45,5)
Болеют легче 24 (17,9)
Отсутствует Болеют редко 29 (21,6)
Болеют часто 18 (13,4)
Отрицательная Болеют чаще 2 (1,5)
системы положительная динамика заболеваемости ОРИ отмечена у 11 (58%), 12 (43,6%) и 4 (44,4%) детей, соответственно. Важно, что у детей с аллергопатологией на фоне вакцинации не было зафиксировано обострений основного заболевания. Из 7 детей с бронхиальной астмой у 1 отмечено снижение частоты приступов после вакцинации, еще у одного стало возможным отменить базисную терапию.
При оценке эффективности вакцинации в зависимости от возраста оказалось, что положительная динамика в группе 2-3-летних детей отмечалась у 53 из 80 (66,3%), в группе 4-5-летних — у 17 из 22 (77,3%), в группе детей старше 5 лет — у 15 детей из 32 (46,8%) (рис. 2).
Рис. 1. Динамика заболеваемости ОРИ в группах детей с разной патологией в течение 6-12 мес после моно- или сочетанной вакцинации
Примечание. ССС — сердечно-сосудистая система; ЧБД — часто и длительно болеющие. Эта и последующая гистограммы построены с использованием программы Statistica 5.0 (StatSoft Inc., США).
Рис. 2. Динамика заболеваемости ОРИ после вакцинации в разных возрастных группах в течение 6-12 мес после моно-или сочетанной вакцинации
Динамика Пневмо 23 (n = 92), абс. (%) Пневмо 23 + Акт-Хиб/ Хиберикс (n = 30), абс. (%) Пневмо 23 + ПГВ (n = 12), абс. (%)
Болеют реже 39 (42) 14 (47) 8 (67)
Болеют легче 15 (16) 6 (2G) 3 (25)
Положительная динамика 54 (59) 20 (67) 11 (92)
Наблюдения показали также, что наиболее эффективным в снижении частоты ОРИ является сочетанное введение Пневмо 23 с вакцинами против гемофильной инфекции тип Ь и особенно — с вакцинами против гриппа, чем иммунизация только одной вакциной Пневмо 23 (табл. 3). Этот вывод подтверждают результаты ряда исследований, в которых изучалась эффективность сочетанной иммунизации против пневмококковой, ХИБ-инфекции и против гриппа у детей с различной хронической патологией 14. Достоверно установлена наибольшая профилактическая эффективность (снижение заболеваемости неспецифическими инфекционными заболеваниями респираторного тракта) сочетанной иммунизации вакциной Пневмо 23 и вакцин против гриппа (Ваксигрип, Гриппол) в группах детей, инфицированных микобактериями туберкулеза [13], больных сахарным диабетом [14] и хроническими заболеваниями почек [15].
Вакцинация Пневмо 23 эффективна по показателю снижения частоты развития ОРИ у детей с различной патологией (ЧБД, патологией ЦНС и сердечно-сосудистой системы, аллергическими заболеваниями, ВИЧ-инфицированных), повышающей риск развития пневмококковой инфекции. Положительная динамика (в виде снижения частоты и тяжести ОРИ в течение 6-12 мес после вакцинации по сравнению с довакцинальным периодом) отмечена у 63% детей. Наибольшая эффективность вакцинации наблюдалась в группах часто и длительно болеющих детей и пациентов с аллергическими заболеваниями. Сочетанная вакцинация Пневмо 23 с вакцинами против гриппа и/или гемофильной инфекции типа Ь продемонстрировала более высокую эффективность в предотвращении частых простудных заболеваний по сравнению с вакцинацией только Пневмо 23.
1. Whitney C. G., Farley M. M., Hadler J. et al. Decline in invasive pneumococcal disease after the introduction of protein-polysaccharide conjugate vaccine // N. Engl. J. Med. — 2003; 348: 1737-1746.
2. Таточенко В. К. Антибактериальная терапия пневмоний у детей // Фарматека. — 2002; 11: 24-26.
3. Tan T. Q., Mason E. O.Jr., Wald E. R. et al. Clinical characteristics of children with complicated pneumonia caused by Streptococcus pneumoniae // Pediatrics. — 2002; 110 (1): 1-6.
4. Вильниц А. А., Иванова М. В., Скрипченко Н. В. и др. Современные клинические особенности пневмококковых и гемофильных менингитов у детей // Эпидемиология и инфекционные болезни. — 2005; 3: 56-58.
5. CDC. Recommendations of the Immunization Practices Advisory Committee: prevention of pneumococcal pisease // MMWR. — 1997; 46: 8.
6. Геппе Н. А., Малахов А. Б. Пневмококковая инфекция респираторной системы в детском возрасте. Практическое руководство для врачей. — М., 2005.
7. Зейгарник М. В. Особенности респираторной формы инфекции некапсульной H. influenzae: Автореф. дис. . канд. мед. наук. — М., 2001. — 24 с.
8. Козлов Р. С. Пневмококки: прошлое, настоящее и будущее. Смоленск: СГМА, 2005. — 128 c.
9. Баранникова Н. В., Деревянкина Г. Н. Влияние сочетанной вакцинации конъюгированной вакцины против ХИБ-инфек-ции и 23-валентной полисахаридной пневмококковой вак-
цины на снижение заболеваемости ОРЗ и внебольничными пневмониями любой этиологии у детей младшего возраста // Вакцинация. — 2009; 2 (58): 9-11.
10. 23-valent pneumococcal polysaccharide vaccine. WHO position paper // Weekly epidemiological record. — 2008; 42 (83): 373-384.
11. Жоголев С. Д., Мосягин В. Д., Демидович В. У. и др. Эффективность применения пневмококковой вакцины в воинских коллективах // ЖМЭИ. — 2003; 2: 36-42.
12. Гольдштейн А. В. Вакцинопрофилактика пневмококковой инфекции // Вакцинация. — 2004; 2 (32).
13. Аксенова В. А. Превентивное лечение детей с латентной туберкулезной инфекцией в комплексе с иммунизацией вакцинами Пневмо 23 и Ваксигрип / Сборник материалов по обмену опытом работы в субъектах РФ: Вакцинопрофилактика инфекционных заболеваний / под ред. Е. Н. Беляева, А. А. Ясинского. — М., 2003.
14. Костинов М. П., Скочилова Т. В., Воробьева В. А. и др. Роль вакцинации против пневмококковой и гриппозной инфекций в клиническом течении сахарного диабета 1-го типа у детей и подростков // Эпидемиология и инфекционные болезни. — 2010; 2: 18-22.
15. Квасова М. А. Формирование иммунного ответа против пневмококковой инфекции и оценка клинического эффекта применения вакцин Пневмо 23 и Гриппол у детей, страдающих гломерулонефритом и хронической почечной недостаточностью: Автореф. дис. . канд. мед. наук. — Н. Новгород, 2006. — 24 с.
ВОПРОСЫ СОВРЕМЕННОЙ ПЕДИАТРИИ /2010/ ТОМ 9/ № 6
[youtube.player]Читайте также:


