Узи при цитомегаловирусной инфекции
В статье проанализированы опубликованные данные по вопросам адекватной диагностики антенатальной и постнатальной цитомегаловирусной инфекции (ЦМВИ), а также лечению острых ЦМВИ у беременной, плода и новорожденного. Представлены отечественные клинические р
The article gives analysis of the data on the issues of relevance of diagnostics of antenatal and postnatal cytomegaloviral infection (CMVI), as well as treatment of acute CMVI in the pregnant, fetus and newborns. National clinical guidelines on diagnostics and treatment of congenital CMVI developed by the Russian Association of antenatal medicine in 2016, were presented; as well as the first unofficial international guidelines on the issues of diagnostics and treatment of congenital CMVI.
Цитомегаловирус (ЦМВ) — чрезвычайно распространенный вирус, поражающий людей всех возрастов и формирующий пожизненную персистенцию в организме инфицированного человека. Считается, что в большинстве случаев персистенция начинается в ранние годы жизни и протекает латентно, не оказывая выраженного патологического влияния на состояние здоровья инфицированного. С другой стороны, доказано, что персистенция вируса может сопровождаться хроническим воспалением, формировать разнообразные многочисленные иммунные дисфункции и определять развитие вторичных иммунных, аутоиммунных и дегенеративных нарушений. Различного рода иммунокомпрометации могут приводить к рецидивам размножения вируса и многообразным клиническим проявлениям с поражением любых органов и систем в любом возрасте.
Особое значение имеют врожденные инфекции детей, которые отличаются высоким риском развития тяжелых генерализованных форм и инвалидизирующих исходов заболевания, таких как потеря слуха, зрения, умственная отсталость, микроцефалия, судорожный синдром и пр. Такие пожизненные проблемы со здоровьем развиваются примерно у каждого пятого ребенка с врожденной цитомегаловирусной инфекцией (ЦМВИ), что определяет потребность в своевременном пренатальном выявлении беременных и плодов с высоким риском развития врожденной ЦМВИ и ранней диагностике и лечении инфекций у новорожденных.
Теоретические дискуссии по вопросам адекватной диагностики антенатальной и постнатальной ЦМВИ, а также лечению острых ЦМВИ у беременной, плода и новорожденного продолжаются с 1990-х гг., но отсутствие единых руководящих принципов затрудняет практическую работу врачей. Российской ассоциацией специалистов перинатальной медицины в 2016 г. выработаны отечественные клинические рекомендации по диагностике и лечению врожденной ЦМВИ. Созданная в рамках 5-й Международной конференции по ЦМВИ (Брисбен, Австралия, 19 апреля 2015) международная группа экспертов на основе консенсусных дискуссий и обзора литературы выработала первые неофициальные международные рекомендации по вопросам диагностики и лечения врожденной ЦМВИ, которые опубликованы в Lancet Infect Dis в марте 2017. Все эти рекомендации будут нуждаться в постоянном обновлении по мере поступления дополнительных данных.
ЦМВ — двухцепочечный ДНК-вирус, член семейства герпес-вирусов (β-герпесвирус человека). Синтез вирусного генома ДНК происходит в ядре клетки-хозяина. Исследования последних лет подтверждают гипотезу о том, что штаммы ЦМВ могут варьировать в их вирулентности, тропизме и патогенном потенциале, который, в свою очередь, вероятно, связан с генетической изменчивостью ключевых для патогенеза генов. Внешняя оболочка вируса содержит множественные гликопротеины, кодируемые вирусом. Гликопротеин B и гликопротеин H, по-видимому, являются основными факторами для формирования гуморального иммунитета — антитела к ним способны нейтрализовать вирус. Эти гликопротеины используют сегодня при разработке анти-ЦМВ-вакцин [3].
Вирус распространяется различными способами: через продукты крови (переливание, трансплантация органов), грудное вскармливание, пролиферацию в местах контактов (кожа, любые слизистые оболочки), перинатально и половым путем. ЦМВИ может протекать в виде первичной инфекции ранее неинфицированных (серонегативных) пациентов, реинфекции или реактивации у инфицированных (серопозитивных) людей; может вызывать острое, латентное и хроническое течение врожденных или приобретенных форм болезни [4].
При острой ЦМВ-инфекции могут поражаться практически все типы клеток человеческого организма — эндотелиальные клетки, эпителиальные клетки, клетки гладкой мускулатуры, фибробласты, нейронные клетки, гепатоциты, трофобласты, моноциты/макрофаги, дендритные клетки и пр. Все типы клеток поражаются и в мозге: нейроны, астроциты, клетки эпендимы, выстилающие желудочки, макроглия, эндотелий капилляров, оболочек, микроглия, сплетения сосудистой оболочки, дендриты и аксоны — т. е. вирус в мозге не имеет избирательной клеточной цели, что объясняет многообразие клинических форм поражения нервной системы у больных [5].
Считается, что ЦМВ реплицируется в эндотелиальных клетках с низкой скоростью, вызывая преимущественно подострые инфекции, однако истинная скорость репликации вируса в клетках определяется эффективностью цитотоксического Т-клеточного иммунитета и степенью иммуносупрессии хозяина. Так, например, на моделях ЦМВИ у животных продемонстрировано, что отсутствие CD4 Т-клеток сопровождалось более тяжелым и стремительным заболеванием ЦМВИ. Известно также, что ВИЧ-инфицированные новорожденные имеют очень высокую частоту врожденной ЦМВИ с высоким риском смерти, неврологических дефектов и прогрессии ВИЧ-инфекции [6–7].
Особое свойство ЦМВИ — способность вызывать депрессию практически всех звеньев иммунитета, резко угнетать продукцию интерферонов (ИНФ), в первую очередь ИНФ-α. Внедрение ЦМВ приводит к иммунной перестройке в виде снижения реакции лимфоцитов на вирусы в связи с угнетением экспрессии антигена макрофагами, подавлением пролиферативной активности лимфоцитов (что коррелирует с тяжестью болезни), угнетением фагоцитарной активности и завершенности фагоцитоза [7].
Доказано, что и первичные и латентные ЦМВИ сами могут индуцировать хронические воспалительные системные реакции с устойчивой иммунной активацией, запускать и поддерживать аутоиммунные процессы, усиливать аллореактивность Т-клеток после трансплантации и, возможно, участвовать в комплексе причин повышения частоты нейродегенеративных состояний с возрастом человека (Jones R. P. The debility cascade in neurological degenerative disease). Установлено также, что ЦМВ-индуцированные иммунные изменения в пожилом возрасте могут отвечать, например, за замедленную элиминацию вируса гриппа из легких, сниженный поствакцинальный иммунитет на гриппозные вакцины, измененную реакцию организма на терапию интерферонами [8].
Многие годы риск развития врожденных инфекций плода ассоциировали преимущественно с первичной инфекцией матери, однако к настоящему моменту не вызывает сомнения, что большая доля врожденных ЦМВИ (до 75%) встречается в условиях рецидивирующей во время беременности материнской инфекции. Допускаются также и экзогенные реинфекции с новыми штаммами ЦМВ — доказательства основываются на молекулярных данных, подтверждающих получение нового штамма вируса.
Вместе с тем степень риска вертикального инфицирования плода в условиях первичной инфекции матери рассматривают по-прежнему как чрезвычайно высокую — в 30–50% случаев острой первичной инфекции беременной развивается врожденная инфекция ребенка. Показано, что ранее существовавший материнский иммунитет хоть и не гарантирует полной защиты, тем не менее обеспечивает снижение риска врожденной ЦМВИ при следующих беременностях на 69% [9].
Недавними исследованиями установлено, что ЦМВ может поражать амниотическую мембрану, ухудшая цитотрофобласт-индуцированный лимфангиогенез и ремоделирование сосудов в плаценте и задерживая правильное развитие клеток — предшественников трофобласта, одновременно вызывает врожденную провоспалительную иммунную реакцию. Это приводит к гипоксии плода, задержке внутриутробного развития и возможным последующим гипоксическим повреждениям головного мозга. Степень поражения плода определяется сроками антенатального инфицирования и вирусной нагрузкой в размножающихся клетках — чем меньше гестационный возраст, тем более выражена альтерация (разрушение) тканей с формированием пороков развития [10]. Особенно быстро ЦМВ достигает максимума в астроцитарных и глиальных клетках, при этом максимальная экспрессия вируса найдена в глиальных клетках развивающегося мозга мышат (что объясняет микрогирию, микроцефалию и другие пороки ЦМВ-инфицированного мозга детей). По мере увеличения срока гестации в клинической картине инфекционного заболевания плода преобладают симптомы системного воспаления с выраженной пролиферацией и экссудацией. У 1/3 умерших от ЦМВИ новорожденных (из них 60% — недоношенные) при морфологическом исследовании выявляют различные пороки развития. У 43% — признаки генерализованной внутриутробной инфекции с геморрагическими и ишемическими инфарктами (в том числе в головном и спинном мозге) [11].
Способность вируса реплицироваться в любых клетках человеческого организма определяет многообразие клинических форм болезни; ЦМВ может вызывать как генерализованные инфекции, так и поражения отдельных органов: печени, головного мозга, сердца, легких, мочеполовых органов, желудочно-кишечного тракта и др.
У беременных острая первичная ЦМВИ протекает чаще бессимптомно (25–50%) или малосимптомно — с неспецифическими проявлениями (обычно лихорадка, астения и головная боль).
Как первичная, так и рецидивирующая ЦМВИ матери может стать причиной антенатальных ультразвуковых признаков поражения плода в результате трансплацентарной инфекции. Самые частые УЗИ-признаки: задержка роста плода, вентрикуломегалия, микроцефалия, перивентрикулярная гиперэхогенность, кальцификаты в мозге, плевральный выпот или асцит, гепатоспленомегалия, гиперэхогенный кишечник и мекониальный илеус и др. Эти УЗИ-аномалии эмбриона прогнозируют тяжелую генерализованную манифестную врожденную ЦМВИ новорожденного с высоким риском формирования инвалидизирующих исходов болезни и смерти. Поэтому первичная острая ЦМВИ во время беременности может являться показанием к ее искусственному прерыванию. Установлено, что около 4% детей с антенатальной ЦМВИ умрут в утробе матери или вскоре после рождения, среди остальных около 60% будут иметь когнитивные дефекты, нейросенсорную потерю слуха и другие неврологические и прочие проблемы [11–12].
Сегодня установлено также, что нейросенсорная тугоухость является прогрессирующим заболеванием и может формироваться в течение 5–6 лет жизни даже у детей, родившихся с бессимптомной ЦМВИ (это связывают с многолетней репликацией ЦМВ в перилимфе), что требует соответствующей длительности наблюдения ребенка.
При инфицировании в поздние сроки гестации ЦМВИ у новорожденного может проявляться и как генерализованная инфекция, и как поражение отдельных органов с нетяжелыми транзиторными симптомами болезни, например, умеренной гепатомегалией, изолированным снижением количества тромбоцитов или повышенным уровнем аланинаминотрансферазы. Возможна и клинически бессимптомная ЦМВИ с изолированной нейросенсорной тугоухостью.
У 10% всех новорожденных в течение первого месяца жизни возникают инфекционные заболевания в результате в основном семейных контактов, в том числе грудного вскармливания. Экскреция ЦМВ с грудным молоком в течение первых недель после родов бывает низкой, достигает максимума к 4–8 неделям, завершается к 9–12 неделям. Считается, что риск трансмиссии вируса коррелирует с вирусной нагрузкой в молоке, передача максимальна при высокой экскреции. У доношенных детей в результате инфицирования ЦМВ через молоко матери формируется, как правило, субклиническое течение инфекции без остаточных явлений; в клинической картине более вероятно развитие энтероколита и транзиторного холестатического гепатита с минимальным цитолизом. Недоношенные дети (вес
И. Я. Извекова 1 , доктор медицинских наук, профессор
М. А. Михайленко
Е. И. Краснова, доктор медицинских наук, профессор
ФГБОУ ВО НГМУ МЗ РФ, Новосибирск
Цитомегаловирусная инфекция в практике врача: современный алгоритм диагностики и лечения/ И. Я. Извекова, М. А. Михайленко, Е. И. Краснова
Для цитирования: Лечащий врач № 4/2018; Номера страниц в выпуске: 90-95
Теги: новорожденные, беременность, инфекция, персистирование
3. Диагностика цитомегаловирусной инфекции
Клиническая диагностика ЦМВИ представляет большие трудности и окончательный диагноз не может быть установлен без лабораторного подтверждения. Поиск маркеров ЦМВИ оправдан у новорожденных, если у них обнаруживаются признаки, которые возможны при врожденной ЦМВИ. К таким признакам можно отнести недоношенность, долго сохраняющуюся желтуху, кровоизлияния на коже, гепатолиенальный синдром, неврологические отклонения и др. Поводом для обследования женщин детородного возраста и беременных является отягощенный акушерский анамнез и осложнения беременности, в частности, выявленные с помощью ультразвукового исследования.
В настоящее время методов лабораторной диагностики ЦМВИ довольно много, но значимость их неодинакова. Наиболее клинически значимыми являются вирусологические методы, имеющие в виду выделение вируса или детекцию его белковых антигенов в культуре клеток, зараженных материалами от больных. Вирусологические методы сочетают с иммунологическими методами, целью которых является определение специфических антител различных классов.
Материалом для лабораторного анализа у новорожденных могут служить кровь из пуповины, венозная кровь, моча, слюна, спинномозговая жидкость; у беременных женщин — кровь, моча, соскоб с канала шейки матки; у родильниц дополнительно обследуется грудное молоко.
Для выделения вируса используется клеточная культура из фибробластов легких эмбриона человека. Однако определение вируса в клеточной культуре по цитопатическому эффекту — длительный процесс (в традиционном исполнении 2—3 недели). Поэтому в последние годы для определения присутствия вируса в клеточной культуре применяют методы, направленные на обнаружение ранних (или предранних) вирусных антигенов. Последние можно выявлять через 24—48 часов от начала культивирования методом непрямой иммунофлюоресценции или иммунопероксидазным методом.
В последнее время широкое распространение получают моле-кулярно-биологические методы, направленные на определение генома вируса. Особенно часто используется полимеразная цепная реакция (ПЦР), как высоко специфический и чувствительный метод, но и при применении этого метода возможны ложноположительные результаты. К тому же надо иметь в виду, что ПЦР, как метод высокочувствительный, выявляет не только ДНК активно реплицирующегося вируса, но и ДНК вируса, пребывающего в фазе латенции. Поэтому метод ПЦР следует, как правило, использовать в дополнение к другим методам лабораторной диагностики ЦМВИ.
С целью обнаружения антител к ЦМВ классов IgM и IgG используют иммуноферментный анализ (ИФА), метод флюоресцирующих антител (МИФ), иммуноблот (ИБ) и другие. Важное диагностическое значение может иметь исследование в динамике парных сывороток с нарастанием титра антител не менее чем в 4 раза.
Следует отметить, что существующие методы диагностики могут иметь разную ценность в зависимости от целей исследования. Например, обнаружение ДНК ЦМВ методом ПЦР в амниотической жидкости, где ее вообще не должно быть, означает инфицирование плода. В то время как выделение ДНК ЦМВ из секрета шейки матки не позволяет оценить активность инфекции.
Выделение вируса из мочи используют для диагностики врожденной и перинатальной инфекции и этот метод признается наиболее эффективным в этих целях.
В настоящее время еще нет четко установившихся взглядов относительно целесообразности широкого использования пренатальной диагностики врожденной ЦМВИ. Пренатальная диагностика ЦМВИ проводится в тех случаях, когда имеется серьезный риск развития врожденной ЦМВИ, особенно при первичной инфекции у матери. Сигналом к такому исследованию могут послужить и данные ультразвукового исследования при выявлении изменений в плаценте и плоде. Пренатальная диагностика проводится в различные сроки беременности, обычно во 2-ом триместре (16—30 недель).
Для получения материала для исследования проводят амниоцентез и кордоцентез. Исследование амниотической жидкости включает: 1) выделение вируса на клеточной культуре с детекцией вирусного антигена или цитопатического эффекта и; 2) выявление ДНК ЦМВ в ПЦР. Исследование крови направлено на: 1) выделение вируса на клеточной культуре и; 2) определение IgM анти-ЦМВ.
Наиболее эффективным для диагностики врожденной ЦМВ при исследовании амниотической жидкости являются прямые методы определения возбудителя — вирусологический и метод ферментной амплификации.
Исследование крови плода является менее результативным, чем исследование амниотической жидкости. Выделить вирус из крови пупочного канатика удается не всегда. Специфические иммуноглобулины IgM удается обнаружить не более чем в 50% случаев доказанной ЦМВИ. К тому же следует помнить, что образование специфических антител IgM анти-ЦМВ начинается с начала второй половины беременности. Определять IgM анти-ЦМВ в более ранние сроки не имеет смысла.
По-видимому, пренатальная диагностика ЦМВИ может найти ограниченное применение. Метод нельзя считать полностью безопасным, и он не позволяет диагностировать врожденную ЦМВИ во всех случаях (эффективность диагностики 75%). Не исключается возможность контаминации материалов, полученных у плода, материнской кровью. Занос инфекции в плод при проведении процедуры также возможен.
Большое значение следует придавать правильной интерпретации полученных результатов лабораторных исследований. Наиболее частым маркером, выявляемым при обследовании женщин, являются специфические иммуноглобулины класса IgG. Если они выявляются в качестве единственного маркера, то это свидетельствует, с одной стороны, об инфицированности цитомегаловирусом, или, иными словами, IgG анти-ЦМВ в этой ситуации становятся индикатором латентной инфекции. С другой стороны, присутствие IgG анти-ЦМВ указывает на наличие гуморального иммунитета к этой инфекции. Обнаружение IgG анти-ЦМВ у детей первого полугодия жизни при отсутствии других маркеров этой инфекции будет указывать на их материнское происхождение.
Нарастание титра специфических антител IgG в динамике в 4 и более раз может свидетельствовать о первичной ЦМВИ, ее реактивации или реинфекции. Труднее оценить значение высоты титра IgG анти-ЦМВ при его изолированном рассмотрении. Если имеется высокий титр специфических IgG при отсутствии других маркеров, то это может указывать на состоявшуюся антигенную стимуляцию, потому как в отсутствие антигенной стимуляции титр специфических антител класса IgG постепенно падает, иногда до столь низкого уровня, что при использовании недостаточно чувствительных тестов они вообще могут не выявляться. Одновременное выявление в сыворотке крови беременных специфических антител классов IgM и IgG указывает на реактивацию ЦМВИ.
Признается, что определение анти-ЦМВ класса IgM — это тест на продуктивную ЦМВИ. Многие исследователи рассматривают IgM анти-ЦМВ как фактор риска по развитию фетальной инфекции, что подтверждается и нашими данными.
Вместе с тем, определение анти-ЦМВ класса IgM, несмотря на широкое распространение, не является безупречным лабораторным методом диагностики продуктивной ЦМВИ. Тест на IgM анти-ЦМВ может давать ложноположительные результаты в силу перекрестных реакций с другими герпесвирусами, а также ложнонегативные результаты, связанные с недостаточной чувствительностью метода (чувствительность не более 75%).
Помимо специфических лабораторных тестов, направленных на верификацию ЦМВ, применяются и другие методы исследования, имеющие целью оценить состояние матери, плода, новорожденного. Эти методы включают:
- клинический анализ крови и мочи;
- биохимическое исследование крови;
- определение иммунного статуса;
- ультразвуковое исследование плода. Важное значение имеет ультразвуковая диагностика, с помощью которой выявляются осложнения беременности и патология плода. И при решении вопроса о сохранении беременности следует учитывать не только результаты лабораторных тестов на маркеры ЦМВИ, но и результаты, полученные другими методами исследования.
За беременными из группы риска проводится систематический вирусологический мониторинг на ЦМВИ с целью своевременного выявления ее активизации. Целесообразные сроки его проведения: 8—12 недель, 23—25 недель, 33—35 недель.
Ультразвуковое исследование плода и плаценты проводится в сроки беременности: до 15 недель, 20—24 недели, 33—35 недель.
Содержание
Цитомегаловирусная инфекция вызывается вирусом герпеса 5 типа.
Изменения в организме при заражении цитомегаловирусом могут происходить различные в зависимости от состояния иммунной системы конкретного человека. Заболевание может вовсе не проявляться никакими симптомами, но также может и сопровождаться тяжелыми нарушениями с поражением разных органов и систем организма.
Причины развития заболевания
Цитомегаловирус является высоко заразным заболеванием, которое может передаваться следующими путями:
- воздушно-капельным
- контактно-бытовым
- половым
- от матери к ребенку внутриутробным путем или в процессе родов
- при проведении медицинских процедур.
Виды цитомегаловируса
В зависимости от клинической картины заболевания выделяются следующие виды цитомегаловируса:
- Врожденный цитомегаловирус.
- Острый цитомегаловирус.
- Генерализованный цитомегаловирус.
Симптомы цитомегаловируса
Симптоматика цитомегаловируса напрямую зависит от состояния иммунитета зараженного человека. При нормальном функционировании иммунной системы цитомегаловирус, как правило, не проявляется какими-либо признаками и не причиняет никакого вреда здоровью носителя.
Симптомы цитомегаловируса схожи с признаками ОРВИ:
- повышенная температура
- насморк
- отек зева
- воспаление шейных лимфоузлов
- увеличение печени и селезенки
- лихорадка
- общая слабость
- мышечные боли
- головные боли
- боли в суставах
- кожные высыпания.
Диагностика цитомегаловируса
Диагностика цитомегаловируса в Клинике ЭКСПЕРТ проводится следующими лабораторными методами:
- полимеразная цепная реакция (ПЦР)
- цитологические анализы слюны и мочи
- серологический анализ сыворотки крови
- другие исследования.
Лечение цитомегаловируса
От цитомегаловируса практически невозможно избавиться полностью после того, как он однажды попадет в организм. На сегодняшний день не существует ни одного терапевтического метода, который позволил бы полностью излечить данную болезнь, поэтому лечение цитомегаловируса проводится в целях облегчения симптоматики, подавления активности вируса и достижения ремиссии.
При нормальном состоянии иммунной системы и отсутствии проявлений заболевания специального лечения не требуется. После выявления цитомегаловируса у пациента иммунолог Клиники ЭКСПЕРТ подбирает ему поддерживающую терапию, направленную на укрепление иммунной системы для поддержания ее нормальной работы.
Для этого наш специалист может назначить пациенту комплекс иммуномодулирующих препаратов. Дозировки препаратов и продолжительность лечения также определяет врач. Кроме того, в процессе терапии пациент должен как можно больше времени проводить на свежем воздухе и правильно питаться.
Прогноз
Для большинства пациентов с цитомегаловирусом прогноз исхода заболевания благоприятен.
Данное заболевание может обернуться тяжелыми последствиями для пациентов с нарушениями в работе иммунной системы, особенно у тех, которые недавно пережили трансплантацию органов.
Профилактика цитомегаловируса
Для профилактики цитомегаловируса иммунолог Клиники ЭКСПЕРТ советует соблюдать следующие рекомендации:
- не допускать близких контактов с зараженным человеком
- избегать случайных и незащищенных половых связей
- пользоваться только индивидуальными гигиеническими принадлежностями
- содержать в чистоте свое тело и свой дом
- тщательно мыть руки с мылом после пребывания на улице
- вести здоровый и активный образ жизни
- регулярно бывать на свежем воздухе
- стараться избегать стрессов
- проводить процедуры закаливания.
При подозрении на цитомегаловирус обратитесь в Клинику ЭКСПЕРТ. Наш опытный иммунолог поставит вам точный диагноз и назначит грамотное лечение, что поможет вам избежать тяжелых последствий для вашего здоровья.
а) Терминология:
1. Сокращения:
• Врожденная цитомегаловирусная инфекция (ЦМВИ)
2. Определение:
• Врожденная инфекция, вызванная трансплацентарной передачей ЦМВ, представителя семейства герпесвирусов:
о Наиболее частый источник внутриутробной инфекции в США
1. Общие характеристики врожденной цитомегаловирусной инфекции (ЦМВИ):
• Лучший диагностический критерий:
о Микроцефалия: спектр и тяжесть повреждения головного мозга зависит от времени инфицирования плода
о Внутричерепные (в 40-70% случаев), перивентрикулярные кальцификаты (субэпендимальные зоны герминального матрикса)
о Аномалии миграции: лиссэнцефалия ↔ пахигирия ↔ полимикрогирия ↔ шизэнцфалические расщелины
о Поражение белого вещества (БВ): задержка миелинизации, демиелинизация
о Атрофия большого мозга, мозжечка
о Перивентрикулярные кисты, вентрикуломегалия, спайки в желудочках, лентикулостриарная васкулопатия
• Гестационный возраст во время инфекции определяет картину повреждения ЦНС:
о До 18 недель → снижение количества нейронов и глии, лиссэнцефалия, малые размеры мозжечка, вентрикуломегалия
о 18-24 недели → аномалии миграции, гипоплазия мозжечка, шизэнцефалия
о Третий триместр → Задержка миелинизации, демиелинизация, перивентрикулярные кисты
о Перинатальная инфекция → задержка созревания миелина, очаги повреждения БВ (астроглиоз)
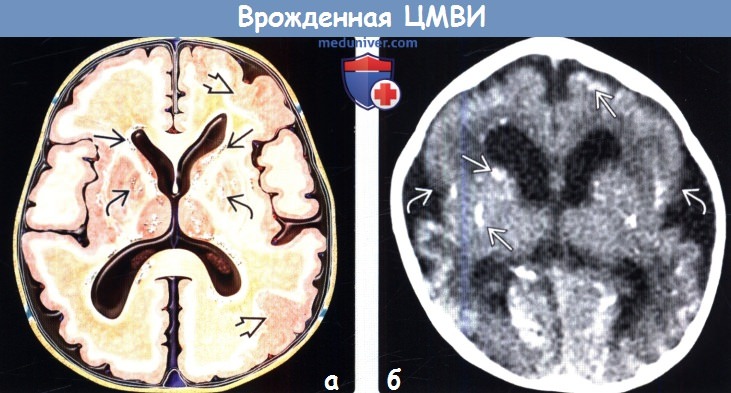
(а) На рисунке аксиального среза изображены многочисленные перивентрикулярные кальцификаты и отложения кальция в базальных ганглиях. Обратите внимание на участки кортикальной дисплазии (полимикрогирия). Расширение желудочков отражает потерю объема смежного белого вещества (БВ). Желтоватые зоны измененного БВ отражают зоны отека, демиелини-зации и/или глиоза.
(б) Бесконтрастная КТ, аксиальный срез: определяются распространенные перивентрикулярные и паренхиматозные кальцификаты. Обратите внимание на открытые сильвиевы щели и упрощенную архитектонику коры в пери-сил ьвиевых отделах. При МРТ была подтверждена полимикрогирия.
2. КТ признаки врожденной цитомегаловирусной инфекции (ЦМВИ):
• Бесконтрастная КТ:
о Внутричерепные кальцификаты (в 40-70% случаев): перивентрикулярные (субэпендимальные) (герминолитические)
о Потеря объема БВ, гиподенсные зоны в БВ, ± перивентрикулярные кисты, вентрикуломегалия
о Аномалии развития коры, извилин
о Гипоплазия мозжечка
3. МРТ признаки врожденной цитомегаловирусной инфекции (ЦМВИ):
• Т1-ВИ:
о Перивентрикулярные субэпендимальные гиперинтенсивные очаги, представляющие собой кальцификаты
о Расширение желудочков и потеря объема перивентрикулярного БВ ± перивентрикулярные кисты
о Гипоплазия мозжечка
• Т2-ВИ:
о Аномалии миграции: лиссэнцефалия, пахигирия, диффузная или очаговая полимикрогирия, шизэнцефалия
о Задержка миелинизации или демиелинизация ± перивентрикулярные кисты (часто в области полюса височных долей)
о Гиперинтенсивные очаги поражения БВ (глиоз/демиелинизация), преимущественно локализующиеся в глубоком БВ теменных долей
о Дисплазия гиппокампа (вертикальная ориентация)
• FLAIR:
о Очаговые, фрагментарные или сливные зоны гиперинтенсивного сигнала, отражающие глиоз ± перивентрикулярные гипо-интенсивные кисты
• Т2* GRE:
о Перивентрикулярное I сигнала, обусловленное Са++
• МРТ-спектроскопия:
о ↓ соотношения NAA: Сг, обусловленное увеличением потери нейрональных элементов, ↑ миоинозитола (глиоз)
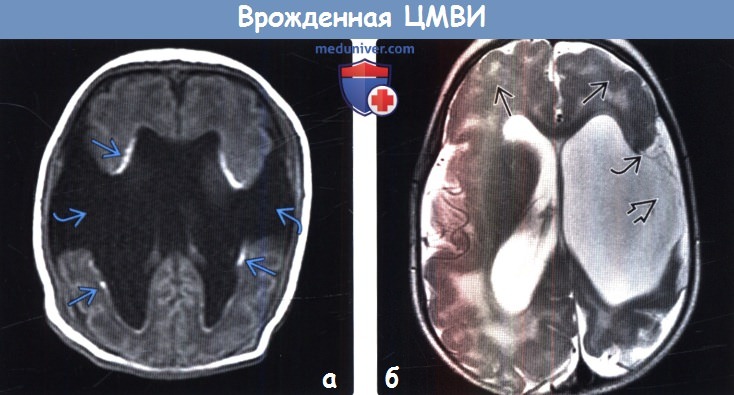
(а) МРТ, Т1 -ВИ: у младенца с врожденной ЦМВИ обнаруживается двусторонняя открытая шизэнцефалия. Обратите внимание на перивентрикулярное повышение интенсивности сигнала, что обусловлено кальцификацией.
(б) МРТ, Т2-ВИ, аксиальный срез: определяется открытая шизэнцефалия левого полушария головного мозга. Расщелина выстлана полимикрогирической корой. Обратите внимание на протяженную двустороннюю полимикрогирию лобных долей. Центральные зоны повышения сигнала от БВ отражают зоны демиелинизации или глиоза.
5. Рекомендации по визуализации:
• Лучший метод визуализации:
о УЗИ для пренатального или неонатального скрининга
о В проведении бесконтрастной КТ необходимость бывает редко
о МРТ головного мозга для комплексной оценки изменений
• Советы по протоколу исследования
о Неонатальная высокоразрешающая нейросонография:
о Бесконтрастная КТ или МРТ с использованием Т2* GRE для обнаружения слабо выраженных кальцификатов или кровоизлияний
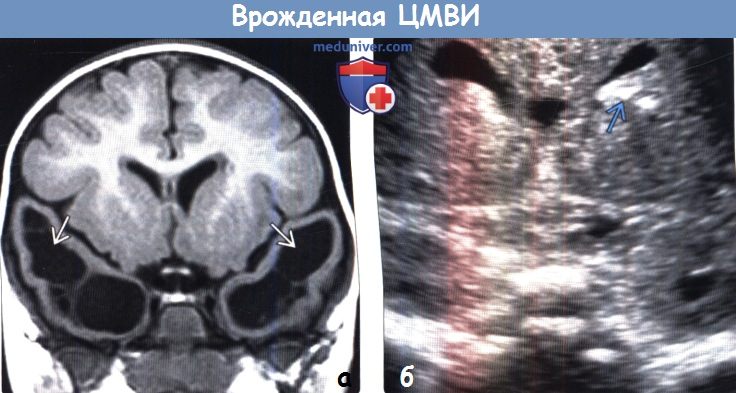
(а) МРТ, Т1-ВИ, корональный срез: у младенца с микроцералией определяются множественные перивентрикулярные полостные герминолитические кисты. Обнаружение этих кист при УЗИ, КТ или МРТ должно побуждать к рассмотрению возможности наличия врожденной ЦМВИ.
(б) Нейросонография, корональный срез: у младенца с врожденной ЦМВИ определяются перивентрикулярные гиперэхогенные очаги, соответствующие кальцификатам.
в) Дифференциальная диагностика врожденной цитомегаловирусной инфекции (ЦМВИ):
1. Врожденный лимфоцитарный хореоменингит:
• Ареновирус, переносимый грызунами: переносится дикими домовыми мышами и хомяками
• Некротизирующий эпендимит приводит к обструкции сильвиева водопровода (макроцефалия в 43% случаев, микроцефалия в 13% случаев)
• При бесконтрастной КТ может очень похоже имитировать ЦМВИ
2. Токсоплазмоз:
• Вызывается протозойными паразитами:
о факторы риска матери включают:
- Контакт с экскрементами кошек во время беременности
- Употребление в пищу сырого или неприготовленного мяса
• В 1/10 случаев частота схожа с ЦМВИ, макрокрания > микрокрания, дисплазия коры встречается реже, церебральные кальцификаты имеют стохастический характер
3. Псевдо-TORCH синдромы:
• Синдромы Берейтсера-Реардона, Айкарди-Гутьерес (плеоцитоз, ↑ α-интерферона в СМЖ)
о Аутосомно-рецессивный характер, прогрессирующая демиели-низация и дегенерация большого мозга и мозжечка
о Кальцификация базальных ганглиев и ствола мозга, перивентрикулярные кальцификаты встречаются менее часто
• Мутации гена OCLN, кодирующего окклюдин:
о Аутосомно-рецессивная микроцефалия
о Полимикрогирия с лентовидными участками субкортикальной кальцификации
1. Общие характеристики врожденной цитомегаловирусной инфекции (ЦМВИ):
• Этиология:
о ЦМВИ - Повсеместно распространенный ДНК-содержащий вирус семейства герпесвирусов
о Нейротропный вирус, который реплицируется в эпендиме, герминальном матриксе, эндотелии капилляров
о Хроническая ишемия вследствие плацентита приводит к вторичной недостаточности перфузии
• Наиболее частая причина внутриутробной инфекции
• Механизмы инфекции:
о Внутриутробная инфекция:
- Первичное инфицирование матери во время беременности или повторная активация латентной инфекции у матери
о Неонатальная инфекция:
- Инфицирование при родах, передача вируса через грудное молоко или при переливании крови
2. Стадирование и классификация врожденной цитомегаловирусной инфекции (ЦМВИ):
• Сроки гестации определяют степень выраженности повреждений:
о Формирование нейронов происходит на 8-20 неделях
о Миграция нейронов - до 24-26 недели
о Образование астроцитов начинается незадолго до окончания процесса формирования нейронов
о Герминальные зоны имеют максимальный размерна 26 неделе
о Образование олигодендроцитов происходит в течение первой половины 3-го триместра
3. Макроскопические и хирургические особенности:
• Микроцефалия
• Инфекция на ранних сроках гестации:
о Некроз герминальных зон, уменьшение количества глии и нейронов, потеря объема БВ
4. Микроскопия:
• Отличительный признак ЦМВИ: цитомегалия с вирусным поражением ядер и наличие цитоплазматических включений
• Фрагментарный и фокальный некроз клеток (в частности, клеток герминального матрикса)
• Воспаление сосудов и тромбоз, сосудистая и субэпендимальная дистрофическая кальцификация
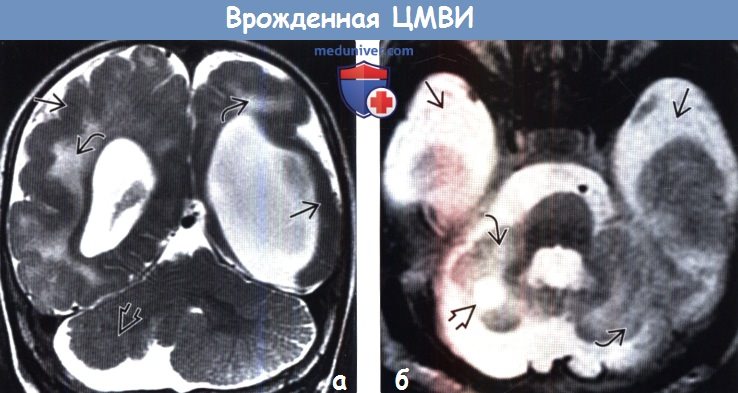
(а) МРТ, Т2-ВИ, корональный срез: определяется вентрикуломегалия, вызванная потерей объема центрального. Повышение сигнала от БВ отражает отек, глиоз или демиелинизацию. Кроме того, визуализируется полимикрогирия. Также обратите внимание на гипоплазию правого полушария мозжечка.
(б) МРТ, Т2-ВИ, аксиальный срез: у новорожденного определяется гипоплазия мозжечка и фокальное кистозное поражение мозжечка. Расширение субарахноидального пространства средней черепной ямки свидетельствует об атрофии височных долей.
д) Клиническая картина:
1. Проявления врожденной цитомегаловирусной инфекции (ЦМВИ):
• Наиболее частые признаки/симптомы:
о Клинические симптомы у большинства инфицированных новорожденных отсутствуют
о У 10% пациентов имеются системные признаки заболевания:
- Гепатоспленомегалия, петехии, хориоретинит, желтуха, задержка внутриутробного развития
о У 55% пациентов с системным заболеванием имеет место поражение ЦНС:
- Микроцефалия, судороги, гипотония или гипертония, ней-росенсорная тугоухость (НСТ)
• Клинический профиль:
о Более высокий риск вертикальной передачи вируса у женщин с серонегативной пробой
• Методы диагностики:
о Однослойная культура клеток для выявления ЦМВ (анализ мочи)
о Поздняя диагностика цитомегаловирусной ДНК методом ПЦР с использованием неонатальной карты Гатри
о Повышение в СМЖ уровня 3-2 микроглобулина, микроцефалия, нейровизуализационные признаки определяют исход
2. Демография:
• Эпидемиология:
о Поражает 1% всех новорожденных (10% из которых имеют признаки и симптомы поражения ЦНС или системного заболевания)
о 40% матерей, заразившихся инфекцией во время беременности, передают вирус плоду
3. Течение и прогноз:
• Три прогностические группы:
о Новорожденные с неврологическими проявлениями (микроцефалия, перивентрикулярное отложение Са++):
- До 95% детей имеют значительные нарушения со стороны неврологического развития
о У новорожденных только с системными проявлениями (гепатоспленомегалия, петехии, желтуха) прогноз более благоприятный, но клиническая картина при этом остается тяжелой
о Инфицированные новорожденные, не имеющие ни неврологических, ни системных проявлений, имеют наиболее благоприятный прогноз, но по-прежнему подвержены риску задержки развития, формирования моторного дефицита и НСТ
о Общая смертность - 5%
4. Лечение врожденной цитомегаловирусной инфекции (ЦМВИ):
• Терапия ганцикловиром инфицированных новорожденных может быть полезна
е) Диагностическая памятка:
1. Обратите внимание:
• Предполагайте врожденную ЦМВИ у отстающих в развитии младенцев с микроцефалией, НСТ
2. Советы по интерпретации изображений:
• Врожденный ЦМВ-энцефалит следует подозревать у ребенка при обнаружении методом МРТ следующих изменений:
о Микроцефалия, аномалии миграции, перивентрикулярные кисты, поражение БВ и гипоплазия мозжечка
• В случае, когда при бесконтрастной КТ обнаруживаются классические признаки ЦМВ-энцефалита, но результаты исследования на предмет (S)TORCH-инфекции отрицательные, следует предполагать:
о Лимфоцитарный хореоменингит (ЛХМ) и псевдо-TORCH синдромы
ж) Список литературы:
- Capretti MG et al: Role of cerebral ultrasound and magnetic resonance imaging in newborns with congenital cytomegalovirus infection. Brain Dev. 36(3):203—11, 2014
- Alarcon A et al: Clinical, biochemical, and neuroimaging findings predict longterm neurodevelopmental outcome in symptomatic congenital cytomegalovirus infection. J Pediatr. 163(3):828—34, 2013
- Fink KR et al: Neuroimaging of pediatric central nervous system cytomegalovirus infection. Radiographics. 30(7):1779—96, 2010
- Lanari M et al: Neuroimaging in CMV congenital infected neonates: how and when. Early Hum Dev. 88Suppl 2:S3-5, 2012
- Manara R et al: Brain magnetic resonance findings in symptomatic congenital cytomegalovirus infection. Pediatr Radiol. 41 (8):962—70, 2011
- Malinger G et al: Imaging of fetal cytomegalovirus infection. Fetal Diagn Ther. 29(2):117-26, 2011
- O'Driscoll MC et al: Recessive mutations in the gene encoding the tight junction protein ocdudin cause band-like calcification with simplified gyration and polymicrogyria. Am J Hum Genet. 87(3)354-64, 2010
- Malm G et al: Congenital cytomegalovirus infections. Semin Fetal Neonatal Med. 12(3)454-9, 2007
Редактор: Искандер Милевски. Дата публикации: 10.4.2019
Читайте также:
- Дельта инфекция может быть у кого
- Что такое дисбактериоз в урологии
- Какие есть инфекционные заболевания кожи у детей
- Снижение заболеваемости управляемыми инфекциями
- Как влияет инфекция на оргазм
 Пожалуйста, не занимайтесь самолечением!При симпотмах заболевания - обратитесь к врачу.
Пожалуйста, не занимайтесь самолечением!При симпотмах заболевания - обратитесь к врачу.

