Урогенитальная инфекция в эко
Бесплодие – состояние организма, возникающее вследствие огромного количества самых разнообразных причин. Одна из них – инфекции. В основном это заболевания, предающиеся половым путём.
Изредка причиной нарушения фертильности становится неспецифическая флора, провоцирующая воспалительные процессы в органах репродуктивной системы.
После незащищенных половых контактов и мужчин, и женщин могут поражать инфекционные заболевания. Бесплодие – одно из наиболее неблагоприятных последствий половых инфекций.
Нередко такие болезни не сопровождаются симптомами. Особенно часто субклиническое их течение наблюдается у женщин.
Поводом для обращения в лечебное учреждение вполне может стать не дискомфорт или выделения из половых путей, а невозможность наступления беременности.
В таком случае патогенные микроорганизмы неожиданно обнаруживаются в ходе комплексного обследования.
- хламидиоз;
- трихомониаз;
- гонорея.
Есть и другие опасные инфекции. Бесплодие они обычно не вызывают, но значительно повышают риск самопроизвольного прерывания беременности, либо формирования у плода пороков развития.
Это вирусные инфекции:
- краснуха;
- цитомегаловирус;
- герпес.
Существуют также инфекции, бесплодие обычно не вызывающие, но опасные тем, что могут передаваться от матери к ребенку во время беременности или родов. В их числе – кандидоз, сифилис, вирусные гепатиты, ВИЧ.
Некоторые инфекции, влияющие на бесплодие, тоже способны заразить плод или новорождённого малыша – это хламидия, микоплазма, гонококк.
У женщин бесплодие обычно связано с поражением маточных труб, при попадании в половые пути инфекции. Причина бесплодия – утолщение стенки труб вследствие их отечности, накопление экссудата в просвете органа. Нарушается проходимость, и сперматозоиды не имеют возможности достичь яйцеклетки.
Такое бесплодие является обратимым. Но длительно протекающие воспалительные процессы могут привести к образованию спаек. В таком случае проходимость маточных труб можно будет восстановить только хирургическим способом (лапароскопия).
Надо сказать, что длительное течение половых инфекций, особенно у женщин, отнюдь не является редкостью, учитывая, что симптомы зачастую полностью отсутствуют, либо выражены очень слабо. У пациентки попросту нет повода для своевременного обращения к врачу, и она может спохватиться лишь тогда, когда обнаружит, что беременность не наступает.
У мужчин инфекции тоже могут вызвать бесплодие.
Доказано, что некоторые возбудители венерических заболеваний способны нарушать подвижность сперматозоидов, это:
- хламидии;
- гонококки;
- трихомонады.
Кроме того, любые инфекции могут спровоцировать обструктивное бесплодие. Обычно это происходит, когда поражены придатки яичек.
Анализы мазков и крови на инфекции выполняются в лаборатории, сертифицированной по международному стандарту качества ISO.
В ходе комплексной диагностики причин бесплодия женщины и мужчины сдают анализы на наиболее распространенные половые инфекции. В случае положительного результата назначается лечение, направленное на уничтожение выявленных возбудителей.
После этого фертильность восстанавливается спустя несколько недель или месяцев, если инфекции не вызывали необратимых изменений в половых органах (формирование спаек в маточных трубах у женщин, в семявыносящих протоках – у мужчин).
Вспомогательные репродуктивные технологии не применяются, пока не будет уничтожен возбудитель инфекции. И ЭКО, и наступление беременности естественным путём противопоказано, потому что бактерии и вирусы способны вызывать внутриутробную инфекцию плода.
В случае развития непроходимости половых путей по причине образования спаек, можно сделать операцию, направленную на восстановление проходимости маточных труб.
Второй вариант – ЭКО. Данная методика искусственного оплодотворения позволяет забеременеть даже в случае, когда имеет место трубный фактор бесплодия.
Бактериальный вагиноз оказывает негативное воздействие на репродуктивный потенциал как фертильных, так и бесплодных женщин, планирующих беременность с помощью вспомогательных репродуктивных технологий. В статье описаны принципы своевременной диагностики и
Bacterial vaginosis has an adverse effect on reproductive potential of women, both of fertile ones, and of infertile ones who plan their pregnancy through assistive reproductive technologies. In this article there are principles of timely diagnostics and 2-phase modern therapy of the women patients.
Микробиоценоз влагалища — это сбалансированная динамичная система, основанная на взаимодействии макроорганизма посредством влагалищного эпителия и микроорганизмов, не вызывающих воспалительную реакцию. Кислая среда как результат этого внутрисистемного взаимодействия обеспечивает благоприятные условия существования для всех участников экосистемы. Следует предположить, что данный симбиоз сложился эволюционно. Одним из проявлений потери равновесия в данной системе является бактериальный вагиноз (БВ).
БВ — общий инфекционный невоспалительный синдром, связанный с дисбиозом влагалищного биотопа и сопровождающийся чрезмерно высокой концентрацией облигатно- и факультативно-анаэробных условно-патогенных микроорганизмов (УПМ) и резким снижением или отсутствием молочнокислых бактерий в отделяемом влагалища [1].
Особенностями эпителиально-бактериальных взаимодействий при БВ являются: стимуляция способности к биопленкообразованию ассоциативных микросимбионтов и резкое угнетение свойств лактобактерий, продуцирующих Н2О2 [3].
По данным различных авторов, на долю БВ приходится от 1/3 до 1/2 всех вульвовагинальных инфекций нижнего отдела половых путей [3, 6, 9]. С проблемой БВ сталкиваются врачи различных специальностей, но чаще акушеры-гинекологи и дерматовенерологи. Так, в странах Европы и США выявление БВ в клинике венерических болезней составляет 33–64%, в общей гинекологической клинике — 15–23%, по данным службы планирования семьи — 23–29%, в акушерской клинике — 10–26% [1].
Причины и патогенез развития БВ дискутабельны.
На современном этапе БВ можно рассматривать как синдром с полимикробной этиологией [2], поэтому при постановке диагноза пациентке могут возникнуть сложности с интерпретацией клинических и лабораторных данных. В мировой медицинской практике с 1983 г. пользуются клинико-лабораторными критериями, предложеными R. Amsel (критерии Амселя), которые включают клинический, клинико-лабораторный и лабораторный аспект диагностики. Успешной является балльная система диагностики, предложенная в 1991 году R. P. Nugent и соавт., — Nugent’s Diagnostic Criteria for Bacterial Vaginosis (диагностические критерии бактериального вагиноза Нугента). Основывается она на лабораторных критериях и широко используется во всем мире. В России Е. Ф. Кира в 1995 г. была предложена оригинальная классификация [4], сочетающая в себе микробиологическую интерпретацию вагинального мазка, клиническую картину и конкретную нозологическую форму (табл.).
Безусловным признаком БВ на сегодняшний день является определение во влагалищных выделениях методом полимеразно цепной реакции (ПЦР) Atopobium vaginae и Clostridium phylum. К высокоспецифичным маркерам БВ также относят ферменты муциназу и сиалидазу.
Лабораторным методом выбора для диагностики БВ является микроскопия вагинального мазка, окрашенного по Граму, и выявление в мазке ключевых клеток (1, 5, 25). Так называемые ключевые клетки (Glue cells) — эпителиальные клетки влагалища, плотно покрытые грамвариабельными палочками. Чувствительность и специфичность метода близки к 100%. Дополнительными признаками при бактериоскопии мазков являются:
- преобладание эпителиальных клеток над лейкоцитами;
- обнаружение при увеличении с иммерсией менее 5 лактобацилл в поле зрения.
Отмечено, что примерно 20% женщин репродуктивного возраста страдают БВ. В 35–50% наблюдений заболевание ассоциируется с другими урогенитальными инфекциями: гонореей, хламидиозом, уреаплазмозом, трихомониазом, папилломавирусной инфекцией и др.
Вторая половина пациенток не предъявляет жалоб, но имеет прямые признаки вагиноза, определяемые с помощью лабораторных методов исследования. Именно с такими пациентками чаще всего сталкивается репродуктолог, обследуя пациентку перед экстракорпоральным оплодотворением (ЭКО). Все пациентки с БВ нуждаются в немедленной комплексной санации с восстановлением нормального биоценоза влагалища, так как установлено, что бактериальный вагиноз может являться основой репродуктивных потерь вне зависимости от клинического течения. При этом осложнения возникают по одному сценарию: снижение колонизационной резистентности микробиоты влагалища → условия для восходящего инфицирования слизистой оболочки матки и маточных труб → воспалительные заболевания органов малого таза (острые эндометрит и сальпингоофорит). Исследования ряда авторов показали, что БВ может привести к развитию самопроизвольного выкидыша, преждевременных родов, хориоамнионита, послеродового эндометрита и рождению детей с низкой массой тела, возникновению воспалительных процессов половых органов, гнойно-септических осложнений у матери и ребенка в послеродовом периоде и т. д., влияя на частоту акушерской и неонатальной патологии [2]. В зоне риска находятся также женщины с БВ, которым предстоят манипуляции на влагалище и матке. Сюда можно отнести женщин после трансвагинальной пункции и переноса эмбрионов в программе ЭКО. Каждое из перечисленных осложнений может привести к нарушению репродуктивной функции женщины вплоть до бесплодия либо усугубить имеющиеся нарушения репродуктивной системы.
Заслуживает интерес точка зрения, согласно которой кислая среда влагалища выполняет роль дополнительного фактора отбора во время зачатия, так как считается, что преодолеть кислотный барьер может только самый подвижный и здоровый сперматозоид. В связи с ощелачиванием влагалища эта функция теряется, и яйцеклетку может оплодотворить и неполноценный сперматозоид, что может повлиять на исход беременности и здоровье новорожденного.
Успешное лечение БВ, как и любого заболевания, зависит от правильной и своевременной постановки диагноза и проведения патогенетически обоснованной терапии. Цель лечения БВ — восстановить нормальную микрофлору влагалища, задержать рост микроорганизмов, не свойственных этому микроценозу. Терапия БВ остается нелегкой задачей ввиду частого рецидивирования или низкой эффективности ряда предложенных препаратов.
Результаты лечения БВ значительно улучшаются при использовании двухэтапного метода комплексной этиотропной и патогенетической терапии, разработанного в 1995 г. Е. Ф. Кира:
1) ликвидация возбудителей БВ (облигатно-анаэробный компонент микрофлоры влагалища);
2) восстановление биоценоза влагалища.
Эффективность комплексной двухэтапной терапии составляет по данным различных авторов от 85,8% до 92,6%. В то время как частота рецидивов после окончания полного курса лечения снижается до 4,4–13,2%.
Следует помнить, что результаты качественной ПЦР и бактериологическое исследование без количественных характеристик не являются поводом для назначения антибактериальных препаратов. Нередки случаи, когда дисбиоз влагалища становится результатом необдуманного ятрогенного воздействия. При нормобиоценозе общая микробная обсемененность не должна превышает 10 6 –10 8 КОЕ/мл, преобладают лактобациллы (более 10 7 КОЕ/мл), а условно-патогенные микроорганизмы определяются в низком титре (10 4 –10 5 КОЕ/мл) или отсутствуют. При БВ общая обсемененность достигает 10 9 –10 11 КОЕ/мл с преобладанием вагиноз-ассоциированной флоры.
Препаратами первого этапа для этиотропной терапии БВ являются медикаментозные препараты против анаэробной микрофлоры. Оптимальны в этом отношении метронидазол, клиндамицин, орнидазол, Поливидон-йод, Хлоргексидин [7]. Клиническая и бактериологическая эффективность указанных препаратов достигает 85–94%. Одновременно с применением антибактериальной терапии проводится системная профилактика вагинального кандидоза [9].
Многочисленные работы последних лет свидетельствуют о том, что препаратами выбора в настоящее время считаются метронидазол и клиндамицин [1, 5, 8].
Эффективным препаратом для лечения БВ является метронидазол (Метрогил® или Трихопол®), который относится к группе антибактериальных препаратов, содержащих имидазольное кольцо. Проникая внутрь микробной клетки, метронидазол превращается в активную форму, связывается с дезоксирибонуклеиновой кислотой и блокирует синтез нуклеиновых кислот. Он широко применяется в различных схемах, причем описана эффективность препарата как при разовых схемах в дозе 2 г, так и при 7-дневных курсах лечения по 500 мг внутрь 2 раза в день. Однако пероральное применение препарата нередко вызывает нежелательные лекарственные реакции (НЛР), такие как металлический вкус во рту, диспепсические расстройства, аллергические реакции, тем самым ограничивая его использование. В результате многочисленных исследований установлено, что влагалищный путь лечения БВ не уступает по эффективности пероральной терапии. Кроме того, влагалищный путь лечения является более предпочтительным из-за меньшей вероятности развития НЛР.
Возможен комбинированный метод лечения: одновременное назначение в течение 7–10 дней пероральной формы метронидазола (Метрогил® или Трихопол® 250 мг 2 раза в день) и вагинальной формы (метронидазол + миконазол), представителями которого являются препараты семейства Нео-Пенотран (Нео-Пенотран®, Нео-Пенотран Форте®, Нео-Пенотран Форте Л®).
Комбинированный метод лечения увеличивает эффективность лечения бактериального вагиноза.
Использование монотерапии только вагинальными формами имеет свои преимущества — снижение рисков возникновения побочных реакций, наступающих при пероральной монотерапии метронидазолом.
Высокоэффективным препаратом, позволяющим быстро восстановить биоценоз, сведя к минимуму НЛР, является клиндамицин в виде вагинальных суппозиториев 100 мг или 2% вагинального крема (Клиндацин®) — антибиотик группы линкозамидов. Данный препарат хорошо зарекомендовал себя при лечении рецидивирующего БВ, в том числе и у беременных женщин. Известно, что он обладает выраженной антибактериальной активностью, подавляя синтез белка в микробной клетке, взаимодействуя с 30S-субъединицами рибосом. Этим обусловлен его широкий спектр действия: Staphylococcus spp., Streptocoссus spp. (кроме Enterocoссus), Streptocoссus pneumonia, Corynebacterium diphtheriae, споро- и неспорообразующие анаэробы, микроаэрофильные грамположительные кокки, фузобактерии, актиномицеты и др. Среди НЛР описаны аллергические реакции, рост дрожжеподобных грибов и т. д. Использование препарата 1 раз в день и короткий курс лечения 3–7 дней обуславливают высокую комплаентность клиндацина.
Перорально клиндамицин назначается в дозировке 300 мг 2 раза в день. Курс лечения 7 дней.
В настоящее время при лечении БВ возможно использование и других препаратов группы нитроимидазола (тинидазол, орнидазол).
Препаратом комбинированного типа с антибактериальной и антимикотической активностью является также Полижинакс (неомицина сульфат, полимиксина В сульфат, нистатин, диметикон). Чувствительность патогенной флоры к компонентам Полижинакса достигает 100%. Этим объясняется тот факт, что резистентность к данному препарату развивается редко и медленно. Курс лечения составляет 12 суток по 1 капсуле во влагалище.
На втором этапе лечения применяются препараты, направленные на восстановление влагалищного микроценоза и муказального иммунитета. Бактериальный вагиноз можно считать излеченным лишь тогда, когда титр лактобактерий в вагинальном секрете составляет не менее 107 КОЕ/мл. Это осуществляется путем местного применения эубиотиков, содержащих живые палочки Lactobacillus casei rhamnosus Doderleini (Лактожиналь®), стимулирующих рост собственной лактофлоры влагалища и способствующих снижению числа рецидивов заболевания за счет повышения защитных свойств влагалища, проявляя иммуномодулирующую активность. In vitro показано, что Lactobacillus casei rhamnosus Doderleini в течение нескольких часов после введения приводят к необходимому снижению рН влагалищного отделяемого. Эубиотики назначают по 1 свече на ночь в течение 14 дней либо по 1 свече 2 раза в день в течение 7 дней после обязательного контрольного микробиологического подтверждения отсутствия грибов. Эубиотики являются эффективным и безопасным средством восстановления и поддержания нормального биоценоза влагалища.
Мы имеем опыт успешного лечению бактериального вагиноза у пациенток, планирующих ЭКО, с использованием вагинальных форм препаратов и двухэтапной схемы лечения. В качестве антибактериальных средств использовались Нео-Пенотран Форте® по 1 свече во влагалище на ночь в течение 7 дней или Клиндацин® по 1 свече в день в течение 1–3 дней. Восстановление нормального биоценоза проводилось препаратом Лактожиналь. Было пролечено 54 пациентки. Рецидив заболевания отмечен у одной пациентки, что потребовало повторного курса лечения с полным выздоровлением. После проведенной санации в результате ЭКО и ПЭ беременность была получена у 19 пациенток (34,9%). Таким образом, результативность программ не отличалась от средней по отделению.
БВ является достаточно распространенным полиэтиологичным инфекционным невоспалительным заболеванием экосистемы влагалища женщин репродуктивного возраста, который имеет сложный патогенез с вовлечением репродуктивной, эндокринной, иммунной и других систем организма, характеризуется длительным течением (иногда годами) и оказывает негативное воздействие на репродуктивный потенциал как фертильных, так и бесплодных женщин, планирующих беременность с помощью вспомогательных репродуктивных технологий. Бесспорной является необходимость своевременной диагностики и двухэтапной современной терапии данной нозологии у всех женщин с выявленным БВ. У пациенток с неудачными попытками ЭКО в анамнезе необходимо проводить обследование и лечение как можно раньше, до начала стимуляции суперовуляции для того, чтобы была возможность провести адекватную коррекцию. Именно на таких принципах построена подготовка к ЭКО в нашем отделении, что позволяет не только повысить эффективность программ вспомогательных репродуктивных технологий, но и снизить риск инфекционных осложнений во время беременности, родов и послеродовом периоде.
Литература
- Белобородов С. М., Анкирская А. С., Леонов Б. В., Фурсова С. А. Микроэкология влагалища и частота беременности после экстрокорпорального оплодотворения и переноса эмбрионов // Акушерство и гинекология. 2001, № 3. С. 29–32.
- Кира Е. Ф., Муслимова С. З. Неспецифический вагинит и его влияние на репродуктивное здоровье женщины (обзор литературы). 2001. С. 5–12.
- Кремлева Е. А. Роль эпителиально-бактериальных взаимодействий в ассоциативном симбиозе репродуктивного тракта женщин. Автореф. дисс. … док. мед. наук. Оренбург, 2013. 8 с.
- Ледина А. В., Прилепская В. Н. Состояние микробиоценоза влагалища, бактериальный вагиноз и возможности его лечения // Consilium medicum. 2013. Т. 15, № 6. С. 48–50.
- Радзинский В. Е., Ордиянц И. М. Двухэтапная терапия вагинальных инфекций. М.: Редакция журнала StatusPraesens. 2012. 6 с.
- Рудакова Е. Б., Мозговой С. И., Лазарева О. В. Бактериальный вагиноз // Лечащий Врач. 2008, № 6, с. 61–65.
- Ших Е. В., Шилер Л. В., Гребенщикова Л. Ю. Современные аспекты фармакотерапии бактериального вагиноза. М., 2010, с. 6–14.
- Liversedge N. H., Turner A., Horner P. J. et al. // Hum. Reprod. 1999. Vol. 14, № 9. P. 2411–2415.
- Ralph S. G., Rutherford A. J., Wilson J. D. // Br. Med. J. 1999. Vol. 319, № 24. P. 220–223.
- Mirmonsef P., Gilbert D., Zariffard M. R. et al. The effects of commensal bacteria on innatе immuneresponses in the female genital tract // Am. J. Reprod. Immunol. 2011. Vol. 65. P. 190–195.
Е. Б. Рудакова 1 , доктор медицинских наук, профессор
Т. В. Стрижова, кандидат медицинских наук
Л. Ю. Замаховская
ГБУЗ МО МОПЦ, Балашиха
Одной из важных причин, вызывающих бесплодие, являются половые инфекции, или, иначе говоря, заболевания, передающиеся половым путем (обозначаются как ЗППП). Особенно это касается вторичного бесплодия, когда один ребенок уже есть, а при попытке планирования второй или последующих беременностей возникают неудачи. Пара обращается за медицинской помощью, а в процессе обследования в половине случаев выясняется, что проблемы с зачатием — следствие инфекционных заболеваний, обычно хронического течения. Не только инфекционные болезни приводят к бесплодию.
Какие инфекции чаще вызывают бесплодие
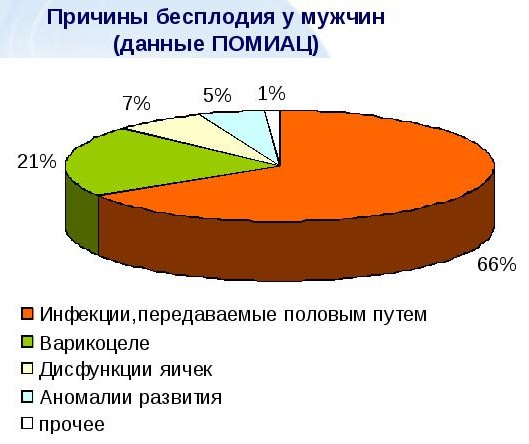
Что же это за инфекции, приводящие к бесплодию? Сюда можно отнести инфекционные агенты, являющиеся возбудителями как венерических болезней, так и воспалительных, вызывающих стойкие изменения в репродуктивной сфере мужчин и женщин. Список будет довольно внушительным. К основным из них относятся:
- гонорея;
- сифилис;
- трихомониаз;
- хламидиоз;
- микоплазмоз;
- уреаплазмоз;
- герпетическая инфекция;
- папилломавирус человека;
- паротит;
- гепатит;
- туберкулез и другие.
В отдельную группу ЗППП (ИППП), влияющих на возникновение бесплодия, можно выделить венерические болезни, возбудители которых передаются преимущественно через сексуальный контакт. В нашей стране из их числа особо распространены сифилис, гонорея, хламидиоз, уреаплазмоз, генитальный герпес, причем первые два заболевания считаются исконно венерическими, а остальные — условно венерическими. Они все могут повлиять на бесплодие.
После незащищенного полового контакта с больным человеком происходит заражение, причем для развития болезни должен пройти определенный период времени, который называют инкубационным периодом. Первые признаками, которые замечает заболевший человек, общие для всех половых инфекций. ИППП проявляются:
- повышением температуры тела;
- недомоганием;
- неприятными ощущениями в области гениталий, зудом, жжением;
- выделениями из половых путей;
- высыпаниями (чаще в интимной зоне).
Хламидиоз — наиболее распространенная на сегодня как в мире, так и в нашей стране, условно венерическая 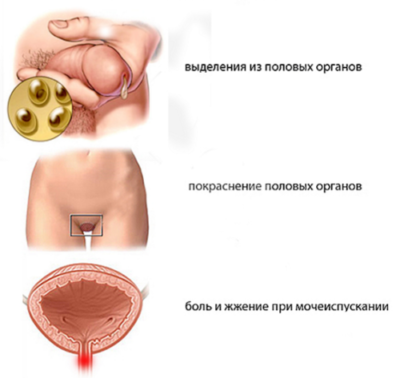
инфекция, вызывающая бесплодие как у женщин, так и у мужчин. Болезнь передается половым путем. Возбудитель — внутриклеточная бактерия. Наиболее восприимчивы к заражению женщины. Люди, страдающие хламидиозом, не всегда проявляют какие-либо жалобы. Встречается бессимптомное течение, особенно на ранних стадиях.
Заболевание в основном поражает урогенитальный тракт, отдаленным последствием чего зачастую является бесплодие. Хламидийная инфекция выявляется более чем у половины пациентов, обратившихся за медицинской помощью по причине бесплодия.
Проявляется болезнь во многих случаях у обоих полов с появления неприятных ощущений в области гениталий, тягучих выделений с заметным запахом. У женщин также отмечается появление хронических тазовых болей тянущего, ноющего характера. Возникают воспалительные изменения матки и придатков у женщин, яичек и предстательной железы у мужчин.
В дальнейшем возникают рубцовые поражения фаллопиевых труб у женщин, семявыводящих путей у мужчин, что приводит бесплодию. Если же беременность наступает на фоне имеющегося хламидиоза, то нередки выкидыши, а у доношенного ребенка значительно повышен риск врожденной хламидийной инфекции.
Уреаплазма и микоплазма — бактериальные инфекции, имеющие, как правило, хроническое течение без особых симптомов, что способствует заражению партнера. Заболевания могут обнаружиться лишь после врачебного осмотра, получения результатов лабораторных обследований, когда у пары беременность не наступает долгий период.
Хламидиоз, уреаплазмоз, микоплазмоз могут одновременно присутствовать в организме человека. Такая комбинация возбудителей достаточно часто встречается, называется микст-инфекцией и требует особого подхода в лечении.
Основные проблемы ЗППП, имеющих бессимптомное течение — это их способность вызывать стойкие изменения в половой сфере, приводящие к бесплодию, спустя месяцы или годы с момента заражения.
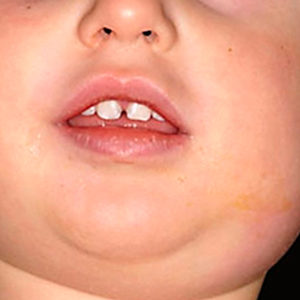
Эпидемический паротит, называемый в простонародье свинкой — болезнь вирусного происхождения, которой чаще страдают дети мужского пола. Вирус паротита занимает не последнее место среди причин, вызывающих бесплодие, хотя и не относится к половым инфекциям, так как передается воздушно-капельным путем.
Инфекция вызывает поражение слюнных желез, но особую опасность для репродуктивного здоровья мужчины представляют осложнения, которые могут стать причиной бесплодия, если заражение произошло в период полового созревания. Паротит способен спровоцировать у мальчиков тяжелое воспаление тестикул, приводящие к полной атрофии органа и бесплодию в будущем.
Генитальный герпес — распространенная инфекция, вызывающая жгучие, очень болезненные пузырьковые высыпания в области паха, ануса, на слизистой гениталий. У женщин и мужчин встречается одинаково часто. Особенностью данной ИППП является рецидивирующее течение.
Болезнь нельзя вылечить полностью, время от времени случаются обострения, особенно на фоне слабого иммунитета. Вирус герпеса, однажды попав в организм, остается в нем навсегда.
Сама инфекция и ее проявления не приводит непосредственно к бесплодию, но способна вызывать серьезные патологии плода у беременной женщины. У мужчин возможно развитие простатита и нарушения сперматогенеза.
Репродуктивные способности пары во многом зависят от общего состояния здоровья. В здоровом теле поддерживается оптимальный баланс разных микробов. От качества этого равновесия во многом зависит состояние иммунитета, функциональность многих органов человека. В норме постоянно существующая в организме микрофлора, называемая условно-патогенной, не причиняет вреда здоровью.
К таким микроорганизмам можно отнести:
- стафилококки, стрептококки;
- энтеробактерии;
- дрожжевые грибки рода кандида;
- гарднереллы и другие.
При ослаблении иммунитета, наличии инфекционных, воспалительных заболеваний, при лечении антибиотиками и в некоторых других случаях, такие группы бактерий активизируются и представляют реальный риск гинекологическому здоровью женщины, угрожая бесплодием, вызывая гарднереллез, кандидоз и подобные заболевания.
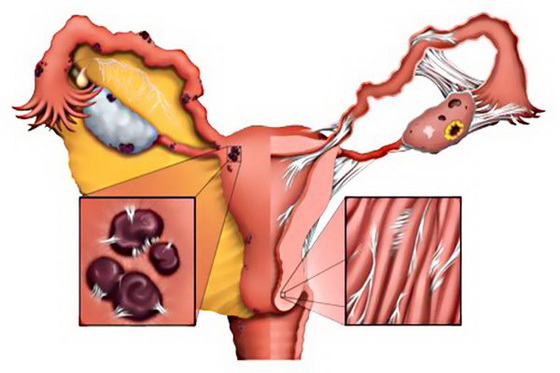
Генитальный туберкулез встречается относительно редко, в отличие от туберкулезного поражения легких, кишечника, костей, других жизненно важных органов. Инфекция не относится к ЗППП, но вызывая стойкое воспаление матки и, даже чаще, маточных труб, приводит к бесплодию у женщин. Микобактерии туберкулеза попадают в мочеполовую сферу с током крови или лимфы. Именно таким путем инфекция разносится по организму из первичного очага. Сложно поддается лечению.
При обследовании пары, обратившейся к медикам с репродуктивными проблемами, обязательно присутствуют анализы на вирусный гепатит. Существует несколько типов гепатита. Серьезно влияние на способность к зачатию оказывают типы В и С. Инфекция относится к ЗППП, также может передаваться с трансфузией крови и от матери к ребенку. Сохраняется в организме на всю жизнь.
Гепатит поражает печеночную ткань. Токсины, вырабатываемые вирусным агентом, обнаруживаются во всех жидкостных средах человеческого организма, вызывают изменения в составе крови. Заболевание ухудшает транспорт и качество спермы, может снижать вероятность зачатия.
Диагностика
Успешно найти причины проблем с оплодотворением у партнеров и сделать все возможное для их 
устранения, способна качественно проведенная диагностика бесплодия. Женское репродуктивное здоровье оценивает гинеколог, мужское — андролог. Врачи проводят всестороннее обследование с применением современных лабораторных, инструментальных, функциональных средств и методов.
Квалифицированные медики-диагносты определяют, есть ли нарушения менструального цикла, и какого характера, проверяют состояние органов малого таза на предмет наличия инфекций и воспаления, степень проходимости фаллопиевых труб у женщин; качество спермы, подвижность сперматозоидов — у мужчин.
О состоянии гормональной системы партнеров, наличии инфекционной составляющей в первичном и вторичном бесплодии пары информирует анализ крови — стандарт обследования.
Лечение
В случае если подозрения на половые инфекции подтвердятся лабораторным путем, необходимо пройти полный курс лечения, неукоснительно соблюдая предписания врачей. Этого, как правило, достаточно, если воспалительный процесс не принял хронический характер и не нанес необратимых повреждений половым органам. Пока инфекция присутствует в организме, то применение современных вспомогательных репродуктивных технологий (ЭКО, ИКСИ и так далее) не целесообразно.
Если же вследствие инфекционных процессов образовались спайки в малом тазу, то понадобится оперативное вмешательство.
Комплекс консервативных и радикальных мер, современные методы репродуктологов с высокими шансами помогут победить мужское бесплодие. Лапароскопия (все малоинвазивные хирургические вмешательства) способна устранить большую часть женских гинекологических проблем, приводящих к потере фертильности.
Лечение бесплодия — процесс дорогостоящий, небыстрый, требует слаженной кропотливой работы команды врачей и самой пары, но наградой за пережитые испытания станет бесценная радость от рождения долгожданного ребенка.
Читайте также:


