Микробиологическая диагностика болезнь лайма
Спирохеты рода Borrelia вызывают антропонозные (возвратный тиф), зоонозные (болезни Лайма) инфекционные болезни с трансмиссивным механизмом передачи возбудителей (клещи, вши).
Морфологические свойства: тонкие спирохеты с крупными завитками. Двигательный аппарат представлен фибриллами. Они хорошо воспринимают анилиновые красители, по Романовскому—Гимзе окрашиваются в сине-фиолетовый цвет. Боррелии обладают генетическим аппаратом, который состоит из небольших размеров линейной хромосомы и набора циркулярных и линейных плазмид.
Культуральные свойства: культивируются на сложных питательных средах, содержащих сыворотку, тканевые экстракты, а также в куриных эмбрионах.
Чувствительны к высыханию и нагреванию. Устойчивы к низким t-рам.
Болезнь Лайма - возбудитель В. burgdorferi. Хроническая инфекция с поражением кожи, сердечной и нервной систем, суставов.
Морфология и культуральные свойства:типичные боррелии.
Антигенная структура: Сложная. Белковые антигены фибриллярного аппарата и цитоплазматического цилиндра, антитела к которым появляются на ранних этапах инфекции. Протективную активность имеют антигены, представленные липидмодифицированными интегральными белками наружной мембраны А, В, С, D, E, F.
Факторы патогенности.Липидмодифицированные белки наружной мембраны обеспечивают способность боррелий прикрепляться и проникать в клетки хозяина. В результате взаимодействия боррелий с макрофагами происходит выделение ИЛ-1, который индуцирует воспалительный процесс.
Патогенез: На месте укуса клеща образуется красная папула. Возбудитель распространяется из места укуса через окружающую кожу с последующей диссеминацией с током крови к различным органам, особенно сердцу, ЦНС, суставам. Клиника подразделяется на 3 стадии:
1.Мигрирующая эритема, которая сопровождается развитием гриппоподобного симптомокомплекса.
2.Развитие доброкачественных поражений сердца и ЦНС
3.Развитие артритов крупных суставов
Иммунитет.Гуморальный, видоспецифический к антигенам клеточной стенки.
Микробиологическая диагностика.Используются бактериоскопический, серологический методы и ПЦР в зависимости от стадии заболевания. Материалом для исследования служат биоптаты кожи, синовиальная жидкость
суставов, ликвор, сыворотка крови. На 1-й стадии заболевания проводится бактериологическое исследование биоптатов кожи из эритемы.
Начиная со 2-й стадии заболевания осуществляется серологическое исследование определением IgM или нарастания титра IgG ИФА или РИФ.
ПЦР используется для определения наличия боррелий в ликворе, суставной жидкости.
Лечение: антибиотики тетрациклинового ряда.
Возвратные тифы— группа острых инфекционных заболеваний, вызываемых боррелиями, характеризующихся острым началом, приступообразной лихорадкой, общей интоксикацией. Различают эпидемический и эндемический возвратные тифы.
Возбудителем эпидемического возвратного тифа является В. recurrentis.
Эпидемический возвратный тиф - антропоноз. Специфические переносчики - платяная, головная вши. Человек заражается возвратным тифом при втирании гемолимфы раздавленных вшей в кожу при расчесывания места укуса.
Эндемический возвратный тиф— зооноз. Возбудители - В. duttoni и В. persica. Резервуар - грызуны, клещи. Человек заражается через укусы клещей.
Патогенез:Попав во внутреннюю среду организма, боррелии внедряются в клетки лимфоидно-макрофагальной системы, где размножаются и поступают в кровь, вызывая лихорадку, головную боль, озноб. Взаимодействуя с АТ, боррелии образуют агрегаты, которые нагружаются тромбоцитами, вызывая закупорку капилляров, следствием чего является нарушение кровообращения в органах.
Иммунитет:к эпидемическому возвратному тифу гуморальный, непродолжительный.
Микробиологическая диагностика.Бактериоскопический метод — обнаружение возбудителя в крови, окрашенной по Романовскому—Гимзе. Биопробу ставят для дифференциации В. recurrentis от возбудителей эндемического возвратного тифа.В качестве вспомогательного используют серологический метод с постановкой РСК.
Лечение: антибиотики тетрациклинового ряда, левомицетин, ампициллин.
Не нашли то, что искали? Воспользуйтесь поиском:
Спирохеты семейству Spirochaetaceae, рода Borrelia вызывают В. burgdorferi антропонозные (возвратный тиф), зоонозные (болезни Лайма) инфекционные болезни с трансмиссивным механизмом передачи возбудителей (клещи, вши). Морфологические свойства: тонкие спирохеты с крупными завитками. Двигательный аппарат представлен фибриллами. Они хорошо воспринимают анилиновые красители, по Романовскому—Гимзе окрашиваются в сине-фиолетовый цвет. Боррелии обладают генетическим аппаратом, который состоит из небольших размеров линейной хромосомы и набора циркулярных и линейных плазмид.
Культуральные свойства: культивируются на сложных питательных средах, содержащих сыворотку, тканевые экстракты, а также в куриных эмбрионах.
Чувствительны к высыханию и нагреванию. Устойчивы к низким t-рам. Болезнь Лайма - возбудитель В. burgdorferi. Хроническая инфекция с поражением кожи, сердечной и нервной систем, суставов. Морфология и культуральные свойства: типичные боррелии. Факторы патогенности. Липидмодифицированные белки наружной мембраны обеспечивают способность боррелий прикрепляться и проникать в клетки хозяина. В результате взаимодействия боррелий с макрофагами происходит выделение ИЛ-1, который индуцирует воспалительный процесс.
Патогенез: На месте укуса клеща образуется красная папула. Возбудитель распространяется из места укуса через окружающую кожу с последующей диссеминацией с током крови к различным органам, особенно сердцу, ЦНС, суставам. Клиника подразделяется на 3 стадии:
1.Мигрирующая эритема, которая сопровождается развитием гриппоподобного симптомокомплекса.
2.Развитие доброкачественных поражений сердца и ЦНС
3.Развитие артритов крупных суставов
Иммунитет. Гуморальный, видоспецифический к антигенам клеточной стенки. Микробиологическая диагностика. Используются бактериоскопический, серологический методы и ПЦР в зависимости от стадии заболевания. Материалом для исследования служат биоптаты кожи, синовиальная жидкость суставов, ликвор, сыворотка крови. На 1-й стадии заболевания проводится бактериологическое исследование биоптатов кожи из эритемы. Начиная со 2-й стадии заболевания осуществляется серологическое исследование определением IgM или нарастания титра IgG ИФА или РИФ. ПЦР используется для определения наличия боррелий в ликворе, суставной жидкости. Лечение: антибиотики тетрациклинового ряда. Профилактика. Неспецифическая. Возвратные тифы — группа острых инфекционных заболеваний, вызываемых боррелиями, характеризующихся острым началом, приступообразной лихорадкой, общей интоксикацией. Различают эпидемический и эндемический возвратные тифы.
Возбудителем эпидемического возвратного тифа является В. recurrentis. Эпидемический возвратный тиф - антропоноз. Специфические переносчики - платяная, головная вши. Человек заражается возвратным тифом при втирании гемолимфы раздавленных вшей в кожу при расчесывания места укуса. Эндемический возвратный тиф— зооноз. Возбудители - В. duttoni и В. persica. Резервуар - грызуны, клещи. Человек заражается через укусы клещей. Патогенез: Попав во внутреннюю среду организма, боррелии внедряются в клетки лимфоидно-макрофагальной системы, где размножаются и поступают в кровь, вызывая лихорадку, головную боль, озноб. Взаимодействуя с АТ, боррелии образуют агрегаты, которые нагружаются тромбоцитами, вызывая закупорку капилляров, следствием чего является нарушение кровообращения в органах. Иммунитет: гуморальный, непродолжительный. Микробиологическая диагностика. Бактериоскопический метод — обнаружение возбудителя в крови, окрашенной по Романовскому—Гимзе. Биопробу ставят для дифференциации В. recurrentis от возбудителей эндемического возвратного тифа. В качестве вспомогательного используют серологический метод с постановкой РСК. Лечение: антибиотики тетрациклинового ряда, левомицетин, ампициллин. Профилактика. Неспецифическая.
№ 7
1.Принципы классификации вирусов.В основу классификации вирусов положены следующие категории:
• тип нуклеиновой кислоты (ДНК или РНК), ее структура, количество нитей (одна или две), особенности воспроизводства вирусного генома;
• размер и морфология вирионов, количество капсомеров и тип симметрии;
• чувствительность к эфиру и дезоксихолату;
• место размножения в клетке;
• антигенные свойства и пр.
Вирусы имеют уникальный геном, так как содержат либо ДНК, либо РНК. Поэтому различают ДНК-содержащие и РНК-содержащие вирусы. Они обычно гаплоидны, т.е. имеют один набор генов. Геном вирусов представлен различными видами нуклеиновых кислот: двунитчатыми, однонитчатыми, линейными, кольцевыми, фрагментированными. Среди РНК- содержащих вирусов различают вирусы с положительным (плюс-нить РНК) геномом. Плюс-нить РНК этих вирусов выполняет наследственную функцию и функцию информационной РНК (иРНК). Имеются также РНК-содержащие вирусы с отрицательным (минус-нить РНК) геномом. Минус-нить РНК этих вирусов выполняет только наследственную функцию. Вирусы — мельчайшие микробы, не имеющие клеточного строения, белоксинтезирующей системы, содержащие только ДНК или РНК. Относятся к царству Vira. Являясь облигатными внутриклеточными паразитами, вирусы размножаются в цитоплазме или ядре клетки. Они — автономные генетические структуры. Отличаются особым — разобщенным (дисъюнктивным) способом размножения (репродукции): в клетке отдельно синтезируются нуклеиновые кислоты вирусов и их белки, затем происходит их сборка в вирусные частицы. Сформированная вирусная частица называется вирионом. Морфологию вирусов изучают с помощью электронной микроскопии, так как их размеры малы (18-400 нм) и сравнимы с толщиной оболочки бактерий.
Форма вирионов может быть различной: палочковидной (вирус табачной мозаики), пулевидной (вирус бешенства), сферической (вирусы полиомиелита, ВИЧ), нитевидной (филовирусы), в виде сперматозоида (многие бактериофаги). Различают просто устроенные и сложно устроенные вирусы. Простые, или безоболочечные, вирусы состоят из нуклеиновой кислоты и белковой оболочки, называемой капсидом. Капсид состоит из повторяющихся морфологических субъединиц — капсомеров. Нуклеиновая кислота и капсид взаимодействуют друг с другом, образуя нуклеокапсид.
Сложные, или оболочечные, вирусы снаружи капсида окружены ли-попротеиновой оболочкой (суперкапсидом, или пеплосом). Эта оболочка является производной структурой от мембран вирус-инфицированной клетки. На оболочке вируса расположены гликопротеиновые шипы, или шипики (пепломеры). Под оболочкой некоторых вирусов находится матриксный М-белок. Тип симметрии. Капсид или нуклеокапсид могут иметь спиральный, икосаэдрический (кубический) или сложный тип симметрии. Икосаэдрический тип симметрии обусловлен образованием изометрически полого тела из капсида, содержащего вирусную нуклеиновую кислоту (например, у вирусов гепатита А, герпеса, полиомиелита). Спиральный тип симметрии обусловлен винтообразной структурой нуклеокапсида (например, у вируса гриппа).
2.Комплемент, его структура, функции, пути активации, роль в иммунитете. Природа и характеристика комплемента. Комплемент является одним из важных факторов гуморального иммунитета, играющим роль в защите организма от антигенов. Комплемент представляет собой сложный комплекс белков сыворотки крови, находящийся обычно в неактивном состоянии и активирующийся при соединении антигена с антителом или при агрегации антигена. В состав комплемента входят 20 взаимодействующих между собой белков, девять из которых являются основными компонентами комплемента; их обозначают цифрами: С1, С2, СЗ, С4. С9. Важную роль играют также факторы В, D и Р (пропердин). Белки комплемента относятся к глобулинам и отличаются между собой по ряду физико-химических свойств. Функции комплемента многообразны: а) участвует в лизисе микробных и других клеток (цитотоксическое действие); б) обладает хемотаксической активностью; в) принимает участие в анафилаксии; г) участвует в фагоцитозе. Следовательно, комплемент является компонентом многих иммунологических реакций, направленных на освобождение организма от микробов и других чужеродных клеток и антигенов(например, опухолевых клеток, трансплантата).Механизм активации комплемента очень сложен и представляет собой каскад ферментативных протеолитических реакций, в результате которого образуется активный цитолитический комплекс, разрушающий стенку бактерии и других клеток. Известны три пути активации комплемента: классический, альтернативный и лектиновый. По классическому пути комплемент активируется комплексом антиген-антитело. Для этого достаточно участия в связывании антигена одной молекулы IgM или двух молекул IgG. Процесс начинается с присоединения к комплексу АГ+АТ компонента С1. Эта реакция имеет характер усиливающегося каскада, т. е. когда одна молекула предыдущего компонента активирует несколько молекул последующего. Затем образуется литический или мембраноатакующий комплекс который нарушает целостность мембраны (образует в ней отверстие), и клетка погибает в результате осмотического лизиса.Альтернативный путь активации комплемента проходит без участия антител. Этот путь характерен для защиты от грамотрицательных микробов. Каскадная цепная реакция при альтернативном пути начинается с взаимодействия антигена (например, полисахарида) с протеинами В, D и пропердином (Р) с последующей активацией компонента СЗ. Далее реакция идет так же, как и при классическом пути — образуется мембраноатакующий комплекс.
Лектиновыи путь активации комплемента также происходит без участия антител. Он инициируется особым маннозосвязывающим белком сыворотки крови, который после взаимодействия с остатками маннозы на поверхности микробных клеток катализирует С4. Дальнейший каскад реакций сходен с классическим путем. В процессе активации комплемента образуются продукты протеолиза его компонентов — субъединицы СЗа и СЗb, С5а и С5b и другие, которые обладают высокой биологической активностью. Например, СЗа и С5а принимают участие в анафилактических реакциях, являются хемоаттрактантами, СЗb — играет роль в опсонизации объектов фагоцитоза, и т. д. Сложная каскадная реакция комплемента происходит с участием ионов Са 2+ и Mg 2+ .
3.Возбудители кишечного иерсиниоза. Таксономия. Характеристика. Микробиологическая диагностика.Кишечный иерсиниоз – инфекционная болезнь, вызываемая Yersinia enterocolitica, характеризующаяся поражением пищеварительного тракта, тенденцией к генерализации с вовлечением в патологический процесс различных органов и систем. Таксономия. Yersinia enterocolitica относится к отделу Gracilicutes, семейству Enterobacteriaceae, роду Yersinia.Морфология и тинкториальные свойства. Возбудитель иерсиниоза полиморфен: может иметь либо форму палочки с закругленными концами (длиной 0,8-1,2 мкм, шириной 0,5-0,8 мкм), либо овоидную форму с биполярным окрашиванием. Спор не образует, иногда имеет капсулу. Перитрих, но подвижен лишь при температуре 18-20ºС, при 37ºС подвижность утрачивает. Некоторые штаммы имеют пили. Грамотрицателен.Культивирование. Y. enterocolitica – факультативный анаэроб. Оптимальным рН среды для его роста является 7,2-7,4. Наиболее благоприятная температура 22-25ºС, что является особенностью этого микроорганизма. Он неприхотлив и растет на простых питательных средах.Ферментативная активность. Биохимическая активность возбудителя иеосиниоза достаточно высока. В зависимости от отношения к некоторым углеводам различают 5 биохимических вариантов.Антигенная структура. Бактерии имеют О- и Н-антигены, у некоторых штаммов обнаружен К-антиген. По О-антигену различают более 30 сероваров; от больных чаще всего выделяют 03 и О9 серовары.Факторы патогенности. Y. enterocolitica имеет эндотоксин, оказывающий энтеротоксическое действие; некоторые штаммы – вещество, соответствующее экзотоксину, обладающее энтеротоксическим и цитотоксическим действием. У иерсиний обнаружен также инвазивный белок. Адгезивная активность иерсиний связана с пилями и белками наружной мембраны. Капсула препятствует фагоцитозу.Эпидемиология. Y.enterocolitica широко распространена в природе, выделяют ее от многих видов животных и птиц. Обнаруживают иерсиний также в открытых водоемах, где они находятся в симбиозе с инфузориями, рыбами, что позволяет отнести кишечный иерсиниоз к сапронозным инфекциям. Источником инфекции для человека являются в основном домашние животные (свиньи, коровы, кошки).
Механизм передачи инфекции – фекально-оральный, основной путь передачи – пищевой: заболевание может возникнуть при употреблении молока, мяса, фруктов, овощей, даже хранившихся в холодильнике. Возможны также контактно-бытовой (при контакте людей с больными животными) и водный пути передачи. Болеют иерсиниозом люди всех возрастов, но более восприимчивы к нему дети 1.3 лет. Заболевание встречается чаще в холодное время года. Патогенез. Возбудитель попадает в организм через рот, в нижних отделах тонкой кишки прикрепляется к эпителию слизистой оболочки, внедряется в клетки эпителия, вызывая воспаление. Иногда в процесс вовлекается аппендикс. У людей ослабленных могут развиться сепсис, септикопиемия с образованием вторичных гнойных очагов в мозге, печени, селезенке. Иммунитет при иерсиниозе изучен мало. Микробиологическая диагностика. Материалом для исследования служат испражнения, моча, кровь, спинномозговая жидкость. Основной метод диагностики бактериологический, позволяющий идентифицировать возбудителя, определить антибиотикограмму, провести внутривидовую идентификацию (установить серовар, биохимический вариант, фаговар). В качестве вспомогательного применяют серологический метод (РНГА). Лечение. Назначают антибиотики. Профилактика. Соблюдение санитарно-гигиенических правил, особенно при хранении и приготовлении пищи.
№ 8
Последнее изменение этой страницы: 2017-01-19; Нарушение авторского права страницы
Лептоспиры. Общая характеристика. Патогенез лептоспирозов, иммунитет, специфическая профилактика. Микробиологическая диагностика лептоспирозов.
1. Классификация: р. Leptospira, в. L. interrogans.
2. Морфология: Гр-, палочка, спиралевидная, концы загнуты в виде крючков, два периплазматических жгутика, споронеобразующая, подвижная
3. Тип питания: хемоорганотроф
4. Биологические свойства:
а) для роста в среде необходима сыворотка крови
б) источник углерода и энергии – ЖК, не используют углеводы и АК.
5. Факторы патогенности и патогенез:
гликопротеид КС – включается в цитоплазматическую мембрану кл-хозяина
Повреждение кожи и слизистых ® проникновение возбудителя без первичных эффектов ® по лимфатическим сосудам ® кровь и паренхиматозные органы (преимущественно в печень, селезенку, легкие, почки, ЦНС) ® размножение и накопление.
6. Клинические проявления: Инкубационный период 4-14 дней. Начало болезни обычно острое, связано с массивным поступлением лептоспир и их токсинов в кровь. Вторичная массивная бактериемия приводит к обсеменению различных органов, где продолжается размножение возбудителей. Отмечаются многочисленные кровоизлияния, выраженная интоксикация, гемолиз эритроцитов, в тяжелых случаях развивается тромбогеморрагический синдром. В печени: отек ткани, некротические изменения паренхимы. В почках: олигурия, уремическая кома. В ЦНС: менингиты. В мышцах: фокальные некротические изменения.
7. Иммунитет: ГИО, типоспецифический длительный гуморальный постинфекционный иммунитет.
8. Эпидемиология. Зоонозная инфекция. Источники инфекции - различные животные (лесная мышь, крысы, собаки, свиньи, крупный рогатый скот и др.), но не человек, больной лептоспирозом. ОПЗ – контактный (при контакте кожи и слизистых с водой, загрязненной выделениями животных) и алиментарный. В воде и почве сохраняются несколько недель.
9. Профилактика: вакцинопрофилактика не разработана.
10. Лечение: АБ (пенициллин), Ig против лептоспир наиболее распространенных сероваров.
Материалы: кровь, моча, сп/м жидкость, вода, пищевые продукты
б) бактериологический метод: выделение гемокультур путем посева на водно-сывороточную среду, затем темнопольная микроскопия + РА с типовыми сыворотками
в) биопроба с заражением кроликов-сосунков и морских свинок с последующей микроскопией и бактериологическим исследованием.
г) серодиагностика: АТ в сыворотке крови в РА, реакции лизиса лептоспир.
1. Классификация: надцарство Procaryota, царство Bacteria, раздел Scotobacteria, класс Bacterias, порядок Spirochetales, группа VII Извитые и гибкие клетки, семейство Spirochetaceae, р.Borrelia, в. В.recurentis (вшивый тиф), B.persica, B.caucasica, B.duttoni, B.burdorferi (клещевой тиф).
2. Морфология: Гр-, палочка, спиральная, три крупных завитка на заостренном конце, споронеобразующая, подвижна
3. Тип питания: хемоорганотроф
4. Биологические свойства:
а) строгие анаэробы
б) культивируются на средах с животными белками, хорошо размножаются в куриных эмбрионах
5. АГ структура: поверхностные АГ чрезвычайно вариабельны.
6. Факторы патогенности и патогенез:
а) инвазин – белок наружной мембраны
б) эндотоксины (компоненты КС, освобождаемые при лизисе МБ)
Патогенез эпидемического вшивого энцефалита.
Проникновения в организм путем попадания гемолимфы раздавленных инфицированных вшей на мелкие повреждения кожи ® размножение в эндотелии сосудов и в клетках ретикуло-эндотелиальной системы® бактериемия (первый лихорадочный приступа ® накопление в крови спирохетолизинов ® лизис боррелий и высвобождение эндотоксина ® часть боррелий с измененной АГ структурой сохраняется, размножается ® бактериемия ® накопление в крови новых спирохетолизинов ® лизис боррелий и высвобождение эндотоксина и т.п. (5-6 раз) ® прекращение поступления боррелий с измененной АГ структурой ® выздоровление.
Патогенез эндемического клещевого энцефалита.
Особенность: проникают в ранку на месте присасывания клеща с его слюной.
7. Клинические проявления:
Инкубационный период около 7 дней. Приступ заболевания начинается остро. Озноб , сменяющийся затем чувством жара. Боли в мышцах. Кожа лица гиперемирована. В результате тромбоцитопении, поражения печени и эндотелия сосудов нередко признаки тромбогеморрагического синдрома (упорные носовые кровотечения, кровоизлияния в кожу и слизистые оболочки, кровохарканье, эритроциты в моче).
8. Иммунитет: ГИО, постинфекционный нестойкий.
9. Эпидемиология. Источник – больной человек. Переносчик – платяная вошь. ОПЗ – втирание гемолимфы при расчесах
10. Профилактика: вакцинопрофилактика не применяется. Раннее выявление, изоляция и госпитализация больных, борьба со вшивостью.
11. Лечение: b-лактамные АБ
а) для вшивого тифа:
Материал – кровь во лихорадочного приступа.
1) Бактериоскопия мазка и толстой капли (окраска по Романовскому-Гимзе)
2) Биопроба: заражение морской свинки. Возбудитель клещевого возвратного тифа для них непатогенен.
б) для клещевого возвратного тифа:
Материал – биоптат с места укуса. Иммунофлуоресценция. Серодиагностика: РСК и другие.
Нам важно ваше мнение! Был ли полезен опубликованный материал? Да | Нет
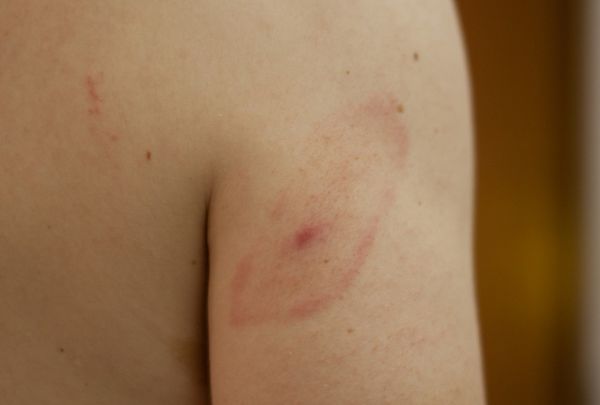
Болезнь Лайма (боррелиоз), является наиболее распространенным полиорганным системным инфекционным заболеванием людей и животных, передающееся через иксодовых клещей, обитающих, в основном, в зоне умеренного климата.
Симптомы боррелиоза
Фактором, вызывающим заболевание, является бактерия Borrelia burgorferi, принадлежащая к семейству спирохет. Болезнь Лайма проявляется дерматологическими изменениями, костно-мышечными нарушениями, поражение суставов, неврологическими и кардиологическими нарушениями.
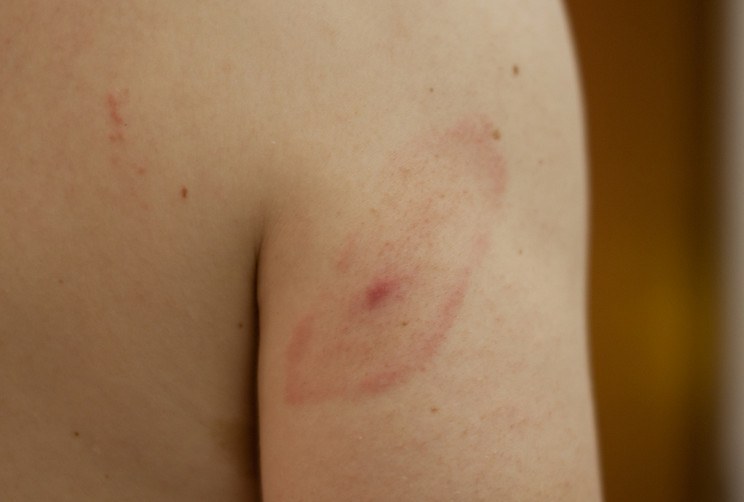
Можно выделить несколько характерных фаз развития заболевания. В первый период болезни, который начинается через 20-30 дней от момента проникновения бактерий в организм, у 60-80 процентов появляются кожные изменения в виде мигрирующей эритемы.
На этом этапе могут возникнуть также легкие симптомы гриппа (головные боли, повышенная температура, боли в горле, артрит). Далее происходит инфицирование внутренних органов и систем (периферической и центральной нервной системы, костно-суставной, сердечно-сосудистой системы).
Кроме того появляются такие симптомы, как:
- Псевдолимфатические узелки – напоминают небольшие пузырьки, заполненные жидкостью. Они содержат бактерий, ответственных за развитие болезни.
- Вторичные симптомы боррелиоза – появляются в случае отсутствия лечения антибиотиками. К их числу относятся: воспаление суставов, неврологические и кардиологические расстройства.
- Хроническая форма боррелиоза – хронической стадии болезнь Лайма достигает через год после укуса клеща. Хронический боррелиоз у людей проявляется следующими симптомами: лихорадка, озноб, головные боли, боли горла и суставов, тики в мышцах, скованность в суставах. Больной может иметь дефекты речи и проблемы с ориентацией в пространстве.
Диагностика боррелиоза
Разнообразные клинические проявления боррелиоза создают трудность для диагностики, так как не позволяют поставить однозначный диагноз. Тщательно собранное интервью от пациента позволяет оценить риск возможного заражения, клиническая картина и диагностические исследования помогут установить правильный диагноз.
Среди основных лабораторных методов можно выделить прямые исследования, то есть микроскопическая оценка патогенного микроорганизма, посев и изоляция, определение специфических для данного штамма бактериальных антигенов и поиск бактериальной ДНК методом цепной реакции полимеразы (англ. polymerase chain reaction, PCR).
В клинической практике важное значение имеет правильный подбор методов диагностики, проведение исследования и правильная интерпретация полученных результатов.
До сих пор не был разработан еще ни один тест, который на 100% мог бы подтвердить или исключить боррелиоз, а все имеющиеся в настоящее время на рынке имеют только указательный и вторичный характер.
Основная суть микробиологического исследования заключается в изоляции возбудителя и его оценка под микроскопом. В случае боррелиоза этот метод применяется сравнительно редко, так как не является эффективным.
Чтобы диагностировать болезнь Лайма необходимо продержать возбудителя три месяца на подходящей культуральной среде, а отрицательный результат не исключает инфекции.
Borrelia burgdoreri можно выделить из кожных изменений, спинномозговой жидкости, синовиальной жидкости и крови, причем в основном положительные результаты получают с кожных изменений. Чувствительность теста (способность распознать возбудителя) колеблется в пределах 10-30%.
Borrelia burgdorferi – это организм, имеющий особые наборы белков, так называемые липопротеины (Ospa, OspB, OspC и другие), которые могут быть использованы в качестве диагностических антигенов.
Эти антигены обладают высокой иммунногенностью, это значит, что после попадания в организм они отвечают за активацию иммунной системы и вызывают против себя определенный тип иммунного ответа, связанный с производством антител.
Различия в строении и составе отдельных белков позволяют выделить несколько серотипов, то есть видов микроорганизмов. В США болезнь Лайма вызывается только один штамм, а именно: Borrelia burgdorferi.
В Европе, кроме основного вида, описаны еще три других патогенных для человека: Borrelia garinii, Borrelia afzelii, Borrelia spielmani, что затрудняет микробиологическую диагностику.
Наиболее удобный вариант при регулярно проводимой диагностике являются серологические исследования. Сегодня на рынке есть много серологических тестов, но существует также и множество проблем, связанных с их использованием, начиная от времени, необходимого для получения соответствующего уровня антител и заканчивая их чувствительностью и специфичностью.
На первом этапе болезни, который продолжается около трех недель, не обнаруживается специфических антител, что может создавать определенные трудности для диагностики. Антитела создаются с целью устранения патогена.
Как и при большинстве инфекций первыми появляются антитела класса IgM. Они обнаруживаются в сыворотке крови приблизительно через 3-4 недели после заражения. Высокий уровень этих антител отмечается через 6-8 недель, а затем происходит постепенное снижение.
Иногда, даже несмотря на эффективную терапию, уровень антител IgM сохраняется в сыворотке крови в течение очень долгого времени (месяцы и даже годы). Через некоторое время после начала болезни появляются антитела класса IgG, которые являются ключевыми в борьбе с патогенами.
Как и в случае антител IgM уровень антител IgG может сохраняться годами, что не позволяет использовать их для контроля процесса лечения боррелиоза. Имейте в виду, что на выработку антител, а следовательно, и на результат исследования может повлиять ранняя терапия антибиотиками.
Когда-то к использованию рекомендовались тесты ELISA, которые в нынешнюю эпоху потерял свое значение, потому что иногда мы наблюдаем неспецифические перекрестные реакции и ложноположительные результаты.
Метод Вестерн-Блота основан на обнаружении антител против бактерий. Заключается в отделении белков (бактериальных антигенов), содержащихся в крови и их идентификации. Однако и в этом случае отрицательный результат теста не может исключить инфекции Borrelia burgdorferi (еще не успели возникнуть антитела, терапия антибиотиками).
Если клиническая картина указывает на боррелиоз, а серологические тесты дают отрицательный результат, необходимо повторить исследование через 3-4 недели для окончательного подтверждения.
В случае подозрения на нейроборрелиоза обнаружение антител в спинномозговой жидкости является достаточным доказательством, подтверждающим диагноз.
Несмотря на значительное развитие серологических методов, по-прежнему трудно дать однозначный ответ о наличии заболевания. В диагностически сложных случаях полезным может оказаться техника цепной реакции полимеразы, так называемый, метод PCR.
Он позволяет многократное тиражировать характерные для данного возбудителя фрагменты ДНК, что позволяет обнаружить даже отдельные, мелкие части в тканях и жидкостях организма. В настоящее время это исследование не является широко применяемым из-за довольно частого ложного срабатывания.
Тесты на боррелиоз не всегда дают 100% уверенности, что пациент подхватил болезнь Лайма. Поэтому полезно проводить также исследования спинномозговой жидкости и исследование потоков мозга (SPECT), в основном, для исключения других заболеваний. В случае диагностики этого заболевания, необходимо применить соответствующее лечение боррелиоза.
Читайте также:


