Лечение вэб инфекции ацикловиром
Одной из актуальных проблем современной медицины является высокая инфицированность населения одним из представителей оппортунистических возбудителей — вирусом Эпштейна–Барр (ВЭБ).
Одной из актуальных проблем современной медицины является высокая инфицированность населения одним из представителей оппортунистических возбудителей — вирусом Эпштейна–Барр (ВЭБ). Практикующие врачи в своей повседневной практике чаще сталкиваются с клинически манифестными формами первичной Эпштейна–Барр-вирусной инфекции (ЭБВИ) в виде острой, как правило, не верифицированной респираторной инфекцией (более 40% случаев) или инфекционным мононуклеозом (около 18% всех заболеваний) [1, 2]. В большинстве случаев эти заболевания протекают доброкачественно и заканчиваются выздоровлением, но с пожизненной персистенцией ВЭБ в организме переболевшего [1, 3–5].
Однако в 10–25% случаев первичное инфицирование ВЭБ, протекающее бессимптомно, и острая ЭБВИ могут иметь неблагоприятные последствия [6–9] с формированием лимфопролиферативных и онкологических заболеваний, синдрома хронической усталости, ВЭБ-ассоциированного гемофагоцитарного синдрома и др. [7, 9, 11–14].
До настоящего времени нет четких критериев, позволяющих прогнозировать исход первичного инфицирования ВЭБ. Перед врачом, к которому обращается пациент с острой ЭБВИ, всегда встает вопрос: что предпринять в каждом конкретном случае, чтобы максимально снизить риск развития хронической ЭБВИ и ВЭБ-ассоциированных патологических состояний Этот вопрос не праздный, и ответить на него действительно очень трудно, т. к. до сих пор нет четкой патогенетически обоснованной схемы лечения больных, а имеющиеся рекомендации часто противоречат друг другу.
По мнению многих исследователей, лечение ЭБВИ-мононуклеоза (ЭБВИМ) не требует назначения специфической терапии [15–17]. Лечение больных, как правило, проводится в амбулаторных условиях, изоляция пациента не требуется. Показаниями к госпитализации следует считать длительную лихорадку, выраженный синдром тонзиллита и/или синдром ангины, полилимфаденопатию, желтуху, анемию, обструкцию дыхательных путей, боли в животе и развитие осложнений (хирургических, неврологических, гематологических, со стороны сердечно-сосудистой и дыхательной системы, синдром Рейе).
При легком и среднетяжелом течении ЭБВ ИМ больным целесообразно рекомендовать палатный или общий режим с возвращением к обычной деятельности на адекватном для каждого конкретного больного физическом и энергетическом уровне. Проведенное многоцентровое исследование показало, что необоснованно рекомендуемый строгий постельный режим удлиняет период выздоровления и сопровождается длительным астеническим синдромом, требующим нередко медикаментозного лечения [18].
При легком течении ЭБВ ИМ лечение больных ограничивается поддерживающей терапией, включающей адекватную гидратацию, полоскание ротоглотки раствором антисептиков (с добавлением 2% раствора лидокаина (ксилокаина) при выраженном дискомфорте в глотке), нестероидные противовоспалительные препараты, такие как парацетамол (Ацетаминофен, Тайленол). По мнению ряда авторов назначение блокаторов Н2 рецепторов, витаминов, гепатопротекторов и местная обработка миндалин различными антисептиками являются малоэффективными и необоснованными способами лечения [19, 20]. Из экзотических методов лечения следует упомянуть рекомендуемое Ф. Г. Боковым и соавт. (2006) применение мегадоз бифидобактерий при лечении больных острым мононуклеозом [21].
Мнения о целесообразности назначения антибактериальных препаратов при лечении ЭБВИМ весьма противоречивы. По мнению Gershburg E. (2005) тонзиллит при ИМ часто асептический и назначение антибактериальной терапии не оправдано. Также нет смысла в применении антибактериальных средств при катаральной ангине [4]. Показанием для назначения антибактериальных препаратов является присоединение вторичной бактериальной инфекции (развитие у больного лакунарной или некротической ангины, таких осложнений, как пневмония, плеврит и др.), о чем свидетельствуют сохраняющиеся более трех суток выраженные воспалительные изменения показателей крови и фебрильная лихорадка. Выбор препарата зависит от чувствительности микрофлоры на миндалинах больного к антибиотикам и возможных побочных реакций со стороны органов и систем.
По данным H. Fota-Markowcka et al. (2002) у больных чаще выделяют гемофильную палочку, стафилококк и пиогенный стрептококк, реже — грибы рода Candida [22], поэтому следует признать обоснованным назначение этим больным препаратов из группы цефалоспоринов 2–3 поколения, линкосамидов, макролидов и противогрибковых средств (флуконазол) в терапевтических дозах на 5–7 дней (реже — 10 дней) [4]. Некоторые авторы при наличии некротической ангины и гнилостном запахе изо рта, вызванных, вероятно, ассоциированной анаэробной флорой, рекомендуют использовать метронидазол по 0,75 г/сут, разделенных на 3 приема, в течение 7–10 дней.
Противопоказаны препараты из группы аминопенициллинов (ампициллин, амоксициллин (Флемоксин Солютаб, Хиконцил), амоксициллин с клавуланатом (Амоксиклав, Моксиклав, Аугментин)) из-за возможности развития аллергической реакции в виде экзантемы. Появление сыпи на аминопенициллины не является IgE-зависимой реакцией, поэтому применение блокаторов Н1 гистаминовых рецепторов не имеет ни профилактического, ни лечебного эффекта [19].
По мнению ряда авторов до настоящего времени сохраняется эмпирический подход к назначению глюкокортикостероидов больным с ЭБВИ [23]. Глюкокортикостероиды (преднизолон, преднизон (Делтазон, Метикортен, Оразон, Ликвид Пред), Солу Кортеф (гидрокортизон), дексаметазон) рекомендуются больным с тяжелым течением ЭБВИМ, с обструкцией дыхательных путей, неврологическими и гематологическими осложнениями (тяжелая тромбоцитопения, гемолитическая анемия) [4, 24]. Суточная доза преднизолона составляет 60–80 мг в течение 3–5 дней (реже 7 дней) с последующей быстрой отменой препарата. Одинаковой точки зрения на назначение этим больным глюкокортикостероидов при развитии миокардита, перикардита и поражениях ЦНС нет.
При тяжелом течении ЭБВИМ показана внутривенная дезинтоксикационная терапия, при разрыве селезенки — хирургическое лечение.
Наиболее дискуссионным остается вопрос о назначении противовирусной терапии больным с ЭБВИ. В настоящее время известен большой перечень препаратов, являющихся ингибиторами ВЭБ репликации в культуре клеток [4, 25–27].
I. Подавляющие активность ДНК-полимеразы ВЭБ:
- ациклические аналоги нуклеозидов (ацикловир, ганцикловир, пенцикловир, валацикловир, валганцикловир, фамцикловир);
- ациклические аналоги нуклеотидов (цидофовир, адефовир);
- аналоги пирофосфатов (Фоскарнет (фоскавир), фосфоноацетиловая кислота);
- 4 оксо-дигидрохинолины (возможно).
II. Различные соединения, не ингибирующие вирусной ДНК-полимеразы (механизм изучается): марибавир, бета-L-5 урацил йододиоксолан, индолокарбазол.
Однако проведенный метаанализ пяти рандомизированных контролируемых испытаний с участием 339 больных ЭБВИМ, принимавших ацикловир (Зовиракс), показал неэффективность препарата [28, 29].
Одна из возможных причин кроется в цикле развития ВЭБ, в котором ДНК вируса имеет линейную либо циркулярную (эписома) структуру и размножается в ядре клетки хозяина. Активная репликация вируса происходит при продуктивной (литической) стадии инфекционного процесса (ДНК ВЭБ линейной формы). При острой ЭБВИ и активации хронической ЭБВИ происходит цитолитический цикл развития вируса, при котором он запускает экспрессию собственных ранних антигенов и активирует некоторые гены клеток макроорганизма, продукты которых участвуют в репликации ВЭБ. При латентной ЭБВИ ДНК вируса имеет вид эписомы (круговой суперспиральный геном), находящейся в ядре. Циркулярный геном ДНК ВЭБ характерен для CD21+ лимфоцитов, в которых даже при первичном инфицировании вирусом практически не наблюдается литической стадии инфекционного процесса, а ДНК воспроизводится в виде эписомы синхронно с клеточным делением инфицированных клеток. Гибель пораженных ВЭБ В лимфоцитов связана не с опосредованным вирусом цитолизом, а с действием цитотоксических лимфоцитов [4].
При назначении противовирусных препаратов при ЭБВИ врач должен помнить, что их клиническая эффективность зависит от правильной трактовки клинических проявлений болезни, стадии инфекционного процесса и цикла развития вируса на этой стадии. Однако не менее важным является и тот факт, что большинство симптомов ЭБВИ связаны не с прямым цитопатическим действием вируса в инфицированных тканях, а с опосредованным иммунопатологическим ответом ВЭБ-инфицированных В лимфоцитов, циркулирующих в крови и находящихся в клетках пораженных органов. Именно поэтому аналоги нуклеозидов (ацикловир, ганцикловир и др.) и ингибиторы полимеразы (Фоскарнет), подавляющие репликацию ВЭБ и уменьшающие содержание вируса в слюне (но не санирующие ее полностью [4], не оказывают клинического эффекта на тяжесть и продолжительность симптомов ЭБВИМ.
Показаниями для лечения ЭБВИМ противовирусными препаратами являются: тяжелое, осложненное течение болезни, необходимость профилактики ВЭБ-ассоциированной В-клеточной лимфопролиферации у иммунокомпрометированных пациентов, ВЭБ-ассоциированная лейкоплакия. Bannett N. J., Domachowske J. (2010) рекомендуют применять ацикловир (Зовиракс) внутрь в дозе 800 мг внутрь 5 раз в сутки в течение 10 дней (или 10 мг/кг каждые 8 часов в течение 7–10 дней). При поражениях нервной системы предпочтителен внутривенный способ введения препарата в дозе 30 мг/кг/сут 3 раза в сутки в течение 7–10 дней.
По мнению E. Gershburg, J. S. Pagano (2005), если под действием каких-либо факторов (например, иммуномодуляторов, при ВЭБ-ассоциированных злокачественных опухолях — применение лучевой терапии, гемцитабина, доксорубицина, аргинина бутирата и др.) удается перевести ДНК ВЭБ из эписомы в активную репликативную форму, т. е. активировать литический цикл вируса, то в этом случае можно ожидать клинический эффект от противовирусной терапии.
В комплексной терапии рекомендуется внутривенное введение иммуноглобулинов (Гаммар-П, Полигам, Сандоглобулин, Альфаглобин и др.) 400 мг/кг/сут, № 4–5.
В последние годы все чаще для лечения ЭБВИ стали применять рекомбинантные альфа-интерфероны (Интрон А, Роферон-А, Реаферон-ЕС) по 1 млн ME в/м в течение 5–7 дней или через день; при хронической активной ЭБВИ — 3 млн ME в/м 3 раза в неделю, курс 12–36 недель.
В качестве индуктора интерферона при тяжелом течении ЭБВИ рекомендуется использовать Циклоферон по 250 мг (12,5% 2,0 мл) в/м, 1 раз в сутки, № 10 (первые двое суток ежедневно, затем через день) или по схеме: 250 мг/сут, в/м на 1-й, 2-й, 4-й, 6-й, 8-й, 11-й, 14-й, 17-й, 20-й, 23-й, 26-й и 29-й день в сочетании с этиотропной терапией. Перорально Циклоферон назначается по 0,6 г/сут, курсовая доза (6–12 г, т. е. 20–40 таблеток).
Медикаментозная коррекция астенического синдрома при хронической ЭБВИ включает назначение адаптогенов, высоких доз витаминов группы В, ноотропных препаратов, антидепрессантов, психостимуляторов, препаратов с прохолинергическим механизмом действия и корректоров клеточного метаболизма [30–32].
Залогом успешного лечения больного с ЭБВИ являются комплексная терапия и строго индивидуальная тактика ведения как в стационаре, так и во время диспансерного наблюдения.
Литература
Высокая инфицированность населения вирусом Эпштейн-Барр является важной проблемой современной медицины. Часто болезнь проходит без видимых симптомов и отличается самостоятельным выздоровлением организма, что вызывает у многих легкомысленное отношение к ВЭБ. Заразиться инфекцией могут дети через игрушки, запачканные слюной вирусоносителя. Передается заболевание от одновременного пользования больными и здоровыми людьми бытовыми предметами, бельем или через поцелуй. Инфекция в скрытой форме при длительном пребывании в организме человека приводит к угасанию иммунитета и вызывает ряд болезней, таких как гепатит, рассеянный склероз, герпетическое поражение кожи и многие другие. Для пострадавших от ВЭБ характерен синдром хронической усталости. Когда организм не справляется с инфекцией самостоятельно, назначаются современные препараты, которые рассчитаны на уничтожение микробов в крови, снятие симптоматики инфекционного процесса.
Противовирусный препарат Ацикловир

При осложненном течении заболевания ВЭБ рекомендуется противовирусный препарат Ацикловир. По своему химическому составу он считается ациклическим аналогом дезоксигуанозина, натурального компонента ДНК, где кольцевое строение сахара заменяется ациклической боковой цепью. Противовирусное средство имеет весомые достоинства, к которым относятся высокая избирательность и низкая токсичность. Назначение Ацикловира при Эпштейн-Барра обосновано снижением уровня вирусной репликации, улучшением прогноза заболевания. В связи с особенным строением вируса медикамент при остром инфекционном мононуклеозе не оказывает действенного влияния. От его приема рекомендуется отказаться беременным, пожилым и кормящим. При терапии Ацикловир может применяться внутрь, инъекцией внутривенно или в виде мази на места поражения инфекцией. Использовать следует исключительно свежеприготовленные растворы.
Вироцидный препарат Изопринозин

Одним из эффективных медикаментов при лечении вируса Эпштейн считается Изопринозин. Он отлично подавляет синтез вирусных белков дезоксирибонуклеиновой кислоты. Основным преимуществом препарата является удачное сочетание противовирусной и иммуномодулирующей функции. Средство с честью прошло клинические проверки для подтверждения своей эффективности в плацебо контролируемых испытаниях. Изопринозин можно смело принимать с первого года жизни, к тому же он обеспечивает следующие результаты:
- Снижение вирусной нагрузки
- Сокращение периода ремиссии
- Отсутствие риска реинфекции и осложнений
- Быстрое развитие обратных воспалительных процессов
- Высокий профиль безопасности
- Ускоренное восстановление здорового функционирования организма после болезни.
Показатели свидетельствуют о том, что медикамент является достаточно эффективным испытанным препаратом, но также имеет свои побочные реакции в виде головных болей, головокружений, тошноты, сонливости.
Для уничтожения вируса Эпштейна широко используется этиотропный график в виде такой программы:
- Первый этап: стартовая терапия Изопринозином, которая длится десять дней. Препарат подавляет репликацию вирусных белков и приостанавливает синтез вируса. Рекомендуется принимать до 100 мг на кг веса внутрь. Суточный рацион составляет четыре приема.
- Второй этап: поддерживающая терапия с повторным употреблением медикамента.
- Третий этап: реабилитационная терапия с использованием пролонгированного графика, при которой стабилизируются клеточные мембраны. Ведется под наблюдением врача.
Эффективный и безопасный результат показывает комбинация медикамента с рекомбинантным Вифероном. Появляется более существенная положительная динамика, исчезают серологические маркеры инфекционного заболевания. Больные ВЭБ требуют длительную закрепляющую терапию с неукоснительным наблюдением клинико-лабораторных показателей интенсивности инфекционного процесса. Проводить рекомендуется 3 курса действий по 10 дней с промежутком 10 дней.
Высокоэффективный препарат Валтрекс

Противовирусный медикамент Валтрекс используют для подавления размножения вируса в клетке. Он противодействует синтезу и развитию вирусной ДНК. Эффективность использования Валтрекса отражается в улучшении показателей клеточного и гуморального иммунитета, воспрепятствует попаданию в организм аутоагрессивных антител. Препарат можно принимать ребенку с двух лет, но дозу и курс назначить должен лечащий врач. Валтрекс практически не имеет побочных явлений, а если они и появляются, то проходят легко и быстро. Попадая в организм, он целиком преобразовывается в Ацикловир, с которым имеет аналогичные фармакокинетические параметры. Валтрекс является достаточно новым медикаментом, который изучен не полностью, поэтому следует его принимать исключительно по рекомендации специалиста.
Виферон при ВЭБ

В качестве иммунокорригирующей терапии при средней и тяжелой форме рекомендуется принимать Виферон. Вследствие медицинских исследований были выявлены следующие клинические эффекты:
- Противовирусная функция
- Сокращение сроков исчезновения интоксикации
- Восстановление активности организма
- Иммунозаместительная и иммуномодулирующая деятельность.
Побочные эффекты не наблюдаются. Виферон можно принимать в комплексной терапии ВЭБ деткам с первых дней жизни и новорожденным, а также беременным и кормящим под наблюдением врача. Противопоказание назначается тем, у кого есть непереносимость к составу лекарства.
Интерферонстимулирующий Циклоферон

Хорошо зарекомендовал себя изученный в клинических сферах медикамент, который используется при любых формах инфекционного мононуклеоза, вызываемого ВЭБ. Эффективность препарата вызвана большим спектром биологических действий:
- Антипролиферативное
- Противовирусное
- Противохламидийное
- Препятствует образованию опухолевых процессов
- Иммуномодулирующее.
Применять препарат можно детям в возрасте от 4-х лет. Перед использованием следует ознакомиться с содержанием противопоказаний и побочных реакций.
Подробная инструкция доступна по ссылке: Способ применения и дозы Циклоферона в ампулах, таблетках и линименте
Ацикловир для детей
Препарат легко можно назвать родоначальником антивирусных лекарств, которые до сих пор активно применяется. Популярность Ацикловиру приносит тот факт, что продается он без рецепта. Это подчеркивает его доступность и безопасность. Ацикловир замедляет процесс образования ДНК вируса и помогает в борьбе с бактериальной инфекцией. Применение лекарственного препарата малышам довольно целесообразно, но делать это нужно лишь с разрешения лечащего врача, так как могут быть побочные эффекты. Растительный иммуномодулятор категорически запрещено использовать, если имеются аутоиммунные заболевания.
Существует не так уж много медикаментов, действующих на инфекцию. За большинством вирусов следит иммунная система. Выбор подходящего препарата зависит от чувствительности к ним организма, а детям не следует давать большинство рекомендуемых взрослым безрецептурных медикаментов.

Почти год назад я написал пост про инфекционный мононуклеоз, но в нем почти ничего не рассказал про роль ацикловира в лечении и возможность вакцинопрофилактики. В этой статье я эту тему немного развил.
Инфекционный мононуклеоз (ИМ) – синдром, который может развиться в ответ на инфицирование человека вирусом Эпштейна-Барра (ВЭБ или EBV). ВЭБ – ДНК-содержащий герпесвирус. В естественных условиях ВЭБ заражает только людей, и к нему формируется сильный пожизненный иммунитет.
Эпидемиологические исследования показывают, что более 95% всех взрослых инфицированы этим вирусом. В индустриально-развитых странах в половине случаев первичное инфицирование происходит в раннем детском возрасте, от 1 года до 5 лет. Другая половина приходится на вторую декаду жизни.
ВЭБ передается со слюной, поэтому преимущественный возраст инфицирования в популяции зависит от санитарно-гигиенических условий и уровня культурного развития. В США этот возраст постепенно смещается к 15-24 годам и старше, когда начинаются поцелуи. Среди американских первокурсников от 30% до 75% не имеют антител против EBV, то есть не инфицированы. От времени года заражение не зависит. Ну, может только весной чаще. Шучу.
Инкубационный период составляет от 30 до 50 дней.
О клинической картине и диагностике читайте статью Инфекционный мононуклеоз.
В большинстве случаев за один месяц клиническая картина и лабораторные параметры приходят в норму, увеличенные шейные лимфатические узлы и слабость сохраняются дольше – обычно 2-3 месяца, но бывает так, что и до полугода.
Несмотря на то, что в большинстве случаев инфекция протекает бессимптомно, у полноценного ИМ бывает довольно яркая картина, с высокой лихорадкой, длящейся несколько дней, выраженным тонзиллитом, очень выраженной слабостью и так далее. Поэтому, помимо рекомендованной поддерживающей терапии хотелось бы иметь возможность специфической профилактики и противовирусного лечения.
Так как ВЭБ относится к группе герпеса, то резонный интерес вызывает ацикловир. Обладает ли этот препарат доказанной эффективностью при полноценном синдроме инфекционного мононуклеоза?
Поможет ли ацикловир?
В разных источниках указывается пять клинических исследований с ацикловиром у пациентов с инфекционным мононуклеозом. Во всех пяти исследованиях ацикловир достоверно не изменял количество вируса в крови, а также не влиял на длительность и тяжесть клинических симптомов, и количество пропущенных дней учебы и работы.
В исследование набрали 94 пациентов в возрасте от 14 до 30 лет с подозрением на инфекционный мононуклеоз. Тех, кто подписывал согласие, проверяли на наличие критериев заболевания:
- Клиническая картина ИМ
- Длительность процесса не больше 7 дней
- Температура во рту > 37.5 0 С
- Атипичные мононуклеары в крови
- Положительный тест гетерофильных антител
Тех, кто соответствовал, рандомизировали на ацикловир плюс преднизолон или на плацебо плюс плацебо. Ацикловир давали в виде таблеток по 800 мг 5 раз в день, либо в виде внутривенных инфузий по 5 мг на килограмм веса каждые 8 часов. Плацебо назначали аналогичным образом.
В течение исследования пациентам не разрешали использовать нестероидные противовоспалительные препараты для купирования симптомов. Состояние участников оценивали на 3й, 4, 7, 9 и 10й день от начала терапии, и дальше раз в неделю до тех пор, пока у них все параметры не приходили в норму.
За три года, которые продолжалось это исследование, в него рандомизировали 86 пациентов. Остальные 8 не прошли по критериям включения. Рандомизированных пациентов поделили пополам – 43 на ацикловир и 43 на плацебо.
Результаты показали, что достоверной разницы в сроках выздоровления по клинической картине и по количеству пропущенных дней учебы и работы между группами не было.

Процент пациентов, у которых все еще больное горло; ацикловир (сплошная линия) против плацебо (пунктир). Достоверной разницы нет.

Процент пациентов на больничном – ацикловир (сплошная линия) против плацебо (пунктир). Достоверной разницы тоже нет.
Единственное, что ацикловир делал – он снижал количество вируса, выделяющегося со слюной. Но эта тенденция сохранялась только в течения приема препарата, а как только лечение закончили – выделение вируса со слюной тут же вернулось к прежним значениям и далее угасало так же, как в группе плацебо.

Клинического значения этот эффект не имеет, то есть он никак не сказывается на выздоравливании.
Пока что это последнее клиническое исследование, изучавшее эффективность ацикловира у пациентов с инфекционным мононуклеозом. На сегодняшний день ацикловир не рекомендован для лечения пациентов с ИМ.
А как с вакцинами?
Геном вируса Эпштейна-Барра кодирует несколько вирусных гликопротеинов, расположенных на поверхности его вириона: Gp350, gB, gH, gL, gp42 и BMRF2. Самый изученный из них – gp350, его больше всего на поверхности вириона, а также на мембранах инфицированных клеток.
Gp350 связывается с молекулой CD21 (aka CR2 или C3d) на мембране В-лимфоцитов, в результате чего вирион эндоцитозом проникает в клетку. ВЭБ внутри В-лимфоцитов становится резервуаром вируса в организме и предопределяет формирование Т-клеточного иммунного ответа.

Еще сам первооткрыватель ВЭБ, Anthony Epstein, в 1985 году обнаружил, что вакцинация обезьян фрагментами мембран инфицированных клеток и очищенным gp350, спрятанным внутри липосом, может защитить животных от ВЭБ-индуцированной лимфомы.

Из клинических исследований вакцин чаще всего цитируют рандомизированное, плацебо-контролируемое, двойное слепое исследование II фазы, изучившее эффективность gp350/AS04 производства GlaxoSmithKline, у здоровых добровольцев.
В исследование набрали студентов, у которых не было антител против ВЭБ, то есть они не были ранее инфицированы. Всего участвовал 181 человек – 90 в группе вакцины и 91 – на плацебо. Препарат и плацебо вводили внутримышечно в дельту, на 0, 1 и 5й месяц. Затем в течение 19 месяцев по совокупности клинических и серологических критериев, свидетельствующих о наличии или отсутствии инфекционного мононуклеоза, оценивали эффективность вакцинации.
Получилось вот такая картина –

По вертикальной оси количество незаболевших участников. Стрелочками обозначены точки введения вакцины или плацебо.
Из 181 участников – 10 человек за 19 месяцев наблюдения заболели подтвержденным инфекционным мононуклеозом:
- Двое из группы вакцинированных и
- Восемь из группы плацебо
Какая-то тенденция, кажется, есть, и на диаграмме она выглядит неплохо, но статистически достоверной разницы исследование не показало. Может быть, вакцина не сработала как следует, а может быть слишком мало было подтвержденных случаев заболевания, а также не хватило длительности наблюдения.
Видимо, эти результаты не вдохновили GSK на продолжение, потому что на clinicaltrials.gov исследования III фазы с этой вакциной нет и не было. Полез посмотреть на сайт GSK, в раздел, посвященный лекарствам в разработке (products pipeline) и обнаружил, что вакцина против EBV там отсутствует. Наверное, сошла с дистанции, или GSK продали ее кому-то.
Так что, в ближайшее время вакцины не будет. Есть, впрочем, надежда на создание особого варианта вируса, который будет представлять собой вирусо-подобную частицу (virus-like particle) со всеми необходимыми для стойкого иммунитета антигенами, но при этом лишенную способности к репликации.
Доклинические исследования с такими вирусоподобными частицами показали, что они формируют сильный В- и Т-клеточный иммунный ответ против ВЭБ в экспериментах in vitro. Если такие вакцины получат свое развитие – мы к ним еще вернемся.
Показалось интересным или полезным — подпишитесь на анонсы новых статей в наших пабликах ВКонтакте и Фейсбуке.

Вирус Эпштейна-Барр из семейства герпес-вирусов (герпес четвёртого типа) называют самой высоконтагиозной и распространённой вирусной инфекцией. Согласно статистике всемирной организации здравоохранения до 60% всех детей и почти 100% взрослых заражены этим вирусом. При этом исследования этого вируса начались относительно недавно и потому нельзя сказать о полном изучении вируса.
Что из себя представляет ВЭБ инфекция
Вирус Эпштейна-Барр передаётся следующими способами:

Воздушно-капельным путём.- С помощью контактов в быту (например, через полотенце). Это самый сложный путь для попадания ВЭБ, т. к. в окружающей среде вирус погибает.
- Через воду и пищу (алиментарный путь). Хотя этот путь и возможен, но таким образом, вирус распространяется крайне редко и потому этот способ часто опускают.
- Через кровь (трансмиссивный путь). В организм попадает путём пересадки костного мозга, других органов, переливания компонентов крови.
- От матери к зародышу и после родов через грудное молоко (вертикальный путь).
Источник инфекции ВЭБ — только люди, чаще всего болеющие бессимптомной и скрытой формой. Причём переболевший этим вирусом человек остаётся заразным для других на протяжении ещё многих лет. Вирус проникает в организм через дыхательные пути.
Далее, попадает в лимфоидную ткань и поражает миндалины, лимфоциты других иммунных клеток, слизистую оболочку печени, селезёнки, верхних дыхательных путей, нейронов ЦНС и лимфатических узлов.
Наиболее подвержены инфицированию вирусом Эпштейна-Барр такие категории людей:
- дети до 10 лет;
- люди, имеющие иммунодефицит;
- ВИЧ-больные, особенно СПИД категории;
- беременные женщины.
Острое инфицирование вирусом для человека не очень опасно. Большую опасность представляет склонность к образованию опухолевых процессов. Единую классификацию вирусной инфекции (ВИЭБ) ещё не придумали и поэтому практическая медицина предлагает следующую:
Тяжесть течения — тяжёлая, средняя и лёгкая.- Приобретённая и врождённая.
- По типу заболевания — типичная (мононуклеоз инфекционный), атипичная: асимптомная, стёртая, повреждение внутренних органов.
- Осложнения.
- Длительность течения — острая, хроническая и затяжная.
- По активности — активная фаза и неактивная.
- Смешанная инфекция — зачастую наблюдают в сочетании с цитомегаловирусной инфекцией.
Болезни, которые вызывает ВЭБ:
- синдром хронической усталости;
- лимфогранулематоз;
- иммунная недостаточность;
- инфекционный мононуклеоз;
- опухоли кишечника и желудка, слюнных желёз;
- злокачественные образования в носоглотке;
- системный гепатит;
- лимфомы;
- поражения спинного и головного мозга (или иначе рассеянный склероз);
- герпес.
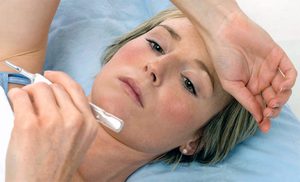
Вирус Эпштейна-Барр: симптоматика болезни
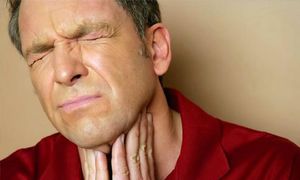
Полиаденопатия — главный признак при протекании ВЭБ в острой форме. Симптом характеризует увеличение передних и задних шейных лимфатических узлов, а также затылочных, подчелюстных, надключичных, подключичных, подмышечных, локтевых, бедренных и паховых лимфоузлов.
Их размеры в диаметре около 0,5–2 см, на ощупь они тестоватые, слабо болезненные или умеренно болезненные. Максимальная стадия выраженности полиаденопатии наблюдается на 5–7 день протекания заболевания, а спустя две недели, лимфоузлы постепенно уменьшаются.
- Инфекционный мононуклеоз — острая инфекция или сокращённо ОВИЭБ, инкубационный период которого исчисляется от двух дней до 2 месяцев. Болезнь начинается постепенно: больной испытывает повышенную утомляемость, недомогание, боли в горле. Температура немного повышается или остаётся нормальной. Спустя несколько суток, температура достигает 39–40 °C, начинается интоксикационный синдром.
- Симптом полиаденопатии влияет и на нёбные миндалины, вследствие чего проступают признаки ангины, нарушается носовое дыхание, голос становится гнусавым, образуется гной в задней части глотки.
- Спленомегалия или увеличение селезёнки, является одним из поздних симптомов. Спустя 2–3 недели, иногда спустя 2 месяца, размер селезёнки возвращается к исходному состоянию.
- Симптом гепатомегалии (или увеличение печени) встречается реже. Для этого симптома характерны потемнение мочи, лёгкая желтуха.
- Нервная система тоже страдает при остром вирусе Эпштейна-Барр. Может развиться серозный менингит, иногда менингоэнцефалит, энцефаломиелит, полирадикулоневрит, но, как правило, очаговые поражения регрессируют.
- Возможны другие симптомы в виде появления различной сыпи, пятен, папул, розеол, точек или кровоизлияний. Экзантема держится порядка 10 дней.
Диагностика вируса Эпштейна-Барр

Диагноз хронический или острый ВЭБ ставят на основе клинических проявлений, жалоб и лабораторных данных.
Общий анализ крови. Диагностируют увеличение лейкоцитов, СОЭ, повышение моноцитов и лимфоцитов, возникновение атипичных мононуклеаров. Вероятны повышение или снижение уровня тромбоцитов, гемоглобина (аутоиммунная или гемолитическая анемия).
На основе биохимического анализа крови выявляют увеличение АЛТ, АСТ, ЛДГ и других ферментов, обнаруживают белки острой фазы (фибриноген, СРБ), увеличение билирубина, щелочной фосфатазы.
Иммунологическое исследование — оценивают уровень интерферона, иммуноглобулинов и прочее.
Серологические реакции. Серологические анализы помогают определить реакцию иммунитета на ВЭБ, при этом содержание вируса в крови не определяют. Серологические реакции позволяют выявить антитела к ВЭБ-инфекции:
- Антитела М-класса (IgM) к антигену капсидному (VCA) — образуются при острой фазе с самого начала инфицирования до полугода от начала болезни или при обострении хронической инфекции ВЭБ.
- Антитела G-класса (IgG) к антигену (VCA) — данные иммуноглобулины образуются после острой стадии заболевания (спустя три недели после инфицирования), во время реконвалесценции количество их растёт, кроме того их выявляют после перенесённого заболевания в течение всей жизни.
- Антитела G (IgG) к раннему антигену (ЕА) — аналогично М-классу эти антитела вырабатываются в период острой фазы ВЭБ-инфекции (в промежутке от одной недели до полугода с момента инфицирования).
- Поздние антитела G-класса (IgG) к ядерному антигену (EBNA) — возникают при полном выздоровлении, как правило, спустя полгода, и характеризуют стойкий иммунитет к ВЭБ-инфекции. Давайте поясним, что означает положительный результат на антитела к ВЭБ.
- Положительный результат определяет уровень иммуноглобулинов выше установленной нормы. Каждая лаборатория имеет свои показатели нормы, которые зависят от методов определения, видов оборудования и единиц измерения. Для удобства показатели нормы указывают в графах полученных результатов.

Диагностика методом полимеразно-цепной реакции является лабораторным методом исследования, направленный не на выявление иммунной реакции, а на определение наличия в организме самого вируса, его ДНК. Этот метод диагностики современный и обладает точностью в 99,9%.
Метод ПЦР позволяет обследовать кровь, мокроту, смывы из носоглотки, биопсионные образования различных опухолей. ПЦР к вирусу Эпштейна-Барр назначается ели имеются подозрения на генерализованную инфекцию ВЭБ, при иммунодефицитах, таких как ВИЧ, в сложных или сомнительных клинических случаях.
Метод также широко используют для выявления различных онкологических болезней. ПЦР не применяется на исследование вируса Эпштейна-Барр в качестве первого анализа, т. к. такого рода анализы очень сложные весьма дорогие.
Различается всего 2 результата ПЦР к ВЭБ: положительный и отрицательный результаты. Первый указывает на наличие ДНК ВЭБ в организме и на активный процесс вируса Эпштейна-Барр. Отрицательный результат, наоборот, свидетельствует об отсутствие вируса в организме.
По показаниям, возможно, проведение других исследований и консультаций. Консультации иммунолога и ЛОР-врача, рентгенография придаточных пазух носа и грудной клетки, УЗИ брюшной полости, проверка свёртываемости крови, консультации гематолога и онколога.
Вирус Эпштейна-Барр: методы лечения

Полностью излечиться от герпетических вирусов невозможно, даже используя самые современные методы лечения, так как ВЭБ хоть и не в активном состоянии, но все же на всю жизнь остаётся в В-лимфоцитах и других клетках.
Если иммунитет ослабнет вирус снова может активизироваться, обостриться ВЭБ-инфекция. Общего мнения как лечить ВЭБ ни у учёных ни у медиков нет до сих пор, и потому в наше время проводят много исследований в области противовирусного лечения. Все ещё не существует эффективных специфических препаратов в борьбе ВЭБ-инфекцией.
Инфекционный мононуклеоз рекомендуют лечить стационарно с возможностью применения в дальнейшем домашнего лечения. При этом если заболевание протекает умеренно, можно обойтись и без госпитализации.
При остром течении инфекционного мононуклеоза необходимо держать щадящую диету и режим: ограничить физические нагрузки, вести полупостельный режим, пить много жидкости, питаться нужно часто, сбалансировано и небольшими порциями, при этом исключить из рациона острую, жареную, солёную, сладкую, копчёную пищу.
Благоприятно действуют на течение заболевания кисломолочные продукты. Важно чтобы рацион содержал много витаминов и белков. Лучше отказаться от тех продуктов, в которых содержатся химические консерванты, усилители вкуса, красители. Необходимо убрать из рациона продукты-аллергены: цитрусы, шоколад, мёд, бобовые, некоторые фрукты и ягоды.
При лечении синдрома хронической усталости полезным будет придерживаться нормального режима труда, отдыха и сна, активных физических нагрузок, положительных эмоций, занятий любимым делом, полноценного питания и комплекса поливитаминов.
Медикаментозное лечение инфекции ВЭБ

Принципы лечения ВЭБ у взрослых и детей одинаковые, разница лишь в дозировках. Противовирусные препараты подавляют активность ДНК-полимеразы ВЭБ. В эту группу входят: Пацикловир, Ацикловир, Цидофовир, Герпевир, Фоскавир.
Данные лекарства эффективны лишь при онкологических заболеваниях, генерализованной ВЭБ-инфекции, хроническом течении заболевания и появлении осложнений.
Другие препараты обладают неспецифическим иммуностимулирующим и противовирусным действием, среди которых выделяют: Виферон, Интерферон, Циклоферон, Лаферобион, Арбидол, Изопринозин (Изопринозин), Ремантадин, Урацил, ИРС-19, Полиоксидоний и прочие. Эти Л. С. назначают только при тяжёлом течении заболевания.
Такие иммуноглобулины, как Полигам, Пентаглобин, Биовен рекомендованы при обострениях хронического ВЭБ, а также для восстановления после острого периода инфекционного мононуклеоза.
В этих иммуноглобулинах содержатся готовые антитела, которые связываются с вирионами вируса Эпштейна-Барр и выводят их из организма. Высоко эффективны при лечении хронической и острой ВИЭБ. Применяются лишь в стационарных клиниках в виде внутривенных капельниц.
К антибактериальным препаратам относят: Линкомицин, Азитромицин, Цефадокс, Цефтриаксон и другие. А вот антибиотики назначают исключительно при присоединении бактериальной инфекции, к примеру, при бактериальной пневмонии, гнойной ангине.
Лечение болезни подбирают индивидуально исходя из тяжести течения болезни, наличия соответствующих патологий и состояния иммунитета пациента.
Синдром хронической усталости можно лечить противовирусными препаратами: Герпевир, Ацикловир, Интерфероны; сосудистыми препаратами: Церебролизин, Актовегин; препаратами, защищающими нервные клетки от вируса: Энцефабол, Глицин, Инстенон, а также антидепрессантами, успокоительными препаратами и поливитаминами.

Лекарственную терапию эффективно дополняют народные методы лечения. Большим арсеналом для укрепления иммунитета обладает природа.
Детям старше 12 лет рекомендуют настойку Эхинацеи по 3–5 капель, а для взрослых по 20–30 капель 2–3 раза в сутки перед едой; настойку Женьшеня 2 раза в сутки по 5–10 капель.
Травяной сбор нельзя применять детям до 12 лет и беременным. В состав сбора входят: мята перечная, цветы ромашки, мать-и-мачеха, цветы календулы, женьшень.
Травы берут в равных пропорциях, размешивают и заваривают чай: на 1 столовую ложку травяного сбора 200,0 мл кипятка. Ждут заваривания 10–15 минут. Три раза в сутки принимают этот настой.
Зелёный чай с мёдом, лимоном и имбирём увеличивает защитные силы организма. Пихтовое масло применяют наружно. А также используют сырые яичные желтки: натощак каждое утро 2–3 недели. Они способствуют хорошей работе печени, содержат в себе много полезных веществ.
Читайте также:


