Лечение красной волчанки моноклональными антителами
С.К. Соловьев
ГУ Институт ревматологии РАМН, Москва
Системная красная волчанка (СКВ) - классическое аутоиммунное ревматичес кое заболевание, в основе патогенеза которого лежат дефекты иммунорегуляции, приводящие к неконтролируемой гиперпродукции В лимфоцитами аутоантител к компонентам собственных тканей и развитию хронического вос паления, затрагивающего многие органы и системы. Прогрессирующее поражение жизненно важных органов определяет жизненный и социальный прогноз больных СКВ, при "катастрофическом" течении летальность достигает 40% в год, в связи с чем принципиальное значение имеет разработка новых методов патогенети ческой терапии этого заболевания.
В последние десятилетия сформиро ваны основные принципы терапии СКВ, в основе которых лежит применение раз личных режимов глюкокортикоидной (ГК) терапии и цитотоксических препаратов. Современные терапевтические схемы с использованием пульс-терапии метилпреднизолоном и циклофосфаном (ЦФ) значительно улучшили отдаленную выжи ваемость и высокоэффективны при развитии угрожающих состояний у больных СКВ. Наиболее ярким примером повыше ния качества лечения СКВ является более чем пятикратное увеличение 5-и летней выживаемости у больных с волчаночным нефритом. Однако, отдаленный жизненный прогноз у этой категории больных остается неблагоприятным. Так, 20-и летняя выжи ваемость при развитии люпус-нефрита, даже при использовании современных терапевтических программ, не превышает 20%. Значительно отягощает кратко срочный и отдаленный жизненный прогноз у больных СКВ развитие таких угрожающих состояний как цитопенических криз, поражение центральной и периферической системы, пневмонит, катастрофическое течение АФС и генерализованный (криоглобулинемический) васкулит. Основными факторами, влияющими на развитие неблагоприятного исхода при СКВ, является резистентность к высоким дозам ГК и циклофосфана и торпидное, прогрес сирующее течение болезни. В тоже время применение высоких доз ГК и ЦФ ассоциируется с повышением риска воз никновения тяжелых вирусных и бакте риальных инфекций, что в значительной степени лимитирует их назначение.
Безусловно, "сверхзадачей" терапии СКВ и других аутоиммунных заболеваний, является создание препаратов селективно влияющих на ключевые звенья патогенеза. В этой связи перспективным направ лением фармакотерапии СКВ являются препараты, блокирующие пролиферацию В - клеток, среди которых одним из наиболее изученных, безусловно является Ритуксимаб (Rituxumab, MabTHera, Roch,), который представляет собой рекомби-нантные химерные (мышь-человек) моноклональные антитела к поверхностным рецепторам В-лимфоцитов - CD20. Пред полагаемый механизм действия ритуксимаба, направленный на подавление активности В клеток, может реализовываться за счет антитело-зависимой клеточной цитотоксичности, комплемент-зависимой цитотоксичности, ингибиции клеточной пролиферации и индукции апоптоза В лимфоцитов. Молекулярные взаимодействия связывания CD20 могут приводить к перестройке мембранных липидов, активации ферментов и регу ляции синтеза интерлейкина 10. Основной мишенью ритуксимаба являются клетки предшественники, незрелые, зрелые и "наивные" В-лимфоциты. На плазмати ческие клетки препарат не оказывает влияния, из-за отсутствия их на мембране CD20.
Впервые ритуксимаб был применен для лечения больных злокачественной В-клеточной лимфомой в 1997 г. Моно терапия ритуксимабом В-клеточных лимфом эффективна у 50% больных и в 10% случаев наблюдается клиническая ремис сия, в тоже время при комбинации его с химиотерапией эффективность лечения возрастает до 81-97%, а частота ремиссий достигает 74%.
Первое сообщение о применении ритуксимаба при СКВ относится к 2001 г когда F.Petschner et al. с успехом исполь зовали его для лечения "катастро фической" СКВ по жизненным показаниям.
В настоящее время, по данным литературы, ритуксимаб применялся в лечении более чем 200 больных СКВ. Назначение препарата в дозах от 1000 до 2000 мг (обычно РМ назначается по 375 мг/м 2 еженедельно в течение 4 недель) оказалось высокоэффективным у больных с поражением суставов, кожи, слизистых оболочек, полисерозитом, лихорадкой и гематологическими нарушениями. Особо го внимания заслуживает тот факт, что высокая эффективность ритуксимаба (око ло 80%) отмечалась при развитии прогрессирующего волчаночного нефрита, тяжелом поражении ЦНС, гематоло гическом кризе, пневмоните и катастро фическом течении АФС - при неэффек тивности пульс-терапии ГК, ударных доз циклофосфана, иммуносорбции, плазмафереза, мофетила микофенолата и цик лоспорина.
В настоящее время проведено нес колько открытых пилотных испытаний эффективности ритуксимаба у больных с волчаночным нефритом. Так, в одном из них (P. Sfikakis et al.) препарат был назначен 10 больным с активным пролиферативным люпус-нефритом (III-IV класс по класси фикации ВОЗ), без признаков почечной недостаточности. До включения в ис следование все пациенты получали вы сокие дозы глюкокортикоидов (ГК), пульс-терапию циклофосфаном (ЦФ) или мофетила-микофенолат (МФ) без существен ного эффекта. Инфузии РМ по 375 мг/м - проводились еженедельно в течение 4-х недель. В результате проведенного лечения частичная ремиссия (улучшение на 50% клинико-лабораторных параметров нефрита) зафиксирована у 8 больных через 1-4 месяца. В последующем полная ремиссия (протеинурия В большинстве исследований пока зано, что эффект терапии этим препаратом при волчаночном нефрите развивается не сразу, как правило значимое уменьшение протеинурии, повышение клубочковой фи льтрации, увеличение содержания альбу мина в сыворотке крови, наблюдается на 2-3 месяце от начала лечения и достигает своего максимума к 5-6 месяцу. Одно временно наблюдается уменьшение ин дексов активности СКВ (BILAG, SLEDAI), антител к ДНК, повышение комплемента. Напротив, применение Ритуксимаба у больных с высокой активностью, обус ловленной внепочечными проявлениями СКВ - цитопенией, полиартритом, серозитом, пневмонитом и АФС, может при вести к развитию положительной динамики уже через несколько дней.
Отчетливый быстрый эффект ритукси маба отмечен у больных с критическим течением СКВ, обусловленным пораже нием ЦНС. Поражение ЦНС (нейролюпус), сопровождающееся развитием состояния угрожающего жизни у больных СКВ, наблюдается достаточно редко, в 2-4% случаев. Терапия таких тяжелых прояв лений волчаночного поражения ЦНС, как судорожный синдром, демиелинизирующая нейропатия, поперечный миелит, психоз - представляет большие трудности, стандартных терапевтических алгоритмов не существует, а летальность превышает 50%. В этой связи особый интерес вызывает публикация Tokunaga, в которой сообщается о применении ритуксимаба у 10 больных СКВ по жизненным пока заниям. У всех описываемых больных наблюдались различные проявления пора жения ЦНС: потеря сознания, судороги, дезориентация, атаксия, сенсорная ней ропатия, психоз. Во всех случаях наз начение ритуксимаба привело к быстрому улучшению, развившемуся в течение нес кольких дней от начала лечения. Авторы отмечают быстрый выход из коматозного состояния, уменьшение и исчезновение двигательных и чувствительных наруше ний, купирование судорожного синдрома, психоза и депрессии. Нарастание поло жительной динамики, переходящее в стабильное улучшение наблюдалось в течение 6-7 месяцев, у всех больных за этот период удалось существенно снизить дозу преднизолона и отменить иммунодепрессанты. Полученные данные свидетельствуют о высокой эффективности инфузий ритуксимаба при СКВ с развитием критических состояний, непосредственно угрожающих жизни пациентов. Особенно важным представляется то, что высокая эффективность терапии наблюдалась у больных с тяжелым, прогрессирующим поражением ЦНС с неэффективностью интенсивной терапии, включающей ударные дозы ГК, ЦФ в комбинации с плазмаферезом и иммуносорбцией.
Применение ритуксимаба у больных СКВ не только индуцирует развитие клинического улучшения, продолжитель ностью от нескольких месяцев до 1 года, но и приводит к появлению различных иммунологических феноменов. Практи чески все исследователи отмечают развитие лимфопении, подавление В-лимфоцитов, наблюдаемое практически сразу после проведения курса лечения ритуксимабом. Leandro, Anolik сообщают о значительном подавлении В лимфоцитов, продолжающееся в среднем около 4 месяцев от начала терапии и корре лирующее с развитием клинического эффекта, нормализацией гемоглобина, СОЭ, комплемента. По мнению авторов, появление на фоне терапии антихиме рических антител может провоцировать развитие аллергических реакций. Те же авторы не выявили достоверного снижения антител к ДНК. Оценивая влияние ритуксимаба на активность люпус-нефрита Stifakis et al. так же обращают внимание на подавление 99% В лимфоцитов у 8 из 10 больных, наблюдаемое от 1 до 7 месяцев. Продолжительность угнетения В клеток соответствовала длительности ремиссии и, напротив, их регенерация предшество вала развитию обострения.
Большинство исследователей отме чают достаточно хорошую переносимость препарата. Подавляющее большинство побочных реакций возникающих во время или после проведения инфузий, так или иначе могут быть связаны с "биоло гической", белковой основой препарата. Как правило, наблюдаются такие явления как озноб, лихорадка, гипотензия, одышка. Обычно такие побочные реакции устра няются более медленной скоростью введения, дробным введением. Для профилактики может использоваться пара цетамол, антигистаминовые препараты или ГК в небольших дозах. Сложившимся правилом, позволяющим практически пол ностью устранять "инфузионные" реакции, является использование инфузомата и внутривенное введение 100-250 мг метипреда непосредственно перед инфузией.
В большинстве исследований посвя щенных применению ритуксимаба как в онкологии, так и при аутоиммунных заболеваниях, не находит свое под тверждение концепция об увеличении риска развития оппортунистических инфекций. Вероятно это связано с тем, что несмотря на значительное снижение циркулирующих В лимфоцитов после инфузии РМ, не наблюдается сколь либо существенного снижения продукции иммуноглобулинов, что в свою очередь можно объяснить наличием значительного количества долгоживущих плазматических клеток.
Российский регистр больных СКВ получающий терапию ритуксимабом
Прогностически неблагоприятные варианты течения СКВ и состояния угрожающие жизни
| • Прогрессирующий нефрит (III-IV класс по ВОЗ) • Поражение ЦНС (поперечный миелит, судороги, кома, психоз) • Геморрагический альвеолит • Гематологический криз • КАФС (тромбозы, мультиорганное поражение) • Генерализованный (fulminant) некротизирующий васкулит | • "Стандартные" методы терапии • Пульс-терапия метилпреднизолоном и циклофосфаном • Внутривенный иммуноглобулин • Плазмаферез • Антикоагулянты • Реанимационные мероприятия Смертельные исходы в течение 1-го года до 40% |
Изменение 5-и летней выживаемости у больных С IV классом ВН (J.Cameron 1998)
| Годы | Выживаемость % |
| 1953-1969 отсутствие патогенетической терапии | 17% |
| 1970-1979 средние и большие дозы ГКС, пульс-терапия | 55 (в 3 раза!) |
| 1980-1983 + циклофосфан | 80 |
| 1990-1995 + мофетила микофенолат, циклоспорин, комбинированная ПТ | 82 |
| XXI век: МабТера, А-BLyS, Октембра . | ? |
20-летняя выживаемость больных СКВ
Анти-В клеточная терапия Ритуксимаб (МабТера, ROCHE)
Показания для назначения Ритуксимаба при СКВ
Неконтролируемая активность болезни
Влияние ритуксимаба на показатели активности СКВ
Эффективность РМ у больных с волчаночным нефритом
- 2002 - 2007 гг. РМ использован для лечения 72 б-ных с рефрактерным к стандартной терапии прогрессирующим ВН ( у 25 в комбинации с ЦС)
- Клинический и лабораторный эффект достигнут у 77%
- Полная или частичная ремиссия достигалась через 6-8-12 недель, продолжительность эффекта от 3 месяцев до 1,5 лет
- Через 1 год значительное уменьшение морфологической активности при повторной биопсии
Показатели активности волчаночного нефрита после терапии Ритуксимабом
Изменение морфологической активности нефрита через год после терапии Ритуксимабом
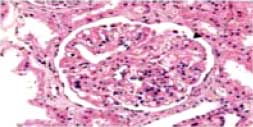 | До лечения Индекс активности 10 |
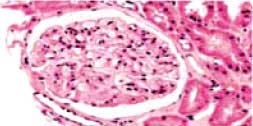 | Через год Индекс активности 1-2 |
Эффективность Ритуксимаба при неиролюпусе
М. Тikunаgа et al. 2006
| Клинические проявления | Результат и скорость достижения эффекта | Длительность эффекта |
| 6 больных Кома, судороги, каталепсия, психоз, нейропатия, галлюцинации, головные боли | Выздоровление 2- 5 дней | 4-29 месяцев |
| 4 больных Депрессия, психоз, нейропатия | Улучшение 1-4 недели | 7-14 месяцев |
Побочные эффекты и осложнения ритуксимаба
- Инфузионные реакции (озноб, гипотония, отеки, высыпания, зуд, лихорадка) могут наблюдаться у 10-20% больных. Возможно обусловлены образованием антихимерных антител (антител против РМ). Вероятность развития при повторных инфузиях уменьшается. Профилактика - метилпреднизолон 100 мг в/в до инфузии.
- Тяжелые, требуюшие антимикробной терапии инфекции редки. Чаще наблюдаются ОРВИ, герпетичекая инфекция.
ЛИТЕРАТУРА
1. Lipsky PE. Systemic lupus erythe matosus: an autoimmune disease of B cell hyperactivity. Nat Immunol. 2001;2:764-766.
2. Silverman GJ. Anti-CD20 therapy in systemic lupus erythematosus: a step closer to the clinic. Arthritis Rheum. 2005;52:371-377
3. Vasoo S, Hughes GRV Perspectives on the changing face of lupus mortality. Autoimmun Rev. 2004;3:415-417.
4. Pryor BD, Bologna SG, Kahl LE. Risk factors for serious infection during treatment with cyclophosphamide and high-dose corti costeroids for systemic lupus erythemato sus. Arthritis Rheum. 1996;39:1475-1482.
5. Chambers SA, Isenberg DA Anti - B cell therapy (Rituximab) in the treatment of autoimmune disease. Lupus. 2005;14:210-214.
6. John Looney, Jennifer H. Anolik, Debbie Campbell, Raymond E. Felgar et al. B Cell Depletion as a Novel Treatment for Systemic Lupus Erythematosus A Phase I/II Dose-Escalation Trial of Rituximab Arthritis Rheum. 2004;Aug;8:2580-2589.
7. Sfikakis PP, Boletis JN, Lionaki S., Vigklis V., Fragiadaki KG, Iniotaki A., and Moutsopoulos HM Remission of Proliferative Lupus Nephritis Following B Cell Depletion Therapy Is Preceded by Down-Regulation of the T Cell Costimulatory Molecule CD40 Ligand An Open-Label Trial. Arthritis Rheum. 2005;52(2):501-513.
8. Mikiko Tokunaga et al. Efficacy of rit uximab (Anti-CD20) for refractory systemic lupus erythematosus involving the central nervous system. 15 Nov 2006; Ann Rheum Dis
9. С.К. Соловьев, Е.Л. Насонов, М.А.Котовская. Ритуксимаб в лечении системной красной волчанки. Русский Медицинский журнал, 2005, 26, 1731-1736.
10. Е.Л. Насонов, С.К. Соловьев. Перспективы применения моноклональных антител к В-лимфоцитам (ритуксимаб) при воспалительных ревматических заболеваниях. Научно-практическая ревматология 1, 2007, 4-8.
Подход к лечению проявлений и симптоматики системной красной волчанки зависит от особенностей заболевания и степени его тяжести.
Для всех больных СКВ подходят общие рекомендации:
- защита от солнечных лучей,
- правильное питание,
- физические упражнения,
- прекращение или ограничение курения,
- коррекция режима иммунизации,
- лечение сопутствующих заболеваний.
При легкой и средней тяжести СКВ обычно используются:
- неспецифические противовоспалительные препараты (NSAIDs),
- противомалярийные,
- кортикостероиды.
При развитии заболевания и выраженности клинических манифестаций дозировки кортикостероидов становятся больше и добавляются препараты, подавляющие иммунные реакции.
Неспецифические противовоспалительные препараты (NSAIDs)
Используются для облегчения мышечных и суставных болей, при наличии припухлостей и отечности. Эта группа препаратов обладает болеутоляющими, противовоспалительными и противосвертывающими свойствами, что благоприятно сказывается на общей симптоматике системной красной волчанки, но при их назначении надо учитывать возможность нежелательных проявлений действия лекарств.
Блокада синтеза простагландинов посредством ингибирования энзимов циклооксигеназ (COX, COX2), вследствие чего развивается противовоспалительный, анальгезирующий и жаропонижающий эффекты.
- раздражение желудочно-кишечного тракта,
- кровотечения,
- нефротоксичность,
- гепатотоксичность,
- гипертензия.
- возможность появления:
- тошноты и рвоты,
- боли в животе,
- темного (до дегтеобразного) стула.
- общий развернутый анализ крови,
- креатитнин сыворотки крови,
- функциональные пробы печени,
- общий анализ мочи.
Противомалярийные препараты
Некоторые антималярийные лекарства доказали свою эффективность при лечении различных проявлений СКВ и ее обострений. Хотя механизм их действия точно не выяснен, предполагается, что противомалярийные средства могут мешать активации Т-лимфоцитов, ингибировать активность цитокинов, внутриклеточные toll-рецепторы, распознающие и связывающие чужеродные элементы . Наиболее часто применяется гидроксихлорохин (Плаквенил) внутрь по в сутки.
- патология желтого пятна,
- мышечная слабость.
глазное дно и поля зрения перед лечением и затем каждые
Кортикостероидные гормоны
Кортикостероидные препараты подменяют естественные гормоны коры надпочечников и помогают контролировать кровяное давление и функции иммунитета (например, блокада активации цитокинов и ингибирование интерлейкинов, γ-интерферона и фактора некроза опухолей-α). Кортикостероиды уменьшают выраженность боли и отечности, связанных с воспалением, которое возникает при обострениях заболевания. Ввиду серьезности побочных эффектов при длительном применении, кортикостероиды надо использовать в настолько малых дозах, насколько это возможно, и только тогда, когда надо купировать активное обострение СКВ.
Обычные дозировки — преднизон внутрь При обострениях — метилпреднизолон внутривенно в сутки в течение дней в зависимости от клиники.
- увеличение веса тела,
- гипертензия,
- гипергликемия,
- остеопороз,
- катаракта,
- отеки,
- гипокалиемия,
- мышечная слабость,
- замедление роста у детей,
- снижение иммунитета к инфекционным заболеваниям,
- глаукома.
- артериальное давление,
- плотность костной ткани (минимум ежегодно),
- уровень глюкозы крови (минимум раз в
- уровень калия крови,
- липидный профиль (минимум ежегодно).
Иммуносупрессоры (лекарства, подавляющие иммунные реакции)
Оказывают комплексное угнетающее действие на иммунитет (например, понижение пролиферации Т- и В-лимфоцитов, разрывы цепочек нуклеиновых кислот). Обычно используются в тяжелых случаях, когда высокие дозы кортикостероидов или антималярийные препараты не помогают. Кроме этого, они применяются тогда, когда надо добиться и поддерживать ремиссию.
Иммуносупрессоры можно давать вместе с высокими дозами глюкокортикоидов при лечении обострений, для снижения дозировок каждого применяемого препарата, для снижения частоты проявлений побочных эффектов. Обычно используются:
циклофосфамид (cyclophosphamide, Cytoxan) внутрь1-3 мГ/кГ/сутки или внутривенно вместе или без кортикостероидов. азатиоприн (azathioprine, Azasan, Imuran) внутрь микофенолат (CellCept) для проблем, связанных с поражением почек при СКВ) — внутрь
- угнетение кроветворения,
- гепатотоксичность,
- нарушение функции почек,
- бесплодие,
- повышение риска инфекционного и/или онкозаболевания.
- общий анализ крови,
- число тромбоцитов,
- креатинин сыворотки,
- печеночные пробы,
- общий анализ мочи.
Моноклональные антитела
Белимумаб (belimumab, Benlysta, ранее известный как LymphoStat-B) разрешен FDA в марте 2011 г. как первый препарат моноклональных антител, предназначенный для лечения системной красной волчанки. По сути, это первый препарат за 50 лет, специально предназначенный для этого.
Белимумаб ингибирует активацию В-лимфоцитов посредством воздействия на белок, необходимый для активных В-лимфоцитов — BLyS.
Белимумаб рекомендован больным с активной СКВ, получающих неспецифические противовоспалительные, антималярийные, глюкокортикоиды и/или препараты, угнетающие иммунитет.
Препарат назначается внутривенно в количестве 10 мГ/кГ; введение осуществляется медленно в течение 1 часа и более. Первые 3 введения — с интервалом 2 недели между введениями, далее интервал между введениями увеличивается до 4 недель.
- тошнота,
- жидкий стул,
- лихорадочные реакции,
- назофарингит,
- бессонница,
- боли в конечностях,
- депрессия,
- мигрень,
- гастроэнтерит,
- инфекции:
- бронхит,
- пневмония,
- целлюлит,
- инфекции мочевыводящих путей.
- деятельность желудочно-кишечного тракта,
- инфекционную симптоматику,
- изменения настроения и поведения,
- реакции на введение препарата.
Ритуксимаб (rituximab, Rituxan) — продукт генной инженерии, химерическое моноклональное антитело к антигену CD20, обнаружившее и определенный потенциал для лечения СКВ.
Предполагается, что В-лимфоциты, отвечающие за синтез патологических аутоантител и других иммуноактивные вещества, имеющие отношение к патогенезу системной красной волчанки, разрушаются ритуксимабом.
В течение последних лет как обнадеживающие, так и неоднозначные данные относительно применения ритуксимаба, назначавшегося вместе с кортикостероидами и иммуносупрессорами при СКВ у детей и взрослых, были получены в нескольких клинических испытаниях.
Польза ритуксимаба была замечена и при волчаночном нефрите, артралгии, артрите, кожном васкулите, воспалении слизистой, высыпаниях, слабости и неврологической симптоматике . Побочные эффекты препарата как правило выражены несильно, хотя зафиксированы и описаны как незначительные, так и более выраженные реакции на введение препарата.
В исследовании Terrier et al. положительное действие ритуксимаба описано у 71% пациентов, причем значительный эффект наблюдался при рефрактерном течении заболевания, а так же были отмечены улучшения со стороны кожи, суставов, почек, крови при приемлемой переносимости препарата. В другом исследовании с участием 188 больных СКВ были получены еще более впечатляющие результаты (значительное улучшение состояния 91% больных, особенно при люпусном нефрите, при том, что побочное действие и инфекции были отмечены у 23% пациентов).
Тем не менее, 2 дополнительных рандомизированных исследования, проводившихся начиная с 2010 г., не продемонстрировали значительных клинических улучшений у пациентов, принимавших ритуксимаб вместе с кортикостероидами.
Таким образом, обоснованность применения ритуксимаба при системной красной волчанке нуждается в дополнительных исследованиях.
Дополнительные возможности лечения СКВ
Исследователи интересуются возможностью трансплантации стволовых клеток как способ внедрения в организм здорового клеточного материала с целью перестройки иммунной системы больного.
Некоторые полагают, что комбинация DHEA (дегидроэпиандростерона), регулирующего половые гормоны, и ритуксимаба особенно хороша для больных, которые не реагируют на традиционные иммуносупрессоры.
(создана: 2013-04-23 16:59:35, дополнена: 2014-04-09 22:36:30)
Белимумаб при системной красной волчанке - клиническая эффективность и обоснование лечения, патофизиология, побочное действие, рекомендации.
Аннотация научной статьи по клинической медицине, автор научной работы — Денисова Рина Валериановна, Алексеева Е. И.
Гемолитическая анемия встречается в 10% случаев системной красной волчанки у детей с гематологическими изменениями. Для лечения данного состояния применяют высокие дозы глюкокортикоидов. Препаратами второй линии при рефрактерном течении заболевания являются азатиоприн, микофенолата мофетил, циклоспорин и циклофосфамид. Ритуксимаб — анти-С020 моноклональное антитело — используют для лечения системной красной волчанки , рефрактерной к стандартной иммуносупрессивной терапии. В данной статье представлен случай успешной терапии гемолитической анемии у девочки-подростка с системной красной волчанкой . Назначение ритуксимаба позволило избежать повышения дозы глюкокортикоидов и назначения циклофосфамида, а также предотвратить развитие тяжелых нежелательных явлений от терапии высокими дозами этих препаратов. Однако для оценки продолжительности эффекта, безопасности терапии, подбора оптимальной дозы препарата необходимы данные многоцентровых рандомизированных контролируемых исследований.
Похожие темы научных работ по клинической медицине , автор научной работы — Денисова Рина Валериановна, Алексеева Е. И.
Anti-CD20 monoclonal antibodies in treatment of haemolytic anemia in a teenage girl with systemic lupus erythematosus
Haemolytic anemia occurs in 10% of the cases of systemic lupus erythematosus in children with hematological disturbances. High doses of glucocorticoids are used for the treatment of this condition. The second-line drugs in cases of refractory disease course are azathioprine, mycophenolate mofetil, cyclosporine and cyclophosphamide. Rituximab (anti-CD20 monoclonal antibodies) is used for treatment of systemic lupus erythematosus , resistant to the standard immunosuppressive therapy. In this article a history case of successful treatment of haemolytic anemia in a teenage girl with systemic lupus erythematosus is demonstrated. Rituximab treatment allowed to avoid the increasing of glucocorticoids dose and cyclophosphamide introduction, as well as to prevent severe side-effects of afore-mentioned drugs. However in order to establish the duration of the clinical effect, safety of performed treatment and adjustment of appropriate drug dosage the data of multicenter randomized controlled trials are needed.
Р.В. Денисова1, Е.И. Алексеева1, 2
1 Научный центр здоровья детей РАМН, Москва, Российская Федерация
2 Первый московский государственный медицинский университет им. И.М. Сеченова, Российская Федерация
Анти-CD20 моноклональные антитела в терапии гемолитической анемии у девочки-подростка с системной красной волчанкой
Гемолитическая анемия встречается в 10% случаев системной красной волчанки у детей с гематологическими изменениями. Для лечения данного состояния применяют высокие дозы глюкокортикоидов. Препаратами второй линии при рефрактерном течении заболевания являются азатиоприн, микофенолата мофетил, циклоспорин и циклофосфа-мид. Ритуксимаб — анти-CD20 моноклональное антитело — используют для лечения системной красной волчанки, рефрактерной к стандартной иммуносупрессивной терапии. В данной статье представлен случай успешной терапии гемолитической анемии у девочки-подростка с системной красной волчанкой. Назначение ритуксимаба позволило избежать повышения дозы глюкокортикоидов и назначения циклофосфамида, а также предотвратить развитие тяжелых нежелательных явлений от терапии высокими дозами этих препаратов. Однако для оценки продолжительности эффекта, безопасности терапии, подбора оптимальной дозы препарата необходимы данные многоцентровых рандомизированных контролируемых исследований.
Ключевые слова: системная красная волчанка, ритуксимаб, гемолитическая анемия, антифосфолипидный синдром. (Вопросы современной педиатрии. 2012; 11 (6): 147-152)
Системная красная волчанка (СКВ) — системное аутоиммунное заболевание, характеризующееся распространенным воспалением сосудов и соединительной ткани. Более 15-20% случаев СКВ дебютирует в детском возрасте. Распространенность СКВ составляет от 10 до 20 на 100 тыс. детей в зависимости от этнической принадлежности [1]. В отличие от взрослых, дебют СКВ у детей более тяжелый и агрессивный 4.
СКВ — это мультифакториальное заболевание: в его этиопатогенезе играют роль генетические, гормональные, иммунные факторы и факторы внешней среды. Многие клинические проявления СКВ обусловлены наличием аутоантител и образованием иммунных комплексов. Повышение концентрации аутоантител может быть результатом дефекта В лимфоцитов, что приводит к большей продолжительности их жизни, длительной активации и экспрессии патологических рецепторов 8. Таким образом, лекарственный препарат, воз-
R.V. Denisova1, E.I. Alekseeva1, 2
1 Scientific Centre of Children Health, RAMS, Moscow, Russian Federation
2 I.M. Sechenov First Moscow State Medical University, Russian Federation
Anti-CD20 monoclonal antibodies in treatment of haemolytic anemia in a teenage girl with systemic lupus erythematosus
Haemolytic anemia occurs in 10% of the cases of systemic lupus erythematosus in children with hematological disturbances. High doses of glucocorticoids are used for the treatment of this condition. The second-line drugs in cases of refractory disease course are azathioprine, mycophenolate mofetil, cyclosporine and cyclophosphamide. Rituximab (anti-CD20 monoclonal antibodies) is used for treatment of systemic lupus erythematosus, resistant to the standard immunosuppressive therapy. In this article a history case of successful treatment of haemolytic anemia in a teenage girl with systemic lupus erythematosus is demonstrated. Rituximab treatment allowed to avoid the increasing of glucocorticoids dose and cyclophosphamide introduction, as well as to prevent severe side-effects of afore-mentioned drugs. However in order to establish the duration of the clinical effect, safety of performed treatment and adjustment of appropriate drug dosage the data of multicenter randomized controlled trials are needed.
Key words: systemic lupus erythematosus, rituximab, haemolytic anemia, antiphospholipid syndrome.
(Voprosy sovremennoi pediatrii — Current Pediatrics. 2012; 11 (б): 147-152)
действующий на В клетки, может оказаться высокоэффективным в лечении СКВ.
Ритуксимаб — многообещающее средство для лечения СКВ, т. к. это моноклональное химерное анитело к CD20-антигену, который экспрессируется на В клетках с пре-В-стадии до зрелых форм, но отсутствует на стволовых, про-В и плазматических клетках. Это приводит к длительной деплеции числа В лимфоцитов в периферической крови, что в результате обусловливает хороший клинический ответ на терапию у больных СКВ. Деструкция В лимфоцитов происходит благодаря различным механизмам, таким как антителозависимая клеточная цитотоксичность, комплементзависимая цитотоксичность, апоптоз и ингибирование клеточного роста 12.
Ритуксимаб продемонстрировал высокую эффективность в лечении лимфопролиферативных заболеваний у детей, однако в настоящее время его использование распространилось и на лечение других аутоиммунных заболеваний, рефрактерных к стандартной иммуносупрес-сивной терапии (идиопатическая тромбоцитопеническая пурпура, синдром Эвана, аутоиммунная гемолитическая анемия, ювенильный идиопатический артрит, ювенильный дерматомиозит, васкулит, СКВ) 16.
Мы хотим представить успешное применение анти-С020 моноклональных антител (ритуксимаба) в терапии гемолитической анемии у девочки-подростка с СКВ.
В возрасте 10 лет, в феврале 2009 г., девочка была госпитализирована в гематологический стационар в связи с длительным носовым кровотечением. Состояние при поступлении было тяжелым, что обусловливалось геморрагическим синдромом: геморрагическая сыпь на конечностях, тромбоцитопения до 43х109/л, гемолитическая анемия (концентрация гемоглобина 56 г/л, положительная реакция Кумбса). Состояние было расценено как аутоиммунная гемолитическая анемия. В стационаре девочке проводились трансфузии эритромассы, свежезамороженной плазмы, внутривенные инфузии глюкокортикоидов, был назначен преднизолон перорально в дозе 2 мг/кг массы тела (65 мг/сут). На фоне проводимой терапии удалось купировать геморрагический синдром, нормализовались лабораторные показатели, было рекомендовано постепенное снижение дозы пред-низолона. В конце марта 2009 г. преднизолон был полностью отменен.
положительный волчаночный антикоагулянт, повышение антинуклеарного фактора до 1/1280 (N до 1/160), титра антител к двуспиральной ДНК до 250 МЕд/мл (N до 20), титра IgG к кардиолипинам до 85 Ед/мл (N до 10), IgG к р2-гликопротеидам до 150 Ед/мл (N до 9), снижение концентрации С4-компонента комплемента до 0,16 г/л (N 0,17-0,35), был подтвержден диагноз СКВ (дерматит, геморрагический синдром, тромбоцитопения, гемолитическая анемия, антифосфолипидный синдром) острого течения. Активность по шкале SELENA SLEDAY соответствовала 6 баллам.
В связи с активным течением болезни, угрозой кровотечения и прогрессированием антифосфолипидного синдрома было принято решение о проведении пульс-терапии метилпреднизолоном в дозе 500 мг в течение трех последовательных дней, а также о назначении преднизолона в дозе 1 мг/кг массы тела (40 мг/сут) и гидроксихлорохина в дозе 200 мг/сут. С учетом высокой активности антифосфолипидного синдрома пациентке проводили инфузию иммуноглобулина человеческого нормального из расчета 1 г/кг массы тела на курс. В связи с выраженной гипокоагуляцией (повышение международного нормализованного отношения до 2,49, активированного частичного тромбопластинового времени — до 92 с, тромбинового времени — до 66 с), а также с угрозой кровотечения была назначена инфузия свежезамороженной плазмы. На фоне лечения у пациентки не образовывалось новых геморрагических элементов на коже, практически полностью купировались явления дерматита на лице, восстановились показатели коагулограммы и клинического анализа крови. В октябре 2009 г. она была выписана с рекомендациями продолжить терапию по месту жительства и постепенно снижать дозу преднизолона.
Во время следующей госпитализации в апреле 2010 г. состояние больной оставалось стабильным, доза преднизолона была снижена до 15 мг/сут (0,3 мг/кг массы тела), клинических признаков заболевания зафиксировано не было, однако сохранялось повышенное содержание антинуклеарного фактора — до 4,5 Ед/л (N до 1,5), антител к двуспиральной ДНК — до 98 МЕд/мл, IgG к кардиолипинам — до 260 ед/мл и низкая концентрация С4-компонента комплемента — 0,075 г/л. В связи с отсутствием клинических проявлений заболевания коррекции терапии не проводилось.
После снижения дозы преднизолона до 10 мг/сут (0,2 мг/кг массы тела) у пациентки вновь рецидивировали носовые кровотечения. По месту жительства проводилась пульс-терапия метилпреднизолоном в дозе 500 мг в течение трех последовательных дней, с временным положительным эффектом. Во время госпитализации в марте 2011 г. в связи с рецидивированием геморрагического синдрома, гемолитической анемии (снижение концентрации гемоглобина до 95 г/л, эритропения до 3,2х1012/л, положительная реакция Кумбса) и высоким титром аутоантител было принято решение о проведении пульс-терапии метилпреднизолоном в дозе 500 мг трижды, назначении микофенолата мофетила в дозе 1,5 г/сут (1 мг/м2 поверхности тела), отмене гидрокси-хлорохина. Коррекция дозы преднизолона в таблетках не проводилась. Девочка была выписана с рекомендациями продолжить терапию по месту жительства.
Несмотря на лечение, продолжали рецидивировать носовые кровотечения, плохо поддающиеся местной терапии, геморрагическая сыпь на конечностях, прогрессирующее снижение концентрации гемоглобина и числа эритроцитов. По жизненным показаниям трижды прово-
дилась пульс-терапия метилпреднизолоном в дозе 500 мг в течение трех последовательных дней.
Применение ритуксимаба у пациентки было одобрено Локальным независимым этическим комитетом НЦЗД РАМН. Перед началом терапии мать пациентки подписала информированное согласие.
Ритуксимаб назначали в дозе 375 мг/м2 поверхности тела 1 раз в нед на протяжении 4 последовательных нед. Перед инфузией препарата проводилась премедикация трописетроном в дозе 5 мг и метилпреднизолоном в дозе 100 мг. Нежелательных инфузионных реакций зарегистрировано не было. После 3-го введения появился кашель, и, по данным компьютерной томографии органов грудной клетки, была диагностирована правосторонняя среднедолевая пневмония, по поводу чего девочка получала антибактериальную терапию цефтриаксоном, кларитромицином, ко-тримоксазолом в течение 10 дней. После окончания курса антибактериальной терапии и рентгенологического контроля грудной клетки было проведено 4-е введение ритуксимаба. На фоне терапии купировались клинические проявления болезни, повысились концентрация гемоглобина (до 110 г/л) и число эритроцитов (до 3,8х1012/л), зафиксировано снижение титра антинуклеарного фактора (до 8,9 ед/л), антител к двуспиральной ДНК (до 119 МЕД/мл), IgG к кардиолипинам (до 168 ЕД/мл). В октябре 2011 г. пациентка была
выписана с рекомендациями продолжить терапию мико-фенолата мофетилом в дозе 1,5 г/сут, преднизолоном в дозе 10 мг/сут, с профилактической целью был назначен ко-тримоксазол в дозе 900 мг/сут, а также в связи с высоким титром антифосфолипидных антител было рекомендовано возобновить прием гидроксихлорохина в дозе 200 мг/сут.
В течение 2012 г. девочке 3 раза проводилось плановое клинико-лабораторное обследование в условиях ревматологического отделения НЦЗД РАМН. В мае 2012 г., несмотря на клиническую ремиссию болезни, в связи с высоким титром аутоантител и низкой концентрацией С4-компонента комплемента (табл.) проводился повторный курс терапии ритуксимабом в дозе 375 мг/м2 поверхности тела 1 раз в нед в течение 4 последовательных нед, без нежелательных инфузионных реакций.
Во время госпитализации в сентябре 2012 г. состояние оставалось стабильным, геморрагический синдром не рецидивировал, с момента инициации терапии ритуксимабом ни разу не проводилась пульс-терапия метилпреднизолоном, доза преднизолона в таблетках не повышалась, нормализовались лабораторные показатели: повысились концентрация гемоглобина (до 140 г/л), число эритроцитов (до 6х1012/л), содержание С4-компонента комплемента, снизились концентрации антинуклеарного фактора (до 1,4 Ед/л), антител к двуспиральной ДНК (до 50 МЕд/мл), ^ к кардиолипинам (до 60 ед/мл) (см. табл).
За время наблюдения серьезных нежелательных инфекционных явлений не наблюдалось, однако 3 раза в течение 2012 г. проводилась заместительная терапия иммуноглобулином человеческим нормальным в связи со снижением концентрации ^М в сыворотке крови (см. табл).
Необходимо отметить, что число С020+ В лимфоцитов перед терапией ритуксимабом было снижено до 5% ^ 6-23%), до 93 клеток в 1 мкл ^ 260-1500), в последующих исследованиях наблюдалась деплеция, единичные В клетки в препарате, что, по-видимому, было причиной гипогаммаглобулинемии.
Таким образом, данный клинический случай демонстрирует высокую эффективность терапии ритуксима-бом у пациентки с тяжелым рефрактерным течением СКВ. Благодаря назначению моноклональных антител к С020 В лимфоцитов удалось купировать жизнеугрожающие клинические проявления заболевания (геморрагический синдром, гемолитическую анемию, антифос-фолипидный синдром), а также значительно снизить продукцию аутоантител и избежать назначения циклофосфамида и повышения дозы глюкокортикоидов, что
Таблица. Динамика клинико-лабораторных показателей у пациентки на фоне терапии ритуксимабом
Параметр Сентябрь 2011 Январь 2012 Май 2012 Сентябрь 2012
Оценка активности по шкале SELENA SLEDAY 6 2 4 2
Концентрация гемоглобина, г/л 94 120 140 140
12 Число эритроцитов, Х10 /л 3,4 5,2 5,5 6,0
Антинуклеарный фактор, Ед/л (N до 1,5) > 12 2,7 4,4 1,4
Антитела к двуспиральной ДНК, МЕд/мл, (N до 20) > 250 63,4 120 50
IgG-антитела к кардиолипинам, Ед/мл, (N до 20) 226 72,3 100 60
С4-компонент комплемента, г/л, (N 0,14-0,47) 0 0,19 0,06 0,18
Иммуноглобулин M, г/л, (N 0,35-2,39) 0,31 0,02 0,05 0,22
CD20 В лимфоциты, число в 1 мкл (N 260-1500) 93 0 2 0
Читайте также:


