Гамэвак вакцина векторная против лихорадки эбола
Показания к применению
Препарат предназначен для профилактики лихорадки Эбола у взрослых, не менее чем за 28 дней до предполагаемого контакта с возбудителем, иммунитет сохраняется в течение 21 дня после второй вакцинации ГамЭваком.
Действующее вещество, группа
Лекарственная форма
Раствор для внутримышечного введения
Вакцинация спасет от смертельной болезни. Ежегодно более чем в 100 странах происходят тысячи случаев заболеваний бешенством. Чуть меньше половины из них – дети. Подробнее.
Противопоказания
ГамЭвак не назначают при гиперчувствительности к какому-либо компоненту вакцины или аллергической реакции, наблюдавшейся при предыдущем введении вакцины.
Вакцинация не проводится при наличии клинических проявлений острых инфекционных заболеваний и обострений хронических инфекционных заболеваний, сопровождающихся лихорадкой, при острых аллергических состояниях.
С осторожностью назначают Вакцину ГамЭвак: при хронических заболеваниях печени и почек, выраженных нарушениях функции щитовидной железы и других заболеваний эндокринной системы (сахарный диабет), тяжелых заболеваниях системы кроветворения, эпилепсии и других заболеваний ЦНС, инфаркт миокарда в анамнезе, миокардиты, эндокардиты, перикардиты, ишемическая болезнь сердца.
Применение в период при беременности и в период грудного вскармливания: не изучено, клинических исследований не проводилось.
Как применять: дозировка и курс лечения
Вакцина ГамЭвак предназначена только для внутримышечного введения. Строго запрещено внутривенное введение препарата. ГамЭвак вводят в дельтовидную мышцу (верхнюю треть наружной поверхности плеча) в дозировке 0,5 мл, при невозможности - в любую другую мышцу. Вакцинацию проводят с соблюдением правил асептики: перед вскрытием ампулы рекомендуется обработать крышку флакона 70% этиловым спиртом, также спиртом обрабатывают место инъекции. Хранение вскрытого флакона не допускается. Для вакцинации используют одноразовые шприцы.
В день проведения вакцинации пациент должен быть осмотрен врачом. Обязательным является общий осмотр и измерение температуры тела, в случае, если температура превышает 37 градусов Цельсия, вакцинацию не проводят.
Вакцинацию ГамЭваком проводят в два этапа с промежутком три недели.
В местах, где проводится вакцинация, должны быть средства противошоковой терапии (в соответствии с Приказом М3 СР РФ от 04.092006 N 626 'Об утверждении стандарта медицинской помощи больным анафилактическим шоком неуточненным'). После введения вакцины пациент должен находиться под наблюдением медицинских работников в течение 30 минут.
Вакцина ГамЭвак не пригодна к применению: во флаконах с нарушенной целостностью и маркировкой, при изменении физических свойств (мутность, интенсивное окрашивание, наличие хлопьев), при истекшем сроке годности, неправильном хранении.
Фармакологическое действие
Препарат представляет собой вакцину, способствующую формированию высокого специфического иммунитета против лихорадки Эбола. После проведения вакцинации эффект развивается в течение 28 дней. У 100% пациентов после вакцинации определяются титры антител к вирусу Эбола. Длительность сохранения иммунитета изучена в течение 3 недель после второй вакцинации.
Вакцина получена биотехнологическим методом, при котором не используется патогенный для человека вирус лихорадки Эбола. Основой вакцины являются рекомбинантные векторы, в которые встроен только один отдельный ген гликопротеина GP вируса лихорадки Эбола. При введении вакцины в организм (внутримышечная инъекция) векторы приникают в клетки организма и происходит экспрессия белка GP вируса лихорадки Эбола, в результате чего происходит формирование высокого уровня специфического иммунитета против лихорадки Эбола. Таким образом, 'живой' или инактивированный вирус лихорадки Эбола при получении вакцины не используется и в состав вакцины не входит.
Побочные действия
У части вакцинированных ГамЭваком в первые двое-трое суток после вакцинации могут развиться кратковременные общие (непродолжительный гриппоподобный синдром, характеризующийся ознобом, повышением температуры тела, артралгией, миалгией, астений, общим недомоганием, головной болью) и местные (болезненность в месте инъекции, гиперемия, отечность) реакции. Реже могут наблюдаться тошнота, снижение аппетита, увеличение регионарных лимфоузлов. Возможно развитие аллергических реакций у некоторых пациентов. Возможно кратковременное (7 дней) повышение уровня печеночных трансаминаз, креатинина и креатинфосфокиназы в сыворотке крови.
Большинство нежелательных явлений имели легкую или среднюю степень тяжести, обычно развивались в 1 -2 сутки после вакцинации и разрешались в течение 3 последующих дней.
Ниже приведены сведения о частоте встречаемости местных и общих поствакцинальных реакций (с указанием диапазона, соответствующего показателям, полученных в рамках настоящего исследования):
- как 'Очень частые - 1/10 назначений (> 10%)' могут быть выделены следующие нежелательные явления: болезненность в месте инъекции, гипертермия, головная боль, гиперемия в месте инъекции; транзиторное повышение уровня креатининфосфокиназы, АЛТ в сыворотке крови.
Повышение температуры тела было зарегистрировано у 26, 38% провакцинированных; при этом фебрильная лихорадка (выше 38,ОС) - отмечалась у 2,78%% провакцинированных, высокофебрильная (выше 39,ОС) - у 1, 38%.
При этом в 2, 78% случаев для купирования гипертеримического синдрома требовалось применение жаропонижающих лекарственных средств.
Действующее вещество:
Инструкция по медицинскому применению
ГамЭвак-Комби Комбинированная векторная вакцина против лихорадки Эбола
Инструкция по медицинскому применению - РУ № ЛП-003390
Дата последнего изменения: 10.03.2017
Раствор для внутримышечного введения
Компонент А содержит:
Активное вещество: рекомбинантные частицы на основе вируса везикулярного стоматита, экспрессирующие ген GP вируса Эбола в дозе (2,5±1,5)х10 7 акт.ед. в 0,5 мл буферного раствора.
Вспомогательные вещества : трис(гидроксиметил)аминометан - 0,605 мг, ЭДТА динатриевая соль - 0,168 мг, сахароза - 50,0 мг, вода для инъекций до 0,5 мл.
Компонент Б содержит:
Активное вещество: рекомбинантные псевдоаденовирусные частицы, экспрессирующие ген GP вируса Эбола (2,5±1,25)х10¹¹ частиц в 0,5 мл буферного раствора. Количество активных рекомбинантных псевдоаденовирусных частиц, экспрессирующих ген GP вируса Эбола, - (4,5±2,5)х10 8 акт.ед./дозу.
Вспомогательные вещества: трис(гидроксиметил)аминометан -1,211 мг, натрия хлорид - 4,38 мг, сахароза - 25,0 мг, полисорбат-80 - 0,0005 мл, магния хлорида гексагидрат - 0,203 мг, этанол 95 % - 0,005 мл, ЭДТА динатриевая соль - 0,0373 мг, вода для инъекций до 0,5 мл.
По внешнему виду вакцина представляет собой столбик замороженной гомогенной жидкости с горизонтальным мениском, при оттаивании - однородный бесцветный или с желтоватым оттенком слегка опалесцирующий раствор.
вакцина индуцирует формирование гуморального и клеточного иммунитета против геморрагической лихорадки Эбола, обеспечивает защитный уровень специфических антител.
Эффективность препарата обусловлена входящими в него компонентами.
Препарат представляет собой вакцину, способствующую формированию высокого специфического иммунитета против лихорадки Эбола. После проведения вакцинации эффект развивается в течение 28 дней. У 100% пациентов после вакцинации определяются титры антител к вирусу Эбола. Длительность сохранения иммунитета изучена в течение 3 недель после вакцинации компонентом Б.
Профилактика лихорадки Эбола у взрослых, не менее чем за 28 дней до предполагаемого контакта с возбудителем, Длительность сохранения иммунитета изучена в течение 3 недель после вакцинации компонентом Б.
Препарат не назначают при гиперчувствительности к какому-либо компоненту вакцины или аллергической реакции, наблюдавшейся при предыдущем введении вакцины.
Вакцинация не проводится при наличии клинических проявлений острых инфекционных заболеваний и обострений хронических инфекционных заболеваний, сопровождающихся лихорадкой, при острых аллергических состояниях.
С осторожностью: при хронических заболеваниях печени и почек, выраженных нарушениях функции щитовидной железы и других заболеваний эндокринной системы (сахарный диабет), тяжелых заболеваниях системы кроветворения, эпилепсии и других заболеваний ЦНС, инфаркт миокарда в анамнезе, миокардиты, эндокардиты, перикардиты, ишемическая болезнь сердца.
Не изучено, клинических исследований не проводилось.
Вакцина предназначена только для внутримышечного введения. Строго запрещено внутривенное введение препарата. Вакцину вводят в дельтовидную мышцу (верхнюю треть наружной поверхности плеча) в дозировке 0,5 мл, при невозможности - в любую другую мышцу. Вакцинацию проводят с соблюдением правил асептики: перед вскрытием ампулы рекомендуется обработать крышку флакона 70% этиловым спиртом, также спиртом обрабатывают место инъекции. Хранение вскрытого флакона не допускается. Для вакцинации используют одноразовые шприцы.
В день проведения вакцинации пациент должен быть осмотрен врачом: обязательным является общий осмотр и измерение температуры тела, в случае, если температура превышает 37 градусов Цельсия, вакцинацию не проводят.
Вакцинацию проводят в два этапа: вначале компонентом А, затем через 3 недели компонентом Б.
Не пригоден к применению препарат во флаконах с нарушенной целостностью и маркировкой, при изменении физических свойств (мутность, интенсивное окрашивание, наличие хлопьев), при истекшем сроке годности, неправильном хранении.
Представленный ниже профиль безопасности основан на данных, полученных в ходе клинических исследований.
У части вакцинированных в первые двое-трое суток после вакцинации могут развиться кратковременные общие (непродолжительный гриппоподобный синдром, характеризующийся ознобом, повышением температуры тела, артралгией, миалгией, астений, общим недомоганием, головной болью) и местные (болезненность в месте инъекции, гиперемия, отечность) реакции. Реже могут наблюдаться тошнота, диспепсия, снижение аппетита, увеличение регионарных лимфоузлов. Возможно развитие аллергических реакций у некоторых пациентов, возможно кратковременное (7 дней) повышение уровня печеночных трансаминаз, креатинина и креатинфосфокиназы в сыворотке крови.
Большинство нежелательных явлений имели легкую или среднюю степень тяжести, обычно развивались в 1-2 сутки после вакцинации и разрешались в течение 3 последующих дней.
Ниже приведены сведения о частоте встречаемости местных и общих поствакцинальных реакций (с указанием диапазона, соответствующего показателям, полученных в рамках настоящего исследования):
Повышение температуры тела было зарегистрировано у 38,1% провакцинированных; при этом фебрильная лихорадка (выше 38, ºС) - отмечалась у 3,57% провакцинированных. *При этом в 7,14% случаев для купирования гипертермического синдрома требовалось применение жаропонижающих лекарственных средств.
-
как «Частые - 1/100 назначений (e1%, но
Лекарственная форма
раствор для внутримышечного введения
Состав
1 флакон (0,5 мл) содержит:
Активное вещество: смесь (1:1) рекомбинантных псевдоаденовирусных частиц, экспрессирующих ген GP вируса лихорадки Эбола, и рекомбинантных псевдоаденовирусных частиц, экспрессирующих ген NP вируса лихорадки Эбола, в суммарном количестве (2,5 ± 1,25) × 10 11 частиц в 0,5 мл буферного раствора.
Количество активных рекомбинантных псевдоаденовирусных частиц, экспрессирующих ген GP вируса Эбола, — (2,5 ± 1,5) × 10 8 акт.ед./дозу; количество активных рекомбинантных псевдоаденовирусных частиц, экспрессирующих ген NP вируса Эбола, — (2,5 ± 1,5) × 10 8 акт.ед./дозу. (Количество активных рекомбинантных псевдоаденовирусных частиц определяют в монополуфабрикатах препарата до добавления буферного раствора).
Вспомогательные вещества: трис(гидроксиметил)аминометан — 1,211 мг, натрия хлорид — 4,38 мг, сахароза — 25,0 мг, полисорбат-80 — 0,0005 мл, магния хлорида гексагидрат — 0,203 мг, этанол 95 % — 0,005 мл, ЭДТА динатриевая соль — 0,0373 мг, вода для инъекций до 0,5 мл.
В состав вакцины входит один препарат 0,5 мл (1 доза).
Описание
Бесцветный, слегка опалесцирующий раствор.
По внешнему виду вакцина представляет собой столбик замороженной гомогенной жидкости с горизонтальным мениском, при оттаивании — однородный бесцветный или с желтоватым оттенком слегка опалесцирующий раствор.
Вакцина получена биотехнологическим методом, при котором не используется патогенный для человека вирус лихорадки Эбола.
Основой вакцины являются рекомбинантные векторы, в которые встроен только один отдельный ген гликопротеина GP вируса лихорадки Эбола.
Фармакологические свойства
Эффективность препарата обусловлена входящими в него компонентами.
Препарат представляет собой вакцину, способствующую формированию высокого специфического иммунитета против лихорадки Эбола. После проведения вакцинации эффект развивается в течение 28 дней. У 100 % пациентов после вакцинации определяются титры антител к вирусу Эбола. Длительность сохранения иммунитета изучена в течение 3 недель после второй вакцинации.
Показания
Профилактика лихорадки Эбола у взрослых, не менее чем за 28 дней до предполагаемого контакта с возбудителем, иммунитет сохраняется в течение 21 дня после второй вакцинации.
Противопоказания
Препарат не назначают при гиперчувствительности к какому-либо компоненту вакцины или аллергической реакции, наблюдавшейся при предыдущем введении вакцины.
Вакцинация не проводится при наличии клинических проявлений острых инфекционных заболеваний и обострений хронических инфекционных заболеваний, сопровождающихся лихорадкой, при острых аллергических состояниях.
С осторожностью
При хронических заболеваниях печени и почек, выраженных нарушениях функции щитовидной железы и других заболеваний эндокринной системы (сахарный диабет), тяжёлых заболеваниях системы кроветворения, эпилепсии и других заболеваний ЦНС, инфаркт миокарда в анамнезе, миокардиты, эндокардиты, перикардиты, ишемическая болезнь сердца.
Применение при беременности и лактации
Не изучено, клинических исследований не проводилось.
Способ применения и дозы
Вакцина предназначена только для внутримышечного введения.
Строго запрещено внутривенное введение препарата.
Вакцину вводят в дельтовидную мышцу (верхнюю треть наружной поверхности плеча) в дозировке 0,5 мл, при невозможности — в любую другую мышцу.
Вакцинацию проводят с соблюдением правил асептики: перед вскрытием ампулы рекомендуется обработать крышку флакона 70 % этиловым спиртом, также спиртом обрабатывают место инъекции. Хранение вскрытого флакона не допускается. Для вакцинации используют одноразовые шприцы.
В день проведения вакцинации пациент должен быть осмотрен врачом. Обязательным является общий осмотр и измерение температуры тела, в случае, если температура превышает 37 градусов Цельсия, вакцинацию не проводят.
Вакцинацию проводят в два этапа с промежутком три недели.
Не пригоден к применению препарат во флаконах с нарушенной целостностью и маркировкой, при изменении физических свойств (мутность, интенсивное окрашивание, наличие хлопьев), при истекшем сроке годности, неправильном хранении.
Побочные эффекты
Представленный ниже профиль безопасности основан на данных, полученных в ходе клинических исследований.
У части вакцинированных в первые двое-трое суток после вакцинации могут развиться кратковременные общие (непродолжительный гриппоподобный синдром, характеризующийся ознобом, повышением температуры тела, артралгией, миалгией, астений, общим недомоганием, головной болью) и местные (болезненность в месте инъекции, гиперемия, отёчность) реакции.
Реже могут наблюдаться тошнота, снижение аппетита, увеличение регионарных лимфоузлов.
Возможно развитие аллергических реакций у некоторых пациентов.
Возможно кратковременное (7 дней) повышение уровня печёночных трансаминаз, креатинина и креатинфосфокиназы в сыворотке крови.
Большинство нежелательных явлений имели лёгкую или среднюю степень тяжести, обычно развивались в 1–2 сутки после вакцинации и разрешались в течение 3 последующих дней.
Ниже приведены сведения о частоте встречаемости местных и общих поствакцинальных реакций (с указанием диапазона, соответствующего показателям, полученных в рамках настоящего исследования):
Повышение температуры тела было зарегистрировано у 26,38 % провакцинированных; при этом фебрильная лихорадка (выше 38,0 °C) — отмечалась у 2,78 % провакцинированных, высокофебрильная (выше 39,0 °C) — у 1,38 %.
При этом в 2,78 % случаев для купирования гипертеримического синдрома требовалось применение жаропонижающих лекарственных средств.
-
как «Частые — 1/100 назначений (≥1 %, но
По данным Минздрава Демократической Республики Конго, на начало декабря этого года в стране зарегистрировано 3201 подтвержденных случаев заболевания лихорадкой Эбола, 2209 заболевших умерли.
Сергей Нетёсов, доктор биологических наук, профессор, заведующий лабораторией биотехнологии и вирусологии факультета естественных наук Новосибирского государственного университета, член-корреспондент РАН
Африканский вирус оказался более актуальным, чем российские
Возбудитель лихорадки — вирус Эбола — впервые был обнаружен в 1976 году во время вспышки болезни в районе реки Эбола, протекающей между тогдашним Заиром (ныне Демократическая Республика Конго) и Суданом.
Если рассмотреть хронику создания вакцины против вируса Эбола и современное состояние дел в этой области в мире и в России, то становится понятным, как это поможет всем нам.
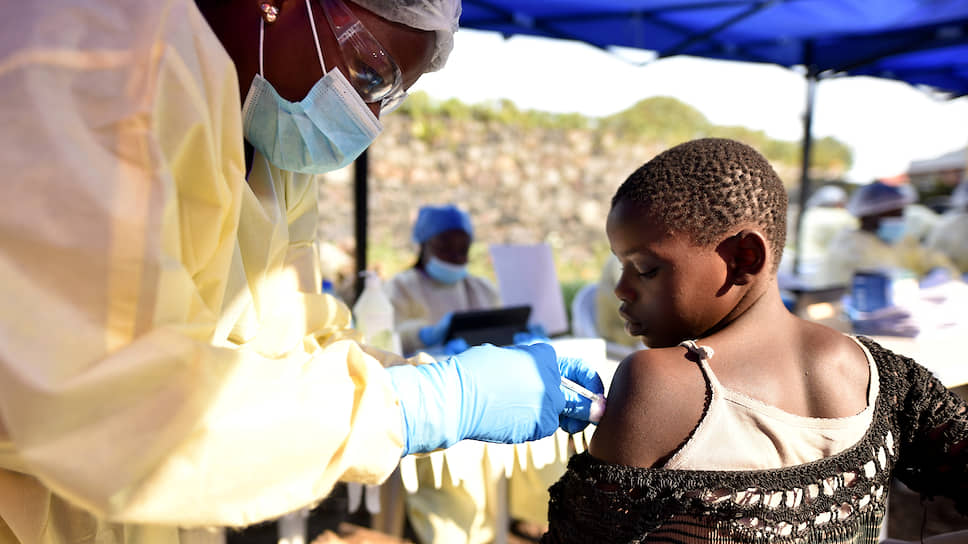
Вирус Эбола был впервые идентифицирован в 1976 году во время крупной вспышки вызванного им заболевания в Судане и тогдашнем Заире (теперь Демократическая Республика Конго; ДРК). Поскольку такие вспышки позднее случались не каждый год и их охват в несколько последующих лет был намного меньше, то ученые ограничились в те времена лишь разработкой иммуноферментных диагностикумов на ее маркеры.
Правда, основные фундаментальные исследования были проведены, в том числе секвенирование генома этого возбудителя, причем российские ученые здесь были одними из первых, включая вашего покорного слугу.
В 1990-е, а особенно в 2000-е годы масштаб и число вспышек заметно увеличились, и некоторые лаборатории в США и Канаде начали разработки и вакцинных препаратов, и средств лечения, а также диагностикумов нового типа на основе полимеразной цепной реакции. Однако для проведения полного цикла доклинических испытаний вакцинных препаратов необходимы весьма значительные средства, а с учетом особой опасности этой инфекции значительную часть таких работ необходимо проводить в лабораториях высшего, четвертого уровня биобезопасности. Ввиду этих причин полного цикла доклинических исследований перспективных, кандидатных, как говорят специалисты, вакцин против Эбола-вирусной инфекции до 2014 года так и не было завершено ни в одной из лабораторий мира.
По самым последним данным, природным резервуаром вируса Эбола вернее всего являются фруктоядные летучие мыши. Три вида таких мышей (Hypsignathus monstrosus, Epomops franqueti и Myonycteris torquata) могут быть носителями вируса без признаков заболевания. Из 24 видов растений и 19 видов позвоночных, экспериментально зараженных вирусом Эбола, удалось заразить только летучих мышей. Причем они не заболели, а просто несли в себе вирус в течение долгого времени. В обследовании в 2002–2003 годах 1030 животных, включая 679 летучих мышей из Габона и Республики Конго, только 13 фруктоядных мышей несли этот вирус. Кроме того, фрагменты вируса Эбола выделяли из тканей некоторых умерших западноафриканских равнинных горилл и центральноафриканских шимпанзе, которые иногда питаются фруктоядными летучими мышами. Что еще более важно, фрагменты РНК вируса Эбола были выявлены у клинически здоровых летучих мышей разных видов. Это означало, что летучие мыши могут быть носителями вируса без признаков заболевания, то есть хроническими носителями. А это и есть главное условие поддержания циркуляции вируса Эбола в природе.
Неожиданная по размаху, месту возникновения и продолжительности вспышка этого заболевания 2014 года в Гвинее, Сьерра-Леоне и Либерии сдвинула ситуацию с места. И уже в конце 2015 года несколько лабораторий и научно-исследовательских институтов в США, Канаде и некоторых других странах объявили о завершении доклинических испытаний нескольких кандидатных, вакцинных препаратов.
О создании прототипной вакцины объявили и у нас в России. Первыми были публикации группы ученых из НИИ эпидемиологии и микробиологии им. Н. Ф. Гамалеи Министерства здравоохранения России о разработке живой вакцины на основе рекомбинантного аденовируса. Однако к этому времени и сама вспышка закончилась, так что испытывать эти вакцины в полевых условиях реальной эпидемии стало негде.
В том же 2018 году, и опять неожиданно, началась вспышка Эбола-вирусной инфекции в ДРК. Как оказалось, один из вакцинных препаратов, разработанный на основе рекомбинантного живого вируса везикулярного стоматита, прошел к этому времени ограниченные клинические испытания в США.
От человека к человеку вирус передается при попадании вируссодержащих жидкостей от больных людей или инфицированных животных на слизистые оболочки или на микротравмы на коже. У больных и умерших концентрация этого вируса в крови и на слизистых оболочках необычайно велика и достигает 10 млн вирусных частиц на 1 мл. Поэтому близкое общение с больным с большой вероятностью приводит к заражению. Наконец, уже выздоровевший человек может нести в себе вирус (в семени мужчин, в грудном молоке женщин) до одного года после выздоровления.
Фото: Артем Геодакян / ТАСС
Производит сейчас этот препарат под названием Ervebo всемирно известный фармгигант MSD (Merck, Sharp and Dohme). Вследствие этого Всемирная организация здравоохранения совместно с правительством ДРК приняли решение о начале клинических испытаний данной вакцины прямо в очаге инфекции.
В настоящее время выявлено пять таксономических видов вируса Эбола, которые отличаются друг от друга процентом летальности. Штаммы вида Заир, которые и циркулируют сейчас в Демократической Республике Конго, самые опасные — со смертностью до 80%.
К настоящему времени, по данным сайта promedmail.org, этой вакциной привито уже более 250 тыс. человек из числа контактных лиц. По имеющимся данным, ни один из вакцинированных не заболел. Однако вспышку пока остановить не удалось, поскольку она развивается в зоне военного межплеменного конфликта, и даже просто находиться там опасно: были случаи убийств местных и иностранных врачей, да и противодействие вакцинации части населения тоже имеет место.
Между тем американская же компания Johnson & Johnson довела до клинических испытаний другую, двухкомпонентную вакцину на основе рекомбинантных аденовируса и вируса осповакцины, производящих при инъекции в организм антигенно значимые белки вируса Эбола. И в середине ноября эта вакцина также была разрешена ВОЗ для проведения полевых испытаний в ДРК, которые в ноябре же и начались.
В России за последнее десятилетие не было ни одного больного эболавирусной инфекцией. В то же время за эти же годы у нас в стране были десятки тысяч больных другими, домашними вирусными инфекциями (ветряная оспа, ротавирус, респираторно-синцитиальный вирус, метапневмовирус, вирусы парагриппа и другие) и сотни умерших от них.
Может, пора вспомнить про эти патогены и начать, наконец, разработки и производство вакцин против них, гораздо более актуальных для России инфекций?
Новая вспышка вируса Эбола в мае 2018 года всколыхнула международное сообщество. Позволят ли новые лекарства победить вирус и не допустить его попадания в США, Великобританию, Россию и другие развитые страны?
Восьмого мая Минздрав Демократической Республики Конго (ДРК) объявил об очередной вспышке инфекции. Для предотвращения масштабного распространения болезни власти страны и международные организации быстро отреагировали, в частности применив новые препараты. Эпидемия 2014-2016 годов в Западной Африке поразила 28 639 человек, из которых 11 316 скончались — на порядок больше, чем за десятки лет с момента открытия вируса.
Увы, у мира нет гарантий того, что заражение подобного масштаба не повторится. Даже с учетом того, что современные технологии позволили разработать вакцины за прошедшее время. По словам президента Resolve to Save Lives и бывшего руководителя Центров США по контролю и профилактике заболеваний CDC Томаса Фрайдена, вирус может добраться до любого крупного города Земли меньше чем за 36 часов, и пока есть угроза заражения хоть в какой-то стране, все мы в опасности. Пока столицы ДРК и девяти близлежащих стран, согласно данным ВОЗ, находятся в зоне высокого риска заражения.
История вирусной лихорадки Эбола
Заражение Эболой протекает крайне мучительно. Первые симптомы неспецифичны и неочевидны, их можно спутать с гриппом или простудой. С развитием болезни пациента лихорадит, появляется рвота, сыпь, диарея и боли в животе. Затем отказывают внутренние органы, и в некоторых случаях начинаются внутренние и внешние кровотечения. До конца неясно, как вирус воздействует на иммунную систему человека. Смертность может достигать 90%.
Поддерживающая терапия способствует выживанию пациентов. В Демократической Республике Конго начали использовать вакцину rVSV-ZEBOV компании Merck, находящуюся на стадии клинических исследований, и несколько экспериментальных препаратов.
Вакцинация в действии
Доброволец получает вакцину в рамках одного из исследований PREVAC, 2017. Источник: NIAID
В Конго направлено более 7500 доз вакцины rVSV-ZEBOV, и медицинские работники уже активно приступили к их использованию. Фармкомпания передала препараты бесплатно, а средства в размере $1 млн на расходы по распространению и на сам процесс вакцинации предоставил Глобальный альянс по вакцинам и иммунизации (GAVI — Global Alliance for Vaccines and Immunisation). Финансовая поддержка также была передана от британских Wellcome Trust и Министерства международного развития DFID.
Вакцина Merck — не панацея
Merck приобрел права на доработку и распространение вакцины rVSV-ZEBOV у небольшой компании-разработчика New Link Genetics, которые, в свою очередь, изначально получили их у Агентства общественного здравоохранения Канады. Общая сумма инвестиций американского правительства в разработку препарата уже превысила $100 млн, которые были потрачены как на создание условий для производства вакцины, так и на проведение клинических исследований.
Тем не менее формально rVSV-ZEBOV остается экспериментальной: сейчас она проходит процедуру регуляторного одобрения, а это длительный бюрократический процесс. Ожидается, что заявка на разрешение рыночного распространения от Управления по санитарному надзору за качеством пищевых продуктов и медикаментов США будет подана не раньше 2019 года.
В случае успеха в разработке данной вакцины Merck может получить ваучер на ускоренное рассмотрение FDA инновационных препаратов в будущем. Такие ваучеры выпускаются на инновационные препараты, нацеленные на редкие или игнорируемые заболевания для стимулирования разработок по этим направлениям. Перепродажи подобных ваучеров в прошлом приносили до $350 млн.
Для вакцинации людей отбирают по кольцевой схеме, то есть прививают всех, с кем контактировал заразившийся пациент. А также тех, с кем общались контактировавшие с инфицированным. Конечно, это не идеальный метод, но лучшего в мире еще не придумали. Есть и другие трудности: условия хранения вакцины не всегда легко соблюсти. rVSV-ZEBOV необходимо хранить при температуре между −60 °C и −80 °C. Электроснабжение в стране не очень надежно, а препарат надо доставить в далекие от больших городов поселки. Кроме того, поскольку вакцина официально еще не одобрена, каждому пациенту нужно подписать информированное согласие на получение препарата.
В поисках альтернативных препаратов
Ни для одного из этих лекарств не удалось доказать снижения риска смерти от Эболы, но не потому, что они плохие или опасные. Причина в том, эффективность нужно показать в клинических исследованиях на большом количестве людей, а исследователи не успели набрать нужного числа добровольцев за время предыдущей вспышки вируса.
Мораль или деньги
Вирусные болезни — по-прежнему нерешенная проблема. Согласно данным Reuters, за последние 60 лет количество новых вирусных заболеваний, атакующих человека, выросло в четыре раза, а ежегодных вспышек стало больше в три раза.
Неудивительно, что эти болезни привлекают большое внимание фармкомпаний. В частности, вакцины против Эболы разрабатывали параллельно с Merck еще два гиганта: GlaxoSmithKline и Johnson & Johnson (J&J). Можно ли сказать, что Merck выиграл эту гонку?
Reuters отмечает, что в отсутствие реальной перспективы окупить вложения компании сомневаются, оправданы ли инвестиции в разработку даже с учетом поддержки правительственных и благотворительных организаций. Так, компания GSK приобрела в 2013 году разработчика вакцины cAd3-EBOV — биотехнологическую компанию Okairos — за €250 млн. В одном из исследований, проводимом PREVAIL (Partnership for Research on Ebola Virus in Liberia), сравнивали продукты Merck и GSK. Оба продукта показали свою эффективность, но rVSV-ZEBOV все же обгонял Ad3-EBOZ по доле пациентов, сохранявших иммунный ответ после вакцинации в течение года. В итоге разработка вакцины GSK сейчас приостановлена.
J&J также активно занимается разработками. Обнадеживающие результаты исследований в людях опубликованы в JAMA в 2016 и 2017 годах. Компоненты вакцины созданы Janssen, фармкомпанией J&J и Bavarian Nordic. BARDA (Biomedical Advanced Research and Development Authority) финансово поддержала Janssen на сумму около $90 млн. Инициатива по инновационным лекарственным средствам (IMI) при поддержке Европейской комиссии предоставила финансирование в размере более €100 млн.
Предполагается, что действие вакцины J&J будет иным, чем у rVSV-ZEBOV. Если вакцина Merck подходит для быстрой кольцевой вакцинации — для людей, которые контактировали с Эболой, то вакцина J&J нацелена скорее на медицинских работников, которым нужна продолжительная защита от вируса: иммунитет вырабатывается, по-видимому, медленнее, но и защитный эффект может длиться 10 лет. У вакцины уже подтверждены безопасность и способность вызывать иммунный ответ. В сентябре 2016 года компания подала заявку на EUAL — Emergency Use Assessment and Listing в ВОЗ, которая сейчас находится на рассмотрении.
Помимо трех фармгигантов, другие компании тоже занимаются разработкой вакцин от Эболы. Например, Novavax также объявляла о запуске клинических исследований своей вакцины в людях — их продукт основан на наночастицах, что компания считает преимуществом перед векторными вакцинами.
Российские разработки
Исследователи из России и Китая даже успели получить лицензии местных регуляторных органов на свои разработки. По данным Reuters, в обеих странах результаты получены на основе ограниченных клинических данных.
Сразу после получения лицензии в адрес российских вакцин поступило немало критики. В частности, заявлялось, что не было проведено исследования на большой выборке людей, чего требует третья (последняя) стадия клинических исследований, а результаты не опубликованы в научных международных журналах. На фоне вышеописанных открытых исследований крупных фармкомпаний действительно логично бы увидеть больше информации о проверках отечественных разработок.
В текущих пострегистрационных клинических исследованиях планируется провести вакцинацию 2000 добровольцев в Гвинее, что не очень масштабно по сравнению с проведенными клиническими исследованиями западных компаний до одобрения препарата (например, в проверке вакцины Merck суммарно участвовало почти 12 000 человек). Итоги проверки планируется получить к концу 2018 года.
Мрачное предсказание Билла Гейтса
Благодаря действиям Минздрава Демократической Республики Конго и международных организаций вспышка лихорадки Эбола не распространилась по всей стране и остается локализованной в нескольких зонах. Согласно официальному заявлению ВОЗ от 18 мая, есть все причины ожидать, что эпидемию удастся удержать под контролем.
Многие мировые деятели бьют тревогу: человечеству следует озаботиться не только борьбой с Эболой, но с вирусными инфекциями в целом. В последние десятилетия заболеваемость вирусами только растет. Среди приоритетных исследований для ВОЗ, например, разработки по вирусу Зика и вирусам, вызывающим ближневосточный респираторный синдром и Конго-Крымскую геморрагическую лихорадку.
Необходимо стимулировать крупные фармкомпании на разработку препаратов против редких болезней, поскольку в современном мире только гиганты фармбизнеса обладают возможностью разработки и производства вакцин в нужном масштабе.
Читайте также:


