Вирус простого герпеса эпидемиология
ГЕРПЕС (herpes; греч, herpo ползти) — вирусные болезни, морфологически характеризующиеся высыпанием на коже, слизистых оболочках сгруппированных пузырьков на гиперемированном основании.
Как самостоятельные нозол, формы различают простой герпес (herpes simplex) — наиболее распространенную и наиболее изученную инфекцию и опоясывающий герпес (herpes zoster).
Содержание
Простой герпес
(син. пузырьковый лишай)
Болезнь вызывается вирусом простого Г. (herpes simplex virus), относящимся к группе ДНК-содержащих вирусов и имеющим широкое распространение. Впервые инфекционный характер простого Г. установил Грютер (W. Griiter, 1912), вызвав эту болезнь у кролика введением патол, материала от больного человека; в пораженных вирусом тканях Липшютц (В. Lipschutz, 1921) обнаружил ацидофильные включения, а Каудри (E. Cowdry, 1934) определил их как тельца включения вируса Г. (см. Герпеса вирусы).
Большинство исследователей подразделяет вирус простого Г. на два типа. Штаммам первого типа отводится роль возбудителя негенитальных поражений; штаммы второго типа, по их мнению, вызывают преимущественно генитальный Г.
. Источником инфекции служит больной человек и вирусоносители. Вирус передается гл. обр. контактным путем. Наибольшее количество заболеваний наблюдается в холодные месяцы, но эпидемий не наблюдается за исключением небольших вспышек в дошкольных учреждениях, школах, больницах. Вирусные болезни кожи у детей весьма распространены, в т. ч. герпес.
Первичное заражение в большинстве случаев происходит в раннем детстве, причем заражение может происходить внутриутробно, в момент родов и в первые дни жизни ребенка; пассивные противовирусные антитела, транспортированные с кровью матери, обычно предупреждают развитие болезни, однако в некоторых случаях возможно развитие Г. у новорожденного. К первому году жизни пассивный иммунитет ослабевает и при провоцирующих условиях вирус активизируется. Попав в организм, вирус простого Г. размножается в тканях экто- и эндодермального происхождения, поражая кожу, слизистые оболочки, роговицу, а при генерализации процесса — иногда печень, мозг и другие органы, сохраняясь в организме на протяжении всей жизни (так наз. хрон, носительство вируса Г.). Клин, проявления болезни и ее рецидивы возникают под влиянием провоцирующих и раздражающих факторов (переохлаждение, травма, напр, удаление зуба, ультрафиолетовые облучения и др.), на фоне ослабления клеточного, гуморального иммунитета. Болезнь возникает как самостоятельная или сопутствует нек-рым инфекционным болезням (крупозной пневмонии, малярии, гриппу, менингококковой инфекции и др.).
Активацию вируса и возникновение рецидивов некоторые авторы объясняют реакцией организма на охлаждение, переутомление и другие явления; при этой происходит увеличенная секреция глюкокортикоидных гормонов, под действием которых интенсифицируется ферментативное расщепление внутриядерных колоний вируса и происходит его активация.
Патогистология: наблюдается так наз. баллонирующая дегенерация эпителия Унны, выражающаяся очаговым изменением клеток шиповидного слоя, которые округляются, увеличиваются в размере и, приобретая вид шаров, отъединяются одна от другой; одновременно в результате амитотического деления образуются многоядерные крупные клетки. Образующийся в эпидермисе серозный экссудат разъединяет измененные клетки, образуется полость пузырька, заполненная экссудатом со взвешенными в нем эпителиальными клетками; в ядрах дегенерированных клеток отмечают ацидофильные включения. В дерме наблюдается отек сосочкового слоя, значительное расширение кровеносных и лимф, сосудов и инфильтрат, состоящий преимущественно из лимфоцитов и нейтрофилов, небольшое количество которых проникает и в полость пузырька.
В пораженных вирусом Г. тканях выявляют характерные гигантские многоядерные клетки с внутриядерными включениями; последние в ранней стадии — диффузные и базофильные, позднее они становятся плотными и эозинофильными. Отмечается выраженная дистрофия ядер и цитоплазмы клеток. В клетках пораженных тканей обнаруживают вирусные частицы. При помощи метода определения флюоресцирующих антител (см. Иммунофлюоресценция) в клетках выявлен герпетический антиген. Данные гистохим. изучения свидетельствуют об извращении обмена пораженных вирусом клеток, об утрате ими способности утилизировать, в частности гликоген.
Клиническая картина характеризуется появлением на коже группы пузырьков диам. 0,1— 0,3 см на фоне ограниченного, слегка отечного розового пятна. Содержимое пузырьков, вначале прозрачное, постепенно мутнеет. Через 3—4 дня пузырьки подсыхают с образованием рыхлых медово-желтых корочек или вскрываются, образуя ряд мелких тесно расположенных поверхностных эрозий, которые заживают также с образованием корочек. Нередко пузырьки сливаются в многокамерный плоский пузырь, по вскрытии к-рого образуется эрозия неправильного мелкофестончатого очертания. Затем корочки отпадают, эрозии эпителизируются и на 6—8-й день заживают, не оставляя каких-либо стойких изменений кожи. Иногда сроки заживления удлиняются до 1 мес. и более.
Чаще появляется один очаг, но иногда одновременно или последовательно через 1—2 дня 2—3 новых, как правило, расположенных близко друг к другу. Высыпание пузырьков сопровождается ощущением зуда, жжения, а иногда боли, общего недомогания.
Методические указания для студентов к практическому занятию № 6.
Тема: Лабораторная диагностика герпесвирусных инфекций.
Цель: Изучение лабораторной диагностики герпесвирусных инфекций.
Модуль 3. Общая и специальная вирусология.
Содержательный модуль 16. Специальная вирусология.
Тема 6:Лабораторная диагностика герпесвирусных инфекций.
Актуальность темы:
Вирус простого герпеса – одна из самых распространенных вирусных инфекций человека, характеризующаяся лихорадочным состоянием и пузырьковыми высыпаниями, которые чаще всего локализуются на коже и слизистых оболочках. Важными особенностями герпетической инфекции являются пожизненное носительство вируса и частые рецидивы болезни.
Вирусная природа простого герпеса установлена в 1912 г. У. Грютером.
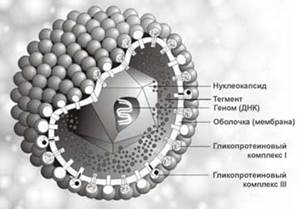
(Трёхмерное изображение вируса герпеса).
Герпесвирусы и вызываемые ими заболевания
| Типы вирусов герпеса | Вызываемые заболевания |
| ВПГ-1 (вирус простого герпеса типа 1) | Поражение: кожи, слизистой оболочки ротовой полости, конъюнктивы или роговицы глаза, энцефалиты |
| ВПГ-2 (вирус простого герпеса типа 2) | Поражение слизистых оболочек гениталий, у новорожденных - центральной нервной системы |
| ВЗВ (вирус ветрянки) | Ветряная оспа, опоясывающий лишай, постгерпетическая невралгия; язвенно-некротическая форма опоясывающего герпеса - СПИД-индикаторный признак заболевания |
| ЦМВ (цитомегаловирус) | Патологии новорожденных; осложнения после трансплантации органов и костного мозга: интерстициальная пневмония, гастроинтестинальные расстройства, гепатиты |
| ВЭБ (вирус Эпштейна-Барра) | Инфекционный мононуклеоз, лимфома Беркитта, рак носоглотки |
| ВГ-6 | Вирус, вызывающий фатальные интерстициальные пневмонии и инфекционные розеолы новорожденных |
| ВГ-7 | Вирус, выделенный от больных с синдромом хронической усталости |
| ВГ-8 | Вирус, выделенный из биоптата больного саркомой Капоши, ассоциированный с лимфопролиферативными заболеваниями |
| Примечание. ВГ - вирус герпеса. |
Таксономия, морфология, химический состав. Возбудитель простого герпеса - ДНК-содержащий вирус, относится к семейству Herpesviridae, роду Simplexvirus. По морфологии и химическому составу не отличается от вирусов ветряной оспы и опоясывающего герпеса.

Культивирование. Вирус простого герпеса (ВПГ) культивируют в куриных эмбрионах, культурах клеток и организме лабораторных животных. На хорионаллантоисной оболочке куриных эмбрионов вирус образует мелкие белые плотные узелки-бляшки; в зараженных культурах - вызывает цитопатический эффект: образование гигантских многоядерных клеток с внутриядерными включениями.
Антигенная структура. Вирус содержит ряд антигенов, связанных как с внутренними белками, так и с гликопротеидами наружной оболочки. Последние являются основными иммуногенами, индуцирующими выработку антител и клеточный иммунитет. Существует два серотипа вируса: ВПГ типа 1 и ВПГ типа 2.
Резистентность. Вирус может выживать на поверхности предметов при комнатной температуре в течение нескольких часов, чувствителен к УФ-лучам, обычным дезинфицирующим средствам, жирорастворителям, термолабилен.
Восприимчивость животных. Вирус простого герпеса патогенен для многих животных, у которых вызывает энцефалит при введении возбудителя в мозг или местный воспалительный процесс при заражении в глаз. В естественных условиях животные не болеют.
Эпидемиология. Простой герпес - одна из самых распространенных инфекций, которая поражает различные возрастные группы людей, чаще в осенне-зимний период. Отмечаются спорадические случаи заболевания, иногда небольшие вспышки в семьях, детских коллективах, больницах. Эпидемий не наблюдается.
Источником инфекции являются больные и носители. Основной механизм передачи - контактный, аэрогенный. Заражение происходит при попадании вирусов на поврежденные кожные покровы или слизистые оболочки.
Эпидемиология герпеса, вызванного вирусами типов 1 и 2, различна. ВПГ типа 1 передается через слюну, зараженные слюной руки и предметы быта, а ВПГ типа 2 - половым путем. Возможно заражение плода через плаценту.
Патогенез и клиническая картина. По клиническим проявлениям различают первичный и рецидивирующий герпес. Входными воротами возбудителя при первичной герпетической инфекции являются поврежденные участки кожи и слизистых оболочек рта, глаз, носа, мочеполового тракта, где вирусы репродуцируются. Затем по лимфатическим сосудам вирусы попадают в кровь и заносятся в различные органы и ткани.
Инкубационный период при первичном герпесе составляет в среднем 6-7 дней. Заболевание начинается с жжения, зуда, покраснения, отека на ограниченных участках кожи и слизистых оболочек, затем на этом месте появляются пузырьковые высыпания, наполненные жидкостью. Иногда заболевание сопровождается повышением температуры тела и нарушением общего состояния. При подсыхании пузырьков рубцов не образуется. Первичный герпес у новорожденных протекает тяжело и нередко заканчивается смертью. Однако у большинства людей первичная инфекция остается нераспознанной, так как протекает бессимптомно.
После первичной инфекции (явной и бессимптомной) 70-90 % людей остаются пожизненными носителями вируса, который сохраняется в латентном состоянии в нервных клетках чувствительных ганглиев. Нередко у носителей появляются рецидивы болезни в результате переохлаждения, перегревания, менструации, интоксикации, различных инфекционных заболеваний, стрессов, нервно-психических расстройств. Для рецидивирующего герпеса характерны повторные высыпания на коже и слизистых оболочках, нередко в тех же местах. Наиболее частой локализацией рецидивирующего герпеса, вызванного ВПГ типа 1, являются губы, крылья носа, полость рта, конъюнктива глаз. ВПГ типа 2 поражает мочеполовую систему и вызывает герпес новорожденных. Доказана роль ВПГ типа 2 в развитии рака шейки матки. Сравнительно редко встречаются генерализованные формы рецидивирующего герпеса, в частности поражения нервной системы и внутренних органов.
Иммунитет. В результате первичной герпетической инфекции в организме образуются сывороточные и секреторные антитела, которые обусловливают иммунитет к первичному герпесу, но не препятствуют сохранению вируса и возникновению рецидивов. Рецидивирующий герпес возникает при высоком уровне антител к вирусу герпеса. Основное значение в развитии рецидивирующего герпеса имеет состояние клеточного иммунитета.
Лабораторная диагностика. Материалом для исследования являются содержимое герпетических пузырьков, слюна, соскобы с роговой оболочки глаза, кровь, цереброспинальная жидкость, в летальных случаях . кусочки головного и спинного мозга.
Экспресс-диагностика заключается в обнаружении гигантских многоядерных клеток с внутриядерными включениями в мазках-отпечатках из высыпаний, окрашенных по Романовскому-Гимзе. Для дифференциации от других вирусов, принадлежащих к этому семейству, используют РИФ, ИФА, РИА, ПЦР. Выделение вируса проводят на куриных эмбрионах, культуре клеток и на лабораторных животных (мыши-сосунки), идентифицируют вирус с помощью РИФ или РН. В последние годы в диагностике простого герпеса начали применять моноклональные антитела, что дает возможность определить серотип вируса. Для серодиагностики заболевания используют РСК, РН, РИФ, ИФА.
Специфическая профилактика и лечение. Для профилактики тяжелых форм рецидивирующего герпеса в период ремиссии применяют многократное введение инактивированной, культуральной герпетической вакцины. Вакцинация, а также применение иммуномодуляторов, например реаферона, удлиняют межрецидивный период и облегчают течение последующих рецидивов. В остром периоде с лечебной целью используют химиотерапевтические препараты (виразол, ацикловир, оксолиновую, тебро-феновую, флореналовую мази, бонафтон), интерфероны и индукторы интерферона.
Вирус цитомегалии

Цитомегалия - инфекционное заболевание, возбудителем которого является цитомегаловирус (ЦМВ) Cytomegalovirus hominis (от греч. cytys - клетка, megas - большой). Вирус вызывает цитомегаловирусную инфекцию человека, характеризующуюся поражением почти всех органов (преимущественно слюнных желез) с образованием в них гигантских клеток с внутриядерными включениями, протекающую в различных формах - от бессимптомного носительства до тяжелой генерализованной формы, заканчивающейся летальным исходом.
Вирус впервые выделен К. Смитом в 1956 г.
Таксономия, морфология, антигенная структура. Возбудитель цитомегалии - ДНК-содержащий вирус, относится к семейству Herpesviridae, роду Cytomegalovirus.
Морфология, химический состав типичны для семейства герпесвирусов. Диаметр вирусной частицы (вириона) около 180 нм. В центре вириона находится двенадцатигранный нуклеокапсид, содержащий генетическую информацию - двухнитевую ДНК-вируса. Установлено 2 антигенных серотипа вируса.
Резистентность. Вирус термолабилен, чувствителен к дезинфицирующим средствам и жирорастворителям.
Эпидемиология. Цитомегаловирусная инфекция широко распространена на земном шаре. Источником вируса является больной человек или носитель. Вирус выделяется со слюной, мочой, секретами организма, реже фекалиями. Предполагается, что ведущий механизм передачи инфекции - контактно-бытовой, возможны аэрогенный и фекально-оральный механизмы передачи. Цитомегаловирус обладает высокой способностью проникать через плаценту (вертикальная передача), вызывая внутриутробную патологию плода.
Патогенез и клиническая картина. Патогенез не вполне выяснен. Инфекция связана с длительным носительством вируса, который в латентном состоянии сохраняется в слюнных железах, почках и других органах. Активация латентной инфекции происходит при иммунодефицитных состояниях, иммунодепрессивной терапии. Вирус поражает ЦНС, костный мозг, почки, печень, клетки крови. У беременных женщин цитомегалия может приводить к недоношенности, мертворождению, развитию аномалий у плода.
Иммунитет. У больных независимо от клинической формы инфекции, а также у носителей образуются антитела, которые, однако, не препятствуют сохранению вируса в организме и выделению его в окружающую среду. Интенсивность развития болезни находится под контролем клеточной иммунной системы хозяина.
Лабораторная диагностика. Обследованию на цитомегалию в первую очередь подлежат дети с поражением ЦНС и врожденными уродствами, а также женщины с неблагополучно протекающей беременностью. Исследуемый материал - слюна, моча, мокрота, цереброспинальная жидкость, кровь, пунктат печени.
Специфическая профилактика и лечение. Разработана живая аттенуированная вакцина. Для лечения применяют химиотерапевтические препараты (ганцикловир, фоскорнет натрия), иммуномодуляторы, интерферон.

Герпетическая инфекция – инфекция, вызываемая герпесвирусами 1-го и 2-го типа – хроническое рецидивирующее заболевание, входящее в группу ТОRСН – инфекций, для которого характерно поражение кожи, слизистых, глаз, нервной системы.
Инфекция, вызванная герпесвирусами, распространена повсеместно. Инфицированность населения очень высокая. По данным Всемирной организации здравоохранения (ВОЗ) герпесвирусная инфекция занимает второе место среди вирусных заболеваний человека, уступая лишь гриппу.
Восприимчивость к инфекции всеобщая, независимо от пола и возраста.
Подъемы заболевания регистрируются в осенне-зимний период.
Проведенные за последние 10 лет эпидемиологические исследования показали, что к 15-летнему возрасту инфицировано 80% детей, а к 30 годам 90% населения имеют антитела к вирусам того или иного типа.
Возбудитель инфекции – вирус простого герпеса 1 или 2 типа (ВПГ 1 или ВПГ 2). Попадая в клетку – вирус вызывает ее гибель. В отдельных клетках вирус может сохраняться длительное время, но при последующей активации вируса, клетка погибнет.
Считается, что ВПГ – 1 чаще поражает дыхательные пути, а ВПГ-2 - урогенитальную систему, но, несмотря на это, роль ВПГ-1 в развитии генитального герпеса увеличивается.
Вирусы простого герпеса неустойчивы к действию физических и химических факторов, легко разрушаются под действием ультрафиолетовых и рентгеновских лучей, чувствительны к этиловому спирту, эфиру. При низких температурах (-20-70 о С) вирус сохраняется десятилетиями.
Источники инфекции – вирусоносители и больные с различными формами болезни.
Пути передачи инфекции:
- Половой (наиболее значимый);
- Гематогенный;
- Воздушно-капельный;
- Контактно-бытовой (через игрушки, предметы обихода, одежду).
Факторами передачи вируса являются: слюна, кровь, слезная жидкость, сперма, секрет влагалища и цервикального канала, различные органы и ткани, используемые при трансплантации, моча, медицинский инструментарий.
Попадает вирус в организм через поврежденные участки кожи и слизистой, затем, в месте внедрения вируса происходит размножение вирусных частиц. Первичное инфицирование вызывает латентную (скрытую, вялотекущую) инфекцию.
Клинические проявления герпетической инфекции отличаются значительным разнообразием. Они зависят от локализации поражения, распространенности, состояния иммунной системы, типа вируса, а также от механизма заражения.
По механизму заражения герпетическая инфекция бывает первичная и рецидивирующая.
Первичная форма – остро возникающее заболевание при первом контакте с вирусом простого герпеса.
По локализации поражения:
- Кожа – простой герпес, герпетиформная экзема;
- Слизистые оболочки ротоглотки – стоматит, фарингит, тонзиллит;
- Верхние дыхательные пути – острое респираторное заболевание;
- Глаза – кератоконъюнктивит;
- Урогенитальный тракт – уретрит, цистит, вульвовагинит;
- Нервная система – менингит, энцефалит, менингоэнцефалит;
- Внутренние органы – гепатит, гломерулонефрит, пневмония.
Генитальный герпес развивается у молодых людей после начала половой жизни. Первичный генитальный герпес отличается более тяжелым и продолжительным течением. Высыпания обильные и занимают большую площадь поражения. При первичном генитальном герпесе отмечается повышение температуры, общая слабость, раздражительность. В области гениталий появляются везикулезные высыпания, сохраняющиеся до 8 суток.
Влияние вируса простого герпеса на беременность и роды.
Первичное инфицирование и рецидивы во время беременности могут привести к мертворождению, выкидышам, а также к формированию пороков у плода. Наиболее опасно заражение в третьем триместре.
При первичном инфицировании матери во время беременности инфицирование плода происходит в 5% случаев. Чаще всего инфицирование ребенка происходит во время родов (85%) или после родов (10%).
Инфицирование ребенка ВПГ во время родов может стать причиной последующего развития герпетической инфекции новорожденного.
Основную опасность представляет выделение вируса со слизистой половых органов в момент родов. Выделение вируса может сопровождаться высыпаниями в области половых органов, а может и не сопровождаться никакими симптомами.
Последствия герпесвирусной инфекции для ребенка:
- распространение вируса по всему организму с поражением головного мозга, легких, печени, надпочечников, кожи, глаз, ротовой полости;
- поражение ЦНС (снижение аппетита, судороги, повышенная возбудимость);
- поражение кожных покровов, слизистой оболочки глаз, рта.
Профилактика герпесвирусной инфекции:
Важным принципом профилактики этого заболевания является прекращение близких контактов с больным человеком в период обострения.
не пользоваться чужими предметами личной гигиены;
после контакта с пораженным герпесом участком (после нанесения противовирусного крема) необходимо тщательно вымыть руки;
Больной герпесвирусной инфекцией должен иметь отдельную посуду и пользоваться личным полотенцем;
Профилактика ВПГ-1 сводится к соблюдению общих правил предупреждения респираторных заболеваний. Профилактика ВПГ-2 соответствует профилактике инфекций передающихся половым путем ( использование презервативов во время половых контактов), использование антисептических растворов после полового акта.
Профилактика инфицирования во время беременности:
Вирус простого герпеса (ВПГ) – ДНК–содержащий вирус Herpes simplex virus семейства Herpesviridae подсемейства Alphaherpesvirinae. Согласно статистическим данным ВОЗ, инфекции, обусловленные ВПГ, занимают второе место по распространенности среди вирусных заболеваний человека. Различают два серотипа ВПГ – ВПГ-1 и ВПГ-2. Оба типа вируса вызывают инфекционные заболевания человека различной степени тяжести от характерных везикулезных или пустулезных высыпаний на коже и слизистых до поражений ЦНС. ВПГ-1 – причина офтальмогерпеса, протекающего в форме кератита или кератоиридоциклита, реже увеита, в единичных случаях — ретинита, блефароконъюнктивита. Заболевание может привести к помутнению роговицы и вторичной глаукоме. ВПГ-1 — основная причина энцефалита у взрослого населения стран умеренного климата, при этом только у 6–10% больных отмечается одновременное поражение кожи.
В ходе проведения эпидемиологических исследований установлено наличие специфических АТ к ВПГ у 90–95% обследуемых лиц среди взрослого населения, при этом первичная инфекция манифестно протекает лишь у 20–30% инфицированных.
ВПГ характеризуется коротким циклом репродукции в клеточных культурах и оказывает сильное цитопатическое действие. Он способен к репродукции в различных типах клеток, чаще персистирует в ЦНС, преимущественно в ганглиях, поддерживая латентную инфекцию с возможностью периодической реактивации. Наиболее часто вызывает кожно-слизистые формы заболевания, а также поражение ЦНС и глаз. Геном ВПГ может интегрироваться с генами других вирусов (включая ВИЧ), вызывая их активацию, также возможен его переход в активное состояние на фоне развития иных вирусных и бактериальных инфекций.
Пути передачи ВПГ: воздушно-капельный, половой, контактно-бытовой, вертикальный, парентеральный. Факторами передачи ВПГ служат кровь, слюна, моча, везикулярный и вагинальный секрет, сперма. Входными воротами являются поврежденные слизистые оболочки и кожа. По периферическим нервам вирус доходит до ганглиев, где сохраняется пожизненно. При активации ВПГ распространяется по нерву к первоначальному очагу поражения (механизм “замкнутого цикла” – циклическая миграция вируса между ганглием и поверхностью кожи). Может происходить лимфогенная и гематогенная диссеминация возбудителя, что особенно характерно для недоношенных новорожденных и лиц с выраженным иммунодефицитом (в т. ч. при ВИЧ-инфекции). ВПГ обнаруживается на лимфоцитах, эритроцитах, тромбоцитах, при проникновении вируса в ткани и органы возможно их повреждение вследствие его цитопатического действия. Сохраняющиеся в течение всей жизни у человека вируснейтрализующие АТ (даже в высоких титрах), хотя и препятствуют распространению инфекции, но не предупреждают рецидивов.
Выделение ВПГ продолжается значительное время при первичном инфицировании (ДНК выявляется в плазме крови в течение 4–6 недель), при рецидивах – не более 10 дней. Формирование противогерпетического иммунитета происходит как при манифестном, так и при бессимптомном течении инфекции. При первом контакте АГ с клетками иммунной системы в течение 14–28 дней формируется первичный иммунный ответ, который у иммунокомпетентных лиц проявляется образованием интерферонов, выработкой специфических АТ (вначале – IgM, впоследствии – IgA и IgG), повышением активности естественных киллеров – NK-клеток и формированием мощного пула высокоспециализированных киллеров. В случае реактивации или реинфекции возникает повторный контакт клеток иммунной системы с АГ, образуются АТ и Т-киллеры. Реактивация сопровождается продукцией АТ IgM (редко даже при наличии типичных высыпаний), АТ IgА (чаще) и IgG.
ВПГ (преимущественно ВПГ-2) вызывает генитальный герпес – хроническое рецидивирующее заболевание. Клинические проявления первичного эпизода инфекции, вызванной разными типами вируса сходны, однако инфекции, вызванной ВПГ-2, в гораздо большей степени свойственен рецидивирующий характер. Передача вируса происходит при половых контактах, очаг инфекции локализуется на слизистой и коже половых органов и перигенитальной зоны. Размножение вируса в клетках эпителия приводит к образованию очага сгруппированных пузырьков (папул, везикул), в которых содержатся вирусные частицы, сопровождается покраснением, зудом. Первичный эпизод протекает острее (обычно с симптомами интоксикации), чем последующие рецидивы. Часто возникают симптомы дизурии, признаки эрозии шейки матки.
На ранних стадиях ВИЧ-инфекции течение заболеваний, вызванных ВПГ-1 или ВПГ-2, короткое и типичное. Частым признаком углубления иммуносупрессии и перехода латентной стадии ВИЧ-инфекции в стадию вторичных заболеваний служит развитие опоясывающего лишая. Наличие стойких глубоких вирусных поражений кожи, повторный или диссеминированный опоясывающий лишай, локализованная саркома Капоши — одни из клинических критериев стадии вторичных заболеваний ВИЧ-инфекции. У больных с количеством CD4+-клеток менее 50 клеток/мкл отсутствует тенденция к самостоятельному заживлению эрозивно-язвенных дефектов. Частота герпетического энцефалита среди поражений ЦНС при ВИЧ-инфекции — около 1–3%. У больных СПИДом с наличием глубокого иммунодефицита заболевание нередко протекает атипично: болезнь начинается подостро и медленно прогрессирует до тяжелейших проявлений энцефалита.
Герпетическая инфекция даже при бессимптомном течении способна вызвать целый ряд патологий у беременной и новорожденного. Наибольшую угрозу репродуктивной функции представляет генитальный герпес, который в 80% случаев обусловлен ВПГ-2 и в 20% – ВПГ-1. Бессимптомное течение чаще имеет место у женщин и более типично для ВПГ-2, чем для ВПГ-1. Первичное инфицирование или рецидивы во время беременности наиболее опасны для плода, поскольку могут привести к самопроизвольному выкидышу, гибели плода, мертворождению, порокам развития. Заражение плода и новорожденного чаще отмечается при бессимптомном течении генитального герпеса, чем при клинически выраженном типичном течении. Новорожденный может приобрести герпетическую инфекцию внутриутробно, во время родов (в 75–80% случаев), либо постнатально.
ВПГ-2 может проникать в полость матки через цервикальный канал с поражением плода в 20–30% случаев; трансплацентарное инфицирование может происходить в 5–20% случаев, инфицирование во время родов – в 40% случаев. Возможна передача вируса при выполнении медицинских процедур. При типичных клинических проявлениях диагноз герпетической инфекции трудностей не представляет, тогда как при атипичных формах верифицируется на основании результатов лабораторных исследований, при этом приоритетными должны быть исследования, направленные на выявление маркеров текущей (активной) инфекции. Активация инфекционного процесса при герпетической инфекции, даже при наличии клинических проявлений в стадии обострения, редко сопровождается выработкой АТ-ВПГ IgM (чаще – при первичной инфекции либо реинфекции), как правило, при этом отмечают появление АТ-ВПГ IgА.
Целесообразными являются диагностические исследования для обнаружения ВПГ или его маркеров при наличии в анамнезе пациента указаний на рецидивирующую инфекцию либо на дебют герпетической инфекции в период беременности.
Дифференциальная диагностика. При наличии инфекционного синдрома (длительный субфебрилитет, лимфаденопатия, гепато- или гепатоспленомегалия) – токсоплазмоз, цитомегаловирусная инфекция и инфекция, вызванная ВЭБ; контактный дерматит, инфекционные заболевания, сопровождающиеся везикулезными высыпаниями на коже и слизистых оболочках (ветряная оспа, опоясывающий герпес, пиодермия и др.); эрозивно–язвенные поражения гениталий, обусловленные Treponema pallidum, Haemophilus ducreyi; болезнь Крона, синдром Бехчета, фиксированная токсикодермия, менингоэнцефалиты и менингиты неясной этиологии, увеиты и кератоконъюнктивиты неясной этиологии).
Показания к обследованию
- Планирование беременности;
- женщины, имеющие в анамнезе либо на момент обращения типичные герпетические высыпания любой локализации, в т. ч. рецидивирующий генитальный герпес, или наличие пузырьковых и/или эрозивных высыпаний на коже, ягодицах, бедрах, слизисто–гнойные выделения из влагалища;
- наличие полового контакта с партнером, имеющим генитальный герпес;
- атипичная форма заболевания: отсутствие зуда или жжения, отсутствие везикул, веррукозные узелки; обширные кожные поражения (до 10% случаев предполагаемого опоясывающего герпеса обусловлено не ВЗВ, а ВПГ);
- женщины с отягощенным акушерским анамнезом (перинатальные потери, рождение ребенка с врожденными пороками развития);
- беременные женщины (в первую очередь имеющие УЗИ-признаки внутриутробной инфекции, лимфоденопатии, лихорадку, гепатит и гепатоспленомегалию неясного генеза);
- дети с признаками внутриутробной инфекции, врожденными пороками развития или наличием на коже или слизистых оболочках везикул или корочек;
- дети, рожденные от матерей, перенесших генитальный герпес во время беременности;
- Пациенты (в первую очередь новорожденные) с сепсисом, гепатитами, менингоэнцефалитом, пневмонией, поражением глаз (увеит, кератит, ретинит, ретинальный некроз), поражением ЖКТ.
Материал для исследования
- Содержимое пузырьков/везикул со слизистых оболочек и кожи половых органов мужчин и женщин – микроскопические исследования, культуральные исследования, выявление АГ, выявление ДНК;
- мазки (соскобы) со слизистых оболочек цервикального канала, уретры (при отсутствии видимых пузырьковых высыпаний или эрозивно-язвенных поражений) – выявление ДНК;
- сыворотка крови, СМЖ (по показаниям) – выявление АТ.
Этиологическая лабораторная диагностика включает микроскопическое исследование, выделение и идентификация вируса в культуре клеток, выявление АГ или ДНК возбудителя, определение специфических АТ.
Сравнительная характеристика методов лабораторной диагностики (вирус простого герпеса - анализ). Среди методов лабораторной диагностики “золотым стандартом” долгое время считали выделение ВПГ в культуре клеток из крови, СМЖ, содержимого везикулезных или пустулезных высыпаний и других локусов (носоглотки, конъюнктивы, уретры, влагалища, цервикального канала). Данный метод предполагает изоляцию вируса при заражении биологическим материалом чувствительных культур клеток с его последующей идентификацией. К неоспоримым преимуществам метода относятся: возможность определения активности инфекции при наличии клинических проявлений и проведения типирования вируса, а также установления чувствительности к противовирусным препаратам. Однако длительность анализа (1–8 дней), трудоемкость, высокая стоимость и необходимость определенных условий проведения исследований затрудняет применение данного метода для рутинной лабораторной диагностики заболевания. Чувствительность достигает 70–80%, специфичность – 100%.
Материал с поверхности высыпаний может быть использован для микроскопических (окраска препаратов по Романовскому–Гимзе) или цитологических (окраска препаратов по Тцанку и Папаниколау) исследований. Названные процедуры имеют низкую диагностическую специфичность (не позволяют дифференцировать ВПГ от других герпес-вирусов) и чувствительность (не более 60%), поэтому не могут считаться надежными методами диагностики.
Выявление АГ ВПГ в крови, СМЖ, содержимом везикулезных или пустулезных высыпаний и других локусов (носоглотки, конъюнктивы, уретры, влагалища, цервикального канала) проводят методами РИФ и РНИФ с использованием моноклональных или высокоочищенных поликлональных АТ. При использовании метода ИФА чувствительность исследования возрастает до 95% и более, специфичность при манифестном герпесе варьирует от 62 до 100%. Однако большинство наборов реагентов для выявления антигена ВПГ методом ИФА не позволяют провести дифференцирование серотипов вируса.
Обнаружение ДНК ВПГ-1 и/или ВПГ-2 при использовании ПЦР в различном биологическом материале превосходит чувствительность обнаружения ВПГ при использовании вирусологического исследования. Выявление ВПГ в соскобах со слизистых оболочек полости рта, урогенитального тракта, в отделяемом пузырьковых высыпаний (везикул) и эрозивно–язвенных поражений кожи с помощью ПЦР является методом выбора. Несомненную ценность имеет определение количества ДНК ВПГ методом ПЦР в режиме реального времени, результаты исследования можно использовать как с диагностической целью, так и для оценки эффективности лечения.
Для выявления АТ к ВПГ разных классов IgА, IgG, IgM, суммарных к антигенам ВПГ обоих типов или типоспецифичных, применяют методы РНИФ или ИФА, для определения авидности АТ IgG – метод ИФА. Наибольшее диагностическое значение имеет детекция АТ IgM как показателя активности процесса, их выявление может свидетельствовать об остром заболевании, реинфекции, суперинфекции или реактивации. Однако в клинически выраженных случаях, в т. ч. при типичном течении генитального или неонатального герпеса, специфические АТ IgM выявляются редко (в 3–6% случаев). Определение авидности АТ-ВПГ IgG несет низкую информационную нагрузку: реактивация при клинически выраженных случаях сопровождалась наличием высокоавидных АТ. Тест на выявление АТ-ВПГ IgА является методом выбора наряду с определением ДНК либо АГ ВПГ при определении активности инфекционного процесса.
Показания к применению различных лабораторных исследований. Определение АТ целесообразно проводить для подтверждения первичной инфекции, а также установления диагноза у пациентов с бессимптомным и атипичным течением заболевания.
У беременных женщин (скрининг) целесообразно проведение исследований для выявления АТ-ВПГ IgМ, а также выявление АТ-ВПГ IgА. Для беременных высокого инфекционного риска дополнительно рекомендуется определение ДНК и АГ ВПГ в лейкоцитарной взвеси или в материале из предполагаемого очага.
При подозрении на внутриутробную инфекцию рекомендуется выявление ДНК вируса в пуповинной крови, у новорожденных – детекция ДНК вируса в различных биологических пробах (отделяемое пузырьковых высыпаний (везикул) эрозивно– язвенных поражений кожи и слизистых оболочек, ротоглотки, конъюнктивы; периферическая кровь, СМЖ, моча и др.), а также определение АТ-ВПГ IgМ и IgА в крови. Учитывая высокую диагностическую значимость определения ДНК вируса методом ПЦР и наличие зависимости между летальностью у новорожденных и виремией, вызванной ВПГ, некоторые исследователи рекомендуют использовать этот метод для лабораторного скрининга генерализованной герпетической инфекции детей, относящихся к группе высокого риска.
Выявление АГ-ВПГ в различных биологических пробах предлагается применять в качестве экспресс-тестов для дифференцирования типов вируса при скрининге популяций с высоким уровнем заболеваемости, а также при мониторинге заболевания.
У больных ВИЧ-инфекцией с атипичными клиническими проявлениями кожных поражений в диагностике отдается предпочтение выявлению ДНК ВПГ методом ПЦР как самому чувствительному методу лабораторной диагностики.
Особенности интерпретации результатов. Обнаружение вирусоспецифических АТ IgM может свидетельствовать о первичной инфекции, реже – о реактивации или реинфекции, выявление АТ-ВПГ IgА – об активности инфекционного процесса (затяжное течение при дебюте герпетической инфекции, реинфекции или реактивации). О врожденной инфекции (неонатальный герпес) свидетельствует присутствие АТ-ВПГ IgM и(или) IgА. Выявление АТ IgG отражает латентную инфекцию (инфицирование).
Выявление ДНК ВПГ свидетельствует о наличии активной (репликативной) стадии вирусной инфекции с учетом выраженности клинических проявлений. Выявление ДНК ВПГ-1 и/или ВПГ-2 методом ПЦР позволяет при однократном тестировании установить факт внутриутробного инфицирования плода; при проведении обследования в первые 24–48 ч после рождения лабораторно подтвердить врожденную инфекцию, вызванную ВПГ.
Диагностическое значение (специфичность и чувствительность) обнаружения ДНК ВПГ в СМЖ у больных ВИЧ-инфекцией с поражением ЦНС окончательно не установлены. Возможно, для подтверждения герпетической этиологии энцефалита необходимо определение концентрации ДНК ВПГ в СМЖ. Исследование для обнаружения ДНК ВПГ в крови малоинформативно в связи кратковременным нахождением ВПГ в сосудистом русле, следовательно, возможно получение отрицательного результата несмотря на развитие клинически выраженного заболевания.
Читайте также:


