Токсический гепатит от парацетамола

Парацетамол (ацетаминофен) — анальгетик и антипиретик хорошо переносится в терапевтических дозах. Он используется один или в комбинациях с опиоидами (декстропропоксифен, кодеин или трамадол), нестероидными противовоспалительными средствами и др.
Тогда как прием парацетамола в дозе 150 мг/кг может привести к цитолитическому гепатиту. С целью уменьшения риска отравления, аптечная упаковка препарата была ограничена 8 граммами на коробку.
Отравление парацетамолом является частым. Оно составило 9,8% преднамеренных отравлений в 2006 году во Франции (первое место в этиологической структуре отравлений медикаментами), по данным центров острых отравлений.
В России, отравления парацетамолом, зарегистрированные токсикологическими центрами Иркутска, Санкт-Петербурга и Екатеринбурга, составляли в 2003-2007 годах от 1,1% до 8,8%.
Отравление парацетамолом обладает рядом особенностей:
- механизмы токсичности хорошо изучены и позволяют понять позднее проявление повреждения печени (дозо-зависимого);
- N-ацетилцистеин (NАС является нетоксичным эффективным антидотом, который при своевременном применении предотвращает индуцированное парацетамолом повреждение печени;
- определение уровня парацетамолемии позволяет предсказать риск развития токсического гепатита и применить NАС в нужное время.
Фармакокинетика и механизмы токсичности парацетамола
В терапевтических дозах парацетамол быстро всасывается в пищеварительном тракте (плазматический пик достигается через 30-60 минут); период полувыведения из плазмы составляет около двух часов.
Токсичность парацетамола связана с действием его активного метаболита N-ацетил-р-бензохинонимина (NAPQI), образуемого системой цитохрома P450 (cyp2E1), преимущественно в печени. NAPQI, образуемый в небольших количествах, детоксицируется восстановленным глутатионом (GSH, триацидаминированная форма глицина, глутамата и цистеина), затем элиминируется в виде дериватов меркаптуровых кислот и цистеина.
При принятии массивной дозы парацетамола GSH расходуется; этап его регенерации лимитируется запасами цистеина. Когда содержание GSH уменьшается ниже 20-30%, NAPQI образует ковалентные связи с макромолекулами мембран гепатоцитов, активируя свободнорадикальные процессы, приводит к возникновению центролобулярных некрозов печени (иногда канальцевых некрозов).
Механизм действия N-ацетилцистеина. NAC, принося цистеин, позволяет восстановить запасы GSH. Предполагаются и другие эффекты NAC: образование связей с NAPQI (восстановление, конъюгация), снижение токсических эффектов NAPQI.
Клиническая картина
Начальная фаза отравления характеризуется бедностью симптомов. Если возможно, то у пострадавшего необходимо уточнить время приема медикамента. Самое большее, что может наблюдаться через два часа с момента отравления это: анорексия, тошнота, рвота, боли в животе; эти симптомы могут отсутствовать.
Увеличение уровня печеночных ферментов (ASAT, ALAT) наблюдается, начиная с 12-24-ого часа, прежде чем появляется чувствительность и болезненность при пальпации в правом подреберье, сопровождающаяся нарушениями пищеварения. Это начальные признаки цитолитического гепатита.
При тяжелых формах отравления на 3-6-ой день развивается фульминантный гепатит с желтухой, расстройствами гемостаза, ДВС синдромом, почечной недостаточностью, энцефалопатией; в этих случаях смертность достигает 25%. Чрезвычайно важно развитие тубулярного некроза почек, лактоацидоза, острого панкреатита. Обсуждается возможность возникновения миокардита.
Вследствие возможной комбинации парацетамола с опиоидами, не следует пренебрегать вероятностью обнаружения парацетамола у пациента с синдромом отравления опиатами.
Парацетамолемия и номограмма
Определение концентрации парацетамола в крови имеет диагностическое и прогностическое значение (предсказание риска гепатита). Знание уровня парацетамолемии и срока между временем отравления и проведения исследования по адаптированной номограмме B.H.Rumack & H.Matthew, позволяет предвидеть риск развития токсического гепатита в зависимости от наличия или отсутствия факторов риска (медикаментозная индукция ферментов печени, алиментарное истощение, хронический алкоголизм).

Примечание. Линия A, проходящая через 200 мг/л к 4 часу, определяет тактику лечения пациента, не имеющего дополнительных факторов риска (гепатотоксичность вероятна, риск более 60% без применения NAC). Линия B, проходящая через 150 мг/л к 4 часу (снижение концентрации на 25% к 4 часу), была введена FDA (Food and Drug Administration), для принятия в расчет вероятных неопределенностей (время приема…; возможная гепатотоксичность) — она мало используется во Франции. Линия C, проходящая через 100 мг/л к 4 часу, определяет тактику лечения больного, имеющего один или несколько дополнительных факторов риска. — 100 мг/л = 0,66 ммоль/л; 0,1 ммоль/л = 15,15 мг/л.
Вследствие замедленного всасывания парацетамола в пищеварительном тракте при больших дозах, эта номограмма поддается интерпретации только спустя 4 часа с момента отравления.
Номограмма не используется для оценки риска в более ранние сроки и при предшествующем повторном приеме парацетамола в больших дозах с терапевтическими целями (например, ошибка в назначении препарата, передозировка при зубной боли), в том числе пролонгированных форм препарата, содержащих замедлители всасывания, а также при определении парацетамолемии в сроке свыше 24 часов с момента отравления.
Неотложная помощь
Госпитализация необходима в случае приема дозы, превосходящей 200 мг/кг у ребенка и 150 мг/кг у взрослого (125 мг/кг при наличии факторов риска) или, если принятое количество препарата неизвестно.
На догоспитальном этапе никакое лечение не рекомендовано, если парацетамол принят один, транспортировка пострадавшего может осуществляться без врачебного сопровождения; не существует рекомендации применения активированного угля на этом этапе.
Определение ASAT, ALAT, билирубина и уровня протромбина должно быть осуществлено при поступлении, затем 12 часов спустя, и возобновлено в следующие дни, в зависимости от тяжести.
Промывание желудка не представляет интереса. Использование активированного угля рекомендовано (одна доза 40-50 г; 1 г/кг у ребенка) через 1-2 часа после отравления.
N-ацетилцистеин показан, если уровень парацетамолемии, измеренный после 4-ого часа с момента отравления, расположен выше линии, соответствующей концентрации 200 мг/л через 4 часа (линия А) или, при наличии факторов риска, выше линии, соответствующей 100 мг/л в этот же срок (линия С).
Существует большое количество протоколов применения NAC пероральным и внутривенным путем, а также множество лекарственных форм NAC. Следует отметить, что никакой специальной формы NAC, предназначенной для перорального приема в качестве антидота, в аптечной сети не имеется.


В соответствии с протоколом внутривенного применения, доза препарата должна быть введена в течение часа, вместо рекомендованных 15 минут (то, что фигурирует еще в справочнике Vidal), это позволяет уменьшить риск появления анафилактоидной реакции.
Для протоколов перорального и внутривенного применения антидота могут быть констатированы следующие положения:
- минимальный риск развития гепатотоксических эффектов отмечается при начале введения NAC через 10 часов после приема токсической дозы парацетамола, независимо от конкретного протокола применения;
- риск гепатотоксичности увеличивается для пациентов, у которых введение антидота начато между 10-ым и 24-ым часом;
- применение NAC позднее 24-го часа неспособно предупредить повреждения печени.
Между тем, имеющиеся наблюдения позволяют утверждать, что использование NAC, осуществленное до 36-ого часа с момента отравления может ограничить тяжесть токсического гепатита.

Выбор пути введения зависит, прежде всего, от наличия или отсутствия рвоты. Ее возникновение обусловлено действием парацетамола, в частности при тяжелой интоксикации, или самим NAC при пероральном введении необходимой дозы.
Хотя, небольшое количество NAC может быть адсорбировано активированным углем, его предшествующее использование не препятствует введению NAC этим путем. Внутривенное введение показано при рефрактерных нарушениях пищеварения, в случае непереносимости перорального приема NAC.
Что касается перорального пути введения, то предпочтительнее использование раствора, предназначенного для эндотрахеобронхиальных инстилляций, по сравнению с использованием порошков в пакетиках по 200 мг, необходимое количество которых может быть весьма значительным.
Тошнотворный серный запах может быть смягчен фруктовым соком или кока-колой. Нежелательные эффекты минимальны (тошнота, рвота) и появляются чаще всего только во время введения препарата.
Протокол внутривенного введения осуществляется более часто, по практическим причинам (наличие на фармацевтическом рынке, отсутствие раздражения пищеварительного тракта, лучшая переносимость перфузии, длительность введения).
Анафилактоидные реакции (дозозависимая гистаминолиберация, индивидуальная чувствительность), средне тяжелые (вазомоторная гиперемия, зуд, сыпь, крапивница) или тяжелые (бронхоспазм, ангионевротический отек, артериальная гипотония), могут появиться в 2-3% случаев. Они, преимущественно, связаны со слишком большой скоростью введения NAC.
Наличие у пациента астмы является фактором риска появления этих побочных реакций. Они представляются более частыми в случаях, когда NAC применяли в отсутствие подтвержденного риска гепатита. Уменьшение скорости инфузии, а также использование блокаторов Н1-рецепторов гистамина снижает тяжесть проявления нежелательных эффектов.
Если реакция тяжелая, то необходимо прекращение введения NAC и проведение симптоматического лечения. В этих случаях требуется критическая оценка соотношения пользы и степени риска продолжения введения NAC.
Введение NAC продолжают (по 300 мг/кг/сут), если имеются обусловленные интоксикацией парацетамолом повреждения печени, почек или метаболический ацидоз.
Печеночно-клеточная недостаточность
Организация ведения больных с печеночно-клеточной недостаточностью не имеет частных особенностей. Перевод пациентов в реанимационное отделение, близкое к центру трансплантации печени, должен быть осуществлен рано.
Уменьшение уровня протромбина и фактора V 3,5 ммоль/л отчетливо коррелируют с неблагоприятным развитием заболевания.
Наиболее известными прогностическими критериями являются факторы King’s College: о неблагоприятном течении свидетельствует снижение рН артериальной крови 6,5), креатининемии >300 мкмоль/л и энцефалопатии 3 или 4 стадии.
Критерии Clichy проще (энцефалопатия 2 или 3 стадии с уровнем фактора V у пациентов старше 30 лет
В Великобритании передозировки парацетамола (ацетаминофена) чаще всего наблюдаются у молодых взрослых людей, которым не назначены врачами психотропные препараты. Там это средство используется примерно в 15—30 % случаев умышленных самоотравлений.
В 1993 г. Система надзора за токсической экспозицией при Американской ассоциации центров борьбы с отравлениями провела примерно 60 000 расследований, связанных с парацетамолом (ацетаминофеном). Только у небольшой доли пациентов отмечен риск тяжелого поражения печени, которая демонстрировала замечательную способность к регенерации. Выздоровление даже после тяжелой передозировки обычно быстрое и полное, а общий уровень смертности низок.
а) Гепатотоксичность парацетамола (ацетаминофена). Хотя точный механизм действия неясен, поражение печени, вероятно, обусловлено в основном токсичным промежуточным соединением, которое, ковалентно связываясь с гепатоцитами, вызывает некроз центральной части печеночных долей. Альтернативное объяснение некроза подразумевает переокисление липидов и окисление тиольных групп ключевых ферментов печени, в частности Са 2+ -транслоказ.
Печень метаболизирует основную часть терапевтических доз парацетамола (ацетаминофена) путем его глюкуронидной и сульфатной конъюгации. Лишь небольшое его количество превращается в высокореактивное производное N-ацетил-р-бензохинонимин (АБХИ) посредством цитохром Р450-зависимой оксидазной системы со смешанной функцией. Глутатион быстро обезвреживает это вещество, преобразуя его в цистеиновый или меркаптуриновый конъюгат. Одно из объяснений гепатотоксичности ацетаминофена предполагает насыщение сульфатного пути метаболизации при приеме внутрь слишком высокой дозы лекарства, что могло бы повысить количество его токсичного производного.
Когда содержание глутатиона в печени опускается ниже критического уровня (примерно 30 % нормального запаса), АБХИ ковалентно связывается с макромолекулами гепатоцитов, обусловливая некротизацию тканей.
Существует значительная индивидуальная изменчивость чувствительности к гепатотоксичности парацетамола (ацетаминофена): как минимум у 20 % лиц с токсическим уровнем этого лекарства в плазме поражение печени отсутствует.
В случайной выборке пациентов с передозировкой тяжелая некротизация печени развивается без применения антидота только у 8 %, несмотря на то что плазменные концентрации ацетаминофена соответствуют токсическому диапазону примерно у 15 %. Летальная печеночная недостаточность наблюдается лишь у 1—2 % больных, не получивших специфического лечения. Одно только истощение гепатоцитарного запаса восстановленного глутатиона не объясняет индуцируемой парацетамолом (ацетаминофеном) гепатотоксичности, поскольку аналогичное экспериментальное снижение его уровня другими лекарствами (например, йодметаном) не приводит к некрозу печени.
По-видимому, на активность цитохром Р450-зависимой оксидазы со смешанной функцией и чувствительность печени к интоксикации влияют возраст, рацион питания, алиментарный и метаболический статус организма, а также прием различных лекарств.
Вещества, индуцирующие Р450-ферменты печени (например, фенобарбитал, 3-метилхолантрен), способны усилить ацетаминофеновую гепатотоксичность. У пациентов, выживших после острой передозировки, хронический гепатит и цирроз развиваются редко.
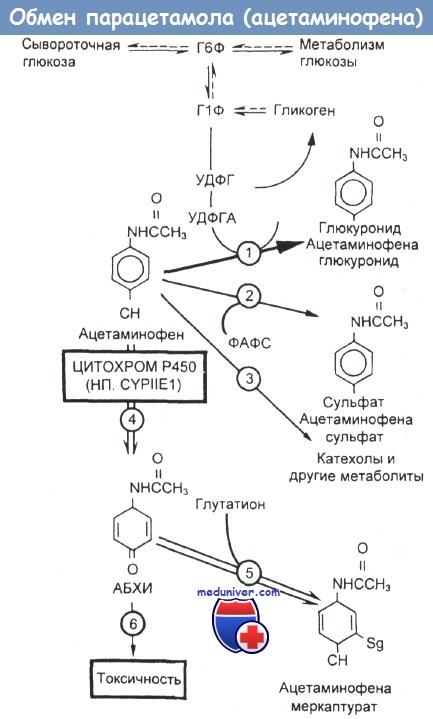
Схема метаболизации ацетаминофена в печени и последствия голодания и потребления алкоголя.
Парацетамол (ацетаминофен) метаболизируется несколькими главными и второстепенными путями (цифры в кружочках).
Путь 1 — это превращение в ацетаминофеновый глюкуронид, катализируемое глюкуронозилтрансферазой.
Парацетамол (ацетаминофен) конъюгирует с глюкуронидом, который предоставляется уридин(дифосфо)ацетилглюкозамином (УДФГА). Этот глюкуронид образуется из глюкозо-1-фосфата (Г1Ф), а последний — либо из гликогена, либо из глюкозо-6-фосфата (Г6Ф). При катаболическом обмене веществ (голодании) печеночные метаболические пути ориентированы на глюконеогенез (пунктирные линии), сокращающий количество предшественников глюкозы, доступных для глюкуронидирования.
Путь 2 соответствует сульфатированию и зависит от фосфоаденилилсульфата (ФАФС) и печеночных запасов серы.
Путь 3 — второстепенный, дающий лишь небольшую долю метаболитов ацетаминофена. Путь 4 ведет к оксидазной системе со смешанной функцией, включающей в себя цитохром Р450, главным образом его фракцию 2E1[CYPIIE1]. Этот фермент образует высокореактивное производное ацетаминофена N-ацетил-р-бензохинонимин (АБХИ).
Количество исходного лекарства, метаболизирующегося таким способом, может увеличиваться (серые стрелки) в результате индукции CYPIIE1 недавним приемом алкоголя или голоданием, а также при ослаблении глюкуронидирования. Путь 5 соответствует главному пути детоксикации АБХИ. Это производное конъюгирует с глутатионом и выводится из организма, пока запасы глутатиона и серы в печени не уменьшатся ниже критического уровня. Путь 6 показывает судьбу неконъюгированного АБХИ.
Он связывается с жизненно важными молекулами внутри клеток печени и в конечном итоге приводит к интоксикации и гибели последних. Недавнее потребление алкоголя индуцирует ферменты главным образом четвертого пути, а голодание подавляет метаболизацию по первому и, возможно, четвертому путям, увеличивает активность ферментов четвертого пути и снижает доступность предшественников для детоксикации АБХИ по пятому, в результате направляя больше ацетаминофена по пути 6.
УДФ — уридинфосфат; УДФГ — УДФ-глюкоза.
б) Факторы риска поражения печени парацетамолом (ацетаминофеном). К факторам риска, предрасполагающим к поражению печени после передозировки парацетамола (ацетаминофена), относятся алкоголизм и хроническое потребление агентов, индуцирующих микросомные ферменты печени (например, изониазида, противосудорожных средств). Голодание истощает запас глутатиона.
У пациентов, неоднократно принимающих парацетамол (ацетаминофен) в избыточном количестве, уровень этого лекарства обычно соответствует токсичному диапазону. Клинический анамнез зачастую неточен.
Примерно в одном из каждых 500 случаев передозировки парацетамола (ацетаминофена) речь идет о поддающемся терапии отравлении, что не отражено в анамнезе и не выявляется у пациентов с печеночной дисфункцией.
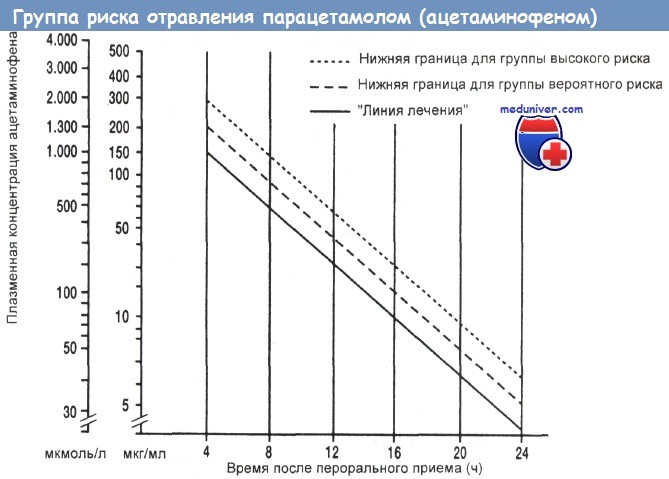
Номограмма для определения групп риска на основе исходной плазменной концентрации ацетаминофена.
в) Токсичная доза парацетамола (ацетаминофена). У взрослых пороговое значение однократной дозы, приводящей к острому тяжелому поражению печени, составляет 150—250 мг/кг. Дети в возрасте до 10 лет, похоже, намного устойчивее взрослых. Vale и Proudfoot отмечают, что риск тяжелого и потенциально летального поражения печени при передозировке, учитывая количество принятого внутрь ацетаминофена или симптомы, наблюдаемые в период максимального защитного действия антидота, достаточно надежно оценить нельзя.
1. Взрослые: 5—15 г (15—45 таблеток по 325 мг).
2. Взрослые: менее 125 мг/кг (печень не страдает);
250 мг/кг (тяжелое поражение печени [50 %]);
350 мг/кг (тяжелое поражение печени [100 %]).
3. Подростки: 125—150 мг/кг (гепатотоксичная доза).
4. Летальная доза: 13—25 г (46—75 таблеток по 325 мг).
в) Печеночный глутатион и отравление парацетамолом (ацетаминофеном). Лекарственные средства могут влиять на токсичность ацетаминофена, сокращая запасы глутатиона или снижая масштабы конъюгации. Судя по фармакокинетическим данным, печеночные резервы восстановленного глутатиона начинают истощаться у человека после перорального приема 0,5—3,0 г ацетаминофена, причем это истощение можно компенсировать введением N-ацетилцистеина.
В метаболизации парацетамола (ацетаминофена) существуют определенные межэтнические различия. Например, одно исследование показывает, что организм индийцев выделяет чуть больше глюкуронидных и несколько меньше сульфатных конъюгатов, чем организм китайцев. В обеих этих группах экскретируется меньше (6 % против 9 %) производных глутатиона, чем у европейцев шотландского происхождения.
Образование окисленных метаболитов и почечная экскреция, по-видимому, происходят в соответствии с кинетикой первого порядка (т. е. скорость линейно зависит от концентрации); сульфатная и глюкуронидная конъюгация следуют уравнению Михаэлиса—Ментена, т. е. кинетике нулевого или первого порядка в зависимости от концентрации субстрата.
Скорость образования токсичного метаболита после приема ацетаминофена внутрь зависит от темпов всасывания последнего, масштабов глюкуронидной и сульфатной конъюгации, а также от микросомной ферментативной активности. Ни табакокурение, ни предшествовавший прием циметидина не изменяют направлений метаболизации парацетамола (ацетаминофена). Печень биотранс-формирует его почти полностью путем конъюгации, а не Р450-зависимого окисления.
Таким образом, циметидин вряд ли влияет на судьбу терапевтических доз парацетамола (ацетаминофена), поскольку главным образом ингибирует микросомное окисление в печени.
Терапевтические дозы кодеина не изменяют ни клиренса ацетаминофена, ни его метаболизации. Высокие дозы ранитидина не влияют на метаболическое выведение терапевтических количеств ацетаминофена у человека. Основными ферментами, катализирующими его окисление до реактивных метаболитов, являются цитохромы Р4501А2 и Р4502Е1. Активность первого из них снижается при конкурентном ингибировании теофиллином, что может ослабить ацетаминофеновую интоксикацию при одновременном применении двух этих лекарств.
г) Парацетамол (ацетаминофен) и СПИД. У больных СПИДом возможно связанное с питанием истощение запасов глутатиона. Вероятно, множественные дозы ацетаминофена противопоказаны при лечении зидовудином лиц с подозрением на пониженный уровень глутатиона вследствие плохого питания, СПИДа или потребления алкоголя, а также при дополнительном применении средств, стимулирующих Р450-зависимые ферменты, например противосудорожных лекарств. Судя по результатам исследований на животных, адренергические агонисты сокращают печеночные запасы глутатиона и могут потенцировать гепатотоксичность ацетаминофена.
д) Парацетамол (ацетаминофен) при беременности. При передозировке парацетамола (ацетаминофена) и будущая мать, и плод подвергаются риску гепатотоксичности, поскольку это лекарство (но не его конъюгаты) легко диффундирует через плаценту как человека, так и подопытных животных. Однако четких указаний на тератогенность ацетаминофена и N-ацетилцистеина нет. Лечение беременных пациенток с передозировкой должно вестись по стандартной схеме. Само по себе отравление ацетаминофеном не служит показанием к прерыванию беременности.
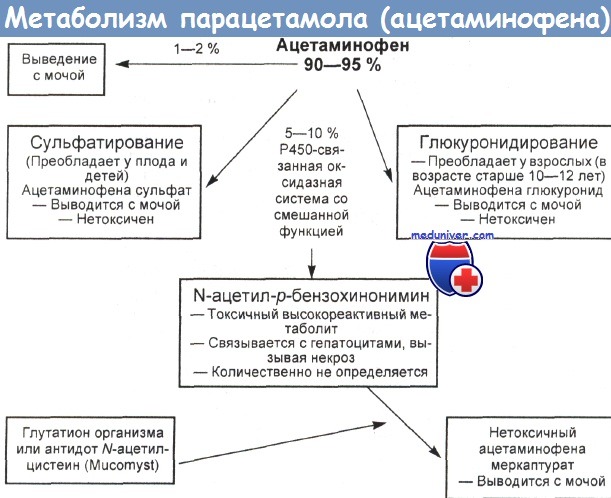
Обмен парацетамола у плода и новорожденного ребенка
Уже на ранних этапах развития плода его гепатоциты могут окислять ацетаминофен до его токсичного метаболита, а способность конъюгировать лекарство с глутатионом достигает взрослого уровня по мере полового созревания человека. Интенсивность сульфатной конъюгации возрастает по мере созревания плода, а глюкуронидирование у плода почти не выявляется. Пониженное отношение цистеиновых и меркаптуриновых конъюгатов к сульфатным и глюкуронидным наводит на мысль о слабой активности соответствующего варианта цитохрома Р450 у новорожденного.
Низкая скорость образования (детоксикации) токсичного метаболита цистеиновым и меркаптуриновым способами может означать меньшую, чем у взрослых, чувствительность новорожденных к индуцируемой ацетаминофеном гепатотоксичности. У новорожденных, матери которых страдали от передозировки ацетаминофена, степень поражения печени ниже, чем у детей старшего возраста и взрослых; однако, если высокая доза ацетаминофена проникает через плацентарный барьер, опасность для плода сохраняется, поскольку его печень окисляет лекарство до токсичного метаболита. Хотя у плода и в раннем возрасте преобладает сульфатирование, начиная с 10 лет на первый план выходит глюкуронизирование. Схему метаболизации ацетаминофена у разных возрастных групп представил Roberts.
Молниеносная печеночная недостаточность
При тяжелом отравлении парацетамолом (ацетаминофеном) молниеносная печеночная недостаточность может развиться на третий — шестой день. Для нее характерны прогрессирующая желтуха, энцефалопатия, повышение внутричерепного давления, сильное нарушение гемостаза с диссеминированным внутрисосудистым свертыванием и кровотечением, гипервентиляция, ацидоз, гипогликемия и почечная недостаточность. Прогноз очень неблагоприятный.
Острая печеночная недостаточность во всех возрастных группах может также наблюдаться при инфекционном гепатите (вирусы гепатитов А, В, С и D, ветряной оспы, герпеса, Коксаки, ECHO, Эпштейна—Барр, аденовирус), синдроме Рейе (характеризующемся неукротимой рвотой в сочетании с аномальной гистологией печени), при обострении хронической патологии печени (болезни Вильсона, хронического активного гепатита), токсическом гепатите (отравлении бледной поганкой Amanita phalloides, пирролизидиновыми алкалоидами, четыреххлористым углеродом, хлорданом) и ятрогенном поражении печени (изониазидом, p-аминосалициловой кислотой, тетрациклином, вальпроевой кислотой, салицилатами, галотаном).
Если у ребенка повышены сывороточные уровни аланин- и аспартатрансаминазы (1500—10 000 ЕД/л), лактатдегидрогеназы и общего билирубина, увеличено протромбиновое и частичное тромбопластиновое время, наблюдаются гипопротеинемия и гипогликемия, а сывороточная концентрация аммония в 2 раза выше нормы, следует заподозрить отравление ацетаминофеном, поскольку это лекарство часто дают детям без назначения врача. Тяжесть нарушения печеночной функции не может служить надежным прогностическим критерием.
У пациентов с концентрацией парацетамола (ацетаминофена) в плазме выше линии на полулогарифмическом графике, соединяющей точки 1,32 ммоль/л (200 мг/л) и 0,20 ммоль/л (30 мг/л) через 4 и 15 ч после его перорального приема соответственно ("лечебная линия"), шансы на развитие тяжелого и часто летального поражения печени, характеризующегося повышением плазменных активностей аланин- и аспартаттрансаминазы выше 1000 МЕ/л, близки к 60 %. Если концентрация ацетаминофена выше параллельной линии на номограмме, соединяющей 2 ммоль/л (300 мг/л) и 0,33 ммоль/л (50 мг/л) в 4 и 15 ч соответственно, эта вероятность повышается до 90 %.
Впрочем, пациенты с концентрациями выше этой линии часто не страдают от поражения печени, тогда как сильная гепатотоксичность изредка отмечается даже при уровне ацетаминофена всего 0,83 ммоль/л (125 мг/л) через 4 ч после приема. В США антидот N-ацетилцистеин назначают при концентрации выше линии, проходящей через точку 1 ммоль/л (150 мг/л) через 4 часа.

Весь контент iLive проверяется медицинскими экспертами, чтобы обеспечить максимально возможную точность и соответствие фактам.
У нас есть строгие правила по выбору источников информации и мы ссылаемся только на авторитетные сайты, академические исследовательские институты и, по возможности, доказанные медицинские исследования. Обратите внимание, что цифры в скобках ([1], [2] и т. д.) являются интерактивными ссылками на такие исследования.
Если вы считаете, что какой-либо из наших материалов является неточным, устаревшим или иным образом сомнительным, выберите его и нажмите Ctrl + Enter.
У взрослых некрозы в печени развиваются после приёма не менее 7,5-10 г препарата, но реально дозу препарата трудно оценить, поскольку быстро развивается рвота, а данные анамнеза ненадёжны.
Алкоголь, индуцируя ферменты, усиливает гепатотоксичность парацетамола, так что у больных алкоголизмом повреждение печени может развиться при ежедневном приёме лишь 4-8 г препарата, а при сопутствующем заболевании печени - при приёме ещё меньшей дозы.
Полярный метаболит парацетамола связывается в печени преимущественно с глутатионом. Когда запасы глутатиона истощаются, метаболит парацетамола арилирует нуклеофильные макромолекулы, необходимые для жизнедеятельности гепатоцитов, вызывая таким образом некроз печени.

[1], [2], [3], [4], [5], [6], [7], [8], [9], [10], [11], [12], [13], [14], [15], [16], [17], [18]
Симптомы
В течение нескольких часов после приёма токсической дозы парацетамола развиваются тошнота и рвота. Сознание не нарушается. Примерно через 48 ч наступает видимое улучшение; затем примерно на 3-и или 4-е сутки состояние больных ухудшается, появляются болезненность печени и желтуха. Повышается активность трансаминаз, уровень протромбина падает. При более тяжёлом поражении состояние быстро ухудшается с развитием острых некрозов печени. Без лечения в 25-30% случаев развивается острый канальцевый некроз. Отмечаются значительная гипогликемия и повреждение миокарда.
При гистологическом исследовании выявляют некроз зоны 3, признаки жировой дистрофии и незначительную воспалительную реакцию. Может отмечаться массивная деградация коллагена, но она не приводит к циррозу.
Длительный (около 1 года) приём парацетамола (по 3-4 г/сут) может привести к хроническому повреждению печени. Сопутствующие заболевания печени и алкоголизм усиливают повреждающее действие парацетамола.

[19], [20], [21], [22], [23], [24], [25], [26], [27], [28], [29],
Лечение
Проводят промывание желудка. Больного госпитализируют. Поскольку признаки некрозов в печени появляются поздно, клиническое улучшение не должно служить основанием для благоприятного прогноза.
Форсированный диурез и гемодиализ не увеличивают экскрецию парацетамола и его метаболитов, уже связавшихся с белками тканей.
Лечение направлено на восстановление запасов глутатиона в гепатоцитах. К сожалению, глутатион плохо проникает в печёночные клетки. Поэтому применяют предшественники глутатиона и вещества с аналогичным действием. Оценку лечения проводят по концентрации парацетамола в плазме. Эту концентрацию наносят на полулогарифмическую шкалу зависимости концентрации от времени и рассматривают относительно отрезка прямой, соединяющей точки, которые соответствуют 200 мкг/мл через 4 ч и 60 мкг/мл через 12 ч. Если концентрация парацетамола у больного располагается ниже этого отрезка, повреждение печени является лёгким и лечение можно не проводить.
При внутривенном введении ацетилцистеин (мукомист, парволекс) быстро гидролизуется до цистеина. Его вводят в дозе 150 мг/кг в 200 мл 5% раствора глюкозы в течение 15 мин, затем 50 мг/кг в 500 мл 5% раствора глюкозы в течение 4 ч и
100 мг/кг в 1 л 5% раствора глюкозы в течение последующих 16 ч (общая доза 300 мг/кг в течение 20 ч). Такое лечение проводят всем больным с повреждением печени парацетамолом, даже если после его приёма прошло более 15 ч. Оно может также оказаться полезным при других формах ФПН.
Применение N-ацетилцистеина в течение 16 ч после приёма препарата настолько эффективно, что в настоящее время повреждение печени при отравлениях парацетамолом наблюдается редко.
При фульминантном течении может потребоваться трансплантация печени. Выживаемость хорошая, поэтому психологическую реабилитацию проводить не сложно.
Прогноз
Среди всех больных, госпитализированных в больницу общего профиля, смертность составила 3,5%. Поздняя госпитализация, кома, увеличение ПВ, метаболический ацидоз и нарушение функции почек отягощают прогноз.
Тяжесть лекарственного поражения можно оценивать по номограммам, учитывающим концентрацию парацетамола в крови и срок после приёма препарата. Смерть наступает на 4-18-е сутки.
Сердечно-лёгочная и почечная недостаточность, нередко наблюдающаяся у пожилых людей, повышает риск повреждения печени даже после приёма умеренных доз парацетамола.

[30], [31], [32], [33]
Читайте также:


