С цитомегаловирусом не взяли в протоколе

Цитомегаловирус и бесплодие - как взаимосвязаны два этих понятия? Цитомегаловирус и бесплодие у женщин действительно находятся в тесной взаимосвязи, и бесплодие можно назвать одним из самых серьезных последствий цитомегаловируса.
Цитомегаловирус – причина бесплодия: почему это случается? Дело в том, что герпес и цитомегаловирус скорее вызывают заболевания, которые впоследствии могут приводить к бесплодию, чем сами являются причиной его возникновения. Цитомегаловирус и герпес были обнаружены в сперме большинства бесплодных мужчин, что позволяет сделать определенные выводы. Кроме того, развитие и активное распространение в женском организме цитомегаловируса, как известно, может приводить к возникновению таких женских заболеваний, как оофорит, вагинит и эндометрит. Все это может через определенное время провоцировать женское бесплодие, как правило, при отсутствии должного лечения этих гинекологических заболеваний.
Распространение цитомегаловируса в организме влечет за собой нарушение функционирования мочеполовой системы, хронизацию заболеваний урологической и гинекологической сфер, а также варикоцеле. Кроме того, вирус имеет тенденцию проникать в половые клетки и разворачивать там свою активность.
Кроме того, цитомегаловирус может даже осложнить наступление беременности искусственным путем, не говоря о ее наступлении естественным способом.
При цитомегаловирусе можно забеременеть или нет? Прямого влияния ЦМВ на наступление беременности не оказывает. Проблема заключается в том, что у женщины с данным вирусом сильно ослаблен иммунитет, что влечет за собой постоянные респираторные заболевания, воспаления в организме, а именно хронизацию некоторых заболеваний, воспаления мочеполовой системы. Все этом часто приводит к образованию спаек, которые становятся большой преградой для наступления беременности( Трихомониаз при беременности ).
Поэтому для наступления успешной беременности встает вопрос лечения данных гинекологических нарушений. Если заболевание затронуло мужчину, нужно лечить нарушения работы его мочеполовой системы.
Цитомегаловирус, ставший причиной бесплодия, иногда вынуждает женщину обратиться за помощью к экстракорпоральному оплодотворению. Может ли проводиться ЭКО женщине с ЦМВ? Цитомегаловирус перед ЭКО не является поводом для отказа от экстракорпорального оплодотворения.
Можно ли делать ЭКО при герпесе и цитомегаловирусе? Да, но перед этим нужно пройти курс лечения. Данная терапия предполагает применение противовирусных препаратов. Кроме того, назначается иммуномодулирующая терапия, которая способна повысить защитные силы организма.
По мнению специалистов, цитомегаловирус и ЭКО совместимы. Однако полностью нельзя избавиться от вируса полностью. Однако подавить его можно.
Обычно для лечения в этот период используются препараты, которые подавляют обратную вирусную транскриптазу. Они называются препаратами нуклеозидного действия. Кроме того, показаны модуляторы и стимуляторы для повышения защитных сил организма. Даже если женщина будет беременеть при помощи ЭКО, она должна обладать крепким иммунитетом. Это необходимо для того, чтобы эмбрион смог полноценно прикрепиться к матке и не произошло его отторжения.
Однако лечение цитомегаловируса показано при переходе его в активную стадию, когда он разворачивает свою жизнедеятельность в женском организме и наносит ему необратимый вред. Однако, перед лечением необходимо проведение соответствующей диагностики, которая позволит определить, имеется ли вирус в организме, когда произошло заражение им и на какой стадии сейчас находится заболевание.
Достигнуть полной ремиссии при таком диагнозе не удастся. Суть терапии заключается в подавлении вирусной активности. В основном для лечения используются следующие нуклеозидные препараты:
Также используются при лечении такие иммуномодуляторы, как Циклоферон и Интерферон.
Грамотно назначенное лечение необходимо для подготовки организма женщины к экстракорпоральному оплодотворению. Интересно то, что входе такой подготовки организм начинает перестраиваться и защитные силы организма заметно повышаются. Это способно привести к беременности естественным путем тогда, когда женщина уже этого не ждет и почти потеряла надежду. Если это произойдет, нужно будет тщательно наблюдаться у врача в период протекания беременности. Это необходимо для предупреждения разного рода осложнений, которые могут навредить здоровью матери и плода, а также привести к развитию у него пороков функционирования систем и органов.
Всем привет, вступаю в программу ЭКО и очередные палки в колеса. Пока получала квоту пришёл результат Пцр цитомегаловирус обнаружен, антитела к LG M 0.13 пролечили герпферон мазь 10 дней, виферон 1млн 10 дней через день и эпингель. Через 10 дней после окончания лечения мазью сдала и снова обнаружен, количество в анализе не написали, доздала антитела lg G>250. Были ли у кого — то похожие результаты и допустили ли вам до протокола?


Комментарии пользователей

![]()
Да, конечно, а почему не должны были допустить? Максимум, что вам порекомендуют, если будут подозревать реактивацию ЦМВ в первые недели беременности (или предполагаемой беременности) свечки виферон во взрослой дозировке курсом (по инструкции) и местно что-то типа эпигена в спрее. Но не более.

Меня взяли в программу и сделали первый укол для стимуляции, на следующей неделе мне идти к ним на мониторинг, но после первого приёма и вступления в программу я получила после лечения повторный анализ пцр CMV обнаружен. Хотя по крови lg G +, LG M -. Врачи, которые выдали результат, сказали, что может мало времени прошло после окончания курса лечения. Боюсь, что выгонят из протокола. Мужа попросила сдать пцр мазок и кровь, мазок количественный 0, LG g +, LG M -, думаю со всеми этими результами сходить к венерологу, пусть напишет, что все хорошо или то, что лучше отложить протокол.

У меня LG G положительный, LG M отрицательный

Насколько я знаю главное что буква М у вас отрицательно.Я сдавала помоему всё что можно и по несколько раз одно и тоже.Ну у каждого врача свои загоны, поэтому вас и лечат.?

мне ничего не лечили, инфекционист дал заключение что всё хорошо, Я их переболела


А пцр вы сдавали?



Это обычная лихорадка(герпес), если есть антитела, значит вы переболели им.
Че они пытаются вылечить то, не понятно

Я уже не знаю как найти в себе терпение с этими врачами, пришла с этими результатами к гинекологу, она мне мол мы с такими результатами не лечим даже, я ей, а как я на ЭКО пойду, если Пцр выявил, что обнаружено, она мне прописала все эти медикаменты, пришла вступать в протокол и говорю ей повторный анализ сдала, он будет готов только завтра, она меня включила в протокол, сделали первый укол, и вот мне идти на следующий неделе на мониторинг, а пцр показал обнаружено, репродуктолог меня может выгнать, вот думаю сходить к инфекционисту, может даст заключение, что это не страшно

А что такое лихорадка герпес?



это то что появляется на губе, когда заболеваете

На губе у меня был, я пролечила ацикловиром, а вот почему пцр положительный непонятно



Антитела IgM
Их концентрация повышается вскоре после заболевания. Антитела IgM определяются уже через 5 дней после его начала и достигают пика в промежутке от одной до четырех недель, затем снижаются до диагностически незначительных уровней в течение нескольких месяцев даже без проведенного лечения. Однако, для полной диагностики недостаточно определения только антител класса М: отсутствие этого класса антител еще не говорит об отсутствии заболевания. Острой формы заболевания нет, но может быть хроническая.
Антитела IgM имеют большое значение в диагностике гепатита А и детских инфекций (краснуха, коклюш, ветрянка), легко передающихся воздушно-капельным путем, так как важно как можно раньше выявить заболевание и изолировать заболевшего.
Антитела IgG
Основная роль антител IgG — это длительная защита организма от большинства бактерий и вирусов — хотя их выработка происходит более медленно, но ответ на антигенный раздражитель сохраняется более устойчивым, чем у антител класса IgM.
Уровни антител IgG повышаются медленнее (через 15-20 дней после начала заболевания), чем IgM, но остаются повышенными дольше, поэтому могут показывать давно текущую инфекцию при отсутствии IgM АТ. IgG могут находиться на низком уровне в течение многих лет, но, при повторном воздействии того же антигена, уровень антител IgG быстро повышается.
РЦРЗ (Республиканский центр развития здравоохранения МЗ РК)
Версия: Клинические протоколы МЗ РК - 2015
Общая информация
Цитомегаловирусная инфекция (синонимы: цитомегалия, вирусная болезнь слюнных желез, инклюзионная цитомегалия, болезнь с включениями; salivarygland virus disease – англ.) хроническая антропонозная болезнь вирусной этиологии, характеризующаяся многообразием форм патологического процесса от латентной инфекции до клинически выраженного генерализованного заболевания [1,2].
Класс III – имеющиеся данные или общее мнение свидетельствует о том, что лечение неполезно/ неэффективно и в некоторых случаях может быть вредным
| А | Высококачественный мета-анализ, систематический обзор РКИ или крупное РКИ с очень низкой вероятностью (++) систематической ошибки результаты которых могут быть распространены на соответствующую популяцию. |
| В | Высококачественный (++) систематический обзор когортных или исследований случай-контроль или Высококачественное (++) когортное или исследований случай-контроль с очень низким риском систематической ошибки или РКИ с невысоким (+) риском систематической ошибки, результаты которых могут быть распространены на соответствующую популяцию. |
| С | |
| D | Описание серии случаев или неконтролируемое исследование или мнение экспертов. |
| GPP | Наилучшая фармацевтическая практика. |


Классификация
Диагностика
II. МЕТОДЫ, ПОДХОДЫ И ПРОЦЕДУРЫ ДИАГНОСТИКИ И ЛЕЧЕНИЯ
Минимальный перечень обследования, который необходимо провести при направлении на плановую госпитализацию: согласно внутреннему регламенту стационара с учетом действующего приказа уполномоченного органа в области здравоохранения.
Диагностические мероприятия, проводимые на этапе скорой неотложной помощи: не проводятся.
У ВИЧ-инфицированных в 3 и 4 стадии: клиника манифестных форм с поражением легких, ЦНС, глаз (ретинит), ЖКТ, печени.
Иммунограмма: снижение CD4+, CD8+, снижение CD4\CD8.
Дифференциальный диагноз
Алгоритм дифференциальной диагностики при цитомегаловирусной болезни


Лечение
Диета: стол № 15 с коррекцией в зависимости от клинической формы.
• меглюмина акридонацетат в таблетках: по 0,45 г (3 табл.) на прием 1 раз в сутки per os по схеме 1,2,4,6,8,11,14,17,21,23 дни., в инъекциях 12,5% - 2 мл в/м, 1 раз №10.
Латентная ЦМВИ: лечение не проводится.
• Панавир 0,004% раствор 5 мл в/в медленно №5 по схеме три инъекции с интервалом 48 часов, две последующие – с интервалом 72 часа и суппозитории ректальные Панавир 200 мкг, по 1 свече на ночь 3-х кратно в течении 1-ой недели с интервалом 48 часов и 2-х кратно в течении 2-ой недели с интервалом 72 часа. Курс лечения 11 дней.
• Валганцикловир 900 мг в сутки или Ганцикловир 5 мг/кг/сутки в течение месяца, перенёсшим ЦМВ – ретинит на фоне ВААРТ до повышения CD4 – лимфоцитов более 100 кл/мкл, сохраняющегося не менее 3 месяцев. Поддерживающий курс у этих больных при других манифестных формах ЦМВИ должен быть не менее одного месяца.
С десенсибилизирующей, противотёчной, противовоспалительной целью при генерализованной ЦМВИ с поражением ЦНС: кортикостероидные препараты: преднизолон 2-5 мг\кг в сутки;
• Рингер раствор для инфузий, 200 мл и 400мл;
Страшный нестрашный цитомегаловирус
Цитомегаловирусная инфекция - коротко
Цитомегаловирус (ЦМВ) очень распространен, заразиться им может любой человек. Большая часть людей переносит ЦМВ инфекцию бессимптомно, даже на зная о ней. Цитомегловирс опасен для беременных и для больных с ослабленной иммунной системой.
После эпизода заражения ЦМВ вирус остается в организме пожизненно. Цитомегаловирус распространяется с биологическими жидкостями: с кровью, слюной, мочой, спермой и грудным молоком.
Если ЦМВ инфекцией заражается беременная, до того не болевшая ЦМВ, то вирус может вызвать проблемы у нерожденного ребенка.
ЦМВ невозможно полностью устранить из организма, однако с помощью современных противовирусных антибиотиков возможно облегчить протекание инфекции.
Симптомы цитомегаловирусной инфекции
Большая часть людей с нормальной иммунной системой переносят ЦМВ инфекцию легко, либо вообще без симптомов. В некоторых случаях после первого контакта с ЦМВ у взрослых развивается заболевание, напоминающее мононуклеоз со следующими симптомами:
- слабость и упадок сил
- ночные поты
- подъем температуры
- увеличение лимфоузлов
- боль в горле
- потеря аппетита
- боли в суставах и мышцах
Диагноз часто трудно поставить, руководствуясь одними симптомами, т.к. они быстро исчезают (к счастью) и довольно неспецифичны (т.е. встречаются и при других заболеваниех, не только при ЦМВ инфекции).
У взрослых больных с ослабленной иммунной системой ЦМВ может особенно тяжело поражать некоторые органы:
- глаза (нарушение зрения и слепота)
- легкие
- желудочно-кишечный тракт (диаррея и внутренние кровотечения)
- печень (гепатит)
- мозг (энцефалит, нарушение поведения, судороги и кома)
Если ЦМВ впервые заболевает беременная, инфекция может поразить и нерожденного ребенка, т.к. ЦМВ проходит через плаценту. К счастью симптомы ЦМВ инфекции проявляются только у 1% зараженных детей при рождении, но если уж симптомы есть, обычно болезнь протекает тяжело и могут привести к инвалидизации.
Часто ЦМВ инфекция не проявляется не при рождении, а спустя несколько месяцев после, чаще всего — глухотой. В небольшом проценте случаев возникает слепота.
В целом, у большинства младенцев с врожденной ЦМВ инфекцией никаких симптомов не возникает.
Симптомы ЦМВ инфекции, проявляющиеся сразу после рождения:
- желтуха
- сыпь на коже
- низкий вес
- увеличение селезенки
- увеличение печени, дисфункция печени
- пневмония
- судороги
Осложнения врожденной ЦМВ инфекции:
- глухота
- проблемы со зрением (потеря центрального зрения, рубцы на сетчатке, увеит)
- нарушения психики
- синдром дефицита внимания
- аутизм
- нарушения координации
- малая окружность головы
- судорожный синдром
Когда обращаться к врачу
Лицам с иммунодефицитом (рак, СПИД, принимающим иммуносупрессанты и кортикостероиды) и беременным при появлении симптомов, напоминающих мононуклеоз (см. список симптомов выше) нужно обратиться к врачу.
Во время ведения беременности акушеры гинекологи проверяют иммунный статус беременной — есть ли у нее иммунитет против цитомегаловируса или нет (есть ли в крови anti-CMV IgG).
Цитомегаловирусная инфекция - подробнее
Заражение может происходить следующими путями:
при касании глаз или слизистой оболочки носа или рта рукой, если на кожу пальцев попали частички зараженной биологической жидкости (отсюда важность тщательного мытья рук!).
- при половом контакте
- мать может передать ребенку инфекцию через грудное молоко.
- через переливание крови или пересадку органов
- заражение плода при заболевании матери
Распространенность цитомегаловируса
ЦМВ широко распространен. К возрасту 40 лет 50-80% населения уже заражены ЦМВ.
Осложнения цитомегаловирусной инфекции
Иногда ЦМВ инфекция вызывает серьезные осложнения даже у человека с нормальной иммунной системой:
- ЦМВ мононуклеоз. Картина заболевания напоминает классический мононуклеоз, который вызываер вирус Эпштейна-Барра (ВЭБ).
- Кишечные осложнения: диаррея, боль в животе, воспаление кишечника, кровь в стуле
- Печеночные осложнения. Гепатит, повышение ферментов печени (АЛТ и АСТ), повышение температуры.
- Неврологические осложнения. Встречаются они относительно редко, но спектр их очень разнообразен. Главное неврологические осложенение — воспаление мозга (энцефалит).
- Легочные осложнения. Пневмонит.
Диагностика ЦМВ
Симптомы ЦМВ инфекции не очень специфичны, поэтому требуется лабораторное подтверждение.
Самый распространенный анализ — антитела к ЦМВ.
Наличие антител класса М (IgM, anti-CMV IgM) говорит об острой инфекции.
Если IgM антител нет, а есть только IgG антитела, то это говорит о перенесенной в прошлом ЦМВ инфекции и о наличии иммунитета к ней.
Во время обострения цитомегаловирус также можно обнаружить в биологических жидкостях с помощью полимеразной цепной реакции (ПЦР) — очень точного и чувствительного анализа.
Про тестирование беременных на ЦМВ я уже написал выше.
Лечение цитомегаловирусной инфекции
Совсем устранить ЦМВ из организма невозможно, да — в случае людей с нормальной иммунной системой — и не нужно.
Новорожденным с ЦМВ и больным с ослабленным иммунитетом вводят специальные противовирусные антибиотики
- ганцикловир
- фоскарнет
- ацикловир
- цидофовир (cidofovir)
Профилактика ЦМВ
Профилактика ЦМВ инфекции особенно важна для беременных, не имеющих противоЦМВ иммунитета и для больных с ослабленной иммунной системой.
- тщательное мыть рук с мылом. Мыть руки надо миниму 15-20 секунд, особенно если у вас был контакт с биологическими жидкостями.
- избегайте контакта со слюной. Например, когда целуете ребенка, не целуйте его в губы, а в щеку.
- не используйте общую посуду, посуда у вас должна быть отдельная!
- помните также и о половом пути передачи вируса!
- больным с тяжелым иммунодефицитом может быть показан профилактический прием противовирусных препаратов.
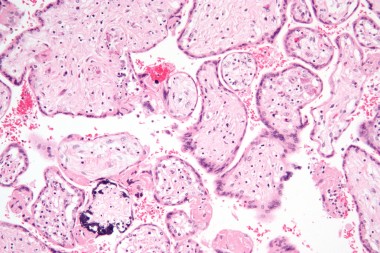
В статье проанализированы опубликованные данные по вопросам адекватной диагностики антенатальной и постнатальной цитомегаловирусной инфекции (ЦМВИ), а также лечению острых ЦМВИ у беременной, плода и новорожденного. Представлены отечественные клинические р
The article gives analysis of the data on the issues of relevance of diagnostics of antenatal and postnatal cytomegaloviral infection (CMVI), as well as treatment of acute CMVI in the pregnant, fetus and newborns. National clinical guidelines on diagnostics and treatment of congenital CMVI developed by the Russian Association of antenatal medicine in 2016, were presented; as well as the first unofficial international guidelines on the issues of diagnostics and treatment of congenital CMVI.
Цитомегаловирус (ЦМВ) — чрезвычайно распространенный вирус, поражающий людей всех возрастов и формирующий пожизненную персистенцию в организме инфицированного человека. Считается, что в большинстве случаев персистенция начинается в ранние годы жизни и протекает латентно, не оказывая выраженного патологического влияния на состояние здоровья инфицированного. С другой стороны, доказано, что персистенция вируса может сопровождаться хроническим воспалением, формировать разнообразные многочисленные иммунные дисфункции и определять развитие вторичных иммунных, аутоиммунных и дегенеративных нарушений. Различного рода иммунокомпрометации могут приводить к рецидивам размножения вируса и многообразным клиническим проявлениям с поражением любых органов и систем в любом возрасте.
Особое значение имеют врожденные инфекции детей, которые отличаются высоким риском развития тяжелых генерализованных форм и инвалидизирующих исходов заболевания, таких как потеря слуха, зрения, умственная отсталость, микроцефалия, судорожный синдром и пр. Такие пожизненные проблемы со здоровьем развиваются примерно у каждого пятого ребенка с врожденной цитомегаловирусной инфекцией (ЦМВИ), что определяет потребность в своевременном пренатальном выявлении беременных и плодов с высоким риском развития врожденной ЦМВИ и ранней диагностике и лечении инфекций у новорожденных.
Теоретические дискуссии по вопросам адекватной диагностики антенатальной и постнатальной ЦМВИ, а также лечению острых ЦМВИ у беременной, плода и новорожденного продолжаются с 1990-х гг., но отсутствие единых руководящих принципов затрудняет практическую работу врачей. Российской ассоциацией специалистов перинатальной медицины в 2016 г. выработаны отечественные клинические рекомендации по диагностике и лечению врожденной ЦМВИ. Созданная в рамках 5-й Международной конференции по ЦМВИ (Брисбен, Австралия, 19 апреля 2015) международная группа экспертов на основе консенсусных дискуссий и обзора литературы выработала первые неофициальные международные рекомендации по вопросам диагностики и лечения врожденной ЦМВИ, которые опубликованы в Lancet Infect Dis в марте 2017. Все эти рекомендации будут нуждаться в постоянном обновлении по мере поступления дополнительных данных.
ЦМВ — двухцепочечный ДНК-вирус, член семейства герпес-вирусов (β-герпесвирус человека). Синтез вирусного генома ДНК происходит в ядре клетки-хозяина. Исследования последних лет подтверждают гипотезу о том, что штаммы ЦМВ могут варьировать в их вирулентности, тропизме и патогенном потенциале, который, в свою очередь, вероятно, связан с генетической изменчивостью ключевых для патогенеза генов. Внешняя оболочка вируса содержит множественные гликопротеины, кодируемые вирусом. Гликопротеин B и гликопротеин H, по-видимому, являются основными факторами для формирования гуморального иммунитета — антитела к ним способны нейтрализовать вирус. Эти гликопротеины используют сегодня при разработке анти-ЦМВ-вакцин [3].
Вирус распространяется различными способами: через продукты крови (переливание, трансплантация органов), грудное вскармливание, пролиферацию в местах контактов (кожа, любые слизистые оболочки), перинатально и половым путем. ЦМВИ может протекать в виде первичной инфекции ранее неинфицированных (серонегативных) пациентов, реинфекции или реактивации у инфицированных (серопозитивных) людей; может вызывать острое, латентное и хроническое течение врожденных или приобретенных форм болезни [4].
При острой ЦМВ-инфекции могут поражаться практически все типы клеток человеческого организма — эндотелиальные клетки, эпителиальные клетки, клетки гладкой мускулатуры, фибробласты, нейронные клетки, гепатоциты, трофобласты, моноциты/макрофаги, дендритные клетки и пр. Все типы клеток поражаются и в мозге: нейроны, астроциты, клетки эпендимы, выстилающие желудочки, макроглия, эндотелий капилляров, оболочек, микроглия, сплетения сосудистой оболочки, дендриты и аксоны — т. е. вирус в мозге не имеет избирательной клеточной цели, что объясняет многообразие клинических форм поражения нервной системы у больных [5].
Считается, что ЦМВ реплицируется в эндотелиальных клетках с низкой скоростью, вызывая преимущественно подострые инфекции, однако истинная скорость репликации вируса в клетках определяется эффективностью цитотоксического Т-клеточного иммунитета и степенью иммуносупрессии хозяина. Так, например, на моделях ЦМВИ у животных продемонстрировано, что отсутствие CD4 Т-клеток сопровождалось более тяжелым и стремительным заболеванием ЦМВИ. Известно также, что ВИЧ-инфицированные новорожденные имеют очень высокую частоту врожденной ЦМВИ с высоким риском смерти, неврологических дефектов и прогрессии ВИЧ-инфекции [6–7].
Особое свойство ЦМВИ — способность вызывать депрессию практически всех звеньев иммунитета, резко угнетать продукцию интерферонов (ИНФ), в первую очередь ИНФ-α. Внедрение ЦМВ приводит к иммунной перестройке в виде снижения реакции лимфоцитов на вирусы в связи с угнетением экспрессии антигена макрофагами, подавлением пролиферативной активности лимфоцитов (что коррелирует с тяжестью болезни), угнетением фагоцитарной активности и завершенности фагоцитоза [7].
Доказано, что и первичные и латентные ЦМВИ сами могут индуцировать хронические воспалительные системные реакции с устойчивой иммунной активацией, запускать и поддерживать аутоиммунные процессы, усиливать аллореактивность Т-клеток после трансплантации и, возможно, участвовать в комплексе причин повышения частоты нейродегенеративных состояний с возрастом человека (Jones R. P. The debility cascade in neurological degenerative disease). Установлено также, что ЦМВ-индуцированные иммунные изменения в пожилом возрасте могут отвечать, например, за замедленную элиминацию вируса гриппа из легких, сниженный поствакцинальный иммунитет на гриппозные вакцины, измененную реакцию организма на терапию интерферонами [8].
Многие годы риск развития врожденных инфекций плода ассоциировали преимущественно с первичной инфекцией матери, однако к настоящему моменту не вызывает сомнения, что большая доля врожденных ЦМВИ (до 75%) встречается в условиях рецидивирующей во время беременности материнской инфекции. Допускаются также и экзогенные реинфекции с новыми штаммами ЦМВ — доказательства основываются на молекулярных данных, подтверждающих получение нового штамма вируса.
Вместе с тем степень риска вертикального инфицирования плода в условиях первичной инфекции матери рассматривают по-прежнему как чрезвычайно высокую — в 30–50% случаев острой первичной инфекции беременной развивается врожденная инфекция ребенка. Показано, что ранее существовавший материнский иммунитет хоть и не гарантирует полной защиты, тем не менее обеспечивает снижение риска врожденной ЦМВИ при следующих беременностях на 69% [9].
Недавними исследованиями установлено, что ЦМВ может поражать амниотическую мембрану, ухудшая цитотрофобласт-индуцированный лимфангиогенез и ремоделирование сосудов в плаценте и задерживая правильное развитие клеток — предшественников трофобласта, одновременно вызывает врожденную провоспалительную иммунную реакцию. Это приводит к гипоксии плода, задержке внутриутробного развития и возможным последующим гипоксическим повреждениям головного мозга. Степень поражения плода определяется сроками антенатального инфицирования и вирусной нагрузкой в размножающихся клетках — чем меньше гестационный возраст, тем более выражена альтерация (разрушение) тканей с формированием пороков развития [10]. Особенно быстро ЦМВ достигает максимума в астроцитарных и глиальных клетках, при этом максимальная экспрессия вируса найдена в глиальных клетках развивающегося мозга мышат (что объясняет микрогирию, микроцефалию и другие пороки ЦМВ-инфицированного мозга детей). По мере увеличения срока гестации в клинической картине инфекционного заболевания плода преобладают симптомы системного воспаления с выраженной пролиферацией и экссудацией. У 1/3 умерших от ЦМВИ новорожденных (из них 60% — недоношенные) при морфологическом исследовании выявляют различные пороки развития. У 43% — признаки генерализованной внутриутробной инфекции с геморрагическими и ишемическими инфарктами (в том числе в головном и спинном мозге) [11].
Способность вируса реплицироваться в любых клетках человеческого организма определяет многообразие клинических форм болезни; ЦМВ может вызывать как генерализованные инфекции, так и поражения отдельных органов: печени, головного мозга, сердца, легких, мочеполовых органов, желудочно-кишечного тракта и др.
У беременных острая первичная ЦМВИ протекает чаще бессимптомно (25–50%) или малосимптомно — с неспецифическими проявлениями (обычно лихорадка, астения и головная боль).
Как первичная, так и рецидивирующая ЦМВИ матери может стать причиной антенатальных ультразвуковых признаков поражения плода в результате трансплацентарной инфекции. Самые частые УЗИ-признаки: задержка роста плода, вентрикуломегалия, микроцефалия, перивентрикулярная гиперэхогенность, кальцификаты в мозге, плевральный выпот или асцит, гепатоспленомегалия, гиперэхогенный кишечник и мекониальный илеус и др. Эти УЗИ-аномалии эмбриона прогнозируют тяжелую генерализованную манифестную врожденную ЦМВИ новорожденного с высоким риском формирования инвалидизирующих исходов болезни и смерти. Поэтому первичная острая ЦМВИ во время беременности может являться показанием к ее искусственному прерыванию. Установлено, что около 4% детей с антенатальной ЦМВИ умрут в утробе матери или вскоре после рождения, среди остальных около 60% будут иметь когнитивные дефекты, нейросенсорную потерю слуха и другие неврологические и прочие проблемы [11–12].
Сегодня установлено также, что нейросенсорная тугоухость является прогрессирующим заболеванием и может формироваться в течение 5–6 лет жизни даже у детей, родившихся с бессимптомной ЦМВИ (это связывают с многолетней репликацией ЦМВ в перилимфе), что требует соответствующей длительности наблюдения ребенка.
При инфицировании в поздние сроки гестации ЦМВИ у новорожденного может проявляться и как генерализованная инфекция, и как поражение отдельных органов с нетяжелыми транзиторными симптомами болезни, например, умеренной гепатомегалией, изолированным снижением количества тромбоцитов или повышенным уровнем аланинаминотрансферазы. Возможна и клинически бессимптомная ЦМВИ с изолированной нейросенсорной тугоухостью.
У 10% всех новорожденных в течение первого месяца жизни возникают инфекционные заболевания в результате в основном семейных контактов, в том числе грудного вскармливания. Экскреция ЦМВ с грудным молоком в течение первых недель после родов бывает низкой, достигает максимума к 4–8 неделям, завершается к 9–12 неделям. Считается, что риск трансмиссии вируса коррелирует с вирусной нагрузкой в молоке, передача максимальна при высокой экскреции. У доношенных детей в результате инфицирования ЦМВ через молоко матери формируется, как правило, субклиническое течение инфекции без остаточных явлений; в клинической картине более вероятно развитие энтероколита и транзиторного холестатического гепатита с минимальным цитолизом. Недоношенные дети (вес
И. Я. Извекова 1 , доктор медицинских наук, профессор
М. А. Михайленко
Е. И. Краснова, доктор медицинских наук, профессор
ФГБОУ ВО НГМУ МЗ РФ, Новосибирск
Цитомегаловирусная инфекция в практике врача: современный алгоритм диагностики и лечения/ И. Я. Извекова, М. А. Михайленко, Е. И. Краснова
Для цитирования: Лечащий врач № 4/2018; Номера страниц в выпуске: 90-95
Теги: новорожденные, беременность, инфекция, персистирование
Читайте также:
- Как избежать вируса папилломы человека
- От гриппа осельтамивир или занамивир
- Вирусы в школах меры предосторожности
- Появился не понятный вирус
- Кому назначается лечение от гепатита с
 Пожалуйста, не занимайтесь самолечением!При симпотмах заболевания - обратитесь к врачу.
Пожалуйста, не занимайтесь самолечением!При симпотмах заболевания - обратитесь к врачу.

