Поражение нервной системы при цитомегаловирусе
Цитомегаловирусная инфекция (ЦМВИ) наиболее часто возникает у пациентов с нарушениями иммунологического статуса, например, у ВИЧ-инфицированных или на фоне иммуносупрессивной терапии пациентов, перенесших операции трансплантации органов. Поражение ЦНС является наиболее редкой формой ЦМВИ, но с наиболее неблагоприятным прогнозом. В случае ЦМВ энцефалита или миелита специфическое лечение необходимо начинать как можно быстрее. На настоящее время не существует международно признанных подходов к лечению, международные руководства рекомендуют ганцикловир и фоскарнет в качестве препаратов выбора. Они обладают сходной эффективностью и оба хорошо проникают в ЦНС, однако имеющихся на настоящий момент данных контролируемых клинических исследований недостаточно для окончательных выводов об эффективности подобной терапии недостаточно.
В группу риска в отношении развития цитомегаловирусной инфекции входят ВИЧ-инфицированные, пациенты, перенесшие трансплантацию органов, костного мозга или клеток периферической крови. У этих пациентов в состоянии иммуносупрессии может проявиться латентная ЦМВИ, однако чаще клиническая картина развивается при первичном инфицировании. При этом могут поражаться самые разные органы, причем инфекция ЦНС занимает последнее место по частоте возникновения.
Формы проявления цитомегаловирусной инфекции с поражением ЦНС могут быть различны. Она может проявляться энцефалитом, менингоэнцефалитом, вентрикулоэнцефалитом и миелорадикулитом. Прогноз зависит от клинических проявлений, так, при миелитах он носит более благоприятный характер, чем в случае энцефалита.
Изучение эффективности и безопасности противовирусных препаратов для лечения цитомегаловирусной инфекции до настоящего времени проводилось только в рамках клинических исследований у пациентов с ЦМВ ретинитами и колитами, так как число пациентов с диагнозом ЦМВ инфекции ЦНС, установленным на ранней стадии заболевания либо прижизненно, невелико.
Изучаемые противовирусные препараты для специфической терапии цитомегаловирусной инфекции (ганцикловир, фоскарнет и цидофовир) обладают вирусостатическим действием, а поэтому не вызывают элиминации вируса, репликация которого может восстанавливаться после окончания курса терапии.
Известно, что ганцикловир эффективен у пациентов с ВИЧ-ассоциированными ЦМВ ретинитами и колитами. Кроме того, препарат предотвращает манифестацию инфекции у пациентов после трансплантации. При этом у некоторых штаммов ЦМВ отмечается резистентность к ганцикловиру, которая может встречаться и при отсутствии предшествующего лечения данным препаратом. Фоскарнет обладает сходной эффективностью при ЦМВ ретинитах и ЦМВ антигенемии после аллогенного замещения периферической крови. Оба препарата хорошо проникают через ГЭБ и обнаруживаются в спинномозговой жидкости в концентрациях 27-64% и 13-68% от их содержания в плазме крови, соответственно.
Результаты исследований показывают, что названные препараты могут быть эффективны в качестве моно- или комбинированной терапии для лечения ЦМВ миелитов и энцефалитов у пациентов с иммуносупрессией в 74% случаев, но при этом средняя продолжительность жизни пациентов после постановки диагноза ЦМВ поражения ЦНС составляет всего лишь около 3 месяцев. В целом, наряду с заметным улучшением состояния пациентов с ЦМВ инфекцией ЦНС, прогноз в большинстве случаев неблагоприятен, особенно это характерно для ВИЧ-инфицированных пациентов.
Цидофовир - новейший противовирусный препарат с активностью против ЦМВ, который по результатам клинических исследований оказался эффективным для лечения поздних и рецидивирующих ЦМВ ретинитов. Соотношение концентраций данного препарата в плазме и в ликворе в настоящее время не известно.
Специфическую терапию при энцефалитах и миелитах необходимо начинать по возможности быстро. В соответствии с рекомендациями Международного общества по СПИДу и Европейской экспертной группы, лечение ВИЧ-инфицированных пациентов с ЦМВ поражением ЦНС необходимо начинать с назначения ганцикловира и фоскарнета, так как они хорошо проникают в ЦНС и в целом эффективны.
Выбор между ганцикловиром и фоскарнетом определяется показателями анализа крови пациентов и состоянием функции почек. Комбинированную терапию данными препаратами целесообразно назначать пациентам, получавших ранее противовирусную терапию, а также в случаях прогрессирования заболевания на фоне монотерапии одним из препаратов. Фоскарнет назначают в/в при выраженной нейтропении или тромбоцитопении, а ганцикловир показан пациентам с нарушениями функции почек, а также получающим сопутствующую терапию гепатотоксичными препаратами. Пациентам, ранее получавшим противовирусную терапию, направленную против ЦМВ, показано назначение комбинации ганцикловира с фоскарнетом из-за возможности у них инфекции резистентными штаммами ЦМВ.
Цидофовир был предложен в качестве препарата второго ряда при неэффективности лечения комбинацией ганцикловира с фоскарнетом. На сегодняшний день этот препарат еще недостаточно изучен и его применение окончательно не одобрено.
В настоящее время проводятся исследования новых противовирусных препаратов для лечения цитомегаловирусной инфекции, таких как валганцикловир, томегловир, марибавир и др.
Наряду с применением препаратов, активных против ЦМВ, у ВИЧ-инфицированных пациентов требуется и высокоактивная антиретровирусная терапия, которая не только действует на ВИЧ, но и улучшает прогноз благодаря восстановлению нарушенных иммунологических показателей. Иммунокомпетентным пациентам с поперечным миелитом показано назначение короткого курса кортикостероидов.
Поддерживающая терапия назначается при улучшении или стабилизации процесса и продолжается до восстановления иммунологических показателей (содержание CD4 клеток >100-150/мл в течение 6 месяцев) у пациентов с ВИЧ или до отмены иммуносупрессивных препаратов у пациентов, перенсших трансплантацию органов. Необходимость проведения поддерживающей терапии у иммунокомпетентных пациентов в настоящее время не изучена.
Cytomegalovirus infection of the CNS is most common in immunocompromised patients.
цитомегаловирус, ЦМВ, цитомегаловирусная инфекция, ЦМВИ, поражение центральной нервной системы (ЦНС), противовирусная терапия, ВИЧ-инфицированные пациенты, пациенты с иммунодефицитами, ганцикловир, фоскарнет
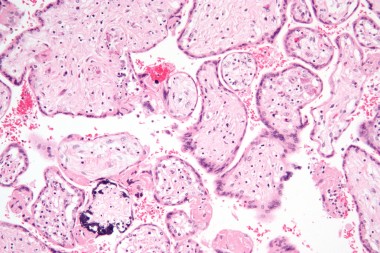
В статье проанализированы опубликованные данные по вопросам адекватной диагностики антенатальной и постнатальной цитомегаловирусной инфекции (ЦМВИ), а также лечению острых ЦМВИ у беременной, плода и новорожденного. Представлены отечественные клинические р
The article gives analysis of the data on the issues of relevance of diagnostics of antenatal and postnatal cytomegaloviral infection (CMVI), as well as treatment of acute CMVI in the pregnant, fetus and newborns. National clinical guidelines on diagnostics and treatment of congenital CMVI developed by the Russian Association of antenatal medicine in 2016, were presented; as well as the first unofficial international guidelines on the issues of diagnostics and treatment of congenital CMVI.
Цитомегаловирус (ЦМВ) — чрезвычайно распространенный вирус, поражающий людей всех возрастов и формирующий пожизненную персистенцию в организме инфицированного человека. Считается, что в большинстве случаев персистенция начинается в ранние годы жизни и протекает латентно, не оказывая выраженного патологического влияния на состояние здоровья инфицированного. С другой стороны, доказано, что персистенция вируса может сопровождаться хроническим воспалением, формировать разнообразные многочисленные иммунные дисфункции и определять развитие вторичных иммунных, аутоиммунных и дегенеративных нарушений. Различного рода иммунокомпрометации могут приводить к рецидивам размножения вируса и многообразным клиническим проявлениям с поражением любых органов и систем в любом возрасте.
Особое значение имеют врожденные инфекции детей, которые отличаются высоким риском развития тяжелых генерализованных форм и инвалидизирующих исходов заболевания, таких как потеря слуха, зрения, умственная отсталость, микроцефалия, судорожный синдром и пр. Такие пожизненные проблемы со здоровьем развиваются примерно у каждого пятого ребенка с врожденной цитомегаловирусной инфекцией (ЦМВИ), что определяет потребность в своевременном пренатальном выявлении беременных и плодов с высоким риском развития врожденной ЦМВИ и ранней диагностике и лечении инфекций у новорожденных.
Теоретические дискуссии по вопросам адекватной диагностики антенатальной и постнатальной ЦМВИ, а также лечению острых ЦМВИ у беременной, плода и новорожденного продолжаются с 1990-х гг., но отсутствие единых руководящих принципов затрудняет практическую работу врачей. Российской ассоциацией специалистов перинатальной медицины в 2016 г. выработаны отечественные клинические рекомендации по диагностике и лечению врожденной ЦМВИ. Созданная в рамках 5-й Международной конференции по ЦМВИ (Брисбен, Австралия, 19 апреля 2015) международная группа экспертов на основе консенсусных дискуссий и обзора литературы выработала первые неофициальные международные рекомендации по вопросам диагностики и лечения врожденной ЦМВИ, которые опубликованы в Lancet Infect Dis в марте 2017. Все эти рекомендации будут нуждаться в постоянном обновлении по мере поступления дополнительных данных.
ЦМВ — двухцепочечный ДНК-вирус, член семейства герпес-вирусов (β-герпесвирус человека). Синтез вирусного генома ДНК происходит в ядре клетки-хозяина. Исследования последних лет подтверждают гипотезу о том, что штаммы ЦМВ могут варьировать в их вирулентности, тропизме и патогенном потенциале, который, в свою очередь, вероятно, связан с генетической изменчивостью ключевых для патогенеза генов. Внешняя оболочка вируса содержит множественные гликопротеины, кодируемые вирусом. Гликопротеин B и гликопротеин H, по-видимому, являются основными факторами для формирования гуморального иммунитета — антитела к ним способны нейтрализовать вирус. Эти гликопротеины используют сегодня при разработке анти-ЦМВ-вакцин [3].
Вирус распространяется различными способами: через продукты крови (переливание, трансплантация органов), грудное вскармливание, пролиферацию в местах контактов (кожа, любые слизистые оболочки), перинатально и половым путем. ЦМВИ может протекать в виде первичной инфекции ранее неинфицированных (серонегативных) пациентов, реинфекции или реактивации у инфицированных (серопозитивных) людей; может вызывать острое, латентное и хроническое течение врожденных или приобретенных форм болезни [4].
При острой ЦМВ-инфекции могут поражаться практически все типы клеток человеческого организма — эндотелиальные клетки, эпителиальные клетки, клетки гладкой мускулатуры, фибробласты, нейронные клетки, гепатоциты, трофобласты, моноциты/макрофаги, дендритные клетки и пр. Все типы клеток поражаются и в мозге: нейроны, астроциты, клетки эпендимы, выстилающие желудочки, макроглия, эндотелий капилляров, оболочек, микроглия, сплетения сосудистой оболочки, дендриты и аксоны — т. е. вирус в мозге не имеет избирательной клеточной цели, что объясняет многообразие клинических форм поражения нервной системы у больных [5].
Считается, что ЦМВ реплицируется в эндотелиальных клетках с низкой скоростью, вызывая преимущественно подострые инфекции, однако истинная скорость репликации вируса в клетках определяется эффективностью цитотоксического Т-клеточного иммунитета и степенью иммуносупрессии хозяина. Так, например, на моделях ЦМВИ у животных продемонстрировано, что отсутствие CD4 Т-клеток сопровождалось более тяжелым и стремительным заболеванием ЦМВИ. Известно также, что ВИЧ-инфицированные новорожденные имеют очень высокую частоту врожденной ЦМВИ с высоким риском смерти, неврологических дефектов и прогрессии ВИЧ-инфекции [6–7].
Особое свойство ЦМВИ — способность вызывать депрессию практически всех звеньев иммунитета, резко угнетать продукцию интерферонов (ИНФ), в первую очередь ИНФ-α. Внедрение ЦМВ приводит к иммунной перестройке в виде снижения реакции лимфоцитов на вирусы в связи с угнетением экспрессии антигена макрофагами, подавлением пролиферативной активности лимфоцитов (что коррелирует с тяжестью болезни), угнетением фагоцитарной активности и завершенности фагоцитоза [7].
Доказано, что и первичные и латентные ЦМВИ сами могут индуцировать хронические воспалительные системные реакции с устойчивой иммунной активацией, запускать и поддерживать аутоиммунные процессы, усиливать аллореактивность Т-клеток после трансплантации и, возможно, участвовать в комплексе причин повышения частоты нейродегенеративных состояний с возрастом человека (Jones R. P. The debility cascade in neurological degenerative disease). Установлено также, что ЦМВ-индуцированные иммунные изменения в пожилом возрасте могут отвечать, например, за замедленную элиминацию вируса гриппа из легких, сниженный поствакцинальный иммунитет на гриппозные вакцины, измененную реакцию организма на терапию интерферонами [8].
Многие годы риск развития врожденных инфекций плода ассоциировали преимущественно с первичной инфекцией матери, однако к настоящему моменту не вызывает сомнения, что большая доля врожденных ЦМВИ (до 75%) встречается в условиях рецидивирующей во время беременности материнской инфекции. Допускаются также и экзогенные реинфекции с новыми штаммами ЦМВ — доказательства основываются на молекулярных данных, подтверждающих получение нового штамма вируса.
Вместе с тем степень риска вертикального инфицирования плода в условиях первичной инфекции матери рассматривают по-прежнему как чрезвычайно высокую — в 30–50% случаев острой первичной инфекции беременной развивается врожденная инфекция ребенка. Показано, что ранее существовавший материнский иммунитет хоть и не гарантирует полной защиты, тем не менее обеспечивает снижение риска врожденной ЦМВИ при следующих беременностях на 69% [9].
Недавними исследованиями установлено, что ЦМВ может поражать амниотическую мембрану, ухудшая цитотрофобласт-индуцированный лимфангиогенез и ремоделирование сосудов в плаценте и задерживая правильное развитие клеток — предшественников трофобласта, одновременно вызывает врожденную провоспалительную иммунную реакцию. Это приводит к гипоксии плода, задержке внутриутробного развития и возможным последующим гипоксическим повреждениям головного мозга. Степень поражения плода определяется сроками антенатального инфицирования и вирусной нагрузкой в размножающихся клетках — чем меньше гестационный возраст, тем более выражена альтерация (разрушение) тканей с формированием пороков развития [10]. Особенно быстро ЦМВ достигает максимума в астроцитарных и глиальных клетках, при этом максимальная экспрессия вируса найдена в глиальных клетках развивающегося мозга мышат (что объясняет микрогирию, микроцефалию и другие пороки ЦМВ-инфицированного мозга детей). По мере увеличения срока гестации в клинической картине инфекционного заболевания плода преобладают симптомы системного воспаления с выраженной пролиферацией и экссудацией. У 1/3 умерших от ЦМВИ новорожденных (из них 60% — недоношенные) при морфологическом исследовании выявляют различные пороки развития. У 43% — признаки генерализованной внутриутробной инфекции с геморрагическими и ишемическими инфарктами (в том числе в головном и спинном мозге) [11].
Способность вируса реплицироваться в любых клетках человеческого организма определяет многообразие клинических форм болезни; ЦМВ может вызывать как генерализованные инфекции, так и поражения отдельных органов: печени, головного мозга, сердца, легких, мочеполовых органов, желудочно-кишечного тракта и др.
У беременных острая первичная ЦМВИ протекает чаще бессимптомно (25–50%) или малосимптомно — с неспецифическими проявлениями (обычно лихорадка, астения и головная боль).
Как первичная, так и рецидивирующая ЦМВИ матери может стать причиной антенатальных ультразвуковых признаков поражения плода в результате трансплацентарной инфекции. Самые частые УЗИ-признаки: задержка роста плода, вентрикуломегалия, микроцефалия, перивентрикулярная гиперэхогенность, кальцификаты в мозге, плевральный выпот или асцит, гепатоспленомегалия, гиперэхогенный кишечник и мекониальный илеус и др. Эти УЗИ-аномалии эмбриона прогнозируют тяжелую генерализованную манифестную врожденную ЦМВИ новорожденного с высоким риском формирования инвалидизирующих исходов болезни и смерти. Поэтому первичная острая ЦМВИ во время беременности может являться показанием к ее искусственному прерыванию. Установлено, что около 4% детей с антенатальной ЦМВИ умрут в утробе матери или вскоре после рождения, среди остальных около 60% будут иметь когнитивные дефекты, нейросенсорную потерю слуха и другие неврологические и прочие проблемы [11–12].
Сегодня установлено также, что нейросенсорная тугоухость является прогрессирующим заболеванием и может формироваться в течение 5–6 лет жизни даже у детей, родившихся с бессимптомной ЦМВИ (это связывают с многолетней репликацией ЦМВ в перилимфе), что требует соответствующей длительности наблюдения ребенка.
При инфицировании в поздние сроки гестации ЦМВИ у новорожденного может проявляться и как генерализованная инфекция, и как поражение отдельных органов с нетяжелыми транзиторными симптомами болезни, например, умеренной гепатомегалией, изолированным снижением количества тромбоцитов или повышенным уровнем аланинаминотрансферазы. Возможна и клинически бессимптомная ЦМВИ с изолированной нейросенсорной тугоухостью.
У 10% всех новорожденных в течение первого месяца жизни возникают инфекционные заболевания в результате в основном семейных контактов, в том числе грудного вскармливания. Экскреция ЦМВ с грудным молоком в течение первых недель после родов бывает низкой, достигает максимума к 4–8 неделям, завершается к 9–12 неделям. Считается, что риск трансмиссии вируса коррелирует с вирусной нагрузкой в молоке, передача максимальна при высокой экскреции. У доношенных детей в результате инфицирования ЦМВ через молоко матери формируется, как правило, субклиническое течение инфекции без остаточных явлений; в клинической картине более вероятно развитие энтероколита и транзиторного холестатического гепатита с минимальным цитолизом. Недоношенные дети (вес
И. Я. Извекова 1 , доктор медицинских наук, профессор
М. А. Михайленко
Е. И. Краснова, доктор медицинских наук, профессор
ФГБОУ ВО НГМУ МЗ РФ, Новосибирск
Цитомегаловирусная инфекция в практике врача: современный алгоритм диагностики и лечения/ И. Я. Извекова, М. А. Михайленко, Е. И. Краснова
Для цитирования: Лечащий врач № 4/2018; Номера страниц в выпуске: 90-95
Теги: новорожденные, беременность, инфекция, персистирование
1. Течение лейкоэнцефалопатии. ПМЛ встречается примерно у 5% больных СПИДом и у 25% из них является первым проявлением заболевания. ПМЛ — результат реактивации вируса полиомы (JC) из семейства паповавирусов. Он попадает в организм человека вскоре после рождения, но вызывает заболевание только при выраженном иммунодефиците. После появления первых симптомов ПМЛ прогрессирование неизбежно и летальный исход наступает не позднее 6 месяцев. Очень редко заболевание течет несколько медленнее. Описаны единичные случаи спонтанного улучшения.
2. Клиническая картина лейкоэнцефалопатии. У больных отмечается подострое прогрессирующее нарушение когнитивных функций, выпадение полей зрения, гемипарезы, атаксия и нарушения речи. У некоторых больных начало может быть острым, с развитием эпилептических припадков или симптомов, напоминающих инсульт.
3. Диагностика лейкоэнцефалопатии. МРТ-исследование обычно позволяет визуализировать множественные асимметричные очаги в белом веществе головного мозга, которые лучше видны в Т2-режиме. Очаги обычно не накапливают контраст и редко дают масс-эффект. КТ —- менее чувствительный метод, но и он выявляет изменения, напоминающие инфаркты. Нередко на начальных стадиях заболевания определяется только единичный очаг. Для подтверждения диагноза необходимо выявление JC-вируса в олигодендроглиоцитах. ПЦР позволяет определить ДНК вируса в ткани и в ЦСЖ, однако чувствительность и специфичность исследования ЦСЖ еще предстоит определить.
4. Лечени лейкоэнцефалопатии. Не существует средств с доказанной эффективностью для лечения ПМЛ. Описаны единичные случаи некоторого улучшения на фоне антиретровирусной терапии и химиотерапии цитозин-арабинозидом (Ара-С). Исследование эффективности антиретровирусной терапии в сочетании с Ара-С, вводимым внутривенно или интратекально, не выявило достоверной разницы результатов лечения. Показано, что эти виды терапии не способствуют продлению жизни больного (AIDS Clinical Trials Group).

5. Ожидаемый результат лечения лейкоэнцефалопатии. При отсутствии лечения больные ПМЛ обычно живут менее 6 месяцев. Лечение неэффективно. Планируется проведение новых клинических исследований.
1. Течение цитомегаловирусной инфекции. Цитомегаловирус (ЦМ6) попадает в организм человека вскоре после рождения и серологические исследования у большинства взрослых американцев позитивны. Сразу после инфицирования могут наблюдаться транзиторные системные проявления, однако нормальное функционирование иммунной системы препятствует дальнейшим проявлениям. ЦМВ распространяется по организму, попадая в биологические жидкости, и у всех ВИЧ-инфицированных серологические тесты положительны. При СПИДе наиболее часто поражаются желудочно-кишечный тракт и сетчатка. По данным аутопсии у 10—40% больных СПИДом имеет место ЦМВ-поражение головного мозга.
2. Клиническая картина цитомегаловирусной инфекции. ЦМВИ поражает все уровни центральной нервной системы, но чаще всего клинически проявляется тремя следующими синдромами. ЦМВ-энцефалит (ЦМВЭ) характеризуется подостро развивающейся спутанностью сознания, дезориентацией или делирием. У больного нарушаются память, внимание и другие когнитивные функции. Очаговая неврологическая симптоматика представлена нейропатиями черепных нервов, нистагмом, фокальной слабостью, спастикой и атаксией. Может наблюдаться фокальный энцефалит, сопровождающийся симптомами менингита. Симптоматика прогрессирует в течение нескольких недель. ЦМВ-полирадикуломиелит (ЦМВ-ПРМ) характеризуется подостро нарастающими периферическими парезами мышц с арефлексией и нарушением функций тазовых органов (преимущественно задержкой мочи).
Заболевание развивается исподволь, достигая стадии развернутых симптомов только через 1—3 недели. При неврологическом обследовании можно обнаружить нарушения чувствительности, включая болевые парестезии в области промежности и нижних конечностях, а также признаки миелопатии, включая сенсорные расстройства с горизонтальным уровнем и симптом Бабинского. Обычно ЦМВ-ПРМ в первую очередь поражает нижние конечности, а затем распространяется вверх, напоминая синдром Гийена-Барре. ЦМВ-мультифокальная нейропатия — подострый процесс, прогрессирующий в течение нескольких недель или даже месяцев. Он характеризуется периферическими парезами, снижением глубоких рефлексов и нарушениями чувствительности вследствие асимметричного поражения нервов нижних и верхних конечностей. Двигательные нарушения обычно преобладают над чувствительными, хотя в некоторых случаях первыми признаками заболевания могут быть парестезии, В редких случаях ЦМВ вызывает менингомиелит или миозит.
3. Диагностика цитомегаловирусной инфекции. Клинические симптомы заболевания позволяют предположить диагноз, но не являются патогномоничными для ЦМВ-поражения нервной системы при СПИДе. МРТ-исследование с контрастированием гадолинием позволяет визуализировать накопление контраста в области эпендимальной выстилки желудочков мозга у 10% больных ЦМВЭ, иногда мозговых оболочек при менингоэнцефалите или менингомиелите, и в ряде случаев корешков спинномозговых нервов в поясничном отделе и конуса спинного мозга при ЦМВ-ПРМ. Однако нередко нейровизуализационные методы не выявляют отклонений от нормы или демонстрируют неспецифические атрофйческие изменения.
В ЦСЖ наблюдается полиморфонуклеарный плеоцитоз, снижение уровня глюкозы, повышение концентрации белка и примерно у половины больных ЦМВ-ПРМ —положительная культура ЦМВ. Для ЦМВЭ плеоцитоз нехарактерен и культура ЦМВ почти никогда не бывает положительной. При мультифокальной мононейропатии состав ЦСЖ нормальный или наблюдается неспецифическое повышение уровня белка. В последние годы для диагностики ЦМВИ стали применять ПЦР, которая позволяет выявить ДНК вируса в ЦСЖ. Ретроспективные исследования показали, что данный метод является чувствительным и специфичным для активной ЦМВИ, однако проспективные исследования еще предстоит провести. Считается, что не бывает изолированного ЦМВ-поражения нервной системы, данные нарушения являются только компонентом системной инфекции, о чем свидетельствует обнаружение изменений в сетчатке глаз и желудочно-кишечном тракте. Также нередко поражаются легкие и надпочечники.
Медицинский эксперт статьи

Инкубационный период цитомегаловирусной инфекции составляет 2-12 нед.

[1], [2], [3], [4], [5], [6], [7], [8], [9], [10]
Основные симптомы цитомегаловирусной инфекции и динамика их развития
При врождённой цитомегаловирусной инфекции характер поражения плода зависит от срока заражения. Острая цитомегаловирусная инфекция у матери в первые 20 недель беременности может привести к тяжёлой патологии плода, результатом которой становятся самопроизвольный выкидыш, внутриутробная гибель плода, мёртворождение, пороки, в большинстве случаев несовместимые с жизнью. При заражении цитомегаловирусом в поздние сроки беременности прогноз для жизни и нормального развития ребёнка более благоприятен. Выраженные симптомы цитомегаловирусной инфекции в первые недели жизни имеют 10-15% инфицированных цитомегаловирусом новорождённых. Для манифестной формы врождённой цитомегаловирусной инфекции характерны гепатоспленомегалия, стойкая желтуха, геморрагическая или пятнисто-папулёзная сыпь, выраженная тромбоцитопения, повышение активности АЛТ и уровня прямого билирубина в крови, повышенный гемолиз эритроцитов. Младенцы часто рождаются недоношенными, с дефицитом массы тела, признаками внутриутробной гипоксии. Характерна патология ЦНС в виде микроцефалии, реже гидроцефалии, энцефаловентрикулита, судорожного синдрома, снижения слуха. Цитомегаловирусная инфекция - основная причина врождённой глухоты. Возможны энтероколит, фиброз поджелудочной железы, интерстициальный нефрит, хронический сиалоаденит с фиброзом слюнных желёз, интерстициальная пневмония, атрофия зрительного нерва, врождённая катаракта, а также генерализованное поражение органов с развитием шока. ДВС-синдрома и смерти ребёнка. Риск летального исхода в первые 6 нед жизни новорождённых с клинически выраженной цитомегаловирусной инфекции составляет 12%. Около 90% выживших детей, страдавших манифестной цитомегаловирусной инфекции, имеют отдалённые последствия заболевания в виде снижения умственного развития, нейросенсорной глухоты или двустороннего снижения слуха, нарушения восприятия речи при сохранении слуха, судорожного синдрома, парезов, снижения зрения. При внутриутробном заражении цитомегаловирусом возможна бессимптомная форма инфекции с низкой степенью активности, когда вирус присутствует только в моче или слюне, и высокой степенью активности, если вирус определяют в крови. В 8-15% случаях антенатальная цитомегаловирусная инфекция, не проявляясь яркой клинической симптоматикой, ведёт к формированию поздних осложнений в виде ухудшения слуха. снижения зрения, судорожных расстройств, задержки физического и умственного развития. Фактором риска развития заболевания с поражением ЦНС служит стойкое наличие в цельной крови ДНК цитомегаловируса в период от момента рождения ребёнка до 3 мес жизни. Дети с врождённой цитомегаловирусной инфекции должны находиться под медицинским наблюдением в течение 3-5 лет, так как нарушение слуха может прогрессировать в первые годы жизни, а клинически значимые осложнения - сохраняться и через 5 лет после рождения.
При отсутствии отягощающих факторов интранатальная или ранняя постнатальная цитомегаловирусная инфекция протекает бессимптомно, проявляется клинически лишь в 2-10% случаях, чаще в виде пневмонии. У недоношенных ослабленных детей с низким весом при рождении, заражённых цитомегаловирусом во время родов или в первые дни жизни путём гемотрансфузий, уже к 3-5-й нед жизни развивается генерализованное заболевание, проявлениями которого служат пневмония, затяжная желтуха. гепатоспленомегалия, нефропатия. поражение кишечника, анемия, тромбоцитопения. Цитомегаловирусная инфекция носит длительный рецидивирующий характер. Максимальная летальность от цитомегаловирусной инфекции приходится на возраст 2-4 мес.
Симптомы цитомегаловирусной инфекции приобретённой у детей старшего возраста и взрослых зависит от формы инфекции (первичное заражение, реинфекция, реактивация латентного вируса), путей заражения, наличия и степени выраженности иммуносупрессии. Первичное инфицирование цитомегаловирусом иммунокомпетентных лиц обычно протекает бессимптомно и лишь в 5% случаев в виде мононуклеозоподобного синдрома, отличительными признаками которого выступают высокая лихорадка, выраженный и длительный астенический синдром, в крови - относительный лимфоцитоз. атипичные лимфоциты. Ангина и увеличение лимфатических узлов не характерны. Заражение вирусом путём гемотрансфузий или при трансплантации инфицированного органа приводит к развитию острой формы заболевания, включающего высокую лихорадку, астению, боли в горле, лимфаденопатию, миалгию. артралгию, нейтропению, тромбоцитопению, интерстициальную пневмонию, гепатит, нефрит и миокардит. При отсутствии выраженных иммунологических нарушений острая цитомегаловирусная инфекция переходит в латентную с пожизненным присутствием вируса в организме человека. Развитие лммуносупрессии ведёт к возобновлению репликации цитомегаловируса. появлению вируса в крови и возможной манифестации заболевания. Повторное попадание вируса в организм человека на фоне иммунодефицитного состояния также может быть причиной виремии и развития клинически выраженной цитомегаловирусной инфекции. При реинфекции манифестация цитомегаловирусной инфекции происходит чаще и протекает более тяжело, чем при реактивации вируса.
Нередко вирус поражает пищеварительный тракт. Цитомегаловирус - основной этиологический фактор язвенных дефектов пищеварительного тракта у больных ВИЧ-инфекцией. Типичными признаками цитомегаловирусного эзофагита выступают лихорадка. загрудинная боль при прохождении пищевого комка, отсутствие эффекта противогрибковой терапии, наличие неглубоких округлых язв и/или эрозий в дистальном отделе пищевода. Поражение желудка характеризуется наличием острых или подострых язв. Клиническая картина цитомегаловирусного колита или энтероколита включает диарею, стойкие абдоминальные боли, болезненность толстой кишки при пальпации, значительное снижение массы тела, выраженную слабость, повышение температуры. Колоноскопия выявляет эрозии и изъязвления слизистой оболочки кишки.
Гепатит - одна из основных клинических форм цитомегаловирусной инфекции при трансплацентарном заражении ребёнка, у реципиентов после пересадки печени, больных, инфицированных вирусом во время гемотрансфузий. Особенность поражения печени при цитомегаловирусной инфекции - частое вовлечение в патологический процесс желчных путей. Цитомегаловирусный гепатит характеризуется мягким клиническим течением, но при развитии склерозирующего холангита возникают боли в верхней части живота, тошнота, диарея, болезненность печени, повышение активности щелочной фосфатазы и ГГТТ, возможен холестаз. Поражение печени носит характер гранулематозного гепатита, в редких случаях наблюдают выраженный фиброз и даже цирроз печени. Патология поджелудочной железы у больных цитомегаловирусной инфекцией обычно протекает бессимптомно или со стёртой клинической картиной при повышении концентрации амилазы в крови. Высокой чувствительностью к цитомегаловирусу обладают клетки эпителия мелких протоков слюнных желёз, преимущественно околоушных. Специфические изменения в слюнных железах при цитомегаловирусной инфекции у детей встречаются в подавляющем большинстве случаев. Для взрослых больных цитомегаловирусной инфекцией сиалоаденит не характерен.
Цитомегаловирус - одна из причин патологии надпочечников (часто у больных ВИЧ-инфекцией) и развития вторичной надпочечниковой недостаточности, проявляющейся стойкой гипотонией, слабостью, похуданием, анорексией, нарушением работы кишечника, рядом психических отклонений, реже - гиперпигментацией кожи и слизистых. Наличие у больного ДНК цитомегаловируса в крови, а также стойкой гипотонии, астении, анорексии требует определения уровня калия, натрия и хлоридов в крови, проведения гормональных исследований для анализа функциональной активности надпочечников. Цитомегаловирусный адреналит характеризуется первоначальным поражением мозгового слоя с переходом процесса на глубокие, а в дальнейшем - и на все слои коры.
Манифестная цитомегаловирусная инфекция нередко протекает с поражением нервной системы в виде энцефаловентрикулита. миелита, полирадикулопатии, полинеиропатии нижних конечностей. Для цитомегаловмирусного энцефалита у больных ВИЧ-инфекцией характерны скудная неврологическая симптоматика (непостоянные головные боли, головокружение, горизонтальный нистагм, реже парез глазодвигательного нерва, невропатии лицевого нерва), но выраженные изменения в психическом статусе (личностные изменения, грубые нарушения памяти, снижение способности к интеллектуальной деятельности, резкое ослабление психической и двигательной активности, нарушение ориентировки в месте и времени, анозогнозии, снижение контроля за функцией тазовых органов). Мнестико-интеллектуальные изменения нередко достигают степени деменции. У детей, перенёсших цитомегаловирусный энцефалит, также выявляют замедление психического и умственного развития. Исследования спинно-мозговой жидкости показывают повышенное количество белка, отсутствие воспалительной реакции или мононуклеарный плеоцитоз. нормальное содержание глюкозы и хлоридов. Клиническая картина полинеиропатии и полирадикулопатии характеризуется болевым синдромом в дистальных отделах нижних конечностей, реже в поясничной области в сочетании с чувством онемения, парастезиеи, гиперестезией, каузалгией. гиперпатией. При полирадикулопатии возможен вялый парез нижних конечностей, сопровождающийся снижением болевой и тактильной чувствительности в дистальных отделах ног. В спинно-мозговой жидкости больных полирадикулопатией выявляют повышение содержания белка, лимфоцитарный плеоцитоз. Цитомегаловирус принадлежит ведущая роль в развитии миелита у ВИЧ-инфицированных пациентов. Поражение спинного мозга носит диффузный характер и выступает поздним проявлением цитомегаловирусной инфекции. В дебюте заболевание имеет клиническую картину полинеиропатии или полирадикулопатии. в дальнейшем. в соответствии с преимущественным уровнем поражения спинного мозга, развиваются спастическая тетраплегия или спастический парез нижних конечностей, появляются пирамидные знаки, значительное снижение всех видов чувствительности, в первую очередь в дистальных отделах ног; трофические нарушения. Все больные страдают грубыми расстройствами функции тазовых органов, в основном, по центральному типу. В спинно-мозговой жидкости определяют умеренное повышение содержания белка, лимфоцитарный плеоцитоз.
Цитомегаловирусный ретинит - самая частая причина потери зрения у больных ВИЧ-инфекцией. Данная патология описана также у реципиентов органов, детей с врождённой цитомегаловирусной инфекцией, в единичных случаях - у беременных. Больные отмечают следующие симптомы цитомегаловирусной инфекции: на плавающие точки, пятна, пелену перед взором, снижение остроты и дефекты полей зрения. При офтальмоскопии на сетчатке по периферии глазного дна выявляют очаги белого цвета с геморрагиями по ходу ретинальных сосудов. Прогрессирование процесса ведёт к формированию диффузного обширного инфильтрата с зонами ретинальной атрофии и очагами кровоизлияний по поверхности поражения. Начальная патология одного глаза через 2-4 мес приобретает двусторонний характер и в отсутствие этиотропной терапии приводит в большинстве случаев к потере зрения. У больных ВИЧ-инфекцией, имеющих в анамнезе цитомегаловирусный ретинит, на фоне ВААРТ возможно развитие увеита как проявления синдрома восстановления иммунной системы.
Сенсорноневральная глухота имеет место у 60% детей с клинически выраженной врождённой цитомегаловирусной инфекцией. Снижение слуха возможно и у взрослых ВИЧ-инфицированных лиц с манифестной цитомегаловирусной инфекцией. В основе связанных с цитомегаловирусрм дефектов слуха лежит воспалительное и ишемическое повреждение улитки и слухового нерва.
Ряд работ демонстрируют роль цитомегаловируса как этиологического фактора патологии сердца (миокардит, дилатационная кардипатия), селезёнки, лимфатических узлов. почек, костного мозга с развитием панцитопении. Интерстициальный нефрит, обусловленный цитомегаловирусной инфекцией, как правило, протекает без клинических проявлений. Возможны микропротеинурия, микрогематурия, лейкоцитурия, редко вторичный нефротический синдром и почечная недостаточность. У больных цитомегаловирусной инфекцией часто регистрируют тромбоцитопению, реже умеренную анемию, лейкопению, лимфопению и моноцитоз.
Классификация цитомегаловирусной инфекции
Общепринятой классификации цитомегаловирусной инфекции не существует. Целесообразна следующая классификация заболевания.
- Врождённая цитомегаловирусная инфекция:
- бессимптомная форма;
- манифестная форма (цитомегаловирусная болезнь).
- Приобретённая цитомегаловирусная инфекция.
- Острая цитомегаловирусная инфекция.
- бессимптомная форма;
- цитомегаловирусный мононуклеоз;
- манифестная форма (цитомегаловирусная болезнь).
- Латентная цитомегаловирусная инфекция.
- Активная цитомегаловирусная инфекция (реактивация, реинфекция):
- бессимптомная форма;
- цитомегаловирусный-ассоциированный синдром;
- манифестная форма (цитомегаловирусная болезнь).
- Острая цитомегаловирусная инфекция.

[11], [12], [13], [14], [15], [16], [17], [18], [19], [20]
Читайте также:
- Можно ли заразиться гепатитом с через маникюрные принадлежности
- О сильнейших вирусах гриппа
- В прививке находится вирус
- Что делает вирус twobee
- Ингавирин от гонконгского гриппа
 Пожалуйста, не занимайтесь самолечением!При симпотмах заболевания - обратитесь к врачу.
Пожалуйста, не занимайтесь самолечением!При симпотмах заболевания - обратитесь к врачу.

