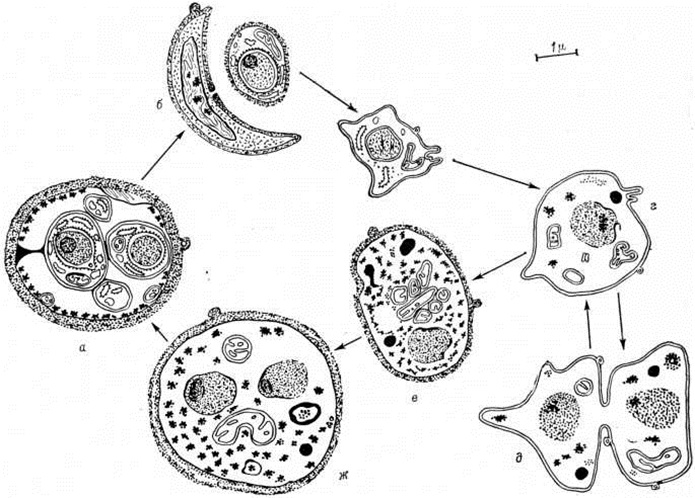
Рис
Схематическое изображение цикла развития Pneumocystis carinii, по данным Френкеля (J. К. Frenkel, 1976): а — зрелая форма цист с внутрицистными включениями, б — свободный трофозоит, покидающий цисту, в — малый трофозоит, грамм — большой трофозоит, д — стадия деления, е — трофозоит, покрывающийся оболочкой, ж — стадия предцисты.
Клиническая картина. Инкубационный период, по данным большинства исследователей, в среднем 30—40 дней, самый короткий 7— 10 дней, самый продолжительный — до 26 недель Заболевание развивается постепенно и проходит три стадии. Первая длится от нескольких дней до нескольких недель и характеризуется появлением учащённого дыхания, одышки, цианоза носогубного треугольника при сосании и крике. Ребёнок отказывается от груди, не прибавляет в весе. Испражнения могут быть жидкими, чаще не меняются. Температура — нормальная или субфебрильная, при присоединении вторичной бактериальной инфекции повышенная.
Во второй стадии Пневмоцистоз клинические, картина характеризуется триадой симптомов: цианоз, одышка, тахипноэ. На 3—4-й неделе заболевания появляется сухой навязчивый кашель. Перкуторно определяется выраженный коробочный звук, увеличение нижних границ лёгких, значительно расширены межреберья. Дыхание не изменено, ослабленное или жестковатое, в паравертебральных областях определяются единичные мелкопузырчатые хрипы. Прогрессирует респираторный ацидоз (смотри полный свод знаний). Возможен разрыв лобулярных вздутий и образование пневмоторакса. Тяжёлые метаболические расстройства дополняет респираторный эксикоз (смотри полный свод знаний: Обезвоживание организма). Массивное поражение лёгких ведёт к развитию легочно-сердечной недостаточности (смотри полный свод знаний: Лёгочное сердце), увеличиваются селезёнка и печень.
В третьей стадии состояние улучшается. Уменьшается одышка, исчезает кашель. Коробочный звук, определяемый перкуторно, исчезает, более чётко определяются границы сердца, прежде перекрытые эмфизематозно увеличенными лёгкими. Аускультативно хрипы не выслушиваются. У части больных встречаются явления рецидивирующего ларингита или упорного астматического синдрома. При всех стадиях Пневмоцистоз в крови возможен лимфоцитоз и моноцитоз. В острой стадии иногда наблюдается нейтрофильный лейкоцитоз; в неосложнённых случаях — РОЭ не изменена, при присоединении вторичной инфекции ускоренная.
Течение Пневмоцистоз может быть волнообразным: периоды улучшения сменяются усилением одышки, кашля и других симптомов. Длительность заболевания в неосложнённых случаях 4—8 недель Осложнение Пневмоцистоз вторичной пневмонией приводит к изменению клинической и рентгенологическое картины (смотри полный свод знаний: Пневмония).
Диагноз базируется на данных анамнеза, эпидемиологической обстановки, клинические, картине, обнаружении пневмоцист в слизи из верхних дыхательных путей, нарастании титра антител, характерных рентгенологических данных.
В слизи верхних дыхательных путей возбудитель обнаруживается к концу 2-й недели после начала заболевания. Из мокроты готовят мазки, фиксируют и окрашивают по Романовскому — Гимзе, Гомори, Массону и другие
Из иммунологический методов для диагностики Пневмоцистоз используют реакцию связывания комплемента (смотри полный свод знаний). Специфичность и чувствительность реакции изучена недостаточно. Наиболее чувствительной является реакция иммунофлюоресценции (смотри полный свод знаний) с антигеном, очищенным от тканевых клеток. Данные о специфичности и чувствительности реакции иммунофлюоресценции противоречивы. Положительно реагирует большой процент здоровых лиц. Внутрикожная проба чаще даёт неспецифические реакции.
При Пневмоцистоз наблюдается своеобразная рентгенологическое картина, позволяющая с большой вероятностью заподозрить Пневмоцистоз В начале развития респираторного синдрома обнаруживают уплотнение корня лёгких слабой интенсивности. Во второй стадии, по данным В. Ф. Баклановой (1980), появляется множество неоднородных по своей интенсивности очаговых теней, так называемый ватные лёгкие. Образовавшиеся ателектазы не всегда удаётся выявить. Возможно уплотнение рёберной плевры и плевры междолевых поверхностей лёгкого. В третьей стадии заболевания по мере исчезновения уплотнённых и эмфизематозных участков воздухоносность лёгочной ткани восстанавливается и в рентгенологическое картине на первом плане видно уплотнение интерстициальной ткани. Усиленный лёгочный рисунок может сохраняться в течение нескольких месяцев.
Лечение разработано недостаточно. Из специфических средств наиболее эффективен пентамидин (антагонист фолиевой кислоты), в дозе 4 мг/кг в сутки в течение 8—14 дней (пневмоцисты исчезают из слизи на 6-й день). Однако применение пентамидина часто может вызвать осложнение, например, подкожные кровоизлияния, гипотонию, азотемию, глюкозурию, олигурию, мегалобластную анемию. Для устранения побочных явлений используют фолиевую кислоту в дозе 6 микрограмм в сутки. Применяют также фуразолидон, трихопол (метронидазол) с аминохинолом (курс 10—14 дней). При присоединении бактериальной инфекции назначают антибиотики. Проводят инфузионную терапию: вводят гамма-глобулин, гемодез, изотонический раствор, плазму, кровь; при анорексии показаны глюкоза, альбумин, альвезин и другие средства парентерального питания.
Прогноз у ослабленных детей с врождёнными иммунодефицитными состояниями (смотри полный свод знаний: Иммунологическая недостаточность) неблагоприятный. Смерть наступает от асфиксии, иногда вследствие присоединения бактериальной инфекции, чаще стафилококковой, или генерализованной цитомегалии (смотри полный свод знаний).
Профилактика. Больных и подозрительных на Пневмоцистоз изолируют в боксы. Обслуживание детей и содержание такое же, как при других инфекционные болезнях лёгких. За больными проводится постоянное и длительное наблюдение. Медперсонал следует обследовать на носительство пневмоцист и при положительной реакции не допускать к работе с детьми. Больные и ослабленные дети не должны контактировать с животными, которые могут быть носителями пневмоцист.
Пневмоцистоз (pneumocystosis; син. плазмоклеточная пневмония) — заболевание, вызываемое пневмоцистами, встречающееся преимущественно у детей и характеризующееся интерстициальной, плазмоцеллюлярной пневмонией.
Содержание
История
Впервые возбудитель Пневмоцистоза — Pneumocystis carinii — описан в 1909 г. Шагасом (С. Chagas), который неправильно посчитал его стадией развития трипаносомы. В 1912 г. в Париже Деланоэ и Деланоэ (Р. Delanoe, М. Delanoe) обнаружили паразита в легких крыс и доказали его видовую самостоятельность. В последующем Pneumocystis carinii был найден в легких разных животных (крыс, мышей, собак, кошек, кроликов, свиней) и человека. В 1952 г. О. Йировец и Ванек (J. Vanek) доказали, что он является возбудителем интерстициальной пневмонии у недоношенных и ослабленных детей.
Этиология и патогенез
Возбудителя Пневмоцистоза — P. carinii — большинство исследователей относит к типу простейших (см.) — Protozoa, хотя систематическое положение и природа пневмоцист пока не выяснены. Многое сближает их с простейшими класса споровиков, но высказывалось мнение о их растительной природе и принадлежности к низшим грибкам рода Candida. Данные о протозойной природе Pneumocystis представляются все же более убедительными.
Паразиты имеют округлую форму, длиной 2—3 мкм, шириной от 1,5 до 2 мкм. Возбудитель хорошо окрашивается по Романовскому — Гимзе (см. Романовского — Гимзы метод). Ядро, заключенное в бесструктурную оболочку, состоящую из гликозаминогликанов, располагается в центре или эксцентрично.
Паразиты размножаются путем деления пополам под оболочкой, после чего и сам слизистый шар перешнуровывается на два шара.
После ряда делений наступает стадия спорогонии. Процесс ее состоит в том, что паразитарное тельце увеличивается, заполняя почти всю слизистую оболочку, и превращается в споробласт. Ядро также увеличивается и последовательно делится на 2, 4 и 8 ядер. Спорогония заканчивается образованием цисты, в к-рой находится 8 овальных или грушевидных спор размером 1—2 мкм каждая.

На рисунке представлена схема цикла развития и морфология отдельных стадий Pneumocystis carinii, по данным Френкеля (J.К. Frenkel, 1976).
П. является одной из причин острого заболевания легких у детей раннего возраста, у недоношенных, ослабленных вследствие других заболеваний различной этиологии, у детей, принимавших кортикостероиды и иммунодепрессанты; иногда является причиной легочной патологии у взрослых, страдающих хроническими болезнями крови, онкологическими заболеваниями и леченных кортикостероидами и иммунодепрессантами, и у больных, перенесших трансплантацию органов. При выраженном снижении сопротивляемости к инфекции P. carinii вызывает генерализованное заболевание.
Воспалительная инфильтрация межальвеолярных перегородок приводит к нарушению газообмена, заполнению альвеол пенистой массой, уменьшает дыхательную поверхность легких, обусловливает кислородную недостаточность различной степени выраженности и тяжесть состояния.
Эпидемиология
Источником Пневмоцистоза могут быть люди и животные — больные и носители возбудителей. Основной путь передачи возбудителей — воздушно-капельный, однако возможен и трансплацентарный. Носители пневмоцист среди работников детских учреждений особенно опасны, от них могут заболеть ослабленные и недоношенные дети, восприимчивые к П. Ввиду того что П. обнаружен у многих домашних и диких животных, некоторые исследователи делают вывод о природной очаговости П.
П. широко распространен. Эпидемии описаны в 17 странах, а спорадические случаи — в 30 странах Европы, Азии, Африки, Америки. В Европе П. встречается в виде эпидемических вспышек, в Америке отмечены только спорадические случаи. В СССР пневмоцистная пневмония зарегистрирована в основном в Москве, Ленинграде, Харькове, Таджикистане и Эстонии.
Патологическая анатомия
Макроскопически легкие выглядят воздушными, с очагами буллезной эмфиземы. Висцеральная плевра при этом несколько утолщена, нередко имеются пятнистые кровоизлияния. Вследствие разрыва эмфизематозных пузырей может развиться пневмомедиастинум (см.), пневмоторакс (см.). На разрезе ткань легких серовато-синюшная, отделяемое вязкое, скудное. Слизистая оболочка гортани, трахеи и крупных бронхов бледная, в просвете дыхательных путей пенистое содержимое. При гистологическом исследовании в просвете альвеол, а иногда в межальвеолярных перегородках обнаруживается большое количество пневмоцист и белковые массы, богатые иммуноглобулинами, в альвеолах, вокруг распадающихся конгломератов паразита — макрофаги, нейтрофильные лейкоциты, эритроциты, фибрин. Строма легких, стенки мелких бронхов и Межальвеолярные перегородки утолщены, инфильтрированы различными клеточными элементами с преобладанием плазматических и лимфоидных клеток. В цитоплазме клеток эпителия слизистой оболочки бронхов обнаруживаются макрофаги с пневмоцистами.
Клиническая картина
Инкубационный период, по данным большинства исследователей, в среднем 30—40 дней, самый короткий 7— 10 дней, самый продолжительный — до 26 нед. Заболевание развивается постепенно и проходит три стадии. Первая длится от нескольких дней до нескольких недель и характеризуется появлением учащенного дыхания, одышки, цианоза носогубного треугольника при сосании и крике. Ребенок отказывается от груди, не прибавляет в весе. Испражнения могут быть жидкими, чаще не меняются. Температура — нормальная или субфебрильная, при присоединении вторичной бактериальной инфекции повышенная.
Во второй стадии Пневмоцистоза клиническая картина характеризуется триадой симптомов: цианоз, одышка, тахипное. На 3—4-й неделе заболевания появляется сухой навязчивый кашель. Перкуторно определяется выраженный коробочный звук, увеличение нижних границ легких, значительно расширены межреберья. Дыхание не изменено, ослабленное или жестковатое, в паравертебральных областях определяются единичные мелкопузырчатые хрипы. Прогрессирует респираторный ацидоз (см.).
Возможен разрыв лобулярных вздутий и образование пневмоторакса. Тяжелые метаболические расстройства дополняет респираторный эксикоз (см. Обезвоживание организма). Массивное поражение легких ведет к развитию легочно-сердечной недостаточности (см. Легочное сердце), увеличиваются селезенка и печень.
В третьей стадии состояние улучшается. Уменьшается одышка, исчезает кашель. Коробочный звук, определяемый перкуторно, исчезает, более четко определяются границы сердца, прежде перекрытые эмфизематозно увеличенными легкими. Аускультативно хрипы не выслушиваются. У части больных встречаются явления рецидивирующего ларингита или упорного астматического синдрома. При всех стадиях П. в крови возможен лимфоцитоз и моноцитоз. В острой стадии иногда наблюдается нейтрофильный лейкоцитоз; в неосложненных случаях — РОЭ не изменена, при присоединении вторичной инфекции ускоренная.
Течение Пневмоцистоза может быть волнообразным: периоды улучшения сменяются усилением одышки, кашля и других симптомов. Длительность заболевания в неосложненных случаях 4—8 нед. Осложнение П. вторичной пневмонией приводит к изменению клинической и рентгенологической картины (см. Пневмония).
Диагноз
Диагноз базируется на данных анамнеза, эпидемиологической обстановки, клин, картине, обнаружении пневмоцист в слизи из верхних дыхательных путей, нарастании титра антител, характерных рентгенологических данных.
В слизи верхних дыхательных путей возбудитель обнаруживается к концу 2-й недели после начала заболевания. Из мокроты готовят мазки, фиксируют и окрашивают по Романовскому — Гимзе, Гомори, Массону и др.
Из иммунологических методов для диагностики П. используют реакцию связывания комплемента (см.). Специфичность и чувствительность реакции изучена недостаточно. Наиболее чувствительной является реакция иммунофлюоресценции (см.) с антигеном, очищенным от тканевых клеток. Данные о специфичности и чувствительности реакции иммунофлюоресценции противоречивы. Положительно реагирует большой процент здоровых лиц. Внутрикожная проба чаще дает неспецифические реакции.
При П. наблюдается своеобразная рентгенол, картина, позволяющая с большой вероятностью заподозрить П. В начале развития респираторного синдрома обнаруживают уплотнение корня легких слабой интенсивности. Во второй стадии, по данным В. Ф. Баклановой (1980), появляется множество неоднородных по своей интенсивности очаговых теней, так наз. ватные легкие. Образовавшиеся ателектазы не всегда удается выявить. Возможно уплотнение реберной плевры и плевры меж-долевых поверхностей легкого. В третьей стадии заболевания по мере исчезновения уплотненных и эмфизематозных участков воздухо-носность легочной ткани восстанавливается и в рентгенол, картине на первом плане видно уплотнение интерстициальной ткани. Усиленный легочный рисунок может сохраняться в течение нескольких месяцев.
Лечение
Лечение разработано недостаточно. Из специфических средств наиболее эффективен пентамидин (антагонист фолиевой к-ты), в дозе 4 мг/кг в сутки в течение 8—14 дней (пневмоцисты исчезают из слизи на 6-й день). Однако применение пентамидина часто может вызвать осложнение, напр, подкожные кровоизлияния, гипотонию, азотемию, глюкозурию, олигурию, мегалобластную анемию. Для устранения побочных явлений используют фолиевую к-ту в дозе 6 мкг в сутки. Применяют также фуразолидон, трихопол (метронидазол) с аминохпнолом (курс 10—14 дней). При присоединении бактериальной инфекции назначают антибиотики. Проводят инфу-зионную терапию: вводят гамма-глобулин, гемодез, изотонический р-р, плазму, кровь; при анорексии показаны глюкоза, альбумин, альвезин и другие средства парентерального питания.
Прогноз и Профилактика
Прогноз у ослабленных детей с врожденными иммунодефицитным и состояниями (см. Иммунологическая недостаточность) неблагоприятный. Смерть наступает от асфиксии, иногда вследствие присоединения бактериальной инфекции, чаще стафилококковой, или генерализованной цитомегалии (см.).
Профилактика. Больных и подозрительных на Пневмоцистоз изолируют в боксы. Обслуживание детей и содержание такое же, как при других инфекционных болезнях легких. За больными проводится постоянное и длительное наблюдение. Медперсонал следует обследовать на носительство пневмоцист и при положительной реакции не допускать к работе с детьми. Больные и ослабленные дети не должны контактировать с животными, которые могут быть носителями пневмоцист.
Библиография: Андреев И. и др. Дифференциальная диагностика важнейших симптомов детских болезней, пер. с болг., с. 250 и др., Пловдив, 1977; Бакланова В. Ф. и Владыкина М. И. Руководство но рентгенодиагностике болезней органов дыхания у детей, Л., 1978; Керпель-Фрониус Э. Педиатрия, пер. с венгер., с. 413, Будапешт, 1977; Матвеев М. П. и др. Пневмоцистоз у детей, Педиатрия, № 2, с. 56, 1979; Рябцева В. А. и др. Пневмоцистоз (распространение, источники и пути передачи), там же, № 6, с. 30, 1974; Цинзерлинг А. В. и Неженцев М. В. О пневмоцистозе легких детей раннего возраста, Арх. патол., т. 32, № 11, с. 21, 1970; Delаnоe P. Sur les rapports des kystes de Carini du poumon des rats avec le Trypanosoma lewisi, C. R. Acad. Sci. (Paris), t. 155, p. 658, 1912; Frenkel J. K. Pneumocystis jiroveci n. sp. from man, Nat. Cancer Inst. Monograph., v. 43, p. 13, 1976; Geormaneanu М., Gherghina S. §i Cernatescu I. Pneumonia alveolo-interstitiala cu Pneumocystis carinii, Rev. Pediat. Obstet. Ginec. (Buc.), V. 25, p. 55, 1976; Jirovec O. u. Vanek J. Zur Morphologie der Pneumocystis carinii und zur Pathogenese der Pneumocystis-Pneumonie, Zbl. allg. Path. path. Anat., Bd 92, S. 424, 1954; Lipson A., Marshall W. C. a. Hayward A. R. Treatment ot pneu-mocystis carinii pneumonia in children, Arch. Dis. Childh., v. 52, p. 314, 1977; Pathology of tropical and extraordinary diseases, ed. by Ch. H. Binford a. D.H. Connor, V. 1, p. 303, Washington, 1976; Proceedings of the Symposium on pneumocystis carinii infection, Washington, 1976; Va Vra J. a. Kucera K. Pneumocystis carinii Delanoe, J. Protozool., V. 17, p. 463, 1970; Walzer P. D. a. o. Pneumocystis carinii pneumonia in the United States, Ann. intern. Med., v. 80, p. 83, 1974.
H. A. Тюрин; Д. H. Засухин, М. И. Шайхутдинов (этиол.).
При третьей, генерализованной форме, кроме поражения головного мозга, наблюдаются гепато- и спленомегалия, желтуха, язвенные поражения кишечника, миокардит, интерстициальная пневмония. В печени и селезенке имеются очаги реактивного миелоэритробластоза. В паренхиматозных органах выявляются некрозы, очаговая или диффузная лимфогистиоцитарная инфильтрация с примесью эозинофилов. Реже наблюдаются висцеральные формы заболевания без поражения головного мозга. Патологоанатомический диагноз врожденного токсоплазмоза ставится только в случаях обнаружения свободно лежащих паразитов — эндозоитов и цист в гистологических срезах или в мазках-отпечатках с поверхности разрезов органов, а также выявления токсоплазм методом биопроб.
Осложнения токсоплазмоза обусловлены поражением головного мозга и глаз, что ведет к истощению, параличам, умственной отсталости, слепоте, психическим заболеваниям. Возможно присоединение бактериальной инфекции с развитием гнойного менингоэнцефалита, пиоцефалии, сепсиса.
Пневмоцистоз, или пневмоцистная пневмония (плазмоцеллюлярная, интсрстициальная пневмония), вызывается возбудителем Pneumocystis carinii. Возбудитель пневмоцистоза легких относится к типу простейших. Форма пневмоцисты округлая, овальная или изогнутая, длина 2—3 мкм, ширина от 1,5 до 2 мкм. Паразиты располагаются эксцентрично в шаровидных слизистых образованиях, окруженных мембраной, дающей отчетливую ШИК-положительную реакцию. Размеры шаровидных образовании значительно крупнее самого паразита. В обычных условиях возбудитель не обладает высокими патогенными свойствами.
Пневмоцистная пневмония чаще возникает и тяжело протекает у недоношенных новорожденных и детей с врожденной гипотрофией. Заражение происходит воздушно-капельным путем от инфицированных матерей или обслуживающего персонала лечебных учреждений. Возможно заражение от домашних животных. Описан случай врожденного пневмоцистоза легких у мертворожденного доношенного плода.
Развитие заболевания происходит постепенно, течение длительное, до 7—8 нед и более. Характерными симптомами являются нарастающая одышка, цианоз, сухой, коклюшеподобный кашель. Прогноз часто неблагоприятный. У детей более старшего возраста пневмоцистоз легких может развиваться как осложнение лейкоза, при современной полихимиотерапии, приводящей к иммунодепрессии. В таких случаях пневмоцистиое поражение легких характеризуется быстрым развитием процесса и является: инкурабельным. Пневмоцистоз встречается как осложнение при злокачественных опухолях. и иммунодефицитных синдромах.
При пневмоцистозе поражаются исключительно легкие. В других органах и системах возбудителя не находят. Аэрогенным путем пневмоцисты попадают в легкие, где размножаются последовательным делением. Массы паразита постепенно заполняют респираторные просветы, уменьшая их объем, что проявляется респираторной недостаточностью. В альвеолярных перегородках возникают реактивные изменения в виде отека, инфильтрации гистиоцитами, лимфоидными клетками, макрофагами и плазматическими клетками. В отношении плазмоцеллюлярной реакции высказывались сомнения.
При исследовании пневмоцистных пневмоний у новорожденных зрелые плазматические клетки действительно не обнаруживаются. Этот вопрос требует дальнейшего изучения.
Поверхность разрезов суховата, при надавливании отделяется небольшое количество слизисто-кровянистой жидкости. В просветах бронхов и трахеи обнаруживается вязкое пенистое содержимое. Слизистая оболочка дыхательных путей остается бледной. Решающим для диагноза пневмоцистной пневмонии является микроскопическое исследование легких. При пневмоцистозе находят утолщенные перегородки альвеол, альвеолярных ходов с инфильтрацией их гистиоцитами и лимфоидными клетками. Просветы альвеол, альвеолярных ходов, бронхиол заполнены скоплениями пневмоцист в виде своеобразной пенистой массы. Среди масс паразита клеточные формы обычно не обнаруживаются. Могут встречаться единичные макрофаги и лейкоциты. Пенистые массы паразита подвергаются уплотнению, уменьшаются в объеме, постепенно резорбируются альвеолярными макрофагами.
В разных полях зрения могут выявляться различные стадии процесса, включая ателектазы, участки эмфиземы. Осложнением пневмоцистоза может явиться присоединение вирусно-бактериальной инфекции, интерстициальная, медиастинальная и подкожная эмфизема, пневмоторакс. При затяжном течении болезни возможно развитие диффузного фиброза легких.

Пневмоцистоз, являясь причиной заболеваемости и летальных исходов у 65-85% больных СПИДом, относится к наиболее важным и значимым СПИД-индикаторным инфекциям.
До эпидемии СПИДа, pneumocystis carinii был известен прежде всего как этиологический фактор оппортунистической инфекции, развивающейся у людей с врожденными или приобретенными иммунодефицитными состояниями (включая пациентов, получающих химиотерапию, реципиентов почечных трансплантатов, детей с недостаточностью белкового питания). В настоящее время инфекция, вызванная p. carinii, преимущественно встречается у больных СПИДом. Заболевание чаще всего проявляется в виде пневмоцистной пневмонии.
Pneumocystis carinii - микроорганизм с циклом жизни, подобным toxoplasma gondii. Возбудитель имеет характерную микроструктуру с внутриклеточными тельцами, типичными для protozoa. Однако изучение последовательностей рибосомальной РНК показывает наиболее вероятную родственную связь с saccharomyces.
Возбудитель пневмоцистоза — pneumocystis carinii — внеклеточный паразит многих видов животных, которого отличает строгий тропизм к легочной ткани.
Весь жизненный цикл пневмоцисты проходит в альвеоле (рис.1). Вегетативная форма пневмоцисты — трофозоит — прикрепляется к эпителию легкого, выстланного альвеолоцитами i порядка. Физиологический контакт паразита с клетками хозяина осуществляется через систему микропиноцитозных пузырьков.
Спорозоит — представлен клетками овальной формы (2-3 мкм), окружёнными слизистой капсулой. После инвазии в ткани лёгкого спорозоиты дифференцируются в трофозоиты — плеоморфные клетки с тонкой клеточной оболочкой. Размножается делением; капсула делится в последнюю очередь, предварительно образуя перетяжку и разделяясь на две особи. При окраске по Романовскому-Гимзе окрашиваются в фиолетовый цвет, ядра — в тёмно-синий.
После ряда делений некоторые трофозоиты вступают в спорогонию (половой цикл размножения): паразитарное тельце увеличивается, заполняя всю цитоплазму, формируется стенка цисты, и ядро вступает в цикл последовательных делений. Образуется циста (диаметром 5-8 мкм), содержащая 8 спорозоитов.

Рисунок 1. Жизненный цикл pneumocystis carinii
При разрыве цисты высвобождаются спорозоиты, дающие при благоприятных условиях начало популяции трофозоитов.
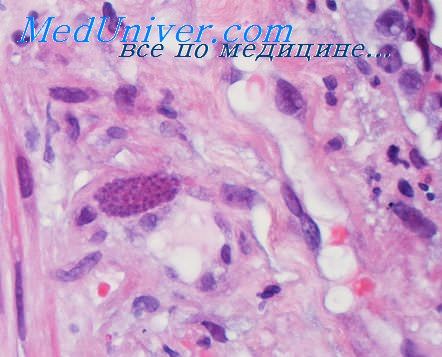
Предцисты и зрелые цисты с внутрицистными тельцами находятся в просвете альвеол, в составе пенистого экссудата (рис. 2 - 6).

Рисунок 2. Предцисты и зрелые цисты с внутрицистными тельцами находятся в просвете альвеол, в составе пенистого экссудата. Окраска - silver methenamine

Рисунок 3. Предцисты и зрелые цисты с внутрицистными тельцами находятся в просвете альвеол, в составе пенистого экссудата. Окраска - silver methenamine

Рисунок 4. Предцисты и зрелые цисты с внутрицистными тельцами находятся в просвете альвеол, в составе пенистого экссудата. Окраска - silver methenamine

Рисунок 5. Электронная микроскопия цисты. Видны nucleus и mitochondria

Рисунок 6. Электронная микроскопия цист, находящихся на различных стадиях развития
Патогенез пневмоцистной инфекции определяется механическим повреждением интерстициальной выстилки легкого как самим паразитом, так и воспалительными клетками: стенки альвеол инфильтрируются мононуклеарами, клетки интерстиция — плазматическими клетками. Толщина альвеолярной стенки увеличивается в 5-20 раз против нормальной; повреждение сурфактанта приводит к ослаблению растяжимости альвеол при длительной экскурсии. Вследствие этих процессов развивается альвеолярно-капиллярный блок, приводящий к тяжелой аноксии и смерти больных от нарастающей дыхательной недостаточности.
Пневмоцистная пневмония (Пп) послужила основанием для диагностики первых 5 случаев СПИДа, описанных в 1981 г., и натолкнула клиницистов на мысль о возможном этиологическом агенте, вызывавшем иммунодефицит у ранее здоровых молодых людей-гомосексуалистов Лос-Анжелеса. Эта инфекция стала в дальнейшем наиболее частым СПИД-ассоциируемым заболеванием.
Решающее значение Пп для прогноза течения СПИДа способствовало значительной интенсификации исследований иммунобиологии и патогенеза данной инфекции. У паразитов были обнаружены антигенные детерминанты, идентичные эпитопам некоторых человеческих тканей. Антигенной мимикрией часто объясняют широко распространенное пневмоцистоносительство. Нарушения в клеточных и гуморальных звеньях иммунитета при СПИДе приводят к переходу из латентной к манифестной форме пневмоцистной инфекции.
Пп у больных СПИДом развивается медленно, исподволь. От начала продромальных явлений до появления основных легочных симптомов проходит 4 нед. и более, лихорадка и одышка выражены нерезко, постепенно усиливается непродуктивный кашель.
Существует 4 показателя, по которым диагноз Пп может предполагаться у больного с ВИЧ-инфекцией:
1) повышение СОЭ > 50 мм/час;
2) повышение ЛДГ > 220 me;
3) выявление молочницы или волосатоклеточной лейкоплакии;
4) обнаружение на рентгенограммах диффузных интерстициальных изменений, распространяющихся от корней к периферии.
Необходимость выявления указанных показателей связана с минимальной информацией, получаемой при объективном осмотре.
Паразитологическое исследование является основным методом верификации диагноза. Считается, что пневмоцисты могут быть обнаружены в альвеолярно-бронхиальном секрете, мокроте из гортани, глотке и даже в желудочном содержимом, однако содержание пневмоцист в перечисленном материале крайне неодинаковое. Эффективность исследования материала, взятого из гортани и глотки, очень низкая (5-15%). Для исследования берут либо самостоятельно отходящую мокроту, либо мокроту, полученную с помощью ингаляции. Более эффективно исследование мокроты после ингаляции, при аспирации ее с помощью бронхоскопа. Было установлено, что при первых двух способах количество цист в препарате бывает небольшим (3-6 в мазке), в то время как при последнем способе их количество существенно большее (до 50 цист в мазке). Из этого следует, что нахождение в мазке мокроты даже единичных цист при наличии соответствующих клинических симптомов может быть расценено как верификация диагноза.
Еще более надежным является исследование лаважной (промывной) жидкости (87%). Эта жидкость получается при инсталляции в дистальные отделы бронхиального дерева теплого физиологического раствора с последующей его аспирацией. Аспират может быть разделен на 3 порции: бронхиальный, бронхоальвеолярный и альвеолярный. Исследованию может быть также подвергнут биоптат, полученный при трансбронхиальной, чрескожной, аспирационной или открытой биопсии легкого. Наилучшие результаты получаются при открытой биопсии легкого (100%). Этот метод приравнивается к хирургическому вмешательству, хотя состояние больных, как правило, не позволяет к нему прибегнуть. В то же время с помощью этого метода получается достаточно большой объем материала, и ложно-отрицательный результат исследования исключается.
Достаточно эффективные методы лабораторного культивирования pneumocystis carinii пока не разработаны. Серологические методы диагностики также мало эффективны. Антитела часто обнаруживаются у здоровых людей. Диагноз обычно устанавливается на основании цитологического исследования бронхоальвеолярного лаважа или ткани легкого, полученного путем трансбронхиальной биопсии при бронхоскопии.
Зрелые формы p. carinii содержат до восьми спорозоитов. При разрыве пневмоцисты спорозоиты освобождаются, превращаются в трофозоиты и цикл повторяется.
Материал для микроскопии обычно окрашивают gomori methenamine silver (gms), cresyl violet, или toluidine blue. В срезах ткани легкого пневмоцисты идентифицируются по окраске клеточной стенки. Лучший результат получается при окраске gms. gms окраска дает более контрастное изображение тканевых срезов и мазков. Микроорганизмы имеют темно-коричневый или черный цвет.

Рисунок 10. GMS окраска P. carinii в ткани легкого

Рисунок 12. Цисты, содержащие спорозоиты. Окраска по Гимзе (Giemsa)
Для диагностики пневмоцистоза используют также иммунофлюоресцентные, иммуногистохимические методы. В последние годы все более широко начинает применяться метод цепной полимеразной реакции.
Для лечения пневмоцистоза у больных СПИДом предложено много препаратов с многочисленными схемами ведения больных. Такая разнообразная лечебная стратегия объясняется частотой побочных эффектов, которые развиваются у больных, ослабленных самой ВИЧ-инфекцией, вследствие чего терапию пневмоцистоза часто приходится прерывать.
Наиболее длительно применяющимся для лечения Пп препаратом является пентамидин. Дозировки пентамидина не отличаются от таковых у больных без ВИЧ-инфекции, однако частота побочных эффектов значительно выше — 45%. Побочные эффекты развиваются в среднем через 10,4 дня (от 6 до 16 дней): анемия, нейтропения, гипонатриемия, повышение уровня креатинина, почечная недостаточность, брадикардия, панкреатит, гипогликемия или гипергликемия. Для предотвращения указанных эффектов предложено проведение ингаляций пентамидина по 600 мг на 1 ингаляцию. Курс — 21 день. При таком введении препарата отмечено только появление кашля и бронхоспазма, который обычно легко купируется бронходилятаторами. Однако часть исследователей считает, что ингаляционная терапия пентамидином способствует возникновению ранних рецидивов пневмоцистоза, чаще отмечаются внелегочные поражения и спонтанный пневмоторакс. Такие осложнения связаны зачастую с неправильным выбором размера частиц для ингаляций. Если частицы ингаляционной смеси имеют диаметр 10 мкм они оседают или в ротоглотке или в верхних дыхательных путях, оптимальным же является размер частиц до 1-2 мкм в диаметре.
Терапия бисептолом больных СПИДом с Пп также представляет большие трудности из-за частых (45-50%) случаев развития побочных осложнений: 1) сыпь; 2) тошнота/рвота; 3) анемия; 4) нейтропения. Наиболее часто осложнения появляются через 11,5 дней от начала терапии, обычно прекращаются после прерывания лечения.
К препаратам резерва относится дапсон, который назначают по 100 мг перорально в течение 21 дня. В связи с меньшей эффективностью, чем первые два препарата (61%) его не рекомендуют для лечения тяжелых форм пневмоцистоза. Предпочтителен курс лечения дапсоном в сочетании с триметопримом: 100 мг дапсона + 20 мг/кг/день триметоприма (в 4 дозах), курс — 21 день. Эффективность лечения 1 эпизода значительно выше, чем при лечении только дапсоном и составляет около 100%. Основным побочным эффектом от сочетания этих препаратов является развитие гемолиза у больных с дефицитом глюкозо-6-фосфат-дегидрогеназы. Так как эти два препарата обладают взаимоактивирующим действием, побочные эффекты от их сочетания также выше. Среди других значимых осложнений терапии отмечена метгемоглобинурия, при появлении которой препараты необходимо отменять, а больному следует назначить в/в 1-2 мг/кг метиленовой сини.
Применение механической вентиляции легких оценивается неоднозначно: большинство исследователей считают ее применение ненужным и даже противопоказанным из-за снижения сроков выживания у многих больных.
При использовании материалов портала активная ссылка на источник обязательна
Учредитель
Министерство науки и высшего образования
Российской Федерации
Читайте также:
 Пожалуйста, не занимайтесь самолечением!При симпотмах заболевания - обратитесь к врачу.
Пожалуйста, не занимайтесь самолечением!При симпотмах заболевания - обратитесь к врачу.