Лечение лейшманиоза у детей
Кожный лейшманиоз также известная под названиями болезнь Боровского, пендинская язва, годовик, восточная язва. Это локализированная болезнь кожи с типичным изъязвлением и рубцеванием.

Leishmania tropica — вид жгутиконосных паразитических протистов рода Leishmania, возбудитель антропонозного кожного лейшманиоза у взрослых и детей. Данные лейшмании – облигатные паразиты. Человек является естественным их резервуаром. Также лейшмании поселяются в организмах грызунов, собак и даманов. Переносят инфекцию москиты, принадлежащие к виду Phlebotomus sergenti.

Симптомы кожного лейшманиоза у детей проявляются следующим образом: на месте укуса москит возникает одна или несколько папул, которые выглядят как некрупные безболезненные бугорки розового или буроватого оттенка, величина которых до 3 мм. Позже папулы разрастаются, созревая, а через 3-5 месяцев превращаются в язвы, далее покрываются корочкой.

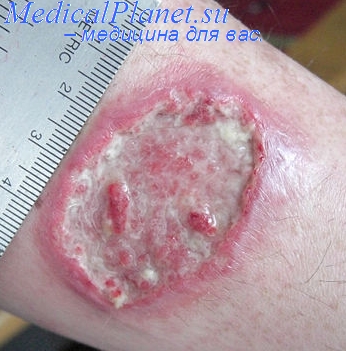
Язвы напоминает кратеры, довольно глубокие. Вокруг них определяется плотный инфильтрат, который возвышается над поверхностью кожи ребенка. На дне язвы – гнойные налеты. В определенный период язвы увеличиваются из-за распада инфильтрата, а к 10-12-му месяцу заболевания они начинают очищаться и заполняться грануляционной тканью. Вместо язвы позже формируется рубец.

От заражения мокнущей формой кожного лейшманиоза до проявления симптомов проходит минимально несколько дней, максимально 1 месяц. На месте попадания инфекции в организм появляется бугорок, он быстро увеличивается и изъязвляется – буквально за 1-2 недели. Формируется язва крупных размеров (15-20 см), края которой подрытые, наличествует обильное серозно-гнойное отделяемое, при пальпации болезненность. Такая язва называется пендинской.

Диагноз кожного лейшамниоза у детей ставят по характерной клинической картине, учитывая эпидемиологические данные, а также обнаруживают возбудитель в биоматериале, взятом со дна язвы и с краевого инфильтрата. В некоторых случаях проводят биологическую пробу на белых лабораторных мышах. Кожный лейшманиоз требует дифференциации с сифилисом, фурункулом, трофическими язвами, лепрой, иными кожными поражениями.

При лечении следует применять примочки из раствора фурацилина, акрихина, грамицидина и мазь Вишневского местно. Также хороший эффект оказывает при данном заболевании мономициновая мазь. Если у ребенка есть обширные инфильтраты, внутримышечно вводят мономицин в дозе, соответствующей возрасту больного. Курс – 7 дней. При присоединении вторичной бактериальной флоры необходима антибиотикотерапия. Также рекомендована стимулирующая и общеукрепляющая терапия.

При профилактике проводите:
- борьбу с москитами и грызунами по существующим актуальным инструкциям.
- как можно раньше выявляют и пролечивают больных детей и взрослых.
- чтобы предупредить распространение инфекции по телу больного, на пораженные участки следует накладывать повязки.
- рекомендованы прививки живой культурой лейшманий.
Диагноз висцерального лейшманиоза подтверждается при обнаружении возбудителя в мазках и при посеве лейкоконцентрата и материала, полученного при пункции селезенки или костного мозга, биопсии печени, пункции или биопсии лимфоузлов. При распространенном в Индии тяжелом висцеральном лейшманиозе и у ВИЧ-инфицированных возбудитель чаще обычного выявляется в моноцитах крови. В пунктате селезенки возбудитель обнаруживается чаще, чем в стернальном пунктате (в 98 и 80—85% случаев соответственно). Пункция селезенки не столь болезненна, но риск осложнений при ней выше. Метод непрямой иммунофлюоресценции позволяет выявить антитела к лейшманиям в 95% случаев.
Чувствительность ИФА и реакции прямой агглютинации превышает 90%. У большинства больных, за исключением страдающих иммунодефицитами (в том числе ВИЧ-инфицированных) и зараженных Leishmania tropica, антитела к лейшманиям обнаруживаются в умеренном или высоком титре.
Результаты кожных проб на аллергические реакции замедленного типа, напротив, становятся положительными лишь после выздоровления. Сегодня поставить диагноз висцерального лейшманиоза можно, не прибегая к пункции внутренних органов или стернальной пункции. Это стало возможным благодаря появлению ПЦР, порог чувствительсти которой — единственный инфицированный макрофаг в 8 мл крови. Исследование среди больных с подтвержденным диагнозом из Индии, Кении и Бразилии показало, что этот метод отличается высокими чувствительностью (90%) и специфичностью (100%). По данным исследования в Судане, ПЦР позволила обнаружить ДНК паразита в 37 из 40 (92%) образцах крови больных висцеральным лейшманиозом
Висцеральный лейшманиоз сопровождается панцитопенией и уменьшением альбумин-глобулинового коэффициента. Последнее изменение обусловлено гипоальбуминемией и гипергаммаглобулинемиеи (преимущественно за счет повышения концентрации IgG), которая развивается в результате выраженной поликлональной активации В-лимфоцитов. Иногда несколько повышена активность аминотрансфераз Лейкопения и анемия (как правило, нормоцитарная нормохромная) отчасти объясняются инфильтрацией паразитами костного мозга и гиперспленизмом. Кроме того, анемии способствуют гемолиз (с положительной пробой Кумбса), кровотечения и гемодилюция. Лейкопения, как правило, сочетается с нейтропенией, выраженной эозинопениеи и относительным лимфоцитозом и моноцитозом.
Дифференциальный диагноз проводят с другими паразитарными инвазиями (такими, как малярия с синдромом тропической спленомегалии, сонная болезнь, шистосомоз и так далее), бактериальными инфекциями (в частности, с милиарным туберкулезом, брюшным тифом и бруцеллезом) и неинфекционными заболеваниями (в частности, с лейкозами, лимфомами, лимфогранулематозом).
Ведущую роль в лечении играют соединения пятивалентной сурьмы используют два препарата: стибоглюконат натрия и меглумина антимонат. Больной должен получать 20 мг/кг/сут пятивалентной сурьмы (максимальная суточная доза 850 мг) в течение 20—28 сут. Ранее считалось, что суточную дозу со временем следует снижать, сегодня от этого подхода отказались. После назначения препаратов необходимо еженедельно определять активность печеночных ферментов, а с 3-й недели лечения — 2 раза в неделю снимать ЭКГ. Лихорадка исчезает уже в первые 4—5 сут лечения. Картина крови на фоне приема препаратов значительно улучшается, в частности возрастает уровень альбумина.
Благоприятным признаком служит появление в крови эозинофилов Однако нормализация лабораторных показателей нередко занимает несколько недель или месяцев. Столь же долго сохраняется спленомегалия. Наиболее достоверный признак стойкого выздоровления — отсутствие рецидива на протяжении по крайней мере 6 мес. Лечение препаратами пятивалентной сурьмы успешно в 80—95% случаев. При рецидиве назначают тот же препарат, но принимать его следует вдвое дольше, чем в предыдущий раз.
Амфотерицин В в дозе 0,5—1,0 мг/кг в/в ежедневно или через день (7—20 мг/кг на курс) эффективен в 98—100% случаев. Липосомный амфотерицин В в дозе 3 мг/кг в/в в течение 5 сут и затем на 10-е сутки был эффективен у 41 больного из 42 (в 98% случаев). В клиническом испытании среди больных с тяжелым висцеральным лейшманиозом, устойчивым к препаратам пятивалентной сурьмы, в 100% случаев был эффективен липидный комплекс амфотерицина В (3 мг/кг через день в/в, всего 5 раз). В Бразилии 20 человек были вылечены холестериновым комплексом амфотерицина В (2 мг/кг/сут в течение 7—10 сут).
Достаточно эффективным считается пентамидин, назначаемый в/в ежедневно или через день в дозе 2—4 мг/кг/сут. Судя по последним данным, препарат дает хорошие результаты при назначении 3 раза в неделю на протяжении 5—9 нед, а побочные эффекты при такой схеме лечения возникают реже.
Некоторым больным после многократных безуспешных попыток лечения препаратами пятивалентной сурьмы в дополнение к ним назначали рекомбинантный интерферон у — мощный активатор макрофагов. В сочетании с препаратами пятивалентной сурьмы можно использовать и паромомицин (15 мг/кг/сут, в/в или в/м). В этом же качестве применяли и аллопуринол внутрь, но результаты были крайне неоднозначны.
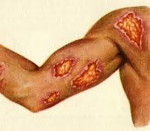
Лейшманиоз представляет собой протозойную инфекцию с трансмиссивным механизмом распространения, характеризующуюся поражением кожных покровов или внутренних органов внутриклеточными паразитами – лейшманиями. Лейшманиозы подразделяют на висциральные, протекающие с поражением легких, печени, селезенки, сердца, и кожные, проявляющиеся трансформирующимися в очаги изъязвления папулами. Диагностика лейшманиоза осуществляется путем выявления лейшманий в крови пациента (при висцеральной форме) или в отделяемом кожных элементов (при кожной форме).
Общие сведения
Лейшманиоз представляет собой протозойную инфекцию с трансмиссивным механизмом распространения, характеризующуюся поражением кожных покровов или внутренних органов внутриклеточными паразитами – лейшманиями.
Характеристика возбудителя
Лейшманиоз вызываются семнадцатью из более чем двадцати видов простейших паразитов рода Leishmania. Лейшмании развиваются внутри клеток хозяина (преимущественно в макрофагах и элементах ретикулоэндотелиальной системы). В течение своего жизненного цикла им необходимо сменить двух хозяев. В организме позвоночных животных лейшмании находятся в безжгутиковой форме, развиваясь в жгутиковую форму в теле членистоногого. Лейшмании отличаются резистентностью к антибиотикам, и чувствительны к препаратам пятивалентной сурьмы.
Подавляющее большинство лейшманиозов – зоонозы (резервуаром и источником инфекции являются животные), только два вида – антропонозы. Виды животных, участвующих в распространении лейшманиоза, довольно ограничены, поэтому инфекция является природно-очаговой, распространяется в пределах обитания соответствующей фауны: грызунов песчаниковых видов, псовых (лисы, собаки, шакалы), а также переносчиков – москитов. Преимущественно очаги лейшманиоза располагаются в странах Африки и Южной Америки. Большинство из них - развивающиеся, среди 69 стран, где распространен лейшманиоз, 13 являются беднейшими странами мира.
Человек является источником инфекции в случае поражения кожной формой лейшмании, при этом москиты получают возбудителя с отделяемым кожных язв. Висцеральная лейшмания в подавляющем большинстве случаев является зоонозной, москиты заражаются от больных животных. Заразность москитов отсчитывается с пятого дня попадания лейшманий в желудок насекомого и сохраняется пожизненно. Человек и животные контагиозны в течение всего срока пребывания возбудителя в организме.
Лейшманиоз передается исключительно с помощью трансмиссивного механизма, переносчики – москиты, получают инфекцию, питаясь кровью больных животных, и переносят здоровым особям и людям. Человек обладает высокой восприимчивостью к инфекции, после перенесения кожного лейшманиоза сохраняется продолжительный стойкий иммунитет, висцеральная форма такового не формирует.
Патогенез
Возбудитель проникает в толщу кожи человека при укусе москита, формируя в области входных ворот лейшманиозную гранулему. Впоследствии, при висцеральной форме инфекции гранулема рассасывается, а при кожной - прогрессирует в язву. Лейшмании разносятся по организму с током лимфы, поражая регионарные лимфатические узлы. Вдоль лимфатического сосуда паразиты могут формировать лейшманиомы – ряд последовательно располагающихся специфических язв.
В Южной Америке отмечаются формы лейшмании, протекающие с поражением слизистых оболочек ротовой полости, носоглотки и верхних дыхательных путей с грубой деформацией глубоких тканей и развитием полипозных образований. Висцеральная форма лейшманиоза развивается в результате рассеивания возбудителя по организму и попадания в печень, селезенку, костный мозг. Реже – в кишечную стенку, легкие, почки и надпочечники.
Возникающий иммунный ответ подавляет инфекцию, при этом заболевание протекает латентно, либо с маловыраженной симптоматикой. При иммунодефиците, сниженных защитных свойствах лейшманиоз прогрессирует, протекает с выраженной клиникой интоксикационного синдрома, лихорадкой. Размножение паразитов в печени способствуют замещению гепатоцитов фиброзной тканью, в селезенке отмечают атрофию пульпы с участками инфарктов и некротизации. Вследствие поражения костного мозга развивается анемия. В целом висцеральный лейшманиоз, прогрессируя, вызывает общую кахексию.
Классификация
Лейшманиозы подразделяются на висцеральные и кожные формы, каждая форма, в свою очередь, разделяется на антропонозы и зоонозы (в зависимости от резервуара инфекции). Висцеральные зоонозные лейшманиозы: детский кала-азар (средиземноморско-среднеазиатский), лихорадка дум-дум (распространена в восточной Африке), носоглоточный лейшманиоз (кожно-слизистый, лейшманиоз Нового Света).
Индийский кала-азар является висцеральным антропонозом. Кожные формы лейшманиоза представлены болезнью Боровского (городской антропонозный тип и сельский зооноз), пендинской, ашхабадской язвами, багдадским фурункулом, эфиопским кожным лейшманиозом.
Симптомы лейшманиоза
Инкубационный период этой формы лейшманиоза составляет от 20 дней до нескольких (3-5) месяцев. Иногда (довольно редко) затягивается до года. У детей раннего возраста в этот период может отмечаться первичная папула в месте внедрения возбудителя (у взрослых встречается в редких случаях). Инфекция протекает в острой, подострой и хронической формах. Острая форма обычно отмечается у детей, характеризуется бурным течением и без должной медицинской помощи заканчивается летально.
Чаще всего встречается подострая форма заболевания. В начальном периоде отмечается постепенное нарастание общей слабости, разбитости, повышенной утомляемости. Отмечается снижение аппетита, побледнение кожи. В этом периоде при пальпации можно выявить некоторое увеличение размеров селезенки. Температура тела может подниматься до субфебрильных цифр.
Подъем температуры до высоких значений говорит о вступлении заболевания в период разгара. Лихорадка имеет неправильный или волнообразный характер, продолжается в течение нескольких дней. Приступы лихорадки могут сменяться периодами нормализации температуры или снижения до субфебрильных значений. Такое течение обычно продолжается 2-3 месяца. Лимфатические узлы увеличены, отмечается гепато- и, в особенности, спленомегалия. Печень и селезенка при пальпации умеренно болезненны. При развитии бронхоаденита отмечается кашель. При такой форме нередко присоединяется вторичная инфекция дыхательной системы и развивается пневмония.
С прогрессированием заболевания отмечается усугубление тяжести состояния больного, развивается кахексия, анемия, геморрагический синдром. На слизистых оболочках ротовой полости возникают некротизированные участки. Ввиду значительного увеличения селезенки происходит смещение сердца вправо, тоны его глухие, ритм сокращений ускорен. Отмечается склонность к падению периферического артериального давления. С прогрессированием инфекции формируется сердечная недостаточность. В терминальном периоде больные кахексичны, кожные покровы бледные и истонченные, отмечаются отеки, выражена анемия.
Хронический лейшманиоз протекает латентно, либо с незначительной симптоматикой. Антропонозный висцеральный лейшманиоз может сопровождаться (в 10% случаев) появлением на коже лейшманоидов – мелких папиллом, узелков или пятен (иногда просто участки со сниженной пигментацией), содержащих возбудителя. Лейшманоиды могут существовать годами и десятилетиями.
Распространен в тропическом и субтропическом климате. Инкубационный период его составляет 10-20 дней, может сокращаться до недели и удлиняться до полутора месяцев. В области внедрения возбудителя при этой форме инфекции обычно формируется первичная лейшманиома, первоначально имеющая вид розовой гладкой папулы около 2-3 см в диаметре, в дальнейшем прогрессирующей в безболезненный или малоболезненный при надавливании фурункул. Спустя 1-2 недели в лейшманиоме формируется некротический очаг, и вскоре образуется безболезненное изъязвление с подрытыми краями, окруженное валиком инфильтрированной кожи с обильным отделяемым серозно-гнойного или геморрагического характера.
Отличается значительной распространенной инфильтрацией кожи. Со временем инфильтрат регрессирует, не оставляя последствий. В исключительных случаях отмечаются мелкие язвы, заживающие без заметных рубцов. Такая форма лейшманиоза достаточно редка, обычно отмечается у пожилых лиц.
Наблюдается в основном у детей и молодых людей. При этой форме вокруг послеязвенных рубцов или на них появляются мелкие бугорки, могущие увеличиваться в размерах и сливаться друг с другом. Изъязвляются такие бугорки редко. Язвы при этой форме инфекции оставляют значительные рубцы.
Характеризуется продолжительным инкубационным периодом, который может достигать нескольких месяцев и лет, а также медленным развитием и умеренной интенсивностью кожных поражений.
Осложнения лейшманиоза
Длительно протекающий лейшманиоз прогрессирует с развитием пневмонии, нефритов, агранулоцитоза, геморрагического диатеза, а также может осложняться гнойно-некротическими воспалениями.
Диагностика лейшманиоза
Общий анализ крови при лейшманиозе показывает признаки гипохромной анемии, нейтропении и анэозинофилии при относительном лимфоцитозе, а также пониженную концентрацию тромбоцитов. СОЭ повышена. Биохимический анализ крови может показать гипергаммаглобулинемию. Выделение возбудителя кожного лейшманиоза возможно из бугорков и язв, при висцеральном - лейшмании обнаруживаются в посеве крови на стерильность. При необходимости для выделения возбудителя производят биопсию лимфоузлов, селезенки, печени.
В качестве специфической диагностики осуществляют микроскопическое исследование, бакпосев на питательной среде NNN, биопробы на лабораторных животных. Серологическая диагностика лейшманиоза проводится с применением РСК, ИФА, РНИФ, РЛА. В периоде реконвалесценции отмечается позитивная реакция Монтенегро (кожная проба с лейшманином). Производится при эпидемиологических исследованиях.
Лечение лейшманиоза
Этиологическое лечение лейшманиоза заключается в применении препаратов пятивалентной сурьмы. При висцеральной форме их назначают внутривенно с нарастанием дозировки на 7-10 дней. В случае недостаточной эффективности терапию дополняют амфотерицином В, вводимым с 5% раствором глюкозы внутривенно медленно. На ранних стадиях кожного лейшманиоза бугорки обкалывают мономицином, сульфатом берберина или уротропином, а также назначают эти препараты в виде мазей и примочек.
Сформировавшиеся язвы являются показанием к назначению мирамистина внутримышечно. Для ускорения заживления язв эффективна лазерная терапия. Препаратами резерва при лейшманиозе являются амфотерицин В и пентамидин, их назначают в случаях рецидивирования инфекции и при резистентности лейшманий к традиционным средствам. Для повышения эффективности терапии можно добавить человеческий рекомбинантный гаммаинтерферон. В некоторых случаях бывает необходимо хирургическое удаление селезенки.
Прогноз и профилактика лейшманиоза
При легко протекающем лейшманиозе возможно самостоятельное выздоровление. Благоприятен прогноз при своевременном выявлении и должных медицинских мерах. Тяжелые формы, инфицирование лиц с ослабленными защитными свойствами, отсутствие лечения значительно ухудшают прогноз. Кожные проявления лейшманиоза оставляют косметические дефекты.
Профилактика лейшманиоза включает меры по благоустройству населенных пунктов, ликвидацию мест расселения москитов (свалок и пустырей, затопленных подвальных помещений), дезинсекцию жилых помещений. Индивидуальная профилактика заключается в использовании репеллентов, других средств защиты от укусов москитов. При обнаружении больного производят химиопрофилактику пириметамином в коллективе. Специфическая иммунная профилактика (вакцинация) производится лицам, планирующим посещение эпидемически опасных районов, а также неимунному населению очагов инфекции.
Аннотация научной статьи по клинической медицине, автор научной работы — Кузьменко Л.Г., Хайтам Ажамаль Шайф
Похожие темы научных работ по клинической медицине , автор научной работы — Кузьменко Л.Г., Хайтам Ажамаль Шайф
Таблица 7. Продолжительность обнаружения антигенов возбудителей в носовых ходах детей и частота внутрибольничных ОРИ на фоне приема препаратов интерферона
Группы наблюдения До лечения После лечения Частота ВБИ,%
Обследовано детей Из них ИФ+, (абс/%) Через 2—3 дня Через 4—5 дней
Всего В том числе > 2 антигена Обследовано детей Из них ИФ+, (абс/%) Обследовано детей Из них ИФ+, (абс/%)
Всего В том числе > 2 антигена
А 1 96 66/68,8 21/31,8 58 30/51,7* 0* ** 30 3/10,0* ** 8,9**
2 70 46/65,7 9/19,6 37 24/64,9 10/41,7* 24 8/33,3 23,0
Б 1 39 28/74,4 11/39,2 22 12/54,5* 0* 21 0* 7,7
2 27 18/66,7 4/22,2 23 7/30,4* 0 20 0* 7* 3,
3 32 20/66,6 4/20,0 18 12/66,7 2/16,7 16 2/12,5* 18,8
А: 1 — гриппферон, 2 — контроль; Б: 1 — интерген, 2 — интерген +ремантадин, 3 — плацебо; * — различия показателей достоверны по отношению к данным до лечения; ** — по отношению к контролю / плацебо; ВБИ — внутрибольничные инфекции
инфекций. Одновременное использование интергена и этиотропного химиопрепарата было более эффективным. Введение препаратов рекомбинантного Ифн а-2 оказывает интерферониндуцирующее и иммунореабили-тирующее действия. Результаты полученных исследований позволяют рекомендовагь названные препараты для включения их в терапию гриппа и других ОРИ у детей.
1. Учайкин В. ф. Острые респираторные заболевания (ОРЗ) у детей // Детский доктор. — 1999. — № 1. — С. 33.
2. Ершов ф. И. Система интерферона в норме и при патологии. — М.: Медицина, 1996.
3. С. А. Кетлинский. Иммунология для врачей / С. А. Кетлинский, Н. М. Калинина // Руководство для врачей. — СПб: Гиппократ, 1998. — 156 с.
4. П. Гапонюк. Гриппферон капли в нос. Профилактика и лечение гриппа и острых респираторных вирусных инфекций / П. Гапонюк, С. А. Коровкин. — М., 2004. — 38 с.
5. Экспериментальное изучение ингибирующей активности гриппферона в отношении некоторых актуальных вирусов, вызывающих поражение респираторного тракта / В. М. Гусева и др. // Мат. Всеросс. НПК «Новые препараты в про-
6. Современные подходы к лечению различных форм дифтерии у детей / В. В. Иванова и др. // Современные подходы в лечении некоторых актуальных инфекций в педиатрической и акушерской практике. Сб. методических рекомендаций и пособий для врачей. — СПб., 1999. — С. 20—43.
8. Методические указания по лабораторным методам диагностики гриппа и других ОРЗ / Приложение 4 к Приказу Минздравмедпрома России, Госкомсанэпиднадзора и РАМП, № 101/46 от 19.04.95. — М., 1995. — С. 28—43.
9. Лабораторная диагностика острых респираторных и других вирусных инфекций / А. А. Соминина и др. // Грипп и другие респираторные вирусные инфекции: эпидемиология, профилактика, диагностика и терапия. — СПб., 2003. — С. 70—95.
10. Метод исследования интерферонового статуса по пробам цельной крови / С. С. Григорян и др. // Вопр. вирусологии — 1988. — № 4. — С. 433—436.
опыт лечения висцерального лейшманиоза у аетей с применением тактивина
Джамаль Шайф Хайтам, Л. Г. Кузьменко
российский университет дружбы народов, радфан, москва (йемен, россия)
Как известно, лейшманиозы — это группа трансмиссивных протозойных болезней человека и животных, возбудители которых передаются двукрылыми
кровососущими насекомыми москитами. Москиты принадлежат к семейству Phlebotoinidae отряда Díptera. Ареал их распространения ограничен следующими кли-
матическими факторами: температура в течение 4 месяцев должна быть не ниже 18 °С, средняя температура воздуха в холодные месяцы — не ниже _6 °С [1].
Одним из эндемичных очагов лейшманиоза является Аравийский полуостров. Заболевание встречается в Саудовской Аравии, Омане, Йемене. На территории Йемена, по данным Министерства здравоохранения Йемена, в 1997 г. было зарегистрировано 9572 больных кожным и висцеральным лейшманиозом, проживавших в 5 из 17 провинций. Все указанные провинции были эндемичными по висцеральному лейшманиозу. При этом в разных провинциях заболевание встречалось с разной частотой: в трех провинциях количество больных было в пределах от 10 до 70, в то время как в других двух — превышало 4500. Такая неравномерность распределения лейшманиоза объяснялась как некоторыми социально-экономическими особенностями разных провинций, так и массовым проведением профилактических мероприятий, направленных на борьбу с переносчиками на разных стадиях их развития [4].
На территории бывшего Советского Союза очаги лейшманиоза были в Узбекистане [1, 8], Азербайджане, Армении, Грузии [5—7]. Однако, учитывая в настоящее время повсеместно распространенную миграцию населения, завозные случаи этого заболевания могут встречаться в местностях неэндемичных по лейшманиозу, как это, например, случилось в Москве [6], Санкт-Петербурге [9], Казани [10].
По данным А. Мушары [4] у детей, находившихся под его наблюдением, висцеральный лейшманиоз часто сочетался с другими заболеваниями, при этом на-
блюдалась возрастная зависимость: у детей в возрасте от 6 мес. до 2 лет висцеральный лейшманиоз сочетался с тяжелой степенью гипотрофии, от 2 до 4 лет — с относительно небольшим дефицитом массы тела, малярией, гельминтозами и острой пневмонией, у детей старше 4 лет — с малярией.
При отсутствии лечения прогноз висцерального лейшманиоза, как правило, неблагоприятный, болезнь заканчивается летальным исходом. При легких формах возможно спонтанное выздоровление.
Для лечения висцерального лейшманиоза применяются разные средства, в том числе диамидены (стиль-бамидин, пентамидин, изотионат) [8], амфотерицин В [11]. Однако наибольшее распространение и наибольшую эффективность имеют препараты сурьмы жирного, ароматического и алифатического рядов, при этом чаще используются соединения алифатического ряда, производимые в разных странах: солюстибазан (ФРГ), сольсурьмин (СССР), пентостам (Англия), глюконтим. Недостатком этих препаратов является их высокая токсичность. В связи с этим предлагаются разные модификации использования препаратов сурьмы с целью уменьшения их дозы [4].
Целью данного исследования явилась оценка эффективности в комплексном лечении висцерального лейш-маниоза у детей иммуномодулирующего препарата так-тивина, полученного в России в лаборатории молекулярной иммунологии (зав. лабораторией — академик РАЕН, д.б.н., профессор В. Арион) НИИ физико-химической медицины МЗ и СР РФ (директор — академик РАМН, д.м.н., профессор Ю. М. Лопухин). Основанием послужили наблюдения высокой эффективности действия данного препарата при включении его в комплекс лечения детей, страдавших острыми и затяжными пневмониями, сепсисом, хроническом пиелонефритом, инфекционным эндокардитом, остеомиелитом и рядом других болезней, включая заболевания, ассоциированные с некоторыми внутриклеточными патогенами (Mycop/asma pneumoniae, Mycoplasma hominis, микроорганизмы семейства Ch/amidiaceae).
Материалы и методы исследования
Под нашим наблюдением в районном госпитале Радфана (Йемен) в течение 2004 года находились 24 ребенка, страдавших висцеральным лейшма-ниозом, в возрасте 5 месяцев — 11 лет (мальчиков 16, девочек 8). По возрасту наблюдавшиеся дети распределялись следующим образом: 5—12 мес. — 6 детей, 1—3 года — 9, 4—7 лет — 6, 8—11 лет — 3 ребенка.
Таким образом, почти 90% наблюдавшихся детей были в дошкольном возрасте.
У 12 детей в возрасте от 10 мес. до 7 лет кроме висцерального лейшманиоза, сопутствующих заболеваний не было. У другой половины наблюдавшихся детей в возрасте от 5 месяцев до 11 лет, помимо висцерального лейшманиоза, были сопутствующие заболевания: пневмония (у 5 детей в возрасте от 10 мес. до 1 г. 8 мес.), тяжелая степень белково-энергетической недостаточности у 1 ребенка, резкое снижение массы тела — у 1 ребенка ( в возрасте 6 лет), малярия (у 4 детей), гельминтозы (амебиаз, гардиаз у 3 детей в возрасте от 8 до 11 лет), брюшной тиф (у 1 ребенка
Таблица 1. Сравнительная эффективность двух схем терапии детей с изолированным вариантом висцерального лейшманиоза
5 месяцев). У 5 детей висцеральный лейшманиоз сочетался с двумя заболеваниями (гипотрофия и брюшной тиф, пневмония и малярия, гипотрофия и два гельминтоза, инвазия несколькими гельминтами).
Диагностика висцерального лейшманиоза проводилась с учетом эндемичности местности, из которой поступал ребенок, клинических проявлений (лихорадочная реакция, анемия, гепато- и спленомегалия, выраженная лимфаденопатия, выраженная лейкопения, тромбоцитопения) и экспресс-теста на лейшманиоз — Рогта1де1-тест. Этот тест, как известно, помимо лейшманиоза, может быть положительным только при малярии, в связи с чем его пытаются отнести к числу неспецифических тестов. Однако диагностика малярии у наблюдавшихся пациентов осуществлялась по обнаружению малярийных плазмодиев в толстой капле крови.
1 группа — дети, получавшие терапию указанным препаратом по традиционной схеме: препарат назначался из расчета 20мг/кг/сут внутримышечно ежедневно в течение 20 дней. Такое лечение получили 9 детей в возрасте 10 мес. — 6 лет, у которых висцеральный лейшманиоз не сочетался ни с какими другими заболеваниями.
2 группа была представлена тремя детьми в возрасте от 1г. 1 мес. до 3 лет, у которых кроме висцерального лейшманиоза, не было также выявлено никаких других заболеваний.
3 группа состояла из 12 пациентов, у которых имела место микстинфекция или микстинвазия (висцеральный лейшманиоз у этих детей сочетался с одним или двумя перечисленными заболеваниями: малярией, пневмонией, глистной инвазией, тяжелой степенью гипотрофии, брюшным тифом). Дети 2 и 3 групп получали пентостам в дозе 10 мг/кг/сут внутримышечно в течение 14 дней и тактивин в дозе 2 мкг/кг на одно введение подкожно 1 раз в сутки ежедневно. Препарат вводился после 16 часов. Курс лечения тактивином состоял из 5 инъекций в стационаре с последующими двумя ежедневными введениями в домашних условиях. Таким образом, курс лечения тактивином состоял из
Поскольку Рогта1де1-тест может сохраняться у пациента в течение некоторого времени после излечения, то основным методом оценки эффективности терапии служило клиническое наблюдение. Эффективность лечения оценивалась по исчезновению лихорадочной реакции, нормализации размеров печени, селезенки, лимфатических узлов, улучшению общего состояния ребенка, нормализации показателей периферической крови, отсутствию рецидивов.
Результаты и их обсуждение
При поступлении в госпиталь у детей наблюдалось повышение температуры тела до 38,5—40,0 °С, увеличение шейных, подмышечных, паховых лимфатических узлов до 1—1,5 см в диаметре, селезенки и печени (выступали ниже края реберной дуги на 3—12 и 2—
8 см соответственно), снижение концентрации гемоглобина до 35 — 88 г/л; количество лейкоцитов колебалось в пределах 2,9 X 109/л — 7,4 X 109/л. У детей с изолированным висцеральным лейшманиозом клинические проявления были менее выраженными. Исходные данные у детей 1 и 2 групп были идентичными. Наибольшая тяжесть состояния была у детей, у которых висцеральный лейшманиоз сочетался с малярией или пневмонией.
Таблица 2. Сравнительная эффективность терапии висцерального лейшманиоза у детей 1 и 3 групп
Показатели Интервал времени (дни), в течение которого происходила нормализация показателей, М ± т Уровень значимости различия результатов, р
1 группа, п = 9 3 группа, п= 12
Нормализация температуры тела 5,4 ± 0,2 4,1 ± 0,3 Не можете найти то, что вам нужно? Попробуйте сервис подбора литературы.
Нормализация размеров печени 10,5 ± 0,8 11,5 ± 0,8 > 0,05
Показатели Интервал времени (дни), в течение которого происходила нормализация показателей, М ± т Уровень значимости различия результатов, р
1 группа, п = 9 2 группа, п = 3
Нормализация температуры тела 5,4 ± 0,2 3,7 ± 0,7 0,05
Данные клинического наблюдения, приведенные в таблице 1, свидетельствуют о более высокой эффективности терапии у детей 2 группы по сравнению с пациентами 1 группы. Помимо этого у детей, получавших в комплексном лечении тактивин, в крови быстрее увеличивалось содержание лейкоцитов. Так, при одинаковом исходном уровне лейкоцитов до лечения (М + т), равном 4,5 + 0,08 X 109/л, на 3-й день от начала лечения у детей первой группы их содержание составило 4,8 + 0,09 X 109/л, у детей второй группы — 5,7 ± 0,2 X 109/л, (р Не можете найти то, что вам нужно? Попробуйте сервис подбора литературы.
Читайте также:


