Холинергическая интоксикация что это такое

Анестезиология – бурно развивающаяся специальность, в этой области проводится множество исследований, выпускается большое количество книг и клинических рекомендаций, развивается международный обмен.
Так, в немецкоязычных источниках всегда можно найти информацию, посвященную ЦАС. В больших изданиях ему отведены целые главы, что неудивительно: ведь по мнению немецких авторов, частота осложнения достигает 1 случая на 10 общих анестезий!
Таким образом, более или менее системный подход к описанию центрального антихолинергического синдрома в анестезиологии ограничивается только изданиями на немецком и обзорными статьями на испанском языках.
В литературе на русском, английском, французском, итальянском языках ЦАС упоминается почти исключительно в литературе по токсикологии. Тем заметнее статьи, в которых поднимаются вопросы, связанные с указанным синдромом. Например, в 1977 г. Baraka и Harik выпустили статью, посвященную использованию галантамина в лечении этого состояния. Несмотря на важность этого исследования, в целом проблема ЦАС в остальной мировой литературе по анестезиологии не ставится, информация об этом синдроме отрывочна и встречается на удивление редко.
В большинстве источников отдельные формы и симптомы его упоминаются по отдельности, без патогенетического объединения в ЦАС, и соответственно предлагается симптоматическое лечение, тогда как немецкие и испанские источники предлагают единый подход к терапии.
С чем может быть связано такое показательное различие в отношении к одному состоянию? Очевидно, что вопрос здесь не в существовании или отсутствии определенного состояния как клинического факта, а в подходе к его анализу и ведению пациентов, у которых оно развивается. Для ответа на этот вопрос следует подробнее рассмотреть само явление.
Итак, что представляет собой центральный антихолинергический синдром? Его можно определить как состояние, обусловленное относительным или абсолютным недостатком ацетилхолина в синапсах ЦНС, когда холинолитические влияния на холинергические рецепторы преобладают над холиномиметическими. Первое описание такого состояния относится к 1958 г. (Forrer), но термин был предложен V. Longo спустя 8 лет.
Эпидемиологические характеристики в разных источниках различаются, частота встречаемости лежит в пределах от 1 до 11% (по данным других обзоров 2-9%). Большинство случаев ЦАС (до 9,4%) возникает после общей анестезии, а после регионарной в сочетании с седацией частота составляет около 3,3%. У седатируемых пациентов на продленной ИВЛ, находящихся в отделении интенсивной терапии, синдром наблюдается примерно в 5% случаев. Если взять максимальную частоту, то получается, что в операционной мы сталкиваемся с ЦАС в каждом 10-м случае, что совсем не редко.
Что касается токсикологической практики, по данным Американской ассоциации центров контроля отравлений (American Association of Poison Control Centers), в 2007 г. в США выявлены 8582 человека с антихолинергическим синдромом, из них у 13 он угрожал жизни, но смертельных исходов не зарегистрировано. В 2008 г. количество случаев составило около 20 тыс., из них 46 тяжелых, но ни одного летального. Всего за 1997-2004 гг. был зарегистрирован 51 случай смерти при этом состоянии.
Антихолинергический синдром примерно с одинаковой частотой встречается у мужчин и женщин. Чаще его можно наблюдать у взрослых, но описан он также у детей и лиц пожилого и старческого возраста.
Клиническая картина центрального антихолинергического синдрома может проявляться в периоде выхода из анестезии в трех формах: коматозной, ажитированной и форме посленаркозной мышечной дрожи. Кроме того, при развитии этого синдрома наблюдаются и периферические симптомы холинергической недостаточности (которые могут отсутствовать, если пациенту проводилась декураризация).
Центральные симптомы включают дезориентацию, угнетение сознания, эмоциональную лабильность, головокружение, атаксию, галлюцинации, психомоторное возбуждение, судороги, амнезию, центральную гиперпирексию, угнетение дыхания.
Коматозная форма проявляет себя угнетением сознания (вплоть до комы) и двигательной активности, сонливостью. Для ажитированной формы характерно наличие психомоторного возбуждения, дезориентации, судорог, галлюцинаций. Остальные симптомы, встречающиеся при ЦАС, наблюдаются при обеих формах синдрома.
Описанная клиническая картина не является полностью специфичной для ЦАС, поэтому для постановки диагноза требуется исключить иные причины, приводящие к указанным симптомам. Список причин, которые надо исключить, обширен и включает гипоксию, гиперкапнию, остаточный эффект миорелаксантов, передозировку опиоидов, судороги, парадоксальные или побочные эффекты транквилизаторов, психоз, передозировку противопаркинсонических средств, делирий.
Выраженные изменения гликемии, нарушение водно-электролитного баланса и эндокринная патология, начальные симптомы сепсиса, болезни Альцгеймера, постагрессивный синдром, психические заболевания, симптомы отмены алкоголя или наркотических средств также могут формировать клиническую картину, сходную с ЦАС.
Некоторые авторы говорят, что следует дифференцировать ЦАС со злокачественной гипотермией, злокачественным нейролептическим синдромом и серотониновым синдромом. Они могут в какой-то мере симулировать ЦАС, но все же совокупность наблюдаемых симптомов позволяет его дифференцировать.
Общий механизм, лежащий в основе ЦАС, – недостаточность эффектов ацетилхолина. Но если механизм один, почему клиническая картина включает в себя такое разнообразие зачастую противоположных симптомов как центральных, так и периферических? Это объясняется фармакологией холинорецепторов и их распределением в организме.
Как известно, они подразделяются на две группы: М- и Н-холинорецепторы. Первая группа возбуждается ацетилхолином и мускарином, в ней выделяют 5 подтипов: М1–М5. Все они влияют на синаптическую передачу через G-белки. Действие ацетилхолина на подтипы М1, 3, 5 реализуется через Gq-белок, что выражается в проявлении эффектов возбуждения. М2, 4-холинорецепторы связаны с Gi-белками, поэтому в результате их стимуляции развиваются тормозные эффекты.
М-холинорецепторы представлены в различных органах и тканях, причем соотношение подтипов рецептора зависит от органа: М1-рецепторы: ЦНС, вегетативные ганглии; М2-рецепторы: сердце; М3-рецепторы: гладкие мышцы, экзокринные железы; М4-рецепторы: ЦНС, сердце, стенки альвеол; М5-рецепторы: ЦНС, слюнные железы, радужная оболочка, мононуклеары крови.
Вторая группа рецепторов возбуждается ацетилхолином и никотином. Эти рецепторы располагаются в нервно-мышечных синапсах, вегетативных ганглиях, ЦНС и каротидных клубочках. Н-холинорецептор – это ионный канал, проницаемый для ионов натрия и калия и в меньшей степени для двухвалентных катионов. При контакте с лигандом-агонистом канал открывается, вызывая деполяризацию мембраны клетки и возникновение потенциала действия.
Стимуляция М-холинорецепторов приводит к известным периферическим эффектам активации парасимпатической нервной системы. Это вазодилатация, отрицательные хронотропный и инотропный эффекты; бронхоспазм; миоз; увеличение секреции экзокринных желез; повышение тонуса, сократимости и перистальтики желудочно-кишечного тракта; тошнота, рвота; сокращение мускулатуры мочевого пузыря, уменьшение его емкости, расслабление сфинктеров. Блокада этих рецепторов приводит к возникновению обратных эффектов.
Стимуляция Н-холинорецепторов приводит к появлению потенциала действия и передаче возбуждения на другой нейрон или на волокно поперечной полосатой мышцы. Стоит заметить, что при аномально высокой концентрации в синаптической щели ацетилхолин способен вызывать стойкую деполяризацию постсинаптической мембраны, нарушая проведение сигнала.
Суммируя сказанное, можно заключить, что разнообразие клинических проявлений ЦАС при едином механизме, их вызывающем, обусловлено различиями физиологического действия разных типов и подтипов холинорецепторов. В частности, существование взаимно-полярных коматозной и ажитированной форм синдрома находит объяснение в различии у разных пациентов функционального состояния и экспрессии представленных в структурах ЦНС М1-, М4-, М5- и Н-холинорецепторов.
Предметом данного обзора является ЦАС после общей анестезии. Синдром этот полиэтиологичен и может быть вызван множеством препаратов, различающихся по механизму действия.
В немецкоязычных руководствах приводятся списки лекарств, которые могут вызывать симптомы ЦАС. Они включают антихолинергические препараты (атропин, скополамин), H1- и Н2-гистаминоблокаторы (например, дифенгидрамин, зантак), противопаркинсонические (акинетон), барбитураты (тиопентал), бензодиазепины (мидазолам, диазепам), ингаляционные (севофлуран, десфлуран) и неингаляционные (кетамин, пропофол, этомидат) анестетики, местные анестетики (лидокаин, мепивакаин), мидриатики (гоматропин, тропикамид), нейролептики (галоперидол), опиоиды (фентанил, морфин), антиспастические (оксибутинин, толтерондин), три- и тетрациклиновые антидепрессанты (элавил, имипрамин) и этанол.
В качестве основных триггеров ЦАС обычно называют атропин, дроперидол, летучие анестетики, пропофол, бензодиазепины, опиаты и кетамин. На возникновение синдрома могут влиять определенные факторы риска, к которым относят особенности организма пациента, вид хирургического вмешательства, метод анестезии и применяемые в ее ходе препараты.
С точки зрения понимания роли и места ЦАС особенно интересно использование для анестезии взаимодействия скополамина и морфина. Известно, что в отличие от атропина скополамин оказывает центральное депрессивное действие. Сначала он угнетает моторные центры, что приводит к снижению тонуса мышц, а затем вызывает седацию, которой могут предшествовать симптомы возбуждения ЦНС (галлюцинации).
При применении его вместе с малыми дозами морфина анальгетический эффект последнего существенно усиливается. Однако сочетание морфина с дозами скополамина, которые сами по себе не действуют наркотически, вызывает общую анестезию. Такая схема анестезии впервые использована Schneiderlin и Korff в 1902 г. Вероятно, морфино-скополаминовый наркоз был исторически самой первой схемой общей анестезии в том смысле, как она стала пониматься значительно позднее: скополамин использовался в качестве гипнотика, а анальгезию обеспечивал морфин. Позже метод был признан опасным в отличие от применения этих препаратов для премедикации перед ингаляционной анестезией, когда использовались меньшие дозы морфина и скополамина.
Следующий яркий пример использования холинолитической активности для угнетения сознания относится к середине XX века. В 1958 г. американские ученые Forrer и Miller описали лечение шизофрении с помощью атропиновой комы. Суть метода – использование атропина в дозах, которые вызывают утрату сознания: сначала 75-125 мг однократно, затем до 275-300 мг. Длится такая кома 3-4 ч, а купируется физостигмином или, что особенно интересно в контексте данного обзора, галантамином.
К началу 1960-х годов интерес к методу ослабевает из-за технической сложности, необходимости постоянного присутствия врача, а также в связи с выраженными вегетативными реакциями. Метод переживал волнообразные колебания интереса, с конца 1980-х – начала 1990-х годов в западной литературе упоминания о нем не встречаются, а в странах СНГ интерес к нему вновь появился с 2000-х годов.
И все же указания об использовании с гипнотической целью холинолитических препаратов присутствуют в мировой литературе по сей день. Например, в руководстве Р. Миллера в главе об анестезии при травмах сказано, что у пациентов с жизнеугрожающей гиповолемией при быстрой последовательной индукции можно обойтись вообще без анестетиков, одними миорелаксантами, а использование скополамина в такой ситуации может предотвратить формирование памяти на происходящие события.
Диагностика ЦАС затруднена из-за неосведомленности врачей о существовании такого синдрома, отсутствия специфичных объективных тестов, а также из-за наличия состояний, имеющих схожие с ЦАС признаки. Для постановки диагноза необходимо наличие минимум одного центрального и двух периферических симптомов. Однако в ряде случаев периферические симптомы могут отсутствовать, например, при использовании прозерина в конце анестезии. Прежде чем принять ЦАС в качестве диагноза надо исключить, как указано выше, другие причины нарушенного пробуждения пациента.
Основное требование к лечебным мероприятиям – поддержание витальных функций пациента. После исключения других причин нарушенного пробуждения проводят лечение, которое само по себе является и критерием диагностики ЦАС. В качестве специфического лекарственного средства в немецких источниках рекомендовано исключительно применение физостигмина (ингибитора ацетилхолинэстеразы).
Для лечения ЦАС физостигмин вводится внутривенно медленно в дозе 0,03-0,04 мг/кг. Начало эффекта отмечается спустя 5-15 мин, а продолжительность действия составляет 20-45 мин (до 2 ч по другим данным). При необходимости введения дополнительных доз физостигмина его вводят из расчета 1 мг каждые 20-30 мин или дозатором в темпе 1-2 мг/ч до исчезновения симптоматики. Физостигмин подвергается гидролизу и ферментативной биодеградации, продукты метаболизма неактивны и выводятся в основном почками.
Побочные эффекты его типичны для холиномиметических препаратов. Для их купирования можно применять холинолитик гликопирролат, который не проникает через ГЭБ, устраняя периферические побочные эффекты физостигмина. Противопоказания для физостигмина включают абсолютные (глаукома, миотоническая миодистрофия, свежий инсульт, отравление арилфосфатами) и относительные (аритмии, сахарный диабет, ИБС, язвенная болезнь, бронхиальная астма).
Кроме применения специфического антидота, в литературе предлагаются и другие меры, которые следует предпринять у пациента, у которого имеются холинолитические симптомы, применение активированного угля и сульфата натрия, промывание желудка до 2-х суток после перорального употребления токсического средства, физические методы борьбы с гиперпирексией, форсированный диурез.
После купирования симптоматики ЦАС следует наблюдать за пациентом еще в течение как минимум 2 ч.
Проблема лечения ЦАС в России заключается в отсутствии регистрации физостигмина; в нашей стране, однако, доступен галантамин (нивалин, реминил). Он может применяться в том числе для проведения декураризации, но менее популярен, чем неостигмин (прозерин), из-за более медленного развития эффекта и существенно большей стоимости.
Однако в отличие от последнего он способен проникать через ГЭБ и поэтому может устранять не только периферические, но и центральные антихолинергические эффекты. Эти свойства галантамина позволяют предположить, что его можно использовать в качестве универсального препарата для декураризации, профилактики и лечения центрального антихолинергического синдрома.
Так, уже в упоминавшейся статье A. Baraka и S. Haris галантамин использовался для реверсии ЦАС, вызванного введением скополамина здоровым добровольцам, у всех наблюдаемых отмечено эффективное восстановление. Авторы приходят к заключению, что галантамин является эффективным, длительно действующим и безопасным средством при ЦАС.
В классическом справочнике по лекарственным средствам М. Д. Машковского в статье, посвященной галантамину, сказано, что его можно применять в качестве антагониста антидеполяризующих миорелаксантов или для устранения нейромышечного блока, вызванного повторными введениями деполяризующего релаксанта. Аналогичную рекомендацию приводят и А.А. Бунятян и соавт. в своем обзоре антихолинестеразных средств.
Поскольку вопросы патогенеза остаются не до конца понятыми, сложно указать конкретные профилактические меры. Однако общие рекомендации могут быть даны, в том числе они включают использование короткодействующих анестетиков, отказ от применения закиси азота, отказ от рутинного использования атропина в премедикации и дополнительной седации во время местной анестезии. Представляется важным и ознакомление медицинского персонала с существованием такого синдрома.
Суммируя изложенное, нужно подчеркнуть, что ацетилхолин играет важную роль в регуляции процессов сна и бодрствования и в осуществлении когнитивных функций. Кроме того, по-видимому, самая первая схема общей анестезии включала использование холинолитика скополамина с гипнотической целью, и такое его применение в ряде случаев рекомендуется до сих пор.
Таким образом, можно прийти к выводу, что угнетение холинергической активности является одним из механизмов, лежащих в основе феномена общей анестезии, а потому наибольшая частота возникновения ЦАС в анестезиологической практике легко объяснима. Однако различные нарушения при пробуждении пациентов после общей анестезии – весьма распространенная клиническая проблема, и показано, что чем больше различных препаратов-триггеров ЦАС используется во время общей анестезии, тем выше вероятность ее проявления.
Так с чем же все-таки мы здесь имеем дело? Действительно ли это самостоятельный синдром или ЦАС представляет собой затянувшиеся проявления необходимого механизма общей анестезии, который у некоторых пациентов по разным причинам не успевает выключиться к назначенному врачом сроку, позволяя нам его зафиксировать?
Такой ответ позволил бы, на наш взгляд, предложить схемы проведения общей анестезии, уменьшающие риски для пациента, например, систематически использовать для декураризации антихолинэстеразные препараты, проникающие через гематоэнцефалический барьер (галантамин). Если мы считаем стандартом плановую реверсию периферического Н-холинолитического действия, то почему бы параллельно не реверсировать в плановом порядке не менее закономерные центральные М- и Н-холинолитические эффекты?
Мы надеемся, что эта статья не только позволит российским анестезиологам по-новому взглянуть на известную им проблему, но и окажется полезной в клинике.
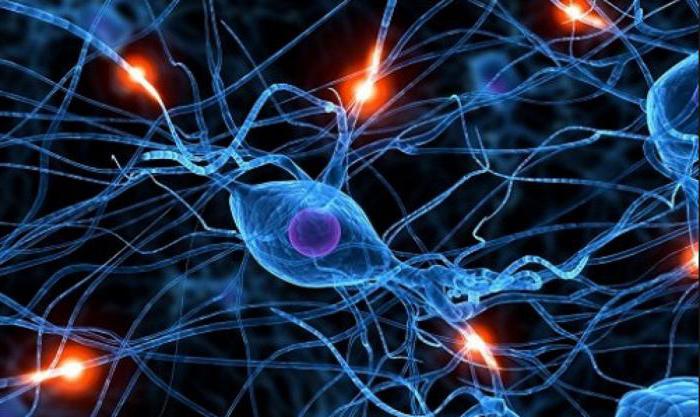
Передача импульсов по нейронам обеспечивается благодаря специальным веществам – медиаторам. Одним из нейромедиаторов является ацетилхолин. Эти вещества, находясь в синапсах, оказывают воздействие на мембраны клеток, вызывая их торможение или возбуждение и обусловливая различные эффекты. Избыток нейромедиаторов расщепляется специальными ферментами.
Антихолинэстеразные препараты: свойства и предназначение
К антихолинэстеразным препаратам относятся те, которые ингибируют фермент холинэстеразу. Этот энзим расщепляет путем гидролиза нейромедиатор ацетилхолин, который обеспечивает передачу импульсов в чувствительных к нему синапсах парасимпатических нервов, ганглиях и во всех соматических волокнах. Для ситуативного усиления действия ацетилхолина на нейроны и стимуляции определенных отделов нервной системы были разработаны антихолинэстеразные средства. Применение этих препаратов оказывает действие на весь организм в целом.
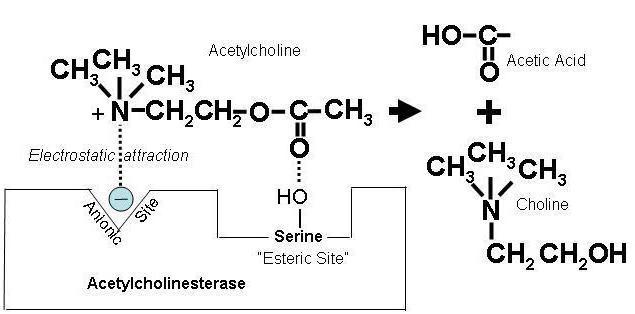
Действие антихолинэстеразных средств сходно с эффектом стимуляции холинэргических нервов. Эти препараты взаимодействуют с тем же участком активности поверхности рецептора, что и ацетилхолин, благодаря чему создается потенциал действия нервного окончания. Холиномиметики и антихолинэстеразные средства являются, по сути, одной и той же фармакологической группой веществ. Существует несколько видов этих препаратов, которые различаются по химической структуре и обратимости действия. Блокаторы холинэстеразы делятся на обратимые и необратимые.
Средства обратимого действия
Антихолинэстеразные средства - препараты обратимого действия, являются по химическому строению сложными эфирами карбаминовой кислоты и различных аминоспиртов. Компонентом реакции, блокирующей холинэстеразу, становится кислотное окончание, которое устанавливает с молекулой фермента намного более устойчивую связь, чем та, которая образуется при взаимодействии с самим ацетилхолином. Полное разрушение этого соединения происходит путем гидролиза в течение 3-4 часов.
К антихолинэстеразным средствам обратимого эффекта относятся "Галантамин", "Физостигмин", "Прозерин" (или "Неостигмин"), "Пиридостигмин", "Оксазил", "Ривастигмин", "Эдрофоний".
Фосфорорганика – вещества необратимого действия
Препараты необратимого действия данной группы представляют собой фосфорорганические соединения. Эти вещества блокируют ацетилхолинэстеразу на длительное время. Фосфор, находящийся в составе их молекул, образует устойчивое соединение с ферментом, которое может просуществовать в организме в течение нескольких дней и даже недель. Восстановление необходимого количества ацетилхолинэстеразы происходит путем образования новых молекул. К данной группе соединений относятся "Фосфакол", "Армин", "Хлорофос", "Карбофос", "Дихлофос", отравляющие вещества, применяемые в ходе военных действий – зарин и зоман.
Фосфорорганические препараты отличаются высокой токсичностью. Они часто применяются в быту в качестве инсектицидов; отравления возможны при их некорректном использовании и несоблюдении мер безопасности.

Эффекты антихолинэстеразных препаратов
При определенном сходстве эффектов, которые производят на организм антихолинэстеразные средства, показания к назначению каждого из них будут особыми. Рассмотреть практическое действие при введении в организм можно на примере "Прозерина".
"Прозерин" выпускается в ампулах в виде 0,05% раствора и вводится подкожно или внутривенно. При попадании в кровь он облегчает прохождение импульсов в нервно-мышечных передачах и ганглиях вегетативной нервной системы. В состоянии больного это проявляется следующим образом:
- вследствие сокращения круговой мышцы радужки сужается зрачок;
- происходит спазм аккомодации, хрусталик принимает более выпуклую форму из-за расслабления цинновой связки, фокус зрения устанавливается на ближнее расстояние, способность различать далеко расположенные объекты резко снижается;
- снижается частота сердечных сокращений;
- повышается тонус гладкой мускулатуры внутренних органов – дыхательных путей, желудка и кишечника, матки, мочевого пузыря;
- усиливаются сокращения скелетных мышц вследствие улучшенного прохождения импульсов в синапсах;
- повышается секреция экзокринных желез – потовых, слюнных, бронхиальных, желудочных.

Применение
Перечисленные эффекты обусловливают использование данной группы препаратов в медицине в различных случаях. Показания к применению антихолинэстеразных средств не ограничены конкретными заболеваниями, так как они оказывают эффект на центральную и периферическую нервную систему, что вызывает общее действие на весь организм. Чаще всего они назначаются при нарушениях иннервации и тонуса скелетной или гладкой мускулатуры.
Рассмотреть возможности лечения антихолинэстеразными средствами можно на примере "Прозерина". Этот препарат обратимого действия применяется при миастении – аутоиммунном заболевании, которое выражается в слабости скелетных мышц. Эта болезнь проявляется сначала снижением тонуса мимической мускулатуры, затем ослаблением мышц шеи, верхних и нижних конечностей; в тяжелых случаях наблюдается нарушение дыхания из-за недостаточной работы диафрагмы. "Прозерин" воздействует симптоматически на организм, восстанавливая передачу импульсов в нервно-мышечных передачах, благодаря чему повышается тонус мускулатуры, и облегчается двигательная активность.
Также данный препарат назначается в послеоперационный период при атонии ЖКТ или мочевого пузыря. В офтальмологии он изредка назначается при глаукоме для снижения внутриглазного давления. Как антагонист применяется при передозировке миорелаксантов и препаратов антидеполяризующего действия. Изредка "Прозерин" используют для стимуляции мышечных сокращений при слабой родовой деятельности.
Болезнь Альцгеймера
Препараты обратимого действия нашли применение при заболевании центральной нервной системы, тяжело поддающемся лечению. При болезни Альцгеймера назначается "Галантамин" - алкалоид, полученный из клубней подснежников рода Galantus ("Ривастигмин", он же "Экселон"), но наиболее терапевтически эффективным стал "Донепезил", который выборочно блокирует ацетилхолинэстеразу в синапсах головного мозга и практически не затрагивает ее на периферии нервной системы.
Противопоказания
Исходя из эффектов антихолинэстеразных препаратов обратимого действия, противопоказаниями к их назначению являются эпилепсия, бронхиальная астма, стенокардия, болезнь Паркинсона и всевозможные нарушения проводящей системы сердца.
Симптомы передозировки и отравления АХЭ
Отравление антихолинэстеразными средствами дает симптомы, напрямую связанные с избыточной стимуляцией рецепторов, чувствительных к ацетилхолину. Наблюдается сужение зрачков, замедление частоты сердечных сокращений (брадикардия), спазм бронхов и - вследствие этого - симптомы удушья, усиленная перистальтика ЖКТ вплоть до рвоты и диареи, учащенное мочеиспускание. Постепенно снижается артериальное давление как следствие тормозного влияния вагусного нерва. Происходят хаотичные сокращения и подергивания скелетной мускулатуры и языка из-за нарушенной проводимости в нервно-мышечных передачах.
Отравление ФОС
Попадание в организм фосфорорганических соединений вызывает клиническую картину, аналогичную отравлению антихолинэстеразными средствами обратимого действия. Симптомы могут проявляться ярче вследствие более высокой токсичности препаратов. К симптоматике отравления на соматическом уровне добавляются эффекты на уровне центральной нервной системы – спутанность сознания, дезориентация, угнетение дыхания.

Фосфорорганические соединения вызывают резкий миоз, ухудшение зрения, удушье, потливость, сильную рвоту, психомоторное возбуждение – у больного начинается паника, он становится неуправляемым. Из-за спазмов гладкой мускулатуры ощущается резкая боль в животе. При ухудшении состояния возникают судороги, падает артериальное давление, развивается кома. Смерть может наступить вследствие паралича дыхательного центра.
Аналогичная симптоматика наблюдается при отравлении мухоморами. Это обусловлено содержанием в них мускарина – яда с холиномиметическим действием.
Действия при отравлении
Врачебную помощь при отравлении антихолинэстеразными средствами может оказать только специалист. В этих случаях вводится раствор "Атропина" подкожно, возможно назначение "Метацина" или других холиноблокаторов. Необходимо поддержать дыхание на должном уровне. Могут применяться трахеотомия, искусственная вентиляция легких и оксигенация.
При бытовом отравлении ФОС определяют источник попадания яда в организм. Если вещество проникло через кожу, его смывают 3-5% раствором соды или водой с мылом. В случае, когда препарат был принят внутрь, проводят промывание желудка, многократные клизмы, дают адсорбенты или слабительные средства. Если фосфорорганическое соединение уже успело в большей мере попасть в кровь, назначается форсированный диурез с помощью мочегонных препаратов. В отдельных случаях прибегают к методам фильтрации крови с помощью гемодиализа и гемосорбции.

Дополнительно при отравлении ФОС назначаются реактиваторы холинэстеразы, которые при введении в первые часы после интоксикации способны восстановить блокированные ферменты. Это могут быть "Изонитрозин", "Тримедоксим", "Дипироксим". Если артериальное давление повышено, симптоматически назначают гипотензивные препараты. Предпочтение стоит отдавать тем, которые не затрагивают ЦНС. При ослаблении самостоятельного дыхания показана искусственная вентиляция легких и дача кислорода.
Есть несколько нейротрансмиттеров, которые влияют на наше тело, регулируя нашу психику и наше поведение. Одним из основных является ацетилхолин , что является фундаментальным в деятельности коры головного мозга и в реализации большого количества психических и физических процессов. Примерами этого являются внимание, осознание, память и активация мышц.
Тем не менее, избыток этого вещества может быть опасным или даже смертельным, множество изменений, называемых холинергическим синдромом .
Что такое холинергический синдром?
Холинергический синдром называется изменения или симптомы, вызванные стимуляцией различных рецепторов ацетилхолина в организме до избытка этого вещества. Интоксикация возникает, как правило, из-за воздействия или введения внешних веществ, которые генерируют такой избыток.
Среди них Передозировка некоторых препаратов с холинергическим действием такие как пилокарпин (лекарство от глаукомы, также используемое для лечения сухости во рту при различных расстройствах), бетанекол (для применения при мегаколоне и везикулярных заболеваниях) или лекарства, которые ингибируют антихолинэстеразу, используемую для борьбы с болезнью Альцгеймера (например, ривастигмин), ввиду его чрезмерного употребления и в чрезмерном количестве по отношению к времени, в которое они воздействуют на организм.
Это может также быть вызвано отравлениями от пестицидов и инсектицидов. Мы также можем найти случаи, вызванные избытком никотина или потреблением некоторых грибов бетон и грибки, такие как мухомор мухомор.
Холинергический синдром потенциально смертелен и обязательно требует медицинской помощи. Наиболее распространенными симптомами являются чрезмерное выделение жидкости (слюна, слезы, пот, слизь и слизистые оболочки на уровне дыхательных путей . ), мышечные боли и паралич (который может включать мышцы, которые позволяют дышать) и кардиореспираторные расстройства ,
Первоначально появляются тахикардия, которая может перерасти в брадикардию (то есть ускорение сердечного ритма, которая может замедлиться) и затрудненное дыхание (включая бронхоспазмы, которые препятствуют прохождению воздуха в легкие). может закончиться остановкой кардиореспираторной системы и смертью в случае отсутствия вспомогательного дыхания , Рвота, летаргия и спутанность сознания и диарея также распространены.
Основные симптомы в зависимости от активации специфических рецепторов
Ацетилхолин имеет различные рецепторы в нервной системе, включая никотиновые и мускариновые рецепторы. В этом смысле может возникнуть холинергический синдром, при котором затрагивается только один из типов рецепторов, или следовать процессу в зависимости от типа активируемых рецепторов. Обычно следующая последовательность обычно происходит.
Этот тип холинергического синдрома характеризуется наличием мышечные боли, судороги и паралич, тахикардия и гипертония это может сопровождаться брадикардией, гипергликемией и избытком кальция. Наличие мидриаза (то есть расширения зрачка) в первые моменты острого отравления также очень характерно.
Однако этот мидриаз является только начальным, потому что со временем симпатическая нервная система активируется, чтобы вызвать миоз (аномальное сокращение зрачка). Мышцы ослаблены и рефлексы потеряны.
На этой стадии синдрома эффект обусловлен чрезмерной активацией мускариновых рецепторов. Появляются миоз или сокращение зрачка, нарушение зрения, снижение частоты сердечных сокращений или брадикардия, слезотечение, слюноотделение (чрезмерное слюноотделение), недержание мочи, тошнота и рвота, а также проблемы с дыханием, которые могут привести к остановке дыхания. Существует также гипотермия и проблемы, такие как гипотония.
Обычно в дополнение к вышеупомянутому появляется неврологический синдром, состоящий из появления головная боль, раздражительность, переохлаждение , изменение сознания, которое может достичь комы, судороги, кардиореспираторная депрессия и даже смерть.
лечение
Как мы уже указывали ранее, холинергический синдром требует немедленного медицинского лечения, поскольку он может привести к смерти больного.
Первым шагом, который необходимо выполнить, является стабилизация состояния пациента с точки зрения поддержания контроля над его сердцем и частотой дыхания и, при необходимости, использования мер по поддержанию жизни и даже искусственного дыхания. Администрация кислорода имеет важное значение. В тяжелых случаях может потребоваться интубация пациента и устранение избыточных выделений тем или иным путем.
Впоследствии на фармакологическом уровне администрация атропина обычно рассматривается как решение для мускариновых симптомов наряду с веществами, которые реактивируют или потенцируют холинэстеразы (природные ферменты, которые разлагают ацетилхолин в нашем организме), чтобы облегчить симптомы никотина. Использование диазепама или других транквилизаторов может потребоваться в тех случаях, когда появляются судороги для снижения уровня активации.
- Bargull-Díaz, I.C.; Лосано, N .; Пинто, J.K. & Aristizábal, J.J. (2012). Промежуточный синдром при остром органофосфатном отравлении: история болезни. Медицина U.P.B. 31 (1): 53-58.
- Gervilla, J.; Отал, J.; Торрес М. и Дуран Дж. (2007). Фосфорорганическое отравление. SEMERGEN. 33: 21-3.
- Морено А. (2014). Основные токсические синдромы и антидоты. Больница 12 октября.
Противоэпилептические средства. Как выучить? (April 2020).
Читайте также:


