Можно ли делать химиотерапию при герпесе
Инфекции — главные причины смерти при раке. Они не только часто встречаются, но нередко имеют более тяжелое течение, чем у других пациентов, менее подверженных действию терапии, и иногда вызываются организмами, которые не патогенны для здоровых людей. Такая восприимчивость является следствием подавления защитных механизмов больного, вызванного опухолью и ее лечением.
Кожа и слизистые оболочки служат барьером для инфекции. Опухолевая инфильтрация и местная лучевая радиотерапия могут привести к повреждению лимфатических или венозных сосудов, что приводит к увеличению восприимчивости к локальной инфекции. Воспроизводство эпителиальных клеток в желудочно-кишечном тракте подавляется химиотерапией, из-за чего повреждается и изъязвляется слизистая, что позволяет организмам из кишечника попасть в систему воротной вены.
Кожа повреждается внутривенными иглами и канюлями, особенно туннельными подкожными каналами. Это частые источники инфекции, которые вызываются такими кожными организмами, как Staphylococcus epidermidis. В носоглоточной полости возникают инфекции, вызванные Candida albicans.
Рак при запущенной стадии иногда связан с ухудшением функций и нейтрофилов, и моноцитов. Было описано подавление хемотаксической, фагоцитарной и бактерицидной активностей.
Ослабленная замедленная гиперчувствительность довольно распространена при запущенной болезни Ходжкина, но менее часта в других случаях злокачественных опухолей. Лимфопения неизменно вызывается действием алкилирующих агентов и массивной радиотерапией. Клеточный иммунитет особенно важен при защите организма хозяина от грибов, вирусов, туберкулеза и простейших.
Интенсивная цитотоксическая химиотерапия ведет к ухудшению образования антител к бактериальным и вирусным антигенам.
Циркулирующие бактерии удаляются фагоцитарными клетками, находящимися в синусах ретикулоэндотелиальной системы, особенно в печени и селезенке. Для этой чистки важны антитела и белки системы комплемента. Спленэкто-мия увеличивает риск серьезной бактериальной инфекции, особенно пневмококковый сепсис в детском возрасте и в меньшей степени во взрослом.
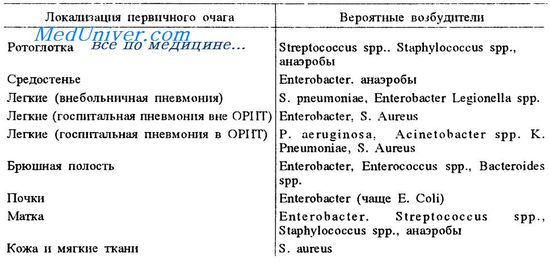
Бактериемия и септицемия у больных раком
Инфекции кровяного русла довольно часты у пациентов с гранулоцитопенией. Патогенами часто являются грамотрицательные бактерии (Escherichia coli, Pseudomonas aeruginosa), стафилококки и стрептококки. Увеличивается частота инфекций, вызванных грамположительными бактериями, особенно Staphylococcus epidermidis. Пациенты с тунельными подкожными каналами особенно подвержены поражениям этим организмом.
Жар у пациента с нейтропенией при раке — показатель присутствия бактерий в крови и под кожей. Если существует очевидный источник инфекции, например инфицированный порт для инфузий, следует взять культуру бактерий и удалить канюлю. Лечение не следует откладываеть для пациента с нейтропенией. Пациенты с лихорадочной нейтропенией с относительно низким риском развития серьезных осложнений относятся к тем, кого лечат короткими циклами химиотерапии для солидных опухолей.
Эти пациенты должны быть госпитализированы. Недавние исследования показали, что пероральный прием амоксициллина-клавуланата комбинированный с пероральным приемом ципрофлоксацина так же эффективен, как и внутривенная химиотерапия в этой группе (70% пациентов). Пациенты с высоким риском (с неконтролируемым раком или на стационарном лечении интенсивной терапией) лечатся внутривенными антибиотиками, в том числе b-лактамом и аминогликозидом или цефтазидимом.
Респираторные инфекции у больных раком
У пациента с серьезным подавлением иммунитета довольно часто возникает жар с легочным инфильтратом. Главные причины этого даны в таблице.
Осложнения в постановке диагноза могут быть значительны, поскольку тесты слюнных и кровеносных культур иногда отрицательны, а более инвазивные процедуры, такие как трансбронхиальная биопсия, невозможны из-за тромбоцитопении или общего состояния пациента.
Существуют некоторые клинические особенности, которые помогают при постановке диагноза. Кавитация наиболее часто сопровождает поражения анаэробными бактериями, стафилококками и микобактериями. Инфекции Pneumocystis вызывают заметную одышку, а на рентгенограмме грудной клетки видны билатеральные инфильтраты, обычно состоящие из хилуса. Болезнь, однако, может протекать вяло и вызвать долевое уплотнение. Цитомегаловирусные инфекции встречаются главным образом у пациентов с серьезным подавлением иммунитета, в частности в течение аллогенной ВМТ. Болезнь может также вызывать миокардит, невропатию или офтальмию.
Легочные инфильтраты обычно билатеральны. Инфекции Candida вызывают широкое разнообразие изменений в рентгенограмме. Инфекции Aspergillus обычно быстро прогрессируют. Тесты культур крови обычно отрицательны, а инфильтраты возможны в одном или двух легких.
При затруднениях в постановке диагноза можно следовать следующей схеме.
У пациентов без нейтропении или тромбоцитопении исследовать посевы крови, слюны, бронхоскопические промывания и трансбронхиальную биопсию там, где это возможно. Если кровяные и слюнные культуры отрицательны, лечить антибиотиками широкого антибактериального спектра действия (обычно в комбинации с аминогликозидом, пенициллином и метронидазолом или аналогичными соединениями). Если возможной причиной инфекции является Pneumocystis, следует давать высокие дозы котримоксазола. Если ответа нет, рассмотрите ацикловир для вируса простого герпеса и противогрибковую терапию с амфотерицином или кетоконазолом. Ацикловир не эффективен против цитомегаловирусов.
Если кровяные или слюнные тесты положительны, лечите соответствующе, но если ответа нет, рассмотрите смешанные инфекции.
Пациентам с нейтропенией или тромбоцитопенией проводят бронхоскопию, но биопсия не всегда возможна, и лечение продолжают без дальнейшего диагностического исследования. До и после бронхоскопии иногда необходимы антибиотики и переливание тромбоцитов.

Инфекции мочевыводящих путей у больных раком
Инфекции часты у пациентов с затрудненным мочеиспусканием. Затруднения могут быть вызваны опухолью или ослаблением мочевого пузыря у пациентов с компрессией спинного мозга и его корешков. Диагноз ставится после исследования уринокультуры, и лечение осуществляется антибиотиками и снятием осложнений, если это возможно.
Желудочно-кишечные инфекции у больных раком
Молочница ротовой полости (инфекция, вызываемая Candida albicans) — частое осложнение химиотерапии. Она особенно распространена у пациентов с подавленным иммунитетом, у пациентов, принимающих стероиды и тех, кого лечат антибиотиками с широким спектром действия. Рот и глотка становятся очень болезненными, а белые пятна грибков видны на эри-темной основе. У плохо питающихся пациентов инфекция может проникать глубже и распространяться по пищеводу, желудку и кишечнику. Обычно эффективен пероральный прием нистатина, амфотерицина или миконазола.
Проявление вируса простого герпеса на губах часто проблематично для пациентов с лейкопенией, и повреждения могут быть довольно обширными. В данном случае необходимо местное применение ацикловира для пациентов с подавленным иммунитетом или систематический прием ацикловира при более серьезных инфекциях.
Инфекции, вызванные Candida в пищеводе, необходимо лечить пероральным приемом суспензии нистатина, но если такое лечение неэффективно, то необходимо применение кетоко-назола или короткий курс амфотерицина. Кишечные инфекции, возникающие при поражении Candida, должны лечиться амфотерицином.
Перианальные инфекции распространены среди пациентов с нейтропенией. Всегда необходимо применять профилактические меры совместно с тщательной гигиеной промежности и смягчителями стула для предотвращения запора и анальных трещин. Распространяющиеся перинеальные (паховые) инфекции могут угрожать жизни пациента, и требуется срочное лечение внутривенными антибиотиками, действующими против грамотрицательных и анаэробных бацилл.
Менингит у больных раком
Инфекции центральной нервной системы (ЦНС) довольно редки, но у пациентов с лимфомой или лейкемией иногда развивается менингит из-за Cryptococcus neoformans. Начало заболевания индивидуально у каждого и сопровождается головной болью. Микроорганизм обнаруживают при окрашивании India ink спинномозговой жидкости (CSF).
Выявление антигенов Cryptococcus в крови и CSF возможно у большинства пациентов. Состояние многих пациентов улучшается при приеме амфотерицина, некоторые вылечиваются.
Кожные инфекции у больных раком
В отличие от инфекции, представленной на портах для вливания, наиболее частое кожное заболевание — опоясывающий лишай (varicella zoster). Возникает из-за реактивации вируса varicella zoster в ганглии дорсального корешка, вызывает кожную пузырчатую сыпь, которая особенно серьезна у людей с подорванным иммунитетом, может распространяться как ветряная оспа и вызывать фатальную пневмонию. Пациентов следует лечить ацикловиром как можно быстрее.
[youtube.player]Из противовирусных препаратов базисным препаратом является синтетический пуриновый нуклеозид - ацикловир (зовиракс), который выпускается в таблетках (200 мг, 400 мг, 800 мг); суспензии (5 мл - по 200 мг) во флаконах по 125 мл для приема внутрь; сухое вещество для инъекций - 250 мг в 1 ампуле; крем - 2, 10 г в тубах.
Схемы лечения ацикловиром:
• При первом клиническом эпизоде генитального герпеса ацикловир целесообразно назначать по 200 мг 5 раз в течение 5-10 дней или до достижения клинического разрешения; лечение ацикловиром эффективно, если оно начато в первые часы после проявления первых клинических симптомов заболевания; валацикловир внутрь 1 г 2 раза в день в течение 10 дней.
• При рецидивирующем генитальном герпесе эпизодическое лечение заключается в назначении ацикловира по 400 мг 5 раз в день в течение 5 дней или по 400 мг 3 раза в день в течение 5 дней, или по 800 мг 2 раза в день в течение 5 дней; лечение целесообразно начинать в продромальном периоде или в первые часы клинических проявлений; супрессивная терапия (для больных, имеющих частые рецидивы) заключается в назначении перманентного метода лечения рецидивирующего герпеса, при котором ацикловир назначают ежедневно по 400 мг 2 раза в день или по 200 мг 4-5 раз в день в течение месяцев и даже лет. При рецидиве валацикловир назначают внутрь по 500 мг 2 раза в день в течение 5 дней. Ежедневная супрессивная терапия снижает частоту генитального герпеса у 75% пациенток. Подтверждена эффективность и безопасность ацикловира у пациентов, получавших ежедневную терапию в течение 5 лет.
• При наличии диссеминированной инфекции (энцефалит, пневмония, гепатит и т.п.) следует рекомендовать внутривенное использование ацикловира каждые 8 часов в течение 5-7 дней из расчета 5-10 мг/кг массы тела.
При генитальном герпесе, обусловленном ацикловирустойчивыми штаммами вируса, альтернативными препаратами являются фоскарнет, или фоскавир (фосфономуравьиная кислота), и фамвир (фамцикловир). Фоскарнет при тяжелом течении заболевания применяется внутривенно медленно ( в течение 2 -х часов) капельно по 60 мг/ кг массы тела 3 раза в сутки в течение 10-14 дней. Фамвир при острой герпетической инфекции назначают по 0,5 г 3 раза в сутки в течение 7 дней. Больным с повышенным риском развития постгерпетической невралгии рекомендовано принимать препарат по 0,5 г 3 раза в день в течение 7 дней. В период беременности и лактации препарат можно назначать по жизненным показаниям.
Другие противовирусные препараты:
• валацикловир (валтрекс) - по 0,5 г, per os 2 раза в день в течение 5-10 дней;
• алпизарин - по 0,1 г (табл.), per os, 3-5 раз в день в течение 15-20 дней;
• флакозид ( из листьев бархата амурского и бархата Лаваля) - по 0,1-0,5 г, per os, 3 раза в день в течение 5-10 дней.
Препараты для наружного использования:
• ацикловир - крем 5% наносить 5 раз в день с интервалом 4 часа, исключая ночное время, в течение 5-10 дней;
• пантенол - аэрозольная упаковка, объем - 140 г; наносится на пораженные участки с расстояния 10 см 4-6 раз в день в течение 2 недель; рекомендуется начинать применять в острый период или в начале возникновения рецидива;
• мегосин - мазь 3%; местные аппликации 4-6 раз в день в течение 5-7 дней;
• госсипол - линимент 3%; местные аппликации 4-6 раз в день в течение 5-7 дней;
• гевизош- мазь; наносится на пораженную поверхность 3-5 раз в течение 3-12 дней;
• оксолиновая мазь 0,25% -3%;
• теброфеновая мазь 0,5%-2%;
• алпизариновая мазь 2-5%;
• риодоксоловая мазь 0,25%-1%;
• хелипин 1 или 5% мазь;
• эпигенинтим (водный экстракт корня солодки) применяется до 6 раз в сутки.
Препараты для наружного лечения следует применять в продромальном периоде и при развитии рецидива до стадии образования эрозий, как правило, от 3 до 4 раз в сутки в течение 5-10 дней. При наличии эрозий или отека необходимо применять примочки с дезоксирибонуклеазой, полуданом, 0,5% - м раствором сульфата цинка, а также использовать антисептики, анилиновые красители.
Лечение беременных.
Лечение беременных обязательно при развитии диссеминированных форм герпетической инфекции (энцефалиты, гепатиты и др.).Ацикловир используется в стандартных дозировках. Кесарево сечение в интересах плода и для профилактики неонатального герпеса необходимо производить или при наличии герпетических высыпаний, или при первичной герпетической инфекции у матери, возникшей за 1 месяц до предполагаемого срока родов. В остальных случаях возможно родоразрешение через естественные родовые пути.
3.1.8. Комбинации антибиотиков, рекомендуемые для лечения воспалительных заболеваний тазовых органов
Применение новых антибактериальных препаратов сыграло важную роль в борьбе с инфекцией в акушерско-гинекологической практике. Вместе с тем возник ряд сложных задач, обусловленных особенностями инфекционных процессов в современных условиях. Антибактериальная терапия с микробиологических позиций представляет собой как бы селективный пресс, подавляющий чувствительную к антибиотикам микрофлору и способствующий размножению устойчивых микроорганизмов, нередко входящих в состав естественной микрофлоры организма (Б.Л.Гуртовой, В.И.Кулаков, С.Д.Воропаева, 1996).
Опыт применения монотерапии антибиотиками, которые были активны в отношении не всех патогенных бактерий, привел исследователей к выводу, что для лечения воспалительных заболеваний гениталий, особенно при распространении инфекции в верхние отделы (матка, трубы, яичники, тазовая клетчатка, брюшина), необходимо применять такие комбинации антибиотиков, которые активны в отношении анаэробов, грамотрицательных факультативных аэробов, N.gonorrhoea и C.trachomatis.
Разнообразие микроорганизмов, которые могут быть возбудителями воспалительных заболеваний гениталий, медленный рост анаэробов в культуре и необходимость применения сложных микробиологических методов для обнаружения анаэробов и C.trachomatis зачастую приводят к тому, что до начала противомикробной терапии не удается поставить бактериологический диагноз, и поэтому антибиотикотерапия должна быть активной в отношении всех потенциальных возбудителей.
В этой связи Центр по борьбе с болезнями и их профилактике (David Zambrano, MD,PhD,1996) рекомендует при тяжелых воспалительных заболеваниях гениталий применять две схемы антибиотикотерапии: цефа-лоспорины второго поколения (цефокситин, цефотетап) и доксициклин или комбинацию клиндамицин и гентамицин. При легких и умеренных инфекциях рекомендуется применять цефалоспорины второго или третьего поколения в сочетании с доксициклином или же сочетание клиндамицина с фторхинолонами (per os). Такие схемы антибиотикотерапии обеспечивают высокую частоту положительных бактериологических и клинических результатов. Новые исследования показали, что гентамицин можно заменить каким-либо препаратом из группы монобактамов (азтреонам и т.д.); такая схема несколько более эффективна и менее токсична. Кроме этого, клиндамицин в ряде случаев может быть заменен инфузионным раствором клиона (метронидазол) или линкомицином.
Комбинации антибиотиков, рекомендованные Центром по борьбе с болезнями и их профилактике для лечения воспалительных заболеваний гениталий в условиях стационара:
• цефокситин по 2,0 г внутривенно каждые 6 часов или цефотетам по 2,0 г внутривенно каждые 12 часов в сочетании с доксициклином по 100 мг внутривенно или per os каждые 12 часов; лечение по этой схеме необходимо продолжать не менее 48 часов, после существенного клинического улучшения и далее больные должны принимать внутрь доксициклин по 100 мг 2 раза в сутки до 14 дня лечения;
• клиндамицин по 900 мг внутривенно каждые 8 часов в сочетании с ген-тамицином по 2 мг/ кг массы тела внутривенно или внутримышечно (насыщающая доза) и далее по 1,5 мг/кг внутривенно или внутримышечно каждые 8 часов (поддерживающая доза); лечение по этой схеме необходимо продолжать не менее 48 часов, после существенного клинического улучшения и далее больные должны принимать внутрь доксициклин по 100 мг 2 раза в сутки или клиндамицин по 450 мг 4 раза в сутки до 14 дня лечения.
Комбинации антибиотиков, рекомендованные Центром по борьбе с болезнями и их профилактике для лечения воспалительных заболеваний гениталий в амбулаторных условиях:
• цефокситин по 2,0 г внутримышечно, однократно с одновременным назначением 1,0 г пробеницида (per os) либо цефтриаксона по 250 мг внутримышечно, либо какого другого цефалоспорина третьего поколения (цефобид, цефотаксим или цефтизосим) в сочетании с доксициклином по 100 мг 2 раза в сутки в течение 14 дней;
• офлоксацин (таривид, заноцин) по 400 мг (per os) 2 раза в сутки в течение 14 дней в сочетании с клиндамицином по 450 мг (per os) 4 раза в сутки в течение 14 дней, также в сочетании с метронидазолом по 500 мг (per os) 2 раза в сутки на протяжении 14 дней.
Инфекции тазовых органов зачастую проявляются незначительной симптоматикой или вообще протекают бессимптомно, и их частота, как правило, занижается. Большинство женщин с воспалительными заболеваниями верхнего отдела гениталий получают лечение в амбулаторных условиях, хотя, по данным ряда исследователей, следует полагать, что лечение в стационаре высокими дозами внутривенных противомикробных средств и соблюдение пациентками постельного режима должно давать лучшие результаты, чем лечение антибиотиками per os в амбулаторных условиях.
В этой связи госпитализация особенно рекомендуется в следующих случаях:
• диагноз не ясен;
• нельзя исключить такие неотложные заболевания, как аппендицит и эктопическую беременность;
• при подозрении на абсцесс тазовых органов;
• при наличии у пациентки беременности;
• пациентка находится в подростковом возрасте;
• тяжелое течение заболевания исключает возможность проведения лечения в амбулаторных условиях;
• больная не может наблюдаться амбулаторно;
• состояние больной не улучшается, несмотря на амбулаторное лечение;
• нет возможности организовать клиническое наблюдение на протяжении 72 часов после начала антибиотикотерапии.
Альтернативные комбинации антибиотиков при лечении острых сальпингитов (салъпингоофоритов) в стационарных условиях:
• инфузионный раствор клиона по 500 мг внутривенно с интервалом в 8 часов в сочетании с гентамицином по 80 мг внутримышечно также с интервалом введения через 8 часов или с тобрамицином по 1,5мг/кг массы тела 2-3 раза в день;
• клиндамицин по 600-900 мг 3 раза в день внутримышечно или внутривенно в сочетании с гентамицином или тобрамицином по 1,5 мг/кг массы тела 2-3 раза в день;
• цефобид (цефаперазон) по 1,0-2,0 г с интервалом введения в 12 часов внутривенно в сочетании с доксициклином по 100 мг 2 раза в день;
• цефотаксим (клафоран) по 1,0-2,0 г 3 раза в день внутривенно или внутримышечно в сочетании с доксициклином по 100 мг 2 раза в день;
• цефтамизин по 1,0-2,0 г 2-3 раза в день внутривенно или внутримышечно в сочетании с амоксициллин - клавулановой кислотой (аугментин) по 500 мг 2 раза в день (per os);
• ципрофлоксацин (ципробай) по 200-400 мг 2 раза в день внутривенно в сочетании с аугментином по 500 мг 3 раза в день (рег os).
Комбинации антибиотиков при тяжелых формах эндометритов, в том числе и после операции кесарево сечение:
• ампициллин в сочетании с аминогликозидами или цефалоспоринами;
• полусинтетические пенициллины с ингибиторами β-лактамаз (уназин, сулациллин);
• цефалоспорины I или II поколения в сочетании с инфузионным раствором клиона (метронидазол) или в сочетании с клиндамицином, или линкомицином;
• аминогликозиды в сочетании с инфузионным раствором клиона (метронидазол) или с клиндамицином, или с линкомицином;
• цефалоспорины I или II поколения в сочетании с аминогликозидами и с метронидазолом.
Представленные выше дозировки (суточные и курсовые) антибиотиков рассчитаны на пациентов с нормальным суточным диурезом; при снижении диуреза менее 800,0 мл суточная доза антибиотиков должна рассчитываться по формуле:А = ( В / С )* D, где А - искомая суточная доза антибиотиков при сниженном (менее 800,0 мл ) диурезе; В - величина сниженного суточного диуреза ( менее 800,0 мл); С - коэффициент 800, на который необходимо разделить величинуВ; D - суточная доза антибиотиков для пациентов с нормальным диурезом.
Согласно формуляру антибактериальной терапии и профилактики инфекций в акушерстве и гинекологии (С.В. Яковлев, 2001), для лечения воспалительных заболеваний малого таза должны быть использованы различные комбинации антибиотиков (табл.15).
Механическое удерживание земляных масс: Механическое удерживание земляных масс на склоне обеспечивают контрфорсными сооружениями различных конструкций.


Папиллярные узоры пальцев рук - маркер спортивных способностей: дерматоглифические признаки формируются на 3-5 месяце беременности, не изменяются в течение жизни.

Организация стока поверхностных вод: Наибольшее количество влаги на земном шаре испаряется с поверхности морей и океанов (88‰).
[youtube.player]Герпес и рак — ученые считали что между ними нет ни какой связи и они несовместимы. Это оказалось не так. Модифицированный вирус герпеса, используется в борьбе с раком. Ученые выявили агрессивное поведение вируса к клеткам опухоли, из чего следует возможность лечения онкологических больных с помощью этой методики. Проведено множество исследований и экспериментов которые по большой части оказались успешными и многообещающими. С другой стороны, есть данные, что генитальная герпетическая инфекция способна спровоцировать рак шейки матки у женщин или простаты у мужчин.
После удаления множества раковых опухолей, пациентам был введен модифицированный вирус. После курса лечения рецидив рака долгосрочно не наблюдалась.
Есть ли связь?
Проведение исследований говорят о том, что в 90% случаях в организме есть раковые клетки и вирус герпеса. Они находятся в так называемой спячке, и могут никогда не проснуться. Существует баланс, при котором организм способен бороться с этими клетками. Но если он нарушится, возможно развитие онкологии. Факторы запуска болезни в большинстве случаев одинаковы. Серьезнейший фактор — ослабленный иммунитет.
- контакт с ядовитыми веществами;
- стресс;
- переохлаждение, перегрев;
- злоупотребление алкоголя;
- курение;
- генетическая предрасположенность.
Вирус герпеса для лечения рака
Модифицированный вирус, используется в комбинации с химиотерапией и облучением. Его вводят в организм человека, вакцина сражается с клетками рака и убивает их. Герпес проникает в матрицу раковой клетки уничтожая ее структуру. Такое лечение не несет никакой опасности для человека, герпес размножается исключительно в онкологических клетках, не затрагивая здоровые ткани. Уже есть положительные результаты лечения рака кожи герпетической вакциной. Дополнительно модифицированный вирус вырабатывает протеин, необходимый для повышения клеточного иммунитета.
Основной плюс такого лечения — безопасность. Но его используют только при локализованном раке области шеи и головы. Пока нед данных об успехе лечения раковых метастаз или опухолей в головной мозгу, молочных железах или желудке. Поэтому метод не считается панацеей и показан в комбинации с классической терапевтической схемой. Вакцинирование помогает только при начальных стадиях заболевания. Но в большинстве случаях рак диагностируют на поздних стадиях.
- безопасность;
- высокий процент полного выздоровления на ранних стадиях рака;
- выработка специфичного белка, который стимулирует иммунитет бороться с онкологией;
- во многих случаях отсутствует рецидив.
- излечение только на ранних стадиях;
- вакцина помогает только при опухолях области шеи и головы.
Опасности
Сама вакцина безопасна для человека. Были замечены несерьезные побочные эффекты, которые возможно были вызваны от введения более радикальных препаратов (химиотерапии). Такое лечение проводится только в присутствии специалистов, под тщательным наблюдением. Не замечено осложнений после применения такого вида лечения у пациентов.
Однозначные выводы относительно масштабности применения терапевтической практики герпетической вакцины в борьбе с раком не сделаны. Ведутся дальнейшие исследования над повышением эффективности техники.
Обратный эффект
Зарубежные и отечественные ученые сошлись на мнении, что генитальный герпес является провокатором многих женских болезней, в частности, вызывает рак шейки матки. Вирус способен спровоцировать опухоль простаты у мужчин. Опасны в этом случае хронические инфекции с регулярными обострениями, как и нелеченные формы герпеса гениталий.
[youtube.player]Учёные постоянно изобретают новые способы борьбы против рака. Не так давно они выдвинули довольно интересную теорию, что модифицированный вирус герпеса в состоянии защитить организм хозяина от онкологических заболеваний и даже провели ряд исследований. Пока доказательств для заключения, что это возможно — мало. Однако у многих затеплилась надежда, что онкологию можно полностью победить. При этом остаётся открытым вопрос: действительно ли рак и герпес не могут сосуществовать в одном организме?
Размножение герпеса

Чтобы проникнуть вглубь клетки, вирусу нужно начать взаимодействие с её рецепторами, расположенными на внешней оболочке. Присоединившись, герпес оставляет часть своих оболочек и проникает внутрь. Добравшись до мембраны клеточного ядра, вирус теряет ещё несколько своих оболочек, после чего проникает внутрь. Размножение происходит непосредственно в ядре. Фактически некогда здоровая клетка начинает продуцировать вирус, а затем погибает в результате разрушения мембраны ядра.
Избавить организм от вируса герпеса не в силах ни один препарат. Более 90% населения земного шара являются его носителями.
Развитие онкологии

Существует три типа онкогенов, приводящих организм к возникновению злокачественной опухоли. Это онкогены, гены-супрессоры опухолей, гены репарации ДНК. Первые приводят к бесконтрольному делению раковых клеток. Вторые призваны защищать от рака, однако в случае повреждения (генетические мутации) они не работают и не в состоянии тормозить рост больных клеток. Третьи исправляют ошибки в генах. В случае сбоя происходят рецессивные генные мутации, развивается рак.
Появление раковых клеток всегда спровоцировано генетическими изменениями в здоровых. Иными словами, это мутации в генах (нарушения структуры ДНК), которые могут быть как случайными, так и наследственными. Также они зависят от некоторых внешних факторов, таких как:
- Курение, приём наркотиков.
- Повреждение кода ДНК.
- Воздействие на организм токсинов, канцерогенов.
- Вирусные заболевания.
Последний факт вызывает вполне обоснованные споры по поводу состоятельности теории, что вирус герпеса эффективен против рака. Научно доказана связь между генитальным герпесом второго типа и раком шейки матки, а также раком простаты. Тогда каким же образом искусственное введение вируса герпеса способно победить меланому – одну из самых агрессивных форм онкологии?
Интересная теория
В XIX веке был отмечен следующий факт – онкобольные входили в ремиссию, если в их организм проникал вирус. Многочисленные опыты подтвердили теорию, что инфицирование раковой клетки вирусом убивает её точно так же, как и здоровую при помощи нового препарата T-VEC. На практике зарегистрированы многочисленные случаи излечения больных от меланомы (рака кожи). Правда, есть и отрицательная статистика – отмечена гибель пациентов, участвующих в эксперименте добровольно.
Фактически нет ничего необычного в таких разработках, так как доказано, что вирус разрушает клетку, используя её ядро с оболочкой для своего размножения. Так как речь идёт о модифицированной форме (talimogene laherparepvec), логично предположить, что после уничтожения раковых клеток он не будет далее распространяться по организму пациента.
Меланома, на которой и проводились испытания, является наиболее агрессивной формой рака. Её клетки бесконтрольно делятся, при этом организм пациента никак не реагирует на наличие болезни. Любые онкозаболевания подрывают иммунитет, поэтому герпесу проще начать свою разрушительную работу.
Современные разработки по использованию вирусов в борьбе против рака уникальны ещё и тем, что в вирусные клетки встроены гены, активизирующие иммунную систему больного, что позволяет эффективнее справиться с болезнью.
Отличным стоп-фактором является то, что модифицированный вирус герпеса в препарате T-VEC (talimogene laherparepvec), одинаково хорошо проникает в любые клетки, однако в здоровых он не способен размножаться.
Самые последние исследования касаются маскировки модифицированного вируса герпеса от иммунной системы. Если эксперимент закончится удачно, лечение можно было бы свести к внутривенным инъекциям. Сейчас же необходимо вколоть препарат непосредственно в опухоль.
Работа над онколитическими вирусами продолжается. Но уже сейчас у многих больных появилась надежда на излечение. Учёные рекомендуют сочетать лечение модифицированным вирусом герпеса с традиционными методами – химио- и радиотерапией.
[youtube.player]Читайте также:


