Перивентрикулярная лейкоэнцефалопатия перинатального генеза что это такое
Вирусные, аутоиммунные и сосудистые заболевания головного мозга нередко сопровождаются разрушением нервных волокон и утратой важнейший функций органа. Так, прогрессирующая лейкоэнцефалопатия характеризуется поражением оболочек отростков нейронов и постепенной дегенерацией центральной нервной системы. Это редкая патология, формирующаяся у пациентов со сниженным иммунитетом.
Существуют и другие механизмы поражения нервной системы. Сосудистая энцефалопатия хорошо поддается лечению, однако при обнаружении вирусной инфекции ЦНС прогноз неблагоприятный.
Классическая лейкоэнцефалопатия
Прогрессирующая мультифокальная лейкоэнцефалопатия – это редкое инфекционное заболевание, характеризующееся постепенным разрушением миелиновых оболочек нервов и нарушением функций ЦНС. Патологические изменения в головном мозге обусловлены активацией полиомавируса человека 2 типа, возникающем у пациентов со сниженным иммунитетом. У 85-90% людей этот вирус присутствует в тканях, но при этом никак себя не проявляет. Разработка полноценного лечения все еще находится на этапе экспериментов и системных исследований, поэтому на сегодняшний день у болезни неблагоприятный прогноз.
До открытия вируса иммунодефицита человека считалось, что очаговая лейкоэнцефалопатия диагностируется примерно у одного пациента из 100 000 человек. Ближе к концу 20 века случаи обнаружения болезни участились. К этому моменту врачи выявили связь между иммунодефицитом, возникающим на фоне ВИЧ-инфекции, и активацией полиомавируса в тканях мозга. ВИЧ-инфекция и СПИД обнаруживаются у 90% пациентов, страдающих от лейкоэнцефалопатии. Оставшиеся 10% случаев возникновения болезни ассоциированы с другими иммунодефицитными состояниями и аутоиммунными патологиями.
Заболевание проявляется неврологической и психической симптоматикой. Многие пациенты с лейкоэнцефалопатией страдают от психических расстройств. Постепенное прогрессирование недуга приводит к развитию мышечного паралича. Существующие методы терапии дают возможность замедлить патологический процесс и облегчить некоторые симптомы, однако в 50% случаев инфекция заканчивается смертью пациентов.
Головной мозг образован нейронами, их отростками и вспомогательными клетками. Это важнейший регуляторный орган, необходимый для поддержания жизненно важных функций организма и сознательной деятельности. Образующие подкорковые ядра и кору больших полушарий нейроны имеют длинные отростки (аксоны), проводящие импульсы в другие отделы мозга и отдаленные участки тела. С помощью аксонов все участки ЦНС сообщаются друг с другом, благодаря чему сохраняется координации в работе. При этом нормальная передача импульса по отросткам невозможна без специальной оболочки.
Миелиновая оболочка — это белково-липидный комплекс, покрывающий отростки нейронов в центральной нервной системе. Образуют миелин глиальные клетки. Эта структура необходима для электрической изоляции аксонов и быстрого проведения сигнала. Миелиновые оболочки очень важны для быстрой регуляции двигательной активности и поддержания когнитивных способностей, включая эмоциональный контроль, память и интеллект.
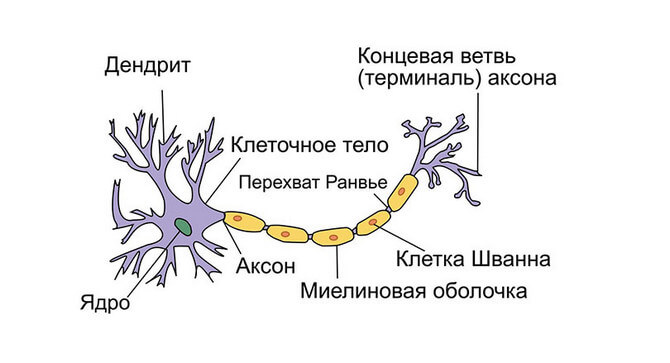
Типичная структура нейрона
Демиелинизация представляет собой процесс разрушения миелиновой оболочки нейронов. Такое осложнение характерно для инфекционных и аутоиммунных заболеваний, включая лейкоэнцефалопатию. Разрушение изоляционной оболочки приводит к тому, что электрические импульсы начинают распространяться в нервах медленно. Возникают разнообразные неврологические расстройства, влияющие на сознательную деятельность и общую регуляцию организма.
Разрушение белого вещества головного мозга наблюдается и при других патологических состояниях.
- Мелкоочаговая лейкоэнцефалопатия — поражение отдельных участков белого вещества головного мозга, возникающее из-за недостаточного кровоснабжения органа. Болезнь преимущественно диагностируется у пожилых мужчин и женщин, страдающих от артериальной гипертензии и атеросклероза.
- Перивентрикулярная лейкоэнцефалопатия. Патология характеризуется одновременным повреждением белого и серого вещества головного мозга. Обнаруживается у пожилых людей с нарушенным церебральным кровообращением и у детей, пострадавших от внутриутробной или родовой гипоксии.
- Задняя обратимая лейкоэнцефалопатия — это тяжелое неврологическое расстройство, формирующееся из-за болезней почек, сниженного иммунитета и лечения кортикостероидами.
- Лейкоэнцефалопатия с накоплением лактата — редкий вид заболевания. Миелин разрушается в основании головного мозга и в структурах спинного мозга.
Другие классификации основаны на области появления патологических изменений и клинических проявлениях болезни. Так, лейкоэнцефалопатия лобных долей в первую очередь негативно влияет на сознательную деятельность человека.
Причины формирования
Патологические изменения в головном мозге, характерные для классической лейкоэнцефалопатии, возникают при первичном заражении или реактивации полиомавируса человека 2 типа в организме. Главным условием формирования болезни является снижение иммунитета. В норме защитные системы организма не позволяют вирусу проявить свои свойства, поэтому инфекционный агент в неактивной форме сохраняется в почках, селезенке и других органах. В случае иммунодефицита полиомавирус активируется в виде оппортунистической инфекции.
Другие виды недуга связаны с нарушением функций сердечно-сосудистой системы. Так, сосудистая лейкоэнцефалопатия представляет собой дегенеративное заболевание головного мозга, характеризующееся постепенным поражением белого и серого вещества на фоне нарушения кровотока. Это отдельная патология, которую можно отнести к разновидностям дисциркуляторной энцефалопатии.
Причины активации вируса:
- Заражение вирусом иммунодефицита человека. Вирусы постепенно уничтожают большое количество иммунокомпетентных клеток, в результате чего механизм сдерживания условно-патогенных инфекционных агентов нарушается. Диффузная лейкоэнцефалопатия диагностируется у 5% людей, страдающих от СПИДа.
- Врожденный иммунодефицит. Это синдром Ди Джорджи, атаксия-телеангиэктазия и другие наследственные патологии, характеризующиеся сниженным иммунитетом и врожденными аномалиями. При такой этиологии лейкоэнцефалопатия нередко выявляется у детей.
- Нарушение кроветворных и иммунных функций при гемобластозах. Онкологические заболевания костного мозга и других структур, образующих компоненты иммунной системы, увеличивают риск возникновения демиелинизирующих процессов.
- Аутоиммунные расстройства — болезни, при которых защитные системы организма начинают атаковать здоровые ткани. Заболевание возникает у пациентов, страдающих от системной красной волчанки, ревматоидного артрита и других патологий иммунитета. Также аутоиммунная лейкоэнцефалопатия появляется при агрессивной иммуносупрессивной терапии.
Таким образом, формирование лейкоэнцефалопатии может быть обусловлено нарушением иммунного контроля организма или недостаточным кровоснабжением нейронов.
Семейство полиомавирусов (Polyomaviridae) было описано во второй половине 20 века. Изначально данные инфекционные агенты были обнаружены в организме птиц и млекопитающих, однако позже ученые доказали опасность отдельных видов вируса для человека. Полиомавирусы способны не только поражать структуры нервной системы, но и увеличивать риск роста опухолей.
Клинически значимые виды вируса:
- полиомавирус человека первого типа — поражает почки и дыхательную систему, часто активируется после пересадки органов;
- полиомавирус человека второго типа — разрушает почки, селезенку и структуры головного мозга, вызывает лейкоэнцефалопатию;
- полиомавирус человека пятого типа — патоген, ассоциированный с редким видом рака кожи.
До 80% людей заражается вирусом еще в детском возрасте. Источником инфекции может быть любой человек с носительством полиомавируса или острой инфекцией. Патогены передаются воздушно-капельным путем. Если иммунодефицит не возникает, вирусные частицы никак себя не проявляют и сохраняются в тканях в течение всей жизни человека.
Врачам известны факторы риска возникновения болезни, связанные с образом жизни, индивидуальным и семейным анамнезом пациентов. Эти признаки увеличивают вероятность появления расстройства, но не обуславливают формирование инфекции или сосудистого недуга напрямую.
Основные факторы риска:
- Медикаментозное лечение рассеянного склероза. В терапии этого демиелинизирующего заболевания иногда используются лекарственные средства, увеличивающие риск активации полиомавируса.
- Патологические состояния, сопровождающиеся сужением просвета артерий и повреждением сосудистой оболочки. Это отложение жировых бляшек в сосудах (атеросклероз), повышенное кровяное давление и врожденные аномалии.
- Пересадка органов с последующей иммуносупрессивной терапией. Защита организма ослабевает, и инфекция начинает поражать головной мозг.
- Аутоиммунные и иммунодефицитные состояния у близких родственников пациента.
- Позднее начало лечения ВИЧ-инфекции и врожденных патологий, нарушающих иммунитет.
- Применение химиотерапии для лечения онкологических заболеваний. Цитостатические препараты негативно влияют на функцию красного костного мозга и снижают иммунитет.
Своевременное обнаружение факторов риска играет важную роль в профилактике заболевания.
Симптомы
Классическая форма болезни вызывает неврологические расстройства уже через несколько дней после активации полиомавируса. В отличие от других инфекций ЦНС, прогрессирующая лейкоэнцефалопатия не проявляется общемозговой и менингеальной симптоматикой. Инфекционные агенты в первую очередь поражают структуры, ответственные за поддержание когнитивных способностей. Позже возникают двигательные нарушения. Разрушение белого вещества мозга ишемической природы также влияет на интеллект и личность, однако патологические изменения развиваются гораздо медленнее. Деменция диагностируется через нескольких лет после начала болезни.

Симптомы и признаки:
- немотивированная смена настроения;
- раздражительность, агрессия;
- снижение остроты зрения;
- апатия и снижение трудоспособности;
- постоянная паранойя;
- снижение интеллекта;
- нарушение памяти;
- неспособность к обучению;
- мышечная слабость;
- нарушение походки.
Вирусная лейкоэнцефалопатия имеет более агрессивное течение. Практически у каждого второго пациента появляются психические расстройства. В случае сосудистой патологии на первый план выходят когнитивные изменения, характерные для деменции.
К какому врачу обращаться
Диагностикой и лечением разных видов энцефалопатии занимаются неврологи. Во время первичного приема врач расспросит пациента о жалобах и изучит анамнестические данные для выявления факторов риска заболеваний ЦНС. Затем проводится общий неврологический осмотр, включающий оценку рефлекторной деятельности. Невролог обращает внимание на походку пациента и координацию работы мышц в целом.
В первичной диагностике может принять участие психотерапевт. Врач этого профиля выявляет психические расстройства, характерные для энцефалопатии, и оценивает степень нарушения когнитивных способностей. Выраженность интеллектуальных и эмоциональных изменений указывает на стадию патологического процесса. Окончательный диагноз может быть поставлен только после проведения инструментальных и лабораторных обследований.
Постановка диагноза
Для обнаружения неврологического расстройства инфекционной природы необходимы визуальные и лабораторные исследования. Важно исключить другие болезни, проявляющиеся похожими симптомами и осложнениями.
- Магнитно-резонансная томография — высокоинформативное визуальное исследование, позволяющее детально оценить состояние всех отделов головного мозга. На изображениях можно обнаружить разнообразные очаги утраты миелина в белом веществе и ядрах органа. Сразу исключается лейкоэнцефалопатия сосудистого генеза.
- Биопсия тканей. С помощью трепанации черепа и пункции врач получает небольшой образец тканей из поврежденного участка органа. Гистологическое исследование материала позволяет подтвердить диагноз.
- Поиск вирусных частиц в спинномозговой жидкости с помощью полимеразной цепной реакции (ПЦР). Это точное лабораторное исследование, направленное на поиск активной инфекции. Для проведения теста проводится люмбальная пункция.
- Офтальмологические обследования, направленные на оценку остроты зрения и поиск специфических отклонений, характерных для болезни.
Основные признаки заболевания можно увидеть на МРТ. Уточняющие исследования необходимы для оценки тяжести состояния.
Этот вид поражения головного мозга обнаруживается с помощью иных инструментальных исследований. Неврологу необходимо оценить состояние церебральных сосудов.
- Ультразвуковая диагностика сосудов головы и шеи — безопасное визуальное исследование, необходимое для оценки эффективности кровоснабжения ЦНС.
- Магнитно-резонансная ангиография. С помощью томографа невролог получает объемные изображения артерий и вен разных участков мозга. МР-признаки сосудистой лейкоэнцефалопатии в основном представлены очагами ишемии и дегенерации нейронов.
- Исследование сердечно-сосудистой системы с помощью электрокардиографии, суточного мониторинга ЭКГ и ультразвукового обследования.
Для уточнения состояния сосудов может быть назначена консультация кардиолога. Также проводится офтальмологическое обследование.
Методы лечения
Многоочаговая лейкоэнцефалопатия вирусной природы не поддается лечению. Существуют только схемы поддерживающей терапии, замедляющей развитие болезни. Пациентам назначают нейропротекторные лекарственные средства. Если заболевание возникло на фоне терапии аутоиммунных патологий, проводится очистка крови (плазмаферез). В последнее время появились сведения об эффективности некоторых нейролептиков и антидепрессантов в лечении заболевания, однако исследования такой терапии еще не завершились.
Сосудистая лейкоэнцефалопатия может быть скорректирована медикаментозно. Врачи подбирают лекарственные препараты, непосредственно влияющие на механизм развития болезни. Необходимо восстановить кровообращение в ЦНС и устранить негативные факторы, включая повышенное кровяное давление и атеросклероз. При обнаружении структурных патологий крупных артерий проводится оперативное вмешательство.
Лекарственные назначения при сосудистой форме патологии:
- блокаторы кальциевых каналов и антагонисты адренорецепторов для улучшения кровоснабжения тканей;
- антиагреганты для предотвращения формирования тромбов в артериях и венах;
- нейропротекторные медикаменты, включая ноотропы, витамины и микроэлементы.
Схема медикаментозной терапии первичных сердечно-сосудистых заболеваний подбирается кардиологом. Пациентам с артериальной гипертензией необходимо постоянно контролировать кровяное давление и соблюдать диету. При любых формах энцефалопатии необходимо отказаться от приема алкоголя и курения. Избыточные физические нагрузки также могут усугубить состояние.
Сколько живут с таким диагнозом
Вирусная лейкоэнцефалопатия характеризуется крайне неблагоприятным прогнозом. Каждый второй пациент впадает в кому и умирает через несколько месяцев после появления патологических изменений. Важно учитывать, что до 90% больных страдает от СПИДа или врожденного иммунодефицита, поэтому прогноз также зависит от сопутствующих заболеваний. Качество жизни выживших пациентов значительно ухудшается из-за когнитивных и неврологических осложнений.
Сосудистое поражение головного мозга не так опасно. Адекватная медикаментозная терапия дает возможность замедлить развитие болезни и значительно улучшить состояние. При регулярном приеме назначенных врачом препаратов и правильном образе жизни больные живут в течение пяти и более лет после постановки диагноза. Если помимо основной патологии у пациента диагностируют инсульт и деменцию, прогноз неблагоприятный.
Версия: Справочник заболеваний MedElement
Общая информация
Примечание. Из данной подрубрики исключена "Субкортикальная сосудистая деменция (F01.2).
Этиология и патогенез
Описаны семейные случаи заболевания с началом до 40 лет, без артериальной гипертензии. Более чем в 80% случаев болезнь дебютирует в возрастном промежутке от 50 до 70 лет.
Страдают также и более крупные артерии диаметром до 500 мкм, и все микроциркуляторное русло.
Эпидемиология
Болезнь (энцефалопатия) Бинсвангера встречается довольно часто. По данным клинико-компьютерно-томографического исследования, она составляет около 1/3 всех случаев сосудистой деменции.
Возраст. Более чем в 80% случаев болезнь дебютирует в возрастном промежутке от 50 до 70 лет.
Факторы и группы риска
Клиническая картина
Клиническая картина болезни Бинсвангера характеризуется прогрессирующими когнитивными нарушениями, нарушениями функции ходьбы и тазовыми расстройствами. На последнем этапе заболевания клиническая картина представлена слабоумием, полной беспомощностью больных (не ходят, не обслуживают себя, не контролируют функцию тазовых органов).
Картина слабоумия может значительно варьироваться по степени тяжести и особенностям симптоматики.
В целом для болезни Бинсвангера характерно неуклонно-прогредиентное течение, но возможны и периоды длительной стабилизации. Причинами слабоумия в этих случаях считаются разобщение корково-подкорковых связей, наступающее в результате поражения подкоркового белого вещества, а также дисфункция базальных ганглиев и таламуса.
Основные характеристики лобной диспраксии ходьбы, связанной с дезавтоматизацией ходьбы, следующие:
• замедление ходьбы;
• укорочение шага;
• затруднение в начале ходьбы (инициация ходьбы);
• неустойчивость при поворотах (постуральная дисфункция);
• расширение базы опоры;
• снижение длины шагов.
Двигательные нарушения могут также характеризоваться (помимо нарушения ходьбы): другой экстрапирамидной патологией в виде паркинсоноподобной симптоматики, а также легкими или умеренными центральными моно- или гемипарезами, часто быстро регрессирующими (регресс очаговой двигательной симптоматики становится неполным по мере прогрессирования заболевания). Характерен псевдобульбарный синдром.
Эмоционально-волевые нарушения представлены астеническим, неврозоподобным или астено-депрессивным синдром. По мере прогрессирования заболевания на первый план выходят не астения и депрессия, а нарастание эмоционального оскудения, сужение круга интересов и спонтанности.
В критериях подчеркивается, что у пациента должны отсутствовать множественные или двухсторонние корковые очаги по данным КТ и МРТ, и тяжелая деменция.
Диагностика
Осложнения
- 1) Транзиторная ишемическая атака .
Транзиторные ишемические атаки (ТИА, преходящие нарушения мозгового кровообращения) характеризуются кратковременными симптомами локальной ишемии мозга.
ТИА обычно связаны с гемодинамической недостаточностью, возникающей при выраженном атеросклеротическом стенозе сонных или позвоночных артерий в их дистальных ветвях или артериальной эмболией.
В большинстве случаев транзиторные ишемические атаки разрешаются в течение 5-20 минут.
Клиническое значение ТИА состоит в том, что они служат предвестниками не только инсульта, но и инфаркта миокарда и представляют собой сигналы опасности, требующие от врача быстрых действий. Больных с ТИА необходимо госпитализировать в инсультное отделение для наблюдения, всестороннего обследования и проведения профилактики ишемического инсульта.
ТИА часто проявляются при снижении АД, физической нагрузке, натуживании, приеме пищи; при этом очаговые неврологические симптомы нередко проявляются на фоне предобморочного состояния, иногда по нескольку раз в день. Больные часто жалуются на предобморочное состояние, головокружение, нарушения зрения, слабость в конечностях, тошноту и рвоту, нарушения памяти, шум в ушах, нарушения чувствительности, неожиданную утрату равновесия.
2) Инсульты - острые нарушения мозгового кровообращения (ОНМК) .
Различают инсульты - ишемический инсульт и внутримозговое (паренхиматозное) кровоизлияние .
Ишемический инсульт возникает в результате критического снижения или прекращения кровоснабжения участка мозга с последующим развитием очага некроза мозговой ткани.
Внутримозговое кровоизлияние возникает в результате разрыва патологически измененных сосудов мозга, приводящего к кровоизлияниям.
Лейкоэнцефалопатия головного мозга может поразить человека любого возраста. Чаще всего возникновение и развитие этой болезни связывают со стабильно повышенным давлением, эпизодами кислородного голодания и распространением полиомавируса.

Лекарственных препаратов, способных остановить развитие заболевания, в настоящее время не существует.
Описание
Лейкоэнцефалопатия – заболевание, характеризующееся стойким разрушением в головном мозге белого вещества. Болезнь развивается быстро и практически всегда приводит к летальному исходу.
Патология впервые описана Людвигом Бинсвангером в 1964 г., поэтому иногда ее называют болезнью Бинсвангера.
Причины
Принято выделять 3 основные причины, приводящие к лейконэнцефалопатии. Это гипоксия, стабильно высокое давление и вирусы. Провоцируют ее возникновение следующие заболевания и состояния:
- эндокринные нарушения;
- гипертония;
- атеросклероз;
- злокачественные опухоли;
- туберкулез;
- ВИЧ и СПИД;
- патологии позвоночника;
- генетический фактор;
- вредные привычки;
- родовая травма;
- прием препаратов, снижающих иммунную реакцию организма.
Провоцирующее действие вредоносных факторов ведет к демиелинизации пучков нервных волокон. Белое вещество уменьшается в объеме, размягчается, изменяет структуру. В нем появляются кровоизлияния, очаги поражения, кисты.

Часто демиелинизацию вызывают полиомавирусы. В неактивном состоянии они присутствуют в жизни человека постоянно, сохраняясь в почках, костном мозге, селезенке. Ослабление иммунитета приводит к активизации вирусов. Лейкоциты переносят их в центральную нервную систему, где они находят благоприятную среду в мозге, поселяются в нем и разрушают его.
Обычно необратимым изменениям подвергается только белое вещество. Однако есть данные и о том, что, вероятно, перивентрикулярный вид лейкоэнцефалопатии ведет также к поражению серого вещества.
Классификация
Определение основной причины патологии и характера ее течения позволяет выделять несколько типов лейкоэнцефалопатии.
Основной причиной появления и развития мелкоочаговой лейкоэнцефалопатии сосудистого генеза является поражение сосудов мозга, вызванное гипертонией, травмами, появлением атеросклеротических бляшек, эндокринными заболеваниями, болезнями позвоночника. Кровообращение нарушается из-за сгущения крови и закупорки сосудов. Ухудшающим состояние фактором является алкоголизм и ожирение. Считается, что болезнь развивается при наличии отягчающих наследственных факторов.
Данную патологию называют также прогрессирующей сосудистой лейкоэнцефалопатией. Сначала появляются небольшие очаги поражения сосудов, потом они увеличиваются в размерах, вызывая ухудшение состояния больного. С течением времени нарастают признаки патологии, заметные окружающим. Ухудшается память, снижается интеллект, возникают психоэмоциональные расстройства.
Больной жалуется на тошноту, головную боль, постоянную усталость. Сосудистая мелкоочаговая энцефалопатия характеризуется скачками давления. Человек не может глотать, с трудом пережевывает пищу. Появляется тремор, отличающий болезнь Паркинсона. Утрачивается способность контролировать процессы мочеиспускания и дефекации.
Очаговая энцефалопатия сосудистого генеза регистрируется в основном у мужчин после 55 лет. Ранее данное нарушение было включено в список МКБ, но в дальнейшем его исключили.
Главной особенностью этого типа нарушения считается появление большого количества очагов повреждения. Вызывают воспаление полиомавирус человека 2 (JC polyomavirus). Он обнаруживается у 80% жителей Земли. В скрытом состоянии живет в организме несколько лет, но при ослаблении иммунитета активируется и, попадая в ЦНС, вызывает воспаление.
Провоцирующими заболевание факторами являются СПИД, ВИЧ-инфицирование, длительное применение иммунодепрессантов и лекарств, предназначенных для лечения онкологических заболеваний. Прогрессирующая мультифокальная энцефалопатия диагностируется у половины пациентов со СПИДом и 5% людей с ВИЧ-инфекцией.

Поражение часто имеет асимметричный характер. Признаками ПМЛ являются параличи, парезы, ригидность мышц, тремор, напоминающий болезнь Паркинсона. Лицо приобретает вид маски. Возможна потеря зрения. Проявляются тяжелые когнитивные нарушения, снижение внимания.
Мультифокальная лейкоэнцефалопатия не лечится. Для улучшения состояния больного убирают препараты, подавляющие иммунитет. Если заболевание вызвано пересадкой органа, он подлежит удалению.
Лейкопатию головного мозга у ребенка вызывает гипоксия, возникшая при родах. Инструментальные методы диагностики позволяют увидеть участки гибели ткани, преимущественно рядом с мозговыми желудочками. Перивентрикулярные волокна несут ответственность за двигательную активность, и их поражение ведет к детскому церебральному параличу. Очаги поражения возникают симметрично, в особо тяжелых случаях обнаруживаются во всех центральных зонах мозга. Поражение характеризуется прохождением 3 стадий:
- возникновение;
- развитие, приводящее к структурным изменениям;
- образование кисты или рубца.
Перивентрикулярная лейкоэнцефалопатия характеризуется 3 степенями заболевания. Легкая степень характеризуется незначительной выраженностью симптомов. Обычно они проходят через неделю после рождения. Для средней степени характерно повышение внутричерепного давления, возникают судороги. При тяжелой ребенок находится в коме.
Симптомы появляются не сразу, некоторые из них можно заметить только через 6 месяцев после рождения ребенка. Чаще всего обращают на себя внимание парезы и парализация. Наблюдается косоглазие, заторможенность, гиперактивность.
Лечение включает массаж, физиопроцедуры, специальные комплексы упражнений.
Основной причиной этого заболевания являются мутации генов, подавляющие белковый синтез. Чаще всего появляется у детей, преимущественно в возрасте от двух до шести лет. К провоцирующим факторам относят сильное психическое напряжение, вызванное травмой или тяжелой болезнью.
Лейкоэнцефалопатия – это такое заболевание, которое приводит к повреждению белого вещества, составляющего основу головного мозга, что провоцирует многочисленные неврологические синдромы. Характеризуется быстрым прогрессированием и развитием демиелинизирующих патологических процессов.
Определение патологии
Лейкоэнцефалопатия всегда сопровождается поражением белого мозгового вещества, которое возникает вследствие разных причин: сосудистых патологий, инфицирования полиомавирусом, генных мутаций. Инфекционная форма развивается из-за реактивации полиомавируса JC, который в латентном состоянии находится в организме многих людей.
Наследственная форма заболевания аутосомно-рецессивного генеза возникает на фоне генной мутации (преимущественно гена EIF2B5). Мелкоочаговая лейкоэнцефалопатия сосудистого генеза – это такое заболевание, которое развивается вследствие поражения небольших элементов кровеносной системы мозга, что провоцирует характерные для гипоксически-ишемического поражения тканей симптомы.
Классификация заболевания
Различают формы патологии в зависимости от причин возникновения. Сосудистая форма лейкоэнцефалопатии, известная как болезнь Бинсвангера – это такое заболевание головного мозга, которое носит прогрессирующий характер, развивается на фоне гипертонической болезни, что указывает на ведущую роль в патогенезе атеросклероза и других патологий сосудов.
Клиническая картина напоминает проявления субкортикальной (подкорковой) энцефалопатии артериосклеротической этиологии. Патогенез связан с поражением белого вещества на фоне атеросклероза мелких артерий и артериол, вследствие чего происходит утолщение сосудистых стенок и сужение просвета, развивается гиалиноз – белковая дистрофия с замещением нормальной ткани более плотной, малоэластичной структурой.
Типичные осложнения: ТИА (преходящие нарушения мозгового кровообращения), инсульты. Третья часть всех клинических случаев сосудистой деменции обусловлена мультифокальной лейкоэнцефалопатией. В 80% случаев возраст пациентов составляет 50-70 лет. Очаговое поражение белого вещества инфекционного генеза возникает вследствие реактивации вируса JC.
Перивентрикулярная лейкоэнцефалопатия, известная как перивентрикулярная лейкомаляция, характеризуется возникновением очагов поражения белого вещества чаще возле желудочковой системы. При масштабном поражении очаги распространяются в центральные отделы белого вещества.
Демиелинизирующий процесс агрессивного, длительного течения приводит к образованию некротических полостей в мозговых структурах. Лейкоэнцефалопатия (лейкомаляция) головного мозга, обнаруженная у детей, часто является причиной развития в детском возрасте церебрального паралича (ДЦП).
Причины возникновения
Основная причина развития формы инфекционного генеза – реактивация полиомавируса. Это безоболочечный вирус JC, который обнаруживается у 80% населения. Обычно не вызывает развитие заболеваний. В этом случае инфицированные люди являются носителями. Активация происходит на фоне подавления деятельности иммунной системы, часто у пациентов с диагнозом ВИЧ.
Инфицирование ВИЧ часто сопровождается типичным симптомом – развитием многоочаговой лейкоэнцефалопатии с прогрессирующим течением патологии. Заболевание возникает как результат терапии иммуномодуляторами (после имплантации органов), иммуносупрессорами или моноклональными антителами, из-за чего происходит угнетение иммунной системы.
Терапия при помощи моноклональных антител проводится в отношении рассеянного склероза, аутоиммунных заболеваний крови, неходжкинской лимфомы, артрита ревматоидной формы. Вирус JC попадает в организм через органы желудочно-кишечного тракта с зараженной водой и пищей или воздушно-капельным путем. Процесс инфицирования протекает бессимптомно.
Вирус пребывает в организме латентно до появления факторов, провоцирующих активацию. Провоцирующие факторы ассоциируются с пересадкой стволовых клеток и лечением препаратами – аналогами пурина (Фопурин, Меркаптопурин, Пуринетол). Мелкоочаговая лейкоэнцефалопатия, которая развилась на фоне сосудистых патологий, обычно спровоцирована факторами:
- Артериальная гипертензия, длительно протекающая, устойчивая.
- Артериальная гипотензия.
- Патологическое изменение циркадного (биологического) ритма артериального давления – резкое повышение или понижение показателей давления в ночное время.
Патологические изменения в мозговых структурах происходят в результате хронической гипоксии – кислородного голодания. Вероятные причины включают врожденные аномалии развития элементов сосудистой системы, возрастные деформации, посттравматические дефекты и другие нарушения, провоцирующие ухудшение церебрального кровотока.
Симптоматика
Мелкоочаговая энцефалопатия инфекционного генеза характеризуется отсутствием признаков воспалительного процесса в мозговом веществе. Проникая в ЦНС вирус вызывает лизис (растворение) олигодендроцитов, что приводит к масштабной демиелинизации – повреждению миелиновых оболочек.
Инфицированные олигодендроциты располагаются по краям очага демиелинизации. Постепенно патологический процесс охватывает обширные участки мозга, что провоцирует нарастающее развитие неврологической симптоматики:
- Гемипарезы (парезы в одной стороне тела).
- Гемисоматосенсорные расстройства (нарушение чувствительности – онемение, покалывание, изменение восприятия температуры, изменение реакции на болевые раздражители, искажение пространственного представления о положении отдельных частей тела относительно друг друга).
- Эпилептические припадки. Наблюдаются у 20% больных, что указывает на близость очага к коре.
В зависимости от локализации очага поражения появляются такие симптомы, как атаксия (нарушение согласованности при сокращении группы мышц), афазия (речевая дисфункция), зрительные расстройства, апраксия (нарушение целенаправленных движений), дисметрия (избыточность или недостаточность при выполнении произвольных движений). Для патологии типичны когнитивные расстройства, нередко перерастающие в деменцию.
Поражение тканей полушарий с соответствующей симптоматикой в клинической практике встречается в 10 раз чаще, чем стволовых структур. В ходе исследования МРТ обнаруживаются крупные субкортикальные (подкорковые) очаги – гиперинтенсивные (режим Т2) и гипоинтенсивные (режим Т1). С увеличением диаметра очага неврологический дефицит нарастает. Сосудистая лейкоэнцефалопатия сопровождается симптомами:
- Когнитивные расстройства (ухудшение памяти и умственной деятлеьности) с тенденцией к прогрессированию.
- Атаксия, моторная дисфункция.
- Нарушение двигательной координации.
- Недержание мочи, непроизвольная дефекация.
Для поздних стадий течения заболевания свойственно развитие слабоумия. Больные теряют способность к самообслуживанию, круглосуточно нуждаются в медицинской помощи. У больных отсутствует интерес к речевой, двигательной, познавательной, психической деятельности. Периодически возникает чувство эйфории. У некоторых пациентов происходят эпилептические припадки.
Для болезни Бинсвангера типична тенденция к прогрессированию. Нередко наблюдаются длительные периоды стабильного состояния. Слабоумие развивается из-за нарушения корково-подкорковых связей, которые возникают вследствие повреждения белого вещества. Не последнюю роль в патогенезе играет дисфункция таламуса и базальных ганглиев.
Очаговая лейкоэнцефалопатия – это такое заболевание, для которого характерно изменение походки, что указывает на поражение сосудистого генеза экстрапирамидной системы. Походка больного становится медленной, семенящей, шаги укорачиваются, наблюдается постуральная дисфункция – затруднение движения на поворотах. Пациенту сложно инициировать (начать) движение. Иногда двигательные расстройства проявляются по типу паркинсонизма (ригидность, скованность мышц, тремор).
Симптоматика дополняется гемипарезами (парез в одной половине тела) и псевдобульбарным синдромом (дизартрия – нарушение произношения, дисфония – ослабление силы голоса, дисфагия – затруднения при глотании, непроизвольный плач или смех). Для постановки диагноза многоочаговая лейкоэнцефалопатия сосудистой этиологии необходимо наличие признаков:
- Деменция.
- Факторы риска развития сосудистых заболеваний или признаки сосудистой патологии, затронувшей кровеносную систему мозга.
- Неврологические синдромы, характерные для поражения субкортикальных (подкорковых) структур мозга (изменение походки, недержание мочи, паратония – непроизвольное сопротивление пассивным движениям).
Исследование КТ показывает двухсторонний лейкоареоз – малую ишемию сосудов, повреждения элементов сосудистой системы белого вещества. При перивентрикулярной лейкоэнцефалопатии на МР-томограмме различается диффузно-очаговое поражение белого вещества преимущественно симметричное.
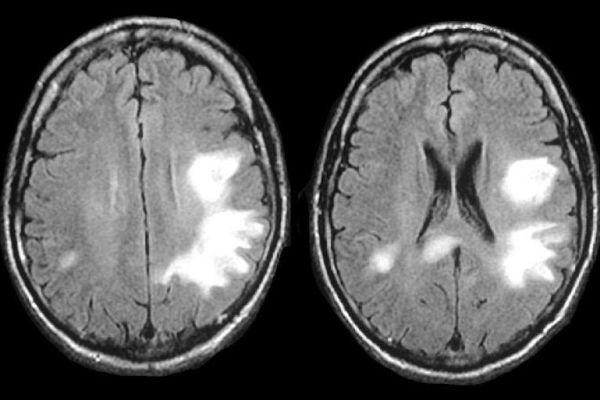
Для сравнения при вирусном поражении очаги расположены преимущественно ассиметрично. Единичный неспецифический очаг лейкоэнцефалопатии может быть ошибочно расценен, как проявление инсульта.
Методы диагностики
Ранняя диагностика JС-ассоциированной инфекции позволяет своевременно начать лечение. Нейровизуализация остается приоритетным способом обнаружения участков патологически измененной ткани. Основные методы инструментальной диагностики:
- МРТ, КТ.
- Допплерография сосудов мозга.
- Электроэнцефалография.
- Биопсия. Исследование мозгового биоптата. Чувствительность метода оценивается в 64-90%.
Исследование типа ПЦР помогает обнаружить ДНК вируса. Чувствительность метода оценивается в 72-92%.
Способы лечения
Лечение патологии сосудистого генеза предполагает устранение причин, спровоцировавших развитие заболевания. Чаще назначают лекарства и другие методы терапии, направленные на стабилизацию повышенного или пониженного артериального давления. Показаны препараты:
- Улучшающие микроциркуляцию крови в мозговых структурах.
- Стимулирующие метаболические процессы в клетках мозга.
- Устраняющие неврологическую симптоматику.
Параллельно проводится терапия атеросклероза и сопутствующих соматических болезней. Специфического лечения при вирусной форме не существует. Эффективными мерами считаются:
- Прекращение приема иммуносупрессоров (кортикостероиды, цитостатики). Или уменьшение их дозировки.
- Отмена Натализумаба – препарата на основе моноклональных антител, если реактивация вируса произошла вследствие его применения. Параллельно рекомендуется проведение плазмафереза до 5 сеансов ежедневно для выведения препарата.
- Назначение Мефлоцина (антималярийный препарат). Некоторые исследования показывают эффективность лекарства, которое замедляет репликацию (размножение) вируса JС.
Антидепрессант Миртазапин ингибирует обратный захват серотонина, препятствует распространению вируса JС. Механизм действия основан на блокировании рецепторов 5-НТ2, которые являются мишенью для полиомавируса.
Прогноз
Сколько живут при диагнозе лейкоэнцефалопатия головного мозга, зависит от причин развития и характера течения патологии. Прогноз продолжительности жизни составляется индивидуально лечащим врачом с учетом возраста и физического состояния пациента. Прогноз заболевания сосудистого генеза условно благоприятный. Своевременная коррекция сосудистых нарушений позволяет отсрочить масштабное повреждение белого вещества.

При диагнозе ВИЧ лейкоэнцефалопатия, обусловленная вирусом, занимает второе место среди причин смертности, уступая только неходжкинской лимфоме. Многочисленные результаты аутопсии показали отсутствие прямой связи между смертностью и морфологическими особенностями строения очагов (размеры, локализация, степень атрофии тканей, гидроцефалия) при вирусной форме болезни.
Профилактические мероприятия
Для профилактики патологии больным рассеянным склерозом, которым проводится терапия Натализумабом, назначают превентивное обследование на наличие вируса JС. Профилактические меры включают общие рекомендации по укреплению иммунитета:
- Закаливающие процедуры.
- Отказ от вредных привычек.
- Организация здорового, полноценного питания.
- Активный образ жизни, дозированные физические нагрузки.
Предотвращение родовых травм в перинатальный период и повреждений в области головы во взрослом возрасте, систематический контроль и коррекция значений артериального давления помогут избежать осложнений и быстрого прогрессирования заболевания.
Лейкоэнцефалопатия – прогрессирующий процесс разрушения белого вещества. Ранняя диагностика и корректная терапия патологии сосудистого генеза способствует значительному улучшению состояния больного.
Читайте также:


