Ответ: Инфекционные — 14, неинфекционные — 25, наследственные — 3.
Определите преимущественный способ размножения растений. Запишите номер каждого из растений в списке в соответствующую ячейку таблицы. В ячейках таблицы может быть записано несколько номеров.
| Половое размножение | Вегетативное размножение |
Видоизмененными подземными побегами | Стеблевыми черенками |
Вегетативное размножение — образование новой особи из многоклеточной части тела родительской особи, один из способов бесполого размножения, свойственный многоклеточным организмам.
Видоизмененными подземными побегами — корневище, клубень, луковица.
Черенкование – это получение молодых растений из кусочков стебля материнской культуры.
Половое размножение отличается наличием полового процесса, который обеспечивает обмен наследственной информацией и создает условия для возникновения наследственной изменчивости. В нем, как правило, участвуют две особи — женская и мужская, которые образуют гаплоидные женские и мужские половые клетки — гаметы.
Ответ: половое размножение — 14, побегами — 35, черенками — 2.
![]()
![]()
Дифтерия - это острое инфекционное заболевание, опасное для жизни. Наиболее восприимчивы к нему дети в возрасте 3–7 лет, в последние годы увеличилась заболеваемость подростков и взрослых.
Дифтерия – это острое инфекционное заболевание, опасное для жизни. Оно протекает в виде острого воспаления верхних дыхательных путей, преимущественно глотки (примерно 90% случаев), носа, кожи в местах ее повреждения, глаз или половых органов.
Основную угрозу, однако, представляет не воспаление, а отравление токсином, который вырабатывает бактерия – возбудитель заболевания, при этом преимущественно поражаются сердечно-сосудистая и нервная системы.
Возбудитель дифтерии и пути заражения
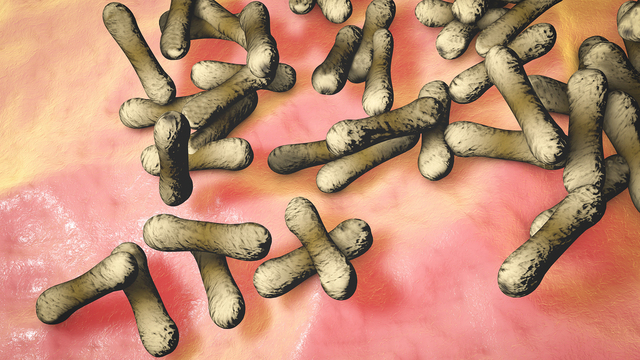
Возбудителем дифтерии являются Corynebacterium diphteriae – грамположительные бактерии в виде палочек с характерными колбовидными утолщениями на концах, которые в мазках располагаются попарно, под углом в виде римской цифры V по отношению друг к другу. Дифтерийные палочки в процессе жизнедеятельности выделяют дифтерийный токсин, фермент нейраминидазу и другие биохимически активные соединения.
Синтез дифтерийного токсина микробными клетками контролируется специальным геном tox. Бактерии могут терять его в процессе жизнедеятельности, утрачивая вместе с ним и свою способность вырабатывать токсин (токсигенность). И, наоборот, изначально нетоксигенные штаммы могут приобретать патогенные свойства, к счастью, это случается крайне редко.
Заболевание передается воздушно-капельным путем от больных дифтерией или от здоровых носителей инфекции, значительно реже – через предметы обихода.
Группа риска
Наиболее восприимчивы к заражению дифтерией дети в возрасте 3–7 лет, но в последние годы увеличилась заболеваемость подростков и взрослых.
Источником инфекции являются больные люди или здоровые носители токсигенных бактерий. Наиболее заразны страдающие дифтерией зева, носа и гортани, так как они активно выделяют возбудителей заболевания с выдыхаемым воздухом. Больные дифтерией глаз, кожи могут распространять инфекцию контактным путем (руки, предметы быта). Здоровые носители бактерий гораздо менее заразны, но отсутствие у них каких-либо внешних признаков их состояния не позволяет контролировать распространение ими инфекции, ведь выявить их можно только случайно в ходе массовых диспансерных обследований. В результате большинство случаев заражения дифтерией обусловлено контактом со здоровыми носителями дифтерийной палочки.
Инкубационный период (время от момента заражения до появления первых признаков заболевания) составляет 2–10 дней.
Дифтерийный токсин
Токсин, вырабатываемый дифтерийной палочкой, состоит из нескольких компонентов. Один из них – фермент гиалуронидаза разрушает гиалуроновую кислоту капилляров и увеличивает их проницаемость, что приводит к выходу из сосудов и пропитыванию окружающих тканей плазмой крови с отложением белка фибриногена. Второй компонент – некротоксин разрушает клетки эпителия с выделением из них фермента тромбокиназы. Тромбокиназа способствует превращению фибриногена в фибрин и образованию на поверхности тканей фибринной пленки. При действии дифтерийного токсина на небные миндалины, которые покрыты несколькими слоями эпителиальных клеток, формируется фибиринная пленка, проникающая вглубь эпителия миндалин и плотно спаянная с ним.
Третий (основной) компонент – собственно токсин способен блокировать процессы клеточного дыхания и синтеза белковых молекул. Наиболее чувствительными к его действию являются капилляры, клетки миокарда и нервные клетки. В результате развивается дистрофия миокарда и инфекционно-токсический миокардит, повреждение капилляров приводит к инфекционно-токсическому шоку, повреждение шванновских клеток (вспомогательные клетки нервной ткани) приводит к демиелинизации нервных волокон (разрушение электроизолирующего слоя миелина с нарушением проведения нервных импульсов по нервным волокнам). Кроме того, дифтерийный токсин вызывает общую интоксикацию организма.
Симптомы и течение
Дифтерия зева обычно начинается с небольшого повышения температуры, незначительной болезненности при глотании, покраснения и отечности миндалин, формированию на них специфического пленчатого налета, увеличения передних верхних шейных лимфатических узлов. Цвет пленок – обычно белый в первые 2–3 дня заболевания, но потом приобретает серый или желтовато-серый цвет. Примерно через неделю заболевание, или заканчивается выздоровлением (легкая форма, как правило, у привитых от дифтерии), или переходит в более тяжелую токсическую форму, обусловленную системным действием дифтерийного токсина.
Токсическая форма дифтерии всегда протекает очень тяжело. Она характеризуется очень высокой температурой тела (39,5-41,0°С), сильными головными болями, сонливостью, апатией. Кожа становится бледной, во рту отмечается сухость, у детей возможна многократная рвота и боль в животе. Отек миндалин становится резко выраженным, может приводить к полному закрытию входа в глотку, распространяется на мягкое и твердое небо, часто также на носоглотку, дыхание затрудняется, голос часто становится гнусавым. Налет распространяется на все ткани ротоглотки. Классическим признаком токсической формы дифтерии зева является отек подкожной клетчатки в области шеи, а иногда и грудной клетки, в результате чего кожа приобретает студнеобразную консистенцию. Передние верхние шейные лимфатические узлы значительно увеличены и болезненны.
Дифтерия носа протекает на фоне нормальной или слегка повышенной температуры тела, интоксикация отсутствует. Из носовых ходов видно серозно-гнойное или кровянисто-гнойное отделяемое. На крыльях носа, щеках, лбу и подбородке появляются участки мокнутия, а затем сухие корочки. Внутри носа видны пленчатые налеты. Патологический процесс может также поражать придаточные пазухи носа. При токсической форме наблюдается отек подкожной клетчатки щек и шеи.
Дифтерия глаза протекает как банальный конъюнктивит и характеризуется умеренной гиперемией и отеком конъюнктивы века, небольшим количеством серозно-гнойного отделяемого из конъюнктивального мешка (катаральная форма). Пленчатая форма проявляется выраженным отеком век, наличием на их конъюнктиве трудно снимаемых пленок серовато-белого цвета. Токсическая форма также сопровождается отеком клетчатки вокруг глазницы.
Дифтерия кожи приводитк длительному не заживлению любых повреждений кожи, гиперемии, на коже присутствует грязно-серый налет, отмечается плотная инфильтрация окружающей кожи.
Диагностика
Диагностику дифтерии проводят на основании данных осмотра больного и результатов анализов. При осмотре за диагноз дифтерия говорят следующие признаки: наличие характерных пленок, а также затруднение дыхания и свистящий шум на вдохе, не характерные для ангины, лающий кашель. Диагноз дифтерии по характерным клиническим признакам при заболевании, протекающем в легкой форме, поставить сложнее.
Общий анализ крови – признаки острого воспалительного процесса.
Исследования мазка под микроскопом (бактериоскопия) – выявление имеющих характерный вид бактерий Corynebacterium diphteriae.
Бактериологическое исследование – посев биологического материала на специальную питательную среду и культивирование колоний микроорганизмов.
Определение уровня (титра) антитоксических антител (высокий титр – 0,05 МЕ/мл и выше позволяет исключить дифтерию).
Серологическое исследование – определение специфических антител в сыворотке крови с помощью методов РПГА, ИФА и др.
Дифтерию зева нужно дифференцировать от острого тонзиллита (фолликулярная и лакунарная формы), ангины Симановского-Венсана (грибковое поражение), сифилитической ангины, ложнопленочной ангины при инфекционном мононуклеозе, паратонзиллярным абсцессом, эпидемическим паротитом, лейкозом. У детей необходимо отвести диагноз ложного крупа.
Лечение
Всех заболевших дифтерией, вне зависимости от тяжести состояния, необходимо госпитализировать в инфекционную больницу.
Лечение состоит в следующем:
Диета – витаминизированная, калорийная, прошедшая тщательную кулинарную обработку еда.
Этиотропная терапия (то есть направленная на устранение причины заболевания) – введение противодифтерийной сыворотки (ПДС), доза и количество раз введения зависят от тяжести и формы заболевания. При легкой форме ПДС вводится однократно внутримышечно в дозе 20–40 тыс. МЕ, при среднетяжелой форме – 50–80 тыс. МЕ однократно или, при необходимости, повторно в той же дозе через 24 часа. При лечении тяжелой формы заболевания суммарная доза увеличивается до 90–120 тыс. МЕ или даже до 150 тыс. МЕ (инфекционно-токсический шок, ДВС-синдром). При этом 2/3 дозы вводится сразу, и в течение первых суток госпитализации должно быть введено 3/4 суммарной дозы.
Антибиотики: при легких формах – эритромицин, рифампицин внутрь, при среднетяжелых и тяжелых формах – инъекционное введение пенициллинов или цефалоспоринов. Продолжительность курса – 10–14 дней. Антибиотики не влияют на дифтерийный токсин, но уменьшают количество бактерий, его вырабатывающих.
Местное лечение – полоскания и орошения дезинфицирующими растворами.
Дезинтоксикационная терапия – глюкозо-солевыми растворами с учетом суточной потребности в жидкости и ее потерь (среднетяжелая и тяжелая форма).
Глюкокортикостероиды – при среднетяжелой и тяжелой формах.
Лечение бактерионосителей проводят антибиотиками: тетрациклины (дети старше 9 лет), эритромицин, цефалоспорины на фоне общеукрепляющей терапии и устранения хронических очагов инфекции.
Осложнения
Среди наиболее серьезных осложненийдифтерии на сердечно-сосудистую систему можно выделить миокардиты, нарушения сердечного ритма.
Неврологические осложнения дифтерии обусловлены поражением различных черепных и периферических нервов и проявляются параличом аккомодации, косоглазием, парезами конечностей, а в более тяжелых случаях параличом дыхательных мышц и мышц диафрагмы.
Вторичными осложнениями дифтерии являются такие тяжелые патологические состояния как острые нарушения мозгового кровообращения (тромбозы, эмболия), метаболическая энцефалопатия, отек головного мозга, токсические поражения почек, дифтерийный гепатит, а также инфекционно-токсический шок и ДВС-синдром (синдром дессиминированного внутрисосудистого свертывания – тяжелое нарушение системы свертывания крови). Токсическая форма дифтерии может приводить к острой почечной, сердечно-сосудистой, дыхательной или полиорганнной недостаточности.
Неспецифическими осложнениями дифтерии являются паратонзиллярный абсцесс, отит, пневмония.
Вакцинация
Вакцинация от дифтерии проводится анатоксином, то есть инактивированным токсином. В ответ на его введение в организме образуются антитела не к Corynebacterium diphteriae, а к дифтерийному токсину.
Согласно российскому прививочному календарю, вакцинация детей в возрасте до года проводится в 3, 4–5 и 6 месяцев. Первая ревакцинация проводится в 18 месяцев, вторая – в 7 лет, третья – в 14. Взрослые должны ревакцинироваться от столбняка и дифтерии каждые 10 лет.
Это группа наследственных тубулопатий, клиническая картина которых в ранние сроки заболевания имитирует рахит, но не связана с дефицитом поступающего в организм витамина D. Встречаются у 1 из 20 000 родившихся.
Витамин-0-зависимый рахит (псевдовитамин-D-дефицитный рахит, псевдорахит)
Этиология. К этой группе относятся два заболевания с аутосомно-рецессивным наследованием. Тип I – генетический дефект синтеза в почках 1,25-дигидроксивитамина D – l,25(OH) 2D 3 Тип II – генетическая резистентность рецепторов органов-мишеней к l,25(OH) 2D 3.
Постоянные лабораторные признаки – выраженная гипокальциемия, гипофосфатемия, высокие уровни паратгормонав крови. У большинства больных имеются повышенная активность щелочной фосфатазы в крови, аминоацидурия, глюкозурия, почечный канальцевый ацидоз.
Несмотря на терапию обычными дозами витамина D, заболевание клинически и рентгенологически прогрессирует. В постоянных зубах обнаруживают гипоплазию зубной эмали. Уровни в плазме крови 2 5(OH)D 3 нормальные, но l,25(OH) 2D 3– снижен.
II тип заболевания клинически ничем не отличается от I типа, но у многих больных имеется тотальная алопеция и резко замедлен рост тела.
Уровень 1,25(OH) 2D 3 в крови нормален и при лечении большими дозами витамина D 2 (1–3 мг в сутки), несмотря на повышение уровня 1,25(OH) 2D 3 в крови до величины, в 2–3 раза превышающей нормальную, гипокальциемия и гипофосфатемия сохраняются. Рентгенологически наиболее типичен остеопороз костей.
Диагноз. Основными критериями служат клинические проявления, семейный характер заболевания с аутосомно-рецессивным типом наследования, отмеченные особенности метаболических сдвигов и отсутствие эффекта от проводимого антирахитического лечения витаминов D. Наибольшие дифференциально-диагностические затруднения возникают при разграничении витамин-Б-зависимого и витамин-Б-дефицитного рахита. В пользу первого свидетельствуют прогрессирующий характер костных деформаций и отсутствие признаков нормализации клинико-биохимических показателей при контрольном лечении витамином D в дозе 4000 ЕД в сутки в течение 6–8 недель.
Лечение. Заместительная терапия оксидевитом – аналогом биологически активного метаболита витамина D 1,25-диоксихолекальциферола. Суточные дозы 0,5–4 мкг в зависимости от индивидуальной переносимости препарата и тяжести течения заболевания. Используют также витамин D в дозах от 10 000-15 000 ЕД до 40 000-60 000 ЕД в сутки. Обязательны препараты кальция и фосфора, витамина А, С, Е, цитратные смеси курсами по 3–5 мес. Положительная динамика показателей фосфорно-кальциевого гомеостаза наблюдается через 4–6 недель после начала комплексной терапии. При отмене препаратов витамина D через 3–6 мес. может развиться рецидив заболевания, поэтому лечение проводят непрерывно в течение нескольких лет.
Витамин-D – резистентный рахит (семейный гипофосфатемический рахит, фосфат-диабет)
Этиология. Характеризуется доминантным типом наследования, сцепленным с полом, возможен также аутосомно-доминантный тип. У родителей больных детей возможны небольшой рост, умеренно выраженные деформации костей, иногда – лишь гипофосфатемия натощак. Развитие болезни связывают с первичным нарушением процессов всасывания кальция и фосфора в кишечнике; с первичным дефектом транспорта неорганических фосфатов в почках и повышением чувствительности эпителия канальцев почек к действию паратгормона; с генетически детерминированным сочетанием этих нарушений; с синтезом в организме фосфатурических метаболитов витамина D и недостаточным образованием 25-оксихолекальциферола в печени.
Витамин-Б-резистентный рахит отличается выраженным клиническим полиморфизмом. Первый вариант характеризуется ранней (на 1-м году) манифестацией, незначительной степенью костных деформаций, гипофосфатемией, гиперфосфатурией, повышением уровня паратгормона в крови, хорошей переносимостью витамина D. Второй вариант характеризуется более поздней (на 2-м году) манифестацией, выраженными костными изменениями, гипофосфатемией, значительной гиперфосфатурией, резистентностью к высоким дозам витамина D. Третьему варианту присущи поздние сроки проявления заболевания (в 5–6 лет), тяжесть поражений скелета, выраженная гипофосфатемия, значительное снижение абсорбции фосфора в кишечнике при нормальной или незначительной гиперфосфатурии; отмечается нечувствительность к витамину D. Четвертый вариант характеризуется манифестацией на 2-м году жизни, умеренной степенью костных деформаций, повышенной чувствительностью к витамину D и склонностью к развитию клинико-биохимической картины гипервитаминоза D (рвота, тошнота, жажда, гиперкальциемия, гиперкальциурия и др.) в ответ на небольшие дозы витамина D.
Диагноз. Основными критериями диагностики служат: клинические проявления; наследственный анамнез; биохимические отклонения в обмене электролитов. Гипофосфатемия и гиперфосфатурия при нормальном содержании кальция в крови – дифференциально-диагностический признак. Никогда не выявляют глюкозурию, калиурию, аминоацидурию. Рентгенологически – рахитоподобные изменения костей, преимущественно нижних конечностей.
Лечение витамин-Б-резистентного рахита должно быть комплексным. Основные препараты – витамин D и его метаболиты. Начальные дозы витамина D – 10 000-15 000 ЕД в сутки. Их увеличивают под контролем показателей кальция и фосфора в сыворотке крови и моче, активности щелочной фосфатазы крови, уровень которых определяют каждые 10–14 дней. Максимальные суточные дозы витамина D при первом варианте 85 000–100 000 ЕД, при втором 150 000–200 000 ЕД, при третьем 200 000–300 000 ЕД. При четвертом варианте болезни назначение витамина D противопоказано. Из метаболитов витамина D используют оксидевит в суточной дозе 0,25-3 мкг, при применении которого необходим строгий контроль (1 раз в 7-10 дней) за уровнем кальция в крови. В амбулаторных условиях проводят реакцию Сулковича. Противопоказания для консервативной терапии – индивидуальная непереносимость препаратов, выраженная гиперкальциурия (более 4 ммоль/ сут), отсутствие активного процесса в костной ткани по данным лабораторных и рентгенологических исследований. В комплекс лечения включают препараты кальция (глюконат кальция или хлорид кальция по 1,5–2 г в сутки) и фосфора (фитин 1–1,5 г в сутки, глицерофосфат кальция 0,5–1 г в сутки). Для улучшения всасывания кальция и фосфора в кишечнике – длительное (5–6 мес.) применение концентрированных цитратных смесей (лимонная кислота 24 г, цитрат натрия 48 г и дистиллированная вода 500 мл) по 20–50 мл в сутки. В активной фазе болезни при наличии болей в костях и суставах показан постельный режим продолжительностью до 2 недель. В период клинико-лабораторной ремиссии ограничивают физические нагрузки, ЛФК и лечебный массаж по специальной программе, назначают соляно-хвойные ванны, показано санаторно-курортное лечение.
Болезнь де Тони-Дебре-Фанкони (глюкоаминофосфат-диабет)
Этиология. Наследуется по аутосомно-рецессивному типу, встречаются спорадические случаи, обусловленные свежей мутацией.
В основе болезни лежит врожденное нарушение функции проксимальных отделов канальцев: неспособность к реабсорбции глюкозы, фосфатов и аминокислот (комбинированная тубулопатия). Развивающийся метаболический ацидоз и недостаток фосфорных соединений способствуют нарушению формирования костной ткани по типу остеомаляции и рахитоподобных изменений скелета.
Клиника. Развернутый симптомокомплекс формируется ко второму году жизни; реже наблюдается поздняя манифестация болезни – в 6–7 лет. Начальные клинические проявления – повышенная жажда, полиурия, иногда длительный субфебрилитет, рвота. На втором году жизни выявляют выраженный дефицит массы тела и роста ребенка, задержку становления статико-моторных функций, рахитоподобные деформации нижних конечностей (вальгусные или варусные), грудной клетки, предплечий и плечевых костей.
Диагноз. Основными критериями диагностики служат: клинические проявления; наследственный анамнез. Характерны биохимические нарушения – снижение уровня кальция и фосфора в крови, повышение активности щелочной фосфатазы, метаболический ацидоз. Экскреция кальция с мочой остается нормальной при повышенном клиренсе фосфатов мочи. Отмечают глюкозурию (20–30 г/л и выше), генерализованную гипераминоацидурию, повышение pH мочи > 6,0. При полиурии до 2 л и более в сутки удельная плотность мочи, как правило, высокая (1025–1035), что обычно связано с глюкозурией.
Рентгенологически определяют системный остеопороз различной степени выраженности, истончение коркового слоя трубчатых костей, разрыхление зон роста, отставание темпов роста костной ткани от биологического возраста ребенка.
Лечение заключается в коррекции электролитных нарушений, сдвигов в кислотно-щелочном равновесии, устранении дефицита калия и бикарбонатов. Повторные курсы витамина D и его метаболитов для ликвидации нарушений фосфорно-кальциевого гомеостаза (начальная суточная доза витамина D 25 000-30 ООО ЕД, максимальная – 75 000–150 ООО ЕД, доза оксидевита 0,5–1,5 мкг в сутки). В комплекс лечения включают препараты кальция, фосфора, витамины А, С, Е, группы В в возрастных дозах. Показано ограничение поваренной соли и включение в рацион продуктов, оказывающих ощелачивающее действие, а также богатых калием. В фазе ремиссии назначают массаж, соляно-хвойные ванны.
Почечный тубулярный ацидоз (синдром Лайтвуда-Олбрайта)
Диагноз. Основные критерии диагностики – клинические проявления; выраженный метаболический ацидоз, высокий pH мочи, гиперкальциурия, нефрокальциноз, гипофосфатемия, гипокальциемия, повышение активности щелочной фосфатазы, значительное снижение концентрационной функции почек (относительная плотность мочи 1001–1008). При рентгенологическом и ультразвуковом исследовании мочевой системы примерно у половины больных выявляют множественные конкременты (нефролитиаз и нефрокальциноз).
Лечение направлено на коррекцию метаболического ацидоза, гипокалиемии с помощью бикарбоната натрия, препаратов калия, цитратных смесей, димефосфона. При явлениях остеопороза и остеомаляции показано назначение препаратов витамина D или его метаболитов (начальные суточные дозы витамина D 10 000-20 000 ЕД, максимальные – 30 000-60 000 ЕД; суточные дозы оксидевита 0,5–2 мкг), препаратов кальция до нормализации его уровня в крови. При оксалатно-кальциевом нефролитиазе окись магния по 0,2–0,25 г в сутки курсами по 3–4 недели в течение длительного времени, 15 % раствор димефосфона в суточной дозе 1 мл на 5 кг массы тела, а также исключение из рациона продуктов, богатых оксалатами (щавель, шпинат, томатный сок, шоколад и др.). Лекарственную терапию проводят на фоне общеукрепляющего лечения с включением щелочных минеральных вод, фруктовых соков, ограничением белков животного происхождения, использованием комплекса витаминов (А, Е, группы В).
Данный текст является ознакомительным фрагментом.
Читайте также:
 Пожалуйста, не занимайтесь самолечением!При симпотмах заболевания - обратитесь к врачу.
Пожалуйста, не занимайтесь самолечением!При симпотмах заболевания - обратитесь к врачу.