Псб 2 при вич
Официально зарегистрировано 4 разновидности вируса иммунодефицита человека, которые отличаются друг от друга наличием разных структурных гликопротеидов оболочки ВИЧ. Наиболее распространенными из них признаны первый и второй типы.
Методы диагностики ВИЧ предусматривают идентификацию этих двух групп вирусов. Что означает, если анализы указывают на различные серотипы ВИЧ 1 и ВИЧ 2?
Информация о ВИЧ-1
В 1983 году из семейства ретровирусов учеными был выделен вирус иммунодефицита человека. Вирус в человеческом организме вызывает угнетение иммунной системы, что клинически проявляется как синдром приобретенного иммунодефицита. Видовой штамм 1 – наиболее распространенная форма вирусных частиц, вызывающих иммунодефицит.
Строение вируса довольно простое: сферическая форма с диаметром около 120 нм, что приблизительно в 60 раз меньше размеров красных кровяных клеток – эритроцитов. Вирионы структурно состоят из нескольких тысяч белковых молекул.
Существует несколько путей передачи вируса от инфицированного человека здоровому: половой, трансплацентарный, через кровь, через грудное молоко. Однако получение вирусных частиц от инфицированного партнера возможно только при наличии входных ворот для инфекции. Это может быть открытая рана на коже, порезы или царапины, дефекты слизистых оболочек, среди которых выделяется эрозия шейки матки.
При попадании в организм человека вирус проникает внутрь иммунных клеток и размножается там, что приводит к гибели защитных структур. Усугубляется состояние тем, что скорость нарастания количества вирусных элементов гораздо выше, чем скорость продукции иммунных клеток системой кроветворения.
Частицы 1-го штамма способны поражать:
- Т-лимфоциты;
- макрофаги;
- клетки нервной системы;
- клеточные элементы сердца и печени.
Клинически это проявляется четырьмя стадиями развития заболевания: инкубационный период, стадии первичных и вторичных проявлений, терминальная фаза – СПИД. На начальных стадиях инфицирования болезнь проявляется как обычная простуда. Больные при этом жалуются на незначительное повышение температуры, апатию, мышечную слабость и так далее. Вирус на этом этапе может не обнаруживаться специфическими исследованиями крови. Однако уже на этот момент могут иметься незначительные изменения в общих анализах крови и мочи. По мере угнетения иммунитета появляются новые, более грозные, симптомы заболевания, что наводит на мысль о СПИДе.
Информация о ВИЧ-2
В 1986 году был обнаружен вирус, который вызывает болезнь, илентичную по клиническим признакам с ВИЧ-инфекцией. Это стало открытием для вирусологии, что повлекло за собой дополнительные исследования по изучению инфекционных агентов, вызывающих иммунодефицит.
2-й тип не встречается у жителей стран Европы и Америки. Выявляют 2-й тип только в сочетании с первым. Наибольшее распространение вирус иммунодефицита 2 типа имеет у населения стран Западной Африки:
2-я разновидность инфекции зарегистрирована у представителей 15 африканских странах. От общей доли инфицированных вирусом иммунодефицита на долю заражения ВИЧ-2 приходится около 70%.
Симптоматика инфекции второго типа не отличается от признаков ВИЧ-1. Следует отметить только, что часто представляется невозможным выявить ВИЧ-2 на первой стадии развития заболевания, что связано с замедленной фазой репликации (размножения) вируса.
Основной путь передачи 2 штамма – половой, преимущественно при гетеросексуальных контактах. Исследования, проводимые в странах Западной Африки, отмечают, что наиболее подвержены заболеваемости женщины с большим количеством половых партнеров. Наибольшее число зараженных выявлено среди проституток. При этом отмечается, что, чем больше возраст женщины, тем более вероятно заражение её вирусом иммунодефицита человека.
Чем отличаются 2 вида вирусов
Несмотря на одинаковое воздействие различных типов вируса на иммунную систему инфицированного человека, существуют и различия между ними. Итак, чем отличаются ВИЧ-1 и ВИЧ-2:
- 1-й и 2-й типы вируса имеют разный антигенный и белковый состав. 1-й вид имеет ген vpu, а в структуре 2-го его нет. Ген vpx, напротив, отсутствует у 1-го типа вируса, но имеется у 2-го.
- Вторым отличием ВИЧ-1 от ВИЧ-2 является разница в молекулярной массе белковых составляющих вириона. Например, гликопротеин оболочки вируса 1-го типа имеет массу 120 кД, а у 2-го типа она составляет 140 кД.
- 2-й тип после инфицирования размножается и проявляет себя в организме человека намного медленнее первого типа. Чтобы удвоилось количество вирусных частиц типа 2-го, необходимо в 6 раз больше времени, чем для типа 1. Также в организме человека медленнее начинают вырабатываться антитела к ВИЧ-2.
- ВИЧ-2 обладает меньшей вирулентной способностью, чем вирус 1-го типа. Поэтому число людей, инфицированных им, намного меньше, чем количество зараженных ВИЧ-1.
- Данные, полученные при исследовании типов ВИЧ, свидетельствуют о том, что в числе инфицированных 2-м типом нет ни наркоманов, ни гомосексуалистов. Это говорит о передаче инфекции преимущественно при гетеросексуальных контактах.
- Отсутствуют зарегистрированные случаи вертикальной передачи 2-й разновидности, т.е. от матери к ребенку, находящемуся в утробе. Также отсутствуют данные о передаче вируса второго типа через грудное молоко.
Очень редко при диагностике по крови идентифицируются сразу два типа вируса у одного пациента. Чаще это говорит о недостоверном результате, так как тест фиксирует перекрестные реакции. Однако при действительном инфицировании обоими вирусными типами болезнь протекает тяжелее, и последняя её стадия (СПИД) наступает намного быстрее даже при лечении антиретровирусными препаратами. При одновременном поражении организма двумя разновидностями вирусных частиц часто уже на первой стадии заболевания пациенту может потребоваться терапия в условиях отделения реанимации.
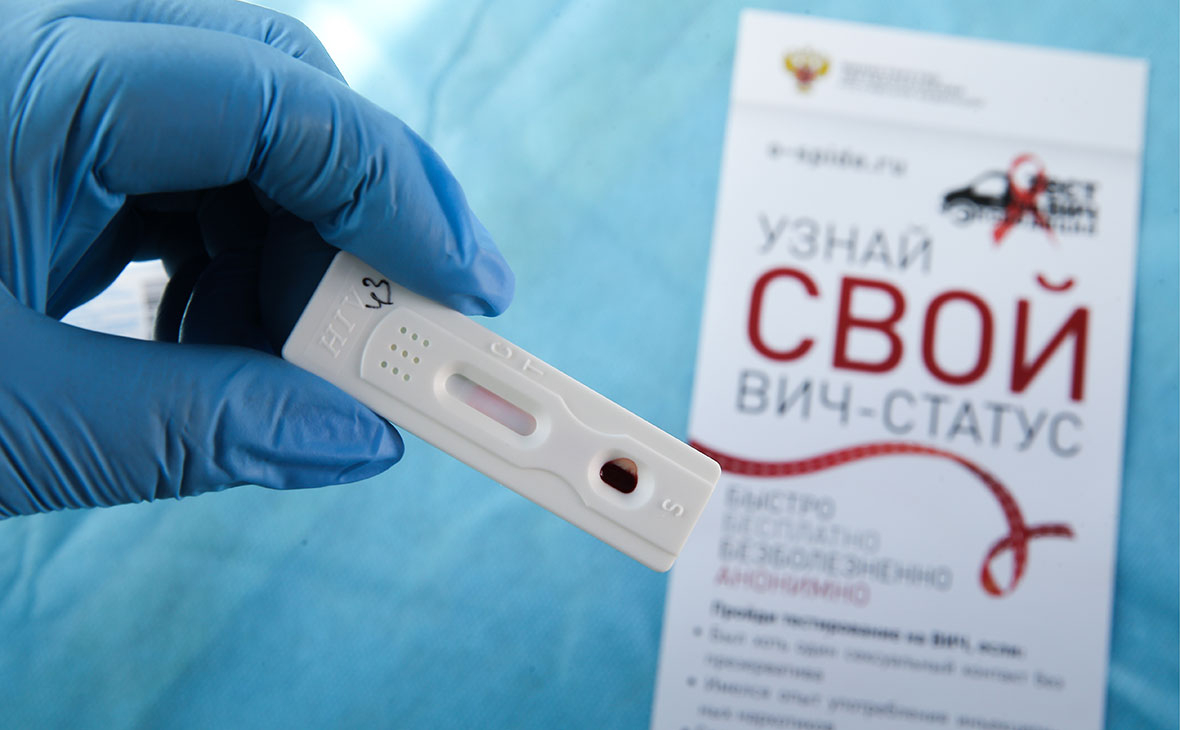
Число заболевших ВИЧ-инфекцией снизилось на 7% по сравнению с 2018 годом — такое значительное снижение наблюдается впервые с 2015 года.
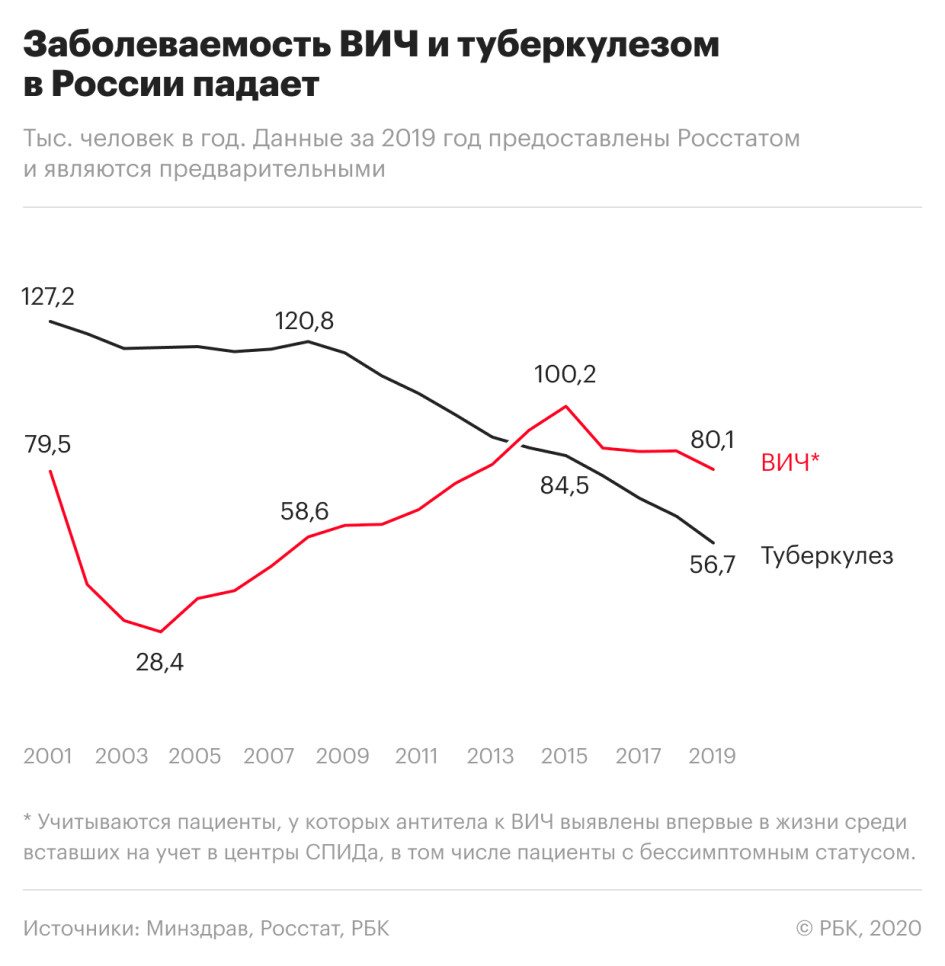
Смертность, связанная с ВИЧ, также уменьшилась — на 8% по сравнению с 2018 годом. В частности, от СПИДа, который развивается на фоне ВИЧ-инфекции, в прошлом году умерли 18,9 тыс. россиян.
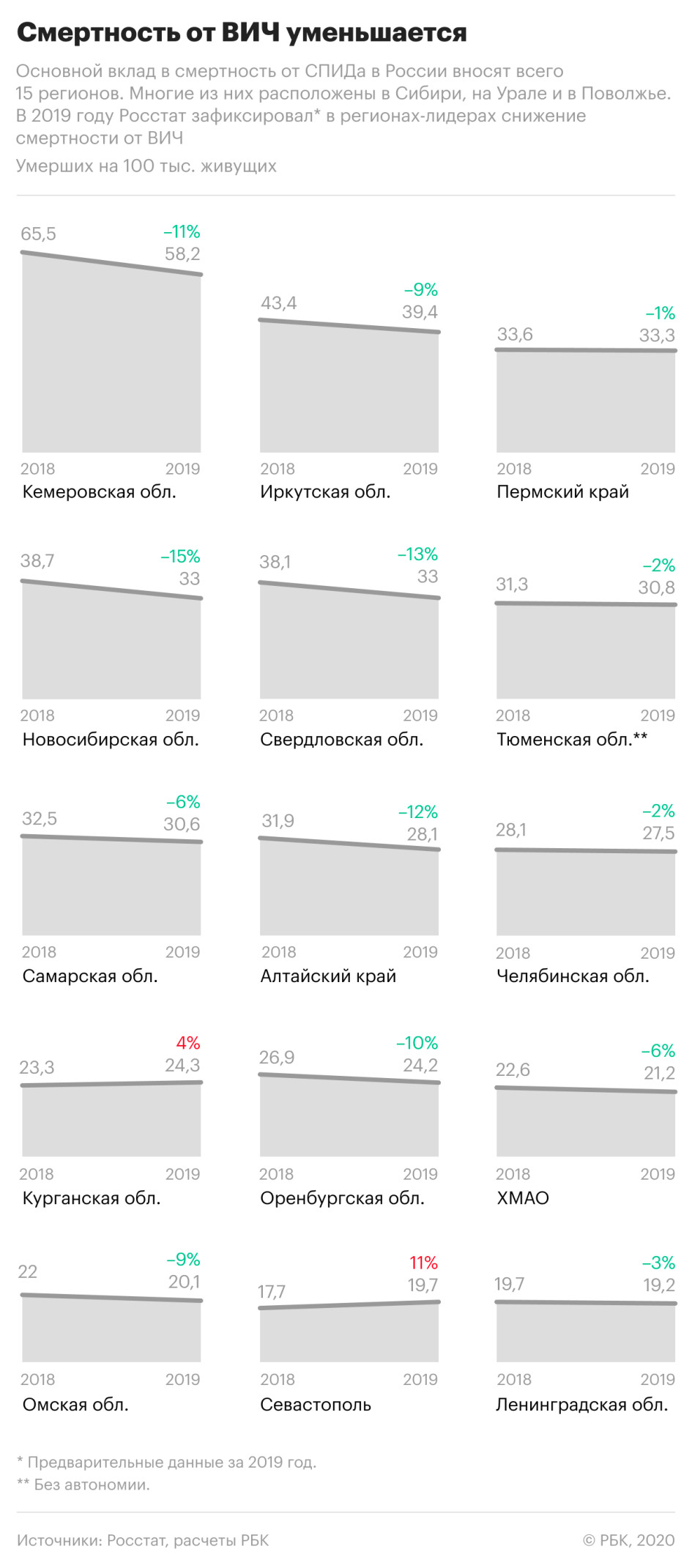
При этом смертность от вызванных ВИЧ-инфекцией заболеваний значительно снизилась в регионах, которые являлись лидерами по этому показателю в предыдущие годы. Так, в Кемеровской области смертность по причинам, связанным с ВИЧ-инфекцией, снизилась на 11%, в Иркутской области — на 9%, в Свердловской области — на 13%, в Новосибирской — почти на 15%.
Одновременно показатель существенно вырос в Севастополе — +11%, рост на 4% зафиксирован в Курганской области. РБК направил запросы властям этих регионов.
Кемеровская область, несмотря на снижение смертности, осталась в России лидером по смертям, вызванным ВИЧ-инфекцией. В 2019 году там умерли около 38 тыс. человек, из них 1552 — от вызванных ВИЧ заболеваний, это каждый 25-й из умерших. В Кузбассе, как и в некоторых других регионах Сибири, от иммунодефицита по-прежнему умирают чаще, чем в результате самоубийств, убийств, ДТП и отравлений алкоголем вместе взятых.
По данным министерства здравоохранения региона, в Кемеровской области живут более 31,5 тыс. носителей ВИЧ — это более 2% трудоспособного населения. Антиретровирусную терапию (АРВТ) получают 73% больных — в министерстве уточнили, что это все, у кого есть показания для назначения лечения. Министр здравоохранения области Михаил Малин рассказал РБК, что в 2019 году регион потратил 288,7 млн руб. на противодействие ВИЧ, в 2020 году эта сумма вырастет в 1,4 раза, причем большую часть ее составляют средства регионального бюджета.
В Новосибирской области охват АРВТ составляет 75%, рассказал РБК министр здравоохранения региона Константин Хальзов. Это позволяет увеличить продолжительность жизни зараженных, уточнил он. Всего в регионе живут 31,3 тыс. носителей ВИЧ — это 2% жителей Новосибирской области трудоспособного возраста. Терапию из них получают 61%. Для борьбы с распространением инфекции в регионе действует программа равного консультирования, которая, по мнению министра, помогает социализации людей, живущих с ВИЧ, и формирует у них желание лечиться. Равные консультанты — это люди, живущие с вирусом и обученные консультировать новых пациентов.
В Иркутской области живут 30,1 тыс. больных ВИЧ, сообщила РБК замминистра здравоохранения Иркутской области Елена Голенецкая. АРВТ получают 58% из них. По словам Голенецкой, это все пациенты, которые нуждаются в терапии. Улучшение ситуации с смертностью от ВИЧ в регионе связывают с ростом числа пациентов, проходящих диспансеризацию.
Наркотрафик и другие причины эпидемии
Регионы, в которых больше всего жителей заразилось ВИЧ-инфекцией и умерло от СПИДа, во многом пересекаются с регионами, в которых популярны наркотики опийной группы. Именно в этих регионах, как показывает статистика МВД, в 2019 году правоохранительные органы изъяли большую часть опиатов.
Осторожный оптимизм и фильм Дудя
В 2019 году каждый четвертый россиянин прошел тестирование на ВИЧ, сообщили РБК в пресс-службе Минздрава. Антиретровирусную терапию получают 68,9% заболевших. Эти показатели выше плановых, указанных в Государственной стратегии по противодействию распространения ВИЧ-инфекции.


Кроме того, по словам Вадима Покровского, в некоторых регионах еще остается практика, когда вместо диагноза СПИД ставят непосредственную причину смерти пациента для улучшения отчетности.
Агрессивный новичок
- Вадим Альбертович, ВИЧ был обнаружен еще в конце прошлого века. Почему лекарство так сложно было создать? Чем этот вирус отличался от других?
- С точки зрения биологии этот вирус очень похож на многие другие. Единственное, его фатальное отличие от других вирусов – это поражение иммунной системы человека, именно поэтому организм не может с ним бороться самостоятельно.
- Это своего рода агрессивный новичок?
Мыши на вес золота
- Вы уже дошли до клинических испытаний?
- До клинических - нет, но лабораторных мышей мы уже успешно лечим.
- Зачем в этом проекте мы и американцы нужны друг другу?
- Во-первых, потому что работа с вирусом ВИЧ требует астрономических денежных ресурсов. Ни одна сторона не хотела брать на себя всю тяжесть потенциальных финансовых потерь, поскольку велик риск, что мы будем много работать, но в итоге не сможем создать препарат принципиально нового поколения. Во-вторых, это крайне сложная работа, ее невозможно было сделать только в России, у нас нет ни адекватных моделей на животных, ни биологических технологий для проведения тестов. Например, для экспериментов на животных надо использовать безумно дорогих мышей, которые есть только в США. В то же время, российская химическая школа является ведущей мировой школой в области тонкого химического синтеза. Мы были лидерами 100 лет назад, и надеюсь, останемся ими в будущем. Именно поэтому наших ученых и привлекли для участия в совместном проекте.
- Почему нужны безумно дорогие мыши? Нельзя было найти подешевле?
- А это особые мыши - гуманизированные. У них с помощью современных технологий создали иммунную систему, которая идентична человеческой, можно сказать, что это просто человеческая иммунная система. Такие мыши - очень удобный лабораторный объект, можно испытать препарат и понять, как он будет воздействовать на человека.
- Как с американцами делили зоны ответственности?
- Как я уже сказал, российская сторона отвечает за химическую составляющую, дизайн и синтез соединений. Американские коллеги занимаются биологической частью и компьютерным моделированием. Выглядело это так: сначала мы с американскими партнерами обсуждали идеи, затем их специалисты на суперкомпьютерах проверяли насколько наши предположения реалистичны. Так формировался некий список перспективных соединений. Синтез этих соединений осуществляется здесь в Москве , в ФИЦ Биотехнологии РАН. И в конечном итоге готовые соединение тестируются в США.
От лаборатории до аптеки дистанция 10 лет
- Когда готовое лекарство может появиться в аптеках?
- От лаборатории до аптеки очень длинная дистанция. При благоприятном раскладе понадобится минимум 10 лет. Быстрее невозможно. Это связано с определенной последовательностью экспериментов и необходимым количеством данных, которые надо накопить. А отчасти с тем, что человечество само себе создало огромное количество преград на пути появления новых лекарств. Пройти согласование во всех регулирующих инстанциях очень тяжело и очень дорого. И это не только у нас, это практика всех стран мира. Кроме того, через год наш совместный проект заканчивается и надо будет искать финансирование под практические работы. Многие фармкомпании и фонды не стремятся вступать в такие долгие и дорогостоящие проекты, именно поэтому и сегодня наши исследования финансируются государственными фондами как со стороны России, так и со стороны США. Разработка лекарства для борьбы с ВИЧ это скорее задача государства.
- Я с большой осторожностью отношусь к заявлениям, что кто-то от чего-то вылечился на единичном примере. Мы не знаем достоверно, вылечился он или нет, это не клинические испытания, которые делаются в соответствии с очень строгим протоколом и которым можно доверять. Вирус может затаиться в нейронах и проснуться, когда пройдет много времени. Мы в своей работе придерживаемся позиций доказательной медицины, когда есть слепые клинические испытания на большой выборке. Что касается стволовых клеток, то это вопрос неоднозначный. Безусловно, есть примеры, когда стволовые клетки работают успешно, но это не касается вируса ВИЧ. Поэтому мы исходим из традиционных подходов: с одной стороны, есть вирус, с другой стороны - надо найти вещество, которым этот вирус можно уничтожить.
- А откуда все-таки появился ВИЧ? Существуют самые разные теории, по одной из версий вирус - это побочный эффект разработок биологического оружия…
- Происхождение вируса не является областью моей компетенции, моя ответственность - это разработка вещества, способного убить вирус. На самом деле есть только одна серьезная научная версия происхождения ВИЧ. Вирус появился в процессе мутации в Африке . Сначала он возник у человекообразных приматов, потом был перенесен на человека. Все остальные версии: космические, Божественные, конспирологические, не имеют отношения к здравому смыслу и научным сообществом не рассматриваются. И это не последний случай появления неизвестных ранее смертельных инфекций. Мы считаем, что новые вирусы будут появляться по мере развития человека, а мы будем придумывать вещества для их уничтожения. Это бесконечный непрерывный процесс.
ЧИТАЙТЕ ТАКЖЕ
В Лондоне выздоровел пациент с ВИЧ: случайный успех или победа человечества над СПИДом?
Пациенту, у которого болезнь перешла в смертельно тяжелую стадию, пересадили костный мозг, и ВИЧ пропал из организма (подробности)
ВИЧ-инфекции свойственно прогрессирующее течение с развитием иммунодефицита и гибелью больных вследствие возникновения и развития оппортунистических инфекций, злокачественных опухолей и аутоиммунных процессов.
Проникший в организм человека ВИЧ захватывается макрофагами и заносится ими в различные системы, в том числе, минуя гематоэнцефалический барьер, в головной мозг, и внедряется в клетки, несущие С04-антиген (Т4-лимфоциты, некоторые В-лимфоциты, моноциты крови, альвеолярные, колоректальные и другие тканевые макрофаги, клетки вилочковой железы, костного мозга и др.). Клеточными корецепторами, участвующими наряду с С04-молекулами в проникновении (фузии) ВИЧ через мембраны клеток, являются хемокиновые рецепторы (фузины) — CXCR4 и CCCKR5.
Диссеминация вируса нередко сопровождается развитием интоксикационного синдрома, гиперплазией лимфатических узлов, увеличением печени и селезенки, определяющими клинические проявления острой фазы инфекции.
При воздействии разнообразных кофакторов, в частности суперинфекции (или коинфекции) герпетическими вирусами, сенсибилизирующего эффекта аллогенной спермой многочисленных половых партнеров, воздействии токсичных веществ (наркотиков, медикаментов и др.), терапевтически или экологически обусловленной иммуносупрессии, происходит интенсивная репликация вирусных частиц, сопровождающаяся гибелью иммуноцитов, развитием иммунодефицита с преимущественным истощением популяции Т-лимфоцитов.
Механизмы гибели зараженной вирусами клетки продолжают уточнять. Одним из них является повреждение клеточной оболочки вследствие массового выхода новых вирионов, связывающих с др 120 фрагментом клеточной мембраны с расположенными на них CD4-антигенами. Большая роль в уменьшении популяции Т4-лимфоцитов отводится иммунным реакциям сенсибилизированных киллерных клеток. Число Т4-лимфоцитов может значительно уменьшаться в результате образования синцития из неинфицированных и инфицированных клеток вследствие взаимодействия С04-антигенов незараженных лимфоцитов с др 120, экспрессированными на поверхности зараженных клеток. Такие лимфоцитарные конгломераты могут включать десятки и сотни клеток с последующим их разрушением. Важное значение придается аутоиммунным эффектам вследствие сенсибилизации цитотоксических лимфоцитов к структурным компонентам собственных лимфоцитов. Этому способствует наличие общих аминокислотных последовательностей у др 120, С04-антигенов и HLA-антигенов.
Повреждение Т4-лимфоцитов, выполняющих ключевую роль в иммунных процессах, инверсия соотношения числа Т4:Т8 (в норме составляющего около 1,2-2) приводят к дезинтеграции кооперации иммунных клеток, утрате ими способности к адекватному ответу на аллогены и аутоантигены, что способствует возникновению разнообразных инфекций и злокачественных новообразований.
Наряду с поражением Т4-лимфоцитов у больных ВИЧ-инфекцией отмечается поликлональная активация В-лимфоцитов с увеличением синтеза иммуноглобулинов всех классов, особенно IgG и IgA и последующим истощением этого отдела иммунной системы. Характерно угнетение антигенраспознающей и антигенпрезентирующей функции макрофагов, увеличение продукции ими провоспалительных цитокинов (фактора некроза опухоли, интерлейкина-1 и др.), определяющих ряд проявлений болезни -лихорадочную реакцию, истощение и др. Фактор некроза опухоли (ФНО) и другие провоспалительные цитокины способны активировать регуляторные гены ВИЧ, а следовательно его репликацию. Не только ВИЧ, но и другие патогены способны усиливать образование ФНО и, тем самым, стимулировать репликацию вируса.
Для поздних стадий прогрессирующей ВИЧ-инфекции характерна анергия кожи и слизистых оболочек, подавление воспалительной реакции. Наблюдается нарушение способности к первичному гуморальному специфическому ответу при сохранении вторичного гуморального ответа.
Нарушение регуляции иммунных процессов проявляется также повышением уровня кислотолабильного интерферона, тимозина, микрогпобупина, снижением уровня интерлейкина-2.
В результате нарушения функции иммунной системы, особенно при снижении числа Т4-лимфоцитов до 400 и менее клеток в 1 мкл крови, возникают условия для неконтролируемой репликации ВИЧ со значительным увеличением количества вирионов в различных средах организма; для развития болезней, вызываемых вирусами (герпесвирусы, паповавирусы и др.), бактериями (атипичные мико-бактерии, легионеллы и др.), грибами (кандида, криптококки, гистоплазмы и др.), простейшими (криптоспоридии, изоспоры и др.) и гельминтами (стронгилониды и др.); для возникновения злокачественных опухолей (саркома Капоши, лимфомы и др.), аутоиммунных процессов (васкулиты, нефропатия и др.). Развивается развернутая картина СПИДа с последующей гибелью больного.
Установлена генетически обусловленная предрасположенность к быстрому развитию СПИДа у лиц с HLA-фенотипом, включающим такие антигены, как: В35, Cw4, DR-1, DR-2, DR-5.
Наряду с иммунными нарушениями и часто вне связи с ними возникает поражение нервной системы в виде подострого энцефалита (ВИЧ-энцефалопатии) или прогрессирующей вакуолярной миелопатии.
Патологоанатомические изменения у больных ВИЧ-инфекцией весьма многообразны. Продолжительное время наблюдается увеличение лимфатических узлов с фолликулярной гиперплазией или инволюцией железистой ткани. Выявляется аплазия костного мозга, демиелинизация и спонгиозная дегенерация нервной ткани, васкулиты, нефропатии, гепатит и другие повреждения, обусловленные действием ВИЧ. Наряду с этим выявляются морфологические изменения, характерные для соответствующих вторичных инфекций и опухолей.
Прослеживается определенная географическая зависимость распространения отдельных субтипов ВИЧ.
ВИЧ отличает исключительно высокая генетическая изменчивость, она в 30-100, а по некоторым данным и в миллион раз выше, чем у вируса гриппа. Касается она не только штаммов вируса, выделенных от разных больных, но и в разное время года от одного и того же больного. Высокая генетическая изменчивость во многом связана с. продуктом гена env вируса — gp120, вариабельность аминокислотной последовательности которого составляет 5-20% для изолятов одного субтипа и 25-35% для разных субтнпов. Особенно вариабелен участок gp120, образующий петлеобразный домен, получивший название V3-петли, состоящий из 35 аминокислот и к которому вырабатывается 80-95% всех нейтрализующих антител.
Исключительная генетическая изменчивость позволяет вирусу выжить в инфицированном организме, ибо всегда в огромном пуле найдется вирус, способный к эволюционному отбору.
Наряду с генетическими особенностями ВИЧ-1 имеет фенотипические различия. Так, у ВИЧ-инфицированных по репликатнвной активности выделяют: a) rapid/high — высокоинфекционные, эффективно реплицирующие изоляты и б) slow /low — низкоинфекцнонные, слабо реплицирующие изоляты. По характеру цитопатического действия изоляты классифицируют на: а) низко реплицирующиеся, не способные к образованию синцития; б) высоко реплицирующиеся, не образующие синцитий (НСО) и в) высоко реплицирующиеся, образующие синцитий (СО). По тропизму классифицируют лимфоцитотропные изоляты (разгар болезни) и моноцитотронные (начальные этапы болезни).
Прогрессирование ВИЧ-инфекции связано с тропизмом вируса к Т-хелперам, способности индуцировать синцитий и/или с высокой репликативной активностью. Мутации в гене env определяют переход изолятов НСО в СО. Переход в СО появляется при снижении CD4+-клеток до 400-500 в 1 мкл. При появлении СО-вариантов изолятов HIV дальнейшее падение уровня CD4+-клеток идет прогрессивнее. В стадии СПИД СО-варианты изолятов выявляются не у всех больных, следовательно и НСО могут обусловить формирование терминальной стадии и смерть больного. Мутации в гене pol обеспечивают у HIV формирование резистентности к ингибиторам обратной транскриптазы. Быстрое уменьшение CD4+ лимфоцитов связано с более высоким уровнем репликативной активности HIV, как образующих, так и не образующих синцитий.
Инфекционный процесс при заражении ВИЧ носит последовательный, фазовый характер: проникновение вируса через слизистую оболочку половых путей или непосредственное поступление в кровоток, связывание вириона с поверхностью клетки, слияние мембраны клетки и вириона, обеспечивающее проникновение вируса внутрь, высвобождение нуклеотида и геномной РНК вируса, интеграция генома вируса в геном инфицированной клетки, латентная фаза, фаза активации транскрипции с ДНК провируса и последующая трансляция белков вируса, наработка всех компонентов вируса и формирование новых (дочерних) вирионов, их высвобождение из клетки, сопровождающееся цитопатическим эффектом для клетки-мишени. Весь каскад этих превращений начинается со связывания вириона с поверхностью клетки-мишени. Это обеспечивается как специфическими, т. е. через специфический для вириона рецептор (молекула CD4), так и неспецифическими, т. е. не зависящими от наличия CD4 компонентами. Высокая плотность CD4 на поверхности Т-хелперов определяет их преимущественное поражение при ВИЧ-инфекции. Плотность рецепторов — величина не постоянная, она зависит от функционального состояния клетки и при активации ее возрастает. Поэтому неактивированные CD4+ лимфоциты более устойчивы к вирусу. Иными словами, одни субпопуляции CD4+ лимфоцитов лучше обеспечивают рецепцию ВИЧ по сравнению с другими.
Процесс инфицирования клетки вирусом осуществляется в две фазы: прикрепления и слияния. Прикрепленный через gp120 к рецептору CD4 клетки-мишени вирус белком gp41 оболочки сливается с мембраной клетки. Дальнейшее проникновение вируса в клетку осуществляется, очевидно, и путем эндоцитоза, и через плазматическую мембрану. В процессе инфицирования клетки белок ВИЧ gp41 не только обеспечивает слияние вирусной мембраны с мембраной клетки, но также определяет слияние мембран соседних инфицированных клеток с образованием одной многоядерной синцитиальной клетки (синцитий), обреченной на гибель, продолжительность жизни синцитиальных клеток не превышает 3-7 дней. Вирулентность ВИЧ коррелирует с возможностью образовывать синцитий.
В цитоплазме клетки-мишени информация с вирусной РНК переписывается на ДНК с помощью обратной транскриптазы с образованием в конечном итоге промежуточной двухнитевой линейчатой ДНК, которая транспортируется в ядро клетки, там приобретает кольцевую форму и интегрирует с ядром клетки, превращаясь в ДНК-провирус. Интеграция осуществляется под влиянием фермента интегразы, взаимодействующей с концевыми последовательностями LTR. Характерная и отличительная особенность ВИЧ от других ретровирусов — сохранение части ДНК в неинтегрированном состоянии, эта ДНК самостоятельно функционирует как репликон. Таким образом, в организме зараженного ВИЧ находится в двух вариантах. Заражение происходит зрелым вирусом, геном которого представлен РНК. В клетках инфицированного человека на геномной РНК, как на матрице, синтезируется провирус с помощью особого вирусного фермента — обратной транскриптазы. ДНК, содержащая провирус, выполняет в свою очередь функцию матрицы для синтеза информационной РНК. С последней транслируются вирусные белки и транскрибируется полноразмерная геномная РНК для новых вирионов.
Заканчивается морфогенез цитопатическим действием ВИЧ, которое может быть выражено: а) прямой деструкцией и цитолизом инфицированной клетки, б) синцитиеобразованием, т. е. слиянием мембран инфицированных и неинфицированных клеток, имеющих CD4, в силу чего клетки теряют свои физиологические функции, в) хронической инфекцией без выраженного цитолиза (дендритные лимфоциты, моноциты/ макрофаги, нейроны), г) патогенным эффектом отдельных белков ВИЧ (около половины гликопротеина gp120, синтезируемого в клетке, идет не на построение новых вири-онов, а, проникая во внеклеточную среду, связываются с CD4, преимущественно неинфицированных ВИЧ клеток, обусловливая этим инактивацию иммунокомпетентных клеток, в частности Т4 (СD4*)-лимфоцитов.
В настоящее время идет интенсивное изучение структуры ВИЧ, патогенеза и морфогенеза, терапии и разработка вакцин. Отрабатываются возможности этих исследований на экспериментальных животных.
Особенности ВИЧ-2. ВИЧ-2 был впервые выделен в 1985 г. от больных СПИДом в Гвинее-Биссау и Островах Зеленого Мыса. Исследования показали, что обусловленные ВИЧ-2 и ВИЧ-1 заболевания являются самостоятельными инфекциями, так как имеются различия в особенностях возбудителей, клинике и эпидемиологии.
ВИЧ-2 преимущественно распространен в странах Западной Африки, антитела к нему обнаружены у жителей 15 африканских стран (Ангола, Буркина-Фасо, Гана, Гамбия, Гвинея, Гвинеи-Биссау, Зимбабве, Камерун, Кот Д’Ивуар, Мали, Мозамбик, Сенегал, Сьерра-Леоне, Того и Центральиоафри-канская Республика). Инфекция за пределами Западной Африки регистрируется довольно редко.
Причем в Гвинея-Биссау ВИЧ-2 является практически единственным циркулирующим среди населения вирусом иммунодефицита, в Сенегале, Гамбии, Мали и Мозамбике среди инфицированных ВИЧ на долю ВИЧ-2 приходится от 37 до 68% и почти у половины выявляется двойная инфекция.
Изучение структуры ВИЧ-2 показало, что при определенном сходстве с ВИЧ-1 он отличается от последнего по антигенной структуре и по последовательности оснований в нуклеиновых кислотах. Белок ВИЧ-2 более близок по своим свойствам, антигенной структуре и составу генетического материала к вирусу иммунодефицита обезьян, чем к ВИЧ-1. Наиболее существенным различием между вирусами является наличие у ВИЧ-1 гена vpu, не обнаруживаемого у ВИЧ-2, зато ВИЧ-2 содержит ген vpx, которого нет у ВИЧ-1. Имеются различия в молекулярной массе белков ВИЧ-1 и ВИЧ-2. В частности, наружный оболочечный гликопротеии имеет молекулярную массу 120 кД, у ВИЧ-2 этот белок имеет молекулярную массу 140 кД. Трансмембранный белок у ВИЧ-2 — 36 кД, а у ВИЧ-1 — 41кД. Белки, кодируемые геном gag, у ВИЧ-1 имеют молекулярную массу 24 и 17 кД, а у ВИЧ-2 — 26 и 15 кД. Сыворотки крови большинства людей, инфицированных ВИЧ-2, не реагируют с оболочечными антигенами ВИЧ-1, но дают перекрестные реакции с антигенами, кодируемыми геном gag. Оба вируса инфицируют те же популяции клеток, связываются с теми же CD4-рецепторами.
Большинство эпидемиологов предполагает, что распространение ВИЧ-2 еще только начинается. ВИЧ-2 передается теми же путями, что и ВИЧ-1. Вирус выделен как от лиц с клинически выраженным СПИДом, так и от бессимптомных носи гелей. Считается, что ВИЧ-2 передается преимущественно путем гетеросексуальных половых связей. При обследовании различных групп населения было выявлено, что число сероположительных результатов к ВИЧ-2 было в 10-15 раз больше среди проституток, чем среди других групп населения. В странах Западной Африки число сероположительных с антигенами ВИЧ-1 лиц было значительно ниже, чем с таковыми ВИЧ-2. В то же время ВИЧ-2 почти отсутствует в центральноафриканских странах.
Как показало наблюдение за проститутками в течение трех лет, ВИЧ-2-инфекция развивается значительно медленнее, чем при инфицировании ВИЧ-1 — через 3 года после выявления серопозитивности к ВИЧ-2 не было выраженных лимфаденопатией или СПИДа, что, очевидно, связано с меньшей вирулентностью ВИЧ-2.
Наблюдения показали, что ВИЧ-2 не передается столь легко, как ВИЧ-1. Но так как основным путем передачи является гетеросексуальный, в 40% семей были сероположн-тельны оба супруга. В то же время нет данных за вертикальную передачу ВИЧ-2, не наблюдалась также передача инфекции вследствие кормления грудью. Большинство серопозитивных детей инфицировано при переливании крови.
Изучение клинической картины показало, что ВИЧ-2-инфекция развивается медленнее, чем ВИЧ-1, хотя симптоматика СПИД, вызванного ВИЧ-2, в целом не отличается от симптоматики СПИДа, вызванного ВИЧ-1. У больных наблюдается резкое снижение количества циркулирующих С04-лимфоцитов. Но течение болезни более благоприятное, у инфицированных ВИЧ-2 даже через 3 года не было выраженных лимфаденопатией или СПИДа.
Существующие лизатные диагностические системы ИФА, предназначенные для диагностики ВИЧ-1, позволяют также распознать инфекцию ВИЧ-2 в 82-84% случаев, поскольку антигены, кодируемые генами gag и pol, обнаруживают значительную гомологию. Перекрестные реакции могут наблюдаться не только в ИФА, но и в иммуноблоте. Реже перекрестные реакции имеют место при использовании конкурентного ИФА.
Читайте также:


