Механизм действия ингибиторов протеазы вич
Прежде, чем приступить к изложению материала, хотелось бы сказать несколько слов о себе: участник сообществ по борьбе с отрицанием ВИЧ („ВИЧ/СПИД диссидентством“): в 2016-2018 годах „ВИЧ/СПИД диссиденты и их дети“, с 2018 года – „ВИЧ/СПИД отрицание и альтернативная медицина“.
Моё – и далеко не только моё – мнение состоит в том, что большинство случаев отказа от лечения ВИЧ-инфекции вызвано банальным непониманием того, что это контролируемая хроническая инфекция, а также стигматизацией людей, живущих с ВИЧ – применением к ним распространённого клише, что ВИЧ – болезнь низших слоёв общества либо же наоборот, „культурной элиты“. Это давно не так – в России примерно 1% населения живёт с ВИЧ, и ситуация не планирует становиться лучше.
Около года назад несколько статей на этом ресурсе сподвигли меня на написание пяти заметок об истории борьбы с вирусами. Целью этих статей было описание принципов работы различных типов лекарств от ВИЧ (консультантами выступали микробиолог и врач-инфекционист). Надеюсь, переложение этих заметок вам понравится.
Итак, несколько слов о вирусах вообще: они занимают промежуточное положение между живым и неживым миром; они неспособны к самостоятельному размножению, для этого требуются клетки организма-хозяина.
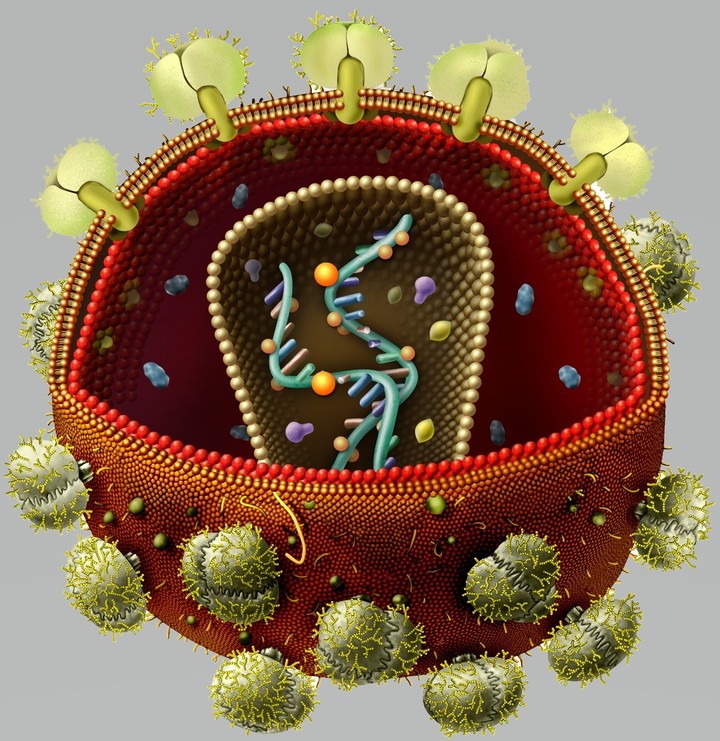
Вирус устроен достаточно просто: он несет в себе генетический код, код закрыт в капсид, капсид иногда окружен оболочкой. Код может быть представлен в самом различном виде. Носитель кода – это ДНК или РНК, т.е. нуклеиновая кислота (НК). Цепочек кода могут быть одна и две: двухцепочечная и одноцепочечная НК. Цепочка может быть замкнутой в кольцо или линейной. В 1971 года Дэвид Балтимор в соответствии с этими признаками разбил вирусы на 7 классов. Эта классификация используется по сей день и будет важна для объяснения принципов работы некоторых лекарств.
Сам по себе код для построения нового вируса не может проникнуть в саму клетку, ему нужен некий механизм проникновения. Поэтому существует белковая оболочка – капсид, которая и защищает НК вируса, и помогает проникнуть ей в клетку. В некоторых случаях у вирусов могут быть дополнительные липидные оболочки.
Чтобы проникнуть в клетку, вирус должен соединиться с её оболочкой. Для этого на поверхности вируса существуют белки, которые связываются с белками-рецепторами клетки организма-хозяина – местами на поверхности клеточной оболочки, к которым вирус способен прикрепляться. И они должны строго подходить вирусу, иначе он не сможет даже прицепиться к клетке.
Одно из средств, предназначенных для борьбы с вирусом – энфувиртид (фузеон) – является ингибитором белка gp41. Энфувиртид соединяется с этим белком, не допуская образования шпильки. Таким образом, капсид вируса не может слиться с клеткой и заражения не происходит. Этот препарат – единственный разработанный и одобренный ингибитор слияния (фузии).
Ретровирусы, к числу которых принадлежит ВИЧ, представляют крайне неудобную цель для лекарственных средств из-за своей изменчивости. Клетки человека гораздо менее изменчивы. Известно, что около 1% населения северной Европы обладают иммунитетом к ВИЧ: они являются носителями мутации CCR5-∂32, которая делает форму рецептора CCR5 неподходящей для соединения с ВИЧ.
К сожалению, изменить навсегда форму этого рецептора, в том числе для продолжающих появляться в организме человека новых клеток – задача крайне сложная (хотя попытки были), но вот разработать ингибитор рецептора – препарат, который бы присоединялся к рецептору клетки и тем самым мешал ВИЧ присоединяться к нему – вполне возможно.
В разработке находилось несколько ингибиторов рецепторов CCR5 и CXCR4, но единственный одобренный на сегодняшний день – это маравирок, ингибитор CCR5.
Что же происходит после слияния вируса с клеткой в случае с ВИЧ?
ВИЧ – вирус класса VI по Балтимору, он хранит свой геном в РНК. В ядре клетки находится ДНК, поэтому ВИЧ нужно превратить одну нуклеиновую кислоту в другую. Таким переписыванием (НК → НК) занимаются соответствующие ферменты, называемые полимеразами. Для РНК-зависимой (т. е. считывающей информацию с РНК) ДНК-полимеразы (т. е. на выходе которой появляется ДНК) существует специальное название – обратная транскриптаза. Обратная транскриптаза берёт нужный дезоксинуклеозид (для простоты изложения – на самом деле в деле участвуют дезоксинуклеозидтрифосфаты) и строит ДНК, комплементарную (соответствующую) вирусной РНК.
Возможно ли прервать этот процесс? Да, для этого нужно просто подсунуть обратной транскриптазе нечто, напоминающее дезоксинуклеозид, но не являющееся им. Именно так действовало самое первое лекарство против ВИЧ – зидовудин (азидотимидин, AZT). Он похож на дезокситимидин, но не является им.
Азидотимидин был разработан в рамках поиска веществ, которые могли бы бороться с опухолями. Предполагалось, что он будет встраиваться в постройку обычной ДНК человека, прерывая её. Таким образом, препарат бы наиболее сильно воздействовал на наиболее быстро делящиеся клетки – клетки опухолей. Были определённые основания думать так – синтезированный ранее другой препарат этой группы, 6-меркаптопурин, был эффективен в лечении лейкозов.
К сожалению, в процессе испытаний на животных препарат показал свою неэффективность и был забыт на какое-то время, пока в 1984 году вирусолог Марти Сент-Клер, работавшая в лабораториях фонда Burroughs Wellcome, не инициировала исследования по проверке всех имеющихся веществ на предмет возможности лечения ими нового заболевания – ВИЧ-инфекции.
Обратная транскриптаза „узнавала“ зидовудин, как дезокситимидин, и пыталась встроить его в ДНК. Синтез ДНК на этом месте прерывался, поскольку препарат был лишь похож на дезокситимидин. Зидовудин полностью подавлял репродукцию вируса, и испытания на людях были начаты практически незамедлительно.
ВИЧ-инфицированные добровольцы были разделены на две группы, одна из которых получала плацебо, а другая – AZT. Разница между двумя группами была настолько разительной, что дальнейшее проведение испытаний было признано негуманным – препарат показывал ошеломляющую эффективность.
Успех зидовудина послужил стимулом к исследованиям других нуклеозидных ингибиторов обратной транскриптазы (НИОТ), и в течение короткого времени появилось множество других лекарств. Наиболее интересным из первых препаратов является ламивудин, аналог другого дезоксинуклеозида, дезоксицитидина. Минусом ламивудина является то, что при монотерапии этим препаратом очень быстро, в течение около месяца, развивается резистентность. Это происходит благодаря одной-единственной точечной мутации ВИЧ, M184V. Несмотря на это, ламивудин желательно было оставлять в схеме. Дело в том, что вирус с этой мутацией оказывается гиперчувствителен к зидовудину, а сама по себе мутация снижает скорость репликации вируса.
В настоящее время ламивудин постепенно начинает уходить в прошлое, уступая место своему более современному аналогу – эмтрицитабину. И ламивудин, и аналог дезоксиаденозина – адефовир – показывают хорошие результаты при лечении гепатита B. К сожалению, адефовир показал свою неэффективность при лечении ВИЧ. Однако после небольшой модификации его молекулы на свет появилась его обновлённая версия – тенофовир. Тенофовир и эмтрицитабин входят в состав многих современных линий терапии.
Комбинация двух НИОТ могла значительно продлить жизнь людям, живущим с ВИЧ, однако было ясно, что для полноценного подавления вируса требуется включить как минимум один препарат иного типа действия, потому что рано или поздно вирус вырабатывал устойчивость к любому сочетанию НИОТ. Одними из первых веществ иного типа действия стал другой тип ингибиторов обратной транскриптазы – ненуклеозидных (ННИОТ). Хотя обратная транскриптаза (ОТ) хочет работать с чем-то, похожим на нуклеозид (нуклеозидтрифосфат), можно попробовать сделать такое вещество, которое будет связываться с ОТ и изменять её форму – так, чтобы она больше не могла выполнять свои функции.
В 1996 и 1998 годах соответственно были одобрены два таких вещества, невирапин и эфавиренз. Каждое их них эффективно подавляет работу ОТ, и в комбинации с двумя НИОТ составляет полную схему высокоактивной антиретровирусной терапии (ВААРТ) – достаточную для того, чтобы человек, живущий с ВИЧ, мог прожить полную жизнь, по продолжительности не сильно отличающуюся от жизни человека без ВИЧ.
В 2006 году был одобрен первый комбинированный препарат, предназначенный для однократного приёма в день: Атрипла. Атрипла состоит из двух НИОТ, эмтрицитабина и тенофовира (в форме тенофовира дизопроксила – пролекарства, химически модифицированной лекарственной формы, которая превращается в лекарство непосредственно в организме), и одного ННИОТ, эфавиренза. Атрипла стала качественно новым шагом на пути улучшения качества жизни пациентов. На сегодняшний день дженерики Атриплы являются одним из наиболее часто используемых лекарств в мире (в развивающихся странах).
Однако сегодня ННИОТ постепенно уходят с рынка – старые препараты вызывают различные побочные эффекты. Так, например, эфавиренц первые два месяца после начала приёма может вызывать у некоторых пациентов (далеко не у всех!) головокружение и другие похожие эффекты. Конечно, это намного лучше, чем неминуемая смерть; длится подобное состояние не так уж и долго, да и бороться с ним уже научились – однако современная тенденция – переход на такие лекарства, побочных эффектов от которых пациент не замечает вовсе.
Если обратная транскриптаза всё-таки выполнила свою работу, возможно ли остановить внедрение вирусной ДНК в ДНК клетки? Этим процессом занимается специальный фермент, называемый интегразой.
Процесс интеграции вирусной ДНК протекает в несколько стадий. Вначале интеграза соединяется с вирусной ДНК, удаляя с 3'-конца каждой цепи динуклеотид GT. Затем весь комплекс транспортируется в ядро, где интеграза катализирует стадию переноса цепи. Эта стадия представляет собой реакцию переэтерификации (обмена радикалами): нуклеотиды ДНК клетки становятся соединены не друг с другом, а с нуклеотидами вирусной ДНК. Интеграза атакует межнуклеотидные связи, расположенные на расстоянии пяти нуклеотидов. Таким образом, после интеграции остаются: процессинг 5'-концов цепей вирусной ДНК, достройка 5 недостающих нуклеотидов и лигирование (соединение двух нитей НК ферментом лигазой), которые выполняются при участии клеточных белков [1].
Скрининг около 250000 веществ в библиотеках химических соединений позволил найти вещества, которые бы ингибировали интегразу ВИЧ. Все они оказались соединениями 2,4-диоксобутановой кислоты. Они координировали ионы металла в активном центре интегразы – в той части, которая отвечала за перенос цепи. Дальнейшие попытки разработки ингибиторов интегразы ВИЧ-1 привели к появлению производного N-пиримидинона, вещества MK-0518, получившего название ралтегравир. [2]
Общими для ралтегравира и последующих ингибиторов интегразы являются хелатирующая триада (координирующая ионы металла) и галогенбензильное кольцо, взаимодействующее с предпоследним дезоксицитозином в 3′-конце связанной с ферментом вирусной ДНК.
Процесс интеграции вируса в клетку – это последний этап, на котором действенна постконтактная профилактика. После этого в организме человека появляются клетки, несущие в своём ядре ДНК ВИЧ. Наиболее эффективное окно для проведения постконтактной профилактики составляет порядка 6-10 часов.
Галогенбензильное кольцо в молекуле ингибитора интегразы взаимодействует с вирусной ДНК, а группа атомов кислорода – с двумя атомами металла. Эти атомы металла интеграза вируса использует для того, чтобы внедрить вирусную ДНК в клетку. В результате процесс интеграции блокируется.
Современные ИИ – такие, как долутегравир – смогли победить „детские болезни“ ралтегравира, связанные с быстрым формированием резистентности.
После того, как геном вируса проходит этап транскрипции, созданные вирусные РНК направляются к выходу из клетки. В процессе создания вириона участвует ещё один вирусный фермент, называемый протеазой. Протеаза разрезает длинные полипротеины на отдельные функциональные белки, в результате чего образуются вирусные ферменты и структурные белки вируса.
Протеаза проявляет активность не только в отношении белков ВИЧ, но и в отношении белков клетки-хозяина, что, возможно, объясняет цитотоксическое действие ВИЧ (гибель клеток).
Если заблокировать работу протеазы, вирион не сможет пройти стадию созревания и останется полностью нефункциональным. Протеаза ВИЧ-1 – это типичная ретровирусная аспартатная протеаза, имеющая в активном центре характерную аминокислотную последовательность Asp25 Thr26 Gly27 (аспаргиновая кислота – треонин – глицин). Первый ингибитор протеазы, саквинавир, был одобрен FDA 6 декабря 1995 года. Таким образом, именно после создания саквинавира впервые стала доступна высокоактивная антиретровирусная терапия.
Другим типичным представителем этой группы лекарственных средств является лопинавир (применяемый совместно с ритонавиром – калетра – одно из наиболее распространённых лекарств от ВИЧ в России). Ритонавир также является ингибитором протеазы, но используется как бустер – благодаря его действию повышается концентрация основного препарата.
Поскольку саквинавир и последовавшие ингибиторы протеазы (ИП) нацелены именно на активный центр фермента, то при развитии резистентности к одному ИП высока вероятность того, что возникнет резистентность и к другим ИП. Решением данной проблемы может быть создание таких ингибиторов, которые направлены на другие зоны протеазы.
Появившийся в 2006 году препарат дарунавир (презиста) в некоторой степени снял остроту проблемы резистентных к ИП штаммов ВИЧ-1, так как образовывал ранее не использовавшуюся связь с аспаргиновой кислотой в позиции 30.
Без участия протеазы вирус не может пройти процесс созревания. Ингибиторы соединяются с активным центром протеазы и не дают ей работать.
Ингибиторы протеазы являются высокоэффективными средствами при высокой вирусной нагрузке: поскольку в этот момент в организме рождается много новых вирионов, ИП не дают им созревать, таким образом, эффективно снижая вирусную нагрузку в течение короткого времени. Тем не менее, в настоящий момент ИП не применяются в терапии первой линии, уступая своё место ингибиторам интегразы (ИИ).
Причиной этого стали побочные эффекты: дело в том, что, например, та же калетра приводила к неспецифическому ингибированию протеолиза белков, поступающих с пищей, в результате эти белки попадали в тонкий кишечник и вызывали диарею. Соблюдение специфической диеты или применение новых ИП, таких, как презиста, позволяет свести этот эффект практически к нулю, но вот другой эффект, связанный с повышением уровня сахара, зачастую не позволяет употреблять ингибиторы протеазы бесконечно долго.
На сегодняшний день самыми современными считаются схемы, состоящие из ингибитора интегразы и из одного или двух НИОТ (долутегравир + абакавир + ламивудин; долутегравир + ламивудин – популярная двухкомпонентная схема, подходящая, однако, не для всех). Эти схемы позволяют человеку прожить полноценную жизнь, не отличающуюся по длительности от жизни человека без ВИЧ.
Несмотря на все успехи, полное излечение от ВИЧ до сих пор невозможно (пересадка стволовых клеток костного мозга от донора с мутацией CCR5-∂32 позволяет добиться такого результата, но, видимо, только в том случае, если возникнет реакция „трансплантат против хозяина“, в большом количестве случаев ведущая к смерти реципиента).
Разработанные методики борьбы с ВИЧ помогли в борьбе и с другими инфекционными заболеваниями: как упоминалось выше, ламивудин и тенофовир эффективны против вируса гепатита B (класс VII по Балтимору – полимераза гепатита B способна переписывать РНК в ДНК, поэтому некоторые НИОТ эффективны в борьбе с ним). Полученные знания помогли разработать препараты прямого действия против гепатита C, которые сегодня позволяют полностью вылечить это заболевание (у гепатита C нет латентной фазы, поэтому при подавлении вирусной нагрузки неоткуда взяться новым вирионам – заболевание полностью вылечено).
[1] Королев С. П., Агапкина Ю. Ю., Готтих М. Б. Проблемы и перспективы клинического применения ингибиторов интеграции ВИЧ-1
[2] Шахгильдян В.И. Ингибиторы интегразы ВИЧ — основа эффективной и безопасной антиретровирусной терапии
К ингибиторам протеазы ВИЧ относятся саквинавир, индинавир, ритонавир, нелфинавир и ампренавир.
Механизм действия
Протеаза ВИЧ - фермент, необходимый для протеолитического расщепления полипротеиновых предшественников вируса на отдельные белки, входящие в состав ВИЧ. Расщепление вирусных полипротеинов крайне важно для созревания вируса, способного к инфицированию. ИП блокируют активный центр фермента и нарушают образование белков вирусного капсида. Препараты этой группы подавляют репликацию ВИЧ, в том числе при резистентности к ингибиторам обратной транскриптазы. В результате угнетения активности ВИЧ-протеазы формируются незрелые вирусные частицы, неспособные к инфицированию других клеток.
Спектр активности
Клиническое значение имеет активность ИП против ВИЧ-1 и ВИЧ-2.
Лечение ВИЧ-инфекции в составе комбинированной терапии.
Химиопрофилактика парентерального заражения ВИЧ.
Саквинавир (INV, FTV)
Первый препарат группы ИП, внедренный в клиническую практику в 1995 г. С этого момента началась эра ВААРТ.
ЖКТ:диарея, боль в животе, тошнота.
Полость рта:изъязвление слизистой оболочки, фарингит.
Гематологические реакции:гемолитическая анемия.
Метаболические нарушения:перераспределение подкожной жировой клетчатки, повышение уровня холестерина (в том числе липопротеидов низкой плотности), триглицеридов, гипергликемия (иногда развивается сахарный диабет 2 типа).
Нервная система:головная боль, спутанность сознания, атаксия, слабость, головокружение, астенический синдром, судороги, периферические нейропатии, онемение конечностей.
Кожа:сыпь, зуд, синдром Стивенса–Джонсона, дерматит.
Опорно-двигательный аппарат:боль в мышцах и суставах, остеопороз.
Другие:аваскулярный некроз (редко).
При сочетании с зальцитабином:парестезии, бессонница, рвота, стоматит, нарушение аппетита.
При сочетании с зидовудином:приливы, изменения пигментации, спутанность сознания, гипермоторика кишечника, сухость во рту, эйфория, бессонница, раздражительность, обесцвечивание кала, глоссит, ларингит, задержка мочеиспускания, анорексия, ксерофтальмия, нейтропения, миелолейкоз (через 2 мес после прекращения лечения).
Противопоказания
Гиперчувствительность к саквинавиру.
Возраст до 16 лет и старше 60 лет.
Беременность.Данные о прохождении саквинавира через плаценту и уменьшении риска трансплацентарной передачи вируса отсутствуют.
Кормление грудью.Данные о проникновении саквинавира в грудное молоко отсутствуют. Матерям с ВИЧ-инфекцией кормление грудью не рекомендуется.
Педиатрия.Эффективность и безопасность саквинавира у детей до 16 лет не изучена.
Гериатрия.Эффективность и безопасность саквинавира у людей старше 60 лет не изучена.
Не рекомендуется одновременный прием саквинавира и ифавиренца, поскольку концентрация последнего понижается на 62%.
При одновременном приеме саквинавира и индинавира концентрация первого увеличивается в 4–7 раз, содержание индинавира не изменяется.
При сочетанном применении саквинавира с ритонавиром концентрация саквинавира повышается в 20 раз, содержание ритонавира не изменяется.
При комбинированном применении саквинавира с нелфинавиром концентрация саквинавира повышается в 3–5 раз, нелфинавира - на 20%.
При одновременном приеме саквинавира и ампренавира концентрация саквинавира уменьшается на 19%, ампренавира - на 32%.
Невирапин понижает концентрацию саквинавира на 25%.
Саквинавир может повышать концентрации в плазме многих ЛС, тормозя их метаболизм в печени (нифедипин, верапамил, дилтиазем, клиндамицин, хинидин, препараты спорыньи, циклоспорин, фентанил, алфентанил, алпразолам, триазолам, дизопирамид, ловастатин, симвастатин).
Нельзя сочетать саквинавир с терфенадином, астемизолом или цизапридом вследствие высокого риска развития потенциально фатальной сердечной аритмии.
Кетоконазол, флуконазол и итраконазол увеличивают концентрацию в плазме крови саквинавира.
Индукторы цитохрома Р-450 (рифампицин, рифабутин, фенитоин и др.) уменьшают концентрацию в плазме саквинавира, уменьшая его эффективность.
Фармацевтика, медицина, биология
Ингибиторы протеазы
Ингибиторы протеазы — это группа антиретровирусных препаратов, механизм действия которых заключается в блокировании фермента вируса ВИЧ — протеазы, который необходим для расщепления полипротеинових предшественников вируса на отдельные белки, входящие в состав вируса и нарушают образование белков вирусного капсида. Препараты группы активны против вируса ВИЧ как I, так и II типа. Некоторые препараты группы активны против вируса гепатита С. К ингибиторов протеазы относятся саквинавир, лопинавир, ритонавир, индинавир, нелфинавир, ампренавир, фосампренавир, атазанавир, дарунавир, типранавир, активные против вируса ВИЧ; и боцепревир и телапревир, активные против вируса гепатита С. Первым препаратом группы, примененным в клинической практике, был саквинавир в 1995 году, что фактически стало началом эры ВААРТ.
Механизм действия
Ингибиторы протеазы после перорального приема проникают в пораженные клетки и ингибируют активный центр фермента вируса ВИЧ протеазы, нарушают образование вирусного капсида и подавляют репликацию вируса ВИЧ с образованием незрелых вирусных частиц, которые не могут инфицировать клетки организма. К ингибиторов протеазы чувствительны вирусы ВИЧ-1, ВИЧ-2 и вирус гепатита С и нечувствительны протеазы человека и других эукариот. Препараты группы могут эффективно подавлять вирус ВИЧ, в том числе при неэффективности ингибиторов обратной транскриптазы.
Фармакокинетика
Большинство ингибиторов протеазы хорошо, но медленно всасываются в желудке, прием препаратов с пищей улучшает всасывание. Максимальная концентрация ингибиторов протеазы в крови достигается в среднем в течение 4:00. Биодоступность препаратов группы колеблется, поэтому часто ингибиторы протеазы применяются с другим препаратом группы — ритонавиром, имеющий высокую степень сходства с некоторыми формами цитохрома P-450 и выполняет роль фармакокинетического усилителя (бустера) для других ингибиторов протеазы. Большинство препаратов группы плохо проникают через гематоэнцефалический барьер. Большинство ингибиторов протеазы проникают через плацентарный барьер и выделяются в грудное молоко. Метаболизируются ингибиторы протеазы в печени с образованием неактивных метаболитов. Выводятся из организма препараты группы преимущественно почками, частично выводятся с калом. Период полувыведения препаратов группы колеблется от 1:00 (саквинавир) до 10:00 (ампренавир), в большинстве препаратов группы это время не изменяется при печеночной и почечной недостаточности.
Применение
Ингибиторы протеазы применяются для лечения ВИЧ-инфекции, вызванной вирусом как I, так и II типа исключительно в составе комбинированной терапии. Боцепревир и телапревир применяются для лечения гепатита С. Препараты группы применяются беременными женщинами для профилактики вертикальной передачи вируса ВИЧ ребенку и используются для предотвращения профессионального заражения медицинскими работниками во время аварийных ситуаций.
Побочное действие
При применении ингибиторов протеазы среди побочных эффектов чаще наблюдаются поражения кожи — высыпания на коже, зуд кожи, аллергический дерматит, крапивница, фолликулит; с аллергических реакций часто наблюдаются синдром Стивенса-Джонсона, синдром Лайелла, анафилактический шок, кашель, лихорадка. Со стороны пищеварительной системы часто наблюдаются тошнота, рвота, диарея, снижение аппетита, боль в животе, гепатит, желтуха, печеночная недостаточность, панкреатит, желудочно-кишечные кровотечения, повышение уровня активности аминотрансфераз и ГГТП в крови, повышение уровня билирубина в крови. Со стороны нервной системы могут наблюдаться головная боль, бессонница, сонливость, повышенная утомляемость, гиперкинезы, парестезии, потери сознания, судороги. Со стороны сердечно-сосудистой системы могут наблюдаться аритмии, иногда — стенокардия, инфаркт миокарда, артериальная гипо- и гипертензия, спазмы периферических сосудов. Со стороны опорно-двигательного аппарата могут наблюдаться миалгии, миопатии, артралгии, рабдомиолиз. Со стороны мочевыделительной системы наблюдаются острая и хроническая почечная недостаточность, дизурия, иногда нефролитиаз. Среди других побочных эффектов наблюдаются липодистрофия, лактатацидоз, сахарный диабет, гинекомастия (преимущественно в комбинации с другими препаратами), повышение риска кровотечений у больных гемофилией. При проведении комбинированной антиретровирусной терапии с применением ингибиторов протеазы у больных возрастает вероятность лактатацидоза и гепатонекроза. При проведении ВААРТ у больных возрастает вероятность развития сердечно-сосудистых осложнений, гипергликемии и гиперлактемии. При проведении ВААРТ возрастает вероятность синдрома восстановления иммунной системы с обострением латентных инфекций.
Противопоказания
Абсолютным противопоказанием для применения препаратов группы ингибиторов протеаз является гиперчувствительность к препарату. Препараты группы с осторожностью применяются при печеночной недостаточности, некоторые препараты с осторожностью применяются при беременности. Препараты группы не применяются во время кормления грудью. Препараты группы не рекомендуется применять вместе с астемизолом, цизапридом, терфенадином, мидазоламом, пимозидом, бепридилом, амиодароном, алкалоидами спорыньи, пропафеноном.
Вирусы могут размножаться только внутри клетки-хозяина, перестраивая ее работу так, что клетка начинает производить новые вирусные частицы. Это серьезно нарушает работу самой клетки и в большинстве случаев ведет к ее гибели. Процесс проникновения и размножения вируса в ней сложный и содержит много стадий, но специальные лекарства могут блокировать его на различных этапах.
В случае с ВИЧ это выглядит так.
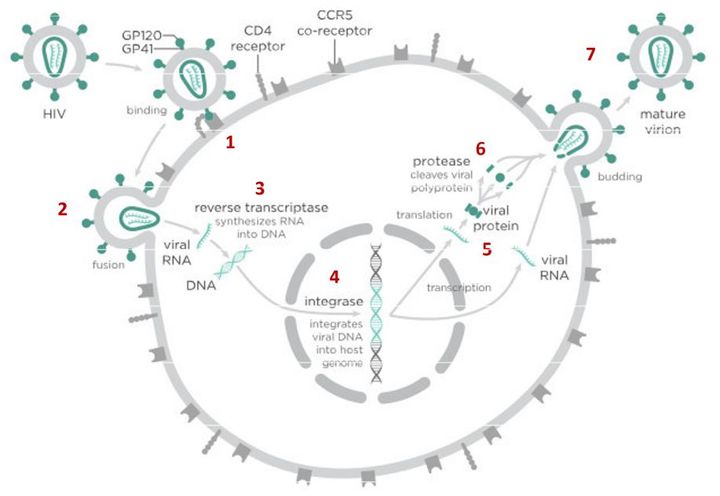
На первом этапе (цифра 1 на схеме) вирус проникает в клетку.
На этом этапе работает другой препарат против ВИЧ — маравирок. Молекула этого лекарства связывается с рецептором CCR5 и блокирует его, что не позволяет вирусу перейти к следующему этапу проникновения в клетку и останавливает заражение. Но у этого вещества есть недостаток — дело в том, что некоторые типы вируса иммунодефицита человека используют на втором этапе другой рецептор — CXCR4. Такому вирусу маравирок не помешает проникнуть в клетку.
(На этом видео можно увидеть как протекает этот и другие этапы репликации вируса в клетке)
После того как вирусная частица приклеилась к рецепторам CD4 и CCR5/CXCR4 и закрепилась на поверхности клетки, другой специальный белок вируса gp41 соединяет оболочку вируса с мембраной клетки-мишени и помогает вирусу проникнуть внутрь клетки (цифра 2 на схеме).
На этом этапе остановить вирус может другая группа препаратов — ингибиторы слияния, например, энфувиртид. Препарат связывается с вирусным белком gp41 и нарушает его работу.
Следующий важный этап (на схеме обозначен цифрой 3) — обратная транскрипция. Для того чтобы клетка начала производить вирусные частицы, вирус должен встроить свою генетическую информацию в ДНК клетки-хозяина.
На этом этапе размножение вируса блокирует очень большое количество препаратов из двух классов — нуклеозидные ингибиторы обратной транскриптазы (НИОТ — ламивудин, абакавир, тенофовир) и ненуклеозидные ингибиторы обратной транскриптазы (ННИОТ — эфавиренз, рилпивирин).
Принцип действия у веществ из обеих групп похожий: молекула лекарства связывается с обратной транскриптазой вируса, нарушает ее работу и так блокирует перенос генов вируса из РНК в ДНК. Это не позволяет генам вируса встроиться в ДНК клетки-хозяина и начать производство новых вирусных частиц.
На следующем этапе инфицирования (цифра 4 на схеме) готовая вирусная ДНК проникает в ядро и встраивается в ДНК клетки-хозяина с помощью специального вирусного фермента — интегразы.
Работу этого фермента блокируют ингибиторы интегразы, например, долутегравир, не позволяя ДНК вируса встроиться в наши гены.
После того как вирусная ДНК встраивается в ДНК клетки-хозяина, клетка получает неправильную программу и начинает производить вирусные белки и РНК, необходимые для сборки новых частиц вируса (цифра 5 на схеме), используя для этого структуры, которые в норме производят собственные белки клетки. Такая перенастройка производства белка сильно нарушает работу клетки и через некоторое время вызывает ее гибель. Лекарств, которые бы влияли на этот этап размножения вируса, нет, так как здесь вирус использует собственные ферментные системы клетки-хозяина и блокирование их работы какими-то веществами навредит здоровым клеткам.
После синтеза вирусных белков клеткой-хозяином в работу вступает еще один фермент вируса — протеаза (цифра 6 на схеме). Дело в том, что белки ВИЧ синтезируются в виде длинных цепочек белков-предшественников, но они неактивные. Протеаза разрезает эти цепочки на более короткие фрагменты, которые становятся активными белками вируса: из одних собирается вирусная оболочка, другие выполняют функции ферментов (обратная транскриптаза, интеграза, протеаза, о которых мы говорили выше). Класс лекарств, нарушающих работу вирусной протеазы (ингибиторы протеазы), включает большое количество препаратов от достаточно старого лопинавира до современного дарунавира. Основной недостаток препаратов этого класса — высокая степень перекрестной устойчивости: если вирус приобретает устойчивость к одному препарату, скорее всего, на него не подействует ни один другой препарат из этого класса.
На последнем этапе (цифра 7 на схеме) вирусные частицы собираются из готовых компонентов (синтезированных клеткой вирусных белков и РНК), как конструктор, и покидают клетку-хозяина. Лекарств, которые бы тормозили эти процессы, пока не существует.
ВИЧ имеет высокую склонность к мутациям, что позволяет ему быстро приобретать устойчивость к лекарствам. Мутации изменяют форму молекул ферментов вируса. Если при этом форма изменится существенно, то фермент не сможет нормально работать и такой вирус размножаться перестанет — это вредная для вируса мутация. Однако в некоторых случаях — при полезных мутациях — форма молекулы фермента меняется не сильно, а так, что сам фермент продолжает нормально работать, но молекула лекарства уже не может с ним связаться.
Поэтому для эффективного подавления размножения ВИЧ обычно назначают три разных препарата из разных групп, влияющих на разные ферменты вируса, блокируя его воспроизводство на разных этапах. Исключением является группа ингибиторов обратной транскриптазы (НИОТ и ННИОТ) — эти лекарства связываются с разными участками молекулы вирусного фермента, поэтому могут назначаться вместе, несмотря на то, что относятся к одной группе. В условиях такой терапии вирусу очень трудно выработать устойчивость, потому что одновременно должно произойти несколько полезных мутаций в разных генах вируса, а это бывает крайне редко.
Есть несколько перспективных технологий, например, CRISPR/Cas9, которые могут позволить полностью удалить вирусную ДНК из организма человека, но пока ни одна из них не прошла все необходимые исследования для подтверждения эффективности и безопасности. Исследования продолжаются.
Читайте также:


