Современные методы диагностики сепсиса реферат
Диагноз синдрома системной воспалительной реакции ставится на основании перечисленных выше признаков. Этот диагноз не может звучать самостоятельно, а только лишь вместе с той или иной нозологической формой (пневмония ССВР-III – что означает наличие пневмонии, сопровождающейся тремя из четырех признаков ССВР). ССВР является важным признаком, свидетельствующим о возможности перехода процесса в более тяжелые формы и требующим принятия адекватных мер по лечению.
Диагноз сепсиса ставится в соответствии с указанными выше критериями. Для него необходимо наличие как минимум трех признаков системной воспалительной реакции на фоне явного местного инфекционного процесса или верифицированной бактериемии (фунгемии, вирусемии и т.д.), сохраняющиеся на протяжении как минимум трех суток, несмотря на проводимую терапию
Диагноз сепсис-синдрома формулируется при наличии указанных выше симптомов системной воспалительной реакции, манифестирующих на фоне верифицированного источника инфекции и лабораторных данных, свидетельствующих о развитии несостоятельности того или иного органа (приложение 1) при отсутствии других явных причин, объясняющих это состояние (крайние стадии хронических заболеваний и т.д.).
Септический шок – снижение артериального давления ниже 90 мм.рт.ст. на фоне септического процесса, несмотря на адекватную инфузионную терапию и проводимое лечение.
Лабораторная диагностика: обязательная и желательная.
К обязательным методам относятся: трехчасовое измерение температуры; анализ крови общий, включая тромбоциты; анализ мочи; почасовой диурез; биохимический анализ крови, включающий К+, Na+, КОС, билирубин, АСТ, АЛТ, креатинин, мочевину, общий белок и протеинограмму, протромбин, фибриноген, фибринолиз; бактериоскопия мазка из раны; микробиологическое исследование крови (2 пробы) на стерильность, мочи, отделяемого из раны, при ИВЛ – посевы бронхиального отделяемого, удаляемого катетера и дренажа; исследование кишечной флоры на дисбиоз.
К желательным методам относятся: иммунный статус; прокальцитонин; С-реактивный белок (численная методика).
Аппаратные методы: УЗИ органов брюшной полости; УЗИ сердца (патология клапанов); R-графия груди; КТ и другие.
6. Первичная лечебная тактика при хирургическом сепсисе.
Обследование и лечение больного с хирургическим сепсис-синдромом и септическим шоком должно проводиться в условиях отделения (палаты) интенсивной терапии совместно хирургом и реаниматологом. Оперативное вмешательство (как правило, вторичная хирургическая обработка) при наличии показаний выполняется в неотложном порядке. Вмешательство может быть отложено лишь при нестабильных показателях гемодинамики, до выполнения мероприятий, ведущих к ее стабилизации.
Объем оперативного вмешательства должен включать в себя: максимально полную некрэктомию, адекватное дренирование очага, преимущественно двухпросветными трубками. Целесообразна установка внутрисосудистых катетеров для регионарной терапии.
7. Эмпирическая антибактериальная терапия. Иммунокоррекция.
Антибактериальная терапия начинается после забора проб для выполнения микробиологических исследований и носит, в подавляющем большинстве, эмпирический характер. Путь введения, в основном, внутривенный. После стабилизации состояния целесообразен переход на другие пути введения. Выбор антибиотиков определяется, во-первых, локализацией очага, обусловившего развитие генерализованного процесса, и, во-вторых, тяжестью состояния больного, оцененной по шкале SAPS (Le Gall). В соответствии с этим рекомендуются следующие варианты.
А) посттравматический сепсис. SAPS 15: фторхинолоны (ципрофлоксацин) + цефалоспорины III - IV (цефоперазон, цефтазидим или цефепим) + метронидазол; карбапенемы;
B) Интраабдоминальный сепсис SAPS
Г) Интраабдоминальный сепсис SAPS>15: цефепим + метронидазол; карбапенемы, при множественных очагах и при деструктивном панкреатите - предпочтительно меропенем Д) Воспалительные заболевания мягких тканей SAPS 15: ванкомицин или фторхинолоны + аминогликозиды III (в случае отсутствия ОПН)+ метронидазол; карбопенемы; при верифицированной стрептококковой природе - пенициллины или амоксиклав.
Заключение
Сепсис - общее инфекционное заболевание, возникающее в связи с существованием в организме очага инфекции и имеющее ряд отличий от других инфекционных болезней , с точки зрения диагностики и лечения - это недостаточная или извращенная общебиологическая реакция макроорганизма в ответ на внедрение неспецифического микробного возбудителя, сопровождающаяся его генерализацией и протекающая в виде стадийного процесса различной протяженности, при которой самостоятельная способность организма бороться с инфекцией.
Взгляды на этиологию и патогенез сепсиса на протяжении XX века претерпевали серьезные изменения: они эволюционировали от признания первостепенной роли микроба как главной причины развития сепсиса (теория Шоттмюллера о септическом очаге) до утверждения решающего значения состояния макроорганизма.
Список литературы
1.Антибактериальная терапия: Практическое рукодство/ Под ред. Л.С. Страчунского,Ю.Б.Белоусова, С.Н.Козлова.-М.: Фарммединфо, 2000.- 357с.
2.Брюсов П.Г., Нечаев Э.А. Военно-полевая хирургия / Под ред. М. Геотара.
3.Раны и раневая инфекция. Под ред. Кузина М.И. М.: Медицина, - 1981, - 688с.
4.Стручков В.И. Хирургическая инфекция. М.: Медицина, - 1991, - 560с.
5.Хирургические инфекции: руководство/ Под ред. И.А. Ерюхина и др. – СПб: Питер, 2003. – 864с.

Актуальность. Стратегия лечения сепсиса у больных основывается на быстром применении эмпирической антибиотикотерапии. Одновременно у пациента берется кровь на бактериальный посев. Это позволяет значительно снизить летальность при данном тяжелом осложнении. Однако срок культивирования посевов составляет 7 суток, и результат микробиологического анализа может быть получен самое раннее через 24 - 48 часов и может лишь подтвердить инфекционную этиологию и идентифицировать возбудителя (к тому же микробиологический метод малоприменим для культивирования микоплазм, нокардий, риккетсий, хламидий и др. - для их диагностики используются серологические и молекулярно-биологические методы). Таким образом, роль бактериологи ческой лаборатории в первый критический период возникновения сепсиса невелика, и успех лечения полностью определяется правильностью проводимой эмпирической антибиотикотерапии. В случае неэффективности проводимой эмпирической терапии критическое значение приобретает быстрая корректировка лечения, так как каждый час ее задержки повышает вероятность летального исхода на 5 - 8% (Kumar A., Roberts D., Wood K.E., et al., 2006). В этот период выявление возбудителя и определение его чувствительности к антибиотикам приобретает решающее значение. В связи с этим понятен интерес к разработке быстрых и в тоже время чувствительных методов диагностики сепсиса и оценки его тяжести.
Современные методы лабораторной диагностики. В.Н. Чеботкевич, Е.И. Кайтанджан, В.В. Бурылев, Е.Е. Щетинкина (Российский НИИ гематологии и трансфузиологии ФМБА России, Санкт-Петербург, Россия; 2013) провели обзор применяемых микробиологических и молекулярно-биологических методов лабораторной диагностики сепсиса.
Разрабатываются также методы выделения ДНК непосредственно из биоматериалов – образцов цельной крови, плазмы и сыворотки. Экстракция из образцов цельной крови, обработанной ЭДТА, позволяет получить большее количество бактерий, чем при выделении из сыворотки или плазмы. Однако присутствие ингибиторов ПЦР в цельной крови снижает чувствительность этого метода. Показана более высокая чувствительность образцов сыворотки для диагностики бруцеллеза, несмотря на то, что представители рода Brucella являются факультативными внутриклеточными паразитами. Это говорит о необходимости выбирать протокол экстракции при разработке стандартной процедуры выделения. Существуют автоматизированные системы прямой экстракции ДНК из цельной крови. Однако их высокая стоимость ограничивает использование в практических лабораториях.
Дальнейшее совершенствование NAT-технологий диагностики позволит внедрить их в работу практических микробиологических лабораторий. На сегодняшний день, наряду с методологическими трудностями, главным препятствием внедрения NAT технологий является их высокая стоимость, однако развитие и совершенствование этих методов, безусловно, позволит удешевить их проведение и ввести NAT-тестирование в алгоритм диагностики сепсиса.
Протеомные технологии с использованием время-пролетной масс-спектрометрии ( MALDI-TOF MS) позволяют идентифицировать бактерии и грибы по их белковому профилю. Также он позволяет определять некоторые маркеры антибиотикорезистентности. Основным недостатком данной технологии является невозможность ее применения непосредственно для биологических образцов. Здесь требуется предварительное культивирование образцов для увеличения числа микробных тел в пробе. Кроме того, ввиду большой стоимости оборудования этот метод является недоступным для многих лабораторий.
Ряд методов используется для идентификации микробов в положительных микробиологических пробах. Наиболее изученным из не микробиологических тестов является PNA-FISH (AdvanDX, США). Метод основан на гибридизации in situ флуоресцентно меченных пептидно-нуклеотидных проб к ограниченному набору бактерий. Метод удобен для использования, и анализ может быть выполнен за 3 часа. Заявленная фирмой чувствительность и специфичность метода близка к 99 - 100%. В наборе Hyplex BloodScreen (BAG, Германия) используется мультиплексная ПЦР. Возможна идентификация нескольких бактериальных видов, включая метициллино-чувствительные и метициллино-резистентные штаммы стафилококков, стрептококков и энтерококков, а также грамотрицательных бактерий (E. coli, Enterobacter aerogenes, Pseudomonas aeruginosa, Klebsiella spp.). Продолжительность проведения исследования 3 – 4 часа при заявленной чувствительности в дифференцировке различных видов от 96,6 до 100% и специфичности от 92,5 до 100%. Метод позволяет определять маркеры резистентности – гены van и несколько генов -лактамаз. Недавно предложен набор с использованием метода микрочипов для определения большого количества видов бактерий и гена mecA (Mobidiag, Финляндия). Анализ занимает 3 часа с заявленной чувствительностью 94% и специфичностью 96%.
Разрабатываются также методы по индикации микробов непосредственно из крови. Набор SepsiTest (Molzym, Германия) представляет собой метод, основанный на выявлении генов 16S рРНК бактерий и генов 18S рРНК грибов. Потенциально этот метод позволяет провести полную видовую дифференцировку бактерий и грибов с помощью секвенирования генома. Однако имеется большой риск контаминирования пробы на пост-амплификационном этапе исследований и получения ложноположительных результатов. Кроме того, секвенирование для его проведения требует 8 - 12 часов, что не позволяет рассматривать его как метод ранней диагностики сепсиса.
Карагандинская Государственная Медицинская Академия
Кафедра глазных, ЛОР – болезней с курсом реаниматологии
"Диагностика и лечение тяжелого сепсиса и септического шока"
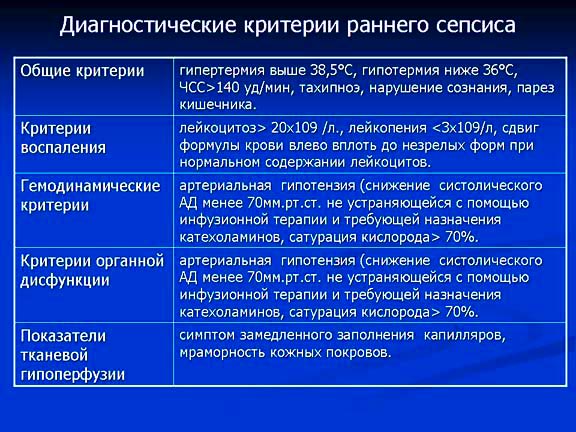
Диагностические критерии сепсиса
| Инфекция, предполагаемая или подтверждённая в сочетании с несколькими из следующих критериев: |
| Общие критерии |
| Критерии воспаления |
| Гемодинамические критерии |
| Критерии органной дисфункции |
| Показатели тканевой гипоперфузии |
| Примечание: a АДсист - систолическое артериальное давление, АДср - среднее артериальное давление.; b АЧТВ – активированное частичное тромбопластиновое время; с Международное нормализованное отношение |
| Патологический процесс | Клинико-лабораторные признаки |
| Синдром системной воспалительной реакции (ССВР) – системная реакция организма на воздействие различных сильных раздражителей (инфекция, травма, операция и др.) | Характеризуется двумя или более из следующих признаков: – температура ³38 o С или £36 o С – ЧСС ³90/мин – ЧД >20/мин или гипервентиляция (РаСО2 £32 мм.рт. ст.) – Лейкоциты крови >12´10 9 /мл или 9 /мл, или незрелых форм >10% |
| Сепсис – синдром системной воспалительной реакции на инвазию микроорганизмов | Наличие очага инфекции и 2-х или более признаков синдрома системного воспалительного ответа |
| Тяжелый сепсис | Сепсис, сочетающийся с органной дисфункцией, гипотензией, нарушениями тканевой перфузии. Проявлением последней, в частности, является повышение концентрации лактата, олигурия, острое нарушение сознания |
| Септический шок | Сепсис с признаками тканевой и органной гипоперфузии, и артериальной гипотонией, не устраняющейся с помощью инфузионной терапии и требующей назначения катехоламинов |
| Дополнительные определения | |
| Дисфункция по 2 и более системам органов | |
| Рефрактерный септический шок | Сохраняющаяся артериальная гипотония, несмотря на адекватную инфузию, применение инотропной и вазопрессорной поддержки |
Критерии органной дисфункции при тяжелом сепсисе
| Системы органов | Клинико-лабораторные критерии |
| Сердечнососудистая система | Систолическое АД ≤90 mmHg или среднее АД ≤ 70 mmHg в течение не менее 1 часа, несмотря на коррекцию гиповолемии |
| Мочевыделительная система | Мочеотделение 3 или их снижение на 50% от наивысшего значения в течение 3-х дней |
| Метаболическая дисфункция | |
| ЦНС | Балл по шкале Глазго менее 15 |
Шкала SOFA (Sequential Organ Failure Assessment)
Применяется для ежедневной оценки состояния пациента и оценки эффективности терапии.
Ингибирование протеолитических ферментовикининов. 5
2. Лечебное питание.
3. Санация первичного очага.
4. Антибактериальная терапия.
5. Управляемая гипокоагуляция.
6. Иммуномодулирующая терапия.
7. Ингибирование протеаз и кининов.
8. Дезинтоксикационная терапия.
10. Симптоматическая терапия.
При подозрении или установлении диагноза сепсиса больного следует госпитализировать в хирургическое отделение. Возможно лечение пациента в других отделениях при некоторых специфических источниках сепсиса. Имеется ввиду урологическое отделение при уросепсисе, ревматологическое, терапевтическое или кардиологическое отделение при септическом эндокардите и т.д. На весь период лихорадочного состояния назначается постельный режим. При снижении температуры тела до нормальных цифр, улучшении общего состояния и лабораторных показателей режим постепенно расширяется, осторожно добавляется лечебная физкультура.
Вначале больному рекомендуется стол №10. В дальнейшем по мере нормализации клинико-лабораторных показателей, отражающих активность воспалительного процесса, и компенсации функций жизненно важных систем можно порекомендовать общий стол с достаточным количеством овощей и фруктов (15б).
Этот этап лечения играет решающую роль в достижении результата. Если не ликвидировать первичный очаг, никакое лечение не ликвидирует септического процесса. Считается, что это утверждение справедливо как для септицемии, так и для септикопиемии, при которой, как известно, обычно имеют место вторичные септические очаги. Часто врачам бывает трудно установить локализацию первичного очага. Большое значение в данной ситуации принадлежит искусству сбора анамнеза. В случае т.н. криптогенного сепсиса врачу может помочь таблица распределения локализации первичного очага.
Санация первичного очага должна быть по возможности радикальной. Тем не менее, при высоком риске оперативного вмешательства и (или) анестезиологического риска допускается проведение паллиативных вмешательств, направленных на вскрытие гнойника, и даже отсроченных вмешательств.
Такой специфический род септического процесса, как септический эндокардит, в большинстве случаев лечится консервативно.
Основные принципы антибактериальной терапии
Лечение антибактериальными средствами нужно начинать сразу же после установления диагноза. При правильной антибактериальной терапии, начатой через 2 недели от начала заболевания, выживаемость больных составляет 100%; если лечение начинается позже 8 недель, выживаемость падает до 56% (Friedberg).
Длительность антибактериальной терапии должна составлять не менее 4-6 недель при раннем и 2-2,5 мес. при поздно начатом лечении (Г.П. Матвейков, 1995). Разумеется, сроки антибактериальной терапии индивидуальны, однако лечение должно продолжаться вплоть до клинического и бактериологического выздоровления, а по мнению А.А. Демина (1987), Ф.И. Комарова (1991) и еще 2-4 недели после этого.
Для оценки адекватности лечения проводят количественное определение чувствительности возбудителя, т.е. устанавливают минимальную подавляющую концентрацию (МПК) – самую низкую концентрацию лекарственного вещества, при которой подавляется рост возбудителя, минимальную бактерицидную концентрацию (МБК) – самую низкую концентрацию, при которой погибает 99,9% патогенных микроорганизмов, измеряют концентрацию лекарственного вещества в крови и бактерицидную активность плазмы, следят за динамикой СОЭ.
Также следует помнить о необходимости смены препаратов каждые 2-4 недели (Г.П. Матвейков, 1995), хотя некоторые авторы (Weinstein, 1984, О.А. Белокриницкая с соавт., 1995) не считают это оправданным.
Тактика антибактериальной терапии
В лечении сепсиса антибиотиками существует 3 этапа назначения препаратов.
· 1 этап – эмпирический, он соответствует тому отрезку времени, пока мы не получили заключения микробиологической лаборатории.
· 2 этап начинается с того момента, когда выделен возбудитель инфекционного процесса.
· 3 этап представляет собой назначение антибиотика согласно данным антибиотикограммы, а также определения МПК и МБК препаратов.
На современном этапе, как правило, 2 и 3 этапы совпадают, поскольку микробиологическая лаборатория выдает нам сразу результаты посева и определения чувствительности к антибиотикам. Нередко врач сознательно идет вразрез с лабораторными данными при хорошем эффекте от антибиотиков, назначенных изначально. Такая тактика, как правило, оправдывает себя, поскольку известно, что далеко не всегда in vivo препараты действуют на микроорганизмы так же, как in vitro. Поэтому, несмотря на огромную помощь, которую нам оказывают параклинические службы, решающим моментом в лечебной тактике является все же клиническая картина заболевания, правильно анализируемая врачом.
Отдельной проблемой является госпитальная инфекция, характеризующаяся полиморфизмом микроорганизмов, устойчивостью их к дезинфектантам и антисептикам. Если бичом 50-60-х годов был золотистый стафилококк, то грозой современной больницы является синегнойная палочка, клебсиелла, коагулазоотрицательные стафилококки, протей, энтеробактер, серрациа и прочие микроорганизмы, ранее относившиеся к условно-патогенным. Нет оснований для паники по поводу устойчивости этих микроорганизмов к антибиотикам. При грамотном выборе препарата и правильной тактике ведения больного мы можем рассчитывать на успех нашего лечения.
При так называемом криптогенном сепсисе, когда не удается выявить первичный очаг, необходимо руководствоваться следующей схемой.
Сепсис – тяжелое состояние, которое вызывается попаданием в кровь и другие ткани организма микроорганизмов и продуктов их жизнедеятельности (токсинов).
Отличительной особенностью этой патологии является то, что воспалительный процесс протекает не локально, а во всем организме и характеризуется тяжелым прогрессирующим течением.
Обычно сепсис является осложнением тяжелых инфекционных процессов (в том числе – артритов) или травм, сопровождающихся инфицированием.
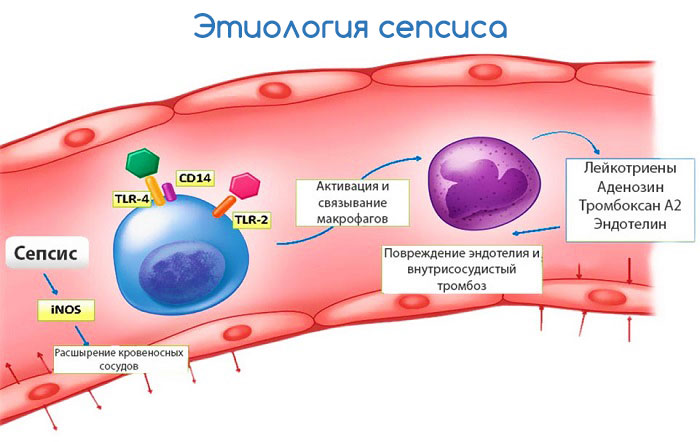
В зависимости от скорости прогрессирования симптомов заболевания, различают следующие варианты течения сепсиса:
- молниеносное (все проявления развиваются в течение 1-2 суток);
- острое (состояние прогрессирует 5-7 дней);
- подострое (длится до 3-4 месяцев);
- рецидивирующее (протекает в виде обострений и ремиссий, длится до 6 месяцев);
- хроническое (до года и более).
Молниеносные формы чаще наблюдаются у детей. У ослабленных и пожилых пациентов патология нередко протекает подостро или хронически.
Традиционно выделяют следующие виды сепсиса:
- септицемия (сопровождается возникновением очагов инфекции в различных органах и тканях);
- септикопиемия (наличие возбудителей инфекции и их токсинов в крови больного, при отсутствии очагов воспаления в органах).
Но такое деление заболевания достаточно условно. Обычно те и другие проявления в той или иной степени сочетаются.
Возбудителями сепсиса являются патогенные и условно-патогенные микроорганизмы – стрептококки, стафилококки, реже – пневмококк, кишечная палочка, менингококк, сальмонелла, энтерококк, синегнойная палочка и другие. В редких случаях, у ослабленных пациентов в условиях иммунодефицита, сходные с сепсисом состояния могут вызываться грибковой инфекцией, вирусами, простейшими.
Основными факторами риска возникновения сепсиса являются:
- иммунодефицитные состояния (как врожденные, так и приобретенные на фоне тяжелой сопутствующей патологии, применения гормональной терапии или химиопрепаратов);
- наличие тяжелых заболеваний (сахарный диабет, алкоголизм, системные заболевания соединительной ткани, новообразования и другие);
- наличие травм и хирургические вмешательства (особенно, сопровождающиеся большой площадью раневой поверхности, кровопотерей, длительной иммобилизацией);
- недостаточность питания (гипотрофия, кахексия).
В зависимости от ворот инфекции (места, через которое она проникла) различают: черезкожный, акушерско-гинекологический, сепсис вследствие хирургических вмешательств и диагностических манипуляций и другие виды сепсиса.
Источником воспаления является очаг острой или хронической инфекции в организме. Это может быть инфекционный артрит, сопровождающийся возникновением других осложнений (флегмона, остеомиелит) или без них. К сепсису также могут приводить тяжелые заболевания дыхательной (пневмония, плеврит) или нервной системы (менингит, энцефалит), желудочно-кишечного тракта (болезнь Крона, неспецифический язвенный колит), заболевания кожи (пиодермии, обширные раневые поверхности после ожогов) и другая патология.
Патогенез сепсиса связан с массивным проникновением микроорганизмов в кровь или лимфатические системы из очага воспаления. Затем возбудитель инфекции разносится по всему организму с током крови и лимфы, оседает в различных органах, вызывая образование вторичных очагов воспаления в них. С такой массивной инфекционной атакой организм не может адекватно справиться, и состояние прогрессивно ухудшается.
Если вторичные очаги воспаления крупные и их можно выявить клинически, то говорят о септицемии. Если видимых мест локализации инфекции не обнаруживается, при наличии симптомов сепсиса и нахождении возбудителя в крови, то говорят о септикопиемии. Симптомы при этих формах могут не сильно различаться, но в случае септицемии могут понадобиться дополнительные хирургические методы лечения (вскрытие очага инфекции и его санация).
В тяжелых случаях сепсис приводит к нарушению свертываемости крови (ДВС-синдрому), может развиваться шоковое состояние (инфекционно-токсический шок), полиорганная недостаточность.
Симптомы сепсиса
Если инфекция попадает в организм извне, то инкубационный период (время от момента проникновения возбудителя до появления клинических симптомов) длится от нескольких часов до нескольких дней. Если возбудитель перенесен из другого очага в организме, то длительность инкубационного периода определить сложно. 
Симптомы сепсиса могут различаться. Для него всегда характерно наличие интоксикации, а другие проявления могут различаться в зависимости от места расположения первичного и вторичных очагов инфекции. К проявлениям этой патологии будут относиться:
- интоксикация, обуславливающая тяжелое общее состояние: высокая лихорадка (чаще держится постоянная температура, но бывают и кратковременные эпизоды снижения), выраженный озноб, нарушение сознания, головные, суставные и мышечные боли, учащенное дыхание и сердцебиение (одышка и тахикардия), могут быть тошнота и рвота, нарушения стула, обезвоживание, кожа становится бледной, с землистым оттенком;
- проявления гнойного артрита (или другой инфекционной патологии, которая привела к возникновению сепсиса): отек, боль и ограничение движений в суставе;
- при образовании очагов гнойного воспаления в органах появляется характерная симптоматика, в зависимости от их локализации (например, появление очаговых неврологических симптомов бывает при поражении головного мозга) – формируются артриты, миозиты, остеомиелит, конъюнктивит, плеврит, менингит и другая тяжелая патология, может быть гнойничковая сыпь на коже;
- в наиболее тяжелых случаях – симптомы полиорганной недостаточности, нарушение свертывания крови (ДВС-синдром) и другие изменения, характеризующие наиболее тяжелое проявление данной патологии – инфекционно-токсический шок.
Подострые, рецидивирующие и хронические формы сепсиса прогрессируют постепенно. Они вначале могут проявлять себя в виде кратковременных беспричинных подъемов температуры до высоких цифр, волнообразного течения или стойкой длительной лихорадки. Постепенно присоединяются и другие симптомы.
Диагноз бывает затруднен из-за наличия проявлений другого инфекционного заболевания (например, гнойного артрита), имеющего сходные симптомы. Однако при наличии сепсиса они обычно более резко выражены.
Помимо осмотра, используются методы лабораторной и инструментальной диагностики.
В лабораторных анализах могут выявляться:
Инструментальные методы диагностики носят вспомогательный и симптоматический характер. Например, для исключения артрита проводится рентгенография, для выявления менингита – пункция спинномозговой жидкости, гнойные очаги в различных органах можно определить с помощью рентгенографии, ультразвукового исследования, магнитно-резонансной томографии.
Но основным методом для постановки диагноза сепсиса должно быть обнаружение патогенных микроорганизмов в крови (проводится бактериологический анализ – посев крови на питательные среды). Как правило, исследование повторяют неоднократно, так как возможно кратковременное нахождение микроорганизмов в крови и при отсутствии сепсиса. Часто встречаются и отрицательные анализы при наличии возбудителя в крови, что бывает на фоне антибактериальной терапии.
Лечение, профилактика и прогноз сепсиса
Терапия всегда проводится в стационаре. Обычно – в отделении реанимации.
- Массивную антибактериальную терапию, направленную на борьбу с инфекцией.
- Симптоматическое лечение: инфузионная терапия, коррекция водно-электролитных нарушений, детоксикация, обезболивающие и гормональные препараты, кислородотерапия, иммуномодуляторы, витаминные препараты и другие методы.
- Хирургическое лечение сопутствующего инфекционного артрита и других его осложнений (флегмон, остеомиелита, затеков), гнойных очагов сепсиса.
- При улучшении состояния постепенно переходят к другим методам лечения: диетическое питание для больных с инфекционными заболеваниями на стадии выздоровления, физиотерапевтические процедуры и лечебная физкультура – в зависимости от характера очагов инфекции и сопутствующей патологии.
Прогноз заболевания часто бывает неутешительным. Фактически, это терминальное состояние. Сепсис отличает тяжелое течение, прогрессирующее ухудшение и развитие шока и полиорганной недостаточности. Большую роль играет фон, на котором возникла данная патология. Особенно тяжело она протекает у ослабленных пациентов с дефектами иммунитета.
Профилактикой является своевременное и полноценное лечение очагов инфекции в организме.
Читайте также:


