Отравление фенобарбиталом у собак
Введение
Судорожные припадки обусловлены пароксизмальными синхронными разрядами нейронов, обычно возникающими в коре головного мозга.
Наиболее эффективное лечение судорожных припадков возможно только в том случае, когда поставлен диагноз.
Причины возникновения судорожных припадков перечислены в таблице 1. Первичные проявления, анамнез и клинические симптомы позволяют приоритизировать дифференциальные диагнозы и выбрать соответствующие диагностические тесты.4
Если подозревается симптоматическая или реактивная эпилепсия (например, 12-летний золотистый ретривер с припадками, появившимися впервые), рекомендуется полное диагностические обследование, включающее минимальный набор данных, тест на толерантность к желчным кислотам, визуализационные исследования головного мозга и анализ цереброспинальной жидкости. Во многих случаях полное обследование не является необходимым при первом появлении припадков (например, в остальном здоровая 3-летняя немецкая овчарка с недавно появившимися припадками), однако всегда рекомендуются получение минимального набора данных, проведение теста на толерантность к желчным кислотам и офтальмоскопия. Тест на толерантность к желчным кислотам не только исключает портосистемный шунт, но и является исходной мерой функции печени, которую можно использовать впоследствии, если животному будут назначены гепатотоксические препараты, например фенобарбитал.
Всем владельцам животных можно выдать список симптомов, за которыми нужно следить и которые могут свидетельствовать о причинном заболевании головного мозга (изменения в поведении, спотыкание, нарушения зрения) и поэтому требуют более развернутого диагностического обследования.
Судорожные припадки являются наиболее частым и, как правило, единственным симптомом, свидетельствующим о наличии опухоли головного мозга.
Поэтому исключительно важно рекомендовать визуализацию мозга посредством компьютерной томографии (КТ) или магнитно-резонансной томографии (МРТ) любой собаке старше 6 лет с судорожными припадками, появившимися впервые. Некоторые породы предрасположены к специфическим болезням, следовательно, первичные симптомы также будут определять рекомендации. Например, впервые появившиеся судорожные припадки у 4-летнего боксера с большей вероятностью обусловлены опухолью головного мозга, чем первичной эпилепсией. Сходным образом первое появление припадков у 2-летнего мопса, вероятнее всего, является результатом энцефалита. Кошки более чувствительны к гипертензии и ее последствиям, чем собаки, но у обоих видов животных важно попытаться измерить кровяное давление и исследовать сетчатку на наличие признаков сосудистого или иного заболевания.
Большинство судорожных состояний вызывают рецидивирующие припадки, которые по природе являются прогрессирующими из-за постепенного включения дополнительных нейронов в судорожные очаги (киндлинг-эффект). Если первопричина припадков может быть идентифицирована, то лечение должно быть направлено на эту причину. Применение противоэпилептических средств показано, если поставлен диагноз первичной эпилепсии или если лечение первопричины припадков при вторичной эпилепсии не обеспечивает контроль припадков (например, у животных с опухолями головного мозга, гидроцефалией или энцефалитом). До начала лечения важно определить частоту припадков, поскольку противоэпилептические средства имеют побочные эффекты и не всегда являются необходимыми. Например, если лечение припадков начато после первого припадка, то уже никогда не будет ясно, был ли этот припадок единственным, и трудно определить, можно ли прекратить лечение или нет. Исключением из этого правила являются случаи, когда диагноз поставлен и дальнейшие припадки могут угрожать жизни животного. Например, если у животного был один припадок и диагностирована опухоль головного мозга, то последующие припадки могут вызвать фатальное повышение внутричерепного давления, и пациенту следует немедленно назначить противоэпилептические средства.
Общее эмпирическое правило состоит в том, что припадки следует лечить, если они возникают чаще, чем раз в месяц, если они возникают кластерами или сочетаются с эпилептическим статусом, или если они сопровождаются неприемлемыми побочными эффектами (например, исключительно длительным послесудорожным периодом, злобой или обструкцией дыхательных путей у брахицефальных пород собак).
Во всех случаях наиболее эффективное лечение животного требует полного понимания и согласия его хозяина, поэтому до начала лечения важно определить ожидания владельца.
Какой лекарственный препарат использовать у собак
Для лечения судорожных припадков у собак исторически использовали два лекарственных препарата – фенобарбитал и бромид калия. Оба лекарства эффективны как по отдельности, так и в комбинации. Примидон не рекомендован из-за его гепатотоксичности, а диазепам не является эффективным оральным противоэпилептическим средством из-за его короткого периода полувыведения у собак. Период полувыведения фенобарбитала составляет от 48 до 72 часов, и его следует давать перорально два раза в день. Стартовая доза равна 2–4 мг/кг перорально два раза в день, и постоянный уровень препарата в крови достигается за 10–14 дней. Если необходимо быстрое прекращение припадков (например, у собаки болезнь начинается с кластерных припадков), введение дозы, равной 12 мг/кг и распределенной на 24–48 часов, обеспечит терапевтические уровни фенобарбитала в крови, хотя эта доза вызовет временную седацию.
Преимуществами фенобарбитала являются хорошая эффективность, доступность, разумная цена, удобный режим дозирования и быстрота, с которой изменения дозы отражаются в концентрациях в крови, что обеспечивает легкость регулирования дозы.
Недостатками являются необходимость ведения документации (это контролируемый лекарственный препарат), полифагия, полиурия/полидипсия, первоначальная седация (должна пройти примерно через неделю) и седация при необходимости более высоких концентраций препарата в крови, гепатотоксичность (чаще всего связанная с концентрациями в крови, превышающими 35 мкг/мл), нейтропения и тромбоцитопения (очень редкое осложнение), некролитический дерматит и взаимодействие с другими лекарственными препаратами (не следует использовать совместно с циметидином, хлорамфениколом или кетоконазолом). Может развиться толерантность к фенобарбиталу, которая с течением времени потребует более высоких доз для поддержания того же уровня в крови. Терапевтические концентрации в крови лежат в диапазоне 15–45 мкг/мл, хотя концентрации, превышающие 35 мкг/мл, связаны с повышенным риском гепатотоксичности. После достижения стабильного состояния изменения дозы, необходимые для достижения желаемого уровня в крови, можно рассчитать с использованием следующего уравнения: новая доза = текущая доза × желаемый уровень в крови / измеренный уровень в крови. Необходимая доза определяется частотой припадков, концентрацией препарата в крови и тяжестью имеющихся побочных эффектов. Состояние собак, получающих лечение фенобарбиталом, следует контролировать через каждые 6–12 месяцев посредством физикального обследования, измерения концентраций фенобарбитала в крови и биохимического профиля с целью выявления признаков гепатотоксичности. При внезапном резком возрастании концентраций ферментов печени (ожидаемым является их умеренное возрастание при лечении фенобарбиталом) или снижении концентрации альбумина необходимо провести дополнительное исследование в форме теста на толерантность к желчным кислотам.
Следует отметить, что резкое прекращение лечения припадков (фенобарбиталом или бромидом калия) может привести к фатальному эпилептическому статусу или рецидиву припадков, которые гораздо труднее контролировать.
Бромид калия с большим успехом использовали как дополнение к терапии фенобарбиталом у собак с устойчивыми к лечению припадками. В настоящее время его все чаще используют как единственное средство при лечении собак. Бромид калия имеет длительный период полувыведения, колеблющийся в диапазоне от 24 до 46 дней, в зависимости от содержания соли в пищевом рационе и функции почек. Его следует давать один раз в день в дозе, равной 25–40 мг/кг/день, и постоянный уровень в крови достигается через 3–4 месяца. Для более быстрого достижения терапевтических концентраций в крови (100–300 мг/дл) можно нагружать животное этим препаратом в дозе, равной 100–130 мг/кг/день, в течение 5 дней, после чего снизить дозу до поддерживающей, равной 30 мг/кг. Концентрацию в крови следует проверить после 5-дневного применения нагрузочной дозы и через 4–6 недель, чтобы убедиться в том, что терапевтические уровни сохраняются. В экстренных случаях терапевтические уровни могут быть достигнуты за один день посредством орального введения 200 мг/кг с небольшим количеством корма с 2–3-часовыми интервалами (общая доза равна 600 мг/кг).
Преимуществами бромида калия являются хорошая эффективность, особенно при использовании дополнительно к терапии фенобарбиталом, отсутствие гепатотоксичности, дозирование один раз в день, разумная цена и отсутствие статуса контролируемого лекарственного средства.
Недостатками являются полиурия/полидипсия и полифагия, седация и слабость задних конечностей при высоких концентрациях в крови (в частности, в сочетании с фенобарбиталом), отсутствие разрешения на использование в ветеринарии, необходимость постоянного пищевого рациона (изменения содержания соли в пищевом рационе изменяют концентрации препарата в крови), раздражение желудочно-кишечного тракта, состояние кожи, называемое бромодермой, и возможная связь с гиперлипемией и панкреатитом. Бромид калия имеется в продаже в жидкой форме и в форме капсул. Считается, что капсулы с большей частотой вызывают побочные эффекты со стороны желудочно-кишечного тракта, поскольку растворение капсулы обеспечивает фокусирование солевого раствора внутри желудка. Раздражение желудочно-кишечного тракта можно минимизировать посредством дачи лекарства с кормом.
Принимая решение о начале лечения фенобарбиталом, бромидом калия или комбинацией обоих препаратов, следует учесть несколько факторов. Например, если собака очень молодая, то желательно начать лечение бромидом калия, а фенобарбитал добавить только в случае необходимости, чтобы минимизировать время, в течение которого собака получает гепатотоксический препарат. Если заболевание впервые проявилось в форме кластера тяжелых припадков, обычно предпочтительно сразу же начать лечение животного фенобарбиталом, поскольку в этом случае можно быстрее достичь постоянных концентраций в крови, а препарат можно вводить внутривенно. Если владелец животного не может давать препарат через каждые 12 часов, то препаратом выбора может быть бромид калия, поскольку его можно давать через каждые 24 часа. Наконец, следует учитывать побочные эффекты препаратов, и собак с заболеванием печени не следует лечить фенобарбиталом, тогда как использования бромида калия лучше избежать при лечении собак с панкреатитом в анамнезе.
В последнее время в США и Европе более доступными стали препараты Леветирацетам (Кеппра) и Зонисамид (Зонегран), которые можно добавлять к бромиду калия и фенобарбиталу или использовать вместо них.
Зонисамид (Зонегран) – это производное сульфонамида, которое впервые было использовано в Японии в 1989 г. Он лицензирован в Соединенных Штатах Америки с 2000 г., однако дженерики появились только в последнюю пару лет. Механизм действия еще не полностью выяснен, однако, по-видимому, он абсолютно иной, нежели у фенобарбитала и бромида калия. Известно, что он блокирует возбуждающие натриевые и кальциевые каналы, предполагалось, что он является ингибитором карбоангидразы (хотя это не считается важным механизмом регулирования судорожных припадков) и влияет на синтез и распад нейромедиаторов. Он метаболизируется печенью (не через цитохром Р450) и имеет достаточно длительный период полувыведения, равный 18–28 часам, так что его можно давать собакам два раза в день – большое преимущество перед многими другими лекарствами, которые нужно давать чаще.
В исследованиях собак, проведенных в Японии, были определены дозы, необходимые для достижения концентраций в крови, признанных терапевтическими, и было показано, что подходящей стартовой дозой для животных, не получающих фенобарбитал, является доза, равная 5 мг/кг два раза в день, тогда как животным, получающим фенобарбитал, необходима доза, равная 10 мг/кг два раза в день. Дозу можно повышать достаточно безопасно; в исследованиях хронической токсичности для собак дозы до 75 мг/кг/день использовали в течение года с минимальными эффектами на аппетит и массу тела.
Побочные эффекты, отмеченные у собак, которых одновременно лечили дополнительными противоэпилептическими средствами, включали атаксию (реагировавшую на снижение дозы), летаргию и рвоту. Недавно у нас был случай, в котором, по-видимому, развилась идиосинкразическая гепатотоксичность, которая разрешилась после прекращения приема препарата. Опубликованы два исследования клинической эффективности зонисамида как дополнительного средства при лечении стойкой эпилепсии у собак, и в обоих случаях были получены впечатляющие реакции со снижением припадков у 58 % и 82 % собак. Однако эти исследования не были контролируемыми и включали относительно малое количество пациентов. Благодаря безопасности, доступности и практичности дозирования (два раза в день) этот лекарственный препарат в настоящее время является препаратом первого выбора для лечения собак с первичной эпилепсией. Хотя в настоящее время еще нет данных относительно его эффективности при использовании в качестве единственного средства, эти данные, по-видимому, появятся в течение следующих нескольких лет. Базовые концентрации в крови взяты из опубликованных данных, полученных у людей, и определены как 10–40 мкг/мл; концентрации в крови могут быть измерены в лаборатории фармакологии Колледжа ветеринарной медицины Обернского университета, но это довольно дорогостоящая процедура. Однако относительная безопасность данного лекарственного препарата делает мониторинг его концентраций в крови менее критичным, чем при использовании таких препаратов, как фенобарбитал. Мы обычно измеряем концентрацию в крови в том случае, если судорожные припадки плохо контролируются, а доза является высокой: это полезно для того, чтобы определить, поможет ли дальнейшее повышение дозы.
Фармакокинетика и токсичность зонисамида также была исследована на кошках, и, хотя препарат показал себя как безопасный, все же в этом случае нельзя повышать дозы так же, как у собак: примерно у половины кошек, получавших 20 мг/кг/день, развивались летаргия и атаксия, а также симптомы со стороны желудочно-кишечного тракта, такие как анорексия, рвота и диарея. Период полувыведения равен 33 часам, и рекомендована доза, равная 5–10 мг/кг один раз в день.4
Концентрации леветирацетама в плазме могут быть измерены в фармакологической лаборатории в Оберне за ту же цену, что и в случае зонисамида, однако отсутствие побочных эффектов делает эти измерения менее критичными. Кроме того, у людей не было отмечено четкой взаимосвязи между концентрацией в плазме и терапевтическим эффектом. Несмотря на то что препарат обычно применяют в виде дополнительной терапии в устойчивых к лечению случаях, основными препятствиями к его использованию являются неудобство дозирования (три раза в день), а также, как и в случае зонисамида, отсутствие в настоящее время данных о его эффективности в качестве единственного средства.
Леветирацетам использовали для лечения кошек.7 Период его полувыведения равен 3 часам, рекомендованная доза была равна 20 мг/кг три раза в день.
Семь из 10 кошек с устойчивой к лечению эпилепсией ответили на лечение леветирацетамом, и лишь у двух возникли побочные эффекты в виде летаргии и снижения аппетита.
Пациентам с острыми психоэмоциональными расстройствами, в качестве успокоительных и снотворных средств, назначаются барбитураты, производные барбитуровой кислоты. Лекарства действуют методом общего угнетения нервной системы, без ориентации на точечные рецепторы. Не выборочный принцип воздействия барбитуратов допустим в минимальной дозировке, при неэффективности стандартных методик. Фактически, препараты, на основе барбитуровой кислоты – наркотик. Отравление фенобарбиталом (производное C₄H₄N₂O₃) аналогично наркотической интоксикации, с угрозой тяжёлых последствий.
Характерные признаки интоксикации
Фенобарбитал назначают пациентам с эпилептическим синдромом, в состояниях глубокой депрессии, при расстройствах сна. Обладает противосудорожным и седативным эффектом. Допустимая дозировка 10-100 мг (в зависимости от назначения), отпускается только по рецепту врача.
Препарат относится к снотворным средствам длительного действия. Эффект ощущается спустя 1,5-2 часа, продолжается в течение 10-13 часов. После поступления в организм проникает в плазму, распределяется по органам и тканям, угнетает работу дыхательной системы, реакцию нервных рецепторов мозга. Спустя сутки внешние симптомы проходят, но концентрация вещества в организме сохраняется 72 часа.
Если принимать фенобарбитал 1–2 раза в сутки, остатки снотворного накапливаются, постепенно наращивая интоксикационный эффект. Результат длительного приёма проявляется в виде седационного состояния, превышение дозы провоцирует глубокий наркоз. Развивается лекарственная зависимость, угнетающая психические и соматические функции.
Симптомы отравления проявляются постепенно, в зависимости от дозировки и длительности курса. При ежедневном приёме фенобарбитала, с дозировкой больше 100 мг в сутки, нарушения развиваются на 5–7 день.
- апатия;
- раздражительность;
- головокружение;
- спутанная речь;
- замедление реакции на звуки, действия;
- нарушение координации движений;
- сонливость;
- медленное моргание.
Возможно появление галлюцинаций, резкая перемена настроения – с апатии на нервное возбуждение, истерики. У пациентов с заболеваниями сердечно-сосудистой системы развивается дыхательная недостаточность, с последующими паническими атаками. В 41% случаев последствия — расстройства желудочно-кишечного тракта (боли, запор, диарея), застой мочи.
- атаксический синдром – стойкое нарушение координации;
- спутанность сознания, потеря адекватности восприятия;
- сильная головная боль;
- снижение выделения мочи, при норме питья;
- падение артериального давления (ниже 80/50);
- синюшность кожных покровов;
- беспорядочное движение зрачков;
- бессмысленная речь;
- тахикардия;
- расстройство дыхания (частота увеличивается, затем резко падает, не хватает воздуха).
При передозировке фенобарбитала, глаза широко открыты, контролировать движение глазных яблок пациент не может. Зрачки сужаются, постепенно спадает пульс, дыхание. На кожных покровах появляется геморрагия – подкожное кровоизлияние. Необходимо определять риски летального исхода.
Смертельная доза
В случаях хронического и острого отравления фенобарбиталом, больной остаётся в сознании, при нарушенном восприятии. Как правило, состояние диагностируется при суточной дозировке от 500 мг, осложняется во время приёма больше 5–7 дней. Учитывая остаточное скапливание фенобарбтала в органах и тканях, количество вещества в организме увеличивается ежедневно. Острая стадия проявляется при концентрации 500–1000 мг.
Однократный приём 2–8 грамм фенобарбитала – смертельная доза препарата. В течение 2–3 часов симптомы не проявляются, затем следует острая, быстропрогрессирующая интоксикация организма, с отказом функций органов.
Последствия
- Отёк лёгких – в связи с проникновением транссудата из сосудов в ткань органа;
- Апноэ;
- Острая сосудистая недостаточность;
- Аритмия;
- Инфаркт миокарда;
- Эмболия лёгочной артерии;
- Застойная сердечная недостаточность;
- Остановка сердца.
Электрическая активность мозга отключается, больной впадает в состояние глубокого наркоза. При одновременном течении гипоксического синдрома, клетки мозга отмирают в течение 4–5 часов, развивается необратимая кома.
Отёк лёгких сопровождается удушьем, кашлем с кровяной мокротой. При смертельной дозе фенобарбитала, течёт в острой форме, нарастает быстро. Без реанимационных мероприятий, через 4–6 часов, следует фатальный исход, в результате апноэ.
В результате воздействия вещества на сосудистую ткань, происходит стремительное расширение капилляров, при недостатке кровотока. Из-за снижения тонуса сосудов, развивается гипоксия органов, пациент теряет сознание. Состояние провоцирует сердечную недостаточность – аритмия, инфаркт, эмболии, остановка сердца.
При однократном приёме смертельной дозы фенобарбитала, риск летального исхода составляет 63%. Ведущая причина смертности – несвоевременная реанимационная терапия.
Первая помощь при остром отравлении
При появлении признаков отравления фенобарбиталом, даже при удовлетворительном состоянии больного, необходимо вызвать неотложку. Госпитализация требуется в 100% случаев. До приезда врачей требуется оказать первую помощь.
- Положить больного набок;
- Вызвать рвоту;
- После очищения желудка, принять сорбенты – активированный уголь, полисорб, сорбекс;
- Очистить ротовую полость от остатков вещества;
- Проветрить помещение;
- Сделать искусственное дыхание (при отсутствии сознания).
Для промывания желудка, необходимо 800 мл воды, с добавлением 2-3 кристаллов марганцовки. Жидкость принимается в 4–5 заходов, по 150–200 мл. После приёма дозы воды, нужно надавить на прикорневую область языка, до появления рвотных рефлексов. Через 15 минут процедуру повторить. Продолжать до тех пор, пока из желудка не начнёт выходить чистая вода.
После очищения принять сорбенты, для впитывания остатков вещества. Ротовую полость очистить ватным тампоном, смоченным водой.
Если больной без сознания, рвоту вызывать нельзя. Его необходимо положить набок, для избежания застоев непроизвольной рвоты в носоглотке.
Фенобарбитал вызывает удушье, поэтому требуется впустить поток свежего воздуха. Если у окружающих есть навыки оказания первой медицинской помощи, привести больного в сознание поможет искусственное дыхание и непрямой массаж сердца.
Дальнейшие действия не предпринимаются до приезда бригады скорой помощи. Лечение проводится в условиях стационара под наблюдением врачей.
Антидот и лечение
В стационаре больному проведут инкубацию трахеи, так как риск остановки дыхания при отравлении фенобарбиталом очень высокий. При необходимости подключается аппарат искусственной вентиляции лёгких. Назначается антидот – бемегрид, снижающий токсичное воздействие фенобарбитала. Терапия блокирует барбитураты, стимулирует ЦНС, кровообращение, восстанавливает дыхание.
Дальнейшее лечение направлено на снятие острых симптомов, выведение токсинов из организма, восстановление функций органов. Проводят процедуры по очищению, в случае необходимости, переливанию крови.
- антидот;
- мочегонные препараты;
- сорбенты;
- для восстановления притока кислорода – пирацетам, мексидол, витамины группы В, винпоцетин;
- солевые слабительные;
- форсированный диурез;
- перитониальный диалез;
- восстановление и контроль АД;
- антибиотики широкого действия (при подозрении пневмонии)- цефалоспорины, фторхинолоны;
- сосудосуживающие препараты – Диазоксид, Эналаприлат;
- профилактика пролежней, застойной пневмонии.
Необходимо ежедневно контролировать содержание фенобарбитала в крови. Пациенту требуется антиаспирационная терапия – кварцевание, проветривание помещения, промывание носа, вибрационный массаж грудной клетки. Рекомендовано чаще ходить, разминаться, переворачиваться с бока на бок, ежечасно откашливать мокроту.
При благоприятном течении, пациент выписывается через 10–14 дней, с назначениями врача. Для устранения синдрома хронической интоксикации, рекомендовано постепенное снижение дозы препарата, до полной отмены (замены). Положительный лечебный эффект даст психотерапия.
Совместимость с алкоголем
Сочетание фенобарбитала с этилосодержащими средствами недопустимо. Провоцируется скоротечность угнетения ЦНС, индекс рисков увеличивается в 3 раза. Тяжёлая интоксикация развивается в течение 0,5-2 часов, в зависимости от дозировки препарата.
Также исключается взаимодействие с алкоголем, если барбитураты принимаются курсом, в допустимой дозе. Приём спиртного, даже через 3 дня после окончания терапии, вызовет интоксикацию с последующими осложнениями. В зависимости от количества выпитого, симптомы проявляются ярко или не выражено внешне. Но отравление органов и угнетение рецепторов мозга происходит в 100% случаев.
При появлении признаков отравления, необходимо промыть желудок, принять сорбент, вызвать скорую помощь. Госпитализация пациента, при совмещённом отравлении алкоголем и фенобарбиталом обязательна. Терапия проводится в стандартном режиме – назначение противоядия, профилактика лёгочной недостаточности, очищение крови, поддержание АД, мочегонные, слабительные препараты.
Приверженцы успокоительных средств – Корвалола, Валокордина, Барбовала должны помнить, что данные лекарства содержат фенобарбитал. На первый взгляд, безобидные средства, при неправильном приёме, провоцируют развитие тяжёлых хронических заболеваний. Именно поэтому препараты во всём мире отпускаются только по рецепту врача.

Центр по изучению мелких животных, Великобритания
• Эпилептический статус — очень опасное заболевание. Для его успешного лечения требуется незамедлительная комплексная терапия, направленная как на купирование припадков, так и на ликвидацию системных нарушений, вызванных патологией.
• Своевременное выявление и устранение причин припадков имеет особенно важное значение при лечении эпилептического статуса.
• Наиболее распространенные лекарственные препараты, применяемые при терапии эпилептического статуса — диазепам, фенобарбитал, бромид калия, пентобарбитал и пропофол.
Эпилептический статус (ЭС) — состояние, характеризующееся частыми и длительными судорожными припадками. ЭС встречается как у собак, так и у кошек. Обычно ЭС развивается как осложнение других заболеваний. Частота наблюдений ЭС в ветеринарной медицине не фиксировалась. Однако у собак, по данным литературы, ЭС и фокальные судорожные припадки отмечаются примерно у 0,44% от общего числа больных животных, приведенных к ветврачу.
ЭС можно определить, как частые судорожные припадки, продолжающиеся свыше 30 минут (или как 2 или более следующих друг за другом припадков, в промежутках между которыми животное полностью в сознание не приходит). Животному требуется оказать помощь до истечения 30 минут с момента начала припадка. Практически все типы припадков могут стать длительными или повторяющимися (а, следовательно, требующими более тщательного лечения, чем единичный припадок).
При ЭС необходимо немедленное лечение, поскольку это состояние может привести к необратимым неврологическим нарушениям и даже к смерти пациента. Кроме того, по данным литературы при раннем агрессивном лечении затянувшегося припадка не только удается его быстрее купировать, но и применить меньшие дозировки препаратов. При такой терапии существенно возрастает и шанс па успех последующего длительного лечения. Если своевременная помощь животному во время припадка не оказана, у него развиваются глубокие нарушения гемодинамики и метаболизма, которые могут привести летальному исходу. Несвоевременное же применение противосудорожных средств может еще более углубить имеющиеся нарушения гемодинамики. Таким образом, лечение при ЭС должно быть своевременным, комплексным, осуществляться в динамике и с применением индивидуального подхода в каждом конкретном случае в зависимости от имеющейся клинической симптоматики.
Обязательный компонент терапии ЭС — быстрое прерывание припадка и стабилизация состояния животного. Быстрое распознавание и лечение факторов, провоцирующих припадки, например, менингоэнпефалита или гипогликемию, позволяет предупредить дальнейшее повреждение нейронов. Для прерывания припадка часто применяются препараты из группы бенздиазепинов, например, диазепам. Они весьма эффективны, но их действие носит кратковременный характер. Для более длительной противосудорожной терапии предпочтительнее использовать фенобарбитал. Лечение особо устойчивых припадков обычно требует комплексного применения пентобарбитала или пропофола.
В данном обзоре рассмотрены причины и последствия ЭС у домашних животных, а также способы лечения этого состояния в условиях стационара. Речь пойдет, в основном, о характерных для ЭС тонико-клонических припадках, поскольку именно они обычно наблюдаются на практике и наиболее часто приводит к смерти животного.
Хотя ЭС является патологией центральной периной системы, при развитии заболевания наблюдаются глубокие патофизиологические сдвиги в функциях почти всех органных систем организма. Эти сдвиги в значительной степени и определяют гибель пациентов при ЭС. В патогенез ЭС вовлечено много различных факторов, но исход состояния определяется, в основном, постоянным системным стрессом вследствие непрекращающихся припадков и развивающихся повреждений нейронов. Взаимосвязь между этими факторами и их относительный вклад в патогенез ЭС были исследованы в моделях этого заболевания па животных. Из результатов исследований вытекает, что вероятность прерывания припадка и непрерывного повреждения нейронов определяется характером заболевания, вызвавшего ЭС, и длительностью его протекания.
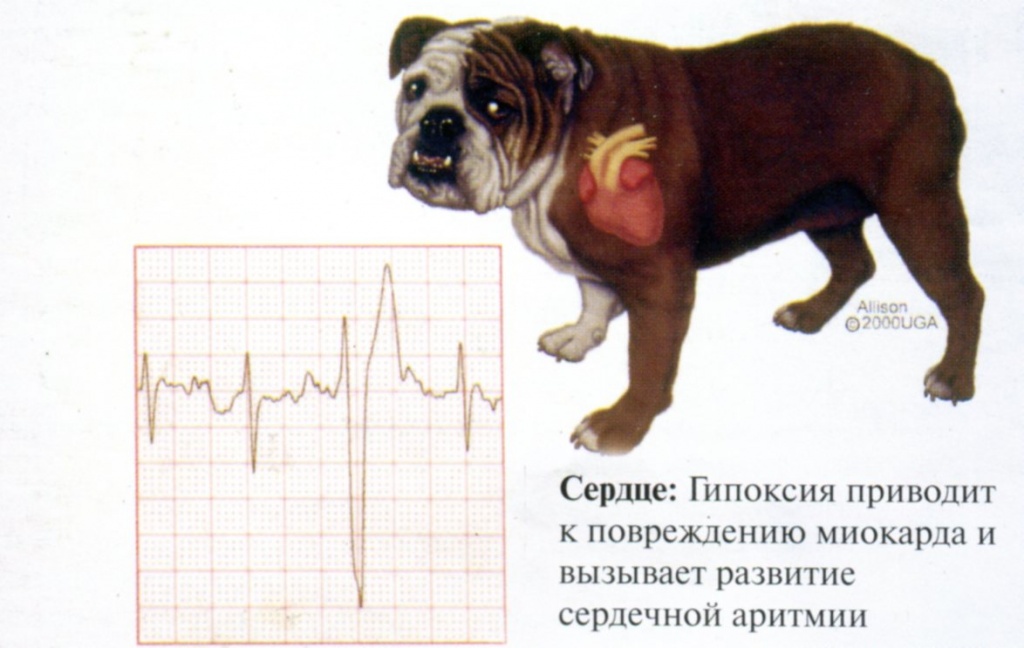
Рисунок 1. В начале припадки наблюдается нарушение сердечного ритма, проявляющееся в виде тахикардии. Однако в дальнейшем из-за гипоксии, ацидоза и угнетения функции миокарда появляется аритмия.

Рисунок 2. Из-за длительных мышечных сокращений у пациента может развиться гипертермия, приводящая к рабдомиолизу.
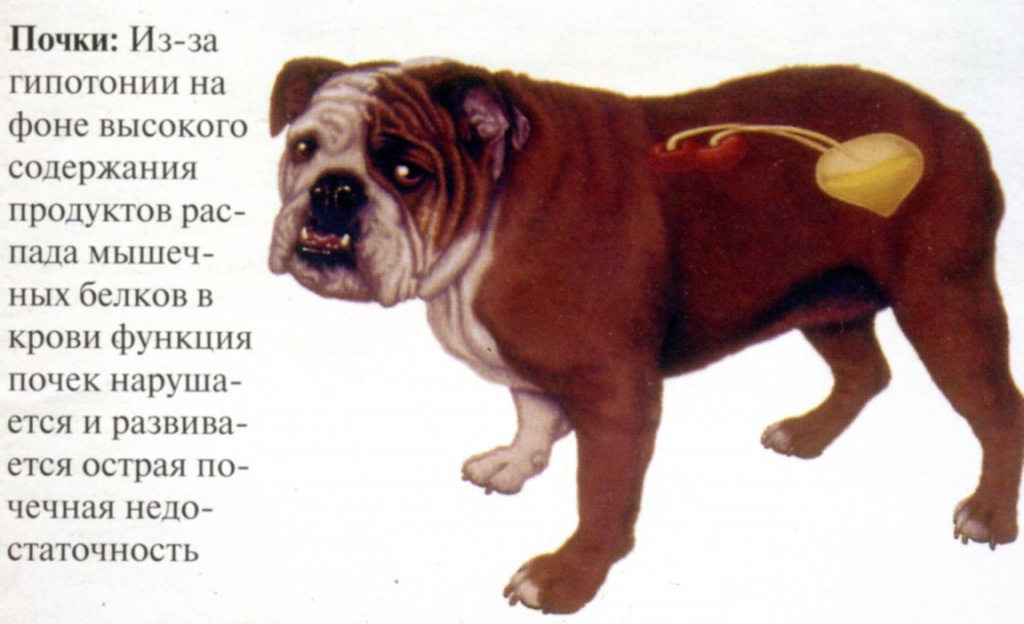
Рисунок 3. Из-за системной гипотонии и большого содержания продуктов распада мышечных белков в крови может развиться острая почечная недостаточность.
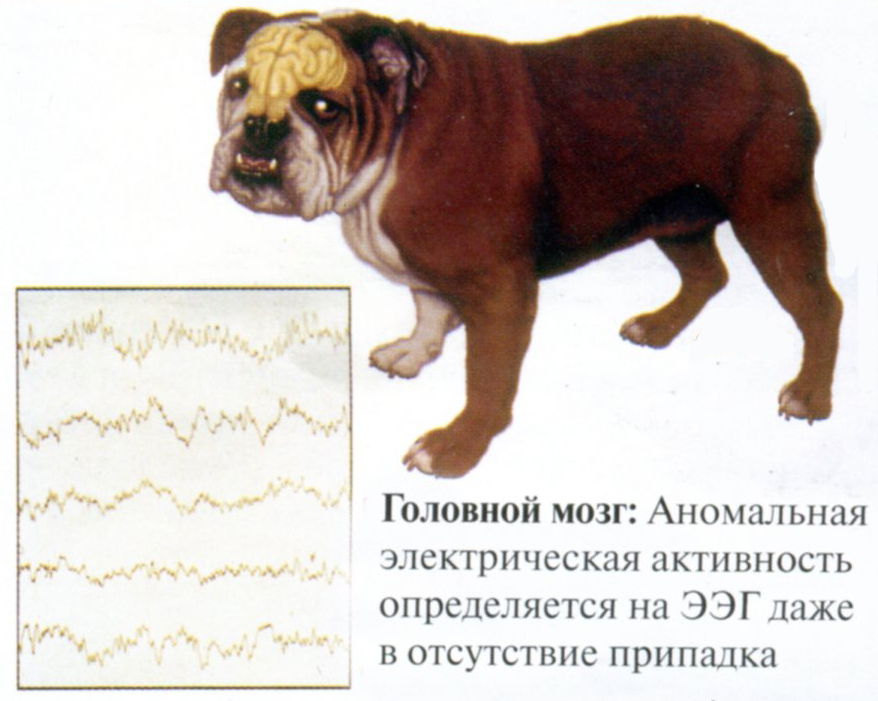
Рисунок 4. Даже в отсутствие внешних признаков припадка на ЭЭГ при эпилептическом статусе, легко заметны зоны аномальной активности коры головного мозга.
На ранних стадиях развития ЭС сопровождается нарушениями в периферической нервной системе, проявляющимися в тахикардии, гипертонии, гипергликемии (Рисунок 1). Повышение системного артериального давления приводит к существенному увеличению объема кровотока через головной мозг. Эта компенсаторная реакция направлена на удовлетворение возрастающих метаболических потребностей чрезмерно активной нервной ткани. Если припадок не прекращается, примерно через 30 минут развивается срыв адаптации и наблюдается резкое падение артериального давления. В это же время развиваются гипогликемия, гипотермия и гипоксия. Из-за срыва регуляции кровообращения кровоток через мозг становится зависимым от артериального давления, и в условиях несоответствия кровоснабжения метаболическим запросам мозга, может произойти необратимое повреждение нервной ткани. Помимо повреждения нервной ткани при длительном судорожном припадке вследствие непрерывных сокращений и нарушения дыхания развиваются метаболические отклонения в скелетной мускулатуре, приводящие к высвобождению в кровь большого количества молочной кислоты, ацидозу, гиперкалиемии, гипоксии, повышению содержания углекислоты в крови и гипертермии (Рисунок 2). Выход в кровь большою количества миоглобина и развитие миоглобинурии на фоне сниженного системного артериального давления может сильно нарушить функцию почек пациента (Рисунок 3).
Неотъемлемая часть патогенеза ЭС — нарушение механизмов, обеспечивающих самопрерывание припадка и переводящих нервную систему в рефрактерное состояние, при котором развитие новою припадка невозможно. Из-за нарушения этих механизмов при ЭС новый припадок развивается на фоне неполного восстановления функции нервной системы от повреждений, вызнанных предыдущим припадком. Показано, что многие нейроны головного мозга обладают спонтанной спайковой активностью. В отдельных группах нейронов спонтанная активность нейронов синхронизирована и ритмизирована. Припадок обычно развивается вследствие нарушения в прилегающих к данным нейронным группам нервных клетках баланса между возбуждением и торможением. По сути своей припадок — это синхронизированное возбуждение целой группы нейронов с повышенной чувствительностью к активирующим факторам (Рисунок 4) (4).
В развитии припадка принимают участие несколько нейромедиаторов. Критическим модулятором функции нейронов в головном мозге в данном случае является у-аминомасляная кислота (ГАМК). Воздействуя на постсинаптические мембраны нейронов гиппокампа, она вызывает развитие тормозных постсинаптических потенциалов, противостоящих возбуждающим импульсам, приходящим в эти нейроны из других участков мозга. В настоящее время появляется все больше доказательств того, что именно сбой ГАМК-эргической регуляции и является основной причиной возникновения припадка на молекулярном уровне. Однако при ЭС существенной частью патогенетических механизмов (как уже указывалось выше) является нарушение механизмов прерывания отдельного припадка, которое происходит либо вследствие очень сильного возбуждения, либо вследствие недостаточно эффективного торможения (3). Можно полагать, что в каждом конкретном случае ведущую роль играет свой фактор, определяемый причиной припадков. Специальные исследования показали, например, что при длительных припадках может произойти существенное нарушение функции рецепторов ГАМК на мембранах нейронов. Эти нарушения — следствие метаболических сдвигов в повторно возбуждающемся нейроне, усиливающих стимулируемое глутаматом возбуждение и блокирующих ГАМК-зависимое ингибирование. Изложенная теория получила название гипотезы повреждения нейронов вследствие токсического перевозбуждения (4). При больших концентрациях кальция в среде его ионы могут проникать в цитоплазму нейронов. Повышение концентрации ионов кальция в цитоплазме запускает целый каскад внутриклеточных нейрохимических механизмов, приводящих клетку к гибели. К нейротоксичпым соединениям, высвобождающимся при ЭС. относятся аспартат. свободные жирные кислоты, арахидоновая кислота, а также свободные радикалы.
Этиология и исход ЭС
В последнем исследовании показано, что при обращении в ветклинику владельцев собак по поводу эпилептических припадков у их питомцев, первичную причину заболевания не удается установить примерно в 25,8% случаев (6) (Таблица 1). Приблизительно 27% случаев заболевания классифицируются как первичная эпилепсия наследственного или идиопатического характера. У 35% животных эпилептические припадки являются вторичным проявлением другого заболевания — эпилепсия у них приобретенная, вторичная. В 7% случаев наблюдаются реактивные эпилептические припадки (6). При реактивной эпилепсии значимых нарушений в структуре головного мозга не выявляется, а причиной припадков являются интоксикация, системные, метаболические или гормональные заболевания (7). Одним из хронических заболеваний, при которых может развиться ЭС. является эпилепсия. При ее наличии ЭС может развиться как при попытке прервать припадок, так и при внезапном прекращении приема противосудорожных препаратов. В ходе вышеупомянутого исследования у 6% собак с ЭС в крови была выявлена аномально низкая концентрация таких препаратов, что и явилось непосредственной причиной развития ЭС. Автор публикации недавно завершил обследование, проводившееся на группе из 50 собак с генерализованной конвульсивной формой ЭС (8). У 28% этих животных в анамнезе была первичная эпилепсия, у 32% — эпилепсия носила вторичный характер, а у 12% — эпилепсия была реактивной. В 28% случаев причину развития ЭС выявить не удалось. У 36% собак с ЭС (12 из 33), наблюдались отклонения в составе спинномозговой жидкости (СМЖ). В группе собак с фокальными припадками такие отклонения наблюдались в 73,5% случаев (у 75 животных из 120 обследованных).
Данных по смертности собак с ЭС пет. Это в большой степени связано с тем. что многие владельцы больных животных предпочитают усыплять своих питомцев. У людей, по данным литературы, смертность от ЭС варьирует от 3 до 22%. Одна из причин — смертность собственно от ЭС в ветеринарной медицине не установлена — сложность интерпретации причины гибели животного при наличии у него многих заболеваний, которые могут привести к развитию ЭС. Поданным автора у 46% животных с ЭС при проведении магнитно-резонансного обследования или рентгеновской компьютерной томографии выявляются отклонения в структуре головного мозга.
Устранение причин ЭС
Во многих случаях ЭС развивается у животных, ранее страдавших хроническими эпилептическими припадками. К сожалению, точной оценки частоты таких случаев в ветеринарной медицине нет. Другие заболевания, приводящие к развитию ЭС — это опухоли, системные инфекционные поражения центральной нервной системы, травмы, метаболические отклонения (например, электролитный дисбаланс) и нарушения кровообращения.
С учетом вышеизложенного при первичном осмотре пациента с ЭС прежде всего нужно обследовать его череп и позвоночник на предмет наличия недавних травм. Голову и позвоночник следует аккуратно пальпировать. Признаками травмы являются крепитация, болезненность, асимметрия. При лабораторном тестировании, кроме обычных показателей, следует определить содержание в крови глюкозы, натрия. кальция, а также активности ферментов печени и показатели функции почек. Необходимо также определить активность ацетилхолинэстеразы в сыворотке крови. Нужно отметить, что в течение некоторого времени сразу после припадка из-за гипоксии и гипотензии активность ферментов печени в крови у животного может быть повышена. Если есть основания предполагать, что причиной ЭС является гипогликемия (или если нет возможности определить концентрацию глюкозы в крови животного), следует ввести пациенту внутривенно в течение 15 минут 50% раствор глюкозы (желательно предварительно разбавить его до 25%) в дозе 0.5 г/кг веса (8). Если установлено, что до развития ЭС животному давали фенобарбитал или другие противосудорожные препараты, желательно определить концентрацию этих препаратов у него в крови. При подозрении на энцефалит нужно сделать анализ спинномозговой жидкости (СМЖ) сразу же после выведения пациента из припадка и стабилизации его состояния. Применение глюкокортикоидов позволяет предупредить развитие отека мозга и воспаления, вызванных гипоксией. Однако кортикостероиды, действуя на нейроны непосредственно во время ишемии, усиливают гипоксическое повреждение нервной ткани и угнетают ее репарацию после устранения гипоксии. При ЭС глюкокортикоиды нужно применять только после прерывания припадка и только для предупреждения распития отека мозга при признаках увеличения внутричерепного давления у животного. Действие больших доз метилпреднизолона при ЭС не исследовалось, но на экспериментальных моделях было показано, что применение этого гормона сразу после повреждения головного мозга, сопровождающегося отеком, существенно улучшает исход заболевания и снижает смертность.
| Классификация и причины развития эпилептического статуса |
| Первичная эпилепсия |
| Идиопатическая Породная предрасположенностьНаследственная |
| Вторичная эпилепсия |
| Менингоэнцефалиты— инфекционные |
— стерильные грануломатозные энцефалиты
Новообразования — первичные (опухоли нервной системы)
Читайте также:


