Билирубиновая энцефалопатия билирубиновая интоксикация
Клиника включает 4 фазы:
2. Появление классических признаков ядерной желтухи. На фоне резкой гипотонии развиваются кратковременные тонические судороги разгибательной мускулатуры, спастичность, ригидность затылочных мышц, вынужденное положение тела с опистотонусом, "негнущимися" конечностями и сжатыми в кулак кистями, периодическое возбуждение и резкий мозговой крик, выбухание большого родничка, подергивание мышц лица, крупноразмашистый тремор рук, исчезновение рефлекса Моро и видимой реакции на сильный звук, сосательного рефлекса, нистагм, спазм взора, симптом заходящего солнца, летаргия, иногда повышение температуры тела. В тяжелых случаях на первый план выступают выраженные стволовые расстройства (брадикардия, брадипноэ). При этом прогноз является весьма серьезным. (Эта фаза занимает от нескольких дней до нескольких недель. У недоношенных эта фаза может длиться несколько часов. Поражение ЦНС при этом носит необратимый характер.
3. Фаза ложного благополучия и полного или частичного исчезновения спастичности, когда создается впечатление о возможности даже полной реабилитации (2-3-й месяц жизни).
4. Фаза резидуальных нарушений - формирование клинической картины неврологических осложнений (могут начинаться с конца периода новорожденности, но чаще с 3-5 месяца жизни): клиника ДЦП: атетоз, хореоатетоз, парезы, параличи, глухота; задержка психического развития; дизартрия и др. Наиболее типичное проявление постбилирубиновой энцефалопатии – дефект слуха, в основном из-за поражения ядра VIII пары черепных нервов. Поэтому у всех детей, в анамнезе которых имеются указания на гипербилирубинемию, нужно проверять слух.
Ретроспективная оценка причин возникновения ядерной желтухив средине 40-50-x гг. прошлого века (до эры активного использования у новорожденных из группы риска фототерапии и операции обменного переливания крови) показала, что данное состояние развивалось чаще всего у новорожденных детей с гемолитической болезнью по Rh-фактору в случаях, когда концентрация общего билирубина в сыворотке крови превышала 298-342 мкмоль/л. При этом вероятность развития ядерной желтухи при ГБН составляла при концентрации 340 - 425 мкмоль/л - 20 %, при концентрации 425 - 510 мкмоль/л - 30-40 %, при концентрации более 685 мкмоль/л - выше 50 %. Гораздо реже выявлялись случаи билирубинового поражения мозга при ГБН по АВО и конъюгационных желтухах. Однако билирубиновая энцефалопатия может возникнуть и при гораздо меньшем уровне НБ в крови. В 50-е-60-е годы было установлено, что риск развития ядерной желтухи у недоношенных детей повышается с уменьшением массы тела при рождении. При этом вероятность развития ядерной желтухи была клинически значимой, если при массе тела ребенка 2000-2499 г. концентрация билирубина крови была больше 298 мкмоль/л; при массе тела 1500-1999 г.> 256 мкмоль/л, при массе тела 1000-1499 г. > 205 мкмоль/л, при массе тела менее 1000 г. > 171 мкмоль/л. Объясняется это врожденной незрелостью энзимных систем печени, повышенной проницаемостью ГЭБ, а также слабым развитием жировой ткани, являющейся местом накопления токсичного НБ. Таким образом, не только уровень НБ определяет риск поражения мозга. Существуют дополнительные факторы, повышающие риск развития билирубиновой энцефалопатии:
§ факторы, повышающие проницаемость ГЭБ для НБ: гиперосмолярность крови (гипергликемия, гиперосмолярные растворы), ацидоз, кровоизлияния в мозг, нейроинфекции, артериальная гипертензия;
§ факторы, повышающие чувствительность нейронов головного мозга к токсическому действию НБ: недоношенность, тяжелая асфиксия, голодание, гипогликемия, анемия, гипотермия;
§ факторы, снижающие способность альбумина крови прочно связывать НБ: недоношенность, гипоальбуминемия, инфекция, ацидоз, гипоксия, повышение уровня неэстерифицированных жирных кислот в крови, использование сульфаниламидов, фуросемида, дифенина, диазепама, индометацина, салицилатов, полусинтетических пенициллинов, цефалоспоринов. Практически весь НБ крови связан с альбумином, но эта связь непрочная
Степень иктеричности кожи не всегда отражает выраженность гипербилирубинемии, хотя и считают, что прокрашивание ладоней характерно для уровня непрямого билирубина более 255 мкмоль/л. Известная корреляция между степенью желтушного прокрашивания кожных покровов и уровнем билирубинемии теряет достоверность при повышении числа факторов риска у наблюдаемого ребенка.
До середины 80-х годов прошлого века выявленные закономерности являлись основанием для проведения операции обменного переливания крови с целью устранения риска ядерной желтухи при соответствующих клинических ситуациях.
Совершенствование перинатальных технологий, широкое использование с профилактической целью фототерапии к началу 90-х годов позволило существенно уменьшить частоту развития билирубиновой энцефалопатии, что привело в ряде экономически развитых стран к пересмотру показаний для операции обменного переливания крови. Вместе с тем, в последние 10 лет в некоторых странах выявлена тенденция к повторному увеличению частоты билирубиновой энцефалопатии. Последнее может быть связано с ранней выпиской условно здоровых новорожденных детей из акушерских стационаров и недостаточно тщательной организацией медицинского наблюдения за ними в домашних условиях.
Это крайне тяжёлое состояние может развиться при желтухе недоношенных, гемолитической болезни и гепатите новорождённых. Частота его значительно снизилась в связи с внедрением фототерапии, обменного переливания крови И лечения фенобарбиталом.
В первые 5 дней жизни у новорождённого с желтухой появляются беспокойство или сонливость, лихорадка, ригидность затылочных мышц и разгибание шеи, переходящие в опистотонус. Также отмечают ригидность конечностей с пронацией рук, косоглазие, ретракцию век, мышечные подёргивания или судороги, пронзительный крик.
Смерть может наступить быстро, в течение 12ч;
70% больных детей умирают в течение 7 дней. 30% могут выжить, но остаться инвалидами вследствие умственной отсталости, церебрального паралича или атетоидного гиперкинеза. Такие дети подвержены интеркуррентной инфекции, которая иногда приводит к смерти.
Билирубин может обладать нейротоксичностью и в сравнительно невысоких концентрациях, и его воздействие обнаруживают только с помощью новых нейрофизиологических методов [97].
При аутопсии выявляют жёлтую окраску базальных ганглиев и других областей головного и спинного мозга, связанную с избирательным накоплением в нервной ткани жирорастворимого неконъюгированного билирубина.
Ядерная желтуха обусловлена циркуляцией неконъюгированного билирубина, проникающего через гематоэнцефалический барьер. Также может иметь значение пониженное связывание билирубина сывороточным альбумином, о чём свидетельствует положительный эффект инфузий альбумина.
Признаками классической ядерной желтухи служат окрашивание мозга билирубином и повреждение нейронов. Немногочисленные экспериментальные исследования позволяют предполагать, что токсическое воздействие билирубина на функции мозга и даже смерть от гипербилирубинемии возможны при отсутствии жёлтой окраски и повреждения клеток [38]. Механизмы токсического действия билирубина и повреждения нейронов неизвестны, однако установлено, что он угнетает функцию нервных клеток [45]. Каждая молекула гема высвобождает 1 молекулу монооксида углерода. С помощью назального катетера можно определить его концентрацию в выдыхаемом воздухе менее чем за 1 мин. Этот метод позволяет выявить новорождённых с риском развития ядерной желтухи.
Ядерную желтуху усугубляют гипоксия, метаболический ацидоз и септицемия [45]. Конкурирующие за места связывания с альбумином органические анионы увеличивают выраженность ядерной желтухи, несмотря на снижение уровня билирубина в сыворотке. К таким анионам относят салицилаты, сульфаниламиды, свободные жёлчные кислоты и гематин.
врождённые ГЕМОЛИТИЧЕСКИЕ НАРУШЕНИЯ
Врождённые гемолитические нарушения могут приводить к неконъюгированной гипербилирубинемии в первые 2 дня жизни. К ним относятся недостаточность ферментов эритроцитов (Г-6-ФД и пируваткиназы), врождённый сфероцитоз и пикноцитоз.
Недостаточность Г-6-ФД. Желтуха обычно появляется на 2-й или 3-й день жизни. Провоцирующим фактором могут служить лекарственные препараты, проникающие в грудное молоко, в частности салицилаты, фенацетин или сульфаниламиды. Заболевание часто встречается в Средиземноморье, на Дальнем Востоке и в Нигерии.
ЖЕЛТУХА ОТ МАТЕРИНСКОГО МОЛОКА
Гипербилирубинемия (уровень билирубина в сыворотке выше 12 мг%) выявляется у 34% новорождённых, вскармливаемых грудью, и только у 15% при искусственном вскармливании [96]. Причиной её возникновения может быть повышенная активность b-глюкуронидазы грудного молока, вызывающая повышение содержания неконъюгированного билирубина в кишечнике с его последующим всасыванием [40]. Высокая концентрация свободных жирных кислот в грудном молоке способна угнетать конъюгацию билирубина.
Продолжительность желтухи — от 2 нед до 2 мес и более. Прекращение грудного вскармливания приводит к снижению уровня билирубина.
ПРЕХОДЯЩАЯ СЕМЕЙНАЯ ГИПЕРБИЛИРУБИНЕМИЯ (СИНДРОМ ЛЮЦЕЯ-ДРИСКОЛА)
Этот тип гипербилирубинемии возникает в первые дни и продолжается до 2—3-й недели жизни. Отмечается у всех братьев и сестёр. Считается, что гипербилирубинемия обусловлена наличием ингибитора конъюгации билирубина в сыворотке крови матери и ребёнка.
Заболевание описано в главе 12. Может развиваться в первые дни жизни.
У девочек гипотиреоз встречается в 3 раза чаще, чем у мальчиков. Новорождённый вял, сонлив, часто обнаруживается небольшая анемия. Подтверждением диагноза служит снижение уровня тироксина и трийодтиронина в сыворотке при высоком уровне тиреотропного гормона и эффективности соответствующего лечения. Механизм возникновения желтухи неясен.
ОСЛОЖНЕНИЯ ПЕРИНАТАЛЬНОГО ПЕРИОДА
Кровотечение с излиянием крови в ткани приводит к повышенному образованию билирубина, что может усугубить желтуху, особенно у недоношенных детей. Анемия обусловливает подавление функции гепатоцитов. Желтуха часто сочетается с кефалогематомой. Необходимо определение протромбинового времени (ПВ) и введение витамина К.
Сепсис, в том числе пупочный, ведёт к появлению неконъюгированной гипербилирубинемии в первые дни жизни. Производят посевы крови, мочи, при необходимости спинномозговой жидкости с последующим введением соответствующих антител.
ОБСТРУКЦИЯ ВЕРХНИХ ОТДЕЛОВ ЖЕЛУДОЧНО-КИШЕЧНОГО ТРАКТА
У 10% младенцев с врождённым стенозом привратника возникает желтуха вследствие неконъюгированной гипербилирубинемии. Вероятно, она развивается по тому же механизму, что и усиление желтухи при голодании у больных с синдромом Жильбера.
Не нашли то, что искали? Воспользуйтесь поиском:
Билирубиновая энцефалопатия возникает в результате воздействия непрямого билирубина на центральную нервную систему.
Временное увеличение концентрации билирубина в крови в течение первых нескольких дней после появления на свет развивается у многих малышей и считается нормой. У недоношенных и у части доношенных новорожденных возникают признаки желтухи (при превышении порога в 70 мкмоль/л).

Желтуха новорожденных может быть физиологической или патологической
Преходящая гипербилирубинемия
В отсутствие всякой патологии, билирубин в крови повышается в связи с рядом особенностей протекания физиологических процессов в организме новорождённых, а именно:
- Сравнительно небольшим сроком жизни эритроцитов с фетальным гемоглобином.
- Физиологической полицитемией.
- Общим преобладанием катаболических процессов над анаболическими.
- Сниженной функциональной активностью печени, замедлением захвата и выведением ею билирубина.
- Поступлением части крови от кишечника напрямую в нижнюю полую вену (мимо печени).
При подобном физиологическом состоянии важной задачей для врачей является наблюдение за младенцем и быстрое оказание помощи ребенку в случае, если оно примет характер патологии.
Когда норма становится патологией?
Таким образом, физиологическая желтуха, появившись спустя примерно сутки после родов, нарастает на протяжении нескольких дней и начинает угасать к концу первой недели жизни ребенка. В случае если все протекает нормально, кожа новорожденного на это время приобретает оранжевый оттенок, но при этом кал и моча сохраняют свой обычный цвет, печень и селезенка младенца не увеличиваются, а общее состояние остается удовлетворительным.
Если же желтуха появляется раньше или позже, стремительно нарастает, продолжается слишком долго (более 1 недели), сопровождается расширением границ селезенки и печени или утяжелением состояния ребенка в целом, то это признак патологической гипербилирубинемии.
Почему развивается патологическая гипербилирубинемия?
В основе данного явления лежат следующие причины:
- избыточная продукция билирубина в случае повышенного разрушения клеток крови (гемолиза);
- сниженный захват билирубина клетками печени ─ гепатоцитами, что говорит об их неполноценной работе;
- нарушение выделения билирубина в кишечник и его выведения;
- сочетание плохого захвата билирубина гепатоцитами и замедленного его выведения.
Билирубиновая энцефалопатия, возникающая у новорожденных, представляет собой ситуацию, опасную для здоровья и жизни ребенка. Ее причиной чаще всего становится усиленный гемолиз или устойчивое нарушение захвата непрямого билирубина клетками печени.

Резус-конфликт возникает, когда у матери отрицательный резус, а ребенок наследует положительный резус от отца
Наиболее часто встречающимися причинами развития гемолиза у детей на первой неделе жизни являются:
- различия крови матери и ребенка по белкам, находящимся на поверхности эритроцитов (AB0, Rh);
- аномалии строения эритроцитарных мембран, а также ошибки строения цепей гемоглобина (талассемии);
- применение некоторых медикаментов (высокие дозировки викасола);
- некоторые врожденные болезни инфекционного генеза (сифилис, цитомегаловирусная инфекция, краснуха и т.п.);
Для того, чтобы из непрямого билирубина, обладающего токсическими свойствами, образовался обезвреженный непрямой, должна беспрепятственно пройти реакция связывания билирубина в клетках печени ─ гепатоцитах.
Последствие нарушения данного процесса ─ так называемая, конъюгационная желтуха. Такое состояние возникает при ряде наследственных заболеваний: синдроме Жильбера и т.д.
Клиническая картина

Клиническая картина билирубиновой энцефалопатии складывается из четырех следующих друг за другом периодов заболевания
Течение билирубиновой энцефалопатии состоит из 4 фаз:
Возникновение билирубиновой энцефалопатии должно быть вовремя предупреждено, если же оно все-таки наступило, то помощь ребенку должна быть оказана в скором порядке еще в течение первой фазы заболевания.
При появлении билирубиновой энцефалопатии основным методом лечения является как можно более скорое обменное переливание крови.

Заменное переливание крови является эффективным способом удаления из организма новорожденного токсичных продуктов гемолиза
Профилактика билирубиновой энцефалопатии
Врачи сразу, при появлении на свет малышей, выделяют детей, у которых в высокой степени возможно развитие гемолитической болезни, в особую группу риска. К ним относят, прежде всего, малышей, чья кровь несовместима с материнской по эритроцитарным антигенам.
У них в крови определяют количество непрямого билирубина, гемоглобина, фиксируют ее групповую принадлежность и резус-фактор.
По результатам проведенных анализов, малышей принимают решение наблюдать, использовать фототерапию или переходить к более решительным действиям. Билирубин, под действием света синих люминесцентных ламп, меняет свою структуру и утрачивает свою токсичность.

Облучение тела новорожденного с помощью флюоресцентной лампы
Если у ребенка концентрация непрямого билирубина в крови нарастает со скоростью более 6,8 мкмоль/л/час (несмотря на проводимое лечение), то врач имеет право назначить применение препаратов, содержащих человеческий иммуноглобулин. При необходимости может быть назначен повторный курс. В крайнем случае, прибегают к обменному переливанию крови.
Если же ребенок рождается уже с признаками гемолитической болезни (бледная желтушная кожа, отечность, увеличенные печень и селезенка), не дожидаясь результатов лабораторных исследований, переходят к переливанию крови.
Таким образом, билирубиновая энцефалопатия новорожденных является состоянием, которое несет существенную угрозу для здоровья и жизни малыша, поэтому все усилия врачей должны быть направлены на его профилактику, своевременное выявление и оказание необходимой помощи.
Билирубиновая энцефалопатия (именуемая также ядерной желтухой) - состояние, характеризующееся гибелью мозговых клеток вследствие токсического влияния на них высокой концентрации билирубина (непрямой фракции). Подобное состояние наиболее часто встречается у новорожденных и требует немедленного лечения, в противном случае может привести к инвалидизации и даже гибели пациента.
Этиология болезни
Возможные причины билирубиновой энцефалопатии у новорожденных следующие:
- гемолитическая болезнь (резус- либо групповая несовместимость мамы и малыша);
- сахарный диабет у матери;
- сепсис новорожденного;
- травматизация ребенка при родах с формированием обширных гематом;
- токсоплазмоз (внутриутробное заражение);
- желтуха у недоношенных деток.
Под влиянием какого-либо из перечисленных процессов непрямой билирубин (то есть непереработанный гепатоцитами) в большом количестве выбрасывается в кровь, оказывая нейротоксическое воздействие на мозговые ткани.
Патоморфологические признаки
Поверхность головного мозга имеет бледно-желтый оттенок. Срез препарата выявляет характерную желтую окраску мозговых структур (мозжечка, гиппокампа, таламуса, ствола и других). Однако непрокрашенные области также претерпевают патологические изменения.
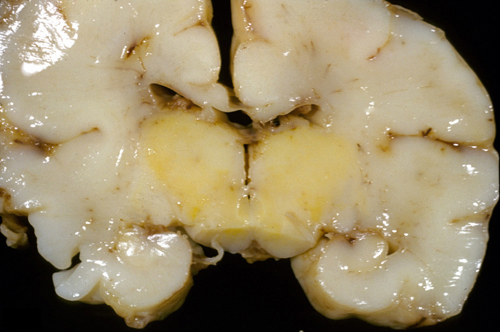
В пораженных областях вследствие гибели нейронов формируется глиоз и происходит атрофия нервной ткани. При этом патоморфологическая картина сходна с таковой при гипоксическом поражении, а значит, с большой долей вероятности можно предполагать, что несвязанный билирубин, повреждая клеточные мембраны, приводит к нарушениям утилизации кислорода в мозговых тканях. А гипоксическое повреждение приводит к еще большему увеличению чувствительности нейронов к токсическим эффектам билирубина.
То есть, ядерная желтуха (билирубиновая энцефалопатия) - это не только изменение окраски мозговых структур под действием билирубина. Это также целый ряд патологических специфических процессов, происходящих на уровне клетки.
Билирубиновая энцефалопатия у взрослых
Причины поражения мозговых структур билирубином у взрослых кроются в тяжелых декомпенсированных патологиях печени (циррозы, гепатиты).
Недуг у взрослых развивается постепенно и сопровождается нарастанием неврологической симптоматики. При этом на первый план выходят нарушения психики и двигательной активности, проявляющиеся бессонницей, когнитивными изменениями, понижением активности и так далее.
Клинические проявления
Чаще всего первые признаки патологии возникают у доношенных деток на 2-5 сутки, а у недоношенных - на 7 сутки. Но присутствие гипербилирубинемии может приводить к развитию недуга в течение всего времени новорожденности (до 28 суток).
Ранние симптомы такой энцефалопатии неспецифичны и могут совпадать с таковыми при гипогликемии, сепсисе, внутричерепных кровоизлияниях, гипоксии и других патологических острых состояниях новорожденного.
Как правило, первыми признаками начинающегося поражения мозга становятся снижение сосательного рефлекса, сонливость, пропадание рефлекса Моро. По мере ухудшения (прогрессирования) болезни пропадают сухожильные рефлексы, нарушается дыхание, возникает опистотонус, большой родничок напряжен, лицевые мускулы и мышцы конечностей судорожно подергиваются, ребенок пронзительно кричит.
Затем появляются судороги, сопровождающиеся резким разгибанием ручек и поворотом кистей, сжатых в кулачки, вовнутрь.
Дальнейшая активность процесса часто приводит к гибели, в другом случае состояние ребенка улучшается, и развитие соответствует норме. Однако к году вновь возникает ригидность мускулов, опистотонус и гиперкинезы. Ко второму году жизни судороги и опистотонус исчезают, однако непроизвольные беспорядочные движения, сочетающиеся с гипотонией либо ригидностью мускулов сохраняются и приобретают устойчивый характер.
В трехлетнем возрасте билирубиновая энцефалопатия у детей обретает стойкий и четкий характер, что проявляется тугоухостью на звуки с высокой частотой, хореоатетозом, судорогами, дизартрией, косоглазием, олигофренией, экстрапирамидными нарушениями. Иногда встречается атаксия, гипотония и пирамидные расстройства.
При легком течении билирубиновой энцефалопатии последствия могут проявляться в виде тугоухости, умеренных либо легких нарушений двигательной координации, синдрома гиперактивности в сочетании с нарушенным вниманием (минимальная мозговая дисфункция). Такие симптомы могут сочетаться либо присутствовать по отдельности. При этом энцефалопатия может быть не диагностирована вплоть до поступления в школу.
Стадийность процесса
Патология имеет четыре стадии развития:
- Симптомы билирубиновой энцефалопатии неспецифичны: присутствует слабость, рвота, монотонный безэмоциональный крик. Тонус мышц и аппетит снижены.
- Появляются симптомы энцефалопатии, конечности малыша согнуты, разогнуть их при этом невозможно, подбородок приведен к груди, ребенок неестественно вскрикивает. В некоторых случаях возможна гипертермия и эпизоды апноэ.
- Состояние больного (чаще 10-12 сутки жизни малыша) заметно улучшается, однако явление это не связано с выздоровлением, напротив - процесс прогрессирует. Скованность мышц отступает, отсутствуют судороги.
- Развивается на 2 месяце жизни малыша. Симптоматика нарастает. Присутствуют признаки, сходные с таковыми при церебральном параличе. Ребенок значительно отстает в психоэмоциональном и физическом развитии.
Диагностические мероприятия
Гипербилирубинемия может расцениваться как физиологическая только в случаях исключения абсолютно всех патологических факторов ее появления. Беря во внимание тот факт, что гипербилирубинемия наиболее часто является следствием гемолитических либо физиологических причин, обследование пациента должно включать следующие анализы:
- исследование крови (общее) с обязательным вычислением количества ретикулоцитов и микроскопией кровяного мазка;
- проба Кумбса (непрямая и прямая);
- выяснение групповой и резус-принадлежности крови матери и малыша;
- определение количества непрямого и прямого билирубина;
Увеличение содержания в пуповинной крови билирубина, наличие симптомов желтухи в первые сутки жизни, если уровень неконъюгированной фракции более 34 мкмоль/л указывают на присутствие патологической желтухи.
В некоторых случаях могут назначаться при билирубиновой энцефалопатии МРТ, УЗИ и КТ.
Терапия состояния
Терапией ядерной желтухи у малышей (вне зависимости от ее стадии) занимается детский невропатолог. Как правило, таких деток госпитализируют.
Лечение недуга у взрослого также проводится в условиях стационара под постоянным контролем врача.
Лечение заболевания заключается в ликвидации причин гипербилирубинемии и восстановлении нормальной концентрации билирубина в крови. В качестве лечения при этом используется фототерапия.
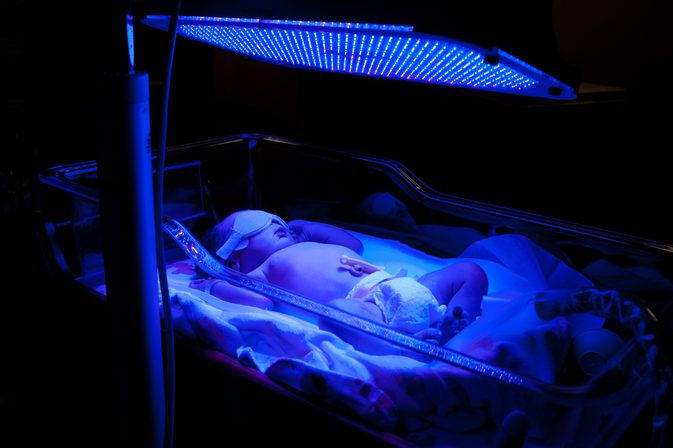
Под влиянием излучения токсичный непрямой билирубин трансформируется в особый изомер, который легко выводится почками и печенью и при этом не связывается с кровяными альбуминами. В случаях, когда концентрация билирубина под влиянием фототерапии не понижается, назначается переливание плазмы.
Если предыдущие методики оказались неэффективными, либо симптоматика стремительно нарастает, пациенту назначаются прямые переливания крови.
Применяемые препараты
Если по каким-то причинам прямое переливание невозможно, назначаются лекарства, влияющие на синтез и трансформацию билирубина ("Протопорфирин").
Вследствие того, что ядерная желтуха - результат токсического воздействия билирубина на нейроны, в лечении ее всегда применяются нейропротекторы.
При наличии показаний назначается противосудорожное лечение.
В случае гемолитической болезни с наличием прямой положительной реакции Кумбса эффективны внутривенные вливания иммуноглобулина.
Частота возникновения, последствия и прогнозы
Согласно данным аутопсии, ядерная желтуха возникает у новорожденных в любом гестационном возрасте при отсутствии адекватной терапии гемолитической болезни и концентрации билирубина свыше 25-30 мг.
Частота возникновения недуга у недоношенных деток с гипербилирубинемией варьируется от 2 до 16 %. Более точные цифры определить невозможно вследствие большого разнообразия симптомов болезни.
Присутствие выраженного неврологического симптомокомплекса является неблагоприятным прогностическим признаком. Так, летальность при этом доходит до 75 %, а 80 % выживших пациентов имеют двусторонний хореоатетоз, сопровождающийся мышечными непроизвольными сокращениями. Кроме того, достаточно часто встречаются осложнения в виде глухоты, олигофрении и спастической тетраплегии.
Детки с гипербилирубинемией в анамнезе должны быть обязательно обследованы на предмет глухоты.
Несмотря на улучшение диагностики, ядерная желтуха все же имеет место. Встречается информация о возникновении ее на фоне гипербилирубинемии без наличия каких-либо причин. А потому специалисты рекомендуют проводить обязательный контроль билирубина на 1-2 день жизни всем новорожденным, дабы выявить пациентов с высокой вероятностью развития тяжелой гипербилирубинемии и, как следствие, энцефалопатии.
Профилактические меры
Важно обязательное исследование концентрации билирубина в случае возникновения желтухи в первый день жизни, а при наличии гипербилирубинемии - исключение развития гемолитической болезни.
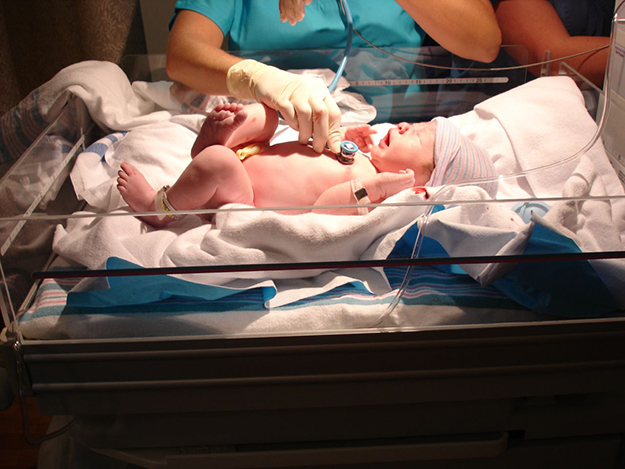
Обязателен контроль состояния младенца в течение 3 суток после выписки, особенно это касается недоношенных (до 38 недель) деток, которые были выписаны из родильного отделения до наступления 2 суток жизни.
Частота наблюдения обуславливается возрастом, при котором малыш был выписан, и присутствием факторов риска. Некоторых деток наблюдают в течение суток. Спрогнозировать риски можно, оценив уровень почасового прироста билирубина.
Наибольший интерес вызывает вопрос нейротоксичности билирубина и возникновения билирубиновой энцефалопатии. Первое патоморфологическое описание желтушного окрашивания ядерных масс мозга новорожденных детей, у которых желтуха появилась сразу после рождения, сделано в 1875 году. В процессе изучения данной патологии выдвигались различные гипотезы о механизмах повреждающего действия билирубина на мозг новорожденных, влекущее за собой возникновение билирубиновой энцефалопатии. Отложения кристаллов практически нерастворимого в водных средах билирубина при данном заболевании обнаруживают не только в головном мозгу (палеокортекс, базальные ядра, субталамические ядра, продолговатый мозг, мозжечок), но и в стенке дыхательных путей, стенке желудочно-кишечного тракта, селезенке, почках, надпочечниках, семенных железах, костном мозгу. Это позволяет рассматривать билирубиновую энцефалопатию как проявление общей билирубиновой интоксикации организма. Здесь уместно было бы предположить, что нарушение собственно барьерной функции ГЭБ может являться следствием повреждения мембранных структур астроцитов и эндотелиоцитов билирубином, который относится к токсическим продуктам метаболизма. Спорным является вопрос о роли печени в нарушении проницаемости ГЭБ при гемолитической болезни. Наличие отчетливых морфологических изменений при нарушении детоксирующей роли печени впервые отметил Zammora (отек, вакуолизация, конечные разветвления астроцитарных отростков при экспериментальном выключении печени крыс из кровотока). Причиной билирубиновой интоксикации может быть дефект микросомальной ферментной системы гепатоцитов, катализирующей конъюгацию билирубина, а также конъюгацию различных иных субстанций алифатического, ароматического и/или стероидного ряда, способных тоже оказывать токсическое действие на организм. В результате многочисленных исследований было установлено, что связанный с сывороточным альбумином билирубин в клетки мозга не проникает, однако следует отметить, что каждая молекула альбумина может связать две молекулы непрямого билирубина, но первую очень прочной связью, а вторую рыхло. Непрямой билирубин в кислой форме находится в рыхлой связи с альбумином и токсичен для мозга.
В последние годы в некоторых работах было предложено определять соотношение билирубин/альбумин вместо определения концентрации билирубина и альбумина отдельно. Тем самым предполагалось достигнуть лучших результатов в прогнозировании и предотвращении билирубиновой энцефалопатии путем оптимизации показаний для заменного переливания крови. Однако существенных результатов эти исследования не дали. Общеизвестно, что существуют факторы, способствующие нарушению связывающей билирубин способности альбумина, а также вещества-лиганды, конкурирующие за места прочного связывания на альбумине (асфиксия, ацидоз, неэстерифицированные жирные кислоты, лекарственные вещества и т.д.).
Гипоксия предрасполагает к развитию билирубиновой энцефалопатии в первую очередь из-за угнетения активности системы глюкоронил-трасферазы. Известно, что митохондрии мозга, равно как и других органов и тканей, содержат билирубиноксидантную систему, окисляющую в присутствии кислорода билирубин. В связи с тем, что процесс гипоксии вызывает повреждение митохондрий и инактивацию оксидаз, может нарушиться механизм окисления билирубина, попадающего в капиллярные субстанции. Этот механизм в норме "срабатывает" у новорожденных в случае достаточной ферментативной активности, тогда как гипоксия нарушает этот процесс. Сочетание желтухи с гипоксией особенно опасно из-за повышенной чувствительности нервных клеток к гипоксии, когда недостаток кислорода вызывает локальный тканевый ацидоз, который может существовать еще некоторое время после коррекции рН крови. Наибольшее значение в патогенезе билирубиновой энцефалопатии имеет проницаемость ГЭБ, который является сложной регуляторной поверхностью, четко контролирующей прохождение веществ через стенку сосудов мозга в клетки мозга. Патоморфологи диагностируют ядерную желтуху не ранее 36 часов после рождения. Таким образом, изменения ЦНС, возникшие в первые 36 часов жизни, могут быть обратимыми. При ядерной желтухе в первую очередь прокрашиваются базальные ганглии: хвостатое ядро, скорлупа, бледный шар. Могут повреждаться также кора мозга, мозжечок, подбугровая область, аммонов рог, ядра продолговатого мозга и мозжечка. Интенсивное поражение ядер дна 4-го желудочка может быть причиной смерти новорожденного. На дне 4-го желудочка чаще прокрашиваются боковые отделы в области кохлеарных и вестибулярных ядер. Значительно реже желтушность находят в зрительном бугре и других отделах мозга. Особенно редуцированы пирамидные клетки 3-го слоя коры, двигательной области спинного мозга и стволовой части головного мозга. После 6-7-го дня жизни ребенка интенсивность острых изменений нейронов снижается, выявляются поля опустошения во многих отделах мозга с последующим развитием глиоза. Нарушается формирование мозга и всего организма ребенка. В клинической картине билирубиновой энцефалопатии наблюдается следующая триада симптомов: гиперкинетическая форма ДЦП, дефект слуха и умственная недостаточность. К сопутствующим проявлениям заболевания относятся ограничение взора вверх, желтушное окрашивание и дефект зубной эмали, дизартрия.
Читайте также:


