Врожденная внутриутробная инфекция цитомегаловирус
В чем трудности диагностики ЦМВ? Каков механизм заражения ЦМВИ? В последние годы отмечена тенденция к увеличению среди беременных частоты вирусных инфекций и возросла их способность, при определенных условиях, к эпидемическому распространению.
В последние годы отмечена тенденция к увеличению среди беременных частоты вирусных инфекций и возросла их способность, при определенных условиях, к эпидемическому распространению.
Особое значение приобретает проблема цитомегаловирусной инфекции (ЦМВИ) при беременности, вследствие того что цитомегаловирус (ЦМВ) может явиться причиной акушерской патологии, эмбрио- и фетопатий, внутриутробной и перинатальной инфекции [1].
Наличие латентных форм ЦМВИ с атипичным течением, инаппарантными проявлениями и поражением тканей органов представляет большие трудности для своевременного распознавания инфекции и является причиной диагностических ошибок.
Среди родившихся живыми 0,2-2,2% детей внутриутробно инфицированы цитомегаловирусом. Внутриутробная ЦМВИ, вне зависимости от формы заболевания, может представлять опасность вследствие поражения ЦНС и привести к возникновению психомоторных нарушений, умственной отсталости детей даже через несколько лет после родов [2].
Беременным принадлежит значительный процент в эпидемиологии ЦМВИ, которая обнаруживается у них в два раза чаще, чем краснуха.
ЦМВИ может способствовать развитию осложнений во время беременности, родов и в послеродовом периоде. Акушерская патология наиболее часто проявляется в виде спонтанных выкидышей, мертворождений, рождения нежизнеспособных детей [3, 4, 11].
Проблема изучения цитомегаловирусной инфекции и ее влияния на течение и исход беременности, разработка основ комплексной профилактики и лечения крайне актуальны и особенно важны для практического здравоохранения.
Цитомегаловирус (ЦМВ) принадлежит к семейству герпетических вирусов, насчитывающих около 40 представителей. Для человека характерны восемь разновидностей герпетических вирусов: простой герпес (1 и 2-го типа), цитомегаловирус, ветрянка-зостер, вирус Эпштейна–Барра, а также вирус герпеса 6, 7 и 8-го типа. Они вызывают обострения хронической инфекции и демонстрируют способность к персистированию в организме [10].
Цитомегаловирус является крупным ДНК-геном со сравнительно низкой вирулентностью и особой способностью к резкому подавлению клеточного иммунитета.
Воздействия экзо- и эндогенных факторов приводят к снижению иммунитета и, соответственно, к активации хронической цитомегаловирусной инфекции.
Источниками инфекции могут являться носители ЦМВ, их биологические жидкости и выделения: кровь, моча, слезы, слюна, грудное молоко, спинномозговая жидкость, амниотическая жидкость, вагинальное отделяемое, слизь из носоглотки, сперма, фекалии и др.
Особый тропизм ЦМВ проявляет к слюнным железам. Отсюда реальная возможность передачи ЦМВ от матери к ребенку при поцелуях. Имеется прямая корреляционная зависимость между инфицированием цитомегаловирусом и сексуальной активностью партнеров.
С учетом возраста и интимности контактов между людьми выявляются две волны атаки ЦМВИ: первая достигается к трехлетнему возрасту, вторая — к периоду половой зрелости.
Входными воротами для вируса являются дыхательные пути, пищеварительный тракт, слизистые. ЦМВ, проникая в кровь, репродуцируется в лейкоцитах и в системе мононуклеарных фагоцитов.
В большинстве случаев имеет место бессимптомное вирусоносительство или субклиническая, инаппарантная, хроническая инфекция, которая вне иммунодепрессии не вызывает никаких субъективных нарушений или объективных клинических проявлений. Длительной (нередко пожизненной) латенции способствует внутриклеточное сохранение ЦМВ в лимфоцитах, где он надежно защищен от действия специфических антител и интерферона.
Морфологические изменения проявляются в виде комплексов из цитомегалических клеток (ЦМК) и интерстициальной лимфогистиоцитарной инфильтрации [3].
Цитомегалические изменения наиболее часто наблюдаются в слюнных железах, легких, почках и головном мозге.
Описаны локальные цитомегалические повреждения глаз (хореоретиниты), кишечника (колиты), кожи (дерматиты), надпочечников, легких, почек, головного мозга [3].
Вопрос о влиянии срока беременности на передачу инфекции от матери к плоду остается открытым. Считается, что наибольшую угрозу для плода представляет развитие цитомегаловирусной инфекции в первой половине беременности.
Реактивация латентной инфекции ведет к передаче вируса от матери к плоду в 0,15%–0,36% случаев [5].
Возможно несколько путей передачи инфекции от матери к плоду:
- трансплацентарный;
- через инфицированные выделения в родовом канале;
- кормление инфицированным материнским молоком.
Трансплацентарная передача ЦМВИ наиболее часто приводит к инфицированию плода [7].
Цитомегаловирус от матери может проникать через плаценту в любом сроке беременности и вызывать поражение плода.
Цитомегаловирусная инфекция у беременных может быть первичной или рецидивирующей. Первичное материнское заражение ЦМВ, возникшее во время беременности, лучше всего диагностируется при изучении сероконверсии антител к ЦМВ. Присутствие антител IgG и IgM можно считать свидетельством первичной материнской инфекции. Рецидивирующая ЦМВ-инфекция во время беременности включает в себя как реактивацию собственного штамма ЦМВ, так и возможную реинфекцию новым штаммом вируса [9].
В большинстве случаев, в популяциях с высоким превалированием антител к ЦМВ, развитие ЦМВИ во время беременности скорее происходит в результате реинфицирования.
Врожденная ЦМВИ возникает либо после первичной инфекции, либо в результате обострения хронической. Более тяжелые последствия наблюдаются в период беременности при первичной инфекции.
При беременности в условиях иммунодефицита возникает неспецифическая депрессия иммунной системы. При ЦМВИ больше всего страдает клеточный иммунитет. Именно характер сдвигов в системе клеточного иммунитета во многом определяет течение и исход цитомегалии.
В ответ на внедрение вируса происходит выработка антител. При цитомегалии комплиментсвязывающие антитела сохраняются на протяжении всей жизни, что позволяет установить случаи имевшего в прошлом заболевания. Очевидно, что специфические антитела важны при защите против цитомегаловируса.
Антитела класса IgG свидетельствуют о том, что женщина ранее встречалась с инфекцией. Беременные имеют более интенсивную и длительную реакцию IgG. Высокие показатели титров антител свидетельствуют об активизации хронического процесса.
Отсутствие IgG в пуповинной сыворотке или сыворотке крови новорожденного исключает врожденную ЦМВИ, в то время как их присутствие может означать пассивный перенос от матери к плоду.
Значительно более высокий уровень IgG у новорожденного, чем у матери, может свидетельствовать о врожденной инфекции.
При исследовании в первые шесть месяцев жизни ребенка врожденная ЦМВИ исключается, если уровень IgG будет постепенно снижаться. Наличие IgМ в сыворотке крови характеризует первичную инфекцию. Антитела IgМ сохраняются в крови от 12 до 18 недель от начала первичной инфекции.
Антитела класса IgM через плаценту не переходят, их синтез осуществляется плодом и новорожденным в ответ на антигенное раздражение.
Механизм передачи ЦМВ предполагает тесный контакт между беременной (родильницей) и плодом (новорожденным). После беременности и родов ЦМВ можно найти почти во всех жидкостях тела, особенно в цервико-вагинальных выделениях и в грудном молоке, что может явиться источником пери- и постнатальной передачи ЦМВ от матери к новорожденному.
Передача инфекции может произойти с кровью при гемотрансфузиях и парентеральных манипуляциях, а также через поврежденную кожу и мацерированные слизистые. Установлено, что интранатальная или ранняя постнатальная передача ЦМВИ происходит в 10 раз чаще, чем трансплацентарная.
В послеродовом периоде эпидемиологическая опасность для новорожденного сохраняется в случаях нарушения женщиной гигиенических норм, а также вследствие передачи вируса с грудным молоком (20% серопозитивных матерей имеют ЦМВ в грудном молоке и 30% из них могут выделять вирус в молоко в течение года после родов) [8].
Перинатальные и постнатальные проявления ЦМВИ у детей почти всегда протекают в легкой форме и асимптоматично.
Многообразие вариантов течения ЦМВИ у беременных связано в большинстве случаев с бессимптомной латенцией и полиморфизмом клинических проявлений заболевания.
Варианты течения ЦМВИ и широкий спектр их проявлений обусловлены сложностью взаимоотношений между ЦМВ и клеткой хозяина.
Нередко клинические симптомы проявляются в виде субфебрильной температуры, ринофарингита, кашля, развития мононуклеозоподобного синдрома.
Диапазон клинических вариантов варьирует от слабо выраженного сиалоаденита и благоприятно текущего мононуклеозоподобного заболевания (лимфоцитоз, атипичные мононуклеары) до тяжелых поражений печени, легких и мозга.
У беременных симптоматическая ЦМВИ обычно проявляется в форме синдрома мононуклеоза, что подтверждается наличием лимфоцитоза, присутствием антител ЦМВ IgG и IgM в сыворотке и культуры ЦМВ в крови, моче, слюне, цервикальных выделениях.
Мононуклеозоподобный синдром характеризуется продолжительной лихорадкой, ознобами, быстрой утомляемостью, болями в мышцах, головными болями, встречается чаще у молодых людей [6].
У беременной женщины наиболее часто происходит обострение хронической ЦМВИ, которая, как правило, не имеет явных клинических проявлений. Однако у данной категории женщин в анамнезе нередко имеются указания на привычное невынашивание или неразвивающуюся беременность, мертворождения, рождение нежизнеспособных детей, а также детей-инвалидов с врожденными пороками развития [11].
Инфицирование возможно в любом триместре, тем не менее наиболее тяжелые последствия возникают при первичной инфекции, возникшей у матери в течение первых 20 недель беременности. Вместе с тем даже при развитии первичной ЦМВИ во время беременности 90-95% женщин имеют шанс родить здорового ребенка [12].
Внутриутробная цитомегаловирусная инфекция может приводить к рождению детей с тяжелыми неврологическими расстройствами, поражениями зрительного и слухового нервов.
Степень поражения плода зависит от срока инфицирования. Заражение на ранних сроках беременности чаще ведет к гибели плода и самопроизвольным выкидышам.
Дети с ЦМВИ (положительным IgM) от серопозитивных матерей имеют более низкий вес и рост при рождении, чем дети серонегативных матерей.
ЦМВ может инфицировать плаценту, плод, амниотическую жидкость. Вирусная культура и характерные цитомегалические клетки могут быть выявлены у плодов от женщин с активной первичной ЦМВИ. Однако наличие признаков или симптомов ЦМВ у плода не всегда является предвестником серьезного заболевания при рождении и в постнатальном периоде.
При выявлении симптомов болезни в течение первых трех недель жизни ребенка ЦМВИ может рассматриваться как врожденная, возникновение заболевания в более поздние сроки чаще характеризует приобретенную форму ЦМВИ (постнатальное инфицирование).
Врожденная ЦМВИ характеризуется, как правило, генерализованным поражением органов плода и целым комплексом клинических симптомов.
Для приобретенной формы ЦМВИ характерно латентное течение, преимущественно с локальным поражением слюнных желез.
У новорожденных, инфицированных внутриутробно, в 90% случаев не бывает симптомов при рождении, у 5-17% их них развиваются осложнения в более позднем периоде [6].
Развитие симптоматики у новорожденного с ЦМВИ коррелируется с симптомами, присутствующими при рождении.
Остальные дети с врожденной ЦМВИ совершенно асимптоматичны и выглядят при рождении здоровыми.
Клинические формы ЦМВИ могут иметь острое или хроническое течение.
По степени тяжести заболевания ЦМВИ выявляют:
- легкую (в том числе стертые и субклинические формы инфекции), при которой поражения внутренних органов незначительны и не сопровождаются функциональными нарушениями (компенсация);
- среднетяжелую, при которой имеется поражение внутренних органов, сопровождаемое функциональными нарушениями различной степени (субкомпенсация);
- тяжелую, при которой резко выражена интоксикация и поражение внутренних органов сопровождается тяжелыми функциональными нарушениями (декомпенсация);
При тяжелом течении врожденной ЦМВИ смерть ребенка чаще наступает в первые дни и недели жизни; при легком — болезнь принимает волнообразное течение.
Следует отметить, что дети с врожденной или перинатальной активной цитомегалией чрезвычайно предрасположены к развитию бактериальных суперинфекций, что обусловлено в первую очередь иммунной недостаточностью.
Симптомы врожденной ЦМВИ включают признаки замедления внутриутробного развития, внутриутробную гипотрофию, конъюгационную желтуху, гепатоспленомегалию, интерстициальную пневмонию, нарушения мозгового кровообращения. Осложнения со стороны ЦНС также очень часты и проявляются у новорожденных повышенной сонливостью, плохим сосательным рефлексом, макро- и микроцефалией, гидроцефалией, порэнцефалией, хориоретинитом, сенсоневральной глухотой [4, 11].
Врожденная ЦМВИ может также иметь необычные проявления, такие как вентрикуломегалия, перивентрикулит или образование кист, гемолитическая анемия, петехии, геморрагическая пурпура, тромбоцитопения, хронический гепатит и асцит [3, 8].
Однако, несмотря на очень большое количество симптомов и осложнений, ассоциируемых с врожденной ЦМВИ, трудно предсказать физическое и интеллектуальное развитие ребенка, основываясь на симптомах, присутствующих при рождении.
Каждое из перечисленных клинических проявлений ЦМВИ заслуживает отдельного рассмотрения.
Гепатомегалия вместе со спленомегалией и петехиями является самым убедительным подтверждением болезни у детей с врожденной ЦМВИ. Обычно присутствуют явления гепатита с нарушениями функции печени (желтуха, гипербилирубинемия).
Функция печени, как правило, нормализуются в первые недели жизни.
Спленомегалия нередко может явиться единственным показателем врожденной ЦМВИ при рождении.
Петехии обычно носят преходящий характер и наблюдаются в течение двух-трех суток после рождения. При врожденной ЦМВИ чаще встречается комбинация петехий с гепатоспленомегалией и тромбоцитопенией.
При исследовании крови выявляется картина гипохромной анемии, эритробластоз, тромбоцитопения.
Врожденная ЦМВИ приводит к ухудшению зрения у 20% детей. Чаще всего наблюдается хориоретинит (односторонний или двусторонний), который может привести к слепоте. Однако врожденная ЦМВИ обычно не вызывает микроофтальмию или катаркту.
Микроцефалия может быть частично причиной замедленного развития новорожденного и сочетаться с внутричерепными кальцификатами, которые локализуются в перивентрикулярной структуре и ликворе.
Компьютерная томография является наиболее чувствительным методом для их определения. Ультразвук и рентгенография черепа относятся к менее чувствительным методам.
Многие дети с микроцефалией и внутричерепными кальцификатами имеют неврологические проявления.
У 10% детей с асимптоматичными проявлениями инфекции могут наблюдаться осложнения, даже в возрасте пяти–семи лет, чаще в виде сенсорной потери слуха, неврологических расстройств или умственного отставания. Половина детей с врожденной ЦМВИ имеют сочетанную потерю слуха. Глухота носит двухсторонний сенсоневральный характер. Нередко также диагностируются врожденные сердечно-сосудистые, гастроинтестинальные, мышечно-скелетные аномалии развития органов [7].
Таким образом, для беременных с цитомегаловирусной инфекцией должен быть предусмотрен комплекс диагностических, профилактических и лечебных мероприятий, направленных на уменьшение случаев возникновения врожденной цитомегаловирусной инфекции, что должно быть обязательным условием создания эффективной системы профилактики и охраны здоровья матери и ребенка.
При цитомегаловирусной инфекции бычно выражены проявления гепатита, желтуха, гипербилирубинемия. Функции печени при ЦМВ инфекции обычно у новорожденных уже в первые недели приходит в норму. Петехии обычно носят преходящий характер, чаще обнаруживаются в комбинации с гепатоспленомегалий и тромбоцитопенией.
По данным S. Stagno с соавторами, проникновение ЦМВ к плоду при острой инфекции составляет 45 %, при этом в 2-4 % случаев развивается тяжелая генерализованная цитомегалия. В исследованиях А. П. Скоромец было показано, что внутриутробная цитомегалия может приводить как к формированию врожденных пороков развития, так и разнообразным изменениям, сходным с описанными при внутриутробном герпесе. У детей, больных ЦМВ, наблюдается угнетение клеточного иммунитета.
Мы провели анализ клинико-лабораторных особенностей перинатальной цитомегаловирусной инфекции у детей, направленных по поводу клинигеских проявлений гепатита. Под наблюдением Центра гепатологии Детской инфекционной больницы Тулы находилось 63 ребенка, впервые обратившихся в возрасте от 12 дней до 6 месяцев с различными проявлениями ЦМВИ. Поводом для направления ребенка в стационар были: гепатоспленомегалия, затянувшаяся желтуха, неврологическая симптоматика в сочетании с соматическими нарушениями.
Для верификации диагноза, помимо общеклинических анализов, мы исследовали биохимические показатели, серологические маркеры перинатальных инфекций, в том числе вирусов гепатитов В, С, CMV, Herpes. В лабораториях НИИЭМ им. Н. Ф. Гамалеи и Центра молекулярной диагностики ЦНИИЭ МЗ РФ определяли DNA CMV и концентрацию антител anti-CMV классов IgM, IgG в динамике. Проводили ультразвуковое исследование органов брюшной полости и нейросонографию (НСГ).
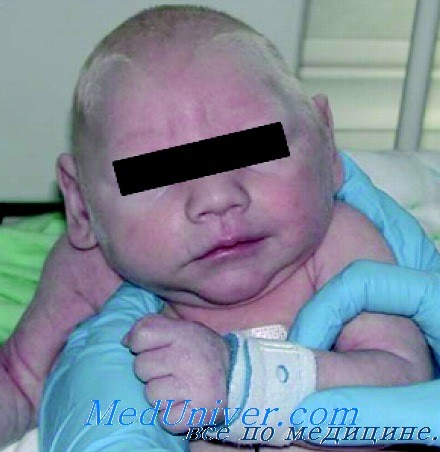
С низкой к сроку гестации массой тела и признаками внутриутробной гипотрофии родились 50 (79,4%) детей. У 33 больных (52,3%) после рождения отмечался кожно-геморрагический синдром, у трех из них — мелена. У 50 (79,4%) детей отмечалось затяжное течение желтухи, которая начиналась, как правило, на 3-5 сутки жизни и сохранялась до 1,5-2-месячного возраста. Преобладала неконъюгированная фракция билирубина. У 25 (39,6 %) новорожденных отмечались дыхательные расстройства, эти дети впоследствии страдали частыми бронхолегочными заболеваниями.
Поражение печени проявлялось в клинической форме гепатита. Увеличение (на 2-5 см из-под края реберной дуги) и плотноватая консистенция печени отмечены у 38 (60,3%) детей. Несколько реже — у 19 (30,2%) — отмечалось увеличение селезенки до 2 см ниже края реберной дуги. У 12 детей (19%) отмечено расширение вен передней брюшной стенки. Функциональные пробы печени были изменены у всех больных: активность АЛТ повышалась в 3-5 раз, ACT — в 2-3 раза, ЩФ — в 1,5-2 раза по сравнению с возрастной нормой.
При УЗИ печени увеличение размеров регистрировалось в основном за счет правой доли, с тенденцией к повышению эхоплотности. Соотношение долей, индекс 1 сегмента, плотность стенок сосудов и желчных протоков мало изменялись, в отличие от УЗИ-картины при врожденных гепатитах В и С. При серологическом исследовании у детей в возрасте до трех месяцев во всех случаях обнаружены антитела anti-CMV класса IgG, в 49,2% (31 человек) обнаружены также anti-CMV класса IgM. При обследовании детей старше трех месяцев более регулярно обнаруживали антитела класса IgG, с нарастанием титра в парных сыворотках.
У 76,2% (48 больных) проведено исследование крови и/или слюны и мочи методом ПЦР, у 31 из них (64,6%) обнаружена DNA CMV. У 39 детей (61,9%) — снижение количества эритроцитов и гемоглобина до уровня легкой и среднетяжелой степени анемии.
Все дети находились под наблюдением невропатолога. Диагностированы: синдром задержки психомоторного развития —у 47 (74,6%), гипертензионно-гидроцефальный синдром — у 27 (42,8%), синдром двигательных нарушений — у 23 (36,5 %). При НСГ отмечалось повышение эхогенности паренхимы мозга, ее неоднородность и зернистость, субэпиндимальные кисты и/или кисты сосудистых сплетений, периваскулярная инфильтрация, проявления смешанной или наружной гидроцефалии. Отличительной особенностью неврологических проявлений цитомегаловирусной инфекции являлась их резистентность к традиционной терапии (сосудистые, ноотропные, витаминные препараты).

Что это за инфекция
Цитомегаловирус относится к группе герпетических инфекций. Отличается латентным течением вызываемой патологии, то есть в большинстве случаев она не имеет клинических проявлений. Признаки заболевания появляются у людей с ослабленным иммунитетом. В их число входят и беременные женщины.
Вирус в организме человека располагается внутриклеточно. Размножается он очень медленно, обладает незначительной заразностью. Но цитомегаловирусная инфекция широко распространена во всем мире. За последние десятилетия отмечается рост заражения среди беременных женщин. Единственный источник — человек. Пути заражения цитомегаловирусом:
- половой;
- воздушно-капельный;
- бытовой;
- трансплацентарный.
Последний путь реализуется, если у беременной женщины произошло обострение хронической цитомегаловирусной инфекции или она заразилась впервые во время беременности. Вирус выходит в кровь, через плаценту проникает в организм плода. Риск заражения плода при первичной инфекции достигает 40%. При обострении хронической — не более 2%.
Цитомегаловирус при беременности способен проникнуть в плаценту через кровь женщины
Поражение органов плода
Чтобы произошло внутриутробное заражение плода, требуется наличие вируса в материнской крови. Ребенок может заразиться в родах, если цитомегаловирусом поражены слизистые оболочки половых путей. После заражения у плода развивается острая или хроническая цитомегаловирусная инфекция. Страдают все органы — сердце, легкие, органы пищеварения, почки, нервная система, глаза.
Основные проявления
Симптомы врожденной инфекции зависят от срока заражения. Если мать впервые заболела на сроке до 20 недель, развиваются тяжелые пороки, большинство из которых несовместимы с жизнью. Ребенок погибает внутриутробно или рождается глубоким инвалидом. На более поздних сроках прогноз относительно благоприятный.
Выраженная симптоматика наблюдается лишь у 15% новорожденных. У остальных инфекционный процесс протекает скрыто. У 2% детей наблюдаются клинические проявления в виде пневмонии. Выраженным процесс бывает редко, но протекает тяжело. Дети рождаются преждевременно, имеют низкую массу тела и признаки кислородного голодания. Характерны следующие признаки:
- увеличение печени и селезенки;
- желтушность кожи;
- пятнистая сыпь;
- водянка головного мозга;
- судороги;
- глухота;
- панкреатит;
- пневмония;
- катаракта.
Ребенок отказывается брать грудь, у него нарушен глотательный рефлекс. У детей с врожденным иммунодефицитом развивается генерализованная форма заболевания. Поражаются все органы, возникает полиорганный шок и нарушение свертываемости крови. Летальный исход наблюдается у 12% детей в возрасте до 6 недель.
У выживших детей развиваются отдаленные осложнения — глухота, задержка умственного и физического развития, ухудшение зрения вплоть до слепоты, судороги.
Бессимптомная инфекция не имеет выраженных клинических проявлений сразу после рождения. Однако часто наблюдается формирование поздних осложнений — потеря слуха, снижение зрения, снижение интеллекта. Проявляются эти состояния в 3-5 лет, поэтому ребенок до этого возраста должен находиться на диспансерном учете у педиатра.
У самой женщины заболевание в большинстве случаев протекает бессимптомно. При клинически выраженной форме признаки напоминают ОРВИ. Наблюдается умеренное повышение температуры, увеличение лимфоузлов и слюнных желез. Часто появляются слизистые выделения из носа.
Основной путь заражения плода - через кровь от матери
Что такое носительство
Некоторым женщинам ставят диагноз "носительство цитомегаловируса". Это самое частое состояние при данной инфекции. Формируется носительство после первичного инфицирования, которое женщина могла даже не заметить. Возбудитель проникает внутрь клеток и находится в неактивном состоянии.
Обнаруживается носительство с помощью исследования крови. Там выявляют высокоавидные IgG. ДНК возбудителя в биологических жидкостях не обнаруживается. Носительство не приводит к внутриутробному инфицированию, но женщине рекомендуют сдавать кровь на ЦМВ каждый триместр, чтобы исключить реактивацию инфекции.
Диагностика
Подтверждают диагноз ЦМВ-инфекции лабораторные анализы. Исследуют в основном кровь, реже мочу и слюну. Обнаруживаемые в крови специфические антитела не являются достоверным подтверждением заболевания. Часть из них новорожденный получает от матери. Диагностическое значение имеет увеличение IgM при двукратном исследовании.
При обнаружении специфических иммуноглобулинов определяют их авидность. Этот показатель говорит о давности их образования. Чем выше авидность, тем больше срок инфицирования. Низкая авидность говорит о недавнем заражении. Авидность определяется в процентах. Низкой она считается до 30%, высокой — более 60%. Промежуток 30-60% — пограничное значение, рекомендуется пересдать кровь еще раз.
Более точный метод диагностики — выявление ДНК вируса с помощью полимеразной цепной реакции. Диагностическое значение имеет обнаружение вируса в моче и крови ребенка. Если ДНК возбудителя обнаруживается в крови беременной женщины — это фактор высокого риска заражения плода.
Трудность диагностики обусловлена частыми случаями скрытого протекания инфекции, отсутствием признаков у женщины и разнообразием поражаемых органов.
Чтобы обнаружить цитомегаловирус при беременности, женщину обследуют по алгоритму:
- кровь на ДНК цитомегаловируса;
- моча;
- кровь на специфические иммуноглобулины;
- пуповинная кровь на ДНК вируса по показаниям.
Обследование проводят дважды за всю беременность. Более частое обследование рекомендуют ранее выявленным носителям ЦМВ-инфекции для исключения реактивации. Также дополнительное исследование проводят при наличии клинических проявлений инфекции.
Возможно провести внутриутробное обследование плода. Для этого берут околоплодные воды или пуповинную кровь. О заражении говорят, если обнаружены IgM или ДНК вируса. Выявить пороки, связанные с инфицированием, помогают ультразвуковое исследование, кардиотокография, допплерометрия.

Для подтверждения диагноза ЦМВИ берут анализ крови на антитела и ДНК возбудителя
Тактика лечения
Если инфицирование произошло у беременной женщины, ей разрешен только один препарат — человеческий иммуноглобулин антицитомегаловирусный. Его назначают по 1 мл на кг массы тела — женщине весом 60 кг потребуется 60 мл препарата. Вводят этот объем внутривенно капельно, в три приема за сутки. Через 1-2 недели повторяют введение лекарства.
Наибольшей эффективностью обладают противовирусные препараты ганцикловир или фоскарнет. Но они отличаются высокой токсичностью, поэтому длительное их применение невозможно. Они используются у новорожденных с генерализованной формой заболевания. Это позволяет снизить риск летального исхода, повысить вероятность излечения пневмонии, уменьшить неврологические проявления.
Новорожденных детей лечат иммуноглобулином или противовирусными препаратами на основе человеческого интерферона. Симптоматическую терапию проводят с учетом сформировавшихся осложнений. В целях дезинтоксикации проводят внутривенное вливание раствора глюкозы или реополиглюкина. При присоединении бактериальной флоры показаны антибиотики широкого спектра действия.
Важно обеспечить детям полноценное питание. Дополнительно назначают поливитамины.
При заражении на раннем сроке лечение малоэффективно. За течением беременности постоянно наблюдают. Если выявляются признаки пороков развития у плода, женщине предлагают прерывание беременности. Решение об этом она принимает самостоятельно.
Тактика ведения беременности и родов определяется индивидуально. Она зависит от клинических проявлений инфекции, вирусной нагрузки, выявленных патологических изменений плода. Если вирус обнаруживают в половых путях, предпочтительный путь родоразрешения — кесарево сечение.
Выздоровление новорожденного определяют при условии отсутствия специфических иммуноглобулинов и ДНК возбудителя в крови. Дети подлежат учету у инфекциониста с обследованием через 1, 3, 6 и 12 месяцев.
Прогноз
Прогнозировать течение ЦМВИ сложно, так как заболевание часто не имеет внешних проявлений или они возникают поздно. Наиболее благоприятный прогноз отмечается при инфицировании плода в конце третьего триместра или во время родов. Если женщина заболела до 12 недели беременности, в 95% случаев происходит выкидыш. Заражение в конце первого триместра или во втором грозит развитием тяжелых пороков у плода.
Меры профилактики
Этиотропной профилактики ЦМВ нет, вакцина тоже не разработана. Вирус активизируется только при снижении иммунитета, поэтому профилактика направлена на его поддержание:
- исключение контакта с инфекционными больными;
- рациональное питание;
- занятия спортом;
- прогулки на свежем воздухе.
Повторные беременности женщинам с активной ЦМВИ разрешены только после полного курса противовирусной терапии. Следует добиться стойкой ремиссии, чтобы ДНК возбудителя не определялась в крови на протяжении года.
Женщины-носители ЦМВ должны находиться под особым контролем гинеколога в случае беременности. Они входят в группу риска по внутриутробному инфицированию плода, что нередко приводит к формированию тяжелых последствий. Обследование на ЦМВ-инфекцию является обязательным для всех беременных или планирующих беременность.
Читайте также:


