Восприимчивость детского организма к инфекциям
Отечественные педиатры до настоящего времени в группу ЧБД относят детей на основании критериев, предложенных А. А. Барановым и В. Ю. Альбицким (табл.).
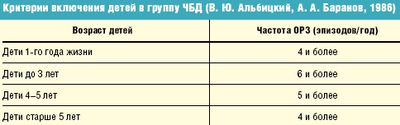
В то же время некоторые клиницисты высказывают мнение, что если у детей раннего возраста, особенно в период адаптации к детскому коллективу, острые респираторные вирусные инфекции (ОРВИ) протекают легко, то допустимая частота заболеваний может достигать до 8 раз в год.
Хорошо известно, что острые респираторные инфекции являются самыми частыми заболеваниями как у детей, так и у взрослых. Но наиболее высокий уровень заболеваемости респираторными инфекциями отмечается у детей дошкольного возраста, посещающих организованные коллективы. Частые ОРЗ у детей в настоящее время представляют не только медицинскую, но и социально-экономическую проблему.
С другой стороны, контакт и взаимодействие с респираторными инфекциями — необходимые условия становления иммунной системы ребенка, приобретение им иммунологического опыта, необходимого для адекватного реагирования на микробную агрессию. Однако частые респираторные заболевания, следующие одно за другим, безусловно, оказывают на ребенка негативное воздействие.
Таким образом, выделение диспансерной группы ЧБД является своевременным и актуальным, однако в каждом конкретном случае необходимо проводить комплексное обследование ребенка для уточнения причин у него высокого уровня респираторной заболеваемости. Диспансерное наблюдение за детьми, у которых повторные эпизоды респираторных инфекций обусловлены стойкими изменениями иммунитета, врожденными или наследственными заболеваниями, должно проводиться в строгом соответствии с основным заболеванием.
Основными возбудителями ОРЗ являются различные вирусы, тропные к эпителию дыхательных путей и способствующие их вторичной колонизации бактериями. Вирусные инфекции повреждают эпителий дыхательных путей и вызывают воспаление слизистой оболочки. Для воспаления респираторного тракта характерно повышение продукции вязкой слизи, что проявляется насморком и кашлем. Вязкий секрет способствует прилипанию (адгезии) возбудителей респираторных инфекций на слизистых оболочках респираторного тракта, что создает благоприятные условия для развития бактериальной суперинфекции. В свою очередь микроорганизмы и их токсины ухудшают движение ресничек эпителия, нарушают дренажные функции бронхиального дерева, снижают бактерицидные свойства бронхиального секрета и местную иммунологическую защиту дыхательных путей с высоким риском развития затяжного и хронического течения воспалительного процесса. Поврежденный эпителий бронхов имеет повышенную чувствительность рецепторов к внешним воздействиям, что значительно повышает вероятность развития бронхоспазма и бактериальной суперинфекции.
Основными бактериальными возбудителями ОРЗ являются пневмотропные микроорганизмы, в т.ч. пневмококк и другие грамположительные кокки, палочка гемофилюс инфлюенца, моракселла катаралис, атипичные возбудители (микоплазма, хламидофила пневмонии) и пр. Считают, что первичная вирусная инфекция часто приводит к активации эндогенной условно-патогенной флоры. Причина более легкой трансформации этой микрофлоры в патогенную у ряда детей связана с индивидуальными особенностями иммунного ответа, нарушением барьерной функции респираторного тракта, снижением местного иммунитета, а также с суперинфицированием бактериальными агентами. Присоединение бактериальной инфекции приводит к нарастанию тяжести заболевания и может быть основной причиной неблагоприятного исхода болезни. Характер клинической картины ОРЗ во многом обусловлен патогенными свойствами возбудителя. Однако известно, что чем моложе ребенок, тем меньше специфических признаков имеет заболевание.
Таким образом, инфекционное воспаление является основным патогенетическим звеном клинических проявлений острых респираторных инфекций. Развитие воспаления слизистой оболочки верхних и нижних дыхательных путей способствует гиперсекреции вязкой слизи, формированию отека слизистой оболочки респираторного тракта, нарушению мукоцилиарного транспорта и бронхиальной обструкции. Это приводит к заложенности носа, выделениям носового секрета, гиперемии зева, боли в горле, отеку миндалин, осиплости голоса, появлению кашля и других симптомов острого респираторного заболевания, в том числе ларинготрахеита и острого бронхита. У части больных развивается обструктивный бронхит.
Лечение
Известно, что до настоящего времени не существует универсальных и безопасных химиопрепаратов, эффективных в отношении большинства респираторных вирусов. Противовирусные химиопрепараты (рибавирин и др.) у детей применяют только при тяжелом течении ОРВИ установленной этиологии. Использование противовирусных мазей типа Оксолиновой может рассматриваться только как профилактическое средство, а назначение таких препаратов, как Ремантадин, детям первых лет жизни противопоказано вследствие его высокой токсичности и недостаточной эффективности.
Достаточно широкое применение при вирусных респираторных инфекциях нашли препараты интерферона, которые как факторы защиты и средства поддержания иммунитета обладают самым широким спектром профилактического и лечебного действия. Интерфероны — естественные факторы защиты, то есть вырабатываются самим организмом при его контакте с инфекциями различного происхождения (вирусами, бактериями, грибами и др.). Следовательно, применение препаратов интерферона абсолютно естественно для человека. Кроме того, в силу своих биологических особенностей воздействия на возбудителей инфекций, интерфероны являются универсальными защитниками, они эффективны в отношении всех респираторных вирусов. Помимо противовирусного и противомикробного воздействия препараты интерферона повышают собственные защитные силы и предотвращают вредное воздействие радиации на организм человека.
Очевидно, что в практическом здравоохранении препараты интерферона широко применяются. Сначала это были препараты лейкоцитарного интерферона, получаемого из донорской крови. Впоследствии развитие биотехнологии позволило создать рекомбинантные (генно-инженерные) препараты человеческих интерферонов, во многом превосходящие препараты первого поколения. В настоящее время существует довольно много препаратов рекомбинантных интерферонов как отечественного, так и зарубежного производства: Виферон, Реаферон, Гриппферон, Реальдирон, Интрон А, Роферон-А и др.
Иммунокоррегирующие и иммуномодулирующие препараты при ОРЗ оказывают как профилактический, так и лечебный эффект. Имеются убедительные данные о высоком терапевтическом эффекте при лечении детей с гриппом и ОРВИ индукторов эндогенного интерферона (Амиксин, Арбидол, Циклоферон). При этом Арбидол может быть использован у детей начиная с 2-летнего возраста, Циклоферон разрешен для применения у детей старше 4 лет, а Амиксин — только у детей старше 7 лет. Безусловно, синтетические иммуностимуляторы, препараты тимического происхождения и некоторые другие обладают выраженными эффектами на иммунную систему, однако решение о необходимости их применения, особенно у детей, должно приниматься только после клинико-иммунологического обследования, уточнения типа дисфункции иммунной системы и при наличии четких клинико-иммунологических показаний. При этом сама терапия должна проводиться при обязательном клиническом мониторинге и иммунологическом контроле.
Очень эффективным иммуномодулятором является повышение температуры тела, когда усиливается синтез естественной иммунной защиты — интерферонов. Многие микроорганизмы не могут размножаться при температуре 38°С. Поэтому снижать температуру до 39°С у взрослых и 38,5°С у детей не рекомендуется (речь идет о здоровых в остальном людях), если подъем температуры не сопровождается сильной головной болью, ломотой в мышцах и суставах. В качестве жаропонижающих препаратов у детей можно использовать только препараты парацетамола или ибупрофена. Комплексные противопростудные препараты, вопреки создающемуся из-за рекламы впечатлению, не лечат респираторную инфекцию, а только облегчают ее симптомы.
Антибактериальная терапия системными антибиотиками при ОРЗ малоэффективна и показана крайне редко, не более чем в 10% всех случаев заболевания. Назначив системный антибиотик без должных оснований, врач повышает риск побочных явлений, нарушает микробиоценоз, способствует снижению иммунитета и распространению лекарственной резистентности. Местная антибактериальная терапия обеспечивает непосредственное воздействие на очаг инфекции, создает оптимальную концентрацию препарата и не имеет системных побочных эффектов. Одним из лучших местных антибактериальных препаратов для лечения ОРЗ у детей и взрослых является фюзафюнжин (Биопарокс), который уникален благодаря своему двойному действию: антибактериальному и противовоспалительному.
Для воспалительных заболеваний респираторного тракта характерно изменение вязкости мокроты и снижение мукоцилиарного клиренса. Если перистальтические движения мелких бронхов и деятельность реснитчатого эпителия не обеспечивают необходимого дренажа, развивается кашель. Следовательно, кашель — это защитный рефлекс, направленный на восстановление проходимости дыхательных путей. Очевидно, что необходимость в подавлении кашля у детей с использованием истинных противокашлевых препаратов с патофизиологических позиций не оправдана. Целью рациональной терапии является разжижение мокроты, снижение ее адгезивности (вязкости) и увеличение тем самым эффективности кашля. Для этого используют лекарственные средства, стимулирующие отхаркивание (фитопрепараты, щелочные растворы) и муколитики (бромгексин, амброксол, ацетилцистеин и др.). Эти препараты улучшают мукоцилиарный клиренс и тем самым способствуют уменьшению воспаления слизистых оболочек респираторного тракта.
Острые респираторные инфекции у часто болеющих детей иногда могут протекать очень тяжело, с выраженным токсикозом, гипертермией, синдромом ацетонемической рвоты, бронхообструктивным синдромом. Лечение в этом случае должно строиться с учетом необходимой посиндромной терапии. При тяжелом и/или осложненном течении ребенок нуждается в госпитализации и проведении лечения в условиях стационара.
Таким образом, лечение острых респираторных заболеваний у часто болеющих детей является актуальной, но непростой задачей. Комплексная терапия должна строиться с учетом основных этиологических и патогенетических факторов заболевания, а использование современных фармакологических препаратов обеспечивает эффективность проводимого лечения. В то же время своевременное проведение профилактических мероприятий может существенно уменьшить частоту респираторных инфекций у детей.
Профилактика
Наилучшей системой профилактики острых респираторных заболеваний у часто болеющих детей, безусловно, является формирование собственного адекватного иммунного ответа. Способствуют этому здоровый образ жизни, рациональный режим дня, полноценное питание, разнообразные программы закаливания.
Профилактика респираторных инфекций часто болеющих детей предусматривает ограничение контактов ребенка с больными гриппом и ОРВИ, проведение санитарно-гигиенических мероприятий, сокращение использования городского транспорта и удлинение времени пребывания ребенка на воздухе. Частая респираторная заболеваемость тесно связана с пассивным курением, поэтому прекращение его — важное условие лечения и профилактики. Все дети, склонные к частым респираторным инфекциям, должны быть осмотрены и, при необходимости, пролечены ЛОР-врачем.
Основными методами повышения сопротивляемости ребенка инфекционным агентам служит закаливание. Систематическое контрастное воздушное или водное закаливание сопровождается повышением устойчивости организма к температурным колебаниям окружающей среды и повышением иммунологической реактивности организма. Адаптационные возможности ребенка хорошо поддаются тренировке. Использование любых методов закаливания совершенствует работу аппарата терморегуляции и расширяет возможности приспособления организма к изменившимся температурным условиям. Закаливание не требует очень низких температур, важна контрастность воздействия и систематичность проведения процедур. Хорошо закаливают воздействия на подошвы ног и, постепенно — на всю кожу туловища и конечностей. Максимальная длительность закаливающих процедур не должна превышать 10–20 минут, гораздо важнее его регулярность и постепенность. Было показано, что у часто болеющих детей сочетание местных закаливающих процедур стоп и носоглотки через 3–4 месяца восстанавливало цитологические показатели носового секрета. Закаливающие процедуры хорошо сочетать с проведением гимнастики и массажа грудной клетки. Закаливание после нетяжелого ОРЗ можно возобновить (или начать) через 7–10 дней, при заболевании с длительностью температурной реакции более 4 дней — через 2 недели, а после 10-дневной лихорадки — через 3–4 недели. Эффективность закаливания можно оценить не ранее чем через 3–4 месяца, а максимальный эффект наблюдается через год от начала регулярных процедур.
Учитывая ведущую роль дисфункций иммунитета в развитии повышенной восприимчивости детского организма к респираторным инфекциям, кроме комплекса общеукрепляющих мероприятий с целью профилактики используется целый ряд иммуномодулирующих лекарственных средств. При этом большинство авторов подчеркивают, что использование иммуномодулирующих препаратов с целью предупреждения респираторных инфекций у часто болеющих детей должно проводиться на фоне обязательного соблюдения общих принципов профилактики и оздоровления.
Так, существуют рекомендации по сезонному курсовому (1–2 раза в год) применению препаратов рекомбинатного интерферона (Виферона, Гриппферона) с целью повысить неспецифическую резистентность часто болеющих детей к острым респираторным заболеваниям.
Через активацию врожденного и адаптивного иммунитета происходит поддержание целостности слизистых и развитие полноценной защиты респираторного тракта. Из средств неспецифической профилактики хорошо известны растительные адаптогены: китайский лимонник, элеутерококк, женьшень, эхинацея, левзея. Наиболее часто применяются препараты, полученные из эхинацеи (Иммунал, Иммунорм, Эхинацин ликвидум). Хорошо зарекомендовал себя Биоарон С (сочетание алоэ и черноплодной рябины).
В настоящее время возрос интерес к иммуномодулирующим лекарственным средствам бактериального происхождения, обладающим также и вакцинальным эффектом, которые не только повышают активность неспецифических факторов иммунной защиты, но и способствуют формированию специфического иммунного ответа к наиболее значимым пневмотропным бактериальным возбудителям. Среди современных иммуномодуляторов бактериального происхождения выделяют высокоочищенные бактериолизаты, мембранные фракции и рибосомальный иммуномодулятор Рибомунил, в состав которого входят не лизаты бактерий, а их рибосомы и фрагменты клеточной стенки (протеогликаны), что и определяет высокую клинико-иммунологическую эффективность и минимальную реактогенность этого препарата, сочетающего свойства вакцины и неспецифического иммуномодулятора.
Часто возникает вопрос о возможности одновременного проведения календарной вакцинации или гриппозной прививки детям, получающим лечение бактериальными вакцинами. Специальными исследованиями было показано, что такое сочетание не только возможно, но и желательно, поскольку оно может сопровождаться усилением иммунного ответа. Вполне оправдано и совмещение профилактической вакцинации с началом лечения бактериальными вакцинами.
Вообще вакцинация часто болеющих детей является одним из самых важных профилактических мероприятий. Частые ОРВИ не фигурируют в списке противопоказаний к проведению прививок. Поскольку частые ОРВИ у этой группы детей не свидетельствуют о наличии иммунодефицита, они не могут быть поводом для отвода от прививок. По окончании ОРВИ, как и других острых заболеваний, прививки возможно проводить через 2–3 недели после нормализации температуры.
По вопросам литературы обращайтесь в редакцию.
ВОСПРИИМЧИВОСТЬ, к инфекции — способность организма реагировать на внедрение инфекционных агентов развитием заболевания, инаппарантной (бессимптомной) инфекции или микробоносительства. Различают В. видовую, присущую всем особям того или иного вида, а также индивидуальную, касающуюся лишь отдельных представителей данного вида. Как видовая, так и индивидуальная В. может быть полной, высокой, умеренно выраженной, слабой или же она полностью отсутствует. В. проявляется по отношению к определенным видам, серологическим и биохим, типам патогенных и условно патогенных микроорганизмов. Степень и конкретные проявления В. к тому или иному возбудителю могут изменяться в процессе эволюции данного вида — реципиента или заражающего его агента.
Под индивидуальной В. принято понимать предрасположенность отдельных индивидов к возникновению у них инфекции или микробоносительства под влиянием заражающего агента. Конкретные проявления и степень индивидуальной В. живых организмов, в т. ч. человека, определяются той или иной степенью их иммунитета, приобретенного в результате ранее перенесенной инфекции той же этиологии, а также профилактических прививок, с пи жен пом реактивности, наличием сопутствующих заболеваний.
Микробы, патогенные для различных видов животных, птиц, рыб, растений, нередко не в состоянии вызвать у человека инфекцию или микробоносительство. Видовая восприимчивость по отношению к различным микроорганизмам генетически обусловлена и в значительной мере определяется особенностями биохим, состава клеток и тканей организма. Пороговая заражающая доза патогенных микроорганизмов зависит от их вирулентности (см.). Известен факт, что штаммы туляремийных бактерий, циркулирующие в отдельных географических зонах, могут существенно различаться по степени своей вирулентности, благодаря чему (в сочетании с определенной В. и реактивностью отдельных людей) клиническая картина заболеваний туляремией отличается значительной вариабельностью.
Видовая В. людей к чуме является всеобщей, хотя индивидуальная В. может существенно снижаться благодаря применению специфических прививок или проведению химиопрофилактики стрептомицином, подавляющим развитие чумных бактерий, уже проникших в организм.
Видовую, а также индивидуальную В. следует рассматривать в тесной связи с конкретным механизмом заражения, входными воротами, через к-рые инфекционный агент проникает в организм. Эти обязательные условия В. человека к различным инфекциям в ряде случаев отличаются высокой специфичностью. Так, напр., человек заболевает дизентерией только при условии проникновения шигелл через пищеварительный тракт, а не каким-либо иным путем. Вместе с тем в отношении ряда инфекционных заболеваний (напр., сибирская язва) В. проявляется независимо от входных ворот инфекции и может обусловить значительный полиморфизм конкретных клинических проявлений болезни. Заболевание ботулизмом может возникнуть как в результате поступления возбудителя и его экзотоксина через пищеварительный тракт, так и при их проникновении в организм через дыхательные пути. Однажды перенесенное инфекционное заболевание в ряде случаев создает невосприимчивость к действию того же агента. После таких заболеваний, как натуральная оспа, корь, В. к реинфекции резко снижается, вследствие чего повторные заболевания представляют большую редкость, организм приобретает прочный, пожизненный иммунитет (см). Вместе с тем однажды перенесенное острое инфекционное заболевание может сопровождаться такими неблагоприятными для организма изменениями его В. к инфекционному агенту, к-рые создают предпосылки для развития рецидивов (брюшной тиф, возвратный тиф, дизентерия и др.), а также затяжных и хронически протекающих форм инфекционных болезней (напр., бруцеллез). В этих случаях проявляется аллергическая перестройка организма, как это имеет место при рецидивирующих формах рожи.
Возраст человека также влияет на его В. У детей отмечают более высокую, чем у взрослых, В. к воздушно-капельным инфекциям (кори, скарлатине, коклюшу, дифтерии). Эта возрастная особенность В. к воздушно-капельным инфекциям отражается и на клиническом течении инфекционных болезней. Известно, что менингококковая инфекция протекает, как правило, тяжелее в детском возрасте. У детей первых двухтрех месяцев жизни происходит передача с молоком матери нек-рых антител, в т. ч. дифтерийного антитоксина, что (несмотря на несовершенство многих механизмов иммунитета, свойственное детям этого возраста) препятствует заражению дифтерией. Вместе с тем В. к ряду инфекций у людей пожилого и старческого возраста также имеет свои особенности, напр, длительное (торпидное) течение туберкулеза легких у людей с пониженной реактивностью организма этих возрастных групп.
Генетические основы индивидуальной В. человека к инфекциям остаются пока еще мало изученными. Исследуется роль вилочковой железы, иммуноглобулинов разных классов, факторов клеточного иммунитета. Изменения индивидуальной В., создаваемые профилактическими прививками, могут колебаться в очень широких пределах, что зависит прежде всего от реактивности организма (см.), степени развития его защитных механизмов, иммуногенных свойств вакцины.
На уровень индивидуальной В. людей к инфекциям оказывают влияние такие факторы, как переохлаждение или перегревание организма, ионизирующая радиация, действие иммунодепрессантов. Повышенная В. людей к инфекционным болезням может быть вызвана аллергическими процессами.
Установлены многочисленные факты более высокой индивидуальной В. людей к инфекционным болезням в тех случаях, когда имеется врожденная или приобретенная гипо- и агаммаглобулинемия (см.) и другие иммунодефицитные состояния (см. Иммунологическая недостаточность). Изменения условий питания человека (в т. ч. алиментарная дистрофия, гипо- и авитаминозы), нарушения гормональных регуляций могут повышать В. людей к инфекциям.
Библиогр.: Бернет Ф. М. Клеточная иммунология, пер. с англ., М., 19 71, библиогр.; Бойд У. Основы иммунологии, пер. с англ., М., 1969, библиогр.; Бун и н К. В. Успехи и задачи клинической иммунологии инфекционных болезней, М., 1972; Эфроимсон Э. П. Иммуногенетика, М., 1971.
Восприимчивость — I)видовое свойство специфического и неспецифического хозяина стать средой обитания для паразита, характеризуется развитием патологических процессов или бессимптомным течением; 2) способность отвечать инфекционным процессом на внедрение возбудителя. Степень восприимчивости определяется неспецифическими
факторами зашиты (воспалительная реакция и др.) и иммунитетом.
Восприимчив организм-это 3 звено эпид процесса. Степень восприимчивости зависит от реактивности,котор определяется неспецифич(резистентность) и специфич( иммунитет)
Резистентность- совокупность неспецифич факторов защиты (непроницаемость кожи,лейкины).
Различают видовую и индивидуальную. Видовая рез-ть- совокупность защитных факторов, присущих данному виду. Индивидуальная- совокупность защитных факторов, присущих данному индивиду.
фактором восприимчивости к инфекциям является возраст. Общеизвестно, что более восприимчивы к инфекции дети и люди пожилого возраста, у детей высокая степень восприимчивости сочетается со слабо выраженными тканевыми изменениями в очаге инфекции
Иммунитет-способ защиты организма от живых тел и веществ, несущих на себе признаки генетической чужеродности. Различают активный и пассивный, постинфекционный и поствакципальный, а по механизму развития — антитоксический, антимикробный, гуморальный,
клеточный, общий и местный иммунитет. Популяция людей неоднородна по способности вырабатывать и сохранять иммунитет.
Иммунный ответ осуществляется имун сист. (совокуп лимфоидн органов и тканей) К центральным органам относятся костный мозг и вилочковая железа, к периферическим - селезенка, лимфоузлы, лимфоидная ткань слизистых оболочек и лимфоидная ткань, ассоциированная с кожей. Централ звено имун сист- Т4-лимфоциты-распознают а/г , выделяют медиаторы и запускают реакции клеточн и гуморал иммунитета. Происходит диф-ка и деление Т-клеток(киллеров) ,и В-лимфоцитов,превращ в плазматич кл-ки и продуцир а/т к дан а/г. После уничтожен чужерод агента-Т-супрессоры останавлив имунопоэз. Выделяют первич и вторич иммун ответ-при повтор встрече с а/г(за счет клеток-памяти
Естественный активный иммунитет появляется в результате контакта с возбудителем (после перенесенного заболевания или после скрытого контакта без проявления симптомов болезни).
Естественный пассивный иммунитет возникает в результате передачи от матери к плоду через плаценту (трансплантационный) или с молоком (колостральный) готовых защитных факторов - лимфоцитов, антител, цитокинов и т.д.
Искусственный активный иммунитет индуцируется после введения в организм вакцин, содержащих микроорганизмы или их субстанции - антигены.
Искусственный пассивный иммунитет создается после введения в организм готовых антител или иммунных клеток. Такие антитела содержатся в сыворотке крови иммунизированных доноров или животных
Первый иммунный кризис по времени совпадает с периодом новорожденности, когда организм впервые встречается с огромным количеством чужеродных антигенов.
Установлено, что у новорожденных, по сравнению со взрослыми, способность к продукции а- и у-интерферона значительно меньше. У детей от 1 года до 3 лет биологические свойства интерферона такие же как у взрослого человека. Однако способность к продукции а- и у-интерферона у детей до 3 лет остается сниженной. Вследствие недостаточности интерфероногенеза у детей раннего возраста отмечается склонность к частым инфекционно-воспалительным заболеваниям. Установлено, что интерфероны обладают антивирусным, антибактериальным, антипролиферативным и иммуномодулирующим действием.
Второй критический период в иммунном статусе ребенка приходится на возраст 3-6 мес. Он характеризуется постепенным ослаблением пассивного гуморального иммунитета из-за уменьшения концентрации материнских иммуноглобулинов, полученных еще в эмбриональном периоде.
Третий иммунный кризис в жизни всех детей связан с резкой гормональной перестройкой организма подростков. У девочек этот этап начинается с 12-13 лет, у мальчиков - с 14-15 лет. В иммунной системе при этом происходят следующие изменения:
уменьшается масса лимфоидных органов, что связано с пубертатным скачком роста и веса детей;
подавляется функция Т-системы (клеточный иммунитет);
стимулируется функция В-системы (гуморальный иммунитет).
Сдвиги в функции иммунитета обусловлены повышенной секрецией половых гормонов.
Не нашли то, что искали? Воспользуйтесь поиском:
М. Л. Земляникина-Огнева
Если ребенок часто болеет. Лечение, профилактика, питание, закаливание, гимнастика
Введение
В практической работе к ЧБД относят пациентов с кратностью острых респираторных заболеваний и/или обострениями хронических воспалительных заболеваний носоглотки:
– в возрасте до 1 года – 4 заболевания и более за год;
– в возрасте 1–3 лет – 6 и более;
– в возрасте 4–5 лет – 5 и более;
– старше 5 лет – 4 и более.
По данным различных авторов, ЧБД составляют в общей популяции детского населения в среднем от 14 до 18 %. Наибольший процент ЧБД регистрируется в первый год посещения детских дошкольных учреждений (до 40 %). Затем с возрастом и с адаптацией ребенка к детскому коллективу количество ЧБД уменьшается.
Заболеваемость часто болеющих детей обусловлена в основном (до 80 %) острыми респираторными вирусными инфекциями (ОРВИ).
Две трети заболеваемости приходится на первые семь лет жизни.
Факторы риска для детей
Возникновению частых респираторных заболеваний способствует повышенное число контактов с источниками инфекции, а также эндогенные (внутри организма, в основном это незрелость иммунной системы) и экзогенные (внешние, из окружающей среды, например, большое число контактов с людьми) факторы, повышающие восприимчивость к ним.
Среди внешних (экзогенных) или, по-другому, управляемых факторов, на которые могут и должны активно влиять родители и врачи, наибольшую роль играют следующие:
– низкий уровень санитарной культуры семьи и, как следствие этого, несоблюдение правил здорового образа жизни в качестве наиболее действенного подхода к формированию здоровья. Дефекты ухода за детьми, пренебрежение закаливанием и занятиями физической культурой, нерациональные питание и режим дня способствуют повышению восприимчивости детского организма к заболеваниям ОРВИ;
– когда ребенка в семье перекармливают, перекутывают, ограничивают прогулки из-за боязни простуды, отказываются от гимнастики и закаливающих мероприятий. Как правило, это семьи с высокими доходами;
– начало посещения детьми дошкольных учреждений в раннем возрасте, в котором наблюдается повышенная восприимчивость детей к респираторным заболеваниям (особенно до 3-летнего возраста). Причиной заболеваний также может быть большое число контактов в транспорте и др.;
– проживание в экологически неблагоприятных районах способствует повышению заболеваемости ОРВИ и увеличению числа ЧБД, что связано с повышением степени бронхиальной гиперреактивности под влиянием вредных примесей в воздухе. Последняя, в свою очередь, приводит к более тяжелым проявлениям ОРВИ, развитию осложнений, более длительному течению заболеваний;
– нерациональное использование различных лекарственных средств (частое длительное и необоснованное применение антибиотиков и жаропонижающих препаратов), которые активно нарушают работу защитных факторов самого организма ребенка;
– нерациональное проведение прививок – непосредственно перед началом посещения садика.
Известно, что проведение ребенку прививки монокомпонентной вакциной ведет к перестройке функционирования иммунной системы с временным ослаблением некоторых защитных механизмов на 1–2 недели, а прививка поливалентной вакциной (против нескольких инфекций одновременно) – на 3–4 недели. Родители же часто откладывают проведение профилактических прививок на время непосредственно перед началом посещения садика. И, конечно, такое искусственно вызванное нарушение в защитных силах организма ребенка ведет к более быстрому и легкому инфицированию. Заболевание возникает на 2-3-й день пребывания в группе;
– хронические заболевания ЛОР-органов у родственников, проживающих с ребенком (особенно матери). При пользовании общей посудой, облизывании ложек, сосок происходит постоянное заражение ребенка в домашних условиях;
– отсутствие профилактики адаптационного синдрома перед началом посещения садика. Ребенок адаптируется к новым условиям жизни в течение 3–6 недель, в это время у него отмечается переутомление, перевозбуждение нервной системы, и как результат стрессовой ситуации возникает снижение защитных сил организма и на этом фоне – заболевание.
К внутренним (эндогенным), или неуправляемым, факторам риска возникновения частых респираторных инфекций у детей можно отнести:
– неблагоприятные до– и/или послеродовые факторы развития ребенка (недоношенность, морфо-функциональная незрелость, гипотрофия, анемия, рахит, раннее искусственное вскармливание), отражающиеся на созревании и функционировании иммунной системы и других защитных факторов и механизмов;
– гипоксия в родах, энцефалопатия ведут к нарушениям функционирования центральной и вегетативной нервной системы и, как следствие, нарушениям процессов адаптации к факторам внешней среды и расстройствам терморегуляции, способствуют повышению восприимчивости организма к респираторной инфекции;
– раннее искусственное вскармливание, отражающееся на созревании и функционировании иммунной системы и других защитных факторов и механизмов.
С молоком матери ребенок получает постоянно весь комплекс необходимых ему иммунных факторов, предохраняющих от заболеваний в первые годы жизни. В норме собственные защитные механизмы начинают активно вырабатываться только к 5 годам, а у детей с неблагоприятным развитием – еще позже;
– аллергия, особенно имеющая наследственный характер, способствует неадекватной иммунной реактивности, ведет к более кратковременной иммунной защите и, как следствие, большей респираторной заболеваемости у детей с аллергическими заболеваниями;
– очаги хронической инфекции рото– и носоглотки, сопровождающиеся снижением эффективности местного иммунитета и местных факторов защиты и способствующие повышению восприимчивости к инфекционным возбудителям;
– нахождение на слизистой оболочке носоглотки вирусов (чаще аденориновирусов) и патогенной микрофлоры (преимущественно стафилококка и стрептококка);
– снижение активности факторов защиты местного иммунитета слизистой оболочки дыхательных путей (уровня секреторных иммуноглобулинов, синтеза интерферона, лизоцима и др.);
– нарушение процессов терморегуляции и термоадаптации, способствующих приспособлению организма к изменениям температуры окружающей среды;
– нарушение нормального состава микрофлоры кишечника, которая, как показали исследования последних лет, активно стимулирует созревание иммунных механизмов ребенка.
У каждого часто болеющего ребенка имеются свои внешние и внутренние факторы, предрасполагающие его к повторным заболеваниям. Поэтому первым делом необходимо проанализировать особенности развития и быта ребенка и активно проводить их коррекцию.
Проведенные исследования показали, что группа ЧБД является разнородной по характеру сопутствующих нарушений в состоянии здоровья. Даже в клинически спокойный период (когда родители и врачи считают их здоровыми) у них выявляются различные нарушения в состоянии здоровья (индивидуальные для каждого конкретного ребенка) в виде: хронических заболеваний ЛОР-органов, аллергически измененной реактивности организма, поражения зубов кариесом, заболеваний нервной системы (последствия перенесенной в раннем возрасте энцефалопатии, невротических состояний, синдрома гиперреактивности с дефицитом внимания и др.), различной патологии внутренних органов, нарушения нормального состава микрофлоры на слизистой носоглотки и кишечника и др. В 60 % случаев выявляется сочетание различных из перечисленных нарушений.
Прежде всего, часто болеющие дети нуждаются в тщательном осмотре педиатром и обязательном осмотре ЛОР-врачом, который оценивает состояние миндалин, аденоидов, придаточных полостей носа и барабанной перепонки (см. рис. 1, 2), так как среди ЧБД хронические заболевания ЛОР-органов встречаются в 58–60 % случаев. И поэтому добиться успеха в оздоровительных мероприятиях без настойчивого лечения хронической ЛОР-патологии невозможно.


Обязательной практикой должно быть проведение посева со слизистой оболочки зева и носа для оценки характера микробного пейзажа. Следует учитывать, что микробиоценоз слизистой оболочки является одним из важнейших звеньев противоинфекционной защиты организма ребенка.
Также может потребоваться обследование на так называемые атипичные инфекции (хламидиоз, микоплазмоз).
При обследовании ЧБД обнаруживается довольно интенсивная микробная колонизация слизистой оболочки грибами рода Candida, стафилококками, гемофильной палочкой, моракселлой катарралис, энтеробактериями (в том числе клебсиеллой и кишечной палочкой), которые не присутствуют в нормальном состоянии организма и требуют проведения специальных мероприятий по их замене на здоровую микрофлору.
Выраженные нарушения микробного пейзажа носоглотки снижают устойчивость организма к патогенным возбудителям, поддерживают длительный воспалительный процесс.
Как показали проведенные научные исследования, основной причиной повторения заболеваний у ЧБД является недостаток факторов местных защитных сил организма во входных воротах инфекции, а именно, на слизистой оболочке носоглотки. Даже в клинически спокойный период у них выявляется снижение уровня иммуноглобулинов, специфических антител к различным вирусам, лизоцима и др. по сравнению с детьми, болеющими эпизодически.
Степень недостаточности защитных факторов местного иммунитета носоглотки определяется ее клиническим состоянием: наличием хронической воспалительной патологии (хронического аденоидита, синусита, тонзиллита, отита, гайморита), аллергическими заболеваниями или, наоборот, их отсутствием. А причиной снижения выработки защитных механизмов является приведенная выше совокупность эндогенных и экзогенных факторов, индивидуальная для каждого конкретного ребенка.
Для проведения оздоровительных мероприятий необходим индивидуальный подход к каждому ребенку и формирование оздоровительных групп и программ исходя из уровня нарушения в состоянии здоровья, определяемого после углубленного врачебного и лабораторного обследования.
Мероприятия, направленные на оздоровление ЧБД, должны учитывать все многообразие причин, способствующих повторным заболеваниям.
Реабилитацию ЧБД следует проводить на всех этапах без исключения: в семье, в садике, в поликлинике, в санатории.
Программа оздоровления обязательно должна включать группы мероприятий, направленных на:
– укрепление состояния здоровья (по индивидуальным программам);
– адекватную терапию основного заболевания;
– восстановительное лечение в период между заболеваниями.
Основополагающими принципами оздоровления должны быть:
– индивидуальность (учитывая особенности нарушений состояния здоровья каждого конкретного ребенка);
Читайте также:


