Внутрибольничные инфекции особенности лабораторной диагностики
На тему: Возбудители внутрибольничных инфекций. Особенности лабораторной диагностики.
Выполнил: Шмонин В.М.
Алматы, 2015 г.
Возбудители внутрибольничных инфекций.
Группы возбудителей внутрибольничных инфекций.
Методы лабораторной диагностики ВБИ.
Основные принципы лабораторной диагностики ВБИ.
Методы лабораторной диагностики.
Возбудители внутрибольничных инфекций. Группы возбудителей внутрибольничных инфекций.
Примерно 90% всех внутрибольничных инфекций имеют бактериальное происхождение. Вирусы, грибы и простейшие, а также эктопаразиты встречаются значительно реже. Попытка суммировать представления о микробной этиологии ВБИ не отражает всего многообразия и сложности их этиологической структуры. Некоторые из микроорганизмов (например, стафилококки, эшерихии, клебсиеллы, синегнойная палочка и др.) вызывают разные клинические формы ВБИ, другие выделяются только при определенных клинических состояниях (анаэробные микроорганизмы, например, встречаются преимущественно как возбудители ВБИ при глубоких инфекциях мягких тканей или при интраабдоминальных хирургических инфекциях). Некоторые возбудители поражают преимущественно определенные группы пациентов (парвовирус В19, вирусы кори, краснухи, ветряной оспы и эпидемического паротита в педиатрической практике; хламидии, микоплазмы, стрептококки группы В у новорожденных и родильниц и т. п.). Различия в экологических свойствах возбудителей ВБИ, среди которых присутствуют все возможные варианты (от облигатных внутриклеточных паразитов до свободноживущих микроорганизмов), также могут быть весьма существенными, определяя, в свою очередь, соответствующие особенности механизма развития эпидемического процесса в ЛПУ.
В таблице представлена группировка возбудителей внутрибольничных инфекций, в основе которой лежат эпидемиологические аспекты. Эта группировка отнюдь не претендует на право классификации возбудителей ВБИ, однако для эпидемиологов является полезной.
Первая группа возбудителей внутрибольничных инфекций — патогенные агенты — возбудители традиционных инфекций, не имеют в госпитальных условиях специфических черт. Они получают, как правило, большее распространение в стационарах в связи с высокой концентрацией и тесным общением в лечебном учреждении госпитализированных больных. Не исключено, что в какой-то степени сказывается и пониженная общая резистентность организма. Вторая подгруппа среди патогенных микроорганизмов также отражает интенсификацию в больницах процессов, которые могут быть и вне лечебного учреждения. Но в данном случае речь идет об интенсификации ятрогенного действия — медицинских вмешательств. В связи с тем, что госпитальный процесс является кратковременным эпизодом в циркуляции этих возбудителей, формирование вирулентных штаммов, опасных для госпитальных больных, не успевает произойти.
Группировка возбудителей внутрибольничных инфекций с учетом эпидемиологических данных 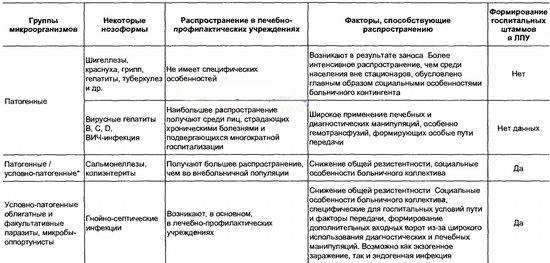
Вторая группа возбудителей внутрибольничных инфекций — это облигатные паразиты, но их патогенность более всего проявляется в госпитальных условиях. Разбираемая группа микроорганизмов вызывает заболевания, которые, в основном, регистрируются среди больничных контингентов. Связано это в первую очередь с пониженной сопротивляемостью организма госпитализированных больных и в определенной степени — с реализацией путей передачи, которые имеют определенный специфический характер. В таких условиях возможно формирование госпитальных штаммов.
Но наиболее специфична для стационаров третья группа возбудителей внутрибольничных инфекций — условно-патогенные микроорганизмы (УПМ), Возникновение и распространение заболеваний, вызванных УПМ, целиком и полностью определяются причинами, которые действуют лишь в госпитальных условиях.
Уже упоминалось, что условно-патогенные микроорганизмы могут вызвать сходные заболевания и по характеру патологического процесса, и по локализации. Однако это совсем не значит, что у них не проявляются определенные специфические характеристики.
Среди специалистов бытовало мнение, что имеет место смена возбудителей (УПМ) внутрибольничных инфекций. Утверждалось, что на смену золотистому стафилококку пришла синегнойная палочка и т. д. Однако современные данные показывают, что речь идет не о закономерной смене возбудителей ВБИ, а их способности существовать в условиях медицинских отделений, специализирующихся на лечении больных с определенной патологией.
Так, в хирургических стационарах общего профиля доминирует кишечная палочка, в урологических — кишечная палочка, протеи, синегнойная палочка, клебсиеллы, в травматологических — золотистый стафилококк, синегнойная палочка, протеи и т. п. При этом иногда наблюдается более или менее четкая закономерность смены возбудителя в ране: стафилококк — затем синегнойная палочка.
[youtube.player]Выявление и характеристика ВБИ невозможна без выявления и характеристики микробных ассоциаций в больницах и контроля за ВБИ. Для этого необходимо получать информацию из самых различных источников.
Диагностика госпитальных инфекций проводится по обычным методикам, которые применяются в бактериологических лабораториях. Специальные методики для внутрибольничных инфекций не разработаны. Однако при микробиологических исследованиях для выделения возбудителей госпитальных инфекций есть некоторые особенности.
Необходимо установить этиологический фактор по многим признакам: род, тип, подтип. - биоценотический принцип.
Необходимо иметь данные по чувствительности выделенных микробов к антибиотикам, антисептикам, дезинфектантам, для организации правильного лечения и профилактики. - Химиотерапевтический принцип.
Всегда следует учитывать степень обсеменения обследуемого материала так как при массивном обсеменении вероятность заболевания увеличивается Количественный принцип.
Надо соблюдать, так называемый, популяционный принцип. Это значит что надо снимать с плотных питательных сред несколько колоний, ибо две колонии одного и того же вида могут отличаться друг от друга.
Больные должны обследоваться в течение пребывания в стационаре несколько раз, т.к. возможна смена возбудителя. - Динамический принцип.
Обязательно изучаются факторы патогенности: выработка токсина, факторов препятствующих фагоцитозу и лизису микроорганизмов, гемолиз выработка лецитиназы у стафилококков и т.д.
Необходимо типирование выделенных микробов (фаготипирование, серотипирование и т.д.) - эпидемиологический приниип.
При изучении специфичности и чувствительности набора тестов, характеризующих внутрибольничный эковар, установлены два высокоспецифичных признака: контаминация штаммом 30% и выше не¬обработанных предметов отделения, в значительной степени представленных медицинскими аппаратами и санитарно-техническим оборудованием, а также контаминация дезинфектанта (Ю.А.Захарова, И.В.Фельдблюм, 2008).
Эпидемиологический стандарт внутрибольничного штамма (эковара) может быть рекомендован к использованию в рамках микробиологического мониторинга в системе эпидемиологического надзора за ВБИ, что позволит улучшить предэпидемическую диагностику ГСИ в ЛПУ с целью принятия своевременных адекватных управленческих решений по снижению заболеваемости ГСИ.
Методы лабораторной диагностики:
1. Микробиологический:
A) Микроскопический:
- окраска по Граму: стафилококки, стрептококки, энтеробактерии, менинго-, гонококки и др.
- Циль-Нельсена: микобактерии туберкулеза;
- Нейсера, метиленовой синькой: дифтерия;
- Романовскому-Гимзе: малярия, лейшманиоз, трипоносомоз, возвратный тиф;
- По Бури: капсулы — пневмококк
- Темное поле: лептоспира;
- серебрение по Морозову: тельца Пашена (вирус натуральной оспы)
- иммунолюминисцентный: грипп (отпечатки со слизистой носа)
Б) Бактериологический - посев на жидкие (МПБ) и плотные (ЖСА, МПАкр., Эндо, Плоскирева, Левина, Сабуро и др.) питательные среды. Идентификация микроорганизмов, определение ферментативной и биохимической активности возбудителей, постановка пестрых рядов и тестов.
B) Биологический - опыты с лабораторными животными.
2. Серологический. РА, РСК, РГА, РИГА, РТГА, ИФА, РИА, ПЦР, Пауля- Буннеля и др.
В основе всех серологических реакций лежит взаимодействие антигена и антитела.
Взятие крови производят натощак (во избежании мутности (хилезности) сыворотки крови) из локтевой вены или уколом из пальца, у грудных детей - из небольшого разреза пятки. При взятии крови необходимо соблюдать правила асептики. Посуда должна быть чистой и сухой, стерилизация необязательна.
Кровь берут в количестве 5—6 мл, затем ставят в термостат на 0,5-1 ч. Затем отделяют сгусток от стенок пробирки и оставляют на 18-20 часов в прохладном месте. Отстоявшуюся сыворотку сливают в другую пробирку (при попадании в пробирку примеси эритроцитов ее центрифугируют). Сыворотка может оставаться на сгустке крови не более 48 часов. Чистую сыворотку можно хранить при температуре 4°С-10°С не более месяца. При необходимости более длительного хранения сыворотку следует заморозить при температуре —20°С - - 70°С, хранить, избегая оттаивания.
Если удалось взять минимальное количество крови (например, у маленьких детей) ее набирают в количестве 0,1 или 0,2 мл и вносят в пробирку с 0,9 мл или 1,8 мл стерильного физиологического раствора (содержащего 0,25% лимоннокислого натрия), что соответствует разведению сыворотки 1:10. Затем взвесь центрифугируют и оставляют в холодном месте до утра. Из отстоявшейся сыворотки делают последующие 2-х кратные разведения (1:20; 1: 40 и т.д.).
Вторым основным компонентом серологических реакций является антиген. Для обнаружения антител в крови ставят реакцию с заведомо известными антигенами. В качестве антигенов применяют взвеси живых или убитых микробов (РА), экстракты или изолированные химические фракции микробов (РГА, РСК преципитации и др.).
3. Вирусологический: материалом для вирусологических исследований служит: кал, смывы зева, носа, сыворотка крови и др. Хранить необходимо при низких температурах или в замороженном виде (исключение: цельная кровь - гемолиз эритроцитов). Вирус является облигатным паразитом, поэтому его культивирование представляет определенные сложности. Для культивирования вирусов необходимы культуры клеток. Исходя из этого, подтверждение диагноза при вирусных исследованиях чаще основывается на иммунолюминисцентном методе (свечение в люминисцентном микроскопе комплекса антиген-антитело), серологических методах (ПЦР, РФА, метод парных сывороток и др.), к сожалению, большинство этих методов имеют лишь ретроспективное значение.
4. В последнее время достаточно широко стали использоваться более информативные молекулярно-биологические методы — ПЦР (полимеразная цепная реакция).
Структура ответа: Основные принципы лабораторной диагностики ВБИ. Методы лабораторной диагностики.
[youtube.player]Внутрибольничная инфекция— это инфекция, заражение которой происходит в больничных учреждениях: наслаиваясь на основное заболевание, она утяжеляет клиническое течение болезни, затрудняет диагностику и лечение, ухудшает прогноз и исход заболевания, нередко приводя к смерти больного.
Классификация ВБИ
1. В зависимости от путей и факторов передачи ВБИ классифицируют:
- Воздушно-капельные (аэрозольные)
- Вводно-алиментарные
- Контактно-бытовые
- Контактно-инструментальные
- Постинъекционные
- Постоперационные
- Послеродовые
- Посттрансфузионные
- Постэндоскопические
- Посттрансплантационные
- Постдиализные
- Постгемосорбционные
- Посттравматические инфекции
- Другие формы.
2. От характера и длительности течения:
3. По степени тяжести:
- Тяжелые
- Среднетяжелые
- Легкие формы клинического течения.
В зависимости от степени распространения инфекции:
- Генерализованные инфекции: бактериемия (виремия, микемия), септицемия, септикопиемия, токсико-септическая инфекция (бактериальный шок и др.).
- Локализованные инфекции
- Инфекции кожи и подкожной клетчатки (ожоговых, операционных, травматический ран, Постинъекционные абсцессы, омфалит, рожа, пиодермия, абсцесс и флегмона подкожной клетчатки, парапроктит, мастит, дерматомикозы и др.);
- Респираторные инфекции (бронхит, пневмония, легочный абсцесс и гангрена, плеврит, эмпиема и др.);
- Инфекции глаза (конъюнктивит, кератит, блефарит и др.);
- ЛОР-инфекции (отиты, синуситы, ринит, мастоидит, ангина, ларингит, фарингит, эпиглоттит и др.);
- Стоматологические инфекции (стоматит, абсцесс, др.);
- Инфекции пищеварительной системы (гастроэнтероколит, энтерит, колит, холецистит, гепатиты, перитонит, абсцессы брюшины и др.);
- Урологические инфекции (бактериурия, пиелонефрит, цистит, уретрит, др.);
- Инфекции половой системы (сальпингоофорит, эндометрит, др.);
- Инфекции костей и суставов (остеомиелит, инфекция сустава или суставной сумки, инфекция межпозвоночных дисков);
- Инфекции ЦНС (менингит, абсцесс мозга, вентрикулит и др.);
- Инфекции сердечно-сосудистой системы (инфекции артерий и вен, эндокардит, миокардит, перикардит, постоперационный медиастинит).
Отличия госпитального штамма от обычного:
- Способность к длительному выживанию
- Повышенная агрессивность
- Повышенная устойчивость
- Повышенная патогенность
- Постоянная циркуляция среди больных и персонала
Выявление и характеристика ВБИ невозможна без выявления и характеристики микробных ассоциаций в больницах и контроля за ВБИ. Для этого необходимо получать информацию из самых различных источников.
Диагностика госпитальных инфекций проводится по обычным методикам, которые применяются в бактериологических лабораториях. Специальные методики для внутрибольничных инфекций не разработаны. Однако при микробиологических исследованиях для выделения возбудителей госпитальных инфекций есть некоторые особенности.
Необходимо установить этиологический фактор по многим признакам: род, тип, подтип. - биоценотический принцип.
Необходимо иметь данные по чувствительности выделенных микробов к антибиотикам, антисептикам, дезинфектантам, для организации правильного лечения и профилактики. - Химиотерапевтический принцип.
Всегда следует учитывать степень обсеменения обследуемого материала так как при массивном обсеменении вероятность заболевания увеличивается Количественный принцип.
Надо соблюдать, так называемый, популяционный принцип. Это значит что надо снимать с плотных питательных сред несколько колоний, ибо две колонии одного и того же вида могут отличаться друг от друга.
Больные должны обследоваться в течение пребывания в стационаре несколько раз, т.к. возможна смена возбудителя. - Динамический принцип.
Обязательно изучаются факторы патогенности: выработка токсина, факторов препятствующих фагоцитозу и лизису микроорганизмов, гемолиз выработка лецитиназы у стафилококков и т.д.
Необходимо типирование выделенных микробов (фаготипирование, серотипирование и т.д.) - эпидемиологический приниип.
При изучении специфичности и чувствительности набора тестов, характеризующих внутрибольничный эковар, установлены два высокоспецифичных признака: контаминация штаммом 30% и выше необработанных предметов отделения, в значительной степени представленных медицинскими аппаратами и санитарно-техническим оборудованием, а также контаминация дезинфектанта (Ю.А.Захарова, И.В.Фельдблюм, 2008).
Эпидемиологический стандарт внутрибольничного штамма (эковара) может быть рекомендован к использованию в рамках микробиологического мониторинга в системе эпидемиологического надзора за ВБИ, что позволит улучшить предэпидемическую диагностику ГСИ в ЛПУ с целью принятия своевременных адекватных управленческих решений по снижению заболеваемости ГСИ.
Современные вакцинные препараты:
1. Корпускулярные (живые и инактивированные) – из целых м/о, это вакцины первого поколения
2. Растворимые (химические и анатоксины) - из отдельных фракций возбудителей или продуктов их жизнедеятельности – второе поколение вакцин
3. Генно-инженерные - рекомбинантные вакцины, третье поколение
Требования к вакцинам:
- высокая иммуногенность и создание достаточно стойкого иммунитета
- остаточная вирулентность аттенуированных штаммов и стабильность их свойств
- безвредность
- отсутствие выраженных побочных действий (ареактивность)
- гипоаллергенность (минимально сенсибилизирующее действие)
- отсутствие в препарат контаминирующих м/о
- доступность производства
Вакцины могут вводиться: перорально, парэнтерально (внутримышечно, подкожно, внутрикожно, в поврежденную кожу (скарифицированную)), интраназально, в свечах и клизмах.
Для выработки прочного и длительного иммунитета необходим достаточный контакт макроорганизма и Аг => применяют ревакцинации черз определенное количество времени, зависящее от свойств биопрепарата.
Не у всех вакцинированных возникает прочный иммунитет (может быть недостаточная иммунореактиность/иммунодефицитные состояния).
Эффективность вакцинации зависит от типа и качества биопрепарата и способности возбудителя вызывать стойкий постинфекционный иммунитет.
Вакцины требуют строгого соблюдения правил хранения и транспортировки.
Преимущества живых вакцин:
высокая иммуногенность (формируют длительный напряженный иммунитет), простота способа введения; при естественных путях введения – местный иммунитет (секреторный IgA)
Недостатки: длительный и трудоемкий процесс получения; особый режим хранения (2-8*С) и чувствительность к его нарушению; есть опасность реверсии вакцинного штамма в вирулентный (при производстве или в организме вакцинированного); возможны осложнения после вакцинации; людям с иммунодефицитами противопоказаны живые вакцины, только инактивированные. После введения живой вакцины противопоказаны антибиотики в течение 2-2,5 мес.
Сейчас применяют вакцины для профилактики:
- бактериальных инфекций (туберкулезная- БЦЖ, сибиреязвенная, чумная, туляремийная, бруцеллезная)
- вирусных инфекций (корь, грипп, краснуха, паротит, желтая лихорадка)
- риккетсиозов (лихорадку-Ку и сыпной тиф)
Вакцины живые выпускают в сухом виде, лиофильно высушенные с добавлением стабилизаторов (желатиново-сахарозная среда). Исключение – живая полиомиелитная вакцина – жидкая.
Билет 49
Генная инженерия.
Генная инженерия - раздел молекулярной генетики, связанный с конструированием несуществующих в природе сочетаний генов при помощи генетических и биохимических методов.
Метод генетической инженерии относится к числу перспективнейших при получении многих белковых биологических веществ, представляющих ценность для медицины.
Генно-инженерные вакцины – это препараты, полученные с помощью биотехнологии, которая по сути сводиться к генетической рекомбинации .
Для начала получают ген, который должен быть встроен в геном реципиента. Небольшие гены могут быть получены методом химического синтеза. Для этого расшифровывается число и последовательность аминокислот в белковой молекуле вещества, затем по этим данным узнают очерёдность нуклеотидов в гене, далее следует синтез гена химическим путем.
Крупные структуры, которые довольно сложно синтезировать получаются путем выделения(клонирования), прицельного выщепления этих генетических образований с помощью рестриктаз.
Полученный одним из способов целевой ген с помощью ферментов сшивается с другим геном, который используется в качестве вектора для встраивания гибридного гена в клетку. Вектором могут служить плазмиды, бактериофаги, вирусы человека и животных. Экспрессируемый ген встраивается в бактериальную или животную клетку, которая начинает синтезировать несвойственное ей ранее вещество, кодируемое эксперссируемым геном.
В качестве реципиентов экспрессируемого гена чаще всего используется E. coli, B. subtilis, псевдомонады, дрожжи, вирусы. некоторые штаммы способны переключаться на синтез чужеродного вещества до 50% своих синтетических возможностей – эти штамм называются суперпродуцентами.
Иногда к генно-инженерным вакцинам добавляется адъювант.
Примерами таких вакцин служат вакцина против гепатита В (энджерикс), сифилиса, холеры, бруцеллёза, гриппа, бешенства.
Есть определённые сложности в разработке и применении:
- длительное время к генно-инженерным препаратам относились настороженно.
- на разработку технологии для получения вакцины затрачиваются значительные средства
- при получении препаратов данным способом возникает вопрос об идентичности полученного материала природному веществу.
Дисбактериоз.
Билет 50
Последнее изменение этой страницы: 2017-01-19; Нарушение авторского права страницы
[youtube.player]Понятие и этиология, главные причины возникновения и распространения внутрибольничных инфекций, провоцирующие факторы. Классификация данной группы заболеваний, патогенез, характеристика возбудителей и механизмы передачи. Меры профилактики и диагностика.
| Рубрика | Медицина |
| Вид | реферат |
| Язык | русский |
| Дата добавления | 30.08.2017 |
| Размер файла | 22,9 K |
Студенты, аспиранты, молодые ученые, использующие базу знаний в своей учебе и работе, будут вам очень благодарны.
Внутрибольничная инфекция. Этиопатогенез, характеристика возбудителей, особенности лабораторной диагностики
внутрибольничный заболевание инфекция
ВБИ во всём мире, включая нашу страну, являются актуальнейшей проблемой современной медицины. Не менее 7% больных, поступающих в лечебные учреждения, приобретают ту или иную внутрибольничную инфекцию. Внутрибольничные инфекции служат основной причиной смертности новорожденных и пациентов реанимационных отделений. В стационарах различного профиля периодически возникают эпидемические вспышки внутрибольничных инфекций.
ВБИ остаются одной из актуальных проблем современной медицины.
Что такое внутрибольничные инфекции?
Внутрибольничные инфекции (ВБИ) (др. термин - нозокомиальные) - это любое клинически выраженное инфекционное заболевание микробного происхождения, которое поражает пациента в результате его поступления в больницу или обращения в неё за лечебной и профилактической помощью, а также сотрудника больницы вследствие его работы в данном учреждении. При этом неважно, когда проявились симптомы заболевания - во время или после пребывания в больнице.
Как правило, внутрибольничные инфекции возникают на фоне основного заболевания либо, реже, первично развиваются у новорожденных.
Факторы, способствующие возникновению внутрибольничной инфекции:
- недооценка эпидемической опасности внутрибольниных источников инфекции и риска заражения при контакте с пациентом;
- наличие не выявленных носителей внутрибольничных штаммов среди медперсонала и пациентов;
- нарушение медперсоналом правил асептики и антисептики, личной гигиены;
- несвоевременное проведение текущей и заключительной дезинфекции, нарушение режима уборки;
- недостаточное оснащение ЛПУ дезинфекционными средствами;
- нарушение режима дезинфекции и стерилизации медицинских инструментов, аппаратов, приборов и т.д.;
- неудовлетворительное состояние пищеблоков, водоснабжения;
- отсутствие фильтрационной вентиляции.
Для развития внутрибольничного очага должны быть:
- источник (хозяин, пациент, медработник);
- окружающая среда (больничная среда, лечебно-диагностические процедуры и т.д.)
Источники ВБИ (внутрибольничной инфекции):
- носители скрытыми формами инфекции;
- больные с острой, стёртой или хронической формой инф. заболеваний, включая раневую инфекцию;
- пыль, вода, продукты;
Группы риска ВБИ (внутрибольничной инфекции):
- без определенного места жительства, мигрирующее население,
- с длительными не долеченными хроническими соматическими и инфекционными заболеваниями,
- не имеющие возможность получать специальную медицинскую помощь;
- назначена терапия подавляющая иммунную систему (облучение, иммунодеприсанты)
- проводятся сложные диагностические, операционные вмешательства;
3) родильницы и новорождённые, особенно недоношенные и переношенные;
4) дети с врождёнными аномалиями развития, родовой травмой;
5) медперсонал ЛПУ (лечебно-профилактического учреждения).
- патогенными микроорганизмами - кишечные, вирусные кишечные, вирусные гепатиты, воздушно-капельные инфекции. Основные причины возникновения: нарушение противоэпидемического режима.
- условно-патогенными микроорганизмами - инфекции в области хирургического вмешательства, инфекции нижних дыхательных путей, инфекция мочевыводящих путей, инфекции кровотока и другие (слизистых и кожи, ЦНС и др.).
Механизмы передачи ВБИ (внутрибольничной инфекции):
- прямой (от источника к хозяину)
- косвенный (через промежуточные объекты: руки, предметы)
- трансплацентарно (при прохождении плода по родовым путям, половым)
- вдыхая капельки и пылинки
- через живого переносчика
Места локализации условно патогенных микроорганизмов в организме человека:
Стафилококк (золотистый стафилококк):
- мочевыводящие пути и т.д.
Ведущими формами ВБИ являются инфекции мочевыводящих путей, в области хирургического вмешательства, нижних дыхательных путей, кровотока.
ВБИ утяжеляют общее состояние больных и увеличивают продолжительность пребывания пациента в стационаре в среднем на 6-8 дней. По данным ВОЗ, летальность в группе лиц с ВБИ значительно (в 10 раз и более) превышает летальность среди аналогичных групп больных без ВБИ.
Интенсивность эпидпроцесса при ВБИ зависит от многих факторов, в частности от:
* фоновые заболевания (исходное состояние пациента);
* состоянием окружающей среды стационара.
Профилактика инфекционных заболеваний
Для борьбы с внутрибольничными инфекциями разрабатываются различные мероприятия, носящие в основном медикаментозный характер (прививки, коррекция иммунологического статуса и прочие дорогостоящие меры).
Основными профилактическими мерами остается соблюдение асептики (использование химических средств для создания чистой, гигиенической среды, в первую очередь исключающей распространение микробов) и антисептики (использование химических средств для уничтожения микробов или контроля их роста на живых тканях, если они уже там присутствуют).
- Раннее и максимально полное выявление больных и носителей среди пациентов и медицинских работников;
- выявление больных с гнойно-воспалительными и другими инфекционными заболеваниями;
- своевременная изоляция и перевод больных с ВБИ в соответствующие отделения и палаты;
- сокращение числа инвазивных вмешательств.
Характеристика основных возбудителей внутрибольничных инфекций
Стафилококки. Род насчитывает 20 видов.
Золотистый стафилококк является одним из ведущих возбудителей внутрибольничных инфекций. Занимает первое место среди возбудителей хирургических раневых инфекций - 17%, на втором месте по частоте выделения из крови и дыхательных путей - 16,5%. Может вызвать синдром токсического шока. Резервуарами и источниками стафилококка в стационаре являются передние отделы носа персонала, инфицированные больные, предметы и поверхности. Профилактика: санация носителей, деколонизация пациентов с высоким риском внутрибольничных инфекций, предоперационная антибиотикопрофилактика.
Эпидермольный стафилококк: постоянно присутствует на кожных покровах человека. В стационарах циркулируют его полирезистентные штаммы. Обладает способностью удерживаться и размножаться в сосудистых катетерах и других устройствах благодаря своей внеклеточной слизи и ограниченным питательным потребностям. Может являться резервуаром генов антимикробной устойчивости в стационаре. Представляет большую опасность для новорожденных. Находится на втором месте после золотистого стафилококка по частоте выделения при хирургической раневой инфекции. Применяются общие меры профилактики.
Все большее значение приобретает метициллин-резистентный стафилококк.
Стрептококки. Играли большую роль в доантибиотиковую эру. Вызывают 2% внутрибольничных инфекций. Наиболее частые источники вспышек инфекции - влагалищные, кожные и ректальные носители. Глоточные носители имеют меньшее значение. Стрептококки особенно опасны в инфекциях родильниц и новорожденных.
Пневмококки. Часто выделяются из дыхательных путей, особенно у дошкольников. Являются главной причиной пневмонии.
Энтерококки. Относительно невирулентная флора кишечника. Являются изначально устойчивыми к антибиотикам, хорошо выживают в окружающей среде и на коже рук. Высевают их из хирургических ран, пролежней.
Семейство кишечных бактерий. Все они являются необязательными анаэробами и могут вызывать анаэробную инфекцию, разлагают нитриты до нитратов, вызывая пищевые отравления. Занимают первое место в инфекциях мочевыводящего тракта (50%). Вызывают 33% всех случаев пневмоний и 25% случаев хирургической раневой инфекции. Для бактериемии не является частым возбудителем. Места носительства - ротоглотка и кишечник. Пути передачи - контактный и водный. Многие из них хорошо сохраняются во влажной среде. Цефалоспорины первого и третьего поколений увеличивают частоту ректальной колонизации некоторыми из них. Антибиотикопрофилактика неэффективна.
Синегнойная палочка. Она устойчива к цефалоспоринам первого и второго поколения. Иногда она чувствительна только к самым современным антибиотикам. Частично она устойчива к хлор-гексидину и фенолам. Часто вызывает бактериемию, протекающую особо тяжело. Является одним из самых частых возбудителей внутрибольничных пневмоний, инфекции ожоговых ран. Источники: прямокишечные, глоточные носители, вода, влажные предметы, свежие овощи, цветы. Часто высевается на эндоскопах, аппаратах для гемодиализа и дыхания.
Грибы. В последнее время грибы рода кандида имеют все большее значение как возбудители внутрибольничных инфекций. К ним необходимо особое внимание, что объясняется следующими причинами: неяркая клиника, трудности микробиологического подтверждения, небольшой выбор средств лечения, высокая устойчивость к дезинфектантам, широкое распространение носительства.
Факторы риска: антибиотико-, гормоно-, химиотерапия, парентеральное питание, катетеризация мочевого пузыря, центральных вен. В последнее время доказана роль рук персонала как резервуара инфекции. Роль предметов окружающей среды окончательно не выяснена.
Виды носительства: поверхностное (временное и постоянное), глубокое (временное и постоянное).
ВБИ, вызванные облигатно-патогенными микроорганизмами, диагностируются на основании клинической картины, эпид. анамнеза, контакта с больными группового характера заболевания и результатов соответствующих методов исследования. Сбор сведений о больном проводится в соответствии с вопросами карты эпидемиологического обследования. Наиболее полную информацию о заболевшем можно получить из истории болезни. Ряд сведений уточняется из журналов операционного, процедурного, перевязочного кабинетов. Важно собрать сведения о всех манипуляциях, инвазивных обследованиях, проведенных больному (катетеризация вен, мочевого пузыря и т.п.).
Для выявления источника инфекции необходимо определить круг лиц (персонал, длительно лежащие в отделении больные), имевшие непосредственный контакт с заболевшим с учетом предрасполагаемого места заражения ВБИ - эти лица подлежат бактериологическому обследованию на носительство микроорганизмов, послуживших этиологическим факторам.
Свободноживущие микроорганизмы определяют в смывах с объектов окружающей среды.
Основной метод диагностики при ВБИ - бактериологический.
Об эпидемическом неблагополучии ЛПУ с внутрибольничными инфекциями свидетельствуют:
- появление одномоментно двух или более случаев инфекции, идентичных по этиологии, а иногда и по клиническим формам;
- увеличение удельного веса штаммов, идентичных по результатам внутривидовой идентификации;
- статистически значимое возрастание гентамицино независимых изолятов (предвестника роста инфекций, вызванных грамотрицательными микроорганизмами);
- статистически значимое возрастание метициллинорезистентных стафилококков (предвестник роста кокковых инфекций);
- рост потребления нитрофурановых препаратов (предвестник роста псевдомонадной инфекции);
- рост числа пирогенных реакций после инфузий более чем в два раза, по сравнению с обычным уровнем (свидетельство загрязнения растворов живыми бактериями).
Индикация госпитальных штаммов является актуальной задачей. В качестве основных критериев (маркеров) госпитальности выделенных штаммов используют исследования из чувствительности к антибиотикам, дезинфектантам и УФ-облучению. Эти признаки кодируются на плазмидном уровне. Молекулярная масса плазмид резистентности (R-плазмид) от 50 до 120 Мд (мегадальтон). Госпитальные штаммы при благоприятных условиях легко обмениваются R-плазмидами между собой и внебольничными штаммами. Наличие у штамма R-плазмид тоже рассматривается как маркер госпитальности.
При выявлении ВБИ, вызванных условно-патогенной флорой следует учитывать длительность пребывания в стационаре и все другие отягощающие факторы (возраст, тяжесть основного заболевания, длительное неэффективное лечение, клиническое ухудшение общего состояния).
Методические подходы к диагностике заболеваний, обусловленных УП микроорганизмами, должны основываться на ряде требований: забор материала для исследования должен производиться до приема а/б препаратов или же необходимо прекращение а/б-терапии за 12-24 часа до обследования; если проводится исследование заведомо нестерильного материала (фекалии, вагинальный секрет, моча, мокрота, слюна и т.д.), то целесообразно использовать количественные методы оценки из пересчета на 1 г или 1 мл исходного материала. Было предложено считать количество выделенных УПМ менее 104 инвазией, а количество УПМ более 104,5 (грибы 103) - диагностически значимым; кроме количественного определения УПМ в исследуемом материале после выделения чистой культуры необходимо максимально изучить их свойства. В перечень исследований должно входить:
1) Определение сероваров (определение серовара E. coli позволит отнести серовары к определенной группе патогенности).
2) Определение фаговаров (позволяет провести эпидемиологический анализ и определить тактику лечения).
3) Определение факторов патогенности (выявление двух факторов патогенности одновременно у одного представителя УПМ свидетельствует о его этиологическом значении).
4) Определение антибиотикограммы выделенной культуры тоже может быть критерием оценки потенциальной патогенности микроорганизма. Считается, что симбионтные микроорганизмы более чувствительны к антибиотикам, чем приобретенные УПМ.
Важным моментом, подтверждающим этиологическую роль УПМ, является повторное выделение этого же возбудителя. Количественные показатели могут варьировать. Поэтому при выделении УПМ желательно проводить 2-3-кратное исследование.
Диагностика заболеваний, обусловленных УПМ, осложняется еще и тем, что как правило данные микроорганизмы взаимодействуют ассоциациями (вирус-бактерия; вирус-микроскопические грибки; вирус-бактерия - микроскопические грибки и т.д.).
Список использованной литературы
внутрибольничный заболевание инфекция
1. Эпидемиология внутрибольничной инфекции. / Яфаев Р. X., Зуева Л.П. - Л.: Медицина, 1989. - 436 с.
2. Профилактика внутрибольничных инфекций: Руководство для врачей. / Под ред. Е.П. Ковалевой, Н.А. Семиной. - М.: Медицина, 1993. - 238 с.
3. Медицинская микробиология / Под ред. акад. РАМН В.И. Покровского. - М.: ГЭОТАР-МЕД, 2001. - 692 с.
4. Внутрибольничные инфекции в условиях современного стационара. - Прямухина Н.С., Коршунова Г.С., Семина Н.А. и др. // Здоровье населения и среда обитания. - 1994. - №12/21. - С. 1-5.
5. Внутрибольничная инфекция. / Н. Шерертц, У. Хэмптон, А. Ристуцина. - Под ред. Р.П. Венцела. - М.: Медицина, 1990. - 503 с.
Размещено на Allbest.ru
Основные факторы, способствующие возникновению внутрибольничных инфекций, их классификация и разновидности, пути борьбы. Источники и группы риска: пожилой возраст, нарушение гигиены ротовой полости, длительное использование лекарственных средств.
презентация [1,4 M], добавлен 17.10.2015
Проблема внутрибольничных инфекций (ВБИ). Причины роста заболеваемости ВБИ. Особенности циркуляции условно-патогенных микроорганизмов как возбудителей оппортунистических инфекций. Методы микробиологической диагностики выявления и схемы профилактики ВБИ.
курсовая работа [96,1 K], добавлен 24.06.2011
Анализ проблемы внутрибольничных инфекций (ВБИ) как заболеваний пациентов, связанных с оказанием медицинской помощи в больницах и лечебно-профилактических учреждениях. Основные виды ВБИ. Факторы, влияющие на рост ВБИ. Механизм передачи возбудителей.
презентация [162,7 K], добавлен 31.03.2015
Понятие и главные причины возникновения внутрибольничных инфекций, клиническая картина их течения, факторы риска и методы профилактики. Требования к санитарно-гигиеническим мероприятиям внутри лечебного учреждения. Задачи госпитального эпидемиолога.
презентация [144,3 K], добавлен 21.04.2014
Понятие и основные причины возникновения внутрибольничной инфекции, ее клинические проявления и факторы быстрого распространения в стенах медицинского учреждения. Механизмы, пути и принципы передачи возбудителя заболевания. Меры профилактики и лечение.
презентация [1014,2 K], добавлен 13.05.2014
Условия, влияющие на возникновение внутрибольничных инфекций - инфекционных заболеваний, полученных больными в лечебных учреждениях. Факторы влияющие на восприимчивость к инфекциям. Механизмы передачи внутрибольничных инфекций, методы профилактики.
презентация [590,7 K], добавлен 25.06.2015
Классификация внутрибольничных инфекций: кишечные, гнойно-септические и вирусные гепатиты В, С, Д. Причины возникновения внутрибольничных инфекций в лечебно-профилактических учреждениях. Правила безопасности сотрудников больницы на рабочем месте.
презентация [96,3 K], добавлен 10.02.2014
Анализ факторов, способствующих росту внутрибольничных инфекций в современных условиях. Артифициальный механизм передачи возбудителей инфекции. Меры по снижению распространенности внутрибольничных инфекций в акушерских стационарах. Методы стерилизации.
презентация [531,0 K], добавлен 04.11.2013
Механизмы передачи возбудителей инфекций, связанных с оказанием медицинской помощи. Система мероприятий по профилактике ИСМП. Основные направления дезинфекции в лечебных учреждениях. Проблема резистентности возбудителей внутрибольничных инфекций.
презентация [1,1 M], добавлен 23.09.2015
Понятие и природа современной ВБИ (внутрибольничная инфекция). Источники ВБИ, механизмы и пути передачи, факторы передачи. Причины способствующие сохранению высокого уровня заболеваемости ВБИ. Контингенты риска. Классификация опасных процедур.
автореферат [19,8 K], добавлен 02.02.2008

Работы в архивах красиво оформлены согласно требованиям ВУЗов и содержат рисунки, диаграммы, формулы и т.д.
PPT, PPTX и PDF-файлы представлены только в архивах.
Рекомендуем скачать работу.
Читайте также:


