Вильпрафен при микоплазменной инфекции
Вопросы антибиотикотерапии урогенитальной микоплазменной инфекции активно дискутируются. Многочисленные исследования посвящены разработке рекомендаций по терапии микоплазменной инфекции. Но по-прежнему наиболее сложным и актуальным на сегодняшний день ост
В последние десятилетия наряду с ростом заболеваемости урогенитальной патологией отмечаются значительные изменения в ее структуре. По данным эпидемиологических исследований, более чем у 40% больных с воспалительными заболеваниями урогенитального тракта выявляется микоплазменная инфекция [1].
Урогенитальная микоплазменная инфекция довольно широко распространена в популяции. Человек является естественным хозяином, по крайней мере, одиннадцати видов микоплазм, из них три вида (Mycoplasma genitalium, Mycoplasma hominis, Ureaplasma urealyticum) способны вызывать воспалительные заболевания урогенитального тракта. Носительство М. hominis и U. urealyticum среди населения варьирует от 10% до 50% [1].
В настоящее время все большее внимание в отечественной и зарубежной литературе уделяется виду U. urealyticum. Данный вид включает в себя два биовара: PARVO (серотипы 1, 3, 6 и 14) и T-960 (серотипы 2, 4, 5, 7, 8, 9, 10, 11, 12, 13). Оба биовара способны инициировать патологические проявления. Так, с биоваром PARVO связывают выраженную лейкоцитарную реакцию при микроскопии мазка, кольпит, пиелонефрит, дистрофические изменения плаценты, а также рождение детей с массой тела менее 3 кг.
Биовар Т-960 считается ответственным за проявления негонококкового уретрита у мужчин, патологические выделения из влагалища у женщин и, в редких случаях, внутриутробную гибель плода [3].
Отличительными особенностями микоплазм и уреаплазм являются отсутствие клеточной стенки и способность паразитировать на мембране клеток хозяина.
Учитывая высокую распространенность микоплазм, в особенности у беременных женщин, их клиническая роль зависит от степени колонизации ими урогенитального тракта [4]. Так, статистически выявлена значительная связь между уровнем колонизации U. urealyticum и M. hominis мочеполовых путей женщин и преждевременными родами, а также дородовым излитием околоплодных вод [4]. В литературе появляется все больше сообщений о внутриутробной микоплазменной инфекции, которая реализуется у новорожденных чаще всего в виде пневмоний, но может носить и генерализованный характер [4].
Основной путь передачи микоплазменной инфекции — половой. Чаще всего микоплазмы обнаруживаются у лиц с повышенной половой активностью. Для развития инфекционного процесса важное значение имеет не столько сам факт наличия или отсутствия микоплазм, сколько широта и массивность их диссеминации. К факторам, провоцирующим развитие инфекционного процесса, относятся: присоединившаяся инфекция другой природы, изменение гормонального фона, беременность и роды; нарушения иммунного и интерферонового статусов организма. Немаловажную роль в развитии инфекции играет и вирулентность конкретного штамма.
Кроме того, широко распространено бессимптомное носительство микоплазм. Во многих случаях они вызывают латентную инфекцию, которая под влиянием различных стрессовых факторов может перейти в хроническую рецидивирующую или острую форму.
Клиническая картина мико- и уреаплазменной инфекции неспецифична и, как правило, не отличается от клинических проявлений инфекций, вызванных другими возбудителями урогенитальных инфекций.
Таким образом, воспалительные заболевания мочеполовых органов, обусловленные патогенными и условно-патогенными микоплазмами, продолжают оставаться серьезной проблемой в связи с возможностью развития тяжелых осложнений, связанных с репродуктивной функцией. Несмотря на неоднозначность мнений исследователей в отношении патогенной роли мико- и уреаплазменной инфекции, в этиологической классификации Всемирной организации здравоохранения (ВОЗ) 2006 г. и синдромальной классификации CDC (Centers for Disease Control and Prevention, центры по контролю и профилактике заболеваний США) эти микроорганизмы выделены как возможные этиологические агенты неспецифических негоноккоковых уретритов, воспалительных заболеваний органов малого таза и бактериального вагиноза [2].
Одним из наиболее сложных на сегодняшний день остается вопрос эффективности терапии урогенитальных инфекций.
Многочисленные исследования посвящены разработке схем и методик применения тех или иных антимикробных препаратов. Оптимизируют антибактериальную терапию с помощью иммуномодуляторов, ферментных и других лекарственных средств. В целом, терапия инфекций, передаваемых половым путем, должна быть комплексной, а применяемые препараты — обладать широким спектром действия. К препаратам, используемым для лечения инфекций, передаваемых половым путем, ВОЗ выдвинуты следующие требования:
- эффективность не менее 95%;
- хорошая переносимость и малая токсичность;
- безопасность использования во время беременности;
- медленное развитие резистентности микроорганизмов к средствам терапии;
- доступная цена.
Основные принципы медикаментозной терапии:
- основные препараты (препараты выбора) — обеспечивают наилучшее соотношение между эффективностью лечения и доказанной безопасностью лечебного средства;
- альтернативные препараты — обеспечивают приемлемые результаты лечения при отсутствии возможности использования основных схем лечения (беременность, кормление грудью, индивидуальная непереносимость лекарственного средства, сопутствующие заболевания и т. д.).
Рациональный выбор антибиотиков для эмпирической терапии следует осуществлять с учетом следующих критериев:
- спектр активности, соответствующий предполагаемому возбудителю;
- фармакокинетика, определяющая проникновение антибиотика в очаг воспаления, кратность введения и длительность курса лечения;
- эффективность при урогенитальных инфекциях, доказанная в рандомизированных клинических исследованиях;
- противопоказания и частота побочных эффектов;
- удобство применения для пациента (повышает аккуратность соблюдения режима лечения);
- фармакоэкономические аспекты лечения.
Вопросы антибиотикотерапии урогенитальной микоплазменной и уреаплазменной инфекции также активно дискутируются. В то же время адекватная антибиотикотерапия должна проводиться лишь с учетом чувствительности конкретного штамма возбудителя [5–6].
С учетом вышеуказанных пунктов можно выделить следующие перспективные группы антибиотиков для лечения мико- и уреаплазменной инфекции: тетрациклины, макролиды, фторхинолоны, азалиды.
Критериями назначения этиотропной терапии при выявлении генитальных микоплазм, по мнению большинства исследователей, являются:
1) клинические и лабораторные признаки воспалительного процесса в органах мочеполовой системы;
2) результаты комплексного микробиологического обследования на наличие патогенных и условно-патогенных микроорганизмов с количественным обнаружением генитальных микоплазм более 104 КОЕ/мл;
3) предстоящие оперативные или другие инвазивные мероприятия на органах мочеполовой системы;
4) бесплодие;
5) беременность (оценка акушерско-гинекологического анамнеза).
Среди наиболее часто применяемых антибиотиков сохраняется стабильно высокая чувствительность мико- и уреплазменной инфекции к джозамицину (94,8% 5 лет назад и 94,4% в настоящее время) и отмечается увеличение числа штаммов, чувствительных к доксициклину, с 93,2% до 97,2%. Вместе с тем чувствительность к другому антибиотику этой же группы, тетрациклину, снизилась с 92,5% до 83,3%.
Препараты, указанные в альтернативных схемах, не имеют каких-либо преимуществ между собой и рассматриваются как равнозначные.
Рекомендованными препаратами в соответствии с Европейским руководством по ведению беременных женщин, инфицированных микоплазмами [7], являются: эритромицин по 500 мг 4 раза в день в течение 7 дней; или амоксициллин 500 мг внутрь 3 раза в день 7 дней; или джозамицин 500 мг 2 раза в день 7 дней.
Для лечения беременных [2] применяется следующая схема: джозамицин по 500 мг внутрь 3 раза в сутки в течение 10 дней (табл. 1 и 2).
Тетрациклины
Одним из основных препаратов для лечения инфекций, передаваемых половым путем, остается представитель группы тетрациклинов — доксициклин. При этом эталоном эффективности различных режимов терапии является пероральный прием доксициклина (100 мг 2 раза в день в течение 10 дней). Доксициклин отличается от тетрациклина лучшими фармакокинетическими свойствами и большей безопасностью. В основе механизма антибактериального действия доксициклина, как и других тетрациклинов, лежит подавление им биосинтеза белка микробной клетки на уровне рибосом [8]. Среди солей доксициклина предпочтение следует отдавать моногидрату, который, в отличие от гидрохлорида, не вызывает развития эзофагита и оказывает минимальное воздействие на микрофлору кишечника [4]. Наиболее удобной в применении является форма доксициклина моногидрата в виде таблеток диспергируемых, которая позволяет применять препарат как в форме таблеток, так и суспензии или раствора. Кроме того, лекарственная форма диспергируемой таблетки обеспечивает стабильное всасывание доксициклина и равномерное нарастание его концентрации в крови. При негонококковом уретрите, вызванном U. urealyticum, M. hominis или M. genitalium, доксициклин применяют в дозе 100 мг 2 раза в день в течение 7–14 дней [4]. Хорошие результаты были получены при применении доксициклина у женщин, инфицированных различными видами микоплазм и страдающих бесплодием или привычным невынашиванием беременности. В ряде случаев после применения доксициклина наступала беременность, которая заканчивалась нормальными родами в срок и без осложнений [4].
С клинической точки зрения наиболее актуальным представляется выбор тех препаратов, к которым U. urealyticum демонстрирует наивысшую чувствительность. Выделение устойчивых к действию доксициклина инфектов отмечается крайне редко. Рост числа штаммов, чувствительных к доксициклину, можно объяснить тем, что в последние годы этот препарат несколько потеснили макролиды (кларитромицин, рокситромицин, азитромицин), активно применяемые в терапии урогенитальной инфекции.
Сохранение высокой чувствительности возбудителя к доксициклину доказывает обоснованность его применения в лечении микоплазмозов. При его применении могут наблюдаться отдельные побочные эффекты, чаще со стороны желудочно-кишечного тракта (ЖКТ). К недостаткам доксициклина относится невозможность его назначения детям до 8 лет и беременным женщинам, а также женщинам в период лактации.
Макролиды
Другие группы антибиотиков, применяемые для лечения микоплазмозов, представлены, в частности, макролидами. Для макролидов в целом характерны более низкие минимальные подавляющие концентрации (МПК), чем для фторхинолонов. По мнению ряда исследователей, при мико- и уреаплазменной инфекции макролиды должны использоваться в качестве препаратов первого ряда [9].
Препарат группы макролидов эритромицин в течение длительного времени применялся в качестве альтернативы тетрациклинам, однако этот препарат часто плохо переносится больными. Согласно опубликованным результатам терапия эритромицином остается достаточно эффективной — 83–95%. Тем не менее многие авторы отмечают, что выраженные побочные эффекты со стороны ЖКТ, а также высокая курсовая доза и необходимость многократного приема (4 раза в день по 500 мг) снижают целесообразность выбора этого антибиотика.
В группе макролидов самые низкие МПК для уреаплазм имеют кларитромицин и джозамицин. Прием 250 мг кларитромицина 2 раза в день в течение 7 дней, как правило, приводит к исчезновению M. hominis, U. urealyticum из половых путей мужчин и женщин. Применение рокситромицина (300 мг 1 раз в день) не уступает по эффективности стандартному режиму приема доксициклина.
Джозамицин обладает широким спектром антибактериального действия, включающим не только все клинически значимые возбудители микоплазмоза (M. hominis, M. genitalium, U. urealyticum), но и другие частые этиологические агенты при урогенитальных инфекциях — хламидии и Neisseria gonorrhoeae.
Преимуществом 16-членных макролидов, к которым относится джозамицин, перед эритромицином и другими препаратами этой группы является более редкое развитие к ним устойчивости у ряда микроорганизмов, например S. pneumoniae [10]. Аналогичная тенденция прослеживается и в отношении внутриклеточных возбудителей. Несмотря на широкое применение джозамицина, клинические штаммы микоплазм и уреаплазм сохраняют высокую чувствительность к нему как за рубежом [11], так и в России [3]. Например, в период с 2001 по 2003 г. был отмечен рост количества устойчивых штаммов к рокситромицину, кларитромицину, левофлоксацину и клиндамицину, в то время как уровень антибиотикорезистентности к джозамицину за это время не изменился [7]. Аналогичные данные были получены и в исследовании, проведенном в Красноярске, где было показано сохранение стабильно высокой чувствительности U. urealyticum к джозамицину на протяжении последних 5 лет [12]. Более высокая активность джозамицина в отношении уреаплазм по сравнению с другими макролидами продемонстрирована и в других отечественных исследованиях [4].
В зарубежном сравнительном исследовании чувствительности к семи антибактериальным препаратам (джозамицин, доксициклин, миноциклин, спарфлоксацин, рокситромицин, офлоксацин и азитромицин) возбудителей смешанной инфекции U. urealyticum и M. hominis, выделенных у больных негонококковым уретритом, также была показана их высокая чувствительность к джозамицину, превышающая таковую к препаратам сравнения [13]. При подобных инфекциях уровень резистентности возбудителей особенно высок, в связи с чем выбор препаратов для их лечения должен проводиться наиболее тщательно. Например, резистентность к азитромицину в данном исследовании составила 90,48%.
Джозамицин накапливается в лимфатических узлах и половых органах, причем его концентрации в этих органах при воспалительных процессах повышаются, т. к. он способен проникать внутрь фагоцитарных клеток (макрофагов, фибробластов, полиморфноядерных гранулоцитов) и переноситься ими в очаг воспаления [14]. Концентрация препарата в полиморфноядерных лейкоцитах человека, моноцитах и альвеолярных макрофагах приблизительно в 20 раз выше, чем во внеклеточном пространстве [15].
В отличие от большинства других макролидов, джозамицин наряду с хорошим проникновением внутрь клеток создает и высокие концентрации в сыворотке крови, что имеет важное значение при системном проявлении инфекции [16]. Препарат не связывается с изоферментами цитохрома Р-450 и не влияет на НАДФ-цитохром-С-редуктазу, поэтому обладает значительно более низким риском лекарственных взаимодействий, чем эритромицин и кларитромицин, и не оказывает отрицательного влияния на функцию печени. Для джозамицина характерны выраженные иммуномодулирующие свойства, которые могут способствовать усилению терапевтического эффекта у больных с воспалительными заболеваниями [17].
После приема внутрь джозамицин быстро абсорбируется из ЖКТ. Сmax достигается через 1–2 ч после приема. Через 45 мин после приема дозы 1 г средняя концентрация джозамицина в плазме составляет 2,41 мг/л. Связывание с белками плазмы не превышает 15%. Прием препарата с интервалом в 12 ч обеспечивает сохранение эффективной концентрации джозамицина в тканях в течение суток. Равновесное состояние достигается через 2–4 дня регулярного приема.
Одним из преимуществ джозамицина является быстрое создание высокой концентрации препарата в клетках и тканях за счет его высокой липофильности. При пероральном применении концентрация препарата в лейкоцитах, моноцитах, фагоцитах, макрофагах и клетках эпителия приблизительно в 20 раз выше, чем в межклеточном пространстве.
Поскольку микоплазмы и уреаплазмы являются внутриклеточными паразитами, вышеуказанные свойства джозамицина делают его идеальным препаратом для лечения инфекций, вызванных этими патогенами.
Доказана также высокая клиническая эффективность джозамицина. По данным Института исследования инфекционных кожно-венерических заболеваний (Австрия), степень излечения микоуреаплазмоза при применении джозамицина составляет 97% (для сравнения: эффективность применения доксициклина при данной патологии составляет 50%, азитромицина — 55,5%) [1].
Достаточно широкий спектр антимикробного действия антибиотика делает его эффективным при лечении смешанных инфекций, включающих анаэробные, к которым женщины особенно восприимчивы. Для лечения урогенитального микоуреаплазмоза рекомендуемая доза препарата — по 500 мг 2 раза в сутки в течение 7–10 дней.
Азитромицин является полусинтетическим антибиотиком широкого спектра действия, первым представителем подкласса азалидов. Подобно другим макролидам, обладает в основном бактериостатическим эффектом, но благодаря способности создавать очень большие внутриклеточные концентрации может действовать бактерицидно. К достоинствам азитромицина следует отнести его хорошую переносимость. Результаты клинических исследований показали, что азитромицин и доксициклин обладают практически одинаковой эффективностью при уреа- и микоплазменной инфекциях (94,9% и 95,9% соответственно).
Фторхинолоны
Фторхинолоны в лечении микоплазмозов относятся к альтернативным препаратам. Среди них предпочтение стоит отдавать офлоксацину и его левовращающему изомеру — левофлоксацину.
Амоксициллин
Согласно рекомендациям американского Центра по профилактике и контролю за заболеваниями, к альтернативным препаратам, применяемым при урогенитальных инфекциях (табл. 1), относится амоксициллин. Однако несмотря на приводимые относительно высокие показатели излечения амоксициллином — 82–94%, нельзя забывать, что in vitro пенициллины оказывают неполный ингибирующий эффект по отношению к внутриклеточным возбудителям, в частности, M. hominis, U. urealyticum.
Резюмируя вышесказанное, необходимо отметить, что на сегодняшний день существует множество рекомендаций и схем лечения микоплазменной инфекции. Эффект лечения зависит от многих причин, поэтому обязательным условием успеха лечения является комплексное обследование пациента до назначения лекарственного препарата с обязательным определением чувствительности выявленного патогена к антибактериальным препаратам. Установление клинико-микробиологических критериев излеченности урогенитальных инфекций, вызванных микоплазмами, проводится через 1 месяц после окончания лечения. При отсутствии клинических проявлений заболевания и выявлении возбудителя в количестве менее 104 КОЕ/мл осуществляется динамическое наблюдение за больными, в больших количествах — повторное лечение с заменой антибиотика [18].
С учетом общих принципов лечения инфекционных больных, терапия микоплазменной инфекции должна быть комплексной, этиологически, патогенетически и симптоматически обоснованной и дифференцированной в соответствии с видом возбудителя, клинической формой и характером болезни, наличием осложнений и остаточных явлений.
Литература
В. Н. Кузьмин 1 , доктор медицинских наук, профессор
М. И. Гусейнзаде
ГБОУ ВПО МГМСУ им. А. И. Евдокимова МЗ РФ, Москва
Abstract. The questions of antimicrobial therapy of urogenital mycoplasma infections are actively discussed. Numerous studies devoted to the development of recommendations for mycoplasma infections treatment. But one of the most difficult and up-to-date questions is the choice of effective therapy.
Сайт предоставляет справочную информацию исключительно для ознакомления. Диагностику и лечение заболеваний нужно проходить под наблюдением специалиста. У всех препаратов имеются противопоказания. Консультация специалиста обязательна!
Антибиотик Вильпрафен
Вильпрафен – антибиотик широкого спектра действия из группы макролидов. Его активно действующее вещество – джозамицин.
В терапевтических дозах препарат действует на болезнетворные микроорганизмы бактериостатически (угнетает их жизнедеятельность), а больших концентрациях действие его становится бактерицидным (губительным для бактерий).
Лекарственное средство эффективно в отношении многих микроорганизмов – грамотрицательных (менингококков, гонококков, гемофильной палочки, Хеликобактер пилори и др.) и грамположительных (стафилококков, стрептококков, пневмококков, коринебактерий дифтерии и др.). Его назначают также для борьбы с внутриклеточными микроорганизмами (хламидиями, микоплазмой, уреаплазмой и др.), а также с некоторыми анаэробными бактериями (пептококками, пептострептококками, бактероидами и клостридиями).
Вильпрафен быстро всасывается из пищеварительного тракта. Уже через час достигается его максимальная концентрация в крови. При этом Вильпрафен обладает длительным терапевтическим эффектом.
Препарат преодолевает плацентарный барьер и может выделяться с грудным молоком.
Лекарство неактивно в отношении энтеробактерий, поэтому практически не влияет на микрофлору кишечника.
80% Вильпрафена выводится с желчью, 20% - с мочой.
Формы выпуска
Препарат производится двумя фирмами: Yamanouchi Pharma S.p.A. (Italy) и Yamanouchi Pharma (Japan).
Вильпрафен выпускается в таблетках и в суспензии:
- Таблетки белого цвета, продолговатые, покрытые оболочкой, содержащие 500 мг активного вещества джозамицина. В картонной упаковке находится блистер из 10 таблеток.
- Диспергируемые (быстродействующие растворимые) таблетки Вильпрафен Солютаб имеют сладкий вкус и запах клубники. Они содержат 1000 мг действующего вещества джозамицина. В упаковке – два блистера с 5 или 6 таблетками.
- Суспензия Вильпрафена содержит 300 мг джозамицина в 10 мл. Расфасована в темные стеклянные флаконы по 100 мл.
Инструкция по применению Вильпрафена
- Повышенная чувствительность к активному веществу - джозамицину, или вспомогательным компонентам препарата;
- аллергия на прием других антибиотиков из группы макролидов;
- заболевания печени, приводящие к тяжелому нарушению ее функций или к нарушению работы желчевыводящих протоков;
- недоношенность детей.
Таблетки Вильпрафен Солютаб можно проглатывать целиком или развести таблетку в 20 мл воды, перемешать и выпить полученную суспензию.
Если пациент забыл принять очередную дозу, то нужно немедленно это сделать, но ни в коем случае не принимать двойную дозу (вместе с "забытой").
Не рекомендуется делать перерыв в лечении или преждевременно прекращать терапию. В этом случае достижение излечения маловероятно.
Дозировка Вильпрафена
Дозировка и курс лечения зависят от диагноза. Вильпрафен может назначить только врач.
Обычно терапевтическая суточная доза препарата для детей старше 14 лет и взрослых составляет 1-2 г и обязательно должна быть распределена на 2-3 приема (по 500 мг). В тяжелых случаях дозу Вильпрафена можно увеличить до 3 г в сутки.
Начальная доза препарата – 1 г.
Курс лечения может составлять 5 - 21 день; длительность его зависит от тяжести воспалительного процесса.
Микоплазмоз – по 500 мг (1 таблетка) 2-3 раза в сутки, курс лечения – 12-14 дней.
Обыкновенные и шаровидные угри – 500 мг (1 таблетка) 2 раза в день в течение первых 2-4 недель лечения, а потом по 500 мг 1 раз в день еще в течение 8 недель, чтобы закрепить результат лечения.
При лечении стрептококковых инфекций терапия должна продолжаться не менее 10 дней.
Антихеликобактерная терапия – 1 - 2 г в сутки 7-14 дней в комплексном лечении с другими препаратами.
Розацеа – по 500 мг (1 таблетка) 2раза в сутки, курс лечения – 10-15 дней.
Пиодермия – по 500 мг (1 таблетка) 2 раза в сутки, курс лечения – 10 дней.
Хронический пародонтит – по 500 мг (1 таблетка) 2 раза в сутки, лечебный курс – 12-14 дней.
Вильпрафен детям
Детям препарат назначают в виде суспензии или в виде разведенных в воде таблеток Вильпрафена Солютаб. Показания и противопоказания к назначению – те же, что и у взрослых.
Недоношенным детям Вильпрафен противопоказан.
Новорожденным и детям до 3 месяцев, а также детям с массой тела менее 10 кг Вильпрафен назначают в редких случаях, только после точного взвешивания.
Суточная доза для детей с массой тела менее 10 кг – 40-50 мг/кг веса ребенка; делится на 2-3 приема.
При весе ребенка 10-20 кг Вильпрафен назначают по 250-500 мг (1/4 или 1/2 таблетки) 2 раза в сутки. Желательно таблетку растворить в воде.
При детской массе тела 20-40 кг препарат назначают по 500-1000 мг (1/2 или целая таблетка) 2 раза в сутки.
Детям с массой тела более 40 кг назначают по 1000 мг (1 таблетка) 2 раза в сутки.
Вильпрафен при беременности и лактации
Вильпрафен гинекологи часто назначают беременным для лечения хламидийной инфекции, но при этом тщательно оценивают состояние беременной и взвешивают все риски.
Лекарственное взаимодействие Вильпрафена
- Не рекомендуется назначать Вильпрафен одновременно с бактерицидными антибиотиками, например, пенициллинами и цефалоспоринами, так как возможно снижение их эффективности.
- Нельзя назначать совместно Линкомицин и Вильпрафен, потому что обоюдно снижается их терапевтический эффект.
- Вильпрафен замедляет выведение из организма Теофиллина, что может привести к интоксикации организма.
- При совместном назначении Вильпрафена и противоаллергических препаратов, содержащих астемизол или терфенадин, может замедлиться их выведение из организма, что приводит к развитию аритмии.
- При одновременном приеме Вильпрафена и алкалоидов спорыньи усиливается вазоконстрикция (сужение просвета кровеносных сосудов).
- При приеме Вильпрафена и циклоспоринов возможно повышение уровня последних в крови, что может обернуться токсическим действием на почки. Поэтому необходим постоянный контроль за количеством циклоспоринов в крови.
- Во время лечения Вильпрафеном возможно снижение эффективности противозачаточных таблеток. В таких случаях рекомендуется на период лечения прибегнуть к дополнительным негормональным методам контрацепции.
- Если принимать Вильпрафен с Дигоксином, возможно повышение концентрации последнего в крови.
Вильпрафен при уреаплазмозе
Вильпрафен – современное средство для лечения уреаплазмоза. При этом терапию проходят оба партнера.
При уреаплазмозе Вильпрафен назначают трижды в день по 1 таб. 500 мг, или дважды в день по 1000 мг (Вильпрафен Солютаб).
При упорном течении уреаплазмоза существует схема, по которой прием Вильпрафена назначают каждые 2 часа. Дозировку при этом определяет только врач, индивидуально.
Одновременно с Вильпрафеном назначают метронидазол, а при необходимости – противогрибковые препараты (например, женщинам – свечи Полижинакс).
Длительность лечебного курса – не менее 10 дней.
Во время лечения нужно воздержаться от половой жизни. Отказаться от алкоголя, курения, соленых, острых и пряных блюд.
При сниженном иммунитете рекомендуется назначать одновременно иммуностимуляторы, такие как "Циклоферон" или "Неовир".
Через две недели после окончания приема антибиотика можно сдавать первый контрольный анализ.
Подробнее об уреаплазмозе
Вильпрафен при хламидиозе
Препарат Вильпрафен предоставляет новые возможности при лечении хламидиоза. Это основное лекарственное средство, которое чаще всего назначают врачи. При этом он отлично переносится больными.
Сам Вильпрафен не убивает хламидии, а только угнетает их жизнедеятельность. Поэтому лечение хламидиоза должно быть комплексным: Вильпрафен назначают по 2 г в сутки, т.е. по 500 мг 4 раза или по 1000 мг 2 раза. Одновременно пациент получает один из следующих антибиотиков: Ровамицин, Тетрациклин, Клиндамицин.
Лечение назначается курсами, каждый из которых длится 7 – 10 дней. В каждом последующем курсе прием Вильпрафена продолжается, а второй антибиотик меняют.
Общую продолжительность лечения определяет врач на основании результатов контрольных анализов.
Подробнее о хламидиозе
Вильпрафен и алкоголь

Вильпрафен с алкоголем сочетать не рекомендуется.
При совместном приеме алкоголя и Вильпрафена возможны нарушения работы пищеварительного тракта, которые проявляются в виде тошноты, рвоты, поноса и болей в животе.
Также реакция может быть замедленной и проявиться со временем в виде цирроза печени из-за токсического воздействия Вильпрафена и алкоголя на печень.
Аналоги Вильпрафена
Отзывы о препарате
В интернете можно найти много положительных отзывов о Вильпрафене, где пациенты отмечают быстрый лечебный эффект препарата (уже при приеме первых доз), особенно при ангине, отите, гайморите, цистите. При этом побочные явления наблюдаются редко.
Авторы некоторых отзывов описывают расстройство стула и тошноту при лечении Вильпрафеном. Отмечается, однако, что эти неприятные эффекты исчезали самопроизвольно через несколько дней.
В отзывах врачей одобрительно отмечается возможность терапии Вильпрафеном при беременности.
Цена препарата в России и Украине
В России Вильпрафен 500 мг стоит от 524 до 613 руб. за упаковку.
В Украине Вильпрафен 500 мг стоит от 270 до 410 грн. за упаковку.
Антибиотики при микоплазме назначаются с целью эрадикации этого микроорганизма.
В идеале лечение проводят до полного его уничтожения, а не уменьшения количества.
Самые эффективные антибиотики при микоплазме
При микоплазмозе далеко не все антибиотики эффективны.
У этих микроорганизмов нет клеточной стенки.
Они имеют лишь цитоплазматическую мембрану.
Соответственно, любые препараты, обладающие бактерицидным эффектом за счет воздействия на клеточную стенку бактерий, не работают.
Поэтому на микоплазму не влияют пенициллины и цефалоспорины, использующиеся для лечения некоторых других половых инфекций (в первую очередь сифилиса и гонореи).
Препаратами выбора для этиотропного лечения микоплазмоза остаются:
Первые две группы антибиотиков работают за счет подавления синтеза белка на рибосомах.
Фторхинолоны блокируют процессы репликации и транскрипции ДНК бактериальной клетки.
В последние годы отмечается учащение случаев резистентности к этой группе препаратов.
Поэтому фторхинолоны старых поколений не назначаются, если не доказана чувствительность микоплазм к ним в ходе бактериологического исследования.
Что же касается макролидов и тетрациклинов, то к ним резистентность встречается нечасто.
Исключение составляет эритромицин.
Некоторые исследования показывают низкую восприимчивость микоплазмы хоминис к этому антибиотику.
Самыми эффективными препаратами для лечения этих инфекций по данным большинства исследований являются доксициклин и джозамицин.

Сохранена чувствительность к тетрациклину.
Но этот антибиотик неудобен в приёме и обладает множеством побочных эффектов.
Если лечение назначается эмпирически (без посева), то в большинстве случаев врач предпочитает один из двух вышеперечисленных антибиотиков.
Другие варианты используются только в таких ситуациях:
- аллергия
- резистентность, подтверждена лабораторно
- неэффективность первого курса терапии
- медицинские противопоказания
Схемы у мужчин и женщин используются одинаковые.
Стандартные методики этиотропного лечения:
- доксициклин внутрь по 100 мг, дважды в сутки
- джозамицин по 500 мг, трижды в день
Курс терапии продолжается от 3 до 5 дней.
Он может быть увеличен, если болезнь хроническая или осложненная.
В таком случае терапию нередко продолжают до 2 недель и более.
Если указанные препараты не работают, может использоваться левофлоксацин.
Его назначают по 250 мг, 1 раз в сутки.
Для повышения эффективности лечения может использоваться посев на микоплазму хоминис с определением чувствительности микроорганизма к антибактериальным препаратам.
Антибиотики при хронических формах микоплазмы
Хронические формы микоплазменной инфекции зачастую с трудом поддаются лечению.
В такой ситуации врачу приходится:
- увеличивать длительность терапевтического курса
- повышать дозы антибиотиков
- использовать больше одного антибактериального препарата
- дополнительно назначать местные процедуры, направленные на уничтожение инфекции в очаге воспаления
- использовать лекарственные средства и процедуры, повышающие эффективность антибиотикотерапии
Хронические формы лучше лечить после проведения бактериологического посева.
Исследования показывают, что в этом случае вероятность успешного излечения болезни после первого курса значительно выше.
По результатам посева врач точно знает, к каким препаратам микоплазма чувствительна, а какие использовать не стоит.
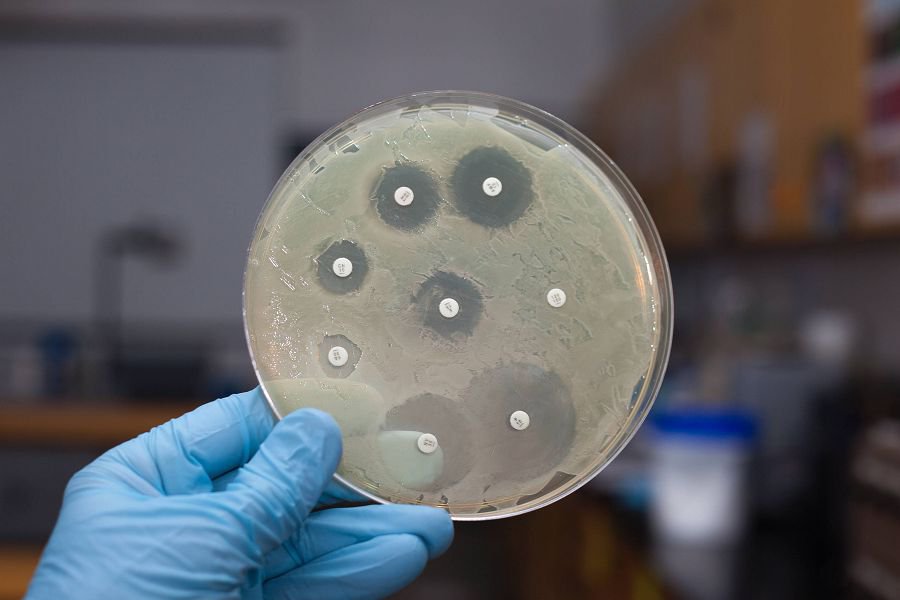
К некоторым лекарствам бактерия приобретает устойчивость.
К другим её чувствительность снижена, поэтому стандартные дозировки могут не приводить к эрадикации микроорганизма.
При хроническом микоплазмозе дополнительно используют:
- ферменты – улучшают проникновение антибактериальных препаратов в воспаленные ткани, повышая их концентрацию в патологическом очаге на 30-50%
- антисептики – применяются местно, в виде инстилляций, тампонад уретры, вагинальных свечей и таблеток, сидячих ванночек
- иммуномодуляторы – помогают усилить иммунитет, так как именно на фоне снижения защитных сил организма прогрессирует микоплазменная инфекция и вызывает активные клинические проявления
Курс лечения может быть дольше в 2-3 раза.
Особенно если пациент лечится не первый раз.
Нередко при обращении в нашу клинику человек уже лечился в других медучреждениях, но не получил ожидаемого результата.
Антибиотики при микоплазме при поражении суставов
На фоне микоплазмоза могут воспаляться суставы.
Это состояние называют болезнью Рейтера.
Микоплазма – вторая по частоте среди половых инфекций причина этой патологии (после хламидиоза).
Она вызывает около 15% случаев болезни Рейтера, обусловленных венерическими заболеваниями.
У человека появляются боли в суставах, они опухают и краснеют.

Подвижность снижается, в полости накапливается выпот.
Возникает это состояние спустя несколько месяцев после заражения.
Продолжается болезнь Рейтера в течение нескольких месяцев.
Нужны ли в этом случае антибиотики?
Конечно же, препараты необходимы.
Но вовсе не для того, чтобы очистить суставы от бактерий.
Никаких микоплазм на самом деле в суставах нет.
Это воспаление носит реактивный характер.
Чтобы устранить иммунную реакцию, нужно убрать раздражитель.
В данном случае раздражителем является микоплазма.
После излечения инфекции состояние пациента улучшается.
Воспаление суставов может продолжаться даже после успешной антибиотикотерапии.
Но через несколько недель, реже – месяцев, оно прекращается.
Проходит воспаление суставов и без антибиотиков.
Но если в организме сохраняются микоплазмы, то высока вероятность рецидива болезни Рейтера.
Каждый такой случай несёт значительную угрозу здоровью человека.
У него воспаляются суставы и сухожилия, и в некоторых случаях сохраняются остаточные явления.
В 20% трудоспособность пациента снижена после перенесенного реактивного воспаления в результате необратимых повреждений тканей.
В отдельных ситуациях поражаются внутренние органы, что грозит тяжелым ухудшением состояния здоровья и даже летальным исходом.
Поэтому болезнь Рейтера, причиной которой является микоплазмоз, является несомненным показанием к назначению антибиотикотерапии.
В том числе в ситуациях, когда количество микоплазм в урогенитальном тракте минимально, и они не вызывают клинических симптомов.
Нужны ли антибиотики при микоплазме хоминис?
Спорным остается вопрос, нужны ли антибиотики при бессимптомной колонизации микоплазмой хоминис.
Если заражение происходит микоплазмой гениталиум, то антибактериальная терапия, безусловно, необходима.
Потому что эта бактерия патогенная.
Она вызывает воспаления репродуктивных органов, опасна для беременных женщин, часто провоцирует осложнения.
В то же время микоплазма хоминис является гораздо менее патогенным микроорганизмом.
Встречается она чаще.
Нередко выявляется у бессимптомных носителей.
Бывает так, что человек приходит обследоваться на венерические инфекции с профилактической целью.
У него находят микоплазмы.
При этом никаких жалоб нет, поэтому пациент не понимает, зачем ему нужно лечиться.
Единого мнения среди врачей по поводу необходимости терапии нет.

Некоторые считают, что лечению подлежит каждый случай микоплазмоза.
Другие полагают, что следует определять количество микоплазм, и проводить терапию, только если бактерий много.
Существует также мнение, что только наличие субъективных симптомов, клинических или лабораторных признаков воспаления может быть поводом для антибактериального лечения.
Вероятно, можно вылечить некоторые категории пациентов, которым антибиотики при микоплазме хоминис не нужны.
Не лечиться можно, если сочетаются все перечисленные ниже обстоятельства:
- микоплазм в урогенитальном тракте мало (меньше 10 в 4 степени копий в мл), признаков воспаления нет, бактерии вам ничем не мешают
- вы точно знаете, что менять половых партнеров не будете никогда, либо вообще не имеете половой жизни (то есть, не представляете эпидемиологической опасности для окружающих)
- вы не планируете беременность (свою или своей супруги) вообще никогда (например, у вас уже есть трое детей, и рождение четвертого стало бы катастрофой, либо вы попросту вышли из репродуктивного возраста)
Тем не менее, такие люди обычно не приходят в клинику и не сдают анализы на микоплазмоз.
Соответственно, инфекция у них попросту не обнаруживается.
Если человек явился в клинику сдавать анализы на венерические заболевания, то наверняка ведет половую жизнь и пребывает в репродуктивном возрасте.
Поэтому фактически большинство пациентов с выявленной микоплазмой хоминис получают лечение.
Небольшое количество бактерий и отсутствие симптомов не говорит о том, что микроорганизм не опасен.
Он вызовет воспаление урогенитального тракта при первом же удобном случае, например:
- при снижении иммунитета
- после антибиотикотерапии препаратами, уничтожающими конкурирующую микрофлору
- на фоне дисбиоза влагалища у женщин
- после наступления беременности
- при присоединении другой инфекции и т.д.
Микоплазмы даже при бессимптомном течении проникают в матку, придатки, простату, яички.
Там они создают условия, благоприятные для развития инфекционного процесса, вызванного грамотрицательной микрофлорой.
У женщин микоплазма хоминис повышает риск бактериального вагиноза.

Это состояние хоть и не опасно для здоровья, но всё же очень неприятно, так как вызывает постоянные выделения и исходящий из половых путей неприятный запах испорченной рыбы.
Антибиотики при микоплазме при аллергии
У некоторых пациентов есть аллергия на антибиотики.
Однако при лечении венерических инфекций встречается она редко.
Лекарственная аллергия среди взрослых – не очень частое явление в целом.
К тому же, реакции развиваются только при повторном курсе антибиотикотерапии.
То есть, он возможны, если назначенный вам препарат ранее уже использовался (возможно, много лет назад).
При микоплазмозе аллергия встречается нечасто, и проявления обычно не тяжелые.
Причин тому несколько:
- Чаще всего встречается аллергия на пенициллины и цефалоспорины, но ими микоплазмоз не лечат.
- Чаще развиваются аллергические реакции на введение больших доз антибиотиков внутривенно или внутримышечно.В то время как при микоплазмозе используются таблетки длительным курсом и в относительно небольших дозировках.
- Для сильной аллергической реакции между первым и повторным курсом антибиотикотерапии должно пройти не много времени (недели, месяцы, но не годы).
Это не столь частое явление.
Обычно если человек не долечился, антибиотик меняют.
Соответственно, аллергия исключена.
Тот же антибиотик может использоваться, разве что если не пролечен источник инфекции, и человек инфицировался повторно.
Риск лекарственной аллергии возрастает на фоне:
- ВИЧ
- цитомегаловируса
- инфекционного мононуклеоза
- подагры
При приёме антибиотиков для лечения микоплазмоза перорально обычно возникают лишь небольшие кожные проявления аллергии.
Они могут купироваться антигистаминными средствами.
Тем не менее, развивающаяся на фоне лечения лекарственная аллергия является основанием для замены антибиотика.
Обычно берут препарат другой фармакологической группы.
Антибиотики при микоплазме в составе микст-инфекций
Бывает так, что при обследовании у человека выявляют сразу несколько инфекций.
Это явление довольно частое.

В венерологии оно встречается более чем у 50% пациентов.
Причин тому несколько:
- одна инфекция часто облегчает процесс проникновения другой
- венерическими заболеваниями нередко болеют люди, ведущие разнообразную сексуальную жизнь, поэтому у них высокий риск инфицирования этими патологиями
- инфекции часто протекают без симптомов, и обнаруживаются спустя годы, когда человек дополнительно заражается другим заболеванием
- к одновременному инфицированию двумя и более болезнями могут привести контакты с человеком, который имеет много половых партнеров (при этом не важно, как часто вы сами их меняете)
Если микоплазмоз сочетается с другими инфекциями, то вариантов лечения два:
- Подбор антибиотика, который одновременно влияет не только на микоплазму, но и на возбудителя сопутствующего заболевания.
- Использование двух антибактериальных препаратов.
В каждом случае врач стремится максимально снизить лекарственную нагрузку на организм пациента.
Поэтому по возможности антибиотик используется только один.
Но не при всех инфекциях это возможно.
К примеру, микоплазмоз может сочетаться с сифилисом, который лечится пенициллинами.
Или на его фоне возникает гонорея, для терапии которой назначают цефтриаксон.
Эти антибиотики не способны уничтожить микоплазму.
Не влияют на неё также антитрихомонадные средства, противогрибковые препараты.
Но микоплазма зачастую чувствительна к клиндамицину, который также используется при гарднереллёзе.
Кроме того, одним антибиотиком можно лечить эту инфекцию, если она сочетается с уреаплазмозом и хламидиозом.
Все эти инфекции восприимчивы к джозамицину и доксициклину.
При лечении микст-инфекций врач всегда учитывает возможность взаимодействия антибиотиков, если они используются в количестве более одного.
Некоторые из них несовместимы, так как снижается эффективность терапии или повышается риск осложнений.
Другие напротив, способны усиливать действие друг друга.
Антибиотики при микоплазме во время беременности
Для лечения микоплазмоза используются три группы антибиотиков.
Две из них противопоказаны на всех сроках беременности, так как повышают риск развития пороков у плода.
Использоваться для лечения микоплазмы могут только макролиды.

Препаратом выбора остается джозамицин.
По возможности стоит воздержаться от терапии.
Если нет активных проявлений воспалительного процесса в урогенитальном тракте, инструментальных и лабораторных признаков воспаления внутренних половых органов, врач может воздержаться от проведения терапии.
Так как сама микоплазма хоминис в неактивной форме может представлять меньшую угрозу здоровью, чем проводимое лечение.
Антибиотики при микоплазме у детей
Микоплазмозом дети обычно заражаются от своих матерей во время родов.
Не исключено и внутриутробное инфицирование.
У них проявления могут развиваться со стороны различных органов и систем, включая:
Для лечения микоплазмоза назначают джозамицин.
Используют возрастные дозировки.
Если речь идёт о новорожденном, назначают 50 мг на 1 кг массы тела в сутки.
Эту дозировку разделяют на три приёма.
Курс лечения длится минимум 10 дней.
Подросткам с массой тела от 45 кг назначают взрослые дозы.
Куда обратиться для диагностики и лечения микоплазмы?
Чтобы сдать анализы на микоплазмоз или пройти лечение, обратитесь в нашу клинику.
Здесь работают высококвалифицированные венерологи.

Они смогут оказать помощь даже в самых трудных ситуациях, включая:
- осложненное течение микоплазмоза
- хроническая форма болезни
- неоднократные безуспешные попытки лечения в прошлом
- сочетанные инфекции урогенитального тракта и т.д.
Мы проводим лечение антибиотиками до полного исчезновения микоплазмы.
После терапии подтверждаем излеченность при помощи высокоточных анализов.
Для диагностики и лечения микоплазмы обращайтесь к автору этой статьи – венерологу в Москве с многолетним опытом работы.
Читайте также:


