Синдром обезвоживания инфекционные болезни
В статье изложены современные подходы к регидратационной терапии при острых кишечных инфекциях у детей, в том числе с использованием комплексных методов, направленных на коррекцию не только синдрома обезвоживания, но и микроэкологических нарушений, ассоци
The article covers modern approaches to fluid therapy in acute intestinal infections in children, including use of complex methods directed not only to correction of dehydration syndrome, but also micro-ecological disorders associated with infectious affection of the intestine.
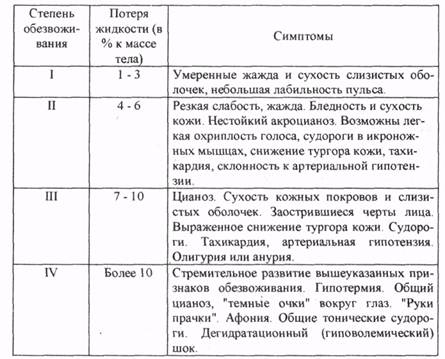
Дегидратационный синдром является ведущим патогенетическим фактором при ОКИ у детей, обуславливая тяжесть заболевания. Поэтому особую значимость для практического здравоохранения приобретает оперативность и правильность оценки степени дегидратации у ребенка, больного ОКИ [9]. Фундаментальные исследования Н. В. Воротынцевой, В. В. Малеева, В. И. Покровского по оценке выраженности обезвоживания на основе оценки острой потери массы тела пациента сохраняют свою актуальность до настоящего времени: эксикозу I степени соответствует потеря до 5% массы тела, что составляет до 50 мл/кг жидкости, эксикозу II степени — потеря 6–10% массы тела (60–100 мл/кг), эксикозу III степени — потеря более 10% массы тела (110–150 мл/кг). Обезвоживание с потерей массы тела более 20% не совместимо с жизнью [10]. Однако применительно к педиатрической практике определение дефицита массы тела ребенка на фоне болезни не всегда возможно ввиду интенсивного роста детей, поэтому оценка степени дегидратации проводится на основе клинических данных. В этой связи в настоящее время широкое распространение получили рекомендации Европейского общества педиатров, гастроэнтерологов и диетологов (European Society for Paediatric Gastroenterology Hepatology and Nutrition, ESPGHAN) от 2014 г. [11]. Однако в них предусмотрена клиническая оценка только внешнего вида, состояния глазных яблок и слизистых оболочек, а также наличие у ребенка слез. Более полная клиническая шкала M. H. Gorelick дополнительно включает определение времени капиллярной реперфузии (в норме не более 2 секунд), снижение диуреза, основные гемодинамические показатели (частота и наполнение пульса) и показатели нарушения дыхания [12]. Существуют и другие шкалы клинической оценки выраженности обезвоживания. Однако значимость каждого из симптомов обезвоживания в клинической практике может быть не всегда достаточно высокой, особенно при эксикозе I степени, что делает их наиболее применимыми при эксикозе II степени (табл. 1).
При ОКИ у детей преобладает изотонический тип обезвоживания, характеризующийся пропорциональной потерей жидкости и электролитов, в первую очередь натрия. При этом не отмечается изменения осмотического давления воды во внутриклеточном и внеклеточном пространствах, что затрудняет его определение лабораторными методами [15].
Объективизация диагностики степени выраженности обезвоживания у детей возможна с применением алгоритма, включающего клинические (увеличение времени капиллярной реперфузии, определяемая клинически сухость слизистых оболочек), анамнестические (выраженность диареи и рвоты), инструментальные (оценка влажности кожных покровов) и лабораторные (дефицит буферных оснований сыворотки крови) данные [16].
Также одним из важных аспектов патогенеза, являющегося закономерным для ОКИ любой этиологии, является развитие нарушений микрофлоры желудочно-кишечного тракта (ЖКТ). Ранее было показано, что при дизентерии Зонне у 67,8–85,1% пациентов, при сальмонеллезе — у 95,1%, иерсиниозе — у 94,9%, ротавирусной инфекции — у 37,2–62,8% нарушения со стороны микрофлоры ЖКТ носят выраженный характер [17–19].
Дестабилизация микробиоценоза ЖКТ на фоне течения инфекционного процесса приводит к снижению колонизационной резистентности микрофлоры, повышению выраженности воспалительных реакций со стороны слизистой оболочки кишки и снижению темпов репаративных процессов в кишечнике, что приводит к усугублению интоксикационного синдрома за счет высвобождения токсинов не только патогенных возбудителей, но и представителей условно-патогенной микрофлоры (УПФ), доля которых при ОКИ возрастает [20].
Основные патогенетические аспекты ОКИ обосновывают и терапевтические подходы — регидратационную и пробиотическую терапию, от своевременности и адекватности назначения которых зависят длительность заболевания и его исходы [10].
При развитии дегидратации основным принципом ведения таких больных является быстрое возмещение потерь жидкости и солей, а также увеличение буферной емкости крови. Общепризнано, что в педиатрической практике следует отдавать предпочтение оральной регидратации, как менее травматичной и более физиологичной для ребенка [21]. Международная практика применения оральной регидратации при ОКИ получила широкое применение с 70-х годов XX века, а ее включение в стандарты ведения больных позволило сократить число случаев госпитализации на 50–60% и значительно, на 40–50%, снизить летальность детей [22]. Однако первые рекомендации, которые можно отнести к регидратационной терапии и включающие в себя назначение рисового отвара, кокосового сока и морковного супа, относятся к периоду более 2500 лет назад и принадлежат древнеиндийскому врачу Sushruta [23]. В 1874 г. во Франции доктором Luton было обосновано назначение дополнительной воды для лечения детей, больных ОКИ. Впервые раствор, в состав которого вошли глюкоза, натрий и хлор, предложил использовать доктор Robert A. Phillips, после открытия механизма потенцирования глюкозой всасывания в кишечнике ионов натрия и калия [23]. В нашей стране в 30–50-х годах XX века проводилась разработка методов регидратационной терапии ОКИ М. С. Масловым (1928, 1945, 1955), В. И. Моревым (1937), В. Е. Балабан (1937). Основные принципы оральной регидратации, состав растворов и методы организации помощи больным ОКИ в нашей стране были разработаны Центральным научно-исследовательским институтом эпидемиологии под руководством В. И. Покровского [10].
Общий терапевтический подход к оральной регидратации предусматривает раннее назначение регидратационных растворов и проводится в два этапа:
- 1-й этап — восполнение потерь, произошедших до момента обращения за медицинской помощью. Назначается суммарное количество жидкости 50–80 мл/кг в течение 6 ч;
- 2-й этап — поддерживающая регидратация, задачей которой является восполнение текущих потерь жидкости при ОКИ. В сутки назначается 80–100 мл/кг жидкости. Длительность второго этапа оральной регидратации продолжается до момента выздоровления или появления показаний для парентеральной коррекции обезвоживания [24].
Согласно действующим современным подходам, для проведения оральной регидратации рекомендовано использование готовых форм растворов, сбалансированных по электролитному составу и осмолярности (75 мэкв/л натрия и 75 мэкв/л глюкозы и осмолярностью 245 мосм/л), при этом значению осмолярности растворов, рекомендуемых для педиатрического применения, уделяется огромное значение.
На заре внедрения метода в рутинную клиническую практику в 1970 г., Всемирная организация здравоохранения рекомендовала для проведения оральной регидратации составы с общей осмолярностью 311 ммоль/л. Несмотря на их эффективность в коррекции обезвоживания главным недостатком данных базовых растворов было отсутствие положительного влияния на диарейный синдром. Одним из достижений, предложенным в 2004 г. ВОЗ, было снижение осмолярности растворов для оральной регидратации до 245 ммоль/л, а концентрации натрия до 75 ммоль/л и глюкозы до 75 ммоль/л. Принципиальным отличием гипоосмолярных формул для оральной регидратации является то, что у предыдущих растворов осмолярность была выше по сравнению с плазмой крови, что не способствовало снижению объема каловых масс при диарее и могло приводить к развитию гипернатриемии [25–28]. В 2001 г. Seokyung Hahn был сделан метаанализ 15 рандомизированных клинических исследований, проведенных в различных странах мира, который показал, что применение растворов для оральной регидратации со сниженной осмолярностью оптимизирует всасывание воды и электролитов в кишечнике в большей степени, чем использование гиперосмолярных растворов, при этом не было зарегистрировано случаев клинически значимой гипонатриемии, за исключением случаев холеры [29].
Также было показано, что данный тип растворов уменьшает потребность в инфузионной терапии, снижает выраженность диарейного синдрома и рвоты и позволяет уменьшить объемы растворов при проводимой оральной регидратации, что является важным преимуществом для педиатрии [16].
Необходимо учитывать, что коррекция обезвоживания должна проводиться с использованием и бессолевых растворов, среди которых предпочтение следует отдать питьевой воде (не минеральной!), возможно использование пектинсодержащих отваров (яблочный компот без сахара, морковно-рисовый отвар). Соотношение глюкозосолевых растворов и питьевой воды должно быть 1:1 при водянистой диарее, 2:1 при выраженной рвоте, 1:2 при инвазивных диареях [24].
Тяжелые формы ОКИ, отсутствие эффекта от оральной регидратации или наличие обильной рвоты, отеков, развитие функциональной (острой) почечной недостаточности являются показаниями для проведения парентеральной регидратации, которая может быть осуществлена с использованием одного из современных отечественных растворов — 1,5% раствора меглюмина натрия сукцината, доказавшего свою эффективность в интенсивной терапии данных состояний [30].
Патогенетическое обоснование необходимости применения пробиотических лекарственных средств при ОКИ не вызывает сомнения как в отечественной, так и в зарубежной литературе. Пробиотическую терапию рекомендовано назначать в составе комплексной стартовой терапии вне зависимости от этиологии заболевания и в как можно более ранние сроки. Данные препараты показаны также всем пациентам в периоде реконвалесценции с целью восстановления параметров микробиоценоза. Их применение при ОКИ у детей является не только патогенетически обоснованным, но и относится к самому высокому уровню доказательности — А — в соответствии с принципами доказательной медицины [31]. Данный факт был подтвержден в 2010 г. результатами метаанализа, включившего в себя результаты 63 рандомизированных контролируемых клинических исследований. В нем было показано, что использование пробиотиков достоверно уменьшает продолжительность диареи в среднем на 24,76 часа и сокращает частоту стула, при этом данные препараты характеризуются высоким профилем безопасности [32].
Одним из патогенетических механизмов, позволяющих рекомендовать пробиотики при ОКИ, является их положительное влияние на муциновый слой слизистой оболочки ЖКТ. На фоне течения инфекционного процесса наблюдается изменение физических характеристик данного барьера — снижение вязкости за счет разрушения дисульфидных связей между цистеиновыми мостиками суперструктуры данного геля, что может приводить к транслокации микроорганизмов из просвета кишечника в ткани. Данные процессы развиваются под действием патогенных микроорганизмов, имеющих соответствующие факторы патогенности в виде ферментов, разрушающих слизь (нейраминидаза, гиалуронидаза, муциназа). Длительное, в том числе в постинфекционном периоде, изменение физических свойств муцинового слоя приводит к риску развития воспалительных заболеваний кишечника [33]. Микроорганизмы, относящиеся к компонентам нормальной микрофлоры ЖКТ человека, а также продукты их обмена оказывают потенцирующее действие на состояние муцинового слоя посредством целого ряда механизмов, в том числе генетических [34, 35].
Современный взгляд на терапию пробиотиками подразумевает штамм-специфичный подход, который включает в себя установление в клинических исследованиях терапевтических эффектов, характерных для определенных генетически сертифицированных штаммов и дальнейшее их использование с учетом штамм-специфичных свойств пробиотиков в различных клинических ситуациях [36, 37].
Применительно к острым кишечным инфекциям у детей рабочая группа ESPGHAN в 2014 г. на основе анализа опубликованных систематических обзоров и результатов рандомизированных клинических исследований, в том числе плацебо-контролируемых, опубликовала меморандум, в котором разделила все пробиотические штаммы на пробиотики с положительной рекомендацией, с отрицательной рекомендацией и пробиотики с недостаточными доказательствами их эффективности. К рекомендованным штаммам (несмотря на низкий уровень доказательной базы по мнению экспертов) для терапии ОКИ у детей были отнесены Lactobacillus GG, Saccharomyces boulardii, Lactobacillus reuteri штамм DSM 17938 (исходный штамм ATCC 55730), а также термически инактивированный штамм Lactobacillus acidophilus LB, который формально к пробиотикам как живым микроорганизмам с заданными полезными свойствами отнесен быть не может, однако он показал свою эффективность при острых инфекционных гастроэнтеритах [38].
Штамм Lactobacillus reuteri DSM 17938 устойчив к следующим антимикробным средствам (возможен совместный прием пробиотиков Lactobacillus reuteri Protectis с этими средствами): амоксициллин, ампициллин, Аугментин, диклоксациллин, оксациллин, пенициллин G, феноксиметилпенициллин, цефуроксим, цефалотин, ванкомицин, доксициклин, тетрациклин, фузидовая кислота, ципрофлоксацин, энрофлоксацин, налидиксовая кислота, метронидазол. Lactobacillus reuteri DSM 17938 чувствительны к цефотаксиму, неомицину, стрептомицину, кларитромицину, эритромицину, рокситромицину, клиндамицину, хлорамфениколу, рифампицину, имипенему, линезолиду, виргиниамицину.
При этом Lactobacillus reuteri DSM 17938 характеризуется хорошим профилем безопасности, что подтверждено Продовольственной и сельскохозяйственной организацией ООН (Food and Agriculture Оrganization of the United Nations, FAO) и ВОЗ в 2002 г.
Клиническая эффективность Lactobacillus reuteri DSM 17938 показана при функциональных коликах у детей первого года жизни, в составе комплексной эрадикационной терапии H. рylori-инфекции, профилактики антибиотик-ассоциированной диареи, при метаболическом синдроме, в терапии аллергических заболеваний. Эффективность данного штамма подтверждена в 163 клинических исследованиях у 14 000 пациентов, из которых 114 — рандомизированные, двойные/слепые или слепые плацебо-контролируемые исследования, 47 — открытые исследования, 56 исследований проводились среди 7300 детей 0–3 лет жизни.
Однако наиболее хорошо изучены клинические эффекты данного штамма при ОКИ, что послужило причиной включения его в рекомендации ESPGHAN. Так, в многоцентровом рандомизированном простом слепом клиническом исследовании, проведенном среди госпитализированных с острым гастроэнтеритом детей, получавших традиционную терапию с или без 1 × 10 8 КОЕ Lactobacillus reuteri DSM 17938 на протяжении 5 дней, было показано, что назначение данного пробиотического штамма сокращает продолжительность диареи через 24 и 48 ч (50% в основной группе против 5% в группе сравнения, p
А. А. Плоскирева 1 , кандидат медицинских наук
А. В. Горелов, доктор медицинских наук, профессор, член-корреспондент РАН
ФБУН ЦНИИЭ Роспотребнадзора, Москва
Острый геморрагический синдром
Нарушение системы свертывания крови - гемостаза является одним из патогенетических звеньев геморрагических лихорадок, менингококцемии, заболеваний с поражением печени, а также некоторых критических состояний. В клинической практике оно нередко определяется как острый геморрагический синдром (ОГС), так как ведущими его проявлениями являются геморрагические экзантема и энантема, кровотечения. Патогенетическим механизмом нарушений гемостаза является ДВС.
Нарушения системы свертывания при различных инфекционных заболеваниях могут быть обусловлены воздействием микробных экзо- и эндотоксинов, способных повреждать эндотелий сосудов и вызывать агрегацию форменных элементов. Их массивное воздействие ведет к молниеносному ДВС, протекающему в сочетании с различными критическими состояниями.
Ключевым компонентом критического состояния синдром ДВС может выступать в случае генерализованного поражения сосудистых стенок (геморрагические лихорадки, риккетсиозы, менинго-кокцемия, грипп и др.), аггрегации тромбоцитов под воздействием биологически активных веществ при ИТШ, анафилактическом шоке, бурно протекающей реакции антиген-антитело, в случаях массивного поступления в кровь тромбопластина и его активаторов (массивный внутрисосудистый гемолиз при малярии, лихорадке Денге, ИТШ, инфекции с капилляротоксическим компонентом), в случаях нарушений реологических свойств крови (шоковые состояния, острая дыхательная недостаточность и др.).
Наличие ДВС, особенно его острой, молниеносной формы, в значительной степени ухудшает прогноз при тяжелом течении различных инфекций, в частности, геморрагических лихорадок, менингококцемии, гриппа, чумы, а также определяет крайне неблагоприятное течение ОДН, ОПечН, ОПочН и других критических состояний.
Прогноз его основывается на учете патогенетических механизмов тяжелых форм инфекционных заболеваний или критических состояний. Для объективной оценки используются определение общего времени свертывания крови, протромбинового времени, количества фибриногена и тромбоцитов, фибринолитической активности крови. Для первой стадии ДВС характерны уменьшение времени свертывания в сочетании с тромбоцитопенией. Во второй стадии происходит увеличение протромбинового времени, отмечается ги-пофибриногенемия и тромбоцитопения, нарушена или отсутствует ретракция сгустка.
Дефицит воды в организме в результате преобладания потери жидкости над ее поступлением ведёт к развитию дегидратацион-ного синдрома (ДС), который всегда сочетается с изменениями электролитного баланса, преимущественно натрия и калия. В зависимости от патогенетических механизмов обезвоживания, характера нарушений водно-электролитного баланса и соответственно коллоидно-осмотического давления крови различают изотоническую, гипертоническую и гипотоническую дегидратацию. При тяжелом течении инфекционных заболеваний чаще встречаются изотонические и гипертонические типы обезвоживания.
Изотоническая дегидратация возникает в результате потерь изотонической жидкости, бедной белком, при профузной диарее, нередко в сочетании со рвотой. Она может развиться вследствие неконтролируемого применения салуретиков. Изотоническая дегидратация является ведущим критическим состоянием у больных холерой, гастроинтестинальными формами сальмонеллеза и других диарейных кишечных инфекций, при которых усиливается транссудация в просвет тонкой кишки изотонической жидкости, избыток которой не в состоянии реабсорбироваться в нижних отделах кишечника. Основанием для ее диагностики, помимо характерной клинической симптоматики, позволяющей определить степень обезвоживания и ориентировочное количество потери жидкости, являются гастроэнтерические синдромы.
Гипертоническая дегидратация может возникнуть у больных с сильной лихорадкой (сап, мелиоидоз, сыпной тиф и другие риккетсиозы, тифо-паратифозные заболевания) вследствие повышенных потерь гипотонической жидкости путем перспирации, при недостаточном поступлении воды у коматозных больных, в случаях
нарушения глотания (ботулизм, энцефаломиелиты и др.). Дефицит воды превышает потери электролитов. В результате повышается коллоидно-осмотическое давление плазмы, происходит перемещение воды в сосудистое русло из интерстициального пространства и в большей степени из клеток с нарушением их функций, прежде всего ЦНС (табл. 4).
Степени обезвоживания у инфекционных больных с дегидратационным синдромом
ко жажда, усиливается характерная для основного патологического состояния слабость. Если дефицит воды достигает 5 л, появляются апатия, сонливость, усиливается жажда. Кожа сухая, морщинистая, слизистые сухие. Язык сухой, покрасневший, иногда с коричневым налетом (при брюшном тифе) Отмечается гипосаливация, в связи с чем затруднен прием твердой пищи. Снижается суточный диурез до
500 мл, может наблюдаться олигурия при повышенной относительной плотности плазмы.
В случаях дефицита воды до 6 - 8 л усиливаются жажда и другие проявления дегидратации. Появляются признаки энцефалопатии, беспокойство, возбуждение, угнетение сознания вплоть до комы. Могут наблюдаться тонические судороги. Появляются выраженные гемодинамические расстройства: на фоне нарастающей тахикардии развивается артериальная гипотензия при повышенном пульсовом давлении. Наступает олигоанурия.
Обычно гипертоническая дегидратация развивается медленно, наблюдается в случаях недостаточной коррекции водно-электролитного баланса. Для нее характерно повышение осмотического давления плазмы за счет увеличения содержания в ней натрия.
Гипотоническая дегидратация возникает в случаях, когда потери жидкости возмещаются водой, не содержащей электролитов, у больных с сильной лихорадкой, при заболеваниях с параличом глотания (ботулизм, энцефаломиелиты), при коматозных состояниях. В связи с гипотоничностью плазмы вода перемещается из внеклеточного пространства в клетки, поэтому в клинической картине доминируют геморрагические расстройства, которые могут быстро привести к шоку. Жажды нет. Быстро нарастают общая слабость, головокружение, ортостатический коллапс.
Эластичность тканей и тургор кожи понижены. Глазные яблоки мягкие. По мере нарастания гипотонической дегидратации усиливается слабость, появляются головокружение, тошнота, рвота, угнетение сознания. Снижается артериальное давление, усиливается тахикардия. Кожа холодная, цианотичная, вены спадаются. Развивается шок. Тяжесть состояния определяется степенью гипонатрие-
Дегидратационный синдром является отражением обезвоживания различной степени и различных патогенетических механизмов. Поэтому в каждом конкретном случае необходимо учитывать динамику заболевания, его патофизиологические механизмы, характер проводившейся терапии. Дегидратационный (гиповолемиче-ский) шок представляет собой крайнюю степень преимущественно изотонического типа обезвоживания, для которого характерны преимущественно гемодинамические расстройства. В случаях гипер-или гипотонической дегидратации страдают в первую очередь клетки, что наиболее ярко проявляется нарушением функции ЦНС в виде энцефалопатии. При этом необходимо дифференцировать обез-
воживание и проявления общей инфекционной интоксикации или поражения ЦНС другого генеза.
Не нашли то, что искали? Воспользуйтесь поиском:

Обезвоживание организма — это патологическое состояние, возникающее, когда потери воды превышают ее поступление. Характеризуется жаждой, уменьшением диуреза, сухостью кожи. В тяжелых случаях отмечаются такие симптомы, как гипотензия, нарушение сознания, диффузный цианоз. Обезвоживание диагностируется по результатам лабораторного обследования, которое позволяет обнаружить рост показателей гематокрита, изменение КОС. Также учитывается уровень центрального венозного давления. Специфическое лечение: восполнение дефицита ОЦК, нормализация гематокрита, коррекция электролитных нарушений .
МКБ-10
Общие сведения
Обезвоживание организма (дегидратация, эксикоз) – патология, связанная с острым недостатком жидкости в организме. По современным представлениям, обезвоживание возникает уже при дефиците воды 40-50 мл/кг. При этом масса тела пациента уменьшается на 4-5% от исходной. Тяжесть состояния нарастает по мере нарушения водного баланса. Смерть наступает после утраты 20-25% от общего объема жидкости, содержащейся в составе крови, межклеточного матрикса и клеток. Причина гибели – тканевая ишемия и метаболические расстройства.

Причины
Основная причина обезвоживания организма – чрезмерно высокая и быстрая потеря воды. Чаще эксикозы развиваются в жарком климате, у лиц, имеющих хронические заболевания или расстройства пищеварения. Ведущие этиофакторы:
- Кишечные инфекции. На их долю приходится около 48% от общего количества случаев дегидратации. Жидкость теряется с рвотными массами и жидким стулом. Обезвоживание на фоне кишечных инфекций обычно выявляют у детей в возрасте до 5-6 лет. Это связано с низкими компенсаторными возможностями у данной категории пациентов.
- Обширные ожоги. Обезвоживание организма возникает на фоне массивного выделения ожогового экссудата, если пациент не получает адекватную инфузионную терапию. Симптомы дефицита жидкости отмечаются уже при II степени термического поражения, если его площадь превышает 10-15% тела.
- Усиленное потоотделение. Происходит при повышенной температуре тела или нахождении в помещениях с высокой температурой окружающего воздуха. Признаки обезвоживания появляются через несколько часов интенсивного выделения пота без компенсации потерь воды за счет обильного питья.
- Недостаточность питания. В норме человек ежедневно теряет около полутора литров жидкости даже при отсутствии факторов, усиливающих ее выведение. Обезвоживание организма происходит, если суточное потребление воды оказывается меньшим, чем объем ее выведения с мочой, калом, потом и другими физиологическими выделениями.
- Одышка. С каждым выдохом из организма выводится некоторое количество водяного пара. Чем больше выдохов делает человек, тем больше влаги он теряет. Этим обусловлено обезвоживание у больных, страдающих респираторной патологией, а также у туристов во время поездок в горные районы.
Существует ряд факторов, которые повышают вероятность развития дегидратации. Люди, подвергающиеся их воздействию, должны много пить и употреблять богатые жидкостью продукты (сельдерей, огурцы, помидоры, болгарский перец), а также постоянно контролировать свое состояние. Условия, провоцирующие обезвоживание:
- проживание в тропическом климате;
- выполнение физической работы на жаре;
- интенсивные занятия спортом;
- регулярный прием диуретиков;
- болезни органов дыхания;
- пребывание в горах.
В группе особого риска − пациенты, длительно находящиеся на ИВЛ. Недостаточно увлажненная дыхательная смесь высушивает альвеолы. За счет активизации компенсаторных механизмов усиливается образование сурфактанта, что требует дополнительного расхода жидкости. Потери компенсируются за счет постоянной инфузии солевых растворов и увлажнения поступающего через аппарат воздуха.
Патогенез
Потеря большого количества воды сопровождается снижением объема циркулирующей в сосудах плазмы и повышением вязкости крови. Сердечный выброс уменьшается, тканевая микроциркуляция замедляется. Возникает гипоперфузия и ишемия внутренних органов, в том числе головного мозга. Отмечается изменение баланса электролитов, снижение концентрации калия, натрия, кальция.
Недостаток минеральных солей приводит к возникновению у пострадавшего симптомов коронарной патологии. Отмечаются значительные нарушения ритма. Проведение нервного импульса замедляется, что становится причиной снижения тонуса гладкой мускулатуры, развития ацидоза. После многократной рвоты желудочным содержимым выявляется алкалоз.
Классификация
Обезвоживание организма разделяется на несколько больших групп:
- по течению патологии (легкое, средней тяжести, тяжелое);
- по причинам (внутренние, внешние);
- по наличию осложнений (осложненное, неосложненное).
Наиболее распространенным и клинически значимым вариантом считается классификация эксикозов по концентрации электролитов крови:
- Гиперосмолярная форма. Утрата воды преобладает над потерей солей. Концентрация последних в крови нарастает. Происходит выделение H2O из клеток и межклеточного пространства в сосудистое русло. ОЦК снижается медленно, артериальное давление длительно сохраняется в пределах нормы. Жизненно опасные симптомы возникают при выраженном нарушении водного баланса.
- Гипоосмолярная форма. Выведение солей протекает быстрее, чем потеря жидкой фракции. Характеризуется быстрым нарушением сознания и возникновением других неврологических симптомов за счет набухания нейронов ЦНС. Даже при сравнительно малом дефиците воды отмечается тяжелая недостаточность кровообращения.
- Изоосмолярная форма. Вода и минералы теряются пропорционально друг другу. Происходит уменьшение внеклеточного пространства. Сосудистая реакция сохраняется на достаточно высоком уровне. Характерные симптомы — снижение диуреза и ЦВД на фоне сохранного или незначительно сниженного артериального давления.
Симптомы обезвоживания организма
При недостатке 40 мл жидкости на килограмм массы тела у пациента отмечаются следующие симптомы: жажда, незначительное психическое беспокойство. Тургор кожи сохранен, слизистые оболочки влажные, пульс в норме или несколько повышен. Время присутствия бледного пятна при нажатии на дистальные отделы конечностей – не более 2 секунд.
Дегидратация проявляется снижением диуреза до 1-0,5 мл/кг/ч. Слизистые оболочки становятся сухими, липкими, глаза западают. Выявляется тахикардия, напряжение и наполнение пульса уменьшается. Психоэмоциональные нарушения становятся более выраженными. Человек беспокоен или заторможен. Уровень артериального давления колеблется в пределах +/- 20 % от привычных показателей.
Тяжелое обезвоживание организма сопровождается психической заторможенностью. Уровень сознания – сопор. Внешние симптомы прогрессируют. Глаза становятся более запавшими, кожа приобретает синеватый оттенок. Накожная температура падает. Белое пятно сохраняется дольше 3 секунд, АД существенно ниже нормы. Пульс учащен за счет активации компенсаторных механизмов. Дыхание глубокое, затрудненное.
Осложнения
Обезвоживание организма легкой степени не приводит к развитию осложнений. Среднетяжелые процессы повышают вероятность образования тромбов с последующей обструкцией кровеносных сосудов сердца, легких, головного мозга. Симптомы тяжелого эксикоза — показание для дальнейшего наблюдения пациента неврологом. Существует риск формирования парезов, хронических головных болей, снижения когнитивных способностей.
Диагностика
Обезвоживание организма диагностируется на основании данных клинического и лабораторного обследования. Симптомы легкого эксикоза выявляет участковый терапевт или педиатр во время самостоятельного визита больного в ЛПУ. Тяжелые и среднетяжелые процессы диагностируют сотрудники скорой помощи. Для постановки диагноза используется:
- Физикальное обследование. Присутствуют характерные клинические симптомы дегидратации. Пациент сообщает о наличии многократной рвоты, диареи или других факторов, способствующих выведению воды. Аускультация и перкуссия малоинформативны. Возможно некоторое ослабление сердечных тонов, однако оно присутствует не во всех случаях.
- Измерение ЦВД. Для определения ЦВД применяют аппарат Вальдмана. В норме давление в правом предсердии и подключичной вене колеблется от 6 до 12 см водного столба. Его снижение на 2 и более сантиметра свидетельствует о гиповолемии.
- Лабораторные анализы. Наибольшее диагностическое значение имеет уровень гематокрита, который не должен превышать 36-45% (зависит от возраста). Рост Ht свидетельствует о сгущении крови вследствие потерь жидкости. Также обнаруживается снижение концентрации электролитов.
Лечение обезвоживания организма
Эксикоз любого генеза и степени тяжести лечится консервативно. Пациентам с легкой степенью патологии помощь оказывают амбулаторно, все остальные категории больных должны быть госпитализированы. Значительные расстройства гемодинамики и высшей нервной деятельности требуют помещения больного в ОРИТ. Методы лечения:
- Оральная регидратация. Показана при легкой степени обезвоживания. Рекомендуется употреблять большое количество подсоленной жидкости, аптечных регидратирующих средств.
- Инфузионная терапия. Неукротимая рвота, симптомы значительного обезвоживания — прямое показание для внутривенного вливания растворов. Объем последних зависит от степени патологии и варьирует в пределах 1-2,5 литров. Применяется р-р глюкозы, солевые субстанции.
- Симптоматическая терапия. Если пациент перенес тяжелую тканевую ишемию, могут быть назначены нейропротекторы или кардиотропные препараты. Кроме того, может потребоваться ИВЛ, введение препаратов калия, искусственное поддержание жизненно важных функций.
Лечение осуществляется до окончательной стабилизации диуреза, гемодинамики и других показателей жизнедеятельности. После восполнения ОЦК выясняется, что привело к развитию обезвоживания.
Прогноз и профилактика
Обезвоживание организма легкой степени имеет благоприятный прогноз. При своевременном начале терапии симптомы патологии полностью исчезают в течение 1-2 дней. При тяжелом эксикозе возможно наступление стойких инвалидизирующих осложнений, летального исхода. К числу профилактических мер относится употребление 1,5 литров воды ежедневно. Следует избегать пребывания в жарких помещениях и воздействия других факторов риска. При длительной диарее показан прием регидратирующих растворов.
Читайте также:


