Ротавирусная инфекция на узи
Внешний вид вирусных частиц напоминает колесо с широкой ступицей, короткими спицами и четко очерченным ободком, поэтому их стали называть ротавирусами (лат. rotа — колесо). Рисунок 1. Слизистая оболочка толстой кишки при ротавирусном гаст
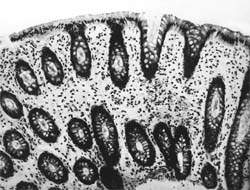 |
| Рисунок 1. Слизистая оболочка толстой кишки при ротавирусном гастроэнтерите. Минимально выраженный катаральный колит. х 100. |
Ротавирусы представляют собой род семейства Reoviridae, который объединяет большое количество сходных по морфологии и антигенной структуре вирусов, вызывающих гастроэнтерит у человека, млекопитающих и птиц. Систематическое изучение ротавирусов человека началось с 1973 года, когда они были обнаружены при электронной микроскопии ультратонких срезов биоптатов слизистой оболочки двенадцатиперстной кишки, полученных от больных острым гастроэнтеритом детей Австралии (Р. Бишоп и соавторы). В том же году Т. Флеветт обнаружил сходный вирус в копрофильтратах больных гастроэнтеритом методом электронной микроскопии при негативном контрастировании препаратов.
Вирусные частицы имеют диаметр от 65 до 75 нм. При проникновении контрастирующего вещества в вирион выявляется электронно-плотный центр диаметром 38 — 40 нм, который представляет собой так называемую сердцевину, окруженную электронно-прозрачным слоем. Внешний вид вирусных частиц напоминает колесо с широкой ступицей, короткими спицами и четко очерченным ободом, поэтому их стали называть ротавирусами (лат. rota — колесо).
Ротавирусы имеют две белковые оболочки — наружный и внутренний капсиды. Сердцевина содержит внутренние белки и генетический материал, представленный двунитчатой фрагментированной РНК. Геном ротавирусов человека и животных состоит из 11 фрагментов, которые могут быть разделены при электрофорезе в полиакриламидном геле (ПААГ) или агарозе. В составе ротавирусов обнаружено четыре антигена; основной из них — это групповой антиген, обусловленный белком внутреннего капсида. С учетом группоспецифических антигенов все ротавирусы делятся на пять групп: A, B, C, D, E. Ротавирусы одной группы имеют общий групповой антиген, который выявляется иммунологическими реакциями: иммуноферментный анализ, иммунофлюоресценция, иммунная электронная микроскопия и др. Большинство ротавирусов человека и животных относятся к группе A.
| Источником инфекции при ротавирусном гастроэнтерите является инфицированный человек — больной манифестной формой заболевания или бессимптомно выделяющий ротавирусы с фекалиями |
Источником инфекции при ротавирусном гастроэнтерите является инфицированный человек — больной манифестной формой заболевания или бессимптомно выделяющий ротавирусы с фекалиями. Вирусы в фекалиях заболевших появляются одновременно с развитием клинических симптомов, наибольшая концентрация их в кале (до 109 — 1011 вирусных частиц в 1 г) регистрируется в первые 3 — 5 дней болезни. В эти дни больные представляют наибольшую эпидемиологическую опасность для лиц, контактирующих с ними. Наиболее частым источником заболевания для детей первого года жизни являются инфицированные ротавирусом матери; для взрослых и детей более старшего возраста — дети, в основном из детских коллективов. Возможность заражения человека от животных не доказана.
Патогенез ротавирусной инфекции характеризуется проникновением вируса в эпителиоциты слизистой оболочки желудочно-кишечного тракта, преимущественно тонкой кишки, что приводит к их повреждению и отторжению от ворсинок. Вследствие этого на ворсинках тонкой кишки появляются функционально и структурно незрелые энтроциты с низкой способностью синтезировать пищеварительные ферменты. При ротавирусном гастроэнтерите это проявляется снижением уровня дисахаридаз, развивается вторичная дисахаридазная недостаточность, при которой в просвете тонкой кишки накапливаются нерасщепленные дисахариды, что создает повышенное осмотическое давление и приводит к выводу в просвет кишечника воды и электролитов из тканей организма. Это является основной причиной диареи и дегидратации и определяет основные клинические проявления болезни.
Ротавирусный гастроэнтерит как инфекционное заболевание имеет циклическое течение. Инкубационный период продолжается чаще всего от 12 — 24 часов до двух суток. Клиническая картина ротавирусного гастроэнтерита характеризуется в основном острым началом, однако в ряде случаев может иметь место продромальный период длительности от 12 до 48 — 72 часов. В этот период больные отмечают недомогание, общую слабость, повышенную утомляемость, снижение аппетита, головную боль, познабливание, урчание и неприятные ощущения в животе, умеренно выраженные катаральные явления: заложенность носа, першение в горле, легкий кашель.
В клинической картине ротавирусного гастроэнтерита в период развернутых клинических проявлений ведущими являются синдромы гастроэнтерита и интоксикации. Выраженность диареи и обусловленной ею той или иной степени дегидратации организма, а также токсикоза, продолжительность этих симптомов в значительной мере определяет тяжесть течения заболевания.
Синдром гастроэнтерита характеризуется развитием диареи, снижением аппетита, появлением урчания и болей в животе, тошноты и рвоты. Наиболее типичен для ротавирусного гастроэнтерита обильный водянистый пенистый стул желтого или желто-зеленого цвета. У больных с легким течением заболевания стул может быть кашицеобразным. Как правило, патологические примеси в стуле отсутствуют. Боль локализуется преимущественно в верхней половине живота или является диффузной, она может быть разной интенсивности. Почти всегда она сопровождается громким урчанием в животе.
Синдром интоксикации появляется в самом начале заболевания. Слабость, зачастую резкая, является наиболее частым проявлением этого синдрома; реже отмечается головная боль. При более тяжелом течении имеют место головокружение, обморочное состояние, коллапс. Обращает на себя внимание следующая особенность ротавирусного гастроэнтерита: два ведущих в клинической картине болезни синдрома развиваются в процессе заболевания не всегда однонаправленно; у некоторых больных на фоне сравнительно слабо выраженных диспепсических явлений могут наблюдаться резко выраженные симптомы общей интоксикации, особенно слабость.
Повышение температуры тела не всегда может отмечаться при ротавирусном гастроэнтерите, особенно у взрослых. У некоторых больных может быть озноб без повышения температуры. В то же время нередко в разгар заболевания выраженность лихорадочной реакции варьируется от субфебрильных цифр и выше и может достигать 38 — 39°С как у детей, так и у взрослых.
Важным в диагностическом плане для ротавирусного гастроэнтерита считается сочетание двух ведущих клинических синдромов с симптомами поражения верхних дыхательных путей. Катаральный синдром встречается приблизительно у 50% больных и проявляется в виде гиперемии и зернистости слизистых оболочек мягкого неба, небных дужек, язычка, задней стенки глотки, а также насморка, заложенности носа, кашля, болей в горле. В ряде случаев катаральные симптомы наблюдаются уже в продромальном периоде, до проявления симптомов гастроэнтерита.
В разгар болезни отмечается изменение функционального состояния сердечно-сосудистой системы, чаще у пациентов с более тяжелым течением и при наличии сопутствующих заболеваний органов кровообращения. У большинства пациентов отмечается тенденция к артериальной гипертензии, тахикардия, определяется глухость сердечных тонов при аускультации. У больных с тяжелым течением заболевания, как правило, возникают обмороки и коллапсы из-за выраженных расстройств гемоциркуляции, в генезе которых наряду с токсическими воздействиями существенное значение имеет гиповолемия. Потери жидкости и электролитов вследствие рвоты и диареи могут быть значительными и приводят к развитию дегидратации. Клинические проявления дегидратации зависят от ее степени. При легком и среднетяжелом течении ротавирусного гастроэнтерита отмечается жажда, сухость во рту, слабость, бледность (дегидратация I — II степени), при тяжелом течении наряду с этими симптомами наблюдаются также осиплость голоса, судороги мышц конечностей, акроцианоз, снижение тургора кожи, уменьшение диуреза (дегидратация III степени).
В связи с развитием при ротавирусном гастроэнтерите возможных осложнений, главным образом циркуляторных расстройств, острой сердечно-сосудистой недостаточности, нарушений гомеостаза, выделяют группы больных повышенного риска, в которые включают новорожденных, детей младшего возраста, лиц пожилого возраста, а также больных с тяжелыми сопутствующими заболеваниями. Описанные в литературе и наблюдавшиеся нами случаи ротавирусного заболевания с летальным исходом относятся именно к этим группам.
Выделяются две основные клинические формы ротавирусного заболевания — гастроэнтерическая и энтерическая. Симптомы только острого гастрита (гастритический вариант) встречаются в 3 — 10% случаев. Функциональные и морфологические нарушения со стороны желудочно-кишечного тракта, возникающие при ротавирусном гастроэнтерите в случае наличия у пациентов фоновой гастроэнтерологической патологии, нередко способствуют развитию таких осложнений основного заболевания, как обострение сопутствующих болезней: хронического гастрита, энтероколита, панкреатита, часто в сочетании с выраженными явлениями дисбактериоза кишечника, требующими коррекции при лечении.
При ротавирусном гастроэнтерите гемограмма изменяется следующим образом: в остром периоде заболевания с высокой частотой выявляются лейкоцитоз с нейтрофилезом и повышенная СОЭ. В периоде реконвалесценции картина крови обычно нормализуется полностью. Изменения урограммы у большинства больных имеют кратковременный характер и проявляются чаще всего небольшой протеин-, лейкоцит- и эритроцитурией; в редких случаях в моче появляются гиалиновые цилиндры в незначительном количестве. При тяжелом течении заболевания нарушения функции почек могут быть более выраженными, с повышением уровня мочевины крови, олигоурией или анурией, снижением клубочковой фильтрации. На фоне проводимой терапии указанные изменения быстро исчезают и при повторных обследованиях не отмечаются.
В качестве примера, иллюстрирующего особенности клинического течения ротавирусного гастроэнтерита, приводим выписку из истории болезни.
Лечение: обильное питье солевых растворов, парентеральная регидратационная и дезинтоксикационная терапия — трисоль 1000 мл внутривенное капельное введение, внутрь ферментные препараты: абомин, панкреатин, тансол, карболен. Течение заболевания без осложнений. На третий день болезни — субфебрильная температура, оставалась слабость; боли в животе прекратились. Стул кашицеобразный до пятого дня от начала заболевания. Полное выздоровление наступило на седьмой день болезни.
Дифференциальный диагноз у больных ротавирусным гастроэнтеритом проводят с другими острыми кишечными инфекциями как вирусной так и бактериальной этиологии, прежде всего в тех случаях, когда в клинической картине на первый план выступает синдром гастроэнтерита: с вирусными диареями различной этиологии (аденовирусы, коронавирусы, астровирусы, калицивирусы, вирус Норфолк, энтеровирусы Коксаки и ЕСНО); с гастроинтестинальной формой сальмонеллеза, с гастроэнтеритическим и гастроэнтероколитическим вариантами острой дизентерии, с пищевыми токсикоинфекциями, вызванными условно-патогенными бактериями; с холерой.
Обнаружение специфических антител и нарастание их титра в сыворотке крови больных и переболевших ротавирусным гастроэнтеритом при помощи серологических реакций с целью текущей диагностики на практике в настоящее время широкого распространения не получило и используется в основном для ретроспективного анализа различных эпидемиологических ситуаций.
Методы обнаружения вирусспецифической РНК, которые можно назвать высокочувствительными и специфичными, имеют, однако, ряд недостатков, ограничивающих их практическое применение (необходимость наличия специальной аппаратуры, реактивов, квалифицированного персонала и др.) Наиболее простой метод в этой группе — электрофорез ротавирусной РНК в полиакриламидном геле. Этот метод, позволяющий идентифицировать штаммы вирусов, вызвавшие заболевание, и дать характеристику штаммов, циркулирующих на данной территории, в основном применяется при эпидемиологических исследованиях.
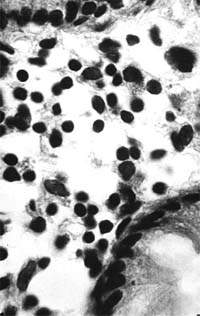 |
| Рисунок 2. Слизистая оболочка толстой кишки при ротавирусном гастроэнтерите. Минимальное содержание плазматических клеток в собственной пластинке, увеличение в ней числа макрофагов. х 400 |
В клинической практике врач нередко сталкивается с обстоятельствами (сомнительные результаты вирусологических и серологических исследований, случаи микст-инфекций), когда возникает необходимость в применении дополнительных методов для верификации диагноза. С этой целью может быть использован доступный для практического здравоохранения интрументальный метод исследования — ректороманоскопия с аспирационной биопсией слизистой оболочки толстой кишки. При гистологическом, морфометрическом и гистохимическом исследованиях биоптатов при ротавирусном гастроэнтерите выявляются характерные изменения в виде поверхностного минимально выраженного катарального колита с незначительной дистрофией эпителия (рис. 1), снижения числа серотонинсодержащих желудочно-кишечных эндокриноцитов (ЕС-клетки) в эпителиальном пласте кишечных желез, умеренной инфильтрацией собственной пластинки плазматическими клетками и увеличением в ней числа макрофагов (рис. 2). Эти особенности имеют дифференциально-диагностическое значение, поскольку отличаются указанным показателем от других острых кишечных инфекций, что может быть использовано в диагностически сложных случаях.
Здравоохранение в настоящее время не располагает препаратами, обладающими специфическим антиротавирусным действием, поэтому терапия ротавирусного гастроэнтерита является патогенетической. Основные ее цели — борьба с дегидратацией, токсикозом и связанными с ними наиболее часто встречающимися при ротавирусном гастроэнтерите нарушениями функции жизненно важных органов — сердечно-сосудистой системы и органов мочевыделения, степень выраженности которых во многом определяет тяжесть течения заболевания и его прогноз.
Для правильного выбора характера и объема проводимой регидратационной терапии в первую очередь необходимо установить степень дегидратации у того или иного пациента. При эксикозе I — II степени следует ограничиваться пероральной регидратационной терапией (препараты регидрон, глюксолан и др.). При дегидратации III степени целесообразно прибегать к комбинированной парентеральной и пероральной регидратации. Для парентеральной регидратации применяют растворы трисоль, квартасоль, ацесоль и др. С целью дезинтоксикации и улучшения гемодинамики при среднетяжелом и тяжелом течении заболевания показаны коллоидные растворы (гемодез, полиглюкин и др.).
| Для ротавирусной инфекции характерно сочетание гастроэнтерита, интоксикации и симптомов поражения верхних дыхательных путей |
Современными представлениями о патогенезе диарейного синдрома при ротавирусном гастроэнтерите обусловлено и назначение соответствующих средств, способствующих нормализации состояния пищеварительного тракта, а также диеты. Учитывая нарушения активности ряда пищеварительных ферментов, в частности лактазы, рекомендуется исключить в острый период заболевания из пищевого рациона больных молоко и молочные продукты. Кроме того, по этой же причине целесообразно ограничивать и пищу, богатую углеводами. В связи с вышеизложенным, в острый период необходимы энзимные препараты (панзинорм-форте, фестал и др). Кроме того, в остром периоде заболевания могут быть использованы адсорбирующие и вяжущие средства, способствующие ускоренному формированию стула (смекта, карболен и др.) также возможно применение хилака-форте. Высокой частотой дисбактериозов кишечника различной степени выраженности у больных ротавирусным гастроэнтеритом обусловлена необходимость применения в комплексной терапии бактерийных биологических препаратов. Лучшая терапевтическая эффективность при ротавирусном гастроэнтерите отмечена при применении лактосодержащих бактерийных биологических препаратов (ацилакт, лактобактерин и др.), что, по-видимому, связано с заместительным действием бактериальной лактазы, содержащейся в лактобактериях. В последние годы в комплексной терапии ротавирусного гастроэнтерита начал применяться комплексный иммуноглобулиновый препарат (КИП), который разработан и выпускается в МНИИЭМ им. Г. Н. Габричевского. Это первый отечественный иммуноглобулиновый препарат для энтерального применения. КИП характеризуется повышенной концентрацией антител к микроорганизмам, возбудителям острых кишечных инфекций, в том числе ротавирусам, сальмонеллам, шигеллам, эшерихиям и др. Применение КИП в комплексной терапии больных ротавирусным гастроэнтеритом оказывает отчетливый положительный терапевтический эффект, существенно сокращая продолжительность интоксикации и диареи, что открывает новые возможности в лечении этого заболевания.
Литература
1. Букринская А. Г., Грачева Н. М., Васильева В. И. Ротавирусная инфекция. М., 1989.
2. Дроздов С. Г., Покровский В. И., Шекоян Л. А., Машилов В. П. и др. Ротавирусный гастроэнтерит. М., 1982.
3. Новикова А. В. и др. Архив патологии, 1989, №6.
4. Щербаков И. Т. и др. Архив патологии, 2995, №3.
5. Юшук Н. Д., Царегородцев А. Д.. Лекции по инфекционным болезням. М., 1996.
Ротавирусная инфекция – одно из распространенных заболеваний, которому чаще всего подвергаются дети. Другое название ротавирусной инфекции – кишечный грипп. Сопровождается заболевание симптомами гастроэнтерита. Важно уметь отличать инфекцию от других заболеваний.
Причины возникновения ротавирусной инфекции

Ротавирусная инфекция – это заразное инфекционное заболевание вызванное ротавирусами
Инфекция в организм попадает от больного или здорового человека, который является носителем вируса: во время контакта или при использовании зараженных вещей и предметов.
Размножение происходит в слизистой оболочке ЖКТ, затем выделяется вместе с калом. При поражении слизистой нарушается процесс переваривания пищи, что приводит к диарее и обезвоживанию.
Передается инфекция преимущественно через пищу, немытые руки. Вредная привычка грызть ногти также может стать причиной развития ротавирусной инфекции. Болезнетворные микроорганизмы попадают на руки и активно размножаются, скапливаясь под ногтями.
Заражение чаще всего наблюдается в весенне-осенний период.
Употребление в пищу немытых овощей и фруктов также может спровоцировать развитие кишечного гриппа. В летний период из-за высокой температуры ротавирус может находиться в пассивном состоянии. Следует помнить, что ротавирусы могут находиться в водопроводной воде, поэтому ее употребление может привести к развитию инфекции.

Боль в животе, диарея, температура, рвота и общая слабость – признаки ротавирусной инфекции
Длительность инкубационного периода, т.е. с момента попадания в организм инфекции составляет 1-5 дней.
Заболевание развивается остро и проявляется следующими симптомами:
- острые, схваткообразные боли в животе
- многократная рвота
- повышение температуры тела
- недомогание
- слабость
- понос
- бледность кожных покровов
- моча темного цвета
- наличие крови в кале
Ротавирусная инфекция чаще встречается у детей с 6 месяцев до 1-2 года. Температура тела не превышает 38 градусов, понос желтого цвета, обильный с характерным неприятным запахом.
Кроме указанных симптомов можно заметить покраснение глаз и признаки воспаленного горла. Указанные симптомы следует отличать от пищевого отравления, холеры или сальмонеллеза. Через 4-7 дней признаки инфекции исчезают при правильном и своевременном лечении. Обычно после ротавируса у больного развивается иммунитет, и повторное заражение происходит редко.
Ротавирусная инфекция опасна обезвоживанием организма из-за обильного поноса.
Анализ на ротавирусную инфекцию: подготовка и сбор материала

Чаще всего для подтверждения ротавирусной инфекции необходимо сдать анализ кала
Для выявления ротавирусной инфекции сдают анализ кала. Определенной подготовки для сбора кала не требуется. Каловые массы запрещается собирать после клизмы, использования ректальных свеч и слабительных препаратов.
Важно, чтобы собранный материал не соприкасался с мочой и унитазом. При несоблюдении данного правила можно получить неточный результат.
Для исследования понадобится не менее 2-5 г кала. Собранный материал поместить в стерильную емкость. Контейнер можно приобрести в аптеке или использовать маленькую баночку. Предварительно ее нужно хорошо помыть и обдать кипятком. У грудных детей каловые массы собирают с подгузника с помощью стерильной палочки.
Каловые массы следует доставить в лабораторию утром, допускается хранение емкости в холодильнике на нижней полке на несколько часов.
Диагностировать ротавирус можно путем исследования мочи и рвотных масс. В анализах мочи отмечается протеинурия, гематурия и лейкоцитурия.
При ротавирусной инфекции во время исследования кала определяют антиген ротавирусов VP6, относящиейся к группе А. Если ротавирус в кале отсутствует, то результат будет отрицательным, а если имеется – то положительный. Для диагностики проводится иммуноферментный тест (ИФА) или полимеразная цепная реакция (ПЦР). Результат может быть ложноположительным или ложноотрицательным, тогда пациент должен сдать повторный анализ кала.
Лечение инфекции: основные методы

Только врач может назначить эффективное лечение ротавирусной инфекции
Груднички тяжелее всех переносят ротавирус, поэтому родители должны вызвать скорую помощь. До приезда бригады медиков необходимо часто поить малыша, чтобы избежать потери жидкости. При рвоте грудничка нужно положить набок, чтобы он не захлебнулся.
- Чтобы предотвратить обезвоживание организма, больному следует как можно больше пить. Регидратационная терапия включает использование Регидрона. В состав этого раствора входят: натрий хлорид, калий хлорид, глюкоза, натрий цитрат. В литре кипяченой теплой воды растворить содержимое пакетика. Ребенку следует давать по 50 мл каждые 30 минут. Взрослый человек должен пить раствор небольшими порциями на протяжении дня. Кроме Регидрона можно использовать Оралит или Глюкосолан. Важно помнить, что сильное обезвоживание организма может привести к гиповолемическому шоку.
- При температуре детям дают жаропонижающие сиропы, Парацетамол или Анальгин. Свечи от температуры ставить нет смысла, так как они вызывают позыв в туалет и не дают положительного эффекта. Следует помнить, что инфекция погибает при температуре тела 38 градусов и ее сбивать не нужно.
- Для избавления от кишечного гриппа назначают сорбенты: активированный уголь, Смектит, Энтеросгель, Сорбекс и другие. Эти препараты обладают противодиарейным и дезинтоксикационным свойствами. Сорбенты связывают и выводят из организма токсические вещества. Признаки дисбактериоза купируются и состояние больного улучшается. Если ребенок отказывается принимать лекарство, то его можно смешать с детским пюре, кашей.
- Из пробиотиков назначают Пробифор, Бифидумбактерин, Ацилакт и др. Эти средства помогают восстановить естественную флору кишечника.
Больше информации о ротавирусой инфекции можно узнать из видео:
У больного аппетит снижен и заставлять принимать пищу не следует. Можно выпить кисель, куриный бульон. Рекомендуется давать жидкую рисовую кашу, приготовленную на воде. Пищу следует принимать маленькими порциями, чтобы не спровоцировать рвотный рефлекс. Разрешается употребление овощей, не вызывающие газообразование.
Ребенку на время лечения запрещается давать молоко и молочные продукты, так как рост бактерий будет увеличиваться.
Диетотерапия предполагает употребление пищи в тушенном, вареном виде. Жареные и жирные блюда не допускаются.
Заниматься самолечением в домашних условиях категорически запрещается. Нельзя использовать противодиарейные и противорвотные препараты. Такие симптомы ротавируса как понос и рвота являются защитной реакцией организма и избавляют от скопившихся токсинов и бактерий.

Профилактические мероприятия заключаются в соблюдение санитарно-гигиенических норм:
- Употреблять следует только чистую питьевую воду. Перед употреблением необходимо всегда ее кипятить.
- Мыть руки с мылом нужно всегда после похода в туалет, перед приемом пищи и после улицы.
- При употреблении в пищу фруктов и овощей, их следует хорошо помыть и желательно ошпарить кипятком.
- Детские пустышки, баночки для кормления важно после использования кипятить.
При симптомах ротавирусной инфекции следует изолировать больного на 7-10 дней до полного выздоровления. При легком течении инфекции лечение проводится в домашних условиях под контролем врача. У больного должны быть свои столовые предметы, полотенце и другие вещи. В тяжелых случаях больного госпитализируют в инфекционную больницу.
После выздоровления необходимо выстирать все вещи ребенка и провести в доме генеральную уборку. При соблюдении санитарно-гигиенических правил можно избежать появления ротавирусной инфекции.
У детей в возрасте до 7 лет с острым ротавирусным гастроэнтеритом выявляются эхографические феномены сладжа и холангиосладжа. Чем меньше возраст ребенка и выше степень токсикоза с эксикозом – тем чаще выявлялись данные специфические для отдельных штаммов ротавирусов феномены.
Ключевые слова: дети, эхография, сладж, холангиосладж.
Echographical phenomena of sladzha and holangiosladzha can be founded at children with acute rotavirus gastroenteritis at the age of 7. Child of younger age with higher level of toxic with eksikosis more often we can observe specific data for separate stamps of rotavirus phenomena.
Key words: children, echography, sladzh, holangiosladzh.
Ротавирусная инфекция остается одной из самых распространенных среди детей [4, 5, 7, 10, 12]. Особенно тяжело это заболевание с выраженным кишечным синдромом протекает у детей раннего возраста.
Доказана высокая степень контагиозности ротавирусного гастроэнтерита [9, 10, 11]. При этом дети часто заражаются в детских дошкольных учреждениях или в семьях, где есть уже больные данной патологией.
В результате внедрения ротавирусов в энтероциты тонкого кишечника возникают значительные структурные и функциональные нарушения пищеварительного тракта с развитием, особенно у детей раннего возраста, в той или иной степени выраженности диареей, с дальнейшим обезвоживанием и токсическими явлениями [8, 11].
Несмотря на то, что достаточно изучены основные диагностические критерии ротавирусной инфекции у детей [5, 7], тем не менее, на начальном этапе развития острого ротавирусного гастроэнтерита возникают известные сложности с верификацией возбудителя кишечной инфекции до получения результатов вирусологического, бактериологического исследований.
В то же время в доступной литературе [1, 2, 3, 4, 6, 12, 13, 14] практически отсутствуют сведения о возможных специфических эхографических критериях состояния пищеварительного тракта у детей, особенно раннего возраста, с ротавирусной инфекцией. Разработки подобных эхографических критериев при ротавирусной инфекции у детей позволят с большой степень достоверности устанавливать данный диагноз с учетом степени тяжести токсикоза и эксикоза. Это, безусловно, повысит эффективность и адекватность проводимой больным детям этиопатогенетической терапии.
Цель исследования – изучить особенности эхографических критериев состояния органов пищеварительного тракта у детей раннего возраста с ротавирусной инфекцией в зависимости от степени тяжести обезвоживания, токсикоза, выраженности других клинических проявлений.
Материал и методы исследования
В дальнейшем основное внимание было уделено исследованию детей с острым ротавирусным гастроэнтеритом и больным с острым ротавирусным гастроэнтеритом, сочетанным с УПФ (условно-патогенной флорой), которые и составили основную группу данного исследования.
Кроме этого нам было повторно амбулаторно (объективно и эхографически) обследовано 70 детей, перенесших острый ротавирусный гастроэнтерит по прошествии 1, 3, 6, 12 месяцев спустя после выписки из стационара.
Все полученные результаты исследований обработаны статистически с использованием прикладных программ Microsoft Excel Windows XP. Определялись средние величины (М), средняя ошибка средней величины (m). Достоверность различий оценивалась с помощью критерия t – критерия Стьюдента. Для проверки различий между тремя и более группами применялся дисперсионный анализ. Различия сравнительных показателей считались достоверными при значении р>0,05.
Результаты и обсуждение
В ходе обследования 268 детей в возрасте от 1 до 11 лет с острыми кишечными инфекциями различной этиологии было установлено следующее распределение больных детей по нозологическим группам: основную массу обследованных больных составили дети с острым ротавирусным гастроэнтеритом (33,6 % от общего числа пациентов), с острым ротавирусным гастроэнтеритом, сочетанным с условно патогенной флорой (16 %), с острым гастроэнтеритом невыясненного генеза (18,6 %), с острым гастроэнтеритом, обусловленным сочетанной УПФ (13,4 %), с острым гастроэнтероколитом, обусловленным одним видом УПФ (6,7 %), с острым энтероколитом невыясненного генеза (6 %) и реже дети с острым Coli-инфекционным энтероколитом (3 %), с сальмонеллезом (2,2 %).
У всех обследованных больных детей отмечались выраженные явления токсикоза и обезвоживания организма. Тяжелый эксикоз и токсикоз не был отмечен ни у кого из обследованных детей с различными вариантами острых кишечных инфекций.
Обезвоживание II – средней степени тяжести было отмечено у 56 % детей с острым гастроэнтероколитом, обусловленным УПФ, одинаково часто (36 %) встречалось у больных с острым ротавирусным гастроэнтеритом и острым ротавирусным гастроэнтеритом в сочетании с УПФ. Реже эксикоз II степени тяжести был зафиксирован у больных детей с острым гастроэнтероколитом, обусловленным сочетанной УПФ (17 %) или с острым гастроэнтерокилоитом невыясненной этиологии, и никогда – у детей с Coli-инфекционным энтероколитом и при сальмонеллезе. Последнее, на наш взгляд, обусловлено современным поступлением этих больных в стационар и адекватным проведением, в том числе инфузионной регидратационной терапии.
Явления токсикоза были более выражены у детей более младшего возраста по сравнению со старшими детьми и при остром ротавирусном гастроэнтерите и при его сочетании с УПФ.
На наш взгляд, это свидетельствует о большей выраженности воспалительных изменений в кишечнике, а не в верхних этажах пищеварительного тракта у детей с острым ротавирусным гастроэнтеритом в сочетании с УПФ по сравнению с детьми, болеющими острым ротавирусным гастроэнтеритом.
В результате ультразвукового исследования гепатобилиарной системы у 90 детей в возрасте ои 1 до 12 лет с острым ротавирусным гастроэнтеритом и 44 детей того же возраста с острым ротавирусным гастроэнтеритом в сочетании с УПФ нами впервые были установлены специфические эхографические изменения, характерные только для данной патологии в отличие от 70 детей из группы сравнения с другими острыми кишечными инфекциями и 65 здоровых детей в возрасте от 1 до 12 лет, не болевших заболеваниями желудочно-кишечного тракта.
Снижение эвакуаторной способности желчного пузыря эхографически (Табл.1) было выявлено более чем у половины обследованных детей с острым ротавирусным гастроэнтеритом в различные возрастные периоды (у 47,5 % детей раннего возраста, у 51 % больных в первом детстве, у 60 % детей во втором детстве) и у детей с острым ротавирусным гастроэнтеритом в сочетании с ПФ (у 50 %, 63 %, 62,3 % больных в различные возрастные периоды, соответственно). У остальных детей в различном возрасте определялась нормальная эвакуаторная способность желчного пузыря (табл.1), и только у 12,5 % больных с острым ротавирусным гастроэнтеритом и у 12 % детей с его сочетанием с УПФ этот параметр был ускоренным.
Снижение эвакуаторной способности желчного пузыря у более чем половины обследованных нами больных детей с острой ротавирусной инфекцией подтверждало факт снижения пассажа желчи у этих больных, что, вероятно, было связано со снижением сократительной способности желчного пузыря и косвенно свидетельствовало о сгущении желчи у значительной части детей с ротавирусной инфекцией. Данный эхографический признак, безусловно, не является специфическим только для ротавирусного поражения, так описан при хроническом некалькулезном холецистите у детей и при ряде других патологических состояний.
А вот впервые описанный нами эхографический симптом ротавирусного поражения печени в виде усиления контуров внутрипеченочных протоков, связанный, на наш взгляд, с токсическими, воспалительными и рефлекторными нарушениями со стороны желчных ходов, обозначенный как «холангиосладж, несомненно, является специфическим для ротавирусного поражения с токсикозом и эксикозом I-II степени тяжести. При холангиосладже внутрипеченочные протоки выглядели как резко очерченные эхопозитивные структуры на гомогенном эхонегативном фоне эхографического среза печени.
Другим специфическим эхографическим симптомом ротавирусной инфекции у детей явился синдром сгущения желчи – синдром сладжа, который впервые был установлен нами в виде эхопозитивного, акустически более или менее неоднородного образования в просвете желчного пузыря у больных ротавирусной инфекцией у детей.
При этом размеры зоны сгущения желчи в просвете желчного пузыря варьировали от 10-30 и более миллиметров до почти точечных или 5-7 мм в диаметре.
Сладжи небольших размеров в 80 % случаев определялись у детей с острым ротавирусным гастроэнтеритом или при его сочетании с УПФ при токсикозе с эксикозом I степени, в 20 % случаев – при токсикозе с эксикозом II степени тяжести, для которых были характерны большие по размерам зоны сгущения желчи в просвете желчного пузыря.
Появление синдрома сладжа у детей с острым ротавирусным гастроэнтеритом, на наш взгляд, можно объяснить выраженными нарушениями гомеостаза, желчеобразующей функции печени вследствие тяжелого инфекционного токсикоза в сочетании с обезвоживанием организма больных детей. Т.е. при выраженном обезвоживании у больных детей с ротавирусным гастроэнтеритом воды недостает не только в коже, подкожной клетчатке,крови больного ребенка, но и в желчи.
Синдром хлангиосладжа (Табл.1) наблюдался наиболее часто у детей младшего возраста и с острым ротавирусным гастроэнтеритом (в раннем возрасте – 1 95 %, в первом детстве – 1 85 %, во втором детстве – у 80% обследованных детей) и при его сочетании с УПФ (соответственно, у 72 %, 64 %, 50 % больных).
Синдрома сладжа такеж чаще встречался у детей младшего возраста с острым ротавирусным гастроэнтеритом (в 1-3 года – 1 90 %, 4-7 лет – у 80 %, в 8-12 лет – у 70 % больных) и при его сочетании с УПФ (90 %, 83 %, 62,5 % больных, соответственно).
То есть, чем младше возраст больного ротавирусным гастроэнтеритом ребенка – тем чаще наблюдались у них данные эхографические феномены.
Синдром сладжа сочетался с холангиосладжем (табл.1) в 25 % случаев у детей с острым ротавирусным гастроэнтеритом в возрасте 1-3 года, в 20 % случаев у детей в возрасте от 4 до 7 лет, и вдвое реже (10 % больных) у детей 8-12 лет.
При остром ротавирусном гастроэнтерите в сочетании с УПФ синдром сладжа был отмечен эхографически одновременно с холангиосладжем, соответственно, у 20 % детей раннего возраста и 25 % больных первого детства, но никогда не отмечалась подобная симптоматика у детей старше 8 лет.
То есть, чем меньше возраст больных детей с ротавирусной инфекцией – тем чаще у них было установлено сочетанное токсико-воспалительное поражение желчевыводящей системы печени, проявляющееся эхографически в виде симптомов сладжа и холангиосладжа.
При остром ротавирусном гастроэнтерите у детей эхографический синдром холангиосладжа встречался в 80 % случаев при эксикозе I степени тяжести и в 75 % случаев при эксикозе II степени тяжести. Синдром сладжа при эксикозе I степени у детей с острым ротавирусным гастроэнтеритом отмечен в 90 % случаев, при эксикозе II степени тяжести – в 100 % случаев. Сочетанное одновременное выявление обоих эхографических синдромов (сладж + холангиосладж) отмечено примерно у половины больных детей с острым ротавирусным гастродуоденитом с эксикозом и легкой, и средней тяжести.
У детей с острым ротавирусным гастроэнтеритом с токсикозом I степени синдром холангиосладжа выявлялся в 79 % случаев и в 75 % случаев при токсикозе II степени, что статистически недостоверно различно при сравнении с помощью критерия Стьюдента. В то же время синдром сладжа выявлялся у детей с острым ротавирусным гастроэнтеритом при токсикозе I степени в 85 % случаев, а при токскизе II степени – в 100 % случаев. Сочетанное выявление обоих эхографических критерией наблюдалось примерно у половины обследованных нами больных детей и с токсикозом I и II степени тяжести при остром ротавирусном гастроэнтерите.
Аналогичные, статистически достоверные закономерности встречаемости различных эхографических критериев поражения гепатобилиарной системы выявлены и у детей с острым ротавирусным гастроэнтеритом в сочетании с УПФ.
Необходимо подчеркнуть, что ни эхографический синдром сладжа, ни холангиосладжа нами ни разу не был выражен при ультразвуковом исследовании детей с другими (неротавирусными) кишечными инфекциями при исследовании группы сравнения. Это позволяет рассматривать данные эхографические феномены как специфические признаки поражения гепатобилиарной системы детей именно ротавирусной инфекцией.
Таким образом, специфическим эхографическим признаком отдельных штаммов ротавирусной инфекции у детей раннего возраста является холангиосладж – в виде усиления контуров внутрипеченочных протоков, который наблюдался в раннем возрасте в 95 % случаев, в первом детстве – в 85 %, во втором детстве – у 80 % больных с острым ротавирусным гастроэнтеритом и при его сочетании с УПФ (у 72 %, 64 %, 50 % больных, соответственно). Холангиосладж был отмечен у 75-80 % больных детей с токсикозо, эксикозом I-II степени.
Специфическим ультразвуковым критерием отдельных видов штаммов ротавирусной инфекции у детей раннего возраста является синдром сладжа, который встречался в возрасте 1-3 года у 90 % детей с ротавирусным гастроэнтеритом и его сочетанием с УПФ, в 4-7 лет – у 80-83 % больных, в 8-12 лет – с 62,5-70 % больных детей. Синдром сладжа установлен у 85-90 % детей с эксикозом, токсикозом I степени, у 100 % больных с токсикозом, эксикозом II степени. Синдромы сладжа и холангиосладжа никогда не выявлялись у детей с другими острыми кишечными инфекциями.
1. Артамонов Р.Г., Рыбина Л.Н., Дворяковский И.В. и др. Диагностическое значение эхографического исследования поджелудочной железы у детей с хроническими заболеваниями органов пищеварения // Вопросы охраны материнства и детства. – 1989. - № 12, - С. 17-19.
2. Баранов А.А. Проблемы детской гастроэнтерологии на современном этапе // Российский Гастроэнтерологический журнал. – 1995. - № 1. – С. 7-11.
3. Бэнкс П.А. Панкреатит / Пер. с англ. – М., 1982.
4. Васильев Б.Я. Острые кишечные заболевания. Ротавирусы и ротавирусная инфекция / Б.Я. Васильев, Р.И. Васильева, Ю.В. Лобзин. – СПб., 2000. – 272 с.
5. Воротынцева Н.В. Острые кишечные инфекции у детей / Н.В. Воротынцева, Л.Н. Мазанкова. – М.: Медицина, 2001. – 480 с.
6. Ганган В.В., Кедик Л.В., Дворяковский И.В. Желудочно-кишечный тракт // Эхография внутренних органов у детей. – М.: Медицина, 1994. – С. 133-208.
7. Григорович М.С., Зайцева Г.А., Бандаренко А.Л. Клинико-иммунологические особенности формирования реконвалесцентного вирусоносительства при ротавирусной инфекции у детей // Эпидемиологи и инфекционные болезни. – 2002. - № 6. – С. 43-46.
8. Мухина Ю.Г. Современные аспекты проблемы лактазной недостаточности у детей раннего возраста / Ю.Г. Мухина, А.И. Чубарова, В.П. Гераськина // Вопросы детской диетологии. – 2003. – Т. 1, № 1. – С. 50-56.
9. NSP4 gene analisis of rotaviruses recovered from infected children with and diarrhea / C.N.Lee, Y.L.Wang, C.L.Kao et al // Journal of clinical microbiology. – 2000. – Vol. 38. – № 12. – P. 4471-4477.
10. Rotavirus infection impairs intestinal brush-border membrane Na+-solute contransport activities in yang rabbits / N.Halaihel, V.Lievin, F.Alvarado, M.Vasseur // American journal physiology – gastrointestinal and liver physiology. – 2000. – Vol. 279. – № 3. – Р. G-587-G-596.
11. Rotavirus infection reduces sucrase-isomaltase expression in human intestinal epithelial cells by perturbing proteintargeting and organization of cellular cytoskeleton / N.Jourdan, J.P.Brunet, C.Sapin et al // Journal of citology. – 1998. – Vol. 72. – № 9. – P. 7228-7236.
12. Сапожников В.Г., Федулова Т.В. ,Демина С.В. Особенности клинических проявлений ротавирусной инфекции у детей.// Вестник новых медицинских технологий(Электронный журнал).-т.8.-№1,2014. – С. 112-116.
13. Сапожников В.Г. Поражение желчевыводящих путей при острой ротавирусной инфекции у детей.// Педиатрия им.Г.Н.Сперанского,том.93 - №6,2014.– С. 54-57.
14. Сапожников В.Г. Ультразвуковое исследование при острых кишечных инфекциях у детей.// Вестник новых медицинскх технологий.-2013 –т.20.,№ 1 - Электронное издание.– С. 91-94.
Читайте также:


