Очаг хронической инфекции у ребенка
На данном этапе лечения существенную роль приобретает санация хронических очагов инфекции, чаще всего в ЛОР-органах (риносинуиты, аденоидит, хронический тонзиллит) и пищеварительном тракте (кариес зубов, инфекция желчевыводящих путей). У детей, больных бронхиальной астмой, сопутствующие очаги инфекции способствуют формированию инфекционной аллергии или повышают уровень сенсибилизации к бактериальным аллергенам.
Хронические воспалительные заболевания ЛОР-органов в значительной мере снижают барьерную функцию слизистой оболочки дыхательного тракта по отношению к экзогенным неинфекционным аллергенам, что может быть причиной поливалентной сенсибилизации.
Обострение хронической инфекции верхних дыхательных путей и других органов нередко является причиной частых обострений бронхиальной астмы. Сопутствующее риносинуитам, аденоидитам затруднение носового дыхания может усугублять обструкцию бронхов у таких детей и способствовать функциональным нарушениям других органов.
В связи с отрицательным влиянием хронических очагов инфекции на течение бронхиальной астмы весьма важно как можно раньше санировать их. Своеобразие поражений ЛОР-органов у детей, больных бронхиальной астмой, определяется во многих случаях участием аллергических реакций, которые влияют и на клинические проявления риносинуитов, аденоидитов и хронического тонзиллита, а также на терапевтические подходы при них.
При аллергических риносинуитах у детей с бронхиальной астмой показаны симпатомиметические средства местно, антигистаминные препараты внутрь, а также эндоназальный электрофорез интала, димедрола или сульфата магния [Карачевцева Т. В. и др., 1982; Мещеряков Л. П. и др., 1982]. При инфекционно-аллергических риносинуитах эффективны антибактериальная терапия и методы физиотерапевтического воздействия (СВЧ, УВЧ).
Нередкие у детей с бронхиальной астмой аденоидные разрастания, связанные с гипертрофией лимфаденоидной ткани носоглоточной миндалины, зачастую являются следствием аллергического поражения слизистой оболочки носоглотки.
Для определения разведения аллергенов, с которого предстоит начать лечение, проводят аллергометрическое титрование. С этой целью ставят внутрикожные пробы с бактериальными аллергенами в разведении 1:1 000 000, 1:100 000, 1:10 000 в дозе 0,1 мл. При возникновении положительных реакций лечение начинают с введения 0,1 мл наибольшего разведения аллергена, давшего сомнительную или отрицательную кожную реакцию. В последующем…
Это наиболее эффективный метод лечения бронхиальной астмы, позволяющий добиться длительной ремиссии и выздоровления. Принцип его заключается во введении больному постепенно возрастающих доз этиологически значимых аллергенов для достижения толерантности организма к ним. Специфическая гипосенсибилизация показана прежде всего при клинических формах бронхиальной астмы, обусловленных сенсибилизацией к аллергенам, устранить которые из окружающей обстановки заболевшего бронхиальной астмой ребенка не…
Снижение синтеза реагинов при специфической гипосенсибилизации может в свою очередь быть следствием изменений в различных звеньях клеточного иммунитета. Полагают, что снижение уровня IgE в процессе иммунотерапии происходит из-за уменьшения функциональной активности Т-лимфоцитов-хелперов и увеличения активности Т-лимфоцитов-супрессоров, приводящих к снижению активности В-лимфоцитов, продуцирующих IgE [Schopf L.E., 1978; Rivlin J. et al., 1981]. Терапевтический эффект при атопической…
Специфическая гипосенсибилизация у детей с бронхиальной астмой ведет к повышению активности неспецифической системы защиты организма — содержания пропердина, титра комплемента, фагоцитарной активности лейкоцитов [Мдинарадзе М. Д., Михеева Г. А., 1971; Михайлова 3. М., Михеева Г. А., 1974]. Снижается также чувствительность рецепторов периферических тканей к медиаторам аллергии. По данным И. С. Гущина (1980), после окончания гипосенсибилизации…
Положительные сдвиги в обмене веществ под влиянием специфической гипосенсибилизации могут рассматриваться как один из факторов, обеспечивающих толерантность организма к воздействию аллергена. Ведущим механизмом специфической гипосенсибилизации бактериальными аллергенами при инфекционно-аллергической форме бронхиальной астмы является повышение функциональной активности клеточного и гуморального иммунитета [Кузнецова Н. И., Молотилов Б. А., Балаболкин И. И., Пазюк Е. А., 1982; Oehling A….
Детей, подверженных частым острым респираторным заболеваниям (ОРЗ), принято называть часто болеющими (ЧБД).
Таким образом, ЧБД — это термин, обозначающий группу детей, характеризующуюся более высоким, чем их сверстники, уровнем заболеваемости острыми респираторными инфекциями. При этом к ЧБД относят детей, у которых частые ОРЗ возникают в силу эпидемиологических причин из-за транзиторных, корригируемых отклонений в защитных системах организма.
Надо отметить, что в детском возрасте среди всех заболеваний респираторного тракта отмечается абсолютное преобладание ОРЗ. На их долю приходится более 90% всех болезней респираторной системы у детей. Максимальная заболеваемость ОРЗ среди детей отмечается в возрасте от 6 месяцев до 6 лет и составляет от 4 до 6 заболеваний в год. Среди школьников заболеваемость снижается до 2–5 случаев в год, а среди подростков — не превышает 2–4 заболеваний на протяжении года. Это всеобщая закономерность, обусловленная особенностями локальных и общих механизмов защиты в раннем и дошкольном возрасте, и она прослеживается у детей во всех странах мира независимо от экономического уровня их развития. На рисунке приведены статистические данные МЗ РФ за 2002 год, отражающие типичную динамику уровня заболеваемости ОРЗ в детском возрасте.
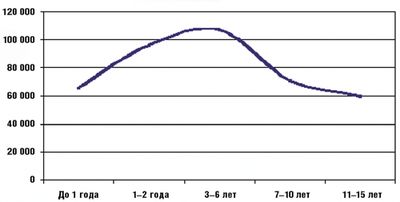
В отечественной педиатрии принято относить в группу ЧБД детей в зависимости от возраста и на основании критериев, предложенных А. А. Барановым и В. Ю. Альбицким (табл.).
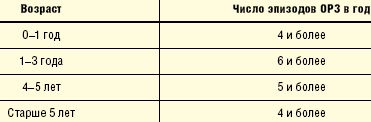
Распространенность ЧБД в детской популяции зависит, как уже упоминалось, от возраста, но также от эпидемиологических и социальных условий и составляет от 5 до 50% среди различных групп детей. Среди детей раннего возраста, посещающих детские сады, группа ЧБД может составлять около 40% и до 50%, в то время как среди школьников частые ОРЗ отмечаются менее чем у 15% детей и подростков. Отмечено, что среди ЧБД значительно чаще выявляются хронические заболевания носоглотки и легких, чаще встречается и тяжелее протекает бронхиальная астма, аллергический ринит, выше частота ревматизма, гломерулонефрита и ряда других заболеваний. Было также отмечено, что ЧБД в подростковом возрасте склонны к хроническим заболеваниям желудочно-кишечного тракта, сосудистым дистониям, у них легче развиваются невротические реакции, они быстрее утомляются, хуже учатся. Эта ситуация потенциально опасна с точки зрения формирования педагогических проблем (низкая успеваемость, отставание от учебной программы и т. д.). Кроме того, страдает психологический климат в семье. Так, установлено, что рекуррентные респираторные заболевания у детей более чем в 50% семей сопровождаются умеренным или значительным напряжением отношений между родителями и более чем в 57% — дефицитом внимания к другим членам семьи, в том числе и к другим детям. В целом показано, что более 70% родителей, дети которых часто болеют ОРЗ, констатируют ухудшение качества своей жизни.
Кроме того, частые ОРЗ требуют значительных материальных затрат, нанося серьезный экономический ущерб, связанный как непосредственно с затратами на лечение, так и с потерей трудового времени родителей.
Таким образом, ЧБД являются проблемой, имеющей не только медицинский, но и социально-экономический аспект, что требует комплексного подхода к ее решению в реализации лечебных, реабилитационных и профилактических мероприятий для ЧБД.
Существует две основных точки зрения на причины повторных и столь частых респираторных заболеваний у ЧБД. Первая — нарушение функционирования иммунной системы, проявляющееся при неблагоприятных воздействиях внешней среды. Вторая — генетическая предрасположенность, также реализующаяся под воздействием неблагоприятных условий внешней среды. Возможно, что оба эти фактора играют роль при возникновении частой заболеваемости ОРЗ у ЧБД. Но в последние годы особое внимание исследователей уделяется состоянию иммунной системы у ЧБД.
Изучение иммунной системы ЧБД выявляет особенности ее функционирования, которые в значительной степени связаны с развитием и созреванием иммунной системы ребенка. Последние исследования показали, что у ЧБД даже в период клинического благополучия и при отсутствии признаков ОРЗ выявляются отчетливые изменения в межклеточном взаимодействии в иммунной системе: достоверно повышено содержание провоспалительных интерлейкинов (IL-2, IL-4), в том числе интерлейкинов, участвующих в хронизации воспаления (IL-6, IL-8). Это сопровождается снижением клеточной цитотоксичности, дисиммуноглобулинемией и повышением уровня клеток, экспрессирующих рецепторы, индуцирующие апоптоз. При этом индуцированная продукция провоспалительных цитокинов была недостаточной, что свидетельствует об истощении резервных возможностей иммунной системы организма ребенка. Снижение количества CD11b-клеток, куда входят гранулоциты, моноциты, натуральные киллеры и макрофаги, экспрессирующие молекулы межклеточной адгезии, а также уменьшение количества эндотелиальных клеток, экспрессирующих межклеточные молекулы адгезии 1 типа и рецепторы к риновирусам, во многом объясняет повышение чувствительности детей к повторным респираторным вирусным инфекциям и склонность их к развитию бактериальных осложнений. А недостаточность резервных возможностей интерфероногенеза, особенно в плане синтеза гамма-интерферона, осуществляющего мощную противовирусную защиту в организме, несмотря на нормальный уровень интерферона в сыворотке крови, объясняет сохранение вялотекущей реакции воспаления в организме ребенка даже при отсутствии клинических признаков ОРЗ.
Таким образом, полученные в последние годы данные свидетельствуют о том, что иммунная система ЧБД хотя и не имеет грубых первичных и приобретенных дефектов, но характеризуется крайней напряженностью процессов иммунного реагирования, нарушением межклеточной кооперации и недостаточностью резервных возможностей, что, по-видимому, является результатом длительного и массивного антигенного воздействия на организм ребенка.
Функциональная активность ЛЭГС находится в тесной зависимости от возраста и морфологической зрелости ребенка. А возрастная эволюция ЛЭГС находится под генетическим контролем и зависит от морфотипа данного индивидуума. Наряду с генетически детерминированной склонностью к гиперплазии и замедленной редукции ЛЭГС на процессы ее эволюции немалое влияние оказывает воздействие внешних, фенотипических факторов. Таких факторов множество. Это — экологическое неблагополучие окружающей среды, проживание в сырых, плохо вентилируемых помещениях, большая скученность в помещениях, посещение детских коллективов, недостаточное и/или неправильное питание, неправильное лечение предшествующих респираторных заболеваний, перенесенные тяжелые заболевания, особенно инфекционные, глистная инвазия, повторяющиеся стрессовые воздействия, а также ряд других. При достаточно интенсивном воздействии фенотипических факторов они способны нарушить хрупкое равновесие между нормой и патологией, и у ребенка, имеющего генетическую предрасположенность, развивается выраженная гиперплазия ЛЭГС, нарушается лимфоэпителиальный симбиоз, создаются предпосылки для неадекватной стимуляции иммунной системы, преодоления порога ее толерантности, формирования иммунной дисфункции.
Таким образом, выявленные у ЧБД особенности клеточного и гуморального иммунитета и фагоцитоза, а также дисбаланс в цитокиновом и интерфероновом статусах свидетельствуют о напряженном функционировании иммунной системы и ЛЭГС и о возможном истощении резервов противоинфекционной резистентности у этой группы детей.
Как уже отмечалось выше, основным критерием выделения пациентов в группу ЧБД является частота заболеваемости ОРЗ. Это, однако, не исключает проведения дополнительного обследования ребенка. Прежде всего, ЧБД нуждаются в тщательном осмотре педиатром и обязательном осмотре ЛОР-врачом, включающем оценку состояния миндалин, аденоидов, придаточных полостей носа и барабанных перепонок, т. к. среди ЧБД хронические заболевания ЛОР-органов встречаются приблизительно в половине случаев.
Обязательной практикой должно быть проведение посева со слизистых зева (с миндалин) и из носа для оценки характера микробного пейзажа слизистых, т. к. микробиоценоз слизистых является одним из важнейших звеньев противоинфекционной защиты. Также может потребоваться исследование на атипичные возбудители (микоплазмоз, хламидиоз) методом ПЦР мазков со слизистой зева (определение титра антител к хламидиям и микоплазмам имеет только вспомогательное значение).
Следует учитывать, что микробиоценоз носоглотки у ЧБД нередко существенно отличается от возрастной нормы. Во-первых, как правило, инфекции респираторного тракта у этой группы детей носят смешанный вирусно-бактериальный характер, в связи с чем им многократно в течение года назначают антибактериальные препараты. Во-вторых, среди ЧБД немало детей, страдающих хроническими заболеваниями носоглотки: хроническим тонзиллитом, фарингитом, синуситом, аденоидитом и т. д., что в свою очередь влияет на микробиоценоз носо- и ротоглотки. При обследовании ЧБД можно обнаружить довольно интенсивную микробную колонизацию слизистых грибами рода Candida, стафилококками, гемофильной палочкой, в том числе гемофильной палочкой типа b, моракселлой катарралис, энтеробактериями (в том числе клебсиеллой и кишечной палочкой), микоплазмами и даже синегнойной палочкой. В носовых пазухах, лакунах небных и глоточной миндалин нередко обнаруживаются анаэробы. Выраженные нарушения микробиоценоза носоглотки снижают резистентность к патогенным возбудителям, поддерживают длительный воспалительный процесс, способствуют нарушению целостности эпителиального барьера и тем самым увеличивают антигенное воздействие и способствуют развитию хронической интоксикации.
Из методов дополнительного лабораторного и инструментального исследования целесообразно также сразу провести анализ периферической крови, общий анализ мочи и R-графию носоглотки и придаточных полостей носа в передней и боковой проекциях.
В более сложных, не поддающихся обычной терапии случаях может потребоваться консультация клинического иммунолога и/или аллерголога, а из дополнительных методов лабораторного обследования — исследование иммунограммы, в первую очередь состояния интерфероногенеза и фагоцитоза, а затем уже гуморального иммунитета, реже — клеточного иммунитета.
Медицинская помощь ЧБД складывается из трех основных направлений:
Первое направление, восстановительное или реабилитационное лечение, хотя и является наиболее трудоемким, но оно — основа успешного ведения таких детей. Включает ряд общегигиенических мероприятий, которые необходимо проводить в семье:
При клиническом обследовании у большинства детей, относимых к группе ЧБД, выявляется патологический преморбидный фон, способствующий повторным респираторным заболеваниям. Таковым является наличие хронических очагов инфекции в носоглотке - аденоидита, синусита, тонзиллита. Обострения очаговой инфекции в большинстве случаев и являются по сути дела повторными респираторными заболеваниями. Отсюда вытекает первоочередная задача реабилитации - санация очагов хронической инфекции.
При наличии аденоидита у часто болеющих детей аденоиды из соратников превращаются в очаг инфекций, увеличиваются и провоцируют повторные ОРЗ. Разрастание аденоидов имеет 3 степени: 1 степень - днем ребенок дышит свободно, а во время сна, когда объем аденоидов увеличивается в горизонтальном состоянии, дышать ему становится тяжелее; 2-3 степень - при этом разрастание аденоидов наполовину или полностью закрывает хоаны, дети часто храпят во сне, вынуждены дышать открытым ртом круглые сутки. Как известно, дыхание через рот приводит:
к хроническому тонзиллиту, фаринго-ларингиту, бронхиту, пневмонии;
к набуханию слизистой оболочки носа, нарушению наполнения воздухом и оттока слизи из околоносовых пазух, синуситу;
к нарушению слуха, т.к. закрывается глоточное устье слуховых труб: ребенок хуже слышит, у него возникают хронические заболевания среднего уха;
затруднения нормального дыхания при аденоидных разрастаниях способствует хронической гипоксии разной степени выраженности, что проявляется астенизацией, снижением иммунитета, повторными ОРЗ.
Имеются и другие рекомендации при аденоидите: 3-4 раза в день в течение нескольких недель ребенок должен дышать над паром отвара будры плющевидной (15 г травы заливают на 1-2 часа стаканом холодной воды, затем кипятят полчаса на медленном огне, постоянно помешивая; отвар следует приготавливать ежедневно). Положительным эффектом обладает закапывание в нос ежедневно в течение 2 недель 3-4 капель масла туи, курс повторяется через 2 недели. Из народных средств рекомендуется следующее - кожу измельченного зеленого грецкого ореха залить холодной водой, довести до кипения и настоять час, процедить. Закапывать в каждую половинку носа 3-4 капли 4 раза в день, курс - 3 недели.
При наличии синуситов у детей к вышеуказанным мероприятиям добавляют закапывание в нос антибактериальных средств - эктерицида, альбуцида, протаргола, диоксидина, используют турунды в нос с иодинолом на 20 минут (при гнойных выделениях иодинол меняет окраску - белеет). Осторожно должны быть назначены сосудосуживающие средства - нафтизин, санорин и их аналоги длительностью не более 7 дней. При выраженной экссудации можно использовать закапывание в нос раствора софрадекса по 2-3 капли 2-3 раза в день.
Из народных средств заслуживают внимания несколько рекомендаций:
- 1) сделать из ваты турунды, смазать их мазью прополиса и вложить в обе половинки носа на 5 мин, повторять несколько раз в день в течение 7-10 дней;
- 2) приготовить настой зеленого чая (1 чайная ложка на стакан кипятка), проце-дить, затем промывать нос маленькой спринцовкой 6-8 раз в день, а на ночь закапывать пипеткой по 3-4 капли теплого настоя в каждый носовой ход, курс - 7-10 дней.
Рекомендуются при хроническом синусите ультразвук в чередовании с СМВТ на проекции околоносовых пазух поровну (5 процедур), электрофорез лекарственных веществ эндоназально или по наружной методике (7-8 процедур), теплолечение на область околоносовых пазух (7-8 процедур).
При лечении (реабилитации) больных с хроническими процессами в околоносовых пазухах применяется комбинированный растительный препарат - Синупрет. В соответствии с терапевтическими задачами при лечении синуситов, такими как сохранение или восстановление вентиляции и оттока из параназальных пазух, Синупрет обладает выраженным секретолитическим и противовоспалительным действием. Данный фитопрепарат проявляет также антивирусное и иммуномодулирующее свойства. Способ применения: детям от 2 до 6 лет - внутрь по 15 капель 3 раза в день; детям старше 6 лет - по 25 капель или по 1 драже 3 раза в день. Курс - 7-14 дней.
При наличии хронического тонзиллита при самых его начальных проявлениях у детей возникает гематогенная и лимфогенная инфекционно-аллергическая атака на весь организм. Хронический воспалительный процесс в зоне глоточного лимфоэпителиального кольца и небных миндалинах представляет собой постоянно действующий источник гомотоксикоза, нарушающий эндоэкологию организма. Элиминация патогенного воздействия хронического очага в носоглотке является важной частью программы реабилитации часто болеющих детей.
Лечение хронического тонзиллита должно проходить в соответствии с клиническим течением заболевания (латентное течение или обострение), с формой заболевания согласно общепринятой классификации. Консервативная терапия проводится больным с простой формой (начальной стадией) хронического тонзиллита и токсико-аллергической формой 1 стадии (ТАФ 1) вне периода обострения и не ранее 1 месяца после него; больным с токсико-аллергической формой 2 стадии (ТАФ 2) показана тонзиллэктомия. На этапе реабилитации ЧБД целесообразно проведение комплексного лечения - общего и местного. Приоритетным следует считать местное воздействие на миндалины, которое можно проводить в поликлинике, на дому, в условиях санаторно-оздоровительного учреждения. У детей тактика восстановительного лечения изначально должна быть направлена на сохранение небных миндалин при полной санации носоглотки, полости рта и околоносовых пазух.
Практика реабилитации детей с хроническим тонзиллитом показала высокую эффективность сочетания промывания миндалин (см. выше) и УФО (наружно) или на миндалины (по 1-2 мин). Традиционная УВЧ- и СВЧ-терапия улучшает кровоток и лимфообращение в миндалинах, а ультразвук оказывает микромассирующий и тепловой эффект, стимулирует метаболизм и иммуно-биологическую реактивность миндалин, уменьшает их размеры. При хроническом тонзиллите очень полезным является использование гелий-неонового лазера с длиной волны 0,63 мкм в противовоспалительных дозах - по 4 мин на каждую миндалину, ежедневно, на курс 10 процедур. Доказано, что при использовании лазера имеет место биостимулирующее, анальгезирующее и противовоспалительное действие. При этом меняется обсемененность небных минадалин - патогены заменяются сапрофитной флорой, улучшается иммуно-гомеостаз в миндалинах.
В комплексной терапии детей с хроническим тонзиллитом важное место занимает фитотерапия, в частности - использование препарата Тонзилгон Н. Активные компоненты ромашки, алтея и хвоща, входящие в данный комбинированный препарат растительного происхождения, стимулируют защитные механизмы организма за счет повышения фагоцитарной активности макрофагов и гранулоцитов. Экстракты этих растений усиливают также внутриклеточное разрушение поглощенных микробов вследствие повышенного образования бактерицидных кислородных метаболитов. Полисахариды, эфирные масла и флавоноиды ромашки, алтея и одуванчика оказывают противовоспалительное действие и уменьшают отек слизистой дыхательных путей. Присутствие коры дуба, богатой танинами, реализует антивирусную активность препарата, в том числе против вируса гриппа. Алгоритм использования препарата:
грудным и детям до 5 лет - по одной капле на 1 кг веса 5-6 раз в сутки,
детям от 5 до 10 лет - 15 капель 5-6 раз в день,
детям от 10 до 16 лет - 20 капель или 1 драже 5-6 раз в день.
После исчезновения острых проявлений заболевания кратность приема Тонзилгона Н сокращается до 3 раз в сутки (при этом однократная доза препарата остается прежней). Длительность базисной терапии - 4-6 недель. Возможна и целесообразна комбинация с антибактериальными средствами.
В периоде вне обострения отношение к антибиотикотерапии хронического тонзиллита однозначно отрицательное, так как с одной стороны, антибиотики сами по себе усиливают иммуносупрессию, а с другой стороны, нарушают флору в полости рта и желудочно-кишечного тракта, и развивается порочный круг.
Критерии эффективного лечения хронического тонзиллита: исчезновение гноя и патологического содержимого в небных миндалинах, уменьшение гиперемии и инфильтрации небных дужек и небных миндалин, уменьшение увеличенных регионарных лимфоузлов. Курсы лечения проводить по возможности 3 раза в год, особенно в период межсезонья. Если у больного с простой формой хронического тонзиллита или ТАФ I возникает рецидив даже после первого курса лечения и в небных миндалинах сохраняется гной, образование казеозных масс, то больного следует ориентировать на тонзиллэктомию.
У часто болеющих детей с хронической очаговой инфекцией в носоглотке (аденоидитом, синуситом, тонзиллитом), помимо перечисленных реабилитационных мероприятий, важное значение имеет стимуляция лимфатического дренажа. Известно, что лимфатическая система - одно из звеньев гомеостаза организма, которое осуществляет не только регионарную, но и общую детоксикацию. Удаление токсических веществ возможно как через кровь, так и через лимфатическую систему, которая в этом процессе наиболее активна. Использование средств, усиливающих гуморальный транспорт в звеньях кровь-интерстиций-лимфа, способствует достижению детоксикационного эффекта.
Из многочисленного арсенала средств, стимулирующих лимфатический дренаж, на этапе реабилитации часто болеющих детей, особенно с проявлениями лимфатизма и наличием очаговой инфекции в носоглотке, рекомендуется использовать следующие доступные средства:
- 1. Овес обыкновенный (семена, овсяные хлопья), обладает энтеро-сорбционным и обволакивающим действием. Для усиления эффекта целесооб-разно сочетание лекарственных форм из овса с применением настоя из листьев черной смородины. Приготовление: на 1 л кипящей воды 2 стакана овса, настаивают 20-30 мин, процеживают, принимают по 100 мл 2-3 раза в день в подогретом виде. Возможен ряд других рецептов.
- 2. Смородина черная (листья, лучше молодые). Настой из листьев черной смородины способствует промыванию межклеточного пространства, вымыванию из него токсинов, повышению барьерной функции лимфатических узлов. Усиление эффекта обеспечивается сочетанием приема настоя из листьев черной смородины с приемом отвара из кукурузных рылец или настоя из овса.
- 3. Плоды шиповника. Препараты из плодов шиповника обладают способностью ускорять потоки жидкости из кровеносных сосудов во внеклеточное пространство и из него в лимфатические капилляры в различных органах и тканях. Особый интерес вызывает способность шиповника и компонентов его повышать барьерную функцию лимфатических узлов.
- 4. Подорожник большой. Настой из листьев подорожника способствует улучшению транспорта жидкости в стенках кишечника и желудка, направляя поток жидкости в лимфатическое русло и улучшая обмен веществ и тканевое дыхание в стенке кишечника, стимулируя МАЛТ-систему.
- 5. Ноготки лекарственные. Обладают выраженной способностью усиливать лимфатический дренаж тканей и органов, оказывая общее очистительное действие на уровне внеклеточного пространства; способствуют освобождению тканей от токсинов вне зависимости от причины их образования.
- 6. Кукурузные рыльца. Способствуют очищению крови, элиминируя токсические вещества через почки и кишечник и очищая внеклеточный сектор организма. Эффект повышается при сочетании с настоем молодых листьев черной смородины.
Среди гомеопатических и антигомотоксических средств заслуживают внимания ангинхель, траумель, лимфомиозот, мукоза-композитум, эуфорбиум, тонзиллотрен, умколор, тонзилло-композитум эхинацея композитум.
Ю.А. Копанев, детский гастроэнтеролог-инфекционист, ФГУН Московский НИИ эпидемиологии и микробиологии им. Г.Н. Габричевского Роспотребнадзора, канд. мед. наук
Современные методы диагностики, в частности определение антител в крови методом ИФА и определение ДНК возбудителя методом ПЦР, продемонстрировали, что инфицированность людей оппортунистическими инфекциями достигает 90–99%.
Что такое оппортунистические инфекции
Так обозначаются распространенные хронические инфекционные заболевания, вызываемые условно патогенными микроорганизмами разных типов (вирусы, бактерии, простейшие, внутриклеточные микробы), поражающими преимущественно слизистые оболочки и лимфатическую систему, передающимися разными путями и имеющими ряд закономерностей.
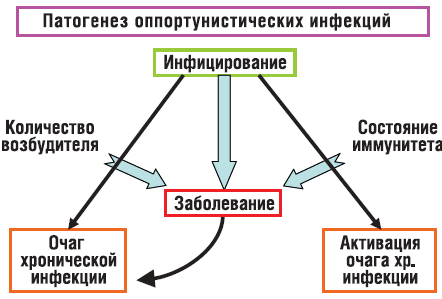
Формирование очагов хронических (оппортунистических) инфекций происходит так, как изображено на рисунке 2. Инфицирование становится заболеванием, если нарушается баланс между количеством возбудителя, попавшего в организм, и состоянием иммунной системы. При ослабленном иммунитете даже небольшое количество микроба может создать проблемы, а большое количество микроорганизмов вызовет заболевание и при неослабленном иммунитете. Некоторые микроорганизмы могут вызвать острое заболевание, а потом перейти в хроническую форму; например, это характерно для вируса Эпштейн Барр – возбудителя инфекционного мононуклеоза. Другие возбудители могут формировать хроническое заболевание без стадии острой болезни, например лямблии (острая форма лямблиоза встречается очень редко). Активизация хронической инфекции может произойти на фоне инфицирования любым другим микробом, тогда к клиническим проявлениям, характерным для этого микроорганизма, присоединяются клинические проявления, характерные для хронического очага. Например, ребенок заболевает ОРВИ, через несколько дней присоединяются симптомы кишечных нарушений. Это может быть активизацией очага хронической инфекции в ЖКТ, спровоцированной ОРВИ.
Эпидемиология
Для оппортунистических инфекций характерны всевозможные пути заражения:
- воздушно капельный (хламидии, легочные микоплазмы); передаваться могут как активные, так и неактивные формы, если человек является не только носителем, но и выделителем микроба в окружающую среду (большинство людей являются носителями, примерно 15% – выделители);
- фекально оральный (хламидии – Ch. psittaci, лямблии); хламидийная инфекция характерна для птиц, животных. Экскременты перемешиваются с землей, загрязняют руки и продукты, при попадании загрязненных и инфицированных элементов в кишечник там может сформироваться очаг хронической инфекции;
- половой (урогенитальный хламидиоз, оппортунистические инфекции); вертикальный (трансплацентарно, во время родов); за счет того, что хронические инфекции существуют в виде активных и неактивных форм (рис. 1), возможен такой способ передачи инфекции от матери плоду: у беременной женщины существует оппортунистическая инфекция в латентной форме, клинических проявлений нет, антитела в крови – в пределах нормы или не выявляются. Происходит вертикальная передача инфекции плоду (передаются неактивные формы), у родившегося ребенка в какой-то момент происходит активизация инфекции;
- трансмиссивный (через кровь и насе комых).
 |
Закономерности влияния на организм
Любой очаг хронической инфекции может вызвать следующие нарушения в организме:
- нарушение функции той системы, где локализуется данный очаг. Очаги хронической инфекции ЖКТ приводят к функциональным нарушениям: дисбактериозу кишечника, диспанкреатизму, дискинезии кишечника и желчевыводящих путей и т.п. Инфекции, тропные к лимфатической системе, вызывают лимфа денопатии. Инфекции дыхательных путей – различные респираторные дисфункции, хронический кашель, хронические заболевания верхних дыхательных путей. Если локализация инфекции мочеполовая система – гинекологические и урологические болезни, а также инфекции мочевыводящих путей;
- ослабление иммунной системы – это не дает возможности организму справиться с очагом хронической инфекции, приводит к появлению новых очагов, а также к частым ОРВИ у детей (часто болеющие дети) и другим проявлениям иммунной дисфункции;
- сенсибилизация с последующим формированием аллергических болезней. Очаги хронической инфекции ЖКТ могут быть одной из главных причин развития атопического дерматита и рецидивирующей крапивницы. Хронические инфекции дыхательной системы способствуют развитию бронхиальной астмы, поллиноза;
- хроническая интоксикация. Продукты жизнедеятельности микроорганизмов и пара зитов могут быть причиной неврологических нарушений, в том числе судорожного синдро ма, бруксизма (скрипение зубами), а также на рушений сна, аппетита, эмоциональной ла бильности, капризности, раздражительности, агрессивности;
- нарушения обмена веществ.
Наличие даже одного направления клинической картины должно наводить педиатра на предположение о поиске хронических (оппортунистических) инфекций.
Принципы диагностики
Выявление инфекционного фактора может идти по двум направлениям.
Трактовка результатов анализов представлена в таблице 2. В двух последних строках – ситуации, не требующие лечения.
| IgG | IgM | IgA | ПЦР | Трактовка |
| ↑ | N | N | ↑ или N | Инфекция есть (или есть иммунная память) |
| ↑ или N | ↑ | N | — | Активная фаза (недавнее первичное инфицирование) |
| ↑ или N | ↑ или N | ↑ | — | Активизация хронической инфекции |
| N | N | N | ↑ | Инфекция неактивна (или убитые микробы) |
| N | N | N | N | Инфекции нет (или нет клинически значимой) |
Повышение антител класса G выше диагностически значимых титров к какой либо хронической инфекции при первичной диагностике должно трактоваться как наличие этой инфекции и требует терапевтических действий: иммунокоррекции или активной этиотропной терапии.
Актуальные в педиатрии хронические инфекции
Бактериальные инфекции, вызванные условно патогенной флорой (УПФ)
Возбудители: гемолизирующая кишечная палочка, золотистый стафилококк, гемолизирующие стрептококки, клебсиеллы, лактозонегативные энтеробактерии и др. Живут на слизистых оболочках и в просвете ЖКТ, дыхательных, мочевыводящих путей.
Тактика педиатра: иммунокоррекция, применение фаготерапии, антисептиков. Применение антибиотиков показано в острую фазу (фебрильная температура, выраженность клинических проявлений).
Хламидийная инфекция
Возбудители: Ch. trachomatis, Ch. pneumoniae, Ch. psittaci. Вызывают внутриклеточные инфекции, поражающие слизистые оболочки и лимфатическую систему. Могут поражать все системы, где есть слизистая оболочка: конъюнктива глаза (интранатальное инфицирование); верхние дыхательные пути (ВДП), нижние дыхательные пути (воздушно капельный путь); слизистая ЖКТ (фекально оральный путь); мочеполовая система (половой путь или занос через лимфатическую систему);
Источники заражения:
- Человек, как здоровые носители, так и те, у кого активная форма болезни, при условии локализации на слизистых, сообщающихся с окружающей средой. Считается, что носителями хламидий являются более 90% людей.
- Птицы (попугаи, голуби, воробьи и др.). Хламидии выделяются с птичьим пометом, помет попадает в почву и на продукты питания, заражение человека происходит фекально оральным или воздушно-капельным путем.
- Кошки, мелкий рогатый скот (козы).
Инфицирование – еще не заболевание. Клинические признаки появляются при ослаблении иммунитета.
Клиническая картина зависит от локализации и активности хламидий:
- конъюнктивит (бывает у новорожденных детей при интранатальном инфицировании);
- хронические рецидивирующие заболевания ВДП (тонзиллит, фарингит), а также острые заболевания (ангина);
- рецидивирующие бронхиты или пневмонии, бронхообструкция, астма;
- хроническая дисфункция ЖКТ, дисбактериоз, не поддающийся лечению;
- атопический дерматит (хламидии, будучи внутриклеточной инфекцией, могут приводить к повреждению гистаминобразующих тучных клеток слизистых оболочек) с торпидным течением без эффекта от лечения;
- острые и рецидивирующие заболевания мочевыводящих путей, вульвиты и другие поражения половой системы.
- у детей диагноз подтверждается методом ИФА по выявлению антител;
- метод ПЦР и другие исследования, направленные на выявление возбудителя, практически не имеют смысла, поскольку локализация инфекции происходит чаще всего в труднодоступных для исследования местах (например, глубоко в бронхах или в слизистой оболочке кишечника);
- мазок из зева на выявление хламидий (методом ПЦР) нужен только для выявления степени эпидемиологической опасности, но не может быть основанием для назначения лечения;
- направление на анализы крови для выявления антител к хламидиям – по клинической картине и при наличии эпидемиологических указаний (при выявлении хламидийной инфекции в близком окружении).
Врачебная тактика при хламидийной инфекции. Применение антибактериальной терапии показано только при наличии признаков активности хламидийной инфекции, иначе не будет эффекта.
Показания для антибактериальной терапии:
- любое острое состояние, требующее назначения антибиотика: ангина, пневмония, острый бронхит, гнойный отит, гнойный тонзиллит, гайморит в стадии обострения;
- ОРЗ с высокой температурой (более 38,0 °С) более 3–5 дней;
- ОРЗ с температурой выше 37,0 °С, если она держится более 7–10 дней подряд;
- бронхообструктивный синдром; приступ бронхиальной астмы (если наличие хламидийной инфекции подтверждено анализами);
- затяжной кашель более 3 недель;
- обострение дерматита (если наличие хламидийной инфекции подтверждено анализами);
- неэффективность лечения аллергических болезней.
Примерная схема лечения в острый период хламидийной инфекции:
- Свечи Виферон и/или КИПферон для укрепления иммунной системы и повышения эффективности антибиотика, 10 дней.
- Антибиотик – макролид (кларитромицин, рокситромицин, мидекамицин, джозамицин, спирамицин), курс 10 дней.
Вне периода активности применяются общеукрепляющие средства и иммунокоррекция.
Микоплазменная инфекция
Возбудители: М. pneumoniae, М. hominis. Вызывают внутриклеточные инфекции, поражающие слизистые оболочки. Излюбленная локализация: дыхательные пути (как верхние, так и нижние) и мочеполовая система (МПС).
Источники заражения: человек – как здоровые носители, так и те, у кого активная форма при условии локализации на слизистых, сообщающихся с окружающей средой. Считается, что носителями микоплазм являются более 90% людей.
Клиническая картина – заболевания дыхательных путей и МПС. До 30% бронхиальной астмы ассоциировано с наличием микоплазменной инфекции, удачное лечение которой может избавить человека от заболевания или существенно улучшить его течение.
Диагностика и лечебная тактика при микоплазменной инфекции не отличаются от таковой при хламидийной инфекции.
Вирусные хронические инфекции Возбудители: вирус Эпштейн Барр (ВЭБ), вирусы простого герпеса 1 го, 2 го, 6 го типов (ВПГ), цитомегаловирусы (ЦМВ) и др.
Для ВЭБ характерны как острое заболевание (инфекционный мононуклеоз), так и хроническое течение по типу оппортунистической инфекции. Для ВПГ 6 го типа характерны острые состояния по клинической картине, напоминающие инфекционный мононуклеоз.
Диагностика. Исследование крови на антитела (ИФА), диагностически значимым критерием является повышение уровня IgG; возможно также выявление методом ПЦР со слизистых зева.
Лечебная тактика. При выявленном носительстве ВЭБ в период протекания ОРЗ нужно проводить противовирусную терапию (Арбидол, Виферон, Изопринозин) в сочетании с иммунокоррекцией; лечебные мероприятия наиболее эффективны в период обострения.
Выводы
Читайте также:


