Обследование на атипичную инфекцию
Какие назначения необходимы при подозрении на инфекцию нижних дыхательных путей? Какие патогенные факторы играют существенную роль? Как вести больных? Респираторные заболевания являются частой причиной обращения к врачу в Великобритании,
 |
Респираторные заболевания являются частой причиной обращения к врачу в Великобритании, причем в большинстве случаев они относятся к инфекционным [1]. Трем четвертям пациентов, обращающихся с признаками острого заболевания нижних дыхательных путей, врач общей практики назначает антибиотики, хотя лишь в немногих случаях удается выделить возбудителя и антибиотики или вообще не влияют, или мало влияют на естественный ход заболевания [2,3].
Назначая антибиотики, врач руководствуется ожиданиями пациента и старается действовать согласно определенной терапевтической стратегии, хотя зачастую, выписывая рецепт, чувствует, что при этом состоянии антибиотики будут неэффективны [4,5].
Причины, по которым пациент первый раз приходит на прием к своему врачу и затем повторно обращается за консультацией, довольно сложны и часто никак не соотносятся с течением болезни. Как правило, они обусловлены обеспокоенностью своим здоровьем или давлением со стороны друзей, семьи и сотрудников.
При необходимости назначить антибиотик для лечения инфекции нижних дыхательных путей обычно выбирают амоксициллин. Пациенты, повторно обращающиеся к врачу, скорее всего, получат другой антибиотик, например эритромицин или новейшее средство из группы макролидов, хинолонов или пероральный цефалоспорин [3,6].
Проведенные нами недавно исследования показали, что повторное обращение пациентов с инфекциями нижних дыхательных путей, уже получивших назначения на первичном приеме, никак не связано с антибиотикотерапией. Только у 4% таких больных сохранялась бактериальная инфекция и ни у одного из них не было устойчивости к амоксициллину [7]. Повторно приходить на прием побуждают пациентов немедицинские факторы, такие как привычка обращаться к врачу.
- Пациент неверно представляет себе естественное течение болезни
- Пациент продолжает беспокоиться по поводу симптомов болезни
- Пациенту нравится ходить на прием к врачу
- По настоянию членов семьи, друзей, сотрудников
- У пациента появились соображения, касающиеся важности симптомов
- Инфекция хронизируется или к ней присоединяется другая инфекция
- Проявляется серьезное основное заболевание
При повторном обращении по поводу респираторного заболевания врач общей практики прежде всего должен попытаться установить причину такого обращения (табл. 1). Вполне возможно, что оно вызвано необоснованными ожиданиями пациента, и наилучшим средством здесь было бы объяснение нормальных сроков выздоровления от простуды. Или же есть какое-то основное заболевание, не распознанное на первичной консультации, например астма, недолеченное хроническое обструктивное легочное заболевание, рак или бронхоэктазы.
В том случае если врач считает, что причина в продолжающейся инфекции, необходимо определить возможного возбудителя и выбрать соответствующий антибиотик (табл. 2). Ниже мы обсудим некоторые сложные случаи, которые необходимо иметь в виду [8,9]. Однако нужно помнить, что наиболее распространенными возбудителями остаются Streptоcoccus pneumoniae и респираторные вирусы, а сложные случаи составляют скорее исключение, чем правило в ежедневной общей практике.
Пенициллин-резистентный Streptococcus pneumoniae. Хотя число случаев развития лекарственной устойчивости неуклонно возрастает и представляет серьезную проблему для целого ряда европейских стран, в Англии антибиотикорезистентность пока не считается причиной неудачного лечения инфекций дыхательных путей. Нужно убеждать врачей общей практики проводить пневмококковую вакцинацию населения, входящего в группу риска, а антибиотики назначать строго по показаниям и в адекватной дозе.
Амоксициллин-резистентный Haemophilus influenzae. Haemophilus influenza (Hi) является частой бактериальной причиной обострения хронических обструктивых заболеваний легких (ХОЗЛ), а также вызывает персистирующий бронхит у здоровых взрослых людей. Некоторые антибиотики, такие как эритромицин и цефалоспорины первого поколения, недостаточно эффективны в отношении Hi. Наличие b-лактамазы объясняет отсутствие реакции на амоксициллин. Такие штаммы называются амоксициллин-резистентными Hi (АRHi).
инфекция
Амоксициллин-резистентный
Haemophilus influenzaе
Распространенные атипичные
инфекции
Mycoplasma pneumoniae
Chlamydia pneumoniae
Moraxella catarrhalis
Пенициллин-резистентный
Streptococcus pneumoniaе
Другие бактериальные возбудители
Иные атипичные инфекции
Chlamydia psittaci
Coxiella burnetti, Legionella pneumophila
Заболеваемость, обусловленная АRHi, растет и составляет сегодня в Великобритании 10-25% общего числа респираторных заболеваний в зависимости от региона. В других странах, таких как Испания, Португалия и некоторые районы Франции, уровень лекарственной устойчивости гораздо выше — это нужно иметь в виду в тех случаях, когда пациент мог заразиться зарубежом.
Об этом возбудителе следует помнить, если у пациента с ХОЗЛ после лечения часто повторяющимися курсами амоксициллина сохраняются симптомы заболевания и гнойная мокрота. В данном случае целесообразным будет недельный курс хинолона или коамоксиклава. От назначения ципрофлоксацина следует воздержаться, если пациент принимает теофиллин.
Moraxella catarrhalis. Некоторым название этого микроорганизма может показаться незнакомым, поскольку раньше его относили к роду Neisseria вида Branhamella.
Это грамотрицательный диплококк, входящий в нормальную микрофлору молодых и пожилых людей. Вслед за Haemophilus influenza и Streptococcus pneumoniae он является третьей по распространенности причиной обострения ХОЗЛ и часто поражает пациентов с тяжелыми хроническими легочными заболеваниями или раком легких.
Обнаружение этого микроорганизма служит показателем тяжести процесса. Сообщалось о недавнем наблюдении 42 случаев пневмонии, вызванной M. catarrhalis, когда около половины пациентов погибло от основного заболевания в течение трех месяцев после обнаружения инфекции.
Важно и то обстоятельство, что практически все штаммы сегодня являются b-лактамазопродуцирующими и соответственно амоксициллинорезистентными. Имеется предположение, что b-лактамаза, продуцируемая M. Catarrhalis, обеспечивает устойчивость к амоксициллину в норме чувствительных респираторных возбудителей, таких как S. pneumoniae и H. influenzae. Проводимая терапия не отличается от той, которая применяется в случаях АРHi (см. выше).
Pseudomonas aeruginosa. Об этом возбудителе нужно помнить в связи с возможностью развития бронхоэктазов и кистозной болезни. Стоит один раз заразиться Pseudomonas aeruginosa, и рецидивы могут следовать один за одним. В настоящее время единственным эффективным пероральным средством является ципрофлоксацин, но к нему быстро развивается устойчивость, и пациентов приходится госпитализировать для проведения внутривенной антибиотикотерапии и физиотерапии.
Другие бактериальные возбудители. Изредка выделяют грамотрицательную кишечную палочку, или Staphylococcus aureus. Эти возбудители чаще связаны с больничными пневмониями, но иногда обнаруживаются у пациентов, недавно выписавшихся из больницы.
- Атипичные инфекции
Под атипичными обычно подразумеваются инфекции, вызываемые Mycoplasma pneumoniae, Chlamydia psittaci, Chlamydia pneumoniae, Coxiella burnetti и Legionella pneumophila. Лихорадка Q, возбудителем которой служит Coxiella burnetti, встречается редко (как правило, в сельской местности), поэтому не будет упоминаться в дальнейшем. Все атипичные инфекции трудно поддаются распознаванию на ранних стадиях; серологические исследования, проведенные как в острый период, так и в период реконвалесценции, редко дают положительный ответ и не представляют клинической ценности.
Ни один из возбудителей атипичных инфекций не поддается воздействию b-лактамных антибиотиков, что объясняет отсутствие эффекта от назначения амоксициллина.
Mycoplasma pneumoniae. Эпидемия, вызванная этим возбудителем, случается каждые три-четыре года, и в такой период может составлять значительную часть всех респираторных заболеваний.
Обычно она охватывает школьников, студентов и людей среднего возраста; маленькие дети и старики страдают редко.
В отличие от бактериальных инфекций, заболевание начинается постепенно, через 10-14 дней после заражения, проявляясь сухим кашлем или выделением скудной чистой мокроты. Общее недомогание и повышение температуры тела обычно умеренные, при исследовании грудной клетки обнаруживаются незначительные изменения. Иногда такие проявления, как сыпь, буллезный мирингит, а также выявление холодовых агглютининов помогают поставить диагноз.
Микоплазменную инфекцию следует заподозрить, если взрослый человек, до этого не жаловавшийся на здоровье, при отсутствии серьезных патологических симптомов и признаков интоксикации не поддается лечению амоксициллином. В этом случае имеет смысл попробовать назначить антибиотик из группы макролидов; альтернативный подход — тетрациклины. Кашель, как правило, медленно поддается лечению.
Хламидии. Большинствo врачей общей практики время от времени сталкиваются со случаями пситаккоза, вызванного длительным контактом с какой-нибудь любимой домашней птичкой. В последние годы установлено, что наиболее распространенным возбудителем инфекций дыхательных путей является Chlamydia pneumoniae, передающаяся от человека к человеку [10]. Эта инфекция проявляется такими же стертыми симптомами, как и микоплазменная, среди которых выделяются кашель и фарингит. Но, в противоположность микоплазменной инфекции, данное заболевание поражает и пожилых людей, часто вследствие реинфекции.
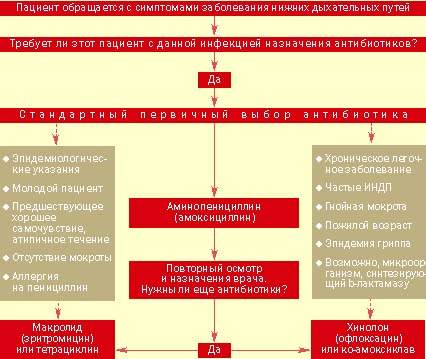 |
| Рисунок 2. Тактика ведения больного с выраженными клиническими показаниями для назначения антибиотиков при остром заболевании нижних дыхательных путей |
В некоторых исследованиях обнаружена связь между Chlamydia pneumoniaе и болезнями коронарных артерий и бронхиальной астмой, возможно обусловленная наличием хламидиального антигена, прикрепляющегося к эндотелию и эпителию. Рекомендуемое лечение — антибиотик из группы макролидов или тетрациклинов.
Legionella pneumophila. Болезнь легионеров все еще находится в центре внимания. Легионелла — редкий возбудитель пневмонии, развивающейся в местах большого скопления людей. Похоже, что легионелла не вызывает такие менее тяжелые заболевания дыхательной системы, как бронхит или инфекции верхних дыхательных путей. Состояние пациентов с болезнью легионеров достаточно тяжелое; обычно им требуется лечение в условиях стационара.
Известна связь этого заболевания с зараженными легионеллами источниками воды, поэтому упоминание пациента о заграничной поездке, пребывании в отеле или больнице, ванне джакузи помогает врачу общей практики правильно поставить диагноз. Нередко встречаются такие осложнения, как дыхательная недостаточность и энцефалит, поэтому все больные, даже в сомнительных случаях, должны быть направлены на госпитальное обследование.
- Практические советы по ведению больных с инфекциями дыхательных путей
Назначение антибиотиков. Подход к ведению больных с острыми инфекциями нижних дыхательных путей представлен на рис. 2. Ключевым моментом является принятие решения о назначении или неназначении антибиотиков. Большинство врачей общей практики считают необходимым применение антибиотиков при серьезных системных нарушениях, постоянном выделении гнойной мокроты, появлении местных признаков поражения легких и отягощенности предшествующими заболеваниями. Если уже решено использовать этот вид лечения, выбор нужного препарата не представляет особого труда.
 |
| Рисунок 3. Пациентам, входящим в группу риска, необходимо провести пневмококковую вакцинацию |
В большинстве случаев назначается амоксициллин. Согласно последним рекомендациям, доза амоксициллина принята равной 500 мг (а не 250 мг, как было раньше), чтобы снизить частоту развития резистентности пневмококков. Однако эта проблема лучше разрешается путем уменьшения общего количества назначений антибиотиков при инфекциях нижних дыхательных путей.
Врач общей практики не должен рекомендовать больному прием антибиотиков просто потому, что это самый легкий способ, или в случае, когда нет четких клинических показаний для их назначения. Проблемы резистентности возбудителей инфекций дыхательных путей решаются при назначении антибиотиков, обусловленном строгими показаниями. Снабжение пациентов простыми информационными листками значительно снижает необходимость повторных консультаций.
Литература
1. Office of Population Censuses and Surveys. Morbidity statistics from general practice: foutrh national study 1992. London: HMSO, 1995 (Series MB5;3).
2. Orr P. H., Scherer K., Macdonald A., Moffatt M. E. Randomosed placebo controlled trials of antibiotics for acute bronchitis: a critical review of the literature. J Fam Pract 1993; 36:507–512.
3. Macfarlane J. T., Holmes W. F., Macfarlane R. M., Lewis S. Contemporary use of antibiotics in 1089 adults presenting with acute lower respiratory tract illness in general practice in the UK: implications for developing managment guidelines. Respiratory Medicine, 1997; 91:427–434.
4. Holmes W. F., Macfarlane J. T., Macfarlane R. M., Lewis S. The influence of antibiotics and other factors on reconsultation for acute lower respiratory tract illness in primary care. Br J Gen Pract (in press).
5. Macfarlane J. T., Holmes W. F., Macfarlane R. M. Acutr lower respiratory tract illness in general practice; a study of the view on 787 patients and their influence on antibiotic prescribing. BMJ, 1997; 315:1211–1214.
6. Macfarlane J. T, Colville A., Guion A., Macfarlane R. M., Rose D. H. Prospective study of aetiology and outcome of adult lower respiratory tract infection in the community. Lancet, 1993; 341:511–514.
7. Macfarlane J., Prewett J., Rose D., Gard P., Guion A., Cunnigham R., Myint S. A prospective, case control study of the aetiology of community acquired lower respiratory tract infections in adult who felt to improve with initial antibiotics. BMJ, 1997; 315:1206–1210.
8. Venkatesan P., Innes J. A. Antibiotic resistance in common acute respiratory pathogenes. Thorax, 1995; 50:481–483.
9. Anon. Lower respiratory tract infections. MeReC Bulletin 1994; 5:5–8.
10. Torres A., ElEbiary M. Relevance of Chlamydia pneumoniae in community acquired respiratory infections. Eur Respir J, 1993; 6:7–8.
11. Macfarlane J. T., Holmes W. F., Macfarlane R. Reducing reconsultations for acute lower respiratory tract illness with an information leaflet. Br J Gen Pract, 1997; 47:710–722.
Далеко не всякая инфекция проявляет себя — многие бактерии и вирусы могут годами жить в нашем организме, не вызывая никаких подозрений. Однако последствия скрытых инфекций бывают очень серьезными. В этой статье мы расскажем о том, как найти и определить возбудителя заболевания и какими бывают анализы на скрытые инфекции.
В основном к скрытым инфекциям относятся заболевания, передающиеся половым путем. Это болезни с продолжительным инкубационным периодом. Они могут никак не проявляться на протяжении нескольких месяцев и даже лет. Таких инфекций более 30. К самым распространенным относятся сифилис, герпес, гонорея, а также менее опасные уреаплазмоз, вирус папилломы человека и хламидиоз. Однако и они могут создать значительные проблемы, особенно при планировании беременности.
Протекая бессимптомно, скрытые инфекции вызывают воспаление и легко переходят в хроническую форму. Последствиями скрытых инфекций, передающихся половым путем, могут быть частые воспалительные заболевания мочеполовой сферы, сложности с зачатием, у мужчин — проблемы с потенцией, у женщин — с менструальным циклом и вынашиванием детей.
Чаще всего скрытые инфекции обнаруживаются практически случайно — во время исследований, которые проводятся по совершенно иному поводу, например, во время выяснения причин бесплодия. Еще хуже, если скрытые инфекции у женщин диагностируются во время планового обследования после наступления беременности — многие из них оказывают негативное воздействие на плод, которое особенно выражено в первые недели беременности.
Именно поэтому сдавать анализы на скрытые инфекции нужно регулярно — если диагностировать их вскоре после заражения, лечение будет более простым и быстрым, они не успеют нанести существенного вреда здоровью. Рекомендуется сдавать анализы на скрытые инфекции через несколько недель после предполагаемого заражения (после незащищенного полового акта), а также перед планированием беременности — причем в этом случае сдать анализы нужно обоим партнерам. Врачи советуют проходить плановое обследование хотя бы раз в год. Анализы на скрытые инфекции доступны и стоят недорого, но при этом они могут помочь вам сохранить здоровье и средства.
Существует несколько методов лабораторной диагностики скрытых инфекций. Все они позволяют обнаружить возбудителя болезни на ранних стадиях, еще до появления первых симптомов заболевания. Некоторые анализы могут также показать стадию болезни, был ли человек заражен определенной инфекцией в прошлом, а также более или менее точно указать время заражения.
Микроскопический анализ. Биоматериалом обычно является мазок — клетки эпителия, которые берут из уретры или цервикального канала при помощи специальной мягкой щеточки, напоминающей щеточку от туши для ресниц. Для того чтобы результат был точным, перед забором материала нельзя пользоваться тампонами, вагинальными свечами и гелями, антибактериальным мылом, желательно также отказаться от половых контактов. Биоматериал из уретры берут до мочеиспускания. Полученный биоматериал переносят на предметное стекло и окрашивают специальными красителями (анилиновые красители, окраска по Граму, окраска по Романовскому), которые позволяют отчетливо увидеть определенных возбудителей заболеваний. Микроскопическое исследование также позволяет заметить косвенные признаки наличия воспалительной реакции — например, повышенное содержание лейкоцитов или фибрина. Такие возбудители, как трихомонады, гонококки, гарднереллы и грибки, отлично видны при микроскопическом исследовании, особенно во время острой стадии заболевания. Но вот при хроническом течении трихомониаза и гонореи точность этого метода не превышает 40%, что довольно небольшой показатель.
Бактериологический посев на микрофлору и чувствительность к антибиотикам. Для этого анализа также используется мазок. Полученный биоматериал переносят на питательную среду. В течение нескольких дней бактерии, полученные вместе с биоматериалом, размножаются в ней, а затем специалист рассматривает их в микроскоп и идентифицирует. У метода бактериологического посева есть один существенный плюс. При этом исследовании возможно не только выявить возбудителя болезни, но и экспериментальным путем выяснить, к какому типу антибиотиков он наиболее чувствителен. Это позволяет врачу сразу подобрать самые действенные препараты, которые однозначно сработают.
Иммуноферментный анализ (ИФА). Методом ИФА исследуют сыворотку крови, взятой утром натощак, или мазок из уретры или цервикального канала. Метод ИФА показывает не самих возбудителей, а антитела к ним. Антитела вырабатываются нашей иммунной системой при столкновении с инфекцией. Эти белки специфичны, то есть для каждой отдельной инфекции защитная система вырабатывает определенный, характерный только для нее белок. ИФА эффективен и точен при выявлении тех инфекций, к которым формируются антитела — уреаплазмам, микоплазмам, хламидиям, различным паразитам и вирусам. Точность метода доходит до 90% [1] .
Реакция иммунофлюоресценции (РИФ). Этим методом чаще всего исследуют мазок. Суть его заключается в окраске биоматериала специальными флуоресцентными антителами. Они соединяются с определенными возбудителями болезни, и специалист может увидеть их при помощи люминесцентного микроскопа — в особом излучении они начинают светиться. Это очень эффективный метод диагностики уреаплазмоза, микоплазмоза, хламидиоза, трихомониаза и некоторых других инфекций, которые порой непросто выявить другими способами. Точность этого метода — около 80% [2] .
Полимерная цепная реакция (ПЦР). Этим методом можно исследовать любой биоматериал, но на практике чаще всего для анализа берут мазок или кровь. Сегодня этот метод считается одним из самых современных и точных. Суть этого способа диагностики скрытых инфекций заключается в многократном копировании фрагмента ДНК или РНК возбудителя. Когда копий будет достаточно много, специалист идентифицирует их и выяснит, какой именно вирус или бактерия присутствует в организме. Преимущество метода ПЦР в том, что для диагностики достаточно наличия всего одного фрагмента РНК или ДНК. На практике это означает, что метод ПЦР позволяет проводить диагностику на самых ранних стадиях заболевания, тогда, когда остальные методы в этом случае могут дать ложноотрицательный результат [3] . Этот способ особенно точен в отношении вирусов, уреаплазм, микоплазм, гарднерелл, грибковых инфекций.
Скорость получения результатов зависит от метода исследования.
Дольше всего придется ждать результатов бактериологического посева. Это исследование никак нельзя отнести к экспресс-методам — результаты можно будет получить самое раннее через неделю, а часто приходится ждать еще дольше.
Результаты анализов, проводимых методом ИФА, РИФ или ПЦР, обычно выдают уже через сутки или через 2 дня.
Если лаборатория перегружена, результаты выдадут позже. Чаще всего это бывает с небольшими лабораториями, у которых нет достаточного количества сотрудников и оборудования. Крупные же учреждения работают быстрее.
Результаты анализов расшифровывает врач, он же выписывает направление на дополнительные исследования, если результат вызывает сомнения. Иногда результаты анализов, проведенных разными способами, не совпадают друг с другом — один дает положительный результат, а другой — отрицательный. Пусть это вас не настораживает — причина подобного положения вещей не в слабости методов, а в их специфике. Например, если ПЦР показал наличие инфекции, а ИФА — нет, это значит, что болезнь давно перешла в хроническую стадию и иммунная система уже не реагирует на нее, так как ПЦР показывает наличие возбудителя как такового, а ИФА — лишь реакцию защиты организма.
Бывает и наоборот: ПЦР — отрицательный, а ИФА — положительный. Это достаточно характерно для пациентов, которые не так давно вылечились от заболевания. Бактерий или вирусов уже нет, но антитела, выработанные организмом, еще присутствуют в биоматериале.
Сдать анализы на скрытые инфекции можно в государственных или частных лабораториях. Первый вариант — бесплатный, однако он сопряжен с некоторыми неудобствами. Нужно записаться на прием к врачу, получить направление, отстоять очередь. Часы работы муниципальных медучреждений не всегда удобны.
Именно поэтому многие предпочитают выбрать более короткий путь и обращаются в коммерческие лаборатории и частные клиники. Сдать анализы там можно и без направления от врача, по собственной инициативе, в любое удобное время, без очередей. Многие лаборатории даже предлагают комплексные обследования, в которые входят анализы на все самые распространенные скрытые инфекции, а также пакеты диагностических услуг для женщин, мужчин и тех, кто планирует стать родителями. Это очень удобно: во-первых, такие обследования дешевле, во-вторых, вам не придется думать, какие именно анализы целесообразно сдавать.
Цена анализов на скрытые инфекции может значительно различаться в разных лабораториях. На стоимость влияет и расположение лаборатории (чем она ближе к центру, тем дороже), и ее оснащение, и, наконец, уровень обслуживания.
Стоимость ПЦР на скрытые инфекции зависит от типа возбудителя. В среднем стоимость исследования составляет приблизительно 200–600 рублей за анализ на одного возбудителя и около 1500–2000 рублей за комплексное обследование.
Микроскопическое исследование стоит примерно 250–400 рублей.
ИФА — метод весьма недорогой и доступный, такой анализ обойдется в сумму около 200–600 рублей.
Бактериологическое исследование с определением чувствительности к антибиотикам стоит около 1400–2000 рублей.
Исследование методом РИФ обойдется для пациента приблизительно в 250–800 рублей.
К стоимости анализа как такового нужно прибавить и стоимость забора биоматериала — в районе 150–250 рублей за забор крови и от 200 рублей — за забор мазка.
Все современные методы диагностики скрытых инфекций информативны, но для того чтобы получить полную картину, нужно сдать несколько анализов — только тогда, сопоставив их результаты, врач сможет установить, есть ли инфекция и как именно нужно ее лечить.
Медицинский эксперт статьи

Коронавирусная инфекция - ОРВИ, которая характеризуется картиной ринита и доброкачественным течением болезни.
ТОРС (атипичная пневмония) - тяжело протекающая форма коронавирусной инфекции, характеризующаяся циклическим течением, выраженной интоксикацией, преимущественным поражением альвеолярного эпителия и развитием острой дыхательной недостаточности.
Тяжелый острый респираторный синдром (ТОРС) вызывается коронавирусом, распространяющимся, возможно, воздушно-капельным путем, имеет инкубационный период 2-10 дней. Развиваются гриппоподобные симптомы, которая иногда приводит к развитию тяжелой респираторной недостаточности. Смертность составляет около 10 %. Диагноз клинический. Для профилактики распространения пациенты изолируются.
Код по МКБ-10
Эпидемиология
Источник возбудителя ОРВИ - больной и носитель коронавирусов. Путь передачи воздушно-капельный, восприимчивость к вирусу высокая. Болеют преимущественно дети, после перенесённой болезни формируется гуморальный иммунитет, сезонность зимняя. У 80% взрослых есть антитела к коронавирусам.
Первый случай атипичной пневмонии зарегистрирован 11 февраля 2003 г. в Китае (провинция Гуандун), последний - 20 июня 2003 г. За этот период зарегистрирован 8461 случай болезни в 31 стране, умерло 804 (9.5%) больных. Источником вируса ТОРС служат больные, считают, что вирус может выделяться уже в конце инкубационного периода и возможно реконвалесцентное носительство. Основной путь передачи вируса атипичной пневмонии также воздушно-капельный, именно он выступает движущей силой эпидемического процесса. Допустима контаминация вирусом предметов в окружении больного. Возможность распространения вируса от источника инфекции определяется многими факторами: выраженностью катаральных явлений (кашля, чихания, насморка), температурой, влажностью и скоростью движения воздуха. Сочетание этих факторов и определяет конкретную эпидемиологическую ситуацию. Описаны вспышки в многоквартирных домах, где люди непосредственно не контактировали друг с другом и распространение вируса, скорее всего, происходило через вентиляционную систему. Вероятность заражения зависит от инфицирующей дозы вируса, его вирулентности и восприимчивости заразившегося. Инфицирующая доза вируса, в свою очередь, обусловлена количеством вируса, выделяемого источником инфекции, и расстоянием от него. Несмотря на высокую вирулентность, восприимчивость к вирусу атипичной пневмонии невысокая, что связано с наличием у большинства людей антител к коронавирусам. Об этом свидетельствует небольшое количество случаев заболевания, а также тот факт, что в большинстве ситуаций заражение произошло при близком контакте с больным в закрытом помещении. Болеют взрослые, случаев развития болезни у детей не зарегистрировано, что, вероятно, обусловлено более высоким уровнем иммунной защиты вследствие недавно перенесённой инфекции.

[1], [2], [3], [4], [5], [6], [7], [8], [9], [10], [11], [12], [13]
Что вызывает атипичная пневмония?
Атипичная пневмония вызывается коронавирусами. Впервые вирус был выделен в 1965 г. от больного острым ринитом, а в 1968 г. было организовано семейство Coronaviridae. В 1975 г. коронавирус был обнаружен Е. Caul и S. Clarke в испражнениях детей, страдающих гастроэнтеритом.
Коронавирусы - крупные РНК-содержащие вирусы сферической формы диаметром 80-160 нм. Поверхность вириона покрыта булавовидными отростками из гликопротеина, которые придают ему легко распознаваемый при электронной микроскопии вид, напоминающий солнечную корону во время солнечного затмения, отсюда и название этого семейства вирусов. Вирион имеет сложное строение, в центре расположена спиралевидная однонитевая молекула РНК, нуклеокапсид окружён белково-липидной оболочкой, в состав которой входят 3 структурных белка (мембранный белок, трансмембранный белок и гемагглютинин). Репликация вируса происходит в цитоплазме поражённых клеток.
Коронавирусы обладают сложной антигенной структурой, их подразделяют на антигенные группы, которые имеют разные антигенные перекресты.
- Первая группа - человеческий коронавирус 229 Е и вирусы, поражающие g свиней, собак, кошек и кроликов. S
- Вторая группа - человеческий вирус ОС-43 и вирусы мышей, крыс, свиней, крупного рогатого скота и индюков.
- Третья группа - кишечные коронавирусы человека и вирусы кур и индюков.
Возбудитель ТОРС - неизвестная ранее разновидность коронавируса.
Секвенирование вируса ТОРС показало, что он отличается по нуклеотидным последовательностям от известных ранее групп коронавирусов на 50-60%. Результаты секвенирования изолятов вируса, проведённые китайскими учёными, существенно отличаются от данных, полученных канадскими и американскими исследователями, что позволяет предположить способность вируса быстро мутировать. Коронавирусы неустойчивы в окружающей среде, мгновенно погибают при нагревании до 56°С, под воздействием дезинфицирующих средств. Имеются данные о более высокой устойчивости вируса ТОРС. Так. на пластиковой поверхности вирус может сохраняться до 2 сут. в канализационных водах до 4 сут. Однако в течение этих сроков количество вирусных частиц постоянно падает. Предполагают, что вирус атипичной пневмонии стал результатом мутаций известных ранее видов коронавируса.
Коронавирусы 229ЕИ, ОС43 известны достаточно давно как вызывающие простуду. В конце 2002 г. была зарегистрирована вспышка респираторно-вирусного заболевания, названного ТОРС. ТОРС был вызван коронавирусом, который генетически отличался от известных человеческих и животных вирусов.
Предполагается, что он является патогеном человека, который был впервые зарегистрирован в провинции Гуандон (Китай) в ноябре 2002 г. Вирус был обнаружен у пальмовых виверр, енотовидных собак, хорькового барсука. ТОРС распространен более чем в 30 странах. По данным на середину июля 2003 г., сообщено о более 8000 случаев заболевания и более 800 летальных исходах (смертность около 10 %); в период позднее 2003 г. все случаи болезни были выявлены в Китае.
Передача инфекции, вероятно, осуществляется воздушно-капельным путем и требует тесного личного контакта. Тем не менее передача может осуществляться случайно, аэрозольным путем. Поражаются люди от 15 до 70 лет.
Правительство королевства Саудовской Аравии, так же как и эксперты ВОЗ, обеспокоены вспышкой нового, пока неизученного заболевания, которое провоцируется коронавирусом нКоВ или nCoV. Первый случай неизвестной болезни был зафиксирован в 2012-м году, но, начиная с мая месяца текущего года, в течение первой недели в стране госпитализировано уже 13 пациентов, семь человек к настоящему моменту скончались. Согласно обновленным сведениям сайта Всемирной организации здравоохранения, вирус может передаваться от человека к человеку, то есть контактным путем.
Коронавирус нКоВ (nCoV) - это штамм, который ранее не встречался у человека, он генетически отличается от вируса, вызывающего SARS – атипичную пневмонию. Новый штамм вируса неизбирателен в смысле возрастных границ, самому младшему больному было 24 года, старшему – 94 года, в основном инфицируются мужчины. Буквально месяц назад специалисты ВОЗ считали, что главное отличие коронавируса от SARS – это низкая трансмиссивность и быстрое развитие почечной недостаточности. Однако, в мае французские медики сообщили о случае заражения человека после пребывания в одной палате с больным коронавирусной инфекцией, эту же информацию подтвердили и эксперты Великобритании. На недавней пресс-конференции в Эль-Рияде помощник генерального директора Всемирной организации здравоохранения К. Фукуда официально заявил о возможности контактного пути передачи нового опасного коронавируса. Поскольку господин Фукуда отвечает за безопасность в области здравоохранения и эпидемического контроля, его слова были восприняты весьма серьезно.
Симптомы, которые может вызвать коронавирус нКоВ, начинаются с острых респираторных осложнений. Клиническая картина очень схожа с картиной SARS - ТОРС или ТОРИ (тяжелый острый респираторный синдром или тяжелая острая респираторная инфекция), симптоматика развивается стремительно, сопровождаясь почечной недостаточностью. Вакцина против нКоВ (nCoV) еще не разработана, поскольку сам вирус пока изучается.
Тем временем, 9 мая 2013 года министр здравоохранения Саудовской Аравии предоставил ВОЗ информацию о двух очередных, лабораторно подтвержденных заболеваниях. Оба пациента живы, один уже выписан. Состояние второго больного оценивается как стабильно тяжелое.
Анализируя тревожную текущую ситуацию, ВОЗ настоятельно рекомендует всем странам, особенно, находящимся в юго-западном секторе Азии, проводить тщательный эпидемический надзор, фиксировать и оповещать ВОЗ обо всех нетипичных случаях инфекций. По состоянию на сегодняшний день, выявленный штамм не обладает высокой трансмиссивностью, тем не менее резкая вспышка заболеваний в Саудовской Аравии в мае этого года вызывает вполне обоснованную тревогу.
Официальные статистические данные о количестве заболевших коронавирусом нКоВ (nCoV) таковы:
- С сентября 2012- го года по май 2013-го года зафиксировано 33 подтвержденных лабораторными исследованиями случая коронавирусной инфекции нКоВ (nCoV).
- Один случай заболевания в Иордании до сих пор вызывает сомнения в смысле принадлежности возбудителя к коронавирусной группе.
- С сентября 2012- го года по 9 мая 2013-го года от коронавируса нКоВ (nCoV) погибло 18 человек.
Специалисты ВОЗ продолжают координировать действия врачей тех стран, в которых диагностируется основное количество заболеваний. Кроме того эксперты разработали руководство по эпиднадзору, с помощью которого клиницисты могут дифференцировать признаки инфекции, уже распространяется руководство по инфекционному контролю и алгоритмы действий врачей. Благодаря совместным усилиям микробиологов, медиков, аналитиков и экспертов созданы современные лабораторные тесты на определение штамма вируса, все крупные больницы стран Азии и Европы снабжены реагентами и прочими материалами для проведения анализов, выявляющих новый штамм.
Патогенез
- Первичное поражение вирусом альвеолярного эпителия.
- Повышение проницаемости клеточных мембран.
- Утолщение межальвеолярных перегородок и скопление жидкости в альвеолах.
- Присоединение вторичной бактериальной инфекции.
- Развитие тяжёлой дыхательной недостаточности, которая служит основной причиной смерти в острой фазе болезни.
Симптомы атипичной пневмонии
Атипичная пневмония имеет инкубационный период, который составляет 2-5 сут., по некоторым данным, до 10-14 сут.
Основной симптом ОРВИ - профузный серозный ринит. Температура тела нормальная или субфебрильная. длительность болезни до 7 сут. у детей раннего возраста возможны пневмония и бронхит.
Атипичная пневмония имеет острое начало, первые симптомы атипичной пневмонии - озноб, головная боль, боли в мышцах, общая слабость, головокружение, повышение температуры тела до 38 °С и выше. Эта лихорадочная (фебрильная) фаза длится 3-7 сут.
Респираторные симптомы атипичной пневмонии, першение в горле не характерны. Большинство пациентов имеет легкую форму заболевания, и они выздоравливают через 1-2 недели. Удругих больных спустя 1 неделю развивается острый респираторный дистресс, который включает диспноэ, гипоксемию и реже ОРДС. Смерть наступает в результате прогрессирования дыхательной недостаточности.
Помимо указанных выше симптомов у части больных наблюдают кашель, насморк, боли в горле, при этом отмечают гиперемию слизистой оболочки нёба и задней стенки глотки. Возможна также тошнота, одно- или двукратная рвота, боли в животе, жидкий стул. Через 3-7 сут. а иногда и раньше болезнь переходит в респираторную фазу, которая характеризуется повторным повышением температуры тела, появлением упорного непродуктивного кашля, одышки, затруднённого дыхания. При осмотре выявляют бледность кожного покрова, цианоз губ и ногтевых пластинок, тахикардию, приглушение тонов сердца, тенденцию к артериальной гипотензии. При перкуссии грудной клетки определяют участки притупления перкуторного звука, выслушивают мелкопузырчатые хрипы. У 80-90% заболевших в течение недели состояние улучшается, симптомы дыхательной недостаточности регрессируют и наступает выздоровление. У 10-20% больных состояние прогрессивно ухудшается и развиваются симптомы, сходные с респираторным дистресс-синдромом.
Таким образом, атипичная пневмония - циклически протекающая вирусная инфекция, в развитии которой можно выделить три фазы.
- Лихорадочная фаза. Если течение болезни завершается на этой фазе, констатируют лёгкое течение болезни.
- Респираторная фаза. Если характерная для этой фазы дыхательной недостаточности быстро разрешается, констатируют среднетяжёлое течение болезни.
- Фаза прогрессирующей дыхательной недостаточности, которая требует проведения длительной ИВЛ, часто завершается летальным исходом. Такая динамика течения болезни свойственна тяжёлому течению ТОРС.
Читайте также:


