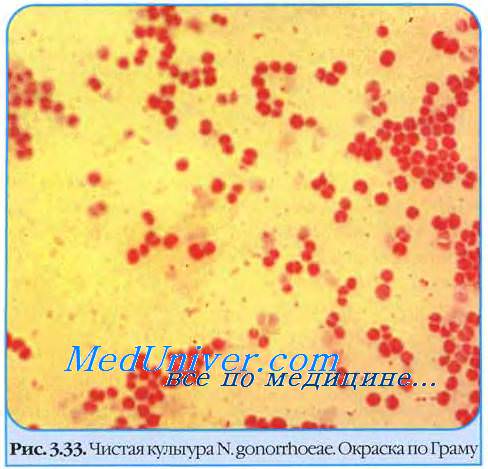
Neisseria flava что это за инфекция

 |
| Безопасные микроорганизмы | Опасные микроорганизмы |
| · бактероиды;
· стрептококк мутанс, зеленящий стрептококк; · палочка Фридлендера (клебсиелла пневмония); · непатогенные нейссерии (neisseria spp) – neisseria perflava, neisseria subflava; · грибки рода кандида; | · гемофильная, коклюшная палочка;
· стрептококки вида A; · escherichia coli (эшерихия коли) – кишечная палочка; Результат вписывают в бланк, в нём указывают род, вид, количество микроорганизмов, уровень патогенности. После определения типа возбудителя проводят тесты на определение чувствительности микробов к антибактериальным средствам, бактериофагам. Справка из лаборатории с результатами анализа Отрицательный результат свидетельствует об отсутствии грибков и болезнетворных бактерий, это означает, что инфекция имеет вирусное происхождение. Положительный результат наблюдается при наличии опасных микроорганизмов, или активном росте представителей условно-патогенной микрофлоры. По времени бактериологическое исследование занимает 5–7 дней, в экстренных случаях делается экспресс-тест для выявления антигенов к бактериям, грибкам, результат можно получить уже через полчаса. Условно-патогенные микроорганизмы, представители сапрофитической микробиоты при сильном иммунитете не вызывают патологические процессы, но при ослаблении защитных функций их число стремительно увеличивается, развиваются болезни воспалительного характера. В норме их количество не должно превышать 10*3–10*4 КОЕ/мл, но у людей с иммунодефицитными состояниями даже при таких показателях могут возникнуть тяжёлые болезни. Наличие большого количества грибков и бактерий в мазке – признак развития ЛОР-заболеваний, каждый микроорганизм провоцирует определённые патологии. Превышение нормы стафилококков наблюдается чаще всего у детей Какие болезни вызывают патогенные микроорганизмы:
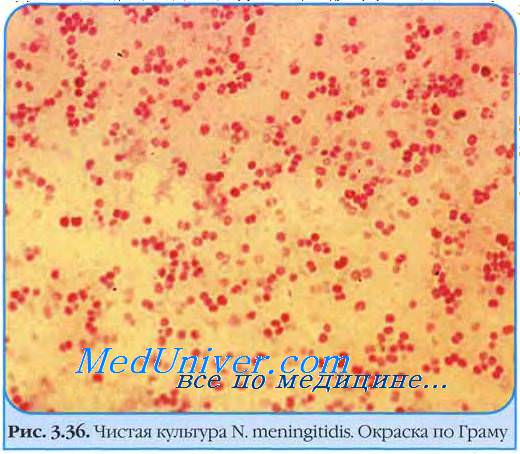
Важно!При показателях более 10*5–10*7 КОЕ/мл вероятность развития воспалительных, инфекционных, гнойных процессов максимальная. Сливной результат – очень высокое содержание патогенных микробов, их количество невозможно посчитать, наблюдается при тяжёлых и запущенных формах заболеваний, требуется срочная антибактериальная терапия. Мазок из носоглотки проводят, если есть подозрения на заболевание ЛОР-органов Мазок из носоглотки – эффективный метод диагностики заболеваний ЛОР-органов, определяет тип возбудителя патологического процесса, стадию развития болезни, позволяет подобрать эффективные методы терапии и снизить риск развития осложнений. NEISSERIA (Neisseria Trevisan 1885) — род кокковидных грамотрицательных бактерий семейства Neisseriaceae, Prevot 1933. Бактерии рода N.— аэробные или факультативноанаэробные кокки, у к-рых одна сторона вогнута, как у боба; располагаются обычно попарно, вогнутой стороной друг к другу, грамотрицательны. Нек-рые виды плохо растут на обычных питательных средах, но хорошо размножаются на сывороточных средах или средах с добавлением крови. Для N. характерна цитохромоксидазиая и каталазная активность. Род N. по классификации Берджи (Bergey’s Manual of Determinative Bacteriology, 1974) включает в себя следующие виды: N. gonorrhoeae — гонококк — возбудитель гонореи (см.), N. meningitidis — менингококк — возбудитель менингита (см.); не патогенны N. sicca, N. subfla-va, N. flavescens, N. mucosa. N. flavescens иногда патогенен для людей (большинство штаммов, по-видимому, патогенно для мышей), серо-логически связан с N. sicca. Входивший ранее в этот род N. catarrhalis отнесен в род Branhamella и название изменено на Branhamella catarrhalis. Neisseria sicca (von Lingelsheim 1908), Bergey et al. 1923 (Diplococcus pharyngis siccus, von Lingelsheim 1906, Diplococcus siccus von Lingelsheim 1903) описан в 1906 г. Лингель-схеймом (W. von Lingelsheim), выделен из слизи носоглотки. Кокки, расположенные поодиночке или парами (диплококки), мельче менингококков, иногда инкапсулированы, хорошо растут на простом агаре. Колонии неправильной округлой формы, непрозрачные, возвышающиеся над поверхностью среды, на кровяном агаре — сероватые, иногда сухие, крошатся при попытке снятия. На асцит-агаре колонии мелкие, 3 мм в диаметре, сероватые или слегка желтоватые, сухие морщинистые, с трудом снимающиеся со среды. Нек-рые штаммы образуют пигмент ксантофил. В изотоническом р-ре хлорида натрия N. sicca спонтанно агглютинируют. Разлагают левулезу, мальтозу без образования газа, Не ферментируют галактозу, лактозу, инулин, маннит, дульцит. Расщепляют сахарозу, Факультативные анаэробы. Оптимальная температура роста 36—38°. Neisseria subflava (Flugge 1886), Trevisan 1889 (Micrococcus subflavus Fliigge 1886; Neisseria fiava, Bergey et al. 1923). По внешнему виду кокков, окраске по Граму, сахаролити-ческим свойствам и по образованию зеленовато-желтого пигмента N. subflava, N. flava и N. perflava объединены в один вид. Обнаруживают на слизистой оболочке дыхательных путей; иногда в цереброспинальной жидкости при менингите (X. Ногучи, 1963). Ферментирует декстрозу и мальтозу без образования газа, не разлагает левулезу, сахарозу, лактозу, галактозу, инулин, маннит и дульцит, факультативный аэроб. Гемолиза не дает. Желатины не разжижает. Сероводород и индол не образует. Оптимум роста при t° 37°; при t° 24° растет не всегда. Часто агглютинирует в изотоническом р-ре хлорида натрия. Neisseria flavescens, Branham 1930 выделен из цереброспинальной жидкости больного эпидемическим цереброспинальным менингитом. Крупные кокки, располагающиеся парами; часты гигантские формы. На агаре с декстрозой растет плохо, хорошо растет на агаре с кровью и на полужидком агаре. Колонии мелкие суховатые, золотисто-желтые. Не разлагает декстрозу, левулезу, мальтозу и сахарозу. Факультативный аэроб. Оптимальная температура роста 37°. Neisseria mucosa Veron et al. 1959, выделен Лингельсхеймом в 1906 г. из носоглотки и цереброспинальной жидкости у больного с пневмонией и явлениями менингита. Кокки имеют капсулу или находятся в массе, окруженной липким слоем. Растет на простых средах, однако лучше на средах с добавлением сыворотки крови или асцитической жидкости; при этих условиях образуется больше слизистого слоя. Оптимум роста при t° 30—37°, отдельные штаммы растут при t° 42°; при t° ниже 22° роста нет. Желатину не разжижает, редуцирует нитрат и нитрит до газа и ферментирует глюкозу, мальтозу, фруктозу, сахарозу. На агаре колонии 1,5—4 мм в диаметре, круглые, слегка сливающиеся, сероватые, слизистые. Верон (М. Veron) с соавт. (1959) описал слегка желтый штамм. Не дает равномерной взвеси при смешивании в изотоническом р-ре хлорида натрия. Ввиду ограниченных возможностей лаб. методов, применяемых для видовой дифференциации, а также разнообразия и непостоянства свойств N., таксономическое положение ряда видов не патогенных N. остается неясным и постоянно меняется. Так, положение ряда Neisseria (N. animalis, N. canis, N. caviae, N. cinerea, N. cuniculi, N. denitrificans, N. elongata, N. ovis, N. suis) в классификационной таблице Берджи (1974) еще не определено. Нет также общепризнанных различий штаммов N. gonorrhoeae по антигенным свойствам из-за большого количества различных серологических вариантов (сероваров). В дальнейших статьях мы рассмотрим только несколько грамотрицательных инфекций. Многие грамотрицательные патогены обсуждены в главах, посвященных отдельным системам органов, включая ЖКТ и мочевыводящие пути. Анаэробные грамотрицательные организмы описаны в этой главе далее. Грамотрицательные бактерии диагностируют в основном культуральным методом. N. meningitidis — основная причина бактериального менингита, особенно среди детей младше 2 лет. Бактерии колонизируют ротоглотку и распространяются через дыхательные пути. Приблизительно 10% населения являются носителями этих бактерий. Каждый эпизод заражения длится в среднем несколько месяцев. Иммунный ответ в большинстве случаев приводит к элиминации возбудителя, при этом иммунитет также защищает при следующем заражении тем же серотипом. Известны по меньшей мере 13 серотипов N. meningitidis. Дети или молодые взрослые, проживающие совместно в больших коллективах, например в детских садах, армейских казармах или институтских общежитиях, заболевают в основном при контакте с новым штаммом, к которому у них нет иммунитета. N. meningitidis эндемична для США, но периодически эпидемии возникают в Африке южнее Сахары и приводят к тысячам смертей. Даже при отсутствии предшествующей иммунизации только у небольшого числа лиц, инфицированных N. meningitidis, развивается менингит. Бактерии должны проникнуть в респираторный эпителий и двигаться в базолатеральном направлении, чтобы попасть в кровь. В крови капсула микроорганизма препятствует опсонизации и деструкции бактерий белками системы комплемента. Несмотря на это, важность системы комплемента как фактора защиты первой линии от N. meningitidis подтверждается тем, что наиболее серьезное течение инфекции отмечается у лиц с наследственными дефектами белков системы комплемента от С5 до С9, которые образуют мембраноатакующий комплекс. Если N. meningitidis удается уклониться от иммунного ответа, последствия могут быть весьма серьезными. N. gonorrhoeae — важная причина заболеваний, передающихся половым путем. Каждый год в США происходит инфицирование около 700 тыс. человек. Эта бактерия является вторым патогеном (после С. trachomatis) в структуре заболеваний, передающихся половым путем. У мужчин инфекция N. gonorrhoeae вызывает уретрит, а у женщин инфекция часто протекает бессимптомно и остается незамеченной, в результате возможны воспалительные заболевания малого таза, приводящие к бесплодию или эктопической беременности. Инфекцию диагностируют с помощью ПЦР и культуральных методов. Инфекция N. gonorrhoeae обычно манифестирует местно в слизистой оболочке половых путей или шейки матки, глотке или аноректальной зоне, но возможна также диссеминация патогена. Так же, как N. meningitidis, N. gonorrhoeae имеет наиболее тяжелое течение у лиц с дефектом белков системы комплемента, образующих мембраноатакующий комплекс. Диссеминированная инфекция у подростков и взрослых обычно вызывает септический артрит, ассоциированный с геморрагической папулезной и пустулезной сыпью. Неонатальная инфекция N. gonorrhoeae приводит к слепоте и сепсису (реже). Глазная инфекция, которую можно предупредить инстилляцией нитрата серебра или антибиотиков в глаза новорожденных, является серьезной причиной слепоты в некоторых развивающихся странах. Патогенез. Нейссерии используют антигенную вариабельность как способ избежать иммунного ответа. Существование множества серотипов N. meningitidis обусловливает возможность развития менингита у некоторых людей даже на фоне иммунизации. Neisseria sp. обеспечивают антигенную вариабельность с помощью особого механизма, позволяющего отдельным бактериальным клонам изменять экспрессируемые ими антигены и уклоняться от иммунной защиты. Нейссерии адгезируют и проникают в эпителиальные клетки без ресничек в месте входа инфекции (носоглотка, уретра, шейка матки). Два поверхностных белка микроорганизма, каждый из которых связывается с клетками организма-хозяина, реализуют антигенную вариабельность через различные механизмы. Эти механизмы используют и N. теningitides, и N. gonorrhoeae, но они наиболее значимы для N. gonorrhoeae: - белок пилей. Белки пилей изменяются путем генной рекомбинации. Прикрепление N. gonorrhoeae к эпителиальным клеткам осуществляют длинные пили, связывающиеся с CD46, белком-регулятором системы комплемента, который экспрессируется на всех клетках организма человека, содержащих ядро. Пили состоят из полипептидов, закодированных в гене пилей, содержащем промотор и кодирующие последовательности для 10-15 вариантов белков пилей. Одномоментно только одна из этих кодирующих последовательностей может связываться с промотором и, следовательно, экспрессироваться. Периодически гомологичная рекомбинация присоединяет то одну, то другую кодирующую последовательность к промотору, что приводит к экспрессии различных вариантов пилей. Иногда присоединяется только часть другой кодирующей последовательности, создавая новые химерные варианты; - ОРА-белки. У N. gonorrhoeae есть 3 или 4 гена ОРА, у N. meningitides — более 12. ОРА-белки (от англ. opaque — мутный) локализованы в наружной мембране бактерий, улучшают связывание нейссерий с эпителиальными клетками и обеспечивают вход бактерий в клетку. Каждый ген ОРА имеет несколько повторов пяти нуклеотидных последовательностей, которые часто подвергаются делеции или дупликации. Эти изменения сдвигают рамку считывания, в результате кодируются новые последовательности. - Рекомендуем ознакомиться со следующей статьей "Патогенез и морфология коклюша" Нейссерии (Neisseria) - род грамотрицательных кокковидных бактерий. Своё название род Neisseria получил в честь немецкого дерматовенеролога и бактериолога Альберта Людвига Нейссера (1855-1916), который открыл возбудителя гонореи (1879 г.). Род Neisseria включает в себя патогенные для человека виды нейссерий: возбудителя гонореи (Neisseria gonorrhoeae) и возбудителя менингита (Neisseria meningitidis). Традиционно Neisseria gonorrhoeae часто называют гонококком, а Neisseria meningitidis - менингококком. Также у человека выделяют непатогенные виды нейссерий, обитающих на слизистых оболочках (Neisseria sicca, Neisseria mucosa, Neisseria perflava). Гонококковая инфекция (гонорея).Гонорея относится к инфекциям, передаваемым половым путем (ИППП). Гонорея вызывается Neisseria gonorrhoeae - грамотрицательной бактерией, принадлежащей к семейству Neisseriaceae, роду Neisseria. Возбудитель гонореи, как и возбудитель урогенитального хламидиоза (Chlamydia trachomatis), имеет высокую тропность к цилиндрическому эпителию, поэтому поражает цервикальный канал, эндометрий, маточные трубы, уретру. Неосложненная гонорея у мужчин протекает чаще всего в форме острого гнойного или гнойно-слизистого уретрита. Признаками гонореи у женщин является цервицит с гнойно-слизистыми выделениями. При аногенитальных и орогенитальных контактах возможно развитие проктита или фарингита. Симптомы и проявления гонококковой инфекции, за небольшим исключением, неспецифичны, для постановки диагноза необходимы лабораторные исследования для выявления возбудителя гонореи. У мужчин до 15% случаев гонококковой инфекции может протекать без клинической симптоматики, а у 5-10% не сопровождаться и лабораторными признаками уретрита. У женщин доля бессимптомных форм гонореи может достигать 45-55%. Как при манифестных, так и при малосимптомных формах гонококковой инфекции при отсутствии лечения высок риск развития осложнений. У мужчин осложнениями гонореи являются стриктуры уретры, простатит, орхоэпидидимит; у женщин - эндометрит, сальпингит, сальпингоофорит, пельвиоперитонит, тубоовариальный абсцесс, внематочная беременность, трубное бесплодие. Своевременно проведенное лабораторное исследование позволяет вовремя начать лечение и предотвратить развитие осложнений. Менингококковая инфекция (менингит).Возбудителем менингококковой инфекции (менингита) является Neisseria meningitidis (менингококк). Менингококк колонизирует заднюю стенку носоглотки человека и в зависимости от вирулентности штамма и резистентности зараженного лица вызывает инфекционный процесс с широким спектром клинических проявлений: бессимптомное носительство, назофарингит и генерализованную форму – менингококцемию и/или менингит. Менингококковая инфекция поражает лиц всех возрастов, но чаще (70%) болеют дети. Показатель летальности при менингите составляет в среднем 10%, что определяет высокую социальную значимость заболевания. Капсульные штаммы менингококка в зависимости от химического строения капсульного полисахарида делятся на ряд серологических групп: А, В, С, X, Y, Z, W-135, 29-E, H, I, K, L. Более чем 90% случаев генерализованных форм менингококковой инфекции (менингита) обусловлены штаммами серогрупп А, В и С, значительно реже – штаммами серогрупп X, Y и W-135, остальные серогруппы не представляют эпидемиологического интереса. Лабораторная диагностика генерализованной формы менингококковой инфекции (менингита) включает микроскопию биологического материала, посев биоматериала с дальнейшей культуральной и биохимической идентификацией возбудителя, определением чувствительности к антибиотикам; обнаружение специфических антител методом РПГА. Продолжая использовать наш сайт, вы даете согласие на обработку файлов cookie, пользовательских данных (сведения о местоположении; тип и версия ОС; тип и версия Браузера; тип устройства и разрешение его экрана; источник откуда пришел на сайт пользователь; с какого сайта или по какой рекламе; язык ОС и Браузера; какие страницы открывает и на какие кнопки нажимает пользователь; ip-адрес) в целях функционирования сайта, проведения ретаргетинга и проведения статистических исследований и обзоров. Если вы не хотите, чтобы ваши данные обрабатывались, покиньте сайт. Copyright ФБУН Центральный НИИ Эпидемиологии Роспотребнадзора, 1998 - 2020
! Продолжая использовать наш сайт, вы даете согласие на обработку файлов cookie, пользовательских данных (сведения о местоположении; тип и версия ОС; тип и версия Браузера; тип устройства и разрешение его экрана; источник откуда пришел на сайт пользователь; с какого сайта или по какой рекламе; язык ОС и Браузера; какие страницы открывает и на какие кнопки нажимает пользователь; ip-адрес) в целях функционирования сайта, проведения ретаргетинга и проведения статистических исследований и обзоров. Если вы не хотите, чтобы ваши данные обрабатывались, покиньте сайт. Читайте также:
 Пожалуйста, не занимайтесь самолечением!При симпотмах заболевания - обратитесь к врачу. Пожалуйста, не занимайтесь самолечением!При симпотмах заболевания - обратитесь к врачу.
|