Молекулярно биологические методы диагностики дерматомикозов
Лабораторная диагностика дерматомикозов
Грибковые заболевания кожи (дерматомикозы) представляют собой одну из важнейших проблем здравоохранения. Патогенные грибы многочисленны, и вызываемые ими заболевания человека и животных разнообразны. Известно более 500000 видов грибов, из которых лишь 50 видов являются строго патогенными (контагиозными), 20 видов являются причиной системных инфекций, 20 видов вызывают поражение кожи, 10 – кожи и подкожной клетчатки. Гораздо большее количество видов относится к условно-патогенным возбудителям, способным поражать практически все ткани и органы на фоне снижения иммунитета.
Дерматомикозы (микозы) – грибковые заболевания кожи, вызванные патогенными грибами.
Дерматомикозы – чрезвычайно разнообразны как по биологическим особенностям их возбудителей, так и по патогенезу и клиническим проявлениям. В основу классификации микозов положен способ их размножения. Все известные микозы можно подразделить на две группы:
1) Микозы, возбудители которых абсолютно, патогенны для человека (дерматофитии, гистоплазмоз) и 2) Микозы, вызванные условно-патогенными грибами (кандидоз, плесневые микозы). В зависимости от локализации очагов поражения принято говорить о поверхностных или глубоких микозах, но следует помнить, что деление это во многом условно.
Грибы – это эукариоты, утратившие хлорофилл, и поэтому не способны к фотосинтезу, являются гетеротрофами. Грибы могут быть паразитами, сапрофитами или симбионтами.
Строение тела гриба: оно состоит из массы тонких ветвящихся трубчатых нитей – гифов, а вся эта масса называется мицелием. Гифы не имеют клеточного строения. Гифы не имеют клеточного строения. Они могут быть разделены поперечными перегородками (септами), которые делят содержимое гиф на отдельные отсеки (компартменты). В каждом компартменте может находиться одно, два или несколько ядер. Гифы, не имеющие перегородок, называются несептированными. Гифы, имеющие перегородки, называются септированными.
Дрожжевые и дрожжеподобные грибы образуют псевдомицелий.
У грибов имеется жёсткая клеточная стенка, которая содержит хитин, формирующий фибриллы.
Размножаются спорами. Неподвижны.
Дерматомикозы развиваются в результате внедрения в кожу патогенных грибов. При обитании вне организма человека или животного грибы могут сохранять свою жизнедеятельность в течение нескольких лет.
Дерматомикозы – заболевания кожи, вызываемые патогенными грибами – дерматофитами.
Микроскопические грибы – это бесхлорофильные споровые растения, размером от нескольких до сотен мкм. Морфология их разнообразна. Клетка гриба имеет ядро, цитоплазму и оболочку. Вегетативное тело паразитарных грибов состоит из ветвящихся различной длины и толщины нитей мицелия с разнообразными концевыми ветвлениями, которые играют большую роль в идентификации грибов. У дерматофитов мицелий септирован поперечными перегородками на множество клеток. Нити развиваются из спор. Споры грибов служат для размножения. Размножение грибов осуществляется половым и безполым путем. Дерматофиты размножаются бесполым путем. Размножение их осуществляется делением, почкованием и спорообразованием.
Грибковые заболевания кожи делятся на 5 групп.
- Кератомикозы – эпикутанные микозы. Возбудители этих микозов поражают самые поверхностные части рогового слоя кожи или кутикулу волоса, не затрагивая его медулярного вещества, не вызывая воспалительной реакции дермы. Лабораторная диагностика этих микозов заключается в выявлении тканевых форм возбудителей с помощью микроскопии неокрашенных препаратов волос и кожных чешуек. Выделение возбудителей на питательных средах не является обязательным.
- Дерматомикозы подразделяются на эпидермофитию, трихофитию, микроспорию, фавус – наиболее распространенные и контагиозные грибковые инфекции. Возбудители эпидермофитии поражают всю толщу рогового слоя кожи, нередко ногтевые пластинки, вызывают воспалительную реакцию со стороны нижележащих слоев кожи, но иногда не поражают волосы. Возбудители трихофитии, паразитируя в роговом слое кожи. Вызывают воспалительную реакцию нижележащих её слоев, иногда нагноение. Поражают волосы, прорастая в их кутикулу и внедряясь в корковое и медулярное вещество волоса.
- Кандидомикозы кожи и слизистых оболочек наиболее часто вызываются дрожжеподобными грибами рода Candida . Чаще поражаются крупные и мелкие складки кожи, слизистые оболочки урогенитальных путей, полости рта, иногда тонкие ногти и ногтевые валики, углы рта.
- Глубокие микозы – бластомикозы, гистоплазмоз, висцеральные кандидомикозы, висцеральные плесневые микозы (пенициллиоз, аспергиллез, мукороз). Возбудители поражают кожу, подкожную клетчатку, мышцы, внутренние органы, вызывая воспалительную реакцию грануломатозного характера, могут распространяться по лимфатическим и кровеносным сосудам.
- Отдельно выделяют псевдомикозы, которые хотя и не являются грибковыми заболеваниями, но по сходству клинических проявлений с истинными микозами нуждаются во взаимной дифференциальной диагностике. К псевдомикозам относят актиномикоз и нокардиоз – хронические гранулематозные гнойно-фистулезные, а так же узловато-язвенные поражения кожи, легких, кишечника и других органов.
Существуют много различных кожных заболеваний , напоминающих по своей клинической картине грибковые поражения кожи, поэтому лабораторные исследования играют большую, нередко решающую роль в диагностике дерматомикозов. Каждый случай грибкового заболевания требует лабораторного подтверждения. Особенно велико значение лабораторных исследований при висцеральных грибковых заболеваниях, при которых клиническая картина похожа на другие заболевания внутренних органов.
Этапы лабораторной диагностики микозов:
-
Обнаружение возбудителя в патологическом материале (микроскопическое исследование нативных или окрашенных препаратов).
- Выделение возбудителя в культуре (посевы на питательные среды).
- Идентификация возбудителя.
- Изучение ответной реакции макроорганизмов по серологическим, иммунологическим реакциям, проведение кожных аллергических проб и др. Иногда проводится гистологическое исследование и экспериментальное заражение животных.
▲ План
▲ Программа
1. Биологические свойства возбудителей кандидоза, дерматомикозов и глубоких микозов; их патогенность, экология, особенности инфекции и эпидемиология вызываемых заболеваний.
2. Микробиологическая диагностика.
3. Диагностические, профилактические и лечебные препараты.
▲ Демонстрация
1.Candida spp. — мазок из чистой культуры (окраска ген-циановым фиолетовым).
2. Candida spp. — нативный препарат "раздавленная" капля из чистой культуры.
3. Candida spp. в патологическом материале от больного (окраска по методу Грама).
4. Типы филаментации грибов рода Candida на картофельном агаре.
5. 

Определение видовой принадлежности грибов рода Candida.
6. РСК и реакция агглютинации при диагностике висцерального кандидоза с парными сыворотками.
7. Морфология и культуральные свойства плесневых и других грибов (рост на плотных питательных средах).
8. Диагностические, профилактические и лечебные препараты.
▲ Задание студентам
1.Указать материал для исследования.
2. Микроскопировать и зарисовать препараты дрожжеподобных грибов рода Candida, приготовленные из чистой культуры и патологического материала.
3. Определить видовую принадлежность грибов рода Candida на основании морфологии клеток и колоний, типа филаментации и биохимических свойств.
4. Оценить результаты РСК для серодиагностики висцерального кандидоза. Сделать заключение.
5. Дать краткую характеристику демонстрируемым диагностическим, профилактическим и лечебным препаратам.
▲ Методические указания
• Микробиологическая диагностика кандидоза
МАТЕРИАЛ ДЛЯ ИССЛЕДОВАНИЯ: налет со слизистых оболочек, кожные чешуйки из очага поражения, мокрота, моча, спинномозговая жидкость, кровь и др.
Микроскопическое исследование.При исследовании препаратов используют окраску простыми методами, а также по методам Романовского—Гимзы, Грама и др. Грибы рода Candida хорошо окрашиваются анилиновыми красителями. При необходимости исследуют нативные препараты. В нативных и окрашенных препаратах видны одноклеточные микроорганизмы круглой или овальной формы.
Микологическое (культуральное) исследование.Делают посев исследуемого материала на агар Сабуро или другие специальные среды. Посевы инкубируют при 20 и 37 "С. Рост колоний начинается на 2—3-й сутки, и окончательное формирование происходит через 5—6 дней. Идентификацию грибов рода Candida проводят на основании морфологии клеток, типа филаментации и биохимических свойств (табл. 23.1.1). Важное диагностическое значение имеют многократные количественные посевы исследуемого материала. Нарастающее количество колоний в посевах подтверждает диагноз.
Таблица 23.1.1. Таксономические признаки дрожжеподобных грибов родаCandida
| Вид | Морфология | Культуральные свойства | Биохимические свойства — ферментация Сахаров | ||
| колонии | преобладающий тип филамента- | глюкозы | сахарозы | мальтозы | лактозы |
| ции |
C.albicans Крупные, Круглые, Мусо- КГ — КГ
круглые, сметано- toruloi-
овальные образные, des края ровные
ные, сметано- toruloi-
удлинен- образные, des
ные суховатые, toruloi-
неровные des края
Условные обозначения: КГ — образование кислоты и газа.
Во многих случаях возможна идентификация выделенной культуры с указанием только родовой принадлежности (Candida spp.).
Экспресс-методы диагностики. Иммунохимические исследования. Метод ИФ и другие серологические реакции применяют для обнаружения антигенов возбудителя в материале.
Серодиагностика.Для обнаружения антител используют реакции агглютинации, РСК и др. Серодиагностика имеет ограниченное применение: нарастание титра антител в сыворотке крови при висцеральном кандидозе подтверждает диагноз.
• Микробиологическая диагностика дерматомикозов
МАТЕРИАЛ ДЛЯ ИССЛЕДОВАНИЯ чешуйки кожи, волосы, соскоб ногтевых пластинок.
Микроскопическое исследование.Для приготовления препарата на предметное стекло наносят каплю 10 % раствора
 |
 |
 |
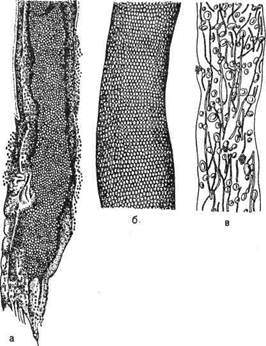
Рис.23.1.1. Дерматофиты в пораженном волосе.
а — Microsporum; б — Trichophyton; в — Achorion.
гидроксида натрия или спирта с глицерином, в которую помещают 2—3 подозрительных волоса, или несколько кожных чешуек. Препарат (со щелочью) осторожно подогревают над пламенем до появления белого ободка из кристаллов щелочи по периферии капли, не доводя ее до кипения. Затем каплю накрывают покровным стеклом и рассматривают под микроскопом с объективом 8х и 40х.
При оценке результатов микроскопического исследования и дифференциальной диагностике учитывают следующие признаки (рис. 23.1.1).
Microsporum canis идр. (микроспория) — волос в фолликулярной части окружен "чехлом" из мозаично расположенных мелких спор гриба. Внутри волоса обнаруживаются фрагменты гриба и споры.
Trichophyton tonsurans (стригущий лишай) — локализация элементов гриба в патологическом материале может быть различной. Споры гриба Trichophyton либо располагаются только внутри пораженного волоса, сплошь заполняя его содержимое (эндотрикс), либо несколькими слоями окружают волос снаружи в виде чехла (эктотрикс), либо споры и мицелий находятся как внутри, так и снаружи волоса (эндоэктотрикс).
Trichophyton (Achorion) schoenleinii (фавус или парша) — в волосе обнаруживают полиморфные грибковые элементы. Наряду с тонким мицелием встречается мицелий широкий, состоящий из прямоугольных клеток. Часто наблюдаются споры круглой или прямоугольной формы, а также пузырьки воздуха.
Epidermophyton floccosum (эпидермофития паховая) — элементы гриба содержатся в чешуйках кожи, где располагаются в виде толстых септированных ветвящихся нитей мицелия наряду со спорами многогранной формы.
Микологическое (культуральное) исследование.Проводят для установления родовой и видовой принадлежности возбудителя путем выделения чистой культуры гриба и изучения его биологических свойств. Материал предварительно обрабатывают кислотами или антибиотиками. Затем делают посев на сахарный питательный агар, сусло-агар, агар Сабуро, овощные среды (см. тему 4.1), куда добавляют антибиотики для задержки роста бактериальной флоры. Посевы инкубируют при 30 °С. В положительных случаях рост наблюдается на 3—5-е сутки в виде разнообразных колоний: гладких, морщинистых, мучнистых, пушистых, часто пигментированных. При микроскопии препаратов, приготовленных из культур, хорошо заметен развитой, широко ветвящийся септированный мицелий. Органами размножения служат споры, которые могут быть как внутренними (эндоспоры), расположенными внутри мицелия, так и наружными (экзоспоры), расположенными на концах или по сторонам нитей мицелия. Специальных органов плодоношения типа асков (сумок) у дерматофитов не обнаружено, что дало основание отнести их к несовершенным грибам — Fungi imper-fecti,
• Микробиологическая диагностика глубоких (системных) микозов
МАТЕРИАЛ ДЛЯ ИССЛЕДОВАНИЯ: мокрота, моча, пораженные ткани, биоптаты кожи и лимфатических узлов, спинномозговая жидкость и др.
Микроскопическое исследование.Обнаружение овальных дрожжевых или других тканевых форм грибов позволяет поставить предварительный диагноз. Иммунофлюоресцентный метод является наиболее эффективным способом выявления возбудителя в патологическом материале (см. ниже).
Микологическое исследование.Производят посев материала на среду Сабуро, кровяной агар и другие среды. Посевы инкубируют в течение нескольких недель при 37 и 20 "С. Выделенные культуры идентифицируют на основании морфологических и




биохимических признаков. Грибы, вызывающие глубокие микозы, относятся к группе возбудителей ООИ, представляющих биологическую опасность IV степени (см. главу 11). Необходимо помнить, что лабораторная диагностика этих инфекций осуществляется только в специализированных лабораториях.
Экспресс-методы диагностики: иммунохимические и молеку-лярно-биологические исследования.Иммунохимические исследования. При криптококкозе определяют антиген в спинномозговой жидкости и в сыворотке крови (у больных ВИЧ/СПИД) в динамике заболевания.
Молекулярно-биологические исследования. Исследуемый материал, полученный из очага инфекции, используют для обнаружения ДНК возбудителя с помощью ПЦР. В случае обнаружения соответствующих молекул можно поставить предварительный диагноз.
Серодиагностика.Проводят для определения антител, которые обнаруживаются в сыворотке крови через 2—4 нед после начала заболевания. Обычно используют РСК, РНГА, реакции иммунодиффузии, ИЭФ и др.
Кожно-аллергические пробы.Применяют для выявления состояния ГЗТ к соответствующим аллергенам.
• Диагностические, профилактические и лечебные препараты
Кандидозный антиген— взвесь 2-суточной агаровой культуры грибов рода Candida в изотоническом растворе хлорида натрия. Применяют для постановки реакции агглютинации для серодиагностики кандидоза.
Кандидозный антигендля РСК— спиртово-водный экстракт из культуры гриба рода Candida. Применяют для постановки РСК и кожно-аллергических проб при кандидозе.
Противогрибковые препараты:полиеновые антибиотики (нистатин, леворин, амфотерицин В), кетоконазол, флуконазол и другие производные имидазола, полиоксины, эхинокандины, 5-фторцитозин, гризеофульвин.
| Глава 24 |
Не нашли то, что искали? Воспользуйтесь поиском:
[youtube.player]Молекулярно-биологические методы исследования играют большую роль в современной медицине, криминалистике и биологии. Благодаря достижениям в области изучения ДНК и РНК, человек способен изучить геном организма, определить возбудителя заболевания, распознать нужную нуклеиновую кислоту в смеси кислот и т.д.
Молекулярно-биологические методы исследования. Что это такое?
Еще в 70-80-х годах ученым впервые удалось расшифровать геном человека. Это событие дало толчок развитию генной инженерии и молекулярной биологии. Изучение свойств ДНК и РНК привело к тому, что теперь можно использовать эти нуклеиновые кислоты в целях диагностики заболевания, изучения генов.
Получение ДНК и РНК
Молекулярно-биологические методы диагностики требуют наличия исходного материала: чаще это нуклеиновые кислоты. Существует несколько способов выделения этих веществ из клеток живых организмов. Каждый из них имеет свои достоинства и недостатки, и это надо учитывать при выборе метода выделения нуклеиновых кислот в чистом виде.
1. Получение ДНК по Мармуру. Метод заключается в обработке смеси веществ спиртом, в результате чего чистая ДНК выпадает в осадок. Минусом этого способа является использование агрессивных веществ: фенола и хлороформа.
2. Выделение ДНК по Буму. Основное вещество, которое используется здесь, – это гуанидин тиоционат (GuSCN). Оно способствует осаждению дезоксирибонуклеиновой кислоты на специализированных субстратах, с которых в последующем можно ее собрать с помощью специального буфера. Однако GuSCN – это ингибитор ПТЦ, и даже небольшая его часть, попавшая в осажденную ДНК, может повлиять на ход полимеразной цепной реакции, которая играет важную роль при работе с нуклеиновыми кислотами.
3. Осаждение примесей. Метод отличается от предыдущих тем, что осаждаются не сами молекулы дехоксирибонуклеиновой кислоты, а примеси. Чтобы это осуществить, используют ионообменники. Недостаток в том, что не все вещества могут осадиться.
4. Массовый скрининг. Используется этот способ в тех случаях, когда не нужны точные сведения о составе молекулы ДНК, а необходимо получить какие-то статистические данные. Объясняется это тем, что структура нуклеиновой кислоты может повредиться при обработке детергентами, в частности, щелочами.

Классификация методов исследования
Все молекулярно-биологические методы исследования делятся на три большие группы:
1. Амплификационные (с использованием множества ферментов). Сюда относится ПЦР – полимеразная цепная реакция, которая играет большую роль во многих из методов диагностики.
2. Неамплификационные. Эта группа методов связана непосредственно с работой смесей нуклеиновых кислот. Примерами являются 3 вида блоттингов, in situ гибридизация и т.д.
3. Методы, основанные на распознавании сигнала от молекулы зонда, который связывается с определенной ДНК или РНК зонда. Пример - система гибридизации в растворе Hybride Capture System (hc2).
Ферменты, которые могут использоваться в молекулярно-биологических методах исследования
Многие методы молекулярной диагностики подразумевают использование обширного диапазона ферментов. Ниже представлены применяемые наиболее часто:
2. ДНК-полимераза – синтезирует двухцепочечную молекулу дезоксирибонуклеиновой кислоты.
3. Обратная транскриптаза (ревертаза) – используется для синтеза ДНК на матрице РНК.
4. ДНК-лигаза – отвечает за образование фосфодиэфирных связей между нуклеотидами.
5. Экзонуклеаза – удаляет нуклеотиды с концевых участков молекулы дезоксирибонуклеиновой кислоты.
ПЦР – основной способ амплификации ДНК
Полимеразная цепная реакция (ПЦР) активно используется в современной молекулярной биологии. Это метод, при котором из одной молекулы ДНК можно получить огромное количество копий (амплифицировать молекулы).
Основные функции ПЦР:
- клонирование участков ДНК, генов.
Для проведения полимеразной цепной реакции необходимы следующие элементы: исходная молекула ДНК, термостабильная ДНК-полимераза (Taq или Pfu), дезоксирибонуклеотид-фосфаты (источники азотистых оснований), праймеры (2 праймера на 1 молекулу ДНК) и сама буферная система, в которой возможно проведение всех реакций.
ПЦР состоит из трех этапов: денатурация, отжиг праймеров и элонгация.
1. Денатурация. При температуре 94-95 градусов по Цельсию просходит разрыв водородных связей между двумя цепями ДНК, и в итоге мы получаем две одноцепочечные молекулы.
2. Отжиг праймеров. При температуре 50-60 градусов по Цельсию происходит присоединение праймеров на концах одноцепочечных молекул нуклеиновой кислоты по типу комплиментарности.
3. Элонгация. При температуре 72 градусов происходит синтез дочерних двухцепочечных молекул дезоксирибонуклеиновой кислоты.

Секвенирование ДНК
Молекулярно-биологические методы исследования часто требуют знания последовательности нуклеотидов в молекуле дезоксирибонуклеиновой кислоты. Для определения генетического кода проводится секвенирование. Молекулярная диагностика будущего будет основана на знаниях, полученных при определении последовательности человека.
Выделяют следующие виды секвенирования:
- секвенирование по Максаму-Гилберту;
- секвенирование по Сэнгеру;
- пиросеквенирование;
- нанопоровое секвенирование.
Что такое молекулярно-генетическая диагностика
Итак, молекулярно-генетическая диагностика — сравнительно новый метод обследования организма, позволяющий точно и быстро выявить вирусы и инфекции, мутации генов, вызывающих патологию, оценить риски наследственных и иных заболеваний. И это далеко не полный спектр возможностей исследования ДНК.
Важнейшим достоинством молекулярно-генетической диагностики является минимальная степень медицинского вмешательства, поскольку исследование проводят in vitro. Метод успешно применяют даже для диагностики заболеваний у эмбрионов, а также у ослабленных и тяжелобольных пациентов. Самый распространенный материал для исследования — кровь из вены, однако возможно выделение ДНК/РНК из других жидкостей и тканей: слюны, соскоба слизистой рта, выделений из половых органов, околоплодной жидкости, волос, ногтей и т.д.
Молекулярная диагностика — значительный шаг к персонализированной медицине, она позволяет учитывать все особенности конкретного пациента при обследовании и терапии.
Итак, исследование ДНК/РНК используется во многих разделах медицины. Давайте рассмотрим задачи и области, в которых активно применяют молекулярную диагностику:
- Выявление существующих патологий. Например, к молекулярной диагностике прибегают в тех случаях, когда инфекционное или вирусное заболевание не может быть определено обычными методами. Она позволяет обнаружить болезнь даже на ранней стадии, когда внешних проявлений нет.
- Исследование аллергических реакций. Молекулярная диагностика успешно применяется для определения аллергии: в отличие от традиционных методов, она более точна и при этом безопасна для пациента, так как отсутствует непосредственный контакт с аллергеном.
- Индивидуальная оценка рисков развития наследственных заболеваний. Молекулярная диагностика помогает выявить у взрослых и детей опасность в будущем подвергнуться различным патологиям. Нужно отметить, что есть болезни, которые вызваны исключительно мутацией гена (моногенные) и те, которые обусловлены в том числе генетическими особенностями (мультифакторные). Информация о первых позволяет, к примеру, оценить риски передачи наследственных заболеваний от родителей к ребенку. Знание о предрасположенности к мультифакторной патологии необходимо еще и для профилактики болезней с помощью изменения образа жизни.
- Перинатальная медицина. Как уже было сказано, молекулярная диагностика способна дать информацию о состоянии здоровья и генетических предрасположенностях человека. Это относится и к эмбрионам: анализ ДНК еще не родившегося ребенка позволяет распознать синдромы Дауна, Эдвардса, Патау, Тернера, Клайнфельтера. Также молекулярная диагностика применяется в области вспомогательных репродуктивных технологий: она позволяет установить генетические причины бесплодия и невынашивания беременности.
- Фармакогенетика. Молекулярная диагностика объясняет, почему на некоторых действуют одни препараты, а на других — иные: все дело в генетических особенностях пациентов. Возможность определения эффективности веществ имеет особое значение при лечении тяжелых заболеваний, например, онкологических.
- Спортивная медицина. Настоящие чудеса исследования ДНК и РНК творят и в области оценки спортивных перспектив. Например, родители малышей могут узнать о том, какой вид занятий принесет ребенку наибольшую пользу для здоровья или позволит достичь спортивных результатов.
Итак, обращение к генетическим исследованиям актуально в тех случаях, когда пациент стремится получить сведения о состоянии своего организма. Обычно это необходимо в следующих ситуациях:
Отдельной группой стоит выделить исследования ДНК, которые проводят в связи с планированием или рождением ребенка. Чаще всего родители обращаются в лабораторию, чтобы:
- изучить свою генетическую совместимость, оценить риски наследственных заболеваний потомства;
- исследовать состояние плода, выявить синдромы и опасные патологии;
- диагностировать заболевания (и оценить риски) и аллергические реакции у малыша;
- определить, какие спортивные занятия, какое питание и образ жизни будут наиболее полезны для ребенка, а чего стоит избегать;
- установить отцовство или материнство.
Независимо от выбранного метода молекулярно-генетического исследования, оно будет включать в себя следующие этапы:
- взятие биоматериала. Как уже было сказано, чаще для исследования используют кровь пациента. Полученный материал маркируют и транспортируют в лабораторию;
- выделение ДНК/РНК;
- проведение исследований в соответствии с выбранным методом;
- изучение и интерпретацию результатов;
- выдачу заключения.
Цитогенетический анализ позволяет выявить наследственные заболевания, психические отклонения, врожденные пороки развития. Суть метода — в изучении хромосом с помощью специальных микроматриц, нанесенных на ДНК-чипы. Для этого из образца крови выделяют лимфоциты, которые затем помещают на 48–72 часа в питательную среду и по истечении этого времени исследуют. Назначают такой анализ нечасто, в основном для изучения причин бесплодия и невынашивания беременности, для уточнения диагноза у детей при подозрении на врожденные заболевания. Анализ очень точен, но достаточно трудоемок и длителен (результат можно получить лишь через 20–30 дней после сдачи).
Достоинство и в то же время недостаток метода — в его специфичности: цитогенетика может выявить лишь небольшое количество патологий (например, аутизм), однако делает это практически без погрешностей.
Полимеразная цепная реакция — метод, изобретенный в 1983 году, по сей день самый популярный и фундаментальный в молекулярной диагностике. Характеризуется высочайшей точностью и чувствительностью, а также скоростью проведения исследования. Молекулярная диагностика ДНК/РНК методом ПЦР позволяет выявить такие патологии, как ВИЧ, вирусные гепатиты, инфекции, передающиеся половым путем, туберкулез, боррелиоз, энцефалит и многие другие.
Для анализа выбирают участок ДНК и многократно дублируют его в лаборатории с помощью специальных веществ. Для диагностики подходит большой перечень биоматериалов: кровь, слюна, моча, выделения из половых органов, плевральная и спинномозговая жидкость, ткани плаценты и т.д.
В данном молекулярном методе объектом исследования становятся уникальные нуклеотидные соединения отдельно взятой хромосомы или ее участок. Для этого используются меченые флуоресцентными маркерами короткие ДНК-последовательности (зонды), которые позволяют выявить фрагменты с атипичными генами. Биоматериал для анализа может быть любой: кровь, костный мозг, плацента, ткани эмбриона, биопсия и т.д. Важно, чтобы образец был доставлен в лабораторию сразу после его изъятия.
Метод особенно активно используют в онкологии (например, для наблюдения за остаточными злокачественными клетками после химиотерапии), а также в пренатальной диагностике (для определения риска развития у плода врожденных пороков), гематологии. FISH-метод очень чувствителен и точен для выявления поврежденных фрагментов ДНК (погрешность около 0,5%), при этом достаточно быстр: результат придется ждать не более 72-х часов. Однако у него есть и недостатки: FISH еще более специфичен, чем микроматричный цитогенетический анализ, и может служить лишь для подтверждения или опровержения предполагаемого диагноза.
Этот метод похож на предыдущий — здесь так же используются меченные флуоресцентом последовательности ДНК. Однако эти зонды сначала выделяют из проб, полученных от пациента, и затем сравнивают с образцами, нанесенными на микрочипы. ДНК-микрочип представляет собой основание (стеклянное, пластиковое, гелевое), на которое может быть нанесено до нескольких тысяч микротестов длиной от 25 до 1000 нуклеотидов. Полученные после очистки биоматериала пробы (зонды) совмещают с микротестами на чипе и наблюдают за реакцией маркёров. Результаты исследования готовы через 4–6 дней после забора материала.
Для анализа используется любой биоматериал, из которого можно получить образец ДНК/РНК. Используют такой метод в онкологии и кардиологии (в том числе для изучения генетической предрасположенности), он точен и чувствителен, однако в России его применяют редко — в этом его главный минус.
Итак, молекулярная диагностика — неинвазивный и точный метод обследования организма с широким спектром применения в разных областях медицины. Если на Западе исследования ДНК/РНК уже распространены повсеместно, то в России подобную услугу предлагают далеко не все клиники.
Сегодня медицина позволяет уже во время планирования беременности узнать о возможных рисках для будущего малыша, поэтому не пожалейте времени и средств — пройдите генетическое исследование еще до зачатия ребенка или, если беременность стала для вас сюрпризом, во время вынашивания. Так вы сможете избежать множества проблем для себя и для малыша в будущем.
[youtube.player]Читайте также:


