Международная классификация инфекция мочевыводящих путей
Рубрика МКБ-10: N39.0
Содержание
Инфекции мочевыводящих путей — самые распространенные бактериальные инфекции во всех возрастных группах. Заболеваемость инфекциями мочевыводящих путей составляет: среди новорожденных — 1%; среди детей дошкольного возраста — 2—3% (соотношение мальчики/девочки 1:10); среди школьников — 1—2% (соотношение 1:30); среди взрослых детородного возраста — 2—5% (соотношение 1:50); среди пожилых — 20—30% (женщины болеют чаще; исключение составляют госпитализированные больные, у которых соотношение составляет 1:1). В нижних мочевых путях постоянно присутствуют различные бактерии. Среди женщин, у которых при надлобковой пункции мочевого пузыря получают стерильную мочу, у 3/4 при посеве средней порции мочи, полученной при самостоятельном мочеиспускании, образуется более 10 000 колоний/мл. Диагностический критерий инфекции мочевыводящих путей — образование более 100 000 колоний бактерий при посеве 1 мл средней порции мочи. Однако клинические проявления инфекций часто развиваются и при меньшем содержании бактерий. Лейкоцитурия в отсутствие других симптомов не служит диагностическим критерием инфекции; она может быть обусловлена иным заболеванием, например злокачественной опухолью. Дифференциальная диагностика пиелонефрита и цистита или цистита и уретрита довольно сложна. Лабораторные исследования, например определение антибактериальных антител в сыворотке и моче, не позволяют установить, где находится источник инфекции — в верхних или нижних мочевых путях.
Согласно Т. Стейми (Stamey, 1980), различают четыре категории инфекций мочевыводящих путей: первичная инфекция; резистентная бактериурия; повторная инфекция (реинфекция) и возвратная инфекция (рецидив).
1. Первичная инфекция. Возбудители обычно чувствительны к большинству антимикробных средств; повторные инфекции возникают лишь у 25% больных.
2. Резистентная бактериурия — возбудитель сохраняется в моче во время лечения. Самая частая причина — неправильное лечение. Другие причины: устойчивость возбудителя к препарату, появление резистентных штаммов микроорганизмов, быстрое повторное инфицирование.
3. Повторная инфекция (реинфекция) обусловлена новым заражением через некоторое время после излечения (которое было подтверждено бактериологическим исследованием и посевом мочи). Врожденные и приобретенные аномалии мочевых путей — предрасполагающие факторы, но отнюдь не обязательные.
4. Возвратная инфекция (рецидив). Несмотря на лечение, во время которого результаты бактериологического исследования и посева мочи были отрицательными, бактерии остаются в мочевых путях. Через 5—10 сут после окончания лечения в моче появляется тот же возбудитель. Причиной часто служат мочевые камни, содержащие фосфаты магния и аммония (трипельфосфаты); врожденные и приобретенные аномалии мочевых путей; хронический простатит.
Собирают анамнез, оценивают клиническую картину заболевания. Физикальное исследование включает осмотр наружных половых органов, промежности, исследование прямой кишки, боковых отделов живота и органов брюшной полости, измерение АД. Проводят общий анализ мочи, посев мочи; измеряют АМК, уровни креатинина и электролитов в сыворотке. При простатите показано раздельное исследование и посев порций мочи, полученных при трехстаканной пробе с массажем и сбором секрета предстательной железы между второй и третьей порциями. Проводят рентгенологические и изотопные исследования мочевых путей, исследования уродинамики (цистометрию, сфинктерометрию и урофлоуметрию).
1. Лабораторные данные. Анализ мочи выявляет макро- или микрогематурию (вследствие воспаления слизистой) и лейкоцитурию (больше 5 лейкоцитов в поле зрения при большом увеличении, агрегаты лейкоцитов, лейкоцитарные цилиндры). Наличие активных лейкоцитов и значительное преобладание числа лейкоцитов над числом эпителиальных клеток — признаки инфекции. Лейкоцитурия — чувствительный, но неспецифический показатель. Кроме инфекций мочевых путей причиной лейкоцитурии могут быть туберкулез, опухоль, инструментальное исследование. Отсутствие лейкоцитурии не исключает инфекцию; примерно у половины женщин с бессимптомной бактериурией лейкоцитурии нет. Наличие бактерий в средней порции мочи у женщин далеко не всегда означает инфекцию мочевых путей; бактериальное загрязнение мочи может произойти при неправильном сборе или хранении образца. И наоборот, отсутствие бактерий в моче не исключает инфекцию. Клинически значимой бактериурией считается 100 000 колоний/мл — в средней порции мочи и 10 000 колоний/мл — в моче, полученной при пункции мочевого пузыря (при условии соблюдения всех правил сбора, транспортировки и культивирования образца). У больных с учащенным мочеиспусканием инфекцию нельзя исключить даже при наличии 100 колоний/мл. У 20% женщин с повторными инфекциями мочевых путей обнаруживают менее 100 000 колоний/мл. Если возбудитель — грамположительный микроорганизм, для развития инфекционного процесса достаточно 10 000 колоний/мл. Для определения очага инфекции и вида возбудителя проводят трехстаканную пробу с бактериологическим исследованием первой и средней порций мочи (бактериоскопия мазков, окрашенных по Граму).
2. Предрасполагающие факторы: обструкция мочевых путей, пороки развития, нейрогенная дисфункция мочевого пузыря, сахарный диабет, сниженный иммунитет, беременность, инструментальные исследования, сексуальная активность (у женщин), госпитализация.
3. Возбудители: Escherichia coli (в 50—80% случаев), Klebsiella spp., Proteus spp., Enterobacter spp., Pseudomonas spp., Serratia spp. (редко) и грамположительные кокки (редко).
4. Определение очага инфекции: катетеризация обоих мочеточников; промывание мочевого пузыря физиологическим раствором; выявление в моче бактерий, покрытых антителами, методом непрямой иммунофлюоресценции (положительный результат говорит в пользу почечного происхождения бактериурии); измерение титра антител в сыворотке; у мужчин — раздельное исследование и посев порций мочи, полученных при трехстаканной пробе с массажем и сбором секрета предстательной железы между второй и третьей порциями.
5. Рентгенологические исследования: обзорная рентгенография брюшной полости, экскреторная урография, микционная цистоуретрография и сцинтиграфия мочевого пузыря с 99mTc-диэтилентриаминопентоацетатом. С помощью этих методов можно выявить пороки развития, обструкцию мочевых путей, камни, инородные тела, свищи, оценить степень повреждения почечной паренхимы и скорость роста почки (особенно важно у детей с бессимптомными и повторными инфекциями).
В ходе обследования у 20—50% детей и 51% беременных обнаруживают врожденные или приобретенные аномалии мочевых путей; у 5—10% мальчиков и 1% девочек — обструкцию мочевых путей. Отклонения от нормы при микционной цистоуретрографии выявляют у 43% девочек с бактериурией, из них у 20% обнаруживают пузырно-мочеточниковый рефлюкс. У женщин с повторными инфекциями мочевых путей очень часто никакой патологии не находят.
6. Исследования уродинамики (цистометрия, сфинктерометрия и урофлоуметрия) показаны при обструкции мочевых путей и неврологических заболеваниях.
7. УЗИ и диафаноскопию брюшной полости и боковых отделов живота проводят новорожденным и грудным детям при подозрении на объемное образование.
Лечение: антимикробная терапия, лечебно-диагностические урологические процедуры и диспансерное наблюдение в дальнейшем.
1. При первичной неосложненной инфекции женщинам и девочкам назначают 7—10-суточный курс ампициллина, ТМП/СМК, сульфаниламидов, нитрофурантоина, цефалоспоринов или метенамина манделата. Дальнейшее обследование необязательно. Снижение температуры наступает через 2—3 сут, нормализация осадка мочи — через 4—5 сут, восстановление концентрационной функции почек — через 3 нед. Неэффективность лечения указывает на обструкцию мочевых путей или устойчивость возбудителя к препарату. При неосложненной инфекции нижних мочевых путей у женщин и девочек хорошие результаты дает однократный прием большой дозы антимикробного препарата (3 г амоксициллина или 320/1600 мг ТМП/СМК внутрь).
2. После излечения повторных и возвратных инфекций для поддержания стерильности мочи показан профилактический прием антимикробных средств. Назначают ТМП/СМК (80/400 мг на ночь), нитрофурантоин (50—100 мг на ночь) или метенамина манделат (0,5—1 г 4 раза в сутки) в течение 3—6 мес.
3. При инфекции мочевых путей, осложненных обструкцией, врожденной или приобретенной аномалией мочевых путей, абсцессом или мочекаменной болезнью, необходимо хирургическое вмешательство. При остром простатите, инфекциях верхних мочевых путей (пиелонефрит), уросепсисе, тошноте, рвоте, кишечной непроходимости больного госпитализируют и вплоть до улучшения состояния (обычно на протяжении 48 ч) проводят инфузионную терапию и в/в антимикробную терапию. При первичных инфекциях применяют ампициллин, амоксициллин, цефалоспорины или ТМП/СМК. При больничных инфекциях, повторных инфекциях верхних мочевых путей и при сниженном иммунитете средство выбора — комбинация аминогликозида и бета-лактамного антибиотика (пиперациллин, мезлоциллин или цефалоспорин). Через 48 ч, после получения результатов посева и тестов на чувствительность к антибиотикам, выбирают подходящий препарат для приема внутрь и продолжают лечение 10—14 сут. При первичном пиелонефрите обычно эффективен прием внутрь фторхинолонов: ципрофлоксацина, норфлоксацина, офлоксацина или ломефлоксацина.
4. При хроническом бактериальном простатите после подтверждения диагноза антимикробную терапию проводят как минимум в течение 4 нед.
5. Новообразования нижних мочевых путей, остроконечные кондиломы, хламидийная инфекция, простая язва мочевого пузыря, инородные тела, вульвовагинит, атрофический вагинит, герпес, болезнь Крона, неспецифический язвенный колит, неинфекционный цистит (химический или лекарственный) сопровождаются симптомами, характерными для инфекций нижних мочевых путей. В этих случаях результаты посева мочи отрицательны. Всем больным показано полное урологическое и гинекологическое обследование с последующим лечением.
6. Инфекции мочевых путей во время беременности. Бактериурию выявляют у 4—6% беременных; из них только у 30% отмечаются клинические проявления инфекции. Без лечения у 20—30% развивается пиелонефрит, и ребенок часто рождается недоношенным. Назначают пенициллины, нитрофурантоин или цефалоспорины. Аминогликозиды, тетрациклины и хлорамфеникол противопоказаны. Сульфаниламиды и ТМП/СМК нельзя применять в последние 4—6 нед беременности.
Спонтанная ремиссия длительностью более 1 года наблюдается лишь у 10% больных. Антимикробная терапия при правильном выборе препарата и дозы приводит к излечению почти всех больных с первичными инфекциями и более 95% больных с повторными инфекциями. Половина больных, прошедших курс лечения, и 80% больных с бессимптомной бактериурией (независимо от числа ранее перенесенных инфекций мочевых путей) впоследствии заболевают вновь, иногда неоднократно. У 5—13% девочек с повторными инфекциями, не осложненными обструкцией мочевых путей, и 13—26% девочек с бессимптомной бактериурией развивается нефросклероз. У мальчиков это осложнение встречается еще чаще, в основном в возрасте до 6 лет. У одной трети детей с инфекциями мочевых путей и 95% детей с нефросклерозом в дальнейшем возникает пузырно-мочеточниковый рефлюкс; примерно у 1% из них — артериальная гипертония и почечная недостаточность. У каждого десятого больного, нуждающегося в гемодиализе, причиной почечной недостаточности послужили инфекции мочевых путей или их осложнения.
1. Stamey, T. A. Pathogenesis and Treatment of Urinary Tract Infections. Baltimore: Williams & Wilkins, 1980.
[youtube.player]Одна из важнейших проблем современной медицины – инфекции мочевыводящих путей (ИМП). Заболевания, связанные с этими инфекциями, распространены во всех уголках мира и вынуждают обращаться за врачебной помощью около 7 млн. человек ежегодно (а каждому седьмому из них приходится проходить лечение в стационаре). ИМП подвержены как мужчины, так и женщины, причем женщины болеют чаще, а у мужчин чаще развиваются осложнения.
Причины инфекции мочевыводящих путей
Причины, которые обычно приводят к развитию осложненных инфекций мочевыводящих путей:
(камни в почках, мочеточнике, мочевом пузыре, опухоли, стриктуры лоханочно-мочеточникового сегмента и мочеточника (стрикутра - сужение трубчатой структуры), осложнение простатита - инфравезикальная обструкция, пролапс гениталий и мочевого пузыря у женщин);
(детрузорно-сфинктерная диссинергия, нестабильность детрузора и уретры, нарушения мочеиспускания центрального генеза: опухоли мозга, острое нарушение мозгового кровообращения, инсульт);
Инфекций мочевыводящих путей могут вызвать присутствие уретрального или мочеточникового катетера, нефростомических и цистостомических дренажных трубок, камней.
Сахарный диабет, почечная недостаточность, печеночная недостаточность, снижение иммунитета, серповидно-клеточная анемия.
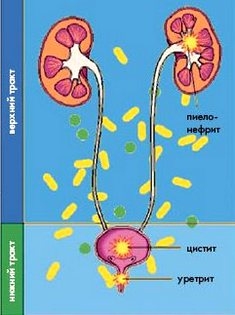
Расскажем подробней о каждой из них.
Обструкции мочевыводящих путей, ведущие к нарушению уродинамического процесса. Ряд научных исследований позволил сделать вывод о том, что чаще всего ИМП протекают в осложненной форме из-за уродинамических нарушений. Эти нарушения развиваются по обструктивному типу с наличием камней, стриктур мочеточника, лоханочно-мочеточникового сегмента, инфравезикальной обструкции. Именно нормализация уродинамики и является основной проблемой, связанной с терапией ОИМП. Если причину, которая привела к обструкции, невозможно устранить в короткие сроки, выполняют дренирование верхних МВП (нефростомическим дренажем). При обнаружении инфравезикальной обструкции необходим цистостомический дренаж мочевого пузыря. Эти процедуры обычно проводят подкожно, с контролем УЗИ.
Присутствие инородного тела. К инородным телам, осложняющим течение ИМП, относятся конкременты (мочевого пузыря, почек), а также дренажи. Лечение инфекций, связанных с инородными делами, часто затягивается и при этом не приносит заметных улучшений. Дело в том, что сверху инородное тело покрывается своеобразной биопленкой. Она образована соединенными друг с другом и с какой-либо поверхностью микробами, которые пребывают в разных фазах роста. Также в состав пленки входят соматические клетки, неорганические и органические вещества. Не следует связывать подобное микробное покрытие исключительно с инородными телами (дренажные трубки, конкременты). Оно характерно и для рубцов, а также тканей, подвергшихся некротическим изменениям в результате хирургического вмешательства.
В той или иной степени почти все осложняющие факторы способствуют формированию биопленки. Важно учитывать, что образующие такое покрытие бактерии не похожи на планктонные микроорганизмы. Отличаются они и от культур, которые применяются для лабораторных исследований. Дозировка антибиотика, дающая хороший результат в условиях лаборатории, может никак не повлиять на микробную пленку. Ситуация осложняется и тем, что организмы из биопленки имеют более выраженную сопротивляемость негативным внешним факторам. Эти факты дают основание полагать, что затруднения, возникающие при лечении пациентов с хронической ОИМП, связаны именно с наличием микробного покрытия.
Нарушения мочеиспускания нейрогенного характера. При этих заболеваниях нарушается уродинамика, и развитие инфекций мочевых путей существенно осложняется. В этом случае справиться с инфекционным процессом можно лишь после эффективного курса коррекции нейрогенной патологии и нормализации уродинамики.
Наличие сопутствующих заболеваний. Некоторые тяжелые заболевания могут серьезно осложнить развитие инфекций мочевыводящих путей. Окончательный список этих заболеваний пока еще составлен не был, однако есть такие болезни, негативное влияние которых не вызывает у медиков никаких сомнений. Прежде всего, речь идет о состояниях, при которых снижается иммунологическая реактивность. Это различные формы иммунодефицита и сахарный диабет. Кроме того, инфекции мочевыводящих путей могут быть осложнены из-за почечной и печеночно-почечной недостаточности. Еще один осложняющий фактор связан с серповидно-клеточной анемией.
[youtube.player]Версия: Клинические рекомендации РФ (Россия)
Общая информация
Союз педиатров России
Клинические рекомендации: Инфекция мочевыводящих путей у детей
N10/ N11/ N13.6/ N30.0/ N30.1/ N39.0


Классификация
Этиология и патогенез
Эпидемиология
Диагностика
У детей более старшего возраста: подъемы температуры (чаще до фебрильных цифр) без катаральных явлений, рвота, боли в животе, дизурия (учащенное и/или болезненное мочеиспускание, императивные позывы на мочеиспускание).
• При физикальном обследовании рекомендовано обратить внимание на: бледность кожных покровов, наличие тахикардии, появление симптомом дегидратации (преимущественно у новорожденных и детей грудного возраста), отсутствие катаральных явлений при наличии повышения температуры (чаще до фебрильных цифр, реже- субфебрильных), резкий запах мочи, при остром пиелонефрите - положительный симптом Пастернацкого (болезненность при поколачивании или, у маленьких детей, - при надавливании пальцем между основанием 12-го ребра и позвоночником).
Комментарии: данные клинического анализа крови: лейкоцитоз выше 15х10 9 /л, высокие уровни С-реактивного белка (СРБ) (≥10 мг/л) указывают на высокую вероятность бактериальной инфекции почечной локализации [1,2,3,4,5].
| Симптом | Цистит | Пиелонефрит |
| Повышение температуры более 38°С | Не характерно | Характерно |
| Интоксикация | Редко (у детей раннего возраста) | Характерно |
| Дизурия | Характерно | Не характерно |
| Боли в животе/пояснице | Не характерно | Характерно |
| Лейкоцитоз (нейтрофильный) | Не характерно | Характерно |
| СОЭ | Не изменена | Увеличена |
| Протеинурия | Нет | Не большая |
| Гематурия | 40-50% | 20-30% |
| Макрогематурия | 20-25% | Нет |
| Лейкоцитурия | Характерна | Характерна |
| Концентрационная функция почек | Сохранена | Снижена |
| Увеличение размеров почек (УЗИ) | Нет | Может быть |
| Утолщение стенки мочевого пузыря (УЗИ) | Может быть | Нет |
Осложнения
2. При рецидивирующем течении инфекции мочевыводящих путей и /или развитии ИМВП на фоне ПМР - развитие рефлюкс-нефропатии.
Лечение
| Препарат (МНН) | Код АТХ | Суточная доза** | Кратность приема (per os) |
| Амоксициллин +клавулановая кислота ж,вк | J01CR02 | 3 раза в день | |
| Цефиксим | J01DD08 | 8 мг/кг/сут | 2 раза в день |
| Цефуроксим ж,вк | J01DC02 | 50-75 мг/кг/сут | 2 раза в день |
| Цефтибутен | J01DD14 | 9 мг/кг/сут | 1 раз в день |
| Ко-тримоксазол ж,вк | J01EE01 | 2-4 раза в день | |
| Фуразидин | J01XE | 3-5 мг/кг /сут | 3-4 раза в день |
**Следует помнить, что при снижении клиренса эндогенного креатинина менее 50 мл/мин доза препарата уменьшается вдвое!
(Сила рекомендации A; уровень доказательств 2a)
(Сила рекомендации B; уровень доказательств 2a)
Таблица 3 - Антибактериальные препараты для парентерального применения
| Препарат | Код АТХ | Суточная доза** | Кратность приема |
| J01CR02 | 90 мг/кг/сут | 3 раза в день | |
| Цефтриаксон ж | J01DD04 | 50-80мг/кг/сут | 1 раз в день |
| Цефотаксим ж | J01DD01 | 150мг/кг/сут | 4 раза в день |
| Цефазолин | J01DB04 | 50 мг/кг/сут | 3 раза в день |
**Следует помнить, что при снижении скорости клубочковой фильтрации менее 50 мл/мин доза препарата уменьшается вдвое!
Комментарии: Как препараты резерва, а также для комбинированной терапии при уросепсисе могут быть использованы аминогликозиды (амикацин ж 20 мг/кг/сут 1 раз в день, тобрамицин ж 5 мг/кг/сут 3 раза в день, гентамицин ж 5-7,5 мг/кг/сут 3 раза в день), карбапенемы. При псевдомонадной инфекции - тикарциллин/клавуланат (250 мг/кг/сут) или цефтазидим ж (100 мг/кг/сут) + тобрамицин ж (6 мг/кг/сут), в особо рефрактерных случаях – фторхинолоны (применение у детей - с разрешения Локального этического комитета медицинской организации, при наличии информированного согласия родителей / законных представителей и ребенка в возрасте старше 14 лет). Эффективность лечения оценивают через 24-48 часов по клиническим признакам и результатам исследования мочи. При неэффективности лечения следует заподозрить анатомические дефекты или абсцесс почки [2,7].
[youtube.player]Инфекции мочевыводящих путей (ИМП) в большинстве стран мира — одна из наиболее актуальных проблем. Так, в США ИМП становятся причиной обращения к врачу 7 миллионов пациентов в год, а для миллиона
Инфекции мочевыводящих путей (ИМП) в большинстве стран мира — одна из наиболее актуальных проблем. Так, в США ИМП становятся причиной обращения к врачу 7 миллионов пациентов в год, а для миллиона пациентов являются причиной госпитализации [9]. Особую категорию ИМП составляют осложненные инфекции. Согласно современной классификации, к осложненным инфекциям мочевыводящих путей (ОИМП) относятся заболевания, объединенные наличием функциональных или анатомических аномалий верхних или нижних мочевых путей или протекающие на фоне заболеваний, снижающих общий иммунный статус.
Необходимо отметить, что группа ОИМП представлена крайне разнородными заболеваниями: от тяжелого пиелонефрита с явлениями обструкции и угрозой развития уросепсиса до катетер-ассоциированных инфекций МВП, которые могут исчезнуть самостоятельно после извлечения катетера.
Наиболее часто встречающиеся причины возникновения ОИМП приведены в табл. 1 [5].
На основании данных можно сделать вывод, что в большинстве случаев причиной осложненного течения ИМП становятся нарушения уродинамики по обструктивному типу при камнях различной локализации, стриктурах мочеточника и лоханочно-мочеточникового сегмента, инфравезикальной обструкции. Восстановление нормальной уродинамики является краеугольным камнем лечения любой мочевой инфекции. В тех случаях, когда причина возникновения обструкции не может быть ликвидирована немедленно, следует прибегать к дренированию верхних мочевых путей нефростомическим дренажем, а в случае инфравезикальной обструкции — к дренированию мочевого пузыря цистостомическим дренажем. Обе операции предпочтительно выполнять чрезкожно под ультразвуковым контролем.
Часто причиной осложнений при ИМП становятся инородные тела в мочевыводящих путях: конкременты почек и мочевого пузыря, различные дренажи. Лечение подобных инфекций длительное и подчас малоэффективное. Причина кроется в образовании на поверхности инородных тел микробной пленки, которая состоит из связанных между собой и с какой-либо поверхностью микроорганизмов, находящихся в различных фазах роста, их внеклеточных продуктов, соматических клеток, органического и неорганического материала [1].
Биопленка может быть ассоциирована не только с поверхностью дренажных трубок и конкрементов, но и с рубцово-измененными и некротизированными тканями, присутствующими в просвете мочевыводящих путей после предшествующих оперативных вмешательств. Так или иначе, но большинство осложняющих факторов благоприятствуют образованию биопленок. Бактерии, формирующие биопленку, значительно отличаются от планктонных свободно плавающих микробных клеток, не говоря уже о культуре микроорганизмов, использующейся для лабораторных тестов. Доза антибиотика, бактерицидная в отношении возбудителя в лабораторных условиях, зачастую не оказывает на биопленку никакого воздействия; кроме того, бактерии в биопленке более устойчивы к факторам окружающей среды. Вышесказанное свидетельствует о том, что именно биопленка в итоге является основной причиной возникновения трудностей, которые часто сопровождают лечение осложненной хронической персистирующей инфекции мочевыводящих путей.
К заболеваниям, нарушающим нормальную уродинамику и осложняющим течение ИМП, относятся и нейрогенные нарушения мочеиспускания. Рассчитывать на успех лечения ИМП можно только после коррекции нейрогенных нарушений и восстановления нормальной уродинамики.
Особую группу составляют осложняющие факторы, связанные с наличием сопутствующих тяжелых заболеваний. Список этих заболеваний является предметом обсуждения, однако некоторые нозологии могут быть внесены в него без колебаний. Это заболевания, обусловливающие общее снижение иммунологической реактивности организма: сахарный диабет, иммунодефицитные состояния. К фоновым заболеваниям, значительно осложняющим течение ИМП, относятся также серповидно-клеточная анемия, почечная и печеночно-почечная недостаточность.
Помимо причин, обусловливающих возникновение ОИМП, существует ряд факторов риска развития этого состояния (табл. 3) [5].
Серьезную проблему для выбора эффективной терапии представляет сочетание ОИМП с хроническим простатитом. Хронический простатит — одно из самых трудных для диагностики и лечения заболеваний в урологии. Любое повышение внутриуретрального давления приводит к рефлюксу мочи и содержащихся в ней микроорганизмов в протоки периферической зоны в обход протоков центральной зоны предстательной железы, соустье которых с уретрой по своей природе почти клапанное. При несостоятельности внутреннего сфинктера нейрогенного происхождения или резекции шейки мочевого пузыря ткань простаты подвергается постоянному риску инфицирования и реинфицирования. Хронический бактериальный простатит характеризуется персистированием преимущественно грамотрицательных бактерий в секрете простаты и рецидивирующими ИМП [1, 3].
В табл. 2 приведены возбудители, наиболее часто являющиеся причиной возникновения ИМП [7]. Обращает на себя внимание, что на втором и третьем местах после наиболее распространенного возбудителя ИМП — кишечной палочки — при осложненных ИМП находятся Enterococcus spp. и Pseudomonas spp., а при катетер-ассоциированных инфекциях — дрожжевые грибки, отсутствующие при неосложненных ИМП.
Микробиологические особенности осложненных ИМП учитываются при выборе препарата для их лечения.
Лечение инфекции мочевых путей подразумевает проведение эффективной антибактериальной терапии при условии восстановления нормальной уродинамики и направлено на профилактику уросепсиса и возникновения рецидивов. Исключения составляют катетер-ассоциированные инфекции, в большинстве случаев исчезающие после удаления катетера. Открытым остается вопрос о необходимости антибактериальной терапии у пациентов с асимптоматической бактериурией. Большинство урологов считают, что лечение в подобных ситуациях не показано.
Дополнительной проблемой, значительно усложняющей лечение ОИМП, является высокая устойчивость микроорганизмов к большинству антибактериальных препаратов, длительно применяющихся в урологической практике. Госпитализация, неадекватные по длительности курсы лечения и некорректное назначение лекарственных препаратов приводят зачастую к возникновению антибиотико-устойчивых штаммов.
В нашей клинике в случае тяжелых инфекций мочевыводящих путей, а также в послеоперационном периоде после масштабных оперативных вмешательств мы в последнее время применяем новый антимикробный препарат группы фторхинолонов — L-изомер офлоксацина — левофлоксацин (таваник). Подобный выбор при назначении антибактериальной терапии объясняется доказанной способностью препаратов этой группы лучше проникать в биопленку [2, 9].
Поскольку на левофлоксацин приходится практически вся противомикробная активность в рацемической смеси изомеров, его активность in vitro в два раза превышает активность офлоксацина. Биодоступность препарата равняется 99 %, а особенности его фармакокинетики таковы, что 87 % препарата экскретируется с мочой в неизмененном виде [4]. Несмотря на наличие перекрестной устойчивости между левофлоксацином и другими фторхинолонами, некоторые микроорганизмы, устойчивые к хинолонам, могут проявлять чувствительность к левофлоксацину.
В исследованиях in vitro левофлоксацин доказал свою эффективность в отношении E.coli, Enterobacter, Klebsiella, Proteus Mirabilis, Pseudomonas aurugenosa, являющихся наиболее частыми возбудителями осложненной и неосложеннной форм урогенитальной инфекции (табл. 2).
Курс лечения таваником в дозе 250 мг однократно в течение суток на протяжении 10 дней проведен нами у 20 больных. Согласно полученным данным, эффективность и безопасность лечения были признаны хорошими и очень хорошими у 95% пациентов. Сходные результаты приводят в своих работах G. Richard, C. DeAbate et al., применявшие препарат по аналогичной схеме и добившиеся клинического эффекта у 98,1% пациентов [8]. Столь высокие показатели объясняются непродолжительностью применения левофлоксацина в урологической практике, чем и обусловлено отсутствие устойчивых к его действию штаммов микроорганизмов. Надо отметить, что устойчивость к препаратам этой фармакологической группы, связанная со спонтанными мутациями in vitro, встречается крайне редко [9].
Наряду с фторхинолонами в лечении ИМП широко применяются цефалоспорины II поколения (цефуроксим) и особенно III поколения (цефотаксим, цефтазидим и др.), а также карбапенемные антибиотики (имипенем/циластатин, меропенем).
При осложненных инфекциях МВП иногда назначают полусинтетические пенициллины (ампициллин, пиперациллин) и их комбинации с ингибиторами b-лактамаз (ампициллин/сульбактам, пиперациллин/тазобактам), ко-тримоксазол, аминогликозиды (обычно в комбинации с b-лактамами). Однако эффективность этих препаратов при ОИМП прогнозировать достаточно сложно из-за существенных различий в чувствительности возбудителей в зависимости от региона, стационара и источника развития инфекции (внебольничные или госпитальные). Таким образом, при назначении указанных препаратов в ходе терапии ОИМП следует опираться на данные бактериологического исследования мочи и учитывать чувствительность выделенных микроорганизмов.
Препараты нитрофуранового ряда — нефторированные хинолоны (налидиксовая кислота), оксихинолины (5-НОК) — не должны применяться для терапии ОИМП, так как они являются уроантисептиками, то есть создают терапевтическую концентрацию в моче, но не в паренхиме почек.
Длительность курса антибактериальной терапии ОИМП должна составлять не менее 14 дней. Более короткие курсы (7-10 дней) допустимы при назначении фторхинолоновых антибиотиков, выделении высокочувствительного возбудителя и устранении факторов, осложняющих течение ИМП [5].
В заключение хочется подчеркнуть, что лечение инфекций мочевыводящих путей — процесс сложный, длительный и зачастую малоэффективный, поскольку из всего многообразия существующих на сегодня антибактериальных препаратов ни один не обладает достаточно высокой эффективностью в отношении биопленок. Поэтому усилия врачей должны быть направлены преимущественно на профилактику возникновения подобных инфекций.
[youtube.player]Читайте также:


