Изменения клеток плоского эпителия характерные для папилломавирусной инфекции
Папилломавирусная инфекция (ПВИ) половых органов — группа заболеваний, ассоциированных с вирусом папилломы человека - ВПЧ.
Генитальные бородавки, генитальные кондиломы.
КОД ПО МКБ-10 В97.7 Папилломавирусы. А63.0 Аногенитальные (венерические) бородавки.
По данным МЗСР РФ за 2001 г., заболеваемость наиболее известной формы папилломавирусной инфекции — остроконечных кондилом — 26 на 100 000 населения. В мире около 300 млн инфицированных ВПЧ. ПВИ гениталий выявлена у 30,3% населения европейской части РФ.
Пик заболеваемости папилломавирусной инфекцией половых органов регистрируют у 15–25летних сексуально активных женщин. Через три года после начала половой жизни 70% женщин инфицированы ВПЧ. Частота папилломавирусной инфекции прямо пропорциональна числу половых партнёров.
Международное агентство по исследованию рака объявило ВПЧ типов 16 и 18 канцерогенными факторами, а типов 31, 33 и 35 — возможными канцерогенами.
Клиникоморфологическая классификация ВПЧ - ассоциированных поражений нижнего отдела половых органов:
- Клинические формы (видимые невооружённым глазом).
-Экзофитные кондиломы (остроконечные типичные, папиллярные, папуловидные).
-Симптоматические ЦИН. - Субклинические формы (невидимые невооружённым глазом и бессимптомные, выявляемые только при кольпоскопии
и/или при цитологическом или гистологическом исследовании).
-Плоские кондиломы (типичная структура с множеством койлоцитов).
-Малые формы (различные поражения многослойного плоского и метапластического эпителия с единичными
койлоцитами).
-Инвертирующие кондиломы (с локализацией в криптах).
-Кондиломатозный цервицит/вагинит. - Латентные формы (обнаружение ДНК ВПЧ при отсутствии клинических, морфологических или гистологических
изменений). - ЦИН или ПИП:
-ЦИН I (ПИП низкой степени) — слабовыраженная дисплазия +/– койлоцитоз, дискератоз;
-ЦИН II (ПИП высокой степени) — выраженная дисплазия +/– койлоцитоз, дискератоз;
-ЦИН III или CIS — тяжёлая дисплазия или карцинома in situ +/– койлоцитоз, дискератоз;
-микроинвазивная плоскоклеточная карцинома.
Возбудитель папилломавирусной инфекции — вирус папилломы человека (ВПЧ). Известно более 100 типов ВПЧ, подробно описано около 80 типов. Из всех идентифицированных типов 34 поражают аногенитальную область.
ВПЧ — мукозотропные высококонтагиозные вирусы с инкубационным периодом 1–8 мес. Передача ВПЧ происходит при непосредственном контакте кожных покровов и слизистых оболочек, преимущественно при половом контакте (в том числе нетрадиционном): ВПЧносители передают половому партнёру в 46–67% случаев, причём при гомосексуальных контактах в 5–10 раз чаще, чем при гетеросексуальных. Кроме того, ВПЧ передаётся от матери к плоду, вызывая папилломатоз гортани плода; поражает клетки трофобласта, приводя к спонтанным абортам. Не исключена возможность контактной трансмиссии ВПЧ через руки и медицинские инструменты. ВПЧ попадает в клетки слизистых оболочек и (или) кожных покровов при контакте через микроповреждения и поражает базальные слои эпителия.
В заражённых клетках вирусный геном может существовать в двух формах: эписомальной (вне хромосом) и интегрированной в клеточный геном. Интеграция вирусной ДНК ведёт к нестабильности клеточного генома и хромосомным нарушениям.
Присутствуя в макроорганизме, вирусы не всегда вызывают заболевание. Установлено транзиторное и постоянное носительство ВПЧ. На трансформацию латентного носительства ВПЧ в клинические и субклинические формы влияют следующие факторы:
- вирусный фактор (типы 16 и 18 персистируют в организме дольше, чем низкоонкогенные);
- иммунологическая реакция организма женщины на внедрение вируса (генетически детерминированная или приобретённая под влиянием факторов окружающей среды);
- кофакторы опухолевой трансформации (гормональный фон и курение).
Носительство ВПЧ не пожизненное. По данным ВОЗ (1997), при отсутствии отягощающих факторов в течение 3 лет ПИП низкой степени, содержащие ВПЧ, подвергаются регрессии в 50–62% наблюдений. У 70% молодых ВПЧ-инфицированных женщин ДНК ВПЧ перестают обнаруживать на протяжении первых 24 месяцев наблюдения, у пожилых пациенток ВПЧ персистирует более продолжительное время. Скорость элиминации зависит от иммунореактивности клеток организма хозяина и значительно снижается при инфицировании несколькими типами ВПЧ.
Клиническая картина ПВИ обусловлена типом вируса и состоянием иммунитета. Папилломавирусная инфекция половых органов — полиморфная многоочаговая патология кожи и слизистых оболочек нижнего отдела полового тракта.
Экзофитные кондиломы могут быть бессимптомными или сопровождаться такими симптомами, как зуд, бели, болезненность. Во время беременности наблюдают склонность к росту кондилом, после родов — к спонтанной регрессии. Субклинические формы папилломавирусной инфекции обычно бессимптомны, в редких случаях наблюдают зуд, жжение, бели. Малые формы папилломавирусной инфекции характеризует небольшая выраженность цитопатического действия ВПЧ (наличие единичных койлоцитов) на фоне различных изменений многослойного плоского и метапластического эпителия, включая гипер и паракератоз, гиперплазию базального слоя, акантоз, цервицит. Предполагают, что малые формы папилломавирусной инфекции (ПВИ) — одна из стадий развития или регресса плоской кондиломы.
Латентные формы папилломавирусной инфекции (бессимптомное вирусоносительство) выявляют при обследовании здоровых женщин или пациенток, обратившихся по поводу другого заболевания.
Симптоматические ЦИН определяют невооружённым глазом, они представлены участками выраженного ороговения (в виде белёсых бляшек), экзофитными образованиями или изъязвлениями. При кондиломатозном цервиците и вагините при осмотре отмечают волнистую (негладкую) поверхность эпителия шейки матки и влагалища.
Субклинические формы диагностируют при кольпоскопическом и цитологическом исследованиях.
Специфического комплекса кольпоскопических признаков папилломавирусной инфекции нет. Наиболее характерными кольпоскопическими признаками субклинических форм папилломавирусной инфекции считают: ацетобелый эпителий, мозаика, пунктация, атипичная зона трансформации.
Выраженные (грубые) кольпоскопические признаки папилломавирусной инфекции:
- грубая лейкоплакия;
- грубые мозаика и пунктация.
Малые кольпоскопические признаки папилломавирусной инфекции:
- тонкая лейкоплакия;
- нежные мозаика и пунктация.
Основной цитологический признак папилломавирусной инфекции — наличие в мазке клеток с койлоцитозом и дискератозом. Обнаружение в мазке клеток с дискариозом предполагает наличие ЦИН. Койлоциты образуются в тканях в результате цитоспецифического эффекта ВПЧ и представляют собой клетки многослойного плоского эпителия промежуточного типа с увеличенными ядрами и обширной околоядерной зоной просветления за счёт дегенеративных изменений и некроза разрушенных цитоплазматических органелл.
К гистологическим проявлениям папилломавирусной инфекции шейки матки относят экзофитные и типичные плоские кондиломы, маловыраженные изменения плоского эпителия (единичные койлоциты при наличии различных изменений эпителия, в том числе кондиломатозный цервицит/вагинит), ЦИН различной степени и без них, РШМ.
- Иммунограмма.
- Обследование половых партнёров.
Эффективность диагностики папилломавирусной инфекции может быть высокой только в случае комплексного применения кольпоскопии, типирования ВПЧ и цитологического исследования.
Экзофитные кондиломы дифференцируют с другими кожными заболеваниями (широкими кондиломами при сифилисе, плоскоклеточными кондиломами, псориазом, контагиозным моллюском и др.), небольшие кондиломы у входа во влагалище — с разрастаниями гимена. Субклинические формы дифференцируют с доброкачественными процессами вульвы (воспалительными и дистрофическими).
- Дерматовенеролог — при наличии экзофитных кондилом атипичного вида.
- Иммунолог — при рецидивирующих и обширных повреждениях.
- Онкогинеколог — пациенткам с ЦИН III.
Плоские кондиломы промежности.
- Деструкция экзофитных кондилом и атипически изменённого эпителия.
- Коррекция иммунного гомеостаза.
- Лечение сопутствующих генитальных инфекций и дисбиоза влагалища.
- Лечение половых партнёров.
Для биопсии, для хирургического лечения. В большинстве случаев лечение проводят амбулаторно или в стационаре одного дня.
Для деструкции атипически изменённого эпителия применяют физические методы (диатермо крио, лазерный и радиоволновый методы), в ряде случаев — химическую коагуляцию и лечение цитотоксическими препаратами. Деструкцию экзофитных кондилом проводят после локальной инфильтрационной анестезии 0,5% раствором лидокаина (или в виде спрея).
При появления гиперемии, зуда, болезненности интервалы между процедурами можно увеличить до 2–3 дней. Цитостатические лекарственные средства: фторурацил (5% крем) применяется самостоятельно в домашних условиях. Смазывать пораженные участки кожи и слизистых оболочек 1 раз в сутки на ночь в течение 7 дней. При отсутствии эффекта от курса лечения химическими коагулянтами и цитотоксическими препаратами показано применение других деструктивных методов.
Показаниями к иммуномодуляции и противовирусной терапии являются рецидивы папилломавирусной инфекции, обширные и множественные поражения.
Иммуномодулирующие препараты (системного и локального действия) при папилломавирусной инфекции гениталий применяются как в монотерапии, так и в сочетании с деструктивными методами. Иммуномодулирующую терапию проводят под контролем иммунограммы. Применяют интерфероны и их индукторы, синтетические иммуномодуляторы, иммуноглобулины. Патогенетически обоснованным является применение иммуномодуляторов с противовирусным и антипролиферативным действием. Иммуномодуляторы применяются за 10 дней до деструкции патологического очага. По показаниям второй курс иммуномодулирующей терапии проводят после деструкции экзофитных кондилом и атипически изменённого эпителия.
Иммуномодулирующие и противовирусные препараты не рекомендуют применять во время беременности и лактации.
При адекватном лечении прогноз благоприятный.
[youtube.player]Все женщины мечтают выглядеть привлекательно. Но иногда кожа способна несколько огорчать представительниц прекрасного пола. Особенно неприятно, когда на ней появляются бородавки или малоэстетичные папилломы. Конечно, такой дефект барышни чаще всего воспринимают исключительно как внешний. А ведь эти образования вызывает неприятная, а иногда и опасная, HPV-инфекция у женщин. Что это такое? Как инфекция проникает в организм? Какими методами с ней бороться? Давайте разбираться.

HPV-инфекция у женщин – что это?
HPV на латыни обозначает название семейства вирусов: Human Papillomavirus. Сокращенная аббревиатура часто используется в медицине. Например, ее можно встретить в анализах.
Итак, если обнаружена HPV-инфекция у женщин, что это за патология? В переводе с латыни, это вирус папилломы человека (ВПЧ). Это большое семейство микроорганизмов. ВПЧ объединяет более 70 разновидностей вирусов. Они способны становиться источниками развития в организме различных заболеваний. Некоторые вирусы ВПЧ приводят к возникновению заболеваний кожи. Иные – провоцируют появление остроконечных кондилом. Сегодня медиками полностью установлена связь между наличием в организме женщины определенных видов ВПЧ и онкологией.
Данная инфекция достаточно опасна для организма. Она отличается слабовыраженной симптоматикой и при этом обладает внушительным инкубационным периодом. Поэтому ВПЧ может длительное время находиться в организме, ничем себя не выдавая. Особенно если речь идет о женщинах. Микрофлора влагалища – это благоприятная среда для вируса.
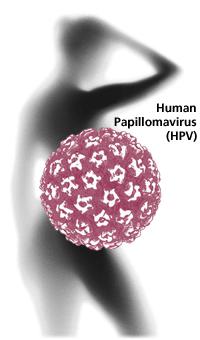
Основными особенностями HPV являются:
- латентность проявлений;
- долгий инкубационный период (иногда затягивающийся на несколько лет);
- слабовыраженная клиническая симптоматика;
- способность быстрой трансформации из папилломы в дисплазию.
Поскольку бородавки, кондиломы могут длительный период не доставлять женщине дискомфорта, патология на протяжении нескольких лет способна оставаться незамеченной. Но вы должны понимать, если выявлена HPV-инфекция у женщин, что это такое. Ведь в некоторых случаях, если своевременно не начато лечение ВПЧ, в организме развивается рак.
Согласно статистическим данным, около 70 % жителей земли инфицированы тем или иным видом ВПЧ.
Пути передачи
Существует всего 2 метода заражения ВПЧ:
- половой (наиболее распространенный);
- бытовой.
Инфекция HPV у женщин может быть спровоцирована следующими причинами:
- Половой контакт с инфицируемой особой. И даже презерватив не всегда становится достаточным средством защиты. Во время оральных ласк высок риск заражения ВПЧ.
- Процедуры в косметологическом салоне. К сожалению, на втором месте стоит именно этот путь заражения вирусом. Инфицирование происходит через недостаточно обеззараженный инструментарий. Чаще всего ВПЧ проникает в организм после процедуры перманентного макияжа либо эпиляции участка бикини. Чтобы защитить себя от риска инфекции, можно попросить продезинфицировать инструменты при вас либо требовать использования исключительно одноразовых предметов.
- Несоблюдение личной гигиены. Если средства для индивидуального туалета используются другими членами семьи, то высок риск заражения. Каждый человек должен обладать своими вещами личной гигиены. Это касается всех предметов: мочалки, полотенца, пемзы, пинцета, маникюрных ножничек.
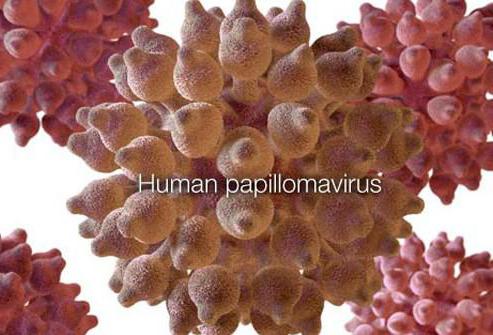
Основные причины
Таким образом, инфекция HPV у женщин чаще всего проникает именно половым путем. Однако нельзя исключать риск заражения через дружеские поцелуи, рукопожатия и даже бытовые предметы. Через небольшие повреждения кожи либо слизистой возбудитель легко проникает в организм.
А выявить на ранних сроках патологию практически невозможно. Ведь вирус может длительное время быть в наличии, но в скрытой форме. В некоторых случаях инкубационный период достигает даже до трех месяцев.
Существует несколько факторов, на фоне которых чаще всего развивается HPV-инфекция у женщин. Причины инфицирования медики приводят следующие:
- частая смена сексуальных партнеров;
- постоянный стресс;
- курение;
- авитаминоз, значительное снижение иммунитета;
- алкоголизм;
- раннее начало половой регулярной жизни;
- нарушенное протекание обменных процессов;
- болезни ЖКТ (гастрит);
- гинекологические недуги (уреаплазмоз, молочница, эрозия шейки матки, гонорея, трихомоноз, хламидиоз);
- частое посещение мест, с высоким риском заражения (бани, сауны, бассейны);
- изменения в гормональном фоне в результате употребления противозачаточных препаратов.
Типы вируса
В семейство ВПЧ входит множество разновидностей вирусов. Именно от вида микроорганизма зависит, как будет проявляться HPV-инфекция у женщин.
Типы вируса классифицируют следующим образом:
- ВПЧ, лежащие в основе появления бородавок. Типы от 1-го до 4-го приводят к образованию подошвенных бородавок. Они напоминают мозоль. Благодаря 3, 10, 28 и 49-му типу появляются плоские бородавки. А к возникновению обыкновенных образований приводит 27-й тип.
- ВПЧ, затрагивающие дыхательные пути, половые органы. В поражении данных органов виновны 6, 11, 13, 16, 18, 31, 33, 35-й типы.
- ВПЧ, которые провоцируют предраковое состояние. Это типы, обладающие высоким онкогенным риском. К данной категории относят 30, 39, 40, 42, 43, 55, 57, 61, 62, 64, 67, 69, 70-й.
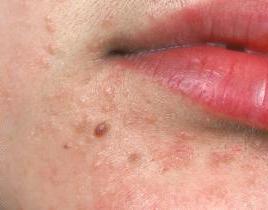
Проявления вируса
Конечно, определить тип можно только при помощи лабораторных методов исследования. Но при этом даже по внешнему виду можно заподозрить, что имеет место HPV-инфекция у женщин. Фото, приведенное в статье, показывает, с какими внешними проявлениями может столкнуться инфицированная особа.
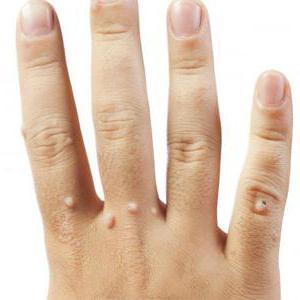
Итак, папилломавирусная инфекция может проявляться следующим образом:
Характерная симптоматика
Какими признаками может сигнализировать о себе HPV-инфекция у женщин?
Симптомы, на которые обязательно следует обратить внимание:
- появление зуда, неприятного жжения в районе половых органов;
- наличие постоянных выделений (белых, желто-зеленых, сукровичных);
- небольшое увеличение лимфоузлов;
- множественные образования (папилломы, бородавки) на разных участках тела.
При наличии даже нескольких симптомов обязательно обратитесь к гинекологу для обследования.

К чему приводит вирус?
Данная инфекция крайне опасна теми последствиями, которые она способна спровоцировать без адекватного лечения.
В некоторых случаях могут развиться следующие осложнения:
- рак головы;
- гиперплазия слизистой ротовой полости;
- рак шеи;
- папилломатоз дыхательных путей;
- онкология лёгких.
Если речь идет о половых органах, то вирус способен привести к развитию:
- онкологии шейки матки;
- дисплазии;
- раку ануса;
- онкологии влагалища или наружных органов.
Диагностика заболевания
Теперь рассмотрим, как определяется HPV-инфекция у женщин.
Диагностика подразумевает комплексный подход и включает такие мероприятия:
- Осмотр у гинеколога. Женщины должны регулярно посещать врача. Даже обычный осмотр способен помочь выявить ВПЧ.
- Кольпоскопия. Такое исследование проводится при помощи специального микроскопа. Кольпоскоп во много раз увеличивает женские органы. Это позволяет отлично рассмотреть кондиломы. Применение дополнительных веществ помогает констатировать ВПЧ.
- Цитологический мазок. Соскоб позволяет детально изучить ткани под микроскопом. Исследование дает возможность определить начальные стадии рака. Обязательно назначается данное обследование при дисплазии. Оно называется тестом Папаниколау.
- Биопсия. Маленький фрагмент ткани матки изучается под большим увеличением. Проведение биопсии категорически противопоказано беременным.
- Гистологическое исследование. Позволяет изучить строение клеток и расположение слоев. Образец ткани изначально проходит специальную подготовку и только затем тщательно анализируется.
- ПЦР. Анализ дает представление о типе вируса и позволяет определить его онкогенность.
Методы лечения
Единой программы для лечения ВПЧ не существует. Для каждого конкретного случая подбирается своя терапия. При этом даже комплексное лечение не способно полностью избавить пациента от данного недуга.
Терапия остроконечных кондилом
Основной способ борьбы – механическое удаление. Какие же методы наиболее эффективны, если диагностируется HPV-инфекция у женщин? Описание процедуры, приведенное к каждому способу, позволит понять суть данного вмешательства.
Итак, для терапии остроконечных кондилом предпринимаются:
- Лазеротерапия. Дефекты удаляют под местной анестезией. Процедура производится лазером.
- Криодеструкция. Неприятные дефекты удаляются при помощи жидкого азота. Процедура совершенно безболезненна и не оставляет после себя рубцов.
- Электрокоагуляция. Терапия производится при помощи электрического тока. Метод достаточно болезненный.
- Радиоволновая коагуляция. Процедура обладает отличным лечебным результатом, проводится под местным обезболиванием. Кондиломы удаляют при помощи радиоволнового ножа.
- Хирургическое удаление. Крайне редкий метод лечения. Используется только при озлокачествлении тканей.
Противовирусная терапия папилломавирусной инфекции
Специального лечения не разработано. Поэтому пациенту назначают противовирусные средства, стимулирующие иммунитет:
Однако ни один из перечисленных выше препаратов не способен полностью излечить от инфекции.
Профилактика папилломавирусной инфекции
Эта тема сегодня крайне актуальна. Не забывайте, что к раку шейки матки может привести именно HPV-инфекция у женщин.
Методы профилактики включают:
- неспецифические способы;
- специфические.
В первом случае речь идет о половом воспитании подрастающего поколения. Очень важно объяснить, как защитить организм и какими способами передается HPV-инфекция у женщин.
Профилактика специфическая – это вакцинирование, направленное на защиту от самых онкогенных типов вируса. Сформированный после прививки стойкий иммунитет позволяет защитить женщину от рака. Подобная вакцинация рекомендована девушкам до начала половой жизни.
Самими эффективными и признанными во всем мире вакцинами против ВПЧ являются:
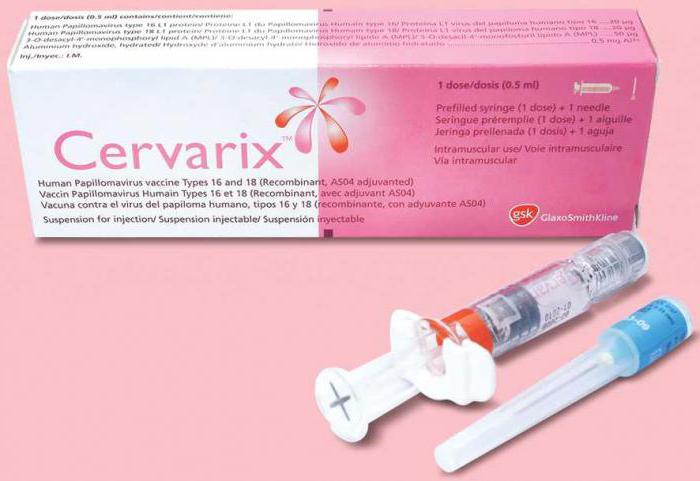
Данные прививки делают и в том случае, если женщина уже ведет половую жизнь. Однако перед вакцинацией ей необходимо пройти назначенное доктором обследование для исключения вероятности наличия в организме ВПЧ.
[youtube.player]Аннотация научной статьи по клинической медицине, автор научной работы — Ершов В. А., Вязовая А. А., Нарвская О. В., Лялина Л. В., Лисянская А. С.
Цитологическими признаками поражения эпителия шейки матки при папилломавирусной инфекции у 16% пациенток являлось наличие койлоцитоза и дискератоза, у 46% — атипия многоядерных клеток типа парабазальных с дистрофическими изменениями ядра и/или цитоплазмы. Повреждение плоского эпителия шейки матки высокой степени (HSIL) сопровождалось, как правило, присутствием ВПЧ 16-го типа в сочетании с ВПЧ других генотипов.
Похожие темы научных работ по клинической медицине , автор научной работы — Ершов В. А., Вязовая А. А., Нарвская О. В., Лялина Л. В., Лисянская А. С.
CERVICAL SQUAMOUS EPITHELIUM LESIONS ASSOCIATED WITH HUMAN PAPILLOMAVIRUS INFECTION
The cytological evidence of cervical squamous epithelium lesions associated with HPV infection was identified as the presence of koilocytes in 16% of patients and atypical multicore cells with core and/or cytoplasm dystrophy of para-basal layer cells in 46%. The high grade squamous intraepithelial lesions were associated with the presence of HPV 16 mostly in combination with other high risk HPV genotypes.
Инфекция и иммунитет 2013, Т. 3, № 1, с. 79-82
ЭПИТЕЛИЯ ШЕЙКИ МАТКИ
ПРИ ПАПИЛЛОМАВИРУСНОЙ ИНФЕКЦИИ
В.А. Ершов1, А.А. Вязовая2, О.В. Нарвская2, Л.В. Лялина2, А.С. Лисянская1
1 СПб ГУЗ Городской клинический онкологический диспансер, Санкт-Петербург
2 ФБУН НИИ эпидемиологии и микробиологии имени Пастера, Санкт-Петербург
Резюме. Цитологическими признаками поражения эпителия шейки матки при папилломавирусной инфекции у 16% пациенток являлось наличие койлоцитоза и дискератоза, у 46% — атипия многоядерных клеток типа парабазальных с дистрофическими изменениями ядра и/или цитоплазмы. Повреждение плоского эпителия шейки матки высокой степени (HSIL) сопровождалось, как правило, присутствием ВПЧ 16-го типа в сочетании с ВПЧ других генотипов.
Ключевые слова: цервикальная интраэпителиальная неоплазия, вирус папилломы человека, койлоцитоз.
CERVICAL SQUAMOUS EPITHELIUM LESIONS ASSOCIATED WITH HUMAN PAPILLOMAVIRUS INFECTION
£rshov V.A., Vyazovaya A.A., Narvskaya O.V., Lyalina L.V., Lisyanskaya A.S.
Abstract. The cytological evidence of cervical squamous epithelium lesions associated with HPV infection was identified as the presence of koilocytes in 16% of patients and atypical multicore cells with core and/or cytoplasm dystrophy of para-basal layer cells in 46%. The high grade squamous intraepithelial lesions were associated with the presence of HPV 16 mostly in combination with other high risk HPV genotypes. (Infekc. immun., 2013, vol. 3, N 1, p. 79-82)
Key words: cervical intraepithelial neoplasia, human papillomavirus, koilocytes.
Рак шейки матки (РШМ) занимает одно из ведущих мест в структуре онкологической заболеваемости женщин репродуктивного возраста в России и в мире [2, 3, 4]. Эпидемиологическими и молекулярно-генетическими исследованиями доказано, что этиология и патогенез заболевания связаны с персистенцией в церви-кальном эпителии вируса папилломы человека высокого канцерогенного риска (ВПЧ ВКР) следующих генотипов: 16, 18, 31, 33, 35, 39, 45, 51, 52, 56, 58, 59 [4, 6, 8, 10, 11].
Развитию РШМ предшествуют морфологические изменения эпителия — цервикальная интраэпителиальная неоплазия (англ. cervical intraepithelial neoplasia, CIN), часто именуемая дисплазией согласно отечественной терминологии. При этом CIN I соответствует легкой (слабой) дисплазии, CIN II — умеренной (средней степени тяжести) дисплазии, CIN III — тяжелой
Основными цитологическими признаками повреждения многослойного плоского эпителия шейки матки папилломавирусами считают наличие койлоцитов, в том числе многоядерных, и клеток с дистрофическими изменениями цитоплазмы. Койлоциты — это клетки с разной степенью изменения ядра и перинуклеарной вакуолизацией. Второй тип клеток, обнаруживаемых наряду с койлоцитами, дискерато-циты — клетки многослойного плоского эпи-
поступила в редакцию 05.07.2012 отправлена на доработку 16.07.2012 принята к печати 21.08.2012
Адрес для переписки:
Вязовая Анна Александровна, старший научный сотрудник лаборатории молекулярной микробилогии ФБУН НИИЭМ имени Пастера
197101, Санкт-Петербург, ул. Мира, 14, ФБУН НИИЭМ имени Пастера. Тел.: (812) 233-21-49. E-mail: elmtree2011@mail.ru
телия, небольших размеров с гиперхромными ядрами различной величины, с различной степенью ороговения цитоплазмы за счет накопления кератина. Отмечено, что по мере прогрес-сирования интраэпителиального повреждения количество койлоцитов может уменьшаться, что сопровождается нарастанием дискератоза, дискариоза и появлением патологических митозов [1, 5, 14].
Целью нашего исследования явилась характеристика клеточных изменений при HSIL и плоскоклеточном раке шейки матки, ассоциированных с присутствием ВПЧ ВКР.
Материалы и методы
Проанализированы результаты цитологических и гистологических исследований материала из шейки матки 140 женщин (20—29 лет — 27, 30-39 лет — 68, 40-49 лет — 34, 50-59 лет — 8, старше 60 — 3 человека), находившихся на лечении по поводу неоплазии шейки матки в Санкт-Петербургском Городском клиническом онкологическом диспансере в 2006-2007 гг.
В предоперационном периоде из соскобов влагалищной части шейки матки и цервикаль-ного канала готовили цитологические препараты, окрашивали их по методу Папаниколау. Результаты цитологического исследования оценивали в соответствии с отечественной цитологической классификацией и терминологической системой Бетесда [7, 9].
Материал для гистологического исследования получали при электроэксцизии шейки матки; препараты готовили по стандартной методике и окрашивали гематоксилином и эозином. Гистологические заключения формулировали в соответствии с международной гистологической классификацией [13].
При цитологическом исследовании образцов материала из шейки матки, полученных от 140 пациенток в предоперационном периоде, выявлено интраэпителиальное повреждение плоского эпителия высокой степени (HSIL). При гистологическом исследовании операционного материала этих пациенток у 49 (35%), 77 (55%) и 14 (10%) из них выявлены CIN II, CIN III и плоскоклеточный рак соответственно.
В 18 случаях CIN II (37%) цитологическую картину HSIL дополняли клетки типа параба-зальных (ПБК) округлой формы с дистрофическими изменениями ядра и/или цитоплазмы. Ядра в 43% клеток были гиперхромные с глыб-чатым хроматином, в 57% — гипохромные с тяжистым хроматином. В 24% клеток видны от двух до пяти ядер, преимущественно сгруппированных в плотные конгломераты. В некоторых клетках отмечены единичные вакуоли в гипохромных ядрах и митозы. В цитоплазме большинства клеток (71%) наблюдали крупную или несколько мелких вакуолей, оттесняющих ядро к одному из краев клетки.
В 56 (73%) из 77 случаев CIN III в цитологических препаратах наблюдали атипичные клетки, среди которых в 16 (21%) образцах выявлены койлоциты, в том числе 2-7-ядерные, и диске-ратоциты. В 40 случаях цитологическую картину HSIL дополняли атипичные клетки типа ПБК с дистрофическими изменениями ядра и/или цитоплазмы (табл.). Ядра гипер- или гипохромные неправильно округлой и уродливой формы занимали практически весь объем клетки. В 16% случаев ядра имели вытянутую палочковидную или серповидную формы и были смещены к одному из краев клетки. Хроматин, смазанный по рисунку, в 73% клеток был расположен мелкими глыбками, в 27% — параллельными тяжами. Каждая третья клетка в препаратах содержала более двух ядер, преимущественно скомпонованных в конгломераты. Митозы (в том числе, патологические) отмечены в единичных клетках. В ядрах 40% клеток выявлены округлые оптически пустые вакуоли, в 20% — мелкие периферические участки, напоминающие по плотности и окраске участки окружающей ядро цитоплазмы. Цитоплазма в 56% клеток была гомогенной, в 44% — с выраженной мелковакуольной дистрофией.
Методом ПЦР выборочно исследованы со-скобы со стекол 25 (45%) из 56 цитологических препаратов HSIL/CIN III. Во всех случаях подтверждено присутствие ВПЧ 16-го генотипа,
Цитологические признаки папилломавирусной инфекции
ТАБЛИЦА. ЦИТОЛОГИЧЕСКИЕ ПРИЗНАКИ ПОРАЖЕНИЯ ПЛОСКОГО ЭПИТЕЛИЯ ШЕИКИ МАТКИ ПАПИЛЛОМАВИРУСАМИ
Результаты гистологического исследования Цитологические признаки поражения эпителия шейки матки ВПЧ
койлоциты, многоядерные клетки, дискератоциты парабазальные клетки
CIN II (n = 49) 4 18
CIN III (n = 77) 16 40
Плоскоклеточный рак (n = 14) 2 5
причем в 17 (68%) из 25 случаев — в сочетании с одним (31, 33, 52, 58) или какими-либо двумя-тремя генотипами ВПЧ (18, 31, 33, 52, 58).
У больных плоскоклеточным раком шейки матки в двух случаях (14%) в цитологических препаратах среди опухолевых клеток были видны единичные крупных размеров дискерато-циты с избыточным накоплением кератинов, вплоть до патологического ороговения; в пяти случаях (36%) — атипичные клетки типа ПБК с мелковакуольной дистрофией ядра и/или мелко- или крупновакуольной дистрофией цитоплазмы (табл.).
Методом ПЦР в соскобах со стекол шести из семи упомянутых цитологических препаратов определены различные комбинации следующих генотипов ВПЧ: 16, 18, 31, 33, 39. Так, сочетания 16-го с 31-м и 33-м генотипами ВПЧ обнаружены в одном и трех случаях соответственно. Присутствие ВПЧ 16-, 31- и 18-го и 16-, 31- и 39-го генотипов выявлено в двух из семи случаев. В одном образце выявлен лишь один 31-й генотип ВПЧ.
В контрольных образцах (цитологические препараты без признаков повреждения плоского эпителия и соскобы из шейки матки 12 клинически здоровых женщин) присутствие ДНК ВПЧ ВКР не выявлено.
Повреждение плоского эпителия высокой степени (ИБ1Ь), выявленное при цитологическом исследовании образцов материала из шейки матки 140 женщин в предоперационном периоде, в 60% случаев сопровождалось цитологическими признаками поражения клеток эпителия ВПЧ. При этом в 16% случаев выявлены койлоцитоз и дискератоз, в 46% — ати-пия многоядерных клеток типа парабазальных с дистрофическими изменениями ядра и/или цитоплазмы.
Методом ПЦР во всех 33 изученных цитологических препаратах ИБ1Ь с признаками поражения клеток эпителия папилломавируса-ми подтверждено присутствие ДНК ВПЧ 16-го типа (за исключением одного образца, где обнаружена лишь ДНК ВПЧ 31-го типа), как правило в сочетании с одним или несколькими генотипами ВПЧ ВКР (18, 31, 33, 39, 52, 58). Определение генотипа ВПЧ важно для прогноза течения
папилломавирусной инфекции. Так, считается, что выявление нескольких генотипов вируса ассоциировано с более длительным носитель-ством. С другой стороны, известно, что перси-стенция ВПЧ 16-го типа является фактором риска малигнизации [2, 5, 6, 7, 10].
Поскольку метод ПЦР позволяет выявлять и идентифицировать ВПЧ ВКР задолго до появления первых цитологических, и тем более — клинических признаков заболевания, скрининг женщин на носительство онкоген-ных ВПЧ будет способствовать профилактике злокачественных новообразований, ассоциированных с хронической папилломавирусной инфекцией.
2. Киселев В.И. Вирусы папилломы человека в развитии рака шейки матки. — М.: Димитрейд График Групп, 2004. — 184 с.
3. Лялина Л.В., Носков Ф.С., Жебрун А.Б., Нарвская О.В. Организация и проведение скрининга на наличие онкогенных вирусов папилломы человека в целях профилактики злокачественных новообразований органов репродуктивной системы: Методические рекомендации. — СПб., 2005. — 28 с.
4. Прилепская В.Н., Роговская С.И., Межевинеа-нова Е.Л. Кольпоскопия: Практическое руководство. — М.: Медицинское информационное агентство, 2001. — 100 с.
5. Роговская С.И., Прилепская В.Н. Профилактика папилломавирусной инфекции и рака шейки матки // Гинекология. — 2005. — Т. 5, № 1. — С. 22-26.
6. Уразова Л.Н., Видяева И.Г. Рак шейки матки и вирусы папилломы: этиопатогенетические аспекты // Сибирский онкологич. журн. — 2009. — № 1 (31) — C. 64-71.
7. Apgar В., Zoschnick L., Wright J. The 2001 Bethes-da system terminology American family physician // American family physician. — 2003. — Vol. 68, N 15. — P. 1992-1998.
8. Bosch F.X., Munoz N. The viral etiology of cervical cancer // Virus Res. — 2002. — Vol. 89. — P. 183-190.
9. Evans M.F., Adamson C.S., Papillo J.L., St. John T.L., Leiman G., Cooper K. Distribution of human papillo-
mavirus types in ThinPrep Papanicolaou tests classified according to the Bethesda 2001 terminology and correlations with patient age and biopsy outcomes // Cancer. — 2006. — Vol. 106, N 5. — P. 1054-1064.
10. Hausen H. Papillomaviruses and cancer: from basic studies to clinical application // Nat. Rev. Cancer. — 2002. — Vol. 2, N 5. — P. 342-350.
11. Herrington CS. Does HPV testing have a role in primary cervical creening? // Cytopathology. — 2001. — Vol. 12, N 2. — P. 71-74.
12. Holowaty P., Miller A.B., Rohan T., To T. Natural history of dysplasia of the uterine cervix // J. Natl Cancer Inst. — 1999. — Vol. 91, N 3. — P. 252-258.
13. Pathology and genetics of tumours of the breast and female genital organs. WHO classification of tumours / Eds. F.A. Tavassoli, P. Devilee. — Lyon: IARC Press, 2003. — 432 p.
14. Jenkins D. Histopathology and cytopathology of cervical cancer // Dis. Markers. — 2007. — Vol. 23. — P. 199-212.
[youtube.player]Читайте также:


