Инфекционный эндокардит научная работа

Инфекционный эндокардит (ИЭ) – грозное заболевание, характеризующееся крайне неблагоприятным прогнозом при естественном его течении. Анализируя литературные данные, можно отметить, что частота ИЭ в Российской Федерации имеет сравнительно высокие показатели распространенности по отношению к другим странам; так, в расчете на 1 млн населения заболеваемость ИЭ составляет: в США 38-92,9 человека, в Канаде – 20-25, в Швеции – 59, Англии – 23-25, Франции – 18-23, Германии и Италии – 16. В России заболеваемость ИЭ достигает 46,3 человека на 1 млн населения [1]. Особую активность проблема данного заболевания приобретает в связи с неуклонным ростом ИЭ интактных клапанов в течение последних десятилетий на фоне общего роста заболеваемости инфекционным эндокардитом в 3-4 раза 3.
Диагностика ИЭ представляет значительные затруднения в связи с ярко выраженным полиморфизмом клиники, широким спектром возбудителей и ростом доли полимикробной инфекции в генезе ИЭ [5]. На ранних этапах заболевание не имеет специфических диагностических признаков. Так, клиническая картина подострого ИЭ характеризуется преобладанием и нарастанием общей астеновегетативной симптоматики на фоне лихорадки и в некоторых случаях миалгии, а острая форма инфекционного эндокардита может манифестировать уже с осложнений в виде отрыва вегетаций и эмболии органов. Результаты лабораторной диагностики также не позволяют врачу-клиницисту заподозрить данное заболевание, так как у пациента будут отмечаться анемия, лейкоцитоз и ускорение скорости оседания эритроцитов (СОЭ), в общем анализе мочи может быть микрогематурия и протеинурия [6; 7]. Доказана чувствительность С-реактивного белка (СРБ) при диагностике ИЭ, но данный воспалительный маркер специфичен для целого ряда воспалительных заболеваний [8].
Даже несмотря на технические достижения современной медицины, постановка диагноза ИЭ во многих случаях значительно растягивается во времени, что, вероятно, связано с небольшим числом работ, описывающих клинико-эпидемиологические характеристики инфекционного эндокардита на современном этапе [9].
Целью нашей работы явилось изучение структуры заболеваемости, основных особенностей клинической и лабораторно-инструментальной картины, вариантов поражения клапанного аппарата, а также осложнений ИЭ.
Результаты и их обсуждение. За исследуемый период времени наблюдается увеличение числа пациентов с ИЭ (рис. 1), что хорошо согласуется с данными общемировой статистики [1].
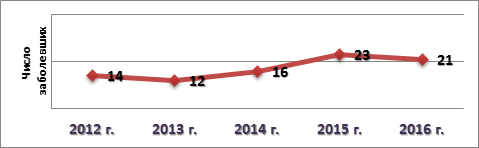
Рис. 1. Случаи выявления ИЭ в период за 2012-2016 гг.
Анализ половой структуры заболеваемости показывает, что мужчины болеют в 3 раза чаще, чем женщины (Z=2,137880, p-level=0,032527), составляя при этом 64% от общего числа.
Результаты анализа возрастной структуры ИЭ позволяют утверждать, что большинство страдающих инфекционным эндокардитом пациентов - это больные молодого и среднего возраста, при этом отмечается отчетливая тенденция к увеличению абсолютного числа пациентов молодого и среднего возраста среди всех пациентов с ИЭ (рис. 2, 3).
Далее нами были проанализированы особенности течения ИЭ по клиническим вариантам: острая форма наблюдалась лишь в 7 клинических случаях (8,14%), подострая – у 91,86% пациентов с ИЭ.
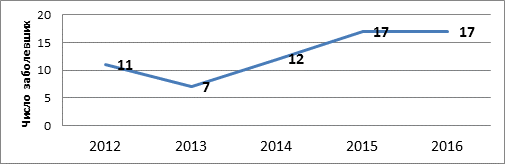
Рис. 2. Динамика заболеваемости ИЭ пациентов молодого и среднего возраста
в период с 2012 по 2016 г.
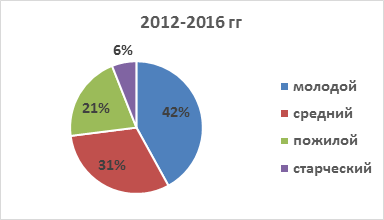
Рис. 3. Возрастная структура пациентов с ИЭ
Анализ поражений клапанного аппарата выявил следующие морфологические варианты инфекционного эндокардита: первичный ИЭ естественных клапанов – 66,27%, вторичный ИЭ естественных клапанов – 15,12%, ранний ИЭ протеза клапанов – 11,63% и поздний ИЭ протеза клапанов в 6,98% случаев.
Среди случаев ИЭ естественных клапанов преобладает эндокардит левых отделов – 65,11%. Сочетанное поражение трикуспидального клапана (ТК) и митрального клапана (МК) наблюдалось в 4,65% случаев в результате сообщения правой и левой полостей сердца вследствие образования абсцессов. Эндокардит правых отделов сердца был выявлен у 33,24% пациентов.
Анализируя случаи эндокардита правых отделов сердца, можно отметить неуклонный рост числа больных с данным видом поражения клапанного аппарата в период с 2013 по 2016 год (рис. 4).
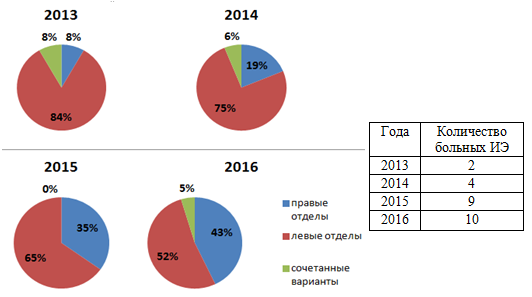
Рис. 4. Рост абсолютного числа больных с эндокардитом правых отделов сердца
Среди наиболее распространенных осложнений ИЭ у пациентов с эндокардитом правых отделов сердца можно отметить: пневмонию, экссудативный перикардит, абсцесс легкого, асцит, гидроторакс, нефритический синдром с явлениями почечной недостаточности.
При этом тяжелая почечная недостаточность с максимальным повышением креатинина до 671 мкмоль/л отмечалась лишь у пациентов с поражением митрального и аортального клапанов.
Среди эндокардита левых отделов характерны осложнения в виде левожелудочковой сердечной недостаточности, нефритического синдрома с развитием почечной недостаточности, экссудативного перикардита, гидроторакса.
Анемия была типичным осложнением как при поражении правых, так и левых отделов, встречаясь в 16,3% случаев.
Эмболические осложнения наблюдались у 8 пациентов, что составило 9% от общего числа. При ИЭ левых отделов сердца у больных развился эмболический инфаркт селезенки в одном случае, а в другом – эмболизация сосудов головного мозга, почек и сердца. При поражении трикуспидального и легочного клапанов в 6 случаях (7% от общего количества больных ИЭ) закономерно развилась тромбоэмболия мелких ветвей легочной артерии.
Проанализировав клиническую симптоматику, можно выявить следующие ведущие симптомы инфекционного эндокардита: одышка в 73% случаев, лихорадка – 72%, астения – 64%, отеки нижних конечностей – 31%, кардиалгия – 30%, миалгия – 10%.
Изучив результаты диагностических методов выявления ИЭ, можно отметить низкую выявляемость положительной гемокультуры среди всех пациентов вне зависимости от формы, сроков возникновения, половозрастной группы (таблица). Положительная гемокультура встречалась только у 23% больных от общего числа, что, вероятно, свидетельствует как о необходимости совершенствования лабораторной диагностики сепсиса, так и о высокой распространенности назначения антибактериальной терапии до проведения бактериологического посева крови.
Структура бактериологически подтвержденных возбудителей ИЭ
*Enterococcus faecium, Klebsiella pneumoniae, Stenotrophomonas maltophilia
Варианты положительной гемокультуры
Анализируя данные лабораторной диагностики, отмечаем повышение СОЭ свыше 20 мм/ч у 57 больных – 67% от общего количества больных, и свыше 40 мм/ч в 27% случаев. Вместе с тем 21% больных имели уровень СОЭ в пределах нормальных значений. В работе [5] Тюрина В.П. и Гогина Е.Е. в качестве одного из патогномоничных симптомов отмечено ускорение СОЭ в 97% случаев у пациентов с ИЭ, что противоречит полученным нами данным. Таким образом, ИЭ не всегда сопровождается увеличением СОЭ (рис. 5).
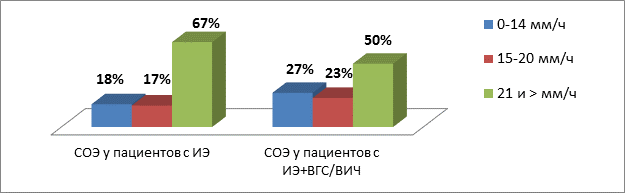
Рис. 5. Показатели СОЭ у пациентов с ИЭ
Примечание к рисунку: СОЭ – скорость оседания эритроцитов, ИЭ – инфекционный эндокардит, ВГС – вирус гепатита С, ВИЧ – вирус иммунодефицита человека
Среднее значение СРБ среди всех пациентов составило 47,99 ±10,49 мг/л. СРБ оставался в пределах нормальных значений (за норму принимали диапазон от 0 до 5 мг/л) у 17,65% пациентов, для большинства пациентов характерно повышение СРБ свыше 10 и более мг/л (76,47%). Подавляющее большинство больных имели значение СРБ свыше 30 мг/л.
Наличие нормальных значений СРБ при ИЭ, очевидно, свидетельствует о крайне низкой реактивности организма. Среди всех пациентов с нормальными значениями СРБ нам встретился лишь 1 пациент в возрасте 46 лет с ИЭ левых отделов сердца. При этом нормальные значения СРБ наблюдались у двух пациентов старческого возраста и 3 больных с ИЭ правых отделов сердца. В первом случае низкая реактивность обусловлена снижением иммунного ответа, связанным с возрастом. Во втором случае – нормальные значения СРБ обусловлены угнетением иммунитета, вероятнее всего, вследствие внутривенной наркомании, определенный вклад в снижение реактивности иммунитета, несомненно, вносит вирусный гепатит С (ВГС). Два из трех пациентов с эндокардитом правых отделов сердца, имевших нормальный уровень СРБ, страдали вирусным гепатитом С.
В целом проанализировать вклад вирусного гепатита С и ВИЧ в ареактивность пациентов с ИЭ практически невозможно, так как значения СРБ у таких больных варьируют в крайне широком диапазоне: от нормальных до крайне экстремальных значений (166, 177 и даже 298 мг/л). Однако при анализе значения СОЭ у пациентов с ИЭ выявляется отчетливая тенденция к более низким значениям СОЭ (рис. 5) у пациентов, страдающих ВГС/ВИЧ, приближающаяся к статистической достоверности (Z=1,676; P=0,09). Вышеописанные изменения СОЭ, вероятно, подтверждают мысль о роли ВГС и ВИЧ в снижении иммунной реактивности организма пациентов с ИЭ.
Необходимо отметить, что в исследовании ряда авторов под руководством Hogevik H., Olaison L. было также установлено, что СОЭ является менее чувствительным показателем по отношению к СРБ, так как нормальные значения СОЭ наблюдались в 28% случаев, в то время когда уровень СРБ был в норме лишь у 4%. В работе также отмечено, что ИЭ стафилококкового происхождения с коротким периодом клинической симптоматики коррелируют с более высокими уровнями СРБ [8].
Таким образом, полученные результаты позволяют отметить, что наблюдающийся рост заболеваемости ИЭ в период за 2012-2016 годы связан с увеличением поражения числа лиц молодого и среднего возраста.
Значительная доля и увеличение числа больных с поражением правых отделов сердца свидетельствуют о том, что вышеуказанные изменения заболеваемости связаны с вероятным распространением внутривенной наркомании.
Таким образом, к 2015-2016 году сформировалось характерное клиническое лицо пациента с ИЭ: молодой больной, чаще мужского пола, с длительным лихорадочным синдромом, проявлениями общей интоксикации, симптомами правожелудочковой сердечной недостаточности в сочетании с инфаркт-пневмонией легкого или деструктивными поражениями легочной ткани.
Согласно анамнестическим данным, проведение посевов крови в большинстве случаев предшествовало проведению антибиотикотерапии, что закономерно привело к значительному снижению лиц с положительной гемокультурой. Выявлен крайне низкий процент высевания микроорганизмов возбудителей ИЭ. Полученные данные убедительно свидетельствуют о первостепенности клинической и инструментальной диагностики (ЭхоКГ, ЧПЭхоКГ). Методы бактериальной диагностики в большинстве случаев имеют вторичное значение в подтверждении диагноза, но играют определяющую роль при выборе антибиотикотерапии в случае выявления положительной гемокультуры у пациента. Отсутствие воспалительной активности в анализах крови при яркой клинической картине ИЭ и положительного результата посева гемокультуры не должно вводить в заблуждение лечащего врача.

Дата публикации: 19.05.2016 2016-05-19
Статья просмотрена: 311 раз
В современной клинической практике проблема инфекционного эндокардитастоит достаточно остро. Это обусловлено довольно высокой заболеваемостью, выраженным клиническим полиморфизмом, нарастанием числа атипичных форм, повышением удельного веса возбудителей, резистентных к антибактериальной терапии [2, 4].
По данным литературы заболеваемость ИЭ у взрослых составляет 1,7–6,5:100.000 населения в год [1], у подростков — более низкая, и составляет 3,0–4,3:1 млн. населения в год [3]. В то же время по данным, поступающим из крупных медицинских центров Европы и США, удельный вес ИЭ среди детей и подростков в специализированных стационарах постепенно нарастает, что связывают с увеличением числа операций на сердце при врожденных пороках, постоянным расширением спектра инвазивных диагностических и лечебных медицинских манипуляций, а также распространением внутривенной наркомании [4]. При этом мальчики заболевают эндокардитом в 2–3 раза чаще, чем девочки. Среди всех случаев эндокардита инфекционный генез составляет 25–40 % [3].
Недостаточная изученность патогенетических механизмов и клинических проявлений ИЭ у детей в зависимости от вариантов течения являются причиной поздней диагностики и заболевания [1].
Целью исследования явилось изучениеклинических, лабораторных и инструментальных методов исследования, инфекционного эндокардита у детей в современных условиях.
Материалы иметоды исследования.
Исследование проводилось при кафедре Госпитальной педиатрии № 2 на базе клиники ТашПМИ. В исследование были включены 8 детей с установленным диагнозом Инфекционный эндокардит, находившихся на лечении с 2013 по 2016гг, и проведён ретроспективный анализ 12 историй болезни детей с диагнозом Инфекционный эндокардит за период с 2010 по 2016гг. Всем детям проводился комплекс клинико-лабораторных исследований включающий в себя посев крови на стерильность, при анализе результатов которого определились нижеследующие результаты.
Результаты иих обсуждение. Наиболее опасным возбудителем ИЭ является S. Aureus. В последние годы его роль как лидирующего возбудителя ИЭ в отдельных регионах возрастает: этот микроорганизм является возбудителем ИЭ не менее чем в 40 % случаев. S. epidermidis встречается реже в 5 раз, чем S. Aureus (табл. 1).
Частота основных возбудителей больных детей ИЭ
Возбудители
Частота,%
S. faecalis (энтерококк)
S. pneumoniae (пневмококк)
B — гемолитические S. spp.
Другие или смешанные
Различные виды бета — гемолитических стрептококков идентифицированы как возбудители ИЭ, наиболее частым является зеленящий стрептококк. Факторы, способствующие его инвазии: манипуляции в полости рта, хирургические вмешательства, тонзиллиты, фарингиты, синуситы. При энтерококковом эндокардите очаги инфекции чаще всего локализуются в гастроинтестинальном, гинекоуринальном трактах, а также в полости рта — парадонтоз. ИЭ, вызываемый Strep. Bovis, развивается на фоне патологии кишечника, нередко осложняет опухолевые процессы в кишечнике. Анаэробные стрептококки чаще всего вызывают ИЭ, связанный с хирургическими операциями, в том числе и с протезированием клапанов.
Развитию грибковых эндокардитов могут предшествовать длительное лечение антибиотиками, глюкокортикоидами, сахарный диабет, внутривенное введение глюкозы, кардиохирургические вмешательства.
Из грамположительных микроорганизмов заслуживают внимания факультативные анаэробы — листерия, дифтероиды, лактобациллы, стрептобациллы, актинобациллы и др. эта группа вызывает эндокардиты протезов клапанов.
Таким образом,положительная гемокультура у больных с инфекционным эндокардитом выявлена в 40 %, из них: грам (+) флора в 69,6 %, грам (-) флора в 26,8 %, грибы рода Кандида в 3 %. Клинико-лабораторные септические и иммунокомплексные проявления при ИЭ, вызванные золотистым стафилококком и зеленящим стрептококком, предопределяют прогноз заболевания и ассоциируются с острым и подострым вариантами ИЭ. При ИЭ, вызванном грам (-) флорой, наблюдается высокий процент тромбоэмболических осложнений (33,3 %) и иммунокомплексных изменений (нефрит, полиартрит, геморрагический васкулит), которые ассоциируются с затяжным вариантом заболевания.
При анализе предрасполагающих факторов развития инфекционного эндокардита у детей определилось, что при ВПС риск развития ИЭ во многом зависит от характера анатомического дефекта сердца и максимален у пациентов с синими пороками Фалло, дефектом межжелудочковой перегородки, при атрио–вентрикулярной коммуникации, аортальном стенозе.
В нашем исследовании у 12 детей инфекционный эндокардит развился на фоне ВПС, при этом у 50 % отмечалисьпороками Фалло, ДМЖП у 25 %, аотральный стеноз отмечался у 8 % исследуемых. Наименьший риск ИЭ имеют пациенты с дефектом межпредсердной перегородки, открытым артериальным протоком.
Выявлены клинико-лабораторные особенности вторичного ИЭ: на фоне ВПС отмечался в 60 %, при врожденных пороках сердца: у половины больных ИЭ проявлялся гломерулонефритом, у трети — миокардитом, у четверти больных- суставным синдромом, на фоне ревматизма ИЭ определился в 33 % случаях и проявлялся наличием в 50 % постоянной формы фибрилляции предсердий, в 30 %- тромбоэмболических осложнений, в основном за счет ЗСН. При ИЭ на фоне дисплазии соединительной ткани при ПМК проявлялся в основном иммунокомплексными поражениями, а при двустворчатом аортальном клапане- умеренным септическим синдромом. Факторами риска неблагоприятного прогноза развития вторичного ИЭ являются: при ревматизме- митрально-аортальные пороки сердца, фибрилляция предсердий; врожденных пороках сердца- пороки сердца синего типа, возникновение ИЭ после перенесенных реконструктивных операций.
Клиническая симптоматика ИЭ появляется в основном через 2 недели с момента возникновения бактериемии. Наиболее ранний и частый симптом заболевания — лихорадка (в большинстве случаев — неправильного типа) с ознобом различной выраженности 100 % и последующим профузным потоотделением 80 % случаях. Характерны быстрая утомляемость, нарастающая слабость, анорексия и потеря веса в 60 %. Нередки распространенные артралгии и миалгии, головные боли, боли в сердце 50 %, носовые кровотечения 20 % (рис. 1).
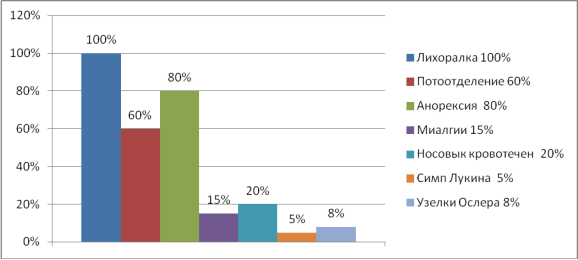
Рис.1. Клиническая симптоматика ИЭ
Основным клиническим синдромом заболевания является эндокардит с быстрым развитием клапанной регургитации (преимущественно — аортальной) при локализации процесса на нативных (естественных) клапанах. При современном ИЭ у детей и подростков наблюдается тенденция к учащению поражения митрального и трикуспидального клапанов, а также клапанов легочной артерии как в отдельности, так и в виде поливальвулярной патологии.
При клиническом исследовании особое внимание уделяется не только однократно фиксируемой аускультативной картине, но и ее динамике. В частности, в дебюте поражения первоначально не измененного аортального клапана может быть выслушан систолический шум по левому краю грудины, вероятно, обусловленный стенозированием устья аорты за счет вегетаций на полулунных клапанах. В дальнейшем появляется нежный протодиастолический шум в V точке с усилением при наклоне тела больного вперед; по мере усугубления клапанной деструкции интенсивность и продолжительность шума нарастает, отмечается ослабление II тона на аорте и снижение диастолического артериального давления.
Заключение. Таким образом,проведена углубленная оценка инфекционного эндокардита с клинико-лабораторных позиций на фоне ревматизма, врожденных пороков сердца, ИБС, дисплазии соединительной ткани сердца и выявлены факторы риска неблагоприятного прогноза. Оценены новые формы инфекционного эндокардита: нозокомиальные и правосердечные. Показана значимость иммунокомплексных и аутоиммунных реакций в развитии и прогрессировании инфекционного эндокардита. Определена прогностическая значимость вспомогательных лабораторных и инструментальных методов исследования в диагностике вариантов инфекционного эндокардита.
- Самсыгина Г. А., Щербакова М. Ю. Кардиология и ревматология детского возраста. М. 2004.
- Мелехов А. В., Гендлин Г. Е., Сторожаков Г. И. Эндокардит внутривенных наркоманов. // Росс. мед. журн. — 2007: выпуск: 42–45. 3.
- Соболева М. К., Белов Б. С. Инфекционный эндокардит у детей. РМЖ. 2006. — том 14. — № 8. — С. 630–636.
- Bitar F. F., Jawdi R. A., Dbaibo G. S. et al. Paediatric infective endocarditis: 19– years experience at a tertiare care hospital in a developing country // Acta Pediatr. — 2000.– V.89.– N.4.– P. 427–430.

Цена:
Авторы работы:
Научный журнал:
Год выхода:
Карпин В.А., доктор медицинских наук, доктор философских наук, профессор
Зульфигарова Б. Т., аспирант Шувалова О.И., кандидат медицинских наук, ассистент Кузьмина Н.В., доктор медицинских наук, профессор
Добрынина И.Ю., доктор медицинских наук, профессор Нелидова Н.В., кандидат медицинских наук, доцент
Бурмасова А.В., кандидат медицинских наук, старший преподаватель Громова Г.Г., кандидат медицинских наук, старший преподаватель (Сургутский государственный университет Ханты-Мансийского автономного округа - Югры)
ИНФЕКЦИОННЫЙ ЭНДОКАРДИТ У ВНУТРИВЕННЫХ НАРКОМАНОВ: ОБЗОР
Введение. По данным официальной статистики, из года в год в мире растет число наркоманов. За последние 5 лет оно увеличилось в 4 раза. Как известно, наркомания вызывает угнетение иммунной системы и снижение резистентности организма, что приводит к частому развитию гнойно-воспалительных процессов. Широкое употребление наркотиков с использованием внутривенного пути введения привело к значительному увеличению числа постинъекционных инфекционных осложнений, нередко сопровождающихся генерализацией гнойного процесса с развитием сепсиса [23,29].
Период с середины 90-х годов ознаменовался прогрессированием новой для нас формы инфекционного эндокардита (ИЭ) - инфекционного эндокардита у внутривенных наркоманов (ИЭВН). Частота заболеваемости ИЭВН в последние годы в несколько раз превышает показатели заболеваемости ИЭ среди лиц, имеющих такие предрасполагающие факторы, как ревматизм или искусственный клапан. Среди наркоманов заболеваемость ИЭ составляет ежегодно от 2 до 5% [5,6,9,24,38]. Поданным многолетних наблюдений, 63% больных, госпитализированных по поводу ИЭ, являлись внутривенными наркоманами [12]. При внутривенном введении наркотических средств ИЭ развивается у 6,4% пациентов [18].
Каковы особенности инфекционного эндокардита инъекционных наркоманов, позволяющие выделить его в особую группу?
Этиология. Микробный пейзаж при ИЭ при многолетнем наблюдении подвергся существенной динамике. Что касается ИЭВН, то здесь авторы практически единодушны: в спектре возбудителей преобладает золотистый стафилококк - Staphylococcus aureus [2-5,8,10,1214,18,21,24,26,27,28,35,42,43]. Источником заражения чаще всего являются кожные покровы больных: многократные инъекции способствуют колонизации кожи золотистым стафилококком. Он является высокоинвазивным микроорганизмом, способным поразить неизмененный эндотелий клапана. В то же время ИЭ левых отделов сердца, как правило, имеющий в своей основе предшествующие клапанные поражения, чаще обусловлен стрептококками [5]. В группе, представленной лицами, не употреблявшими наркотики, такая закономерность от-
сутствовала - в большинстве случаев преобладали полимикробные ассоциации в различных вариантах [21]. Важной особенностью ИЭВН является высокая частота (до 85%) выявления возбудителя в посевах крови. Отрицательная гемокультура обычно свидетельствует о погрешностях в заборе или исследовании материала [12,43]. По данным [5], ИЭВН с истинно отрицательными гемокультурами является редкостью и составляет всего 5%.
Золотистый стафилококк, выделенный из крови больных ИЭ с наркотической зависимостью, в большинстве наблюдений отличался высокой вирулентностью и резистентностью к антибактериальным препаратам [15,16,26].
Патогенез. Для ИЭВН характерно поражение правых камер сердца: характерной особенностью является вовлечение в патологический процесс трикуспидального клапана, по данным разных авторов, от 46 до 86% случаев [2,12-14,17,18,20,21,28,31,37,41]. По данным [32], 61% больных изолированным ИЭ трикуспидального клапана составляли внутривенные наркоманы.
Определенную роль в патогенезе ИЭВН играет нарушение системы иммунитета при длительном употреблении наркотических средств [18].
В клинической картине ИЭВН большинство авторов выделяют два ведущих момента -острое течение и полисиндромность [5,10,13,14,17,18,26,27]. Острота и тяжесть течения заболевания очень характерны для стафилококковой инфекции [27]. Ведущие синдромы - ин-фекционно-токсический (75-92%) и тромбоэмболический (65-78%) [17,28].
Аускультативная симптоматика недостаточности трикуспидального клапана проявляется обычно на поздних стадиях заболевания. Это объясняется особенностями морфологии клапанного аппарата сердца и характером внутрисердечной гемодинамики. Размеры трикуспи-дального отверстия сравнительно велики, а давление в полости правого желудочка примерно в 5 раз меньше, чем в левом. Даже при частичном разрушении трехстворчатого клапана возникающая трикуспидальная недостаточность относительна, больные удовлетворительно переносят ее за счет компенсаторных механизмов и малого объема крови, возвращающегося в правое предсердие [2].
Миокардит у инъекционных наркоманов развивается в два раза чаще, чем у больных ИЭ, не употребляющих наркотики (78,8% против 37,2%); токсическим влиянием стафилококка объясняют нередкое развитие тяжелой дистрофии миокарда у данного контингента больных [21,26,27].
Нередким осложнением ИЭВН является диффузный гломерулонефрит, более выраженный у наркоманов. Можно полагать, что это связано с иммунологическими нарушениями, вызванными длительной наркотической интоксикацией [2,8,21]. У них также чаще встречается спленомегалия [11,24].
Эхокардиографические особенности. Эхокардиографическое исследование является краеугольным камнем диагностики ИЭВН. При возникновении лихорадки у внутривенных наркоманов физикальные и лабораторные методы исследования могут оказаться неэффективными в выявлении ИЭ. Ключевой находкой при эхокардиографическом исследовании является сочетание вегетаций с трикуспидальной регургитацией. Необходимо подчеркнуть, что в отличие от левостороннего ИЭ, где практически обязательным является не только трансторакальный, но и более информативный чрезпищеводный доступ, преимущество последнего при исследовании трехстворчатого клапана (ТК) для выявления вегетаций не столь однозначно. Обычно при трансторакальной эхокардиографии удается получить достаточно высококачественное изображение ТК, так как он расположен достаточно близко к ультразвуковому датчику. Кроме того, вегетации на ТК обычно имеют достаточно большие размеры. Это позволило некоторым авторам усомниться в целесообразности применения чрезпищеводного исследования у больных с подозрением на эндокардит правых отделов сердца [10,12,20,22,47]. Так, по данным [5], при проведении трансторакальной эхокардиографии у больных ИЭВН вегетации выявлены у 86% больных.
Сопутствующие инфекции. Вирусные гепатиты. Печень часто страдает у наркоманов с ИЭ. У больных этой группы имеет значение не только длительная наркотическая интоксикация, но и высокий риск заражения вирусными гепатитами, особенно вирусным гепатитом С [7,10,11,21,25,40,45,48,49,51-53]. Риск инфицирования этого контингента составляет 6090%, тогда как в обычных группах он не превышает 5% [5]. По данным [6], вирусный гепатит С диагностирован у 57% больных, вирусный гепатит В - у 15%, сочетание В и С - у 28%. Авторы считают, что присоединение вирусного гепатита способствует рецидивирующему течению ИЭВН. Относительная редкость вирусного гепатита В у этих больных объясняется быстрой элиминацией вируса гепатита В в присутствии вируса гепатита С [26].
ВИЧ-инфицирование. Больные ИЭ, страдающие внутривенной наркоманией, нередко инфицируются вирусом иммунодефицита человека (ВИЧ) [8,10,12,18,21,24,25,33,34]. От 40 до 97,2% больных ИЭВН являются ВИЧ-инфицированными. Преобладание ВИЧ-серопози-тивных пациентов сред
Для дальнейшего прочтения статьи необходимо приобрести полный текст. Статьи высылаются в формате PDF на указанную при оплате почту. Время доставки составляет менее 10 минут. Стоимость одной статьи — 150 рублей.
БУРМАСОВА А.В., ДОБРЫНИНА И.Ю., ЗУЛЬФИГАРОВА Б.Т., КАРПИН В.А., КУЗЬМИНА Н.В., НЕЛИДОВА Н.В., ШУВАЛОВА О.И. — 2014 г.
*Импакт фактор за 2018 г. по данным РИНЦ
Журнал входит в Перечень рецензируемых научных изданий ВАК.
Читайте в новом номере
В статье описан инфекционный эндокардит – заболевание, регистрируемое во всех странах мира независимо от климатогеографическоих зон. Приводятся характеристика патогенеза, клинических и “периферических” симптомов, течения заболевания, основные схемы антибиотикотерапии инфекционного эндокардита.
The paper describes bacterial endocarditis, a disease notified in all countries of the world irrespective of climatic and geographical zones. It characterizes the pathogenesis, clinical and “peripheral” symptoms, clinical picture of bacterial endocarditis, basic schemes of its antibiotic therapy.
Б.С. Белов Институт ревматологии РАМН (дир. акад. РАМН В.А. Насонова), Москва
B. S. BelovInstitute of Rheumatology, Russian Academy of Medical Sciences (Director V.A. Nasonova, Acad. RAMS), Moscow
И нфекционный эндокардит (ИЭ) – заболевание инфекционной природы. Возбудитель первично локализуется на клапанах сердца, пристеночном эндокарде, реже – на эндотелии аорты и крупных артерий.
Заболевание регистрируется во всех странах мира и в различных климатогеографических зонах. Заболеваемость, по данным разных авторов, составляет от 1,7 до 5,3 случая на 100 000 населения в год. Мужчины заболевают в 1,5 – 3 раза чаще женщин, а в возрастной группе старше 60 лет это соотношение достигает 8:1.
Средний возраст заболевших составляет 40 – 44 года. В последнее время отмечается четкая тенденция к нарастанию частоты заболевания в пожилом и старческом возрасте.
Этиология ИЭ связана с различными видами возбудителей.
Наряду с зеленящим стрептококком важную роль играют золотистый и белый стафилококки, энтерококки, реже – грамотрицательные микроорганизмы, патогенные грибы Aspergillus и Candida.
В отдельных случаях в качестве причинных агентов могут выступать Coxiella burnetii (возбудитель Q-лихорадки), бруцеллы, легионеллы и хламидии.
Первое важное звено патогенеза – повреждения эндотелия сердечных клапанов и пристеночного эндокарда, обусловленные врожденной или приобретенной сердечной патологией (дефект межжелудочковой перегородки, открытый артериальный проток, ревматизм, атеросклероз, пролапс митрального клапана с регургитацией, кардиомиопатия, оперированное сердце) и приводящие к формированию асептических вегетаций, состоящих из тромбоцитов и фибрина. Впоследствии во время транзиторной бактериемии, возникающей после экстракции зуба, тонзиллэктомии, родов, аборта, катетеризации мочевых путей, вскрытия абсцесса и прочих вмешательств, относящихся к области малой хирургии, а также без видимых причин происходит инфицирование тромбовегетаций с формированием бородавчатых разрастаний, разрушением клапанов и развитием эмболий. В дальнейшем уже присутствующая бактериемия ведет к стимуляции гуморального и клеточного иммунитета, запуская иммунопатологические механизмы воспаления.
| ДИАГНОСТИЧЕСКИЕ КРИТЕРИИ ИЭ ОПРЕДЕЛЕННЫЙ ИЭ Патологические критерии: микроорганизмы, выделенные из вегетаций, эмболов или миокардиальных абсцессов, или патоморфологические изменения – вегетации или абсцессы миокарда, подтвержденные гистологически. Клинические критерии: два больших критерия, или один большой и три малых критерия, или пять малых критериев. ВОЗМОЖНЫЙ ИЭ Результаты исследований согласуются с ИЭ, но для определенного ИЭ недостаточно критериев, а в отвергнутый ИЭ данные не укладываются. ОТВЕРГНУТЫЙ ИЭ Точный альтернативный диагноз. Регресс симптомов при антибиотикотерапии до 4 дней. Отсутствие патоморфологических признаков ИЭ в операционном или аутопсийном материале при антибиотикотерапии до 4 дней. Определенный диагноз ИЭ правомочен при наличии либо одного из двух патологических критериев, выявляемых при исследовании операционного или аутопсийного материала, либо определенной совокупности клинических критериев. Последние в соответствии с их диагностической значимостью подразделяются на большие и малые аналогично критериям Джонса для диагноза острой ревматической лихорадки. КЛИНИЧЕСКИЕ КРИТЕРИИ ИЭ БОЛЬШИЕ КРИТЕРИИ Положительная гемокультура: типичные для ИЭ возбудители, выделенные из двух раздельно взятых проб крови: зеленящие стрептококки (включая штаммы с измененными питательными потребностями), Streptococcus bovis, или НАСЕК-группа (Haemophilus spp, Actinobacillus actinomycetemcomitans, Cardiobacterium hominis, Eirenella spp, Kingella kingae), или внебольничные Staphylococcus aureus или энтерококки при отсутствии первичного очага, или | согласующиеся с ИЭ возбудители, выделенные из гемокультуры при соблюдении следующих условий: как минимум два положительных результата исследования проб крови, взятых с интервалом не менее 12 ч, или три положительных результата из трех, или большинство положительных результатов из четырех проб крови и более (интервал между взятием первой и последней пробы должен составлять как минимум 1 ч). Доказательства поражения эндокарда Положительные данные эхокардиографии: свежие вегетации, или абсцесс, или частичная дегисценция клапанного протеза, или вновь сформированная клапанная регургитация (нарастание или изменение имевшегося сердечного шума не учитывается). МАЛЫЕ КРИТЕРИИ Предрасположенность: кардиогенные факторы или частые внутривенные инъекции лекарств*1. Температура 38°С и выше. Сосудистые феномены: эмболии крупных артерий, инфаркт легкого, микотические аневризмы, внутричерепные кровоизлияния, геморрагии на переходной складке конъюнктивы и повреждения Джейнуэя. Иммунологические феномены: гломерулонефрит, узелки Ослера, пятна Рота *2 и ревматоидный фактор. Микробиологические данные: положительная гемокультура, не удовлетворяющая большому критерию *3 или серологическое подтверждение активной инфекции, обусловленной потенциальным возбудителем ИЭ*4. Эхокардиографические данные, согласующиеся с ИЭ, но не удовлетворяющие большому критерию *5. *1 В том числе наркомания и токсикомания. |
Патоморфологической основой болезни является полипозно-язвенный эндокардит, характеризующийся наличием обширных наложений-вегетаций на клапанных створках, пристеночном эндокарде с распространением на интиму аорты и крупных сосудов. Во многих органах развиваются межуточные воспалительные процессы, васкулиты, кровоизлияния, инфаркты, обусловленные тромбоэмболическим синдромом.
Клиническая симптоматика ИЭ развивается, как правило, спустя 2 нед с момента возникновения бактериемии. Одним из частых и наиболее ранних симптомов заболевания является лихорадка (в большинстве случаев неправильного типа), сопровождающаяся ознобом различной выраженности. В то же время температура тела может быть субфебрильной (и даже нормальной) у пожилых или истощенных пациентов, при застойной недостаточности кровообращения, печеночной и/или почечной недостаточности. Характерны значительная потливость, быстрая утомляемость, прогрессирующая слабость, анорексия, быстрая потеря массы тела (до 10 – 15 кг).
“Периферические” симптомы ИЭ, описываемые при классической клинической картине, в настоящее время встречаются значительно реже, в основном при длительном и тяжелом течении болезни у пожилых пациентов. Однако геморрагические высыпания на коже, слизистых и переходной складке конъюнктивы (симптом Лукина), узелковые плотные болезненные гиперемированные образования в подкожной клетчатке пальцев кистей или на тенаре ладоней (узелки Ослера), мелкие эритематозные высыпания на ладонях и подошвах ( повреждения Джейнуэя), несмотря на их низкую встречаемость (от 5 до 25%), по-прежнему сохраняют свою диагностическую значимость и входят в состав малых клинических критериев ИЭ.
Симптомы поражения опорно-двигательного аппарата встречаются примерно в 40 % случаев, нередко являясь начальными признаками, а иногда и опережая на несколько месяцев истинную картину ИЭ. Характерны распространенные миалгии и артралгии (реже моно- или олигоартрит) с преимущественным вовлечением плечевых, коленных и (иногда) мелких суставов кистей и стоп. Примерно в 10% случаев встречаются миозиты, тендиниты и энтезопатии. Возможно развитие септических артритов различной локализации. Наблюдается интенсивный болевой синдром в нижнем отделе спины, обусловленный развитием метастатического бактериального дисцита или позвонкового остеомиелита.
| Антибиотикотерапия ИЭ | ||
| Возбудитель | Используемые препараты и дозы | Продолжительность курса |
| Зеленящие и другие
стрептококки: высокочувствительные к пенициллину (МИК* но в то же время не набирается достаточного числа критериев для определенного ИЭ. В подобных ситуациях окончательное решение вопроса о наличии ИЭ и целесообразности проведения эмпирической антибактериальной терапии принимается лечащим врачом. 1. Durack DT, Lukes AS, Bright DK., et al. New Criteria for Diagnosis of Infective Endocarditis: Utilization of Specific Echocardiographic Findings. Am J Med 1994;96 (3):200-9. Читайте также:
 Пожалуйста, не занимайтесь самолечением!При симпотмах заболевания - обратитесь к врачу. Пожалуйста, не занимайтесь самолечением!При симпотмах заболевания - обратитесь к врачу.
| ||

