Инфекции вызванные clostridium difficile это
Бактерия Клостридиум диффициле обитает в организме каждого человека. Имеет склонность к интенсивному размножению, из-за чего становится опасной, так как приобретает патогенные свойства и вызывает определенные заболевания. Относится к облигатным анаэробам и может существовать без кислорода. Задействуется в работе важнейших процессов, таких как расщепление белков, стимуляция и тонизирование стенок кишечника.
Что представляет собой клостридиум диффициле?
- Клостридиум ботулинум, является возбудителем ботулизма;
- Клостридиум тетанум, способствует возникновению столбняка;
- Клостридиум перфриндженс, влияет на появление анаэробной инфекции;
- Клостридиум диффициле, вызывает псевдомембранный колит.
Клостридия имеет палочковидную форму. Может располагаться цепочками и попарно. Достаточно подвижна. В условиях полного отсутствия кислорода начинает интенсивно размножаться. Микробы создают споры, что дает им устойчивость к антибиотикам, нагреванию и различным препаратам для дезинфекции. Центральная спора имеет форму веретена, а та, что расположена терминально, - форму барабанных палочек.
Клостридиум диффициле вызывает диарею от антибиотиков. Обычно обитает в кишечной среде. При хорошем здоровье полезные микроорганизмы сдерживают рост этой бактерии. После использования антибиотиков полезных бактерий становится меньше, а численность Клостридиум возрастает, что может спровоцировать появление колита, стать причиной развития серьезной патологии и даже смерти человека. Особенно это касается пожилых и ослабленных болезнью пациентов.
Все разновидности клостридий формируют токсины, провоцирующие появление определенной патологии. В результате своего размножения вырабатывает токсин А и В Клостридиум диффициле. Первый называется энтеротоксином, а второй - цитотоксином. Именно они становятся причиной диареи и колита у многих людей.
Заражение инфекцией
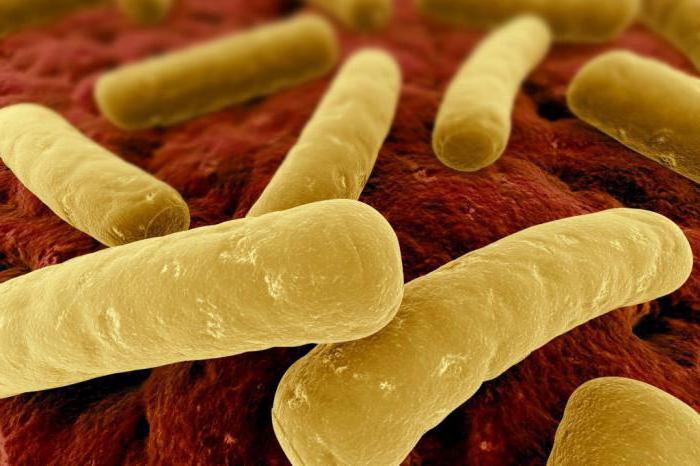
Клостридиум диффициле чаще всего обитает в больницах и домах престарелых. Может находиться где угодно: на полу, подоконниках, прикроватных столиках, в постели и туалетах. Споры микроорганизма беспрепятственно попадают на руки при соприкосновении с зараженной поверхностью. Преимущественно распространяются фекально-оральным путем.
После того как споры проникли в тело, они с легкостью проходят через среду желудка и остаются в кишечнике. В среде тонкого кишечника преобразуются в вегетативную форму и активно начинают размножаться. В толстом кишечнике бактерия оседает в кишечных складках и начинает выделять токсины А и В, в результате чего происходит тяжелое воспаление кишечной среды, что вызывает вытеснение продуктов распада и слизи. Происходит образование псевдомембран. Токсин А начинает притягивать лейкоциты, в то же время токсин В участвует в разрушительных действиях клеток эпителия. Указанные процессы провоцируют появление колита, водянистый стул и появление псевдомембран.
В основном все патологии с участием Клостридиум диффициле возникают после лечения антибиотиками, а также после операций. Особенно подвержены воздействию микроорганизмов пожилые люди после 60 лет и лица, находящиеся на продолжительном лечении в стационаре, а также пациенты, принимающие иммунодепрессивные медикаменты.
Клостридиум диффициле провоцирует слабую или умеренную диарею и незначительные спазмы желудка. Но в исключительных случаях заболевание переходит в более тяжелую форму колита. Что вызывает такие симптомы, как:
- водянистый стул;
- болевые ощущения в области живота;
- вздутие;
- повышение температуры тела;
- обезвоживание;
- тошноту.
В 3% случаев у пациентов появляется тяжелая форма болезни. Из них 30-85 % умирают. У 20-25% больных заболевание может возникать повторно. Рецидивы патологии происходят из-за тех бактерий, что остались в толстом кишечнике после терапии или из-за нового заражения Клостридиум диффициле. Заболеванием могут страдать дети, особенно ослабленные.
Болезни, вызываемые бактерией

Клостридиум диффициле в одной трети случаев провоцирует диарею, связанную с приемом антибиотиков. В остальных ситуациях на появление болезни влияют другие бактерии. Чаще всего заболевание встречается в больницах. Дети практически не страдают при этом
Анитибиотико-ассоциированная диарея (ААД) может иметь различные стадии развития, от легкого расстройства кишечника вплоть до тяжелой формы энтероколита, который называют псевдомембранозным колитом. Причиной возникновения данной патологии является инфекция, вызванная Клостридиум диффициле, которая появляется в ряде случаев из-за применения антибиотикотерапии.
Вызвать диарею или псевдомембранозный колит способен даже однократный прием антибиотика, обладающего широким спектром действия. Причем появление заболевания не зависит от дозировки и способа введения лекарственного средства.
Клостридиум диффициле: симптомы инфекции

Клостридиоз, вызванный Clostridium difficile, может протекать в следующих формах:
- бессимптомное заражение;
- легкая диарея;
- тяжелая форма развития болезни, перешедшая в псевдомембранозный колит.
ААД возникает у больных, которые прошли курс длительной терапии - более четырех недель в условиях стационара. Клостридии в кишечной среде приобретают определенную устойчивость к лекарствам. При возникновении данной патологии наличествует болезненность в околопупочной зоне, которая в дальнейшем затрагивает весь живот. Стул пациентов становится более частым, но в целом самочувствие остается удовлетворительным.
Псевдомембранозный колит, вызванный клостридиум диффициле, симптомы имеет более тяжелые. У больных появляется дисбактериоз, причем деятельность Clostridium difficile преобладает. Бактерия заселяет слизистую кишечника и производит цитотоксин и энтеротоксин. Начинается воспалительный процесс слизистой оболочки с формированием псевдомембран. При отсутствии своевременного лечения болезнь прогрессирует и дает более тяжелые осложнения. Происходит прободение стенки кишечника, что вызывает перитонит. В некоторых случаях болезнь ведет к летальному исходу.
Подобному заболеванию наиболее подвержены онкобольные, пожилые люди и пациенты, перенесшие операцию. Развитие патологии сопровождается лихорадкой, болями в животе и голове, метеоризмом, отрыжкой, рвотой. Наблюдаются и другие симптомы интоксикации организма. Больные теряют в весе, у некоторых появляется анорексия, моральная подавленность, возникает депрессия. Ещё отмечается кахексия, потуги, тенезмы, диарея с гнилостным запахом и наложением фибрина до 20 раз в сутки.
При отравлении токсинами может развиться некротический энтерит. В этом случае на стенках кишечника образуются эрозии и язвы, очаги некроза. Повышается температура тела. Возникает озноб. Наблюдается диспепсия, стул становится жидким, с примесью крови. Диагностируется гепатоспленомегалия, парез кишечника, сопровождающийся вздутием живота. Возможны кишечные кровотечения, прободение язв, а также тромбоз венул и артериол.
Часто вызывают пищевую токсикоинфекцию клостридии, в том числе Клостридиум диффициле. Клинические симптомы данного заболевания проявляются в форме отравления. Как правило, это лихорадка, боль в области живота, диарея, потеря аппетита, диспепсия. При этом заболевании проявляются все формы диспепсической и интоксикационной симптоматики. Пациенты становятся раздражительными, вялыми и беспокойными. Отрицательная симптоматика длится около 4 дней и постепенно утихает.
Основной особенностью инфекции являются рецидивы, которые проявляются в 25% случаев. Причиной их возникновения служат находящиеся в кишечной среде споры. Нельзя исключать случаи повторного заражения. Как правило, сразу после проведенной терапии наступает выздоровление, но на 2-28 сутки может развиться рецидив, схожий по своей симптоматике с начальным проявлением болезни.
Причины возникновения
При обнаружении в организме Клостридиум диффициле лечение нужно начинать незамедлительно. Причинами возникновения данной инфекции служат следующие факторы:
- плохая экология;
- стрессы, депрессия, неврозы;
- продолжительная терапия гормонами и антибиотиками;
- иммунодефицит;
- нарушение функционирования центрально-нервной системы;
- недоношенность у детей;
- бессонница, перешедшая в хроническую форму развития;
- респираторные заболевания;
- возбудители инфекций, живущие в больничных стенах;
- хирургические операции.
Указанные причины ослабляют организм и способствуют размножению Клостридиум диффициле. Лечение недуга должно проходить только после тщательной диагностики пациента.
Диагностика
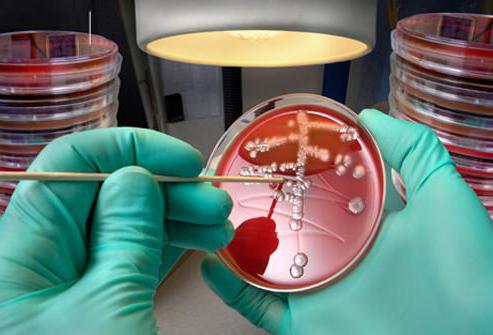
Диагностика заболевания базируется на выявлении симптомов патологии и причин её возникновения. Учитывается анамнез, а также эпидемиологические факторы. Обращают внимание на клинические проявления болезни. Для установления диагноза используют инструментальные и лабораторные методики.
Делается анализ кала на Клостридиум диффициле. В лабораторных условиях определяют грамположительные палочки и их споры. При микроскопическом исследовании биоматериал засевают особым образом и на основе этого определяют колонии патогенных микроорганизмов. Специальная подготовка для сдачи подобного анализа не нужна. Численность клостридий определяют по мазку Грамма. После этого идентифицируют вид бактерии. Кал на Клостридиум диффициле исследуют в бактериологической лаборатории.
При диагностировании болезни проводят биологическую пробу на белых мышах, которая определяет стадию интоксикации организма, выявляет токсин и помогает определиться с методами лечения болезни. При диагностике заболевания делают антигенный тест в особых иммунологических лабораториях.
В особых случаях назначается экспресс-диагностика, помогающая определить наличие энтеротоксина в фекалиях. Проводится биопсия кишечного органа, позволяющая узнать о расположении очагов воспаления.
Серодиагностика позволяет выявить наличие токсина в РНГА. Он определяется совместно с антительным диагностикумом. Наблюдают за реакцией, которая происходит в результате встречного иммуноэлектрофореза.
Инструментальная диагностика – это не что иное, как рентгенография кишечного органа, позволяющая определить, где скопился газ в тканях человеческого организма.
Наиболее точным считается томографическое и эдоскопическое обследование. Оно показывает воспалительный процесс, а также образование псевдомембран.
Повышенная активность клостридии у грудничков говорит о наличии дисбактериоза. У грудного ребенка при данной патологии может наблюдаться вздутие живота, уменьшение аппетита, срыгивания. Иногда беспокоит нарушение сна и нерегулярный стул. Количество бактерий у грудничков не должно быть более 103-104 КОЕ/г. Превышение показателя считается патологией, которую нужно лечить.
Если содержание клостридий в норме при сдаче анализа на дисбактериоз, то это означает, что кишечник работает стабильно. При увеличении количества патогенных бактерий следует проводить лечение кишечника.
Как проявляется недуг у детей?

Бактерия Клостридиум диффициле редко затрагивает новорожденных детей и крох первого года жизни. Это связано с тем, что молоко матери содержит особые антитела, которые эффективны в отношении клостридий.
При возникновении антибиотик-ассоциированной диареи в детском возрасте возникают все те же симптомы, что и у взрослых людей. Энтероколит и нетяжелый колит у детей протекает без интонсикации и лихорадки. Пациентов могут беспокоить болевые ощущения в области живота, которые возникают при методе пальпации в этом районе.
Иногда возникает учащение стула, которое провоцирует диарея, что приводит к водно–электролитным сбоям в организме.
Бактерия может вызвать повторяющиеся рецидивирующие формы клостридиоза, сопровождающегося колитом. Это возникает, когда болезнь не излечена до конца. В этом случае клостридиоз возникает по прошествии 7-14 дней после прекращения лечения.
Псевдомембранозный колит в детском возрасте развивается в острой форме. В начальной стадии развития болезни отсутствует аппетит. Появляется лихорадка, отрыжка и спазмы в животе. Наблюдается интоксикация организма, диарея и вздутие живота. При пальпации области живота наблюдается болезненность. Стул учащается. В нем появляется кровь и слизь. Могут наблюдаться обрывки фибринозных наложений. Если диарея частая, то возникает эксикоз, сопровождающийся сбоями кровообращения. В единичных случаях отмечался коллапс.
Развитие псевдомембранозного колита иногда усугубляется перфорацией, кровотечением и возникновением перитонита. В таких случаях за детьми должен наблюдать не только педиатр, но и хирург.
Недуг, вызываемый Клостридиум диффициле: методы лечения
Клостридиоз лечат только в стационаре. При возникновении интоксикации, а также диспепсических расстройств назначают промывание желудка и очищают кишечник при помощи клизмы. В первый день рекомендуют водно-голодную диету.
Проводится симптоматическое лечение энтеросорбентами, гепатопротекторами, витаминами, ноотропами, сердечными гликозидами, а так же жаропонижающими препаратами.
Считается, что проводимая терапия эффективна, если:
- снижается частота стула;
- консистенция стула становится более густой;
- происходит улучшение общего состояния;
- наблюдаются положительные изменения в клинических и лабораторных анализах;
- не происходит развитие болезни.
Если при применении антибактериальной терапии не проходят симптомы Клостридиум диффициле, лечение корректируют.
Иногда колит, спровоцированный Clostridium difficile, лечат хирургическим путем. Обычно это происходит при перфорации ободочной кишки и когда наблюдается развитие воспалительного процесса с возникновением токсического мегаколона, а также имеет место кишечная непроходимость. Операцию делают только в том случае, если адекватное консервативное лечение не дало результата.
Можно ли вылечить Clostridium difficile?
Инфекция Клостридиум диффициле проявляется в различной степени тяжести. Имеет определенный характер течения и степень осложнений.
Когда болезнь не запущена и имеет легкую или среднюю степень тяжести, то заболевание излечивается на 100%. Лихорадка исчезает на 1-2 сутки, а диарея прекращается на 4-7 день. При непроходимости кишечника, почечной недостаточности и псевдомембранозном колите ситуация утяжеляется.
Профилактические меры

Анализ на Клостридиум диффициле позволяет вовремя предупредить развитие болезни, а избавить от патологии совсем помогут своевременные профилактические мероприятия, которые проявляются в:
- соблюдение правил личной гигиены;
- мытье продуктов;
- тепловой обработке продуктов питания;
- повышении иммунитета;
- стабилизации микрофлоры кишечника;
- своевременном выявлении зараженных лиц;
- применение антибактериальной терапии.
Патогенные микроорганизмы устойчивы к воздействию аммиака, но погибают от воздействия гипохлорита натрия, этиленоксидсодержащих веществ, а также при обработке щелочным глутаральдегидом. При заражении Клостридиум диффициле необходимо тщательно очищать все поверхности указанными средствами, для того чтобы уничтожить бактериальные споры микроба. Бактерии не погибают при обработке спиртом, но мытье рук с мылом способно предупредить возникновение патологии.

Клостридии диффициле (лат. Clostridioides difficile, традиционное наименование Clostridium difficile, синоним Peptoclostridium difficile) — вид повсеместно распространенных бактерий. Инфекции, вызванные Clostridioides difficile, являются основной причиной диарей и смертности в больницах.
До недавнего времени вид клостридии диффициле относился к роду клостридии (Clostridium), который входит в семейство Clostridiaceae, порядок Clostridiales, класс Clostridia и именовался Clostridium difficile. В последнее время место этого вида в систематике бактерий несколько раз менялось, его реклассифицировали в род Peptoclostridium, присвоили наименование Peptoclostridium difficile, а в 2016 году перенесли во вновь организованный род Clostridioides который был включён в семейство Peptostreptococcaceae, те же порядок Clostridiales и класс Clostridia, тип Firmicutes, Terrabacteria group, царство Бактерии и поэтому стал именоваться Clostridioides difficile (допустимое эквивалентное имя Clostridium difficile.
*Исходя из соображений определённости и удобства пользования мы ориентируемся на систематику Национального центра биотехнологической информации США (National Center for Biotechnology Information), не утверждая, что она чем-то лучше или хуже других.
Clostridioides difficile — грамположительные спорообразующие строго анаэробные бактерии, по форме представляющие собой большие удлиненные палочки с выпуклостью в середине. Clostridioides difficile способны длительное время сохраняться во внешней среде. Его споры устойчивы к тепловой обработке.
Clostridioides difficile обладает природной устойчивостью к большинству антибиотиков.
Токсикогенные штаммы Clostridioides difficile продуцируют несколько патогенных факторов. Наиболее изученными среди них являются:
- токсин А (энтеротоксин)
- токсин B (цитотоксин)
- белок, угнетающий перистальтику кишечника
Анитибиотикоассоциированные диареи (ААД) — одно из осложнений, встречающееся у 5–25 % пациентов, принимающих антибиотики. Clostridium difficile — не единственная причина ААД, хотя и достаточно распространенная (примерно одна треть случаев). Причиной ААД также могут быть Salmonella spp., Clostridium perfringens тип А, Staphylococcus aureus, Klebsiella oxytoca, грибы рода candida и другие микроорганизмы. ААД — одна из широко распространенных внутрибольничных инфекций. Только в США ежегодно регистрируется до 1 млн. случаев ААД. Несмотря на значительное носительство Clostridium difficile, дети младенческого возраста практически не болеют ААД, вызванными Clostridium difficile.
Возникновение ААД обусловлено тем, что антибиотики подавляют не только патогенную, но и нормальную микрофлору кишечника, которая в обычных условиях не дает размножаться патогенным и условно-патогенным микроорганизмам. В результате воздействия антибиотиков на нормальную микрофлору количество устойчивых к лекарственным препаратам патогенных и условно-патогенных микробов (в том числе Clostridium difficile) в организме человека может значительно увеличиваться.
Причиной ААД может быть практически любое антимикробное средство, однако частота заболеваний существенно зависит от типа антибиотика (при этом почти не зависит от дозы). Наиболее часто ААД вызывает прием клиндамицина, цефалоспоринов, ампициллина.
Основным фактором риска возникновения тяжелых форм ААД, обусловленных Clostridium difficile является антибиотикотерапия. Даже однократный прием антибиотика широкого спектра действия, вне зависимости от дозы и способа введения, может привести к развитию ААД и псевдомембранозного колита. Фактором риска также является продолжительное пребывание в стационаре, особенно в одной палате с носителями Clostridium difficile.
 |
| Псевдомембранозный колит (Бунова С.С. и др.) |
Псевдомембранозный колит характеризуется обильным частым водянистым поносом, иногда с примесью крови, слизи, гноя. Как правило, понос сопровождается лихорадкой, повышенной до 38,5–40°С температурой, умеренными или интенсивными болями в животе схваткообразного или постоянного характера. Летальность при отсутствии лечения заболевших псевдомембранозным колитом — 15–30 %
Особенностью инфекции Clostridium difficile являются ее частые рецидивы — в среднем 20–25%, причиной которых является связанные с нахождением в кишечнике спор Clostridium difficile или повторным заражением. Обычно после проведения лечения наступает выздоровление или улучшение, однако на 2–28-й день (в среднем через 3–7 дней) развивается рецидив, идентичный первоначальному эпизоду.
Основными поражающими факторами человеческого организма при заболеваниях, вызываемых Clostridium difficile являются токсины А и В. Не все штаммы Clostridium difficile продуцируют эти токсины. С целью выявления инфицирования токсигогенными штаммами Clostridium difficile выполняют анализ кала на наличие в нем токсинов А и В или анализ кала — посев на Clostridium difficile. В норме результаты анализов должны быть отрицательны.
При выявлении ААД обязательно отменяют антибиотик, вызвавший заболевание. Лечение тяжелых случаев ААД и пседомембранозного колита включает терапию ванкомицином или метронидазолом, к которым чувствительны большинство штаммов Clostridium difficile. Не допустим прием антидиарейных лекарств и спазмолитиков из-за опасности развития тяжелого осложнения — токсического мегаколона.
Из пробиотиков эффективен Энтерол, содержащий лиофилизированные дрожжевые грибы Saccharomyces boulardi, обладающие прямым антимикробным действием в отношении не только Clostridium difficile, но и других микроорганизмов, способных вызвать ААД. Для профилактики развития ААД и восстановления микрофлоры кишечника после отмены антибиотика (ванкомицина или метронидазола) применяют препараты, содержащие штаммы представителей естественной микрофлоры: Lactobacillus acidophilus, Lactobacillus rhamnosus, Bifidobacterium longum, Enterococcus faecium и других (Линекс, Бифиформ и т.п.).
Всемирная гастроэнтерологическая организация отмечает эффективность применения для лечения Clostridium difficile-ассоциированной диареи штамма Lactobacillus casei DN-114 001, а также для её профилактики следующих пробиотческих штаммов (Пробиотики и пребиотики. Практические рекомендации):
- Lactobacillus casei DN-114 001 в ферментированном молоке с Lactobacillus bulgaricus и Streptococcus thermophilus10 10 Кое, 2 раза в день
- Lactobacillus acidophilus + Bifidobacterium bifidum (специальные штаммы) — 2 х 10 10 Кое каждого, 1 раз в день
- Saccharomyces cerevisiae (boulardii). Возраст 1 год — 2 х 10 10 Кое в день
- Олигофруктоза — 4 гр, 3 раза в день по 4 г.
В настоящее время доказана связь между лечением антисекреторными препаратами и развитием Clostridium difficile-ассоциированной диареи
Имеются исследования, показывающие, что у пациентов, получающих ингибиторы протонной помпы (ИПП), применяемые для подавления кислотопродукции в желудке, частота диарей, ассоциированных с инфекцией Clostridium difficile, увеличивается на 65% (Самсонов А.А., Одинцова А.Н.). Управление по контролю за продуктами и лекарствами США (FDA) опубликовало 8 февраля 2012 года сообщение, в котором предупреждает пациентов и врачей о том, что использование ингибиторов протонной помпы, возможно увеличивает риск Clostridium difficile-ассоциированных диарей. Для пациентов, принимающих ИПП и страдающих не проходящей диареей, необходимо рассматривать, как возможный диагноз, Clostridium difficile-ассоциированную диарею.
Также существует связь между терапией Н2-блокаторами и Clostridium difficile-ассоциированной диареи. При этом у пациентов, дополнительно получавших антибиотики, вероятность развития такой диареи значительно выше. Количество пациентов, которое надо пролечить Н2-блокаторами одного случая Clostridium difficile-ассоциированной диареи к 14 дню после выписки из стационара у пациентов, получавших или не получавших антибиотики, составило 58 и 425, соответственно (Tleyjeh I.M. et al, PLoS One. 2013;8(3):e56498).

21 октября 2016 года FDA США допустило к применению на территории США новый препарат для предотвращения рецидивов инфекции Clostridium difficile у пациентов старше 18 лет — безлотоксумаб, торговое наименование Zinplava. Безлотоксумаб представляет собой моноклональное антитело, предназначенное для нейтрализации токсина B Clostridiumdifficile.
Заявителем регистрации является компания Merck & Co., Inc. (США).
В России, а также в странах Европейского Союза, безлотоксумаб не имеет регистрации.
Инфекция, вызываемая Clostridium difficile, в настоящее время является серьезной угрозой госпитальной среде, удлиняет время пребывания многих больных в стационаре, а также становится причиной смерти некоторых из них.
а) Причины и механизмы развития. Носительство С. difficile как коменсалов отмечается у 2-3% взрослых и достигает 10-20% у лиц пожилого возраста.
Заражение этим микроорганизмом происходит контактным путем через руки и другие загрязненные поверхности. С. difficile представляет собой анаэробную спорообразующую грамположительную палочку. Это очень жизнестойкая бактерия, которая резистентна ко многим дезинфицирующим средствам, включая спиртсодержащий гель, но гибнет при воздействии дезинфектантов, выделяющих хлор.
Последовательность событий, лежащих в основе заболевания, состоит в колонизации кишечника госпитализированного больного токсигенным штаммом С. difficile, который при назначении больному антибиотиков, нарушающих нормальное микробное равновесие, трансформируется из спор в вегетативные формы.
Последние, пролиферируя, вызывают клостридиальную бактериальную инфекцию. Патогенные штаммы С. difficile продуцируют энтеротоксин (токсин А) и цитотоксин (токсин В), которые связываются поверхностью клеток слизистой оболочки кишечника. Осложнения клостридиальной инфекции включают дегидратацию, нарушение электролитного баланса, развитие псевдомембранозного колита, перфорацию толстой кишки, токсический мегаколон, смерть.
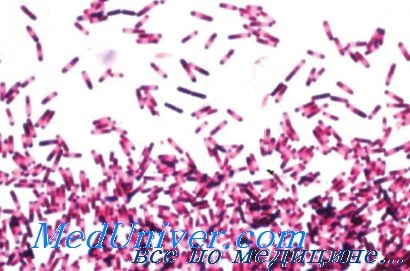
Возбудитель псевдомембранозного колита - Clostridium difficile
б) Факторы риска. Некоторые антибиотики, в частности антибиотики широкого спектра действия и клиндамицин, особенно склонны вызывать описанную последовательность событий.
Поэтому перечень предпочтительных для применения антибиотиков рекомендует микробиолог лечебного учреждения. а антибиотики, которые склонны вызывать клостридиальную инфекцию, назначают лишь при крайней необходимости.
Нередко больным до госпитализации назначают ингибиторы протонной помпы по поводу рефлюкс-эзофагита. Эти препараты способствуют росту С. difficile и потому являются серьезным фактором риска клостридиальной инфекции. Из других факторов риска следует отметить возраст больного старше 65 лет, лечение антибиотиками в последние 3 месяца до госпитализации, госпитализация в анамнезе, воспалительные заболевания кишечника, лечение цитотоксическими препаратами.
в) Симптомы и клиника. Критериями диагностики клостридиальной инфекции являются жидкий стул или токсический мегаколон и положительные результаты исследования кала на клостридиальный токсин иммуноферментным методом. При легкой форме инфекции отмечается лишь жидкий стул, но при среднетяжелой форме появляются также гипертермия, интенсивная боль в животе, кровотечение из нижних отделов ЖКТ и нейтрофилия.
Тяжелая форма характеризуется усугублением перечисленных симптомов. Диарея становится профузной, снижается уровень альбумина в сыворотке крови, повышается концентрация в ней лактата, нарушается функция почек.
г) Лечение инфекции Clostridium difficile. Важное значение имеют ранняя диагностика и своевременное лечение.
Инфекцию, вызванную Clostridium difficile, следует заподозрить при появлении у госпитализированного больного диареи, особенно если она повторилась более 3 раз в течение 24 ч. Больного следует перевести в изолированную палату в течение 4 ч и соблюдать меры, направленные на профилактику заражения и распространения инфекции (мытье рук после каждого контакта с больным, использование перчаток и фартука. Палату, где лежал больной, дезинфицируют раствором гипохлорита.
В течение 4 ч два образца кала больного направляют на микробиологическое исследование и анализ на энтеротоксин и консультируются с инфекционистом.
Лечение включает внутривенное возмещение потери жидкости. Назначают метронидазол или ванкомицин внутрь в течение 10 дней. При тяжелой форме инфекции препаратами выбора являются ванкомицин, назначаемый внутрь, и вводимый внутривенно метронидазол. Всем больным с подозрением на тяжелую форму клостридиальной инфекции следует незамедлительно выполнить рентгенологическое исследование брюшной полости и вызвать ответственного гастроэнтеролога, хирурга и микробиолога.
После консультации микробиолога ингибиторы протонной помпы и антибиотики следует отменить.
*Импакт фактор за 2018 г. по данным РИНЦ
Журнал входит в Перечень рецензируемых научных изданий ВАК.
Читайте в новом номере
Р ациональная антибиотикотерапия является одной из важнейших составляющих в лечении детей с различными инфекционно–воспалительными заболеваниями. Однако широкое и не всегда обоснованное применение антибиотиков в педиатрической практике нередко приводит к развитию разнообразных осложнений (аллергические и токсические реакции, дисбактериозы и др.) [8,12]. Особое место среди антибиотико–индуцированных осложнений занимают дисбактериозы кишечника, которые могут сопровождаться суперинфекцией и клинически значимой активацией условно–патогенных энтеробактерий с развитием колитов и энтероколитов. При этом В.Ф. Учайкин и А.А. Новокшенов (1999) подчеркивают, что до 20% всех антибиотико–ассоциированных диарей и 90–100% псевдомембранозных колитов обусловлено Clostridium difficile–инфекцией [9].
Clostridium difficile–инфекция (клостридиоз диффициле) – острая, антропонозная, анаэробная инфекция с энтеральным путем заражения, характеризующаяся различной степенью выраженности клинических проявлений – от бессимптомного бактерионосительства и легких диарей до тяжелых форм заболевания в виде псевдомембранозного колита.
Этиология. Возбудитель клостридиоза диффициле – Clostridium difficile – строго анаэробная, спорообразующая, грамположительная бацилла [7]. Вегетативные формы Clostridium difficile обладают способностью продуцировать экзотоксины, среди которых идентифицированы повреждающие кишечную стенку энтеротоксин (токсин А) и цитотоксин (токсин В) [7,11,16]. Установлено, что токсин А, стимулируя гуанилатциклазу, повышает секрецию жидкости в просвет кишечника и способствует развитию диареи. Токсин В обладает выраженным цитопатогенным действием. Предполагают, что ингибируя процессы синтеза белка в энтеро– и колоноцитах, токсин В нарушает функции их клеточных мембран. Это приводит к потере калия и развитию электролитных нарушений. Споры Clostridium difficile проявляют высокую устойчивость к факторам внешней среды и стандартным дезсредствам, а вегетативные формы резистентны к большинству антибиотиков (природные и полусинтетические пенициллины, ингибитор–защищенные пенициллины, цефалоспорины, линкозамиды и др.) [5,7,11,14].
Эпидемиология. Clostridium difficile часто обнаруживаются в окружающей среде и могут быть изолированы из почвы [7,9,12]. Основной механизм передачи инфекции – фекально–оральный. Источником инфекции является человек (чаще – пациенты, получающие антибиотики широкого спектра действия, и дети). Установлено, что частота контаминации кишечника Clostridium difficile у здоровых новорожденных и младенцев может составлять более 50%, тогда как у детей старше 2 лет, а также у здоровых взрослых уровень инфицированности не превышает 5% [3,9,12]. В то же время у взрослых, находящихся на лечении в различных стационарах, частота носительства Clostridium difficile значительно выше и может достигать 10–20% [4,5]. При этом отмечено, что трансмиссия вегетативных форм Clostridium difficile от инфицированных (дети, медицинский персонал, лица, осуществляющие уход за больными и сами пациенты) к здоровым лицам осуществляется через такие факторы передачи, как руки и предметы ухода. Кроме этого, установлена возможность широкого контаминирования Clostridium difficile различных внутригоспитальных объектов (постельные принадлежности, мебель, душевые, туалеты и др.) [3–6]. Бытовая передача Clostridium difficile с участием различных факторов создает серьезный риск развития внутрибольничной инфекции, особенно у пациентов, получающих массивную антибактериальную терапию. Контингентами риска по развитию тяжелых форм нозокомиальной Clostridium difficile–инфекции являются и дети раннего возраста (ослабленные), а также пациенты, длительно находящиеся в стационаре [3,9,12].
Установлено, что основным фактором риска по развитию тяжелых форм заболевания является антибиотикотерапия. При этом В.А. Малов и соавт. (1999) подчеркивают, что даже однократный прием антибиотика широкого спектра действия, независимо от дозы и способа введения, может привести к развитию диареи и псевдомембранозного колита, обусловленных Clostridium difficile [6]. К факторам риска также относят повторные очистительные клизмы, длительное использование назогастрального зонда, оперативные вмешательства на органах желудочно–кишечного тракта и продолжительное пребывание пациентов в стационаре [2–6,12]. В то же время установлено, что диарея и колит, обусловленные Clostridium difficile, могут развиваться не только в стационаре, но и в амбулаторных условиях при использовании антибиотиков широкого спектра действия, особенно у ослабленных пациентов и детей раннего возраста [15].
Патогенез и патоморфология. В основе патогенеза клинически манифестных форм Clostridium difficile–инфекции – антибиотико–ассоциированной диареи и псевдомембранозного колита – лежит снижение колонизационной резистентности кишечника. Под действием антибиотиков и других повреждающих факторов нарушается интестинальный микробный пейзаж. Значительное угнетение при этом анаэробной части нормальной микрофлоры кишечника сопровождается возникновением благоприятных условий для размножения Clostridium difficile и перехода её в токсинобразующую форму. При этом основными факторами патогенности Clostridium difficile являются токсины А и В, приводящие к повреждению стенки кишечника, в то время как непосредственно сам возбудитель не обладает инвазивными свойствами и не оказывает цитотоксического воздействия на слизистые кишечника [5,7,11,16].
При легких вариантах Clostridium difficile–ассоциированной диареи морфологическая картина характеризуется умеренной гиперемией и незначительным отеком слизистой кишечника, тогда как при тяжелых – отмечаются выраженные воспалительные изменения. При развитии наиболее тяжелой формы заболевания (псевдомембранозный колит) на фоне резко выраженных воспалительно–геморрагических изменений слизистой кишечника обнаруживают небольшие по размеру (чаще – до 2–5 мм, реже – до 20 мм и более в диаметре) возвышающиеся желтоватые бляшки, плотно связанные с подлежащими тканями. Бляшки образованы скоплением фибрина, муцина и клеток, участвующих в воспалении. Сливаясь, бляшки образуют псевдомембраны. В отдельных случаях слизистая может быть покрыта толстым слоем фибринозно–пленчатых наложений на значительном протяжении кишечника. Пленки, при расплавлении, могут отторгаться, обнажая изъязвленную поверхность кишечной стенки [1,2,9,17].
Значительное распространение (более 50%) асимптоматического бактерионосительства Clostridium difficile у новорожденных детей и младенцев и крайне низкая частота развития у них манифестных форм инфекции объясняется, по–видимому, особенностями строения клеточной мембраны кишечного эпителия. Предполагается, что у детей раннего возраста эпителиальные клетки слизистых оболочек кишечника не имеют рецепторов к токсинам Clostridium difficile. Вероятно, что в формировании транзиторной резистентности к данной инфекции имеет значение и наличие у детей первого полугодия жизни материнских антиклостридиальных антител, полученных трансплацентарно [5,6,9].
Clostridium difficile–ассоциированная диарея у детей часто характеризуется клиническими симптомами нетяжелого колита или энтероколита и обычно протекает без лихорадки и интоксикации. При этом возможно появление болей в животе, но чаще болезненность со стороны кишечника выявляется лишь при его пальпации. Отмечается легкое или умеренное учащение дефекации, как правило, не приводящее к выраженным водно–электролитным нарушениям [9,12].
Клинические проявления псевдомембранозного колита у детей обычно развиваются остро и характеризуются отказом от еды, лихорадкой, интоксикацией, диареей, срыгиванием, вздутием и болями в животе спастического характера (абдоминальные колики), болезненной пальпацией живота по ходу толстого кишечника [9,12]. Стул частый, в каловых массах – примесь слизи и крови (реже). Иногда бoльшая часть испражнений представлена густой белесоватой слизью и обрывками фибринозных наложений. В случаях резко выраженного учащения стула развивается эксикоз с нарушениями кровообращения, значительно реже отмечается коллапс без предшествующей диареи. Течение псевдомембранозного колита может осложниться кишечным кровотечением, перфорацией и развитием перитонита [6,9,12]. Поэтому для своевременного выявления этих грозных осложнений за пациентами с тяжелыми формами клостридиоза диффициле должно проводиться совместное наблюдение педиатра и хирурга.
Крайне тяжелые и летальные случаи Clostridium difficile–инфекции в большинстве случаев отмечаются у детей с выраженной нейтропенией на фоне лейкемии, у младенцев с болезнью Гиршпрунга и у пациентов с хроническими воспалительными заболеваниями кишечника (болезнь Крона, неспецифический язвенный колит) [12].
Описаны случаи рецидивирующего течения манифестных форм клостридиоза диффициле, при которых отмена этиотропной терапии или использование антибиотиков в последующие периоды жизни ребенка вновь сопровождались развитием колита. Причинами рецидивов при этом считают такие факторы, как неполная элиминация кишечника от Clostridium difficile и реинфекция [5,12].
Следует еще раз подчеркнуть, что хотя наиболее часто Clostridium difficile–ассоциированная диарея и псевдомембранозный колит возникают у детей, находящихся в стационаре и получающих антибиотики, но могут встречаться и у лиц, уже выписанных из больницы, или развиться спустя 1–2 недели после отмены антибактериальной терапии.
Нельзя забывать и о том, что в редких случаях клостридиоз диффициле возникает без предшествующей госпитализации, а использование антибиотиков в амбулаторных условиях также может сопровождаться развитием заболевания [12,15].
Следует отметить, что для этиологической расшифровки диареи у новорожденных и детей первых месяцев жизни выявление токсинов А и В не имеет диагностического значения. Это связано с транзиторной резистентностью детей данного возраста к токсинам Clostridium difficile, что и определяет минимальный риск развития у них манифестных форм заболевания [9].
При бактерионосительстве Clostridium difficile и легких вариантах антибиотико–ассоциированной диареи гемограмма, как правило, характеризуется нормальными показателями. При манифестных формах инфекции изменения в клиническом анализе крови носят неспецифический характер и характеризуются нейтрофильным лейкоцитозом, сдвигом лейкоцитарной формулы влево, а также ускорением СОЭ [6,9].
Лечение. Асимптоматическое бактерионосительство Clostridium difficile у здоровых детей не требует проведения терапевтических мероприятий.
При развитии манифестных форм инфекции, независимо от степени выраженности клинических проявлений, принципиальным положением является незамедлительная отмена используемых антибиотиков (табл. 1).
Вопрос о необходимости назначения этиотропной терапии в каждом конкретном случае должен решаться индивидуально с учетом возраста ребенка, тяжести заболевания и фоновых состояний. Так, при легких вариантах Clostridium difficile–ассоциированных диарей, развившихся у детей с благополучным преморбидным фоном, назначение этиотропного лечения не требуется. В то же время у детей раннего возраста, ослабленных, у пациентов с нейтропенией, тяжелыми хроническими заболеваниями и пороками развития (особенно ЖКТ) даже при легких формах инфекции назначение антиклостридиальных препаратов считается обоснованным. Абсолютными показаниями для этиотропной терапии являются тяжелые формы заболевания, продолжающаяся после отмены антибиотиков диарея, а также рецидив инфекции на фоне повторного приема антибиотиков (табл. 1).
Метронидазол для лечения Clostridium difficile–инфекции применяется в суточной дозе 30 мг/кг. Суточная доза вводится ребенку в 3–4 приема [12]. При этом метронидазол, в отличие от ванкомицина, может вводиться как перорально, так и парентерально – путем внутривенной инфузии. В тех случаях, когда у ребенка с клостридиозом диффициле выражены тошнота, срыгивания или рвота, стартовая этиотропная терапия должна начинаться с парентерального введения метронидазола. При купировании указанных симптомов и улучшении общего состояния целесообразно заменить внутривенное введение метронидазола на оральный его прием. При приеме внутрь препарат быстро и хорошо всасывается (биодоступность – 80–100%). Связывание с белками крови составляет 20%. При внутривенном введении достигаются высокие концентрации метронидазола во всех тканях организма [18]. Метаболизируясь в печени путем окисления и глюкуронизации, метронидазол экскретируется почками (до 80%) и кишечником (до 15%). Метронидазол замедляет метаболизм непрямых антикоагулянтов, что приводит к усилению их эффекта и может способствовать развитию геморрагических осложнений. Терапевтический эффект метронидазола могут уменьшить индукторы печеночного метаболизма (барбитураты, противосудорожные препараты, рифампицин). В то же время препараты, ингибирующие микросомальные ферменты гепатоцитов (циметидин), снижают метаболизм метронидазола, что может привести к повышению его содержания в организме [18].
Особое внимание необходимо обратить на то, что при пероральном введении этиотропных лекарственных средств недопустимо одновременно применять энтеросорбенты (холестирамин, активированный уголь и др.). Это объясняется возможным уменьшением терапевтического эффекта антибиотиков из–за их связывания с энтеросорбентами в просвете кишечника [6,12]. В целом использование энтеросорбентов может быть оправдано лишь при легких вариантах Clostridium difficile–ассоциированной диареи, когда нет показаний для назначения этиотропных лекарственных средств или в тех случаях тяжело протекающего заболевания, когда метронидазол вводится парентерально.
По показаниям при тяжелых формах клостридиоза диффициле проводится также по–синдромная терапия, направленная на нормализацию выявленных изменений гомеостаза (водно–электролитный дисбаланс, токсикоз, гемодинамические нарушения, геморрагический синдром и др.) [9]. При тяжелых вариантах инфекции обсуждается также возможность применения внутривенных иммуноглобулинов [6]. Обоснованием для этого явилось обнаружение антитоксинов А и В (антитела к экзотоксинам Clostridium difficile) в препаратах нормального человеческого иммуноглобулина для внутривенного введения. При этом В.А. Малов и соавт. (1999) подчеркивают, что включение внутривенных иммуноглобулинов в комплексную терапию тяжелых форм клостридиоза диффициле сопровождалось быстрым прекращением диареи, купированием болей в животе и нормализацией температуры тела.
Особо следует отметить, что при тяжелых формах Clostridium difficile–ассоциированной диареи и псевдомембранозном колите нельзя использовать препараты, уменьшающие моторику кишечника [12, 18].
После отмены антимикробных препаратов детям, перенесшим Clostridium difficile–инфекцию, для полной санации кишечника от спор возбудителя целесообразно провести курсовое лечение пробиотиками (бифидимбактерин и др.) [2,6,9].
Профилактика клостридиоза диффициле заключается в строгом соблюдении правил личной гигиены, а также в неукоснительном выполнении всех требований по соблюдению санитарно–противоэпидемического режима лечебных учреждений. Нельзя также недооценивать и такой фактор в профилактике Clostridium difficile–инфекции, как уменьшение частоты бесконтрольного и необоснованного использования антибиотиков. Таким образом, основными резервами снижения заболеваемости у детей клостридиозом диффициле являются улучшение санитарной культуры населения в целом и повышение профессионализма медицинских работников.
1. Аруин Л.И., Капуллер Л.Л., Исаков В.А. Морфологическая диагностика болезней желудка и кишечника. – М.: Триада–Х, 1998.
3. Клостридиозы. // Профилактика внутрибольничных инфекций. Руководство для врачей под ред. проф. Е.П.Ковалевой, проф. Н.А.Семиной. – М.: Рарогъ, 1993. – С. 55–59.
4. Ковалева Е.П., Семина Н.А., Семененко Т.А., Галкин В.В. Справочник госпитального эпидемиолога. – М.: Хризостом, 1999. – С. 136–139.
5. Малов В.А., Бондаренко В.М., Пак С.Г. Роль Clostridium difficile в патологии человека.//Журн.микробиол.–1996.–№1.–С.91–96.
6. Малов В. А., Пак С. Г., Беликов Д. В.// Лечащий врач. 1999. – 2–3.
7. Медицинская микробиология./ Под ред. В.И.Покровского, О.К.Поздеева. – М: ГЭОТАР МЕДИЦИНА, 1999.
8. Планельес Х.Х., Харитонова А.М. Побочные явления при антибиотикотерапии бактериальных инфекций. – М.: Медицина, 1976. – 430.
9. Учайкин В.Ф. Руководство по инфекционным заболеваниям у детей. – М.: Гэотар Медицина, 1998. – С. 492–494.
10. Фэкети Р. (Fekety R.), Дюпон Х.Л. (DuPont H.L.), Куперсток М. (Cooperstok M.) и др. Лечение колита, связанного с приемом антибиотиков. // Европейское руководство по клинической оценке противоинфекционных лекарственных средств/ Под ред. Т.Р.Бим (T.R.Beam) – Пер. с англ. под ред. академика РАМН А.Г.Чучалина и проф. Л.С.Страчунского. – Смоленск: Амипресс, 1996. – С. 302–306.
11. Bartlett J.G. Antibiotic–associated pseudomembranous colitis due to toxin producing clostridia. //N. Engl.J.Med. – 1978. – Vol.298. – P.531.
12. Clostridium difficile. // In Red Book: 2000. Report of the Committee on Infection Diseases. 25rd: American Academy of Pediatrics, 2000, P. 214–216.
13. Larson H.E., Prise A.B., Honour P. et al. Pseudomembranous colitis: present of clostridial toxin. // Lancet. – 1977. – P. 1312–1314.
14. Larson H.E., Prise A.B., Honour P. et al. Clostridium difficile and etiology pseudomembranous colitis. // Lancet. – 1978. – №1. – P. 1063–1066.
15. Mitchell D.K., Van R., Mason E.H. at al. Prospective study of toxigenic Clostridium difficilе children given amoxicillin/clavulanate for otitis media. // Pediatr. Inf. Dis. J. – 1996. – 15. – P. 514–519.
16. Mitchell T.J., Ketley J.M., Haslam S.C. et al. Effect of toxin A and B of Clostridium difficile on rabbit ileum and collon. // Gut. – 1986. – 27. – P. 78–85.
17. Prise A.B., Davies D.R.D. Pseudomembranous colitis. // J. Clin. Pathol. – 1977. –30. – P. 1–12.
18. The Pharmacological Basis of Therapeutics – Goodman &. Gilman’s. – 8th Ed.
Читайте также:


