Хламидийная инфекция клинические рекомендации по лечению
Рассмотрен цервицит у женщин, развивающийся вследствие симптомной урогенитальной хламидийной инфекции, подходы к диагностике урогенитальной хламидийной инфекции у женщин. Приведены современные международные и российские рекомендации по лечению хламидийной
Cervicitis Is examined in women, developing as a result of the symptomal uro genital chlamydia infection, approaches to diagnostics of uro genital chlamydia infection in women. Contemporary international and Russian recommendations regarding treatment of chlamydia infection in midwifery and gynaecology are also provided.
Хотя инфекция, вызванная Chlamydia trachomatis, считается наиболее распространенной из всех инфекций, передаваемых половым путем (ИППП), реальная частота и распространенность данного заболевания остаются неизвестными [1]. По данным Всемирной Организации Здравоохранения (ВОЗ) в мире ежегодно регистрируется почти 100 млн новых случаев C. trachomatis [2]. В 2009 г. в Центры по контролю и профилактике заболеваний США (Centers for Disease Control and Prevention (CDC)) поступили сообщения о 1 244 180 случаях хламидийной инфекции [3], однако реальное количество по меньшей мере в 2 раза больше — около 3 млн случаев, поскольку большинство (70–90%) эпизодов хламидийной инфекции нижних отделов урогенитального тракта у женщин протекают бессимптомно и поэтому остаются недиагностированными [4–6]. По данным систематического обзора, посвященного изучению инфицирования C. trachomatis, распространенность хламидийной инфекции варьировала от 1,7 до 17% [7], а среди молодых женщин, обращавшихся в клиники, занимающиеся лечением ИППП, частота выявления хламидийной инфекции превышала 10% [8]. Как в США, так и в большинстве стран Европы за последние 10 лет отмечается рост частоты хламидийной инфекции [3, 9], однако в ряде европейских государств хламидийная инфекция не относится к заболеваниям, подлежащим регистрации. В Российской Федерации в 2009 г. заболеваемость хламидийной инфекцией составила 80,3 на 100 000 населения [10].
При развитии симптомной урогенитальной хламидийной инфекции у женщин чаще всего возникает цервицит. В случае бессимптомного течения нелеченная хламидийная инфекция может привести к поражению верхних отделов генитального тракта и возникновению воспалительных заболеваний органов малого таза (ВЗОМТ). Ежегодно в США диагностируется около 750 000 случаев ВЗОМТ [11]. Как клинически диагностированные случаи ВЗОМТ, так и субклинические варианты поражения органов малого таза могут привести к фиброзу, образованию рубцов и нарушению проходимости маточных труб, что нередко является причиной серьезных нарушений репродуктивной функции, включая трубное бесплодие, эктопическую беременность и развитие синдрома хронической тазовой боли [3].
Около 10–15% нелеченных случаев хламидийной инфекции приводят к клинически диагностируемым случаям ВЗОМТ, из которых 15% могут привести к развитию трубного бесплодия [12, 13]. Доля трубного бесплодия среди всех других видов бесплодия варьирует от 10% до 40% [14, 15]. Хламидийная инфекция является лидирующей предотвращаемой причиной трубного бесплодия [14]. Прямые медицинские затраты на хламидийную инфекцию, включая диагностику и лечение бесплодия, вызванного хламидийной инфекцией, составляют 701 млн долларов ежегодно (2010 г.) [3].
Что касается хламидийной инфекции у беременных, то, по данным ВОЗ, частота обнаружения C. trachomatis у беременных колеблется в очень широких пределах (от 2% до 37%), в среднем составляя 6–8% и достигая 70% у пациенток с хроническими ВЗОМТ и отягощенным акушерско-гинекологическим анамнезом [16–18). Ежегодно в США у 100 000 беременных женщин диагностируется хламидийная инфекция [19].
Данные о влиянии хламидийной инфекции на течение и исход беременности неоднозначны. Результаты ряда исследований свидетельствуют о том, что наличие хламидийной инфекции половых путей у матери может приводить к повышению частоты случаев невынашивания беременности, мертворождения, преждевременных родов, преждевременного разрыва плодных оболочек, к развитию эндометрита и сальпингита в послеродовом периоде, а также к рождению детей с низкой массой тела [20–25]. Так, например, в ходе проспективного исследования, выполненного в США, показано, что инфицирование C. trachomatis во время беременности приводит к задержке внутриутробного развития плода, а также повышает риск преждевременных родов [23]. В других исследованиях связь хламидийной инфекции с неблагоприятными исходами беременности не была доказана [26].
С другой стороны, не подлежит сомнению, что урогенитальный хламидиоз у беременных является фактором риска развития хламидийной инфекции у новорожденных. Инфицирование происходит в 23–70% случаев, преимущественно во время родов при прохождении плода через инфицированные родовые пути. При этом у 11–50% детей, рожденных женщинами с хламидиозом, в первые две недели жизни развивается конъюнктивит, а у 3–16% на 1–3 месяц жизни хламидийная пневмония [26, 27].
Диагноз урогенитальной хламидийной инфекции устанавливается на основании клинической картины заболевания и выявления C. trachomatis при проведении лабораторных исследований [28]. Как отмечено выше, наиболее частой клинической формой локализованной хламидийной инфекции у женщин является цервицит [6, 28]. Симптомы заболевания обычно возникают спустя 1–3 недели после инфицирования. Пациентки могут предъявлять жалобы на выделения из половых органов слизисто-гнойного характера, зуд, жжение, дискомфорт в области наружных половых органов, боль в нижней части живота, межменструальные или посткоитальные кровянистые выделения. При гинекологическом обследовании у пациенток с хламидийным цервицитом выявляются гиперемия и отечность в области наружного зева цервикального канала и слизисто-гнойные выделения, нередко — цирцинарная эрозия [6, 28]. Но — нельзя не подчеркнуть данный факт еще раз — у большинства пациенток с хламидийным цервицитом отмечается отсутствие субъективных симптомов заболевания [6, 28, 29].
К основным методам лабораторной диагностики хламидийной инфекции относятся:
- молекулярно-биологические методы (методы амплификации нуклеиновых кислот или ПЦР-диагностика);
- культуральное исследование;
- метод прямой иммунофлюоресценции.
Метод прямой иммунофлюоресценции (ПИФ) с моноклональными антителами отличается высокой степенью субъективной оценки результатов и низкой воспроизводимостью. Чувствительность и специфичность данного метода составляет не более 60–80%, что зависит от качества получения материала для исследования и квалификации персонала лаборатории [10, 28].
В опубликованных в 2010 г. Рекомендациях по лечению заболеваний, передаваемым половым путем (Sexually Transmitted Diseases Treatment Guidelines), CDC [29] и Европейском руководстве по ведению пациентов с инфекцией, вызванной C. trachomatis (European guideline for the management of Chlamydia trachomatis infections) [6] основными препаратами в лечении хламидийной инфекции у небеременных пациенток являются азитромицин и доксициклин, у беременных женщин — азитромицин (табл. 1).
По данным метаанализа 12 рандомизированных исследований, в котором проводилось сравнение азитромицина и доксициклина в лечении урогенитальной хламидийной инфекции, оказалось, что сравниваемые режимы лечения эквивалентны по эффективности с достигнутой частотой эрадикации патогена, которая составила 97% и 98% соответственно [31].
Существенным преимуществом азитромицина в терапии урогенитального хламидиоза является возможность однократного приема внутрь 1 г препарата, что делает азитромицин наиболее целесообразным антибиотиком (в том числе и с экономической точки зрения) в лечении всех пациенток, особенно женщин с рискованным сексуальным поведением, недостаточной комплаентностью назначенному лечению или с невозможностью проведения оценки излеченности во время последующих визитов к врачу [29]. Как показали исследования, комплаентность лечения значительно выше в случае однократного применения азитромицина как пациентками, так и их партнерами [32–34].
Указанный в Рекомендациях CDC эритромицин рассматривается (по сравнению с азитромицином или доксициклином) как менее эффективный препарат, что, в первую очередь, связано с достаточно часто возникающими нежелательными явлениями со стороны ЖКТ, в значительной степени влияющими на комплаентность [29]. Левофлоксацин и офлоксацин являются эффективной альтернативной, однако не имеют преимуществ по режимам дозирования и длительности использования [29].
В российских схемах терапии хламидийной инфекции у небеременных пациенток, помимо азитромицина, доксициклина, эритромицина, левофлоксацина, офлоксацина и джозамицина, указаны и другие антибиотики (в частности, в Клинических рекомендациях Российского общества акушеров и гинекологов, 2009 г., указаны макролиды спирамицин, рокситромицин и кларитромицин, что не противоречит Европейскому руководству по ведению пациентов с инфекцией, вызванной C. trachomatis, а также ломефлоксацин, отсутствующий во всех других рекомендациях и протоколах ведения больных).
Кроме того, нельзя не остановиться на крайне широком диапазоне дозирования джозамицина и рекомендуемой длительности использования. По данным исследований, приведенным в табл. 3, дозирование джозамицина при урогенитальной хламидийной инфекции варьировало от 500 мг 2 раза в сутки до 500 мг 3 раза в сутки, длительность исследования — от 7 до 14–15 дней.
Что касается терапии хламидийной инфекции у беременных пациенток, то и в Рекомендациях по лечению заболеваний, передаваемым половым путем, CDC, 2010 г. и в Европейском руководстве по ведению пациентов с инфекцией, вызванной C. trachomatis, основным препаратом является азитромицин, также используются амоксициллин и эритромицин (табл. 1) [6, 29].
Принципиальными отличиями российских схем лечения (табл. 4) являются: 1) рекомендации по использованию 16-членных макролидов джозамицина и спирамицина, отсутствующих в Европейском руководстве по ведению беременных пациенток с хламидийной инфекцией (в США препараты не зарегистрированы); 2) рекомендации по более длительному лечению (10-дневные курсы джозамицина и спирамицина).
В настоящее время наиболее оптимальным препаратом для лечения урогенитального хламидиоза во время беременности представляется азитромицин. Первые сведения о возможности применения азитромицина при хламидийной инфекции у беременных были получены еще в 1996 г., когда в сравнительном исследовании было установлено, что по клинической и бактериологической эффективности при цервиците, вызванном C. trachomatis, азитромицин в дозе 1 г однократно не уступает эритромицину, назначаемому в дозе 500 мг 4 раза в сутки в течение 10 дней. Никаких различий между группами по исходам беременности выявлено не было [49].
Для подтверждения эффективности и безопасности применения азитромицина при лечении хламидийной инфекции во время беременности при поддержке CDC в США было инициировано ретроспективное когортное исследование. При анализе результатов лечения 277 беременных женщин с хламидийной инфекцией оказалось, что эффективность азитромицина в данной популяции составила 97%, амоксициллина — 95% и эритромицина — 64%. Таким образом, в данном исследовании эффективность азитромицина оказалась достоверно (p
А. А. Хрянин*, доктор медицинских наук, профессор
О. У. Стецюк**, кандидат медицинских наук
И. В. Андреева**, кандидат медицинских наук, доцент
* ГБОУ ВПО НГМУ Минздравсоцразвития России, Новосибирск
** НИИ антимикробной химиотерапии ГБОУ ВПО СГМА Минздравсоцразвития России, Смоленск
![]()
Хламидийная инфекция мочеполовой системы является всемирно распространенной инфекцией, передающейся половым путем (ИППП; также известна, как заболевание, передающееся половым путем, ЗППП). Микроорганизмом, который провоцирует заболевание, является Chlamydia trachomatis. Инфекция обычно протекает бессимптомно у мужчин и женщин.
У женщин хламидийная инфекция, как правило, возникает в эндоцервикальном канале. У некоторых женщин с не осложненной формой инфекции шейки матки отмечается уже и субклиническое поражение верхних половых путей. Симптомы могут включать кровотечение после секса или между периодами менструаций; наличие слизистых выделений из влагалища без какого-либо запаха; боли в области таза; или дизурию. У мужчин хламидийная инфекция может начать развиваться в половом канале, вызывая выделения из полового члена.
Отсутствие лечения или неадекватное лечение хламидийной инфекции может спровоцировать развитие более серьезных проблем по типу воспалительного заболевания тазовых органов, внематочной беременности и бесплодия у женщин, а также эпидидимита и простатита у мужчин.
Инфекции вызваны бактерией Chlamydia trachomatis и являются наиболее распространенными инфекциями, передающимися половым путем. Почти всегда передается при сексуальном контакте. Бактерии могут вызывать симптомы, но у большинства больных инфекция протекает бессимптомно.
Chlamydia trachomatis является небольшой грамотрицательной бактерией, которая существует в качестве облигатного внутриклеточного паразита.
Она имеет две фазы жизненного цикла. На первой фазе микроорганизм проникает в клетку и образует крупные включения, которые называются элементарными тельцами. Элементарные тельца повторно реорганизовываются в меньшие, ретикулярные тельца. Ретикулярные тельца реплицируют и дозревают в элементарные тельца. После завершения созревания клетки разрываются в течение 2–3 дней. Освобожденные бактерии после этого проникают в другие клетки для продолжения процесса репликации.
Благодаря этой уникальной способности жизненного цикла микроорганизма, он не может быть культивирован в условиях искусственной среды.
После контакта с C trachomatis инкубационный период обычно составляет 7-21 день. Инфекция мочеполового тракта приводит к воспалению уретры у мужчин или к воспалению шейки матки у женщин. В некоторых случаях инфекция может продвинуться вверх в область половых путей у женщин и вызвать инфекцию органов таза, воспалительное заболевание тазовых органов или перигепатит (синдром Фитц-Хью-Куртиса). В мужчин продвижение инфекции может привести к развитию эпидидимита или простатита.
Благодаря тому, что приблизительно у 85% женщин и мужчин патология протекает бессимптомно, высокий индекс подозрений на наличие заболевания основан на фактах анамнеза пациента и наличии факторов риска.
Типичные факторы риска включают возраст менее 25 лет, сексуальную активность с инфицированным партнером, наличие нового сексуального партнера или нескольких сексуальных партнеров, наличие сексуального партнера, имеющего других сексуальных партнеров, наличие ИППП в анамнезе, а также факты не использования презервативов.
Диагностика и лечение являются относительно простым при клиническом подозрении наличия инфекции.
У женщин могут наблюдаться кровотечения после секса или в период между менопаузами, а также вагинальные выделения без запаха, дизурия или же боли в области таза. Инфекция может подняться к верхней части мочеполового тракта и спровоцировать развитие лихорадки, озноба, миалгии, тошноты, рвоты и боли в брюшной полости или же в области таза. В редких случаях это может вызвать лихорадку и боль в верхнем правом квадранте брюшной полости вторично по отношению к перикапсулярной инфекции печени. Осмотр шейки матки может выявить мутные или желтые выделения. Шейка матки может кровоточить при легком трении дакроновым тампоном.
У мужчин возможно наличие дизурии и светлых или белесоватых выделений из мочеиспускательного канала. Также при физикальном осмотре могут быть обнаружены выделения из полового члена. При отсутствии видимых выделений давление вдоль полового члена может спровоцировать их появление от основания до кончика. Боли в области мошонки, от легких до тяжелых, могут развиваться в случаях восходящей инфекции, которая провоцирует развитие эпидидимита или простатита. При тяжелых формах инфекции симптомы также включают лихорадку, тошноту и рвоту. Область мошонки может быть чувствительна на прикосновение и являться теплой на ощупь.
Симптомы и признаки ректальной инфекции являются редкими, но при их наличие могут наблюдаться слизисто-гнойные ректальные выделения или болезненные позывы на испражнение или мочеиспускание.
В настоящее время рекомендуется использовать тесты амплификации нуклеиновой кислоты (NAATs). Чувствительность МАНК составляет >90%, а специфичность – 94– 99,5%. Положительные результаты МАНК указывают на наличие Chlamydia trachomatis и необходимость проведения лечения. Ложноположительные результаты МАНК из-за остаточных нежизнеспособных образцов ДНК могут отмечаться на протяжении до 3 недель после успешного лечения. При клиническом подозрении на инфекцию и негативном результате диагностики, диагностический тест следует повторить, поскольку могли быть получены ложно-отрицательные результаты. После того, как инфекция была диагностирована, необходимо обеспечить строгое отслеживание контактов для выявления бессимптомных носителей.
NAATs можно проводить, используя самостоятельно собранные образцы (первые порции мочи или вагинальный мазок), или же образцы, собранные врачом (вагинальный, из области шейки, или уретральный мазок).
Ректальные и ротоглоточные локализации инфекции C. trachomatis могут быть диагностированы путем тестирования анатомических областей, подвергшихся контакту с возбудителем. В США МАНК не одобрены Управлением по контролю за качеством пищевых продуктов и медикаментов для использования с образцами мазков из ректальной или ротоглоточной областей. Однако некоторые лаборатории соответствуют Поправкам, направленным на повышение качества анализов в клинических лабораториях (CLIA), сформулированных Центрами по контролю и профилактике заболеваний относительно требований для МАНК, и могут выполнять эти тесты. Существует также хорошее доказательство того, что эффективность NAATs при использовании мазков собранных пациентом из ректальной области, и мазков собранных врачом, является сопоставимой, поэтому метод самостоятельного забора материала для мониторинга хламидийных поражений является весьма приемлемым.
Если метод NAAT недоступен, необходимо использовать методы гибридизации и трансформации нуклеиновой кислоты, а также методы иммуноферментного анализа и прямой реакции имуннофлуоресценции.
Диагностику можно провести посредством анализа клеточной культуры (например, культивирование на среде МакКоя), однако такой подход является дорогостоящим, сложным для выполнения и требует специального оборудования. Специфичность метода близка к 100%, но чувствительность составляет от 70% до 90% в зависимости от лабораторного выполнения и особенностей забора материала. Из-за изменчивости и расходов данный тест должен использоваться только в тех случаях, когда речь идет о решении определенных юридических вопросов.
ЦКЗ рекомендует проводить эмпирическую антибиотикотерапию в качестве немедленного лечения при высоком подозрении на наличие инфекции.
| Заболевание | Дифференциальные признаки/симптомы | Дифференциальные обследования |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Основная цель лечение заключается в искоренении инфекции и наблюдении за сексуальными контактами. Отсрочка лечения может увеличить риск развития последующего бесплодия.
Азитромицин или доксициклин рекомендованы в качестве антибиотиков первой линии. Альтернативными антибиотиками являются эритромицин, офлоксацин, левофлоксацин или доксициклин отсроченного действия.
Азитромицин безопасен во время беременности и может уменьшить риск преждевременных родов, при этом беременным женщина следует избегать приема доксициклина и фторхинолонов. Альтернативные препараты, которые можно принимать во время беременности включают амоксициллин или эритромицин.
Согласно Кокрановскому обзору вмешательств для лечения генитальной хламидийной инфекции во время беременности, в эффективности и осложнениях беременности при сравнении антибактериальных препаратов (амоксициллин, эритромицин, клиндамицин, азитромицин) не было разницы; однако азитромицин и клиндамицин, судя по всему, имеют меньше побочных эффектов, чем эритромицин.
При высоком риске хламидийной инфекции, лечение следует начинать эмпирически, прежде чем станут известны результаты анализов. Пациентам рекомендуется избегать сексуальных контактов на протяжении 7 дней после начала лечения. Все сексуальные контакты в течение последних 60 дней должны быть исследованы, а партнеры должны пройти курс лечения против хламидиоза. По крайней мере пациентисточник заболевания должен проинформировать сексуальных партнеров о том, что, очевидно, у них произошел контакт с хламидийными микроорганизмами. В некоторых штатах США закон разрешает проводить ускоренную терапию партнеров (УТП), которая, по сути, является лечением сексуальных партнеров пациентов с инфекциями, передаваемыми половым путем (ИППП), без обеспечения промежуточной медицинской диагностики или профессиональной профилактической консультации.
Это может рассматриваться как вариант для облегчения процедуры лечения партнера гетеросексуальных мужчин и женщин с диагностированной хламидийной инфекцией. Американская коллегия акушеров и гинекологов выступила с заявлением, поддерживая алгоритм УТП для лечения хламидиоза и гонорейной инфекции в случаях, когда партнер не может пройти надлежащее обследование или получить соответствущую терапию другим путем.
[youtube.player]МИНИСТЕРСТВО ЗДРАВООХРАНЕНИЯ РОССИЙСКОЙ ФЕДЕРАЦИИ
Год утверждения (частота пересмотра): 2016 (пересмотр каждые 2 года)
- Российское общество дерматовенерологов и косметологов, Российское общество акушеров-гинекологов
- Инфекции, передаваемые половым путем
ВИЧ - вирус иммунодефицита человека
ДНК - дезоксирибонуклеиновая кислота
ИППП - инфекция, передаваемая половым путем
ИФА - иммуноферментный анализ
МКБ - Международная классификация болезней
ПИФ - прямая иммунофлюоресценция
ПЦР - полимеразная цепная реакция
ПЦР-РВ - полимеразная цепная реакция в режиме реального времени
РКИ - рандомизированные контролируемые исследования
РНК - рибонуклеиновая кислота
РТ - ретикулярное тельце
ЭТ - элементарное тельце
NASBA (Nucleic Acids Sequence-Based Amplification) - реакция транскрипционной амплификации
Термины и определения
Урогенитальная хламидийная инфекция - инфекция, передаваемая половым путем, возбудителем которой является Chlamydia trachomatis.
Chlamydia trachomatis - грам-отрицательная внутриклеточная бактерия, относящаяся к порядку Chlamydiales, семейству Chlamydiaceae, роду Chlamydia.
1. Краткая информация
Урогенитальная хламидийная инфекция - инфекция, передаваемая половым путем, возбудителем которой является Chlamydia trachomatis.
1.2 Этиология и патогенез
Хламидии представляют собой неподвижные, грамотрицательные бактерии, являющиеся облигатными внутриклеточными паразитами эукариотических клеток. Chlamydia trachomatis принадлежит к роду Chlamydia семейства Chlamydiacea. Серотипы Chlamydia trachomatis A, B, Ba, C являются возбудителями трахомы; D - K - урогенитального хламидиоза; L1, L2, L3 - венерической лимфогранулемы.
Хламидии существуют в двух формах, различающихся по морфологическим и биологическим свойствам. Высокоинфекционной, спороподобной, внеклеточной формой является элементарное тельце (ЭТ), а вегетативной, репродуцирующейся, внутриклеточной - ретикулярное тельце (РТ).
На первом этапе инфекционного процесса при участии электростатических сил происходит адсорбция ЭТ хламидий на плазмалемме клетки хозяина и внедрение хламидий в клетку. Участки плазмалеммы с адсорбированными на них ЭТ инвагинируются в цитоплазму с образованием фагоцитарных вакуолей. Этот этап занимает 7 - 10 часов. В клетке могут одновременно находиться несколько элементарных телец, т.е. в цитоплазме клеток может оказаться несколько микроколоний хламидий. Далее, на втором этапе, в течение 6 - 8 часов происходит реорганизация инфекционных ЭТ в метаболически активные неинфекционные, вегетативные, внутриклеточные формы - ретикулярные тельца, способные к росту и делению. Эти внутриклеточные формы, представляющие собой микроколонии, называют хламидийными включениями - тельцами Гальберштедтера-Провачека. В течение 18 - 24 часов развития они локализуются в цитоплазматическом пузырьке, образованном из мембраны клетки хозяина. На следующем этапе, в течение 36 - 42 часов происходит процесс созревания, через переходные (промежуточные тельца), и трансформации РТ путем деления в ЭТ. ЭТ путем разрушения инфицированной клетки выходят из нее. Освободившиеся и находящиеся внеклеточно ЭТ через 48 - 72 часа снова проникают в новые клетки хозяина, где начинается новый цикл развития хламидий. В случае воздействия неблагоприятных условий, например, применения неадекватных доз антибактериальных препаратов, хламидии могут трансформироваться в L-формы, обладающие слабой антигенной способностью воздействовать на иммунокомпетентные клетки. При бессимптомном течении хламидийной инфекции происходит высвобождение ЭТ из инфицированной клетки через узкий ободок цитоплазмы. При этом клетка может сохранять свою жизнеспособность.
Хламидии обладают тропизмом к цилиндрическому эпителию и способны поражать слизистую оболочку уретры, цервикального канала, прямой кишки, ротоглотки и конъюнктивы глаз. У взрослых женщин микроорганизмы не способны размножаться в неизмененном многослойном плоском эпителии влагалища, т.к. проявляют высокую чувствительность к кислой среде его содержимого, поэтому первичным очагом поражения, как правило, является слизистая оболочка шейки матки. У детей и подростков хламидии могут вызывать поражение слизистых оболочек вульвы и влагалища, чему способствуют анатомо-физиологические особенности репродуктивной системы девочек (несовершенность физиологических защитных механизмов, небольшое количество слоев поверхностного эпителия, щелочная реакция вагинального отделяемого).
Инфицирование взрослых лиц происходит при любых формах половых контактов с больным хламидийной инфекцией, детей - перинатальным путем и при половом контакте; в исключительных случаях девочки младшего возраста могут инфицироваться при нарушении правил личной гигиены и ухода за детьми.
Урогенитальная хламидийная инфекция является широко распространенной инфекцией, передаваемой половым путем (ИППП). По оценкам Всемирной организации здравоохранения, ежегодно 131 миллион человек инфицируются Chlamydia trachomatis. Распространенность хламидийной инфекции в популяции варьирует в зависимости от возраста, при этом наиболее высокая заболеваемость отмечается у лиц моложе 25 лет.
В Российской Федерации заболеваемость хламидийной инфекцией в 2015 году составила 41,3 случаев на 100000 населения: у лиц в возрасте от 0 до 14 лет - 0,5 случаев на 100000 населения, у лиц в возрасте 15 - 17 лет - 44,7 случаев на 100000 населения, у лиц в возрасте старше 18 лет - 49,7 случаев на 100000 населения. Однако эти цифры скорее отражают неполную регистрацию заболевания, чем реальную заболеваемость.
1.4 Кодирование по МКБ 10
Другие хламидийные болезни, передающиеся половым путем (A56):
A56.0 - Хламидийные инфекции нижних отделов мочеполового тракта;
A56.1 - Хламидийные инфекции органов малого таза и других мочеполовых органов:
Хламидийный(ые): эпидидимит (N51.1*), воспалительные заболевания органов малого таза у женщин (N74.4*), орхит (N51.1*);
A56.2 - Хламидийная инфекция мочеполового тракта, неуточненная;
A56.3 - Хламидийная инфекция аноректальной области;
A56.8 - Хламидийные инфекции, передаваемые половым путем, другой локализации;
1. Хламидийные инфекции нижних отделов мочеполового тракта:
[youtube.player]
Урогенитальная хламидийная инфекция – одна из наиболее распространенных форм инфекций, передаваемых половым путем, которая вызывается первичным патогеном человека – Chlamydia trachomatis. Заболевание привлекает внимание не только дерматовенерологов, но и акушеров-гинекологов. Объясняется это тем, что хламидии относятся к одной из самых частых причин уретритов и эндоцервицитов у женщин, восходящих воспалительных процессов мочеполовых органов, перигепатитов, поражения прямой кишки и других патологических состояний.
По данным литературы, частота обнаружения C. trachomatis среди женщин репродуктивного возраста в среднем составляет 2-11% [1; 2]. В Европе на сегодняшний день она является самой частой бактериальной инфекцией, передающейся половым путем [3]. По данным ВОЗ, частота обнаружения C. trachomatis у беременных колеблется в пределах от 2% до 37%, в среднем составляя 7%, и достигает 70% у пациенток с хроническими воспалительными заболеваниями органов малого таза [1; 2; 4].
Последние исследования, включающие скрининг экстрагенитальных участков беременных, являются новой практикой во многих странах [4; 5]. Подобная практика, подчеркивая распространенность хламидийной инфекции в ротоглотке и прямой кишке женщин, позволяет судить о гораздо большем количестве беременных, зараженных данной инфекцией. При этом у беременных женщин, которые занимаются оральным и анальным сексом, ротоглотка и прямая кишка служат скрытыми резервуарами для передачи инфекции [5].
Данные о влиянии Chlamydia trachomatis на течение и исход беременности противоречивы. Результаты некоторых рандомизированных контролируемых исследований (РКИ) указывают на то, что наличие урогенитальной хламидийной инфекции половых путей у матери может приводить к повышению частоты случаев невынашивания беременности, мертворождений, неонатальной пневмонии, преждевременных родов, преждевременного разрыва плодных оболочек, к развитию эндометрита и сальпингита в послеродовом периоде, а также к рождению детей с низкой массой тела [1; 2]. В других исследованиях связь хламидийной инфекции с неблагоприятными исходами беременности не была доказана [3].
Учитывая высокую частоту инфицирования C. trachomatis у беременных и значение данного патогена в развитии возможных осложнений у матери и плода, целесообразность антибактериальной терапии хламидийной инфекции в период беременности в настоящее время не вызывает сомнений.
Лечение беременных, больных урогенитальной хламидийной инфекцией, осуществляется акушерами-гинекологами (или дерматовенерологами при участии акушеров-гинекологов) на любом сроке беременности антибактериальными препаратами с учетом их влияния на плод. Однако вопросы, связанные со сложным выбором препаратов в терапии данного контингента больных, продолжают привлекать внимание научных исследователей, оставаясь важной медико-социальной проблемой [6; 7].
Европейское агентство по оценке лекарственных средств (англ. European Medicines Agency (EMEA)) в настоящее время наметило конкретные требования к критериям отбора лекарственных средств, для которых необходим активный эпидемиологический надзор во время беременности, руководство по мониторингу случайного или предполагаемого воздействия лекарственных препаратов во время беременности и конкретные требования к отчетности и представлению данных о неблагоприятных исходах их воздействия во время беременности [8].
В России подобных требований нет, напротив, различные стандарты лечения и клинические рекомендации порой противоречат не только зарубежным руководствам, но и друг другу. Так, например, в последних отечественных клинических рекомендациях дерматовенерологов (2015) есть ряд нарушений в разделе лечения хламидийной инфекции, которые не соответствуют мировым стандартам [9].
В связи с вышеизложенным считаем важным выяснить, какой из препаратов по факту сегодня чаще всего назначают в лечении хламидийной инфекции беременных практикующие акушеры-гинекологи, каких рекомендаций придерживаются и оправдан ли их выбор.
Проанализировать обоснованность выбора акушерами-гинекологами отдельных антибактериальных препаратов в терапии урогенитальной хламидийной инфекции у беременных женщин.
Материалы и методы исследования
Нами был проведен ретроспективный анализ 210 историй болезней (родов) беременных женщин с сопутствующим диагнозом: урогенитальная хламидийная инфекция. Все женщины в течение последних трёх лет находились на стационарном лечении в отделениях патологии беременности краевого клинического перинатального центра и различных других государственных медицинских учреждений г. Ставрополя.
Большинство женщин относилось к возрастной группе от 22 до 35 лет.
Во всех случаях (согласно медицинской документации) диагноз хламидийной инфекции был установлен женщинам на основании лабораторной диагностики. При этиологическом обследовании использовались ПЦР, ПЦР Real Time. Проводились и культуральные исследования для определения Tr. vaginalis и N. gonorrhoeae.
Контрольная ПЦР-диагностика проводилась спустя месяц после окончания терапии.
Статистическую обработку результатов проводили на персональном компьютере с помощью пакета прикладных программ StatSoft Statistica v10 Russian Portable 10.0.1011.0x86.
Результаты и обсуждение
Согласно проведённому анализу медицинской документации у 83 беременных (39,5%) отмечалось отсутствие субъективных симптомов заболевания, в то время как в остальных 127 случаях (60,5%) пациентки предъявляли жалобы на выделения из влагалища, зуд, жжение и дискомфорт в области наружных половых органов.
Из 127 женщин с жалобами на выделения хламидийный цервицит был описан у 103 (81,1%), при этом его клиническая картина чаще была представлена в виде незначительных выделений слизистого характера из канала шейки матки, иногда слизисто-гнойных, сопровождаемых умеренными выделениями из влагалища. Шейка матки у всех была гиперемирована, отечна. У 78 (61,4%) беременных цервицит сочетался с уретритом, поражением парауретральных желез или дизурией. У части женщин наблюдалось обострение процесса: повышалась температура тела до 38-39 °С, наступал озноб.
Во всех случаях терапия, направленная на лечение урогенитальной хламидийной инфекции, была проведена женщинам на сроках беременности больше 12 недель. Международные наименования оригинальных антибактериальных препаратов в зависимости от частоты их назначаемости акушерами-гинекологами отражены на рисунке 1.
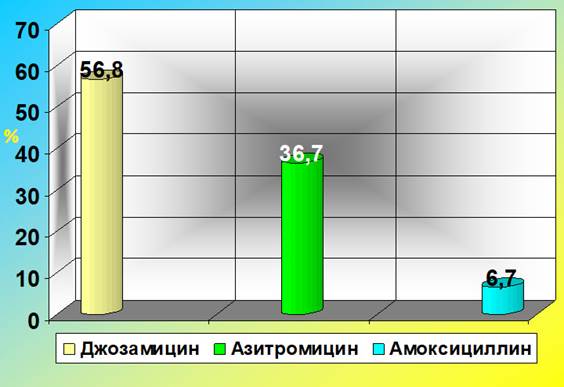
Рис. 1. Выбор акушерами-гинекологами препаратов для лечения хламидийной инфекции у беременных (2015-2017 гг.)
Как видно из рисунка, в 119 из 210 случаев (56,8%) терапия урогенитальной хламидийной инфекции у беременных проводилась джозамицином. Его назначали в дозировке 500 мг 3 раза в день в течение 10 дней. В 77 случаях (36,7%) препаратом выбора стал азитромицин в дозировке 1 г на однократный приём. В остальных 14 случаях (6,7%) терапия проводилась амоксициллином в дозировке 500 мг 3 раза в день 10 дней (при непереносимости макролидов).
Таким образом, по факту назначения беременным, больным урогенитальной хламидийной инфекцией, в отделениях патологии беременности на первое место вышел джозамицин. Однако оправдан ли такой выбор врачей и есть ли доказательная база данного препарата в лечении беременных с данной патологией? Мы считаем, что нет.
При назначении препарата важно учитывать силу рекомендаций (A-D) (рис. 2). Кроме того, следует помнить, что в лечении беременных рейтинг препаратов должен снижаться на одну ступень.
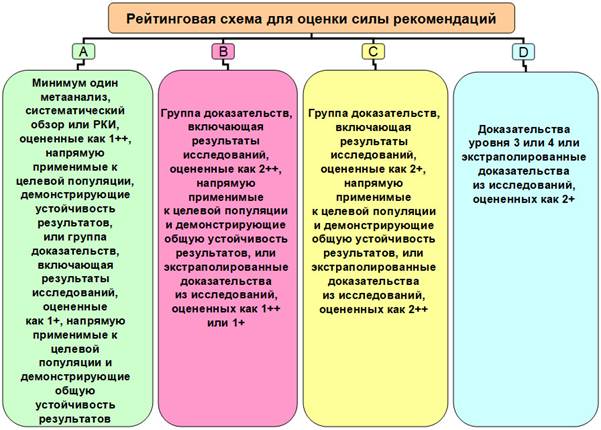
Рис. 2. Рейтинговая схема для оценки силы рекомендаций (A-D)
Согласно Европейским рекомендациям по диагностике и лечению инфекций, вызываемых Chlamydia trachomatis (2013), однократное назначение азитромицина и семидневный курс доксициклина обладают одинаковой эффективностью (класс рекомендаций А, уровень обоснованности I). Метаанализ, в который вошли 587 беременных, показал, что азитромицин, эритромицин и амоксициллин обладают одинаковой эффективностью [10]. Однако в группе, получавшей азитромицин, побочные эффекты встречались гораздо реже [10]. Следовательно, препаратом выбора при лечении урогенитальной хламидийной инфекции у беременных является азитромицин, допустимо назначение амоксициллина. Эритромицин для лечения беременных не рекомендуется. А что касается джозамицина, то он не был включен в Европейские рекомендации (2013) ни в схему выбора, ни даже в альтернативную схему лечения беременных.
Подтверждает это и Европейское руководство по борьбе с хламидийной инфекцией (2015), где азитромицин указан препаратом выбора, в то время как джозамицин также отсутствует в схемах лечения беременных [11].
Согласно руководству по лечению заболеваний, передаваемых половым путем (2015), центров по контролю и профилактике заболеваний США (Centers for Disease Control and Prevention, CDC) единственным препаратом выбора при лечении урогенитальной хламидийной инфекции у беременных является азитромицин, который считается наиболее безопасным и эффективным средством. Доксициклин не включен в схему лечения, так как, по данным этого же руководства, он противопоказан во втором и третьем триместрах беременности. К альтернативным препаратам отнесен амоксициллин, а джозамицин в США вообще не зарегистрирован [12].
1. Наиболее часто акушеры-гинекологи при лечении беременных, больных урогенитальной хламидийной инфекцией, назначают джозамицин (56,8%), на второе место по частоте назначения ими выходит азитромицин (36,7%), на третье – амоксициллин (6,7%). Вероятнее всего, это связано с тем, что у большинства практикующих врачей отсутствует осведомленность о рейтинговой схеме для оценки силы рекомендаций: А, В, С, Д, а также представление о стандартах лечения хламидийной инфекции у беременных в развитых странах.
2. Назначения препаратов акушерами-гинекологами больше всего соответствуют отечественным клиническим рекомендациям дерматовенерологов (2015). И хотя клинические рекомендации не обладают юридической силой, оставаясь лишь рекомендациями, практикующие врачи часто доверяют им, забывая, что любые возможные неблагоприятные исходы назначения тех или иных лекарственных средств будут возлагаться именно на назначающих их врачей.
[youtube.player]Читайте также:


