Гемофильная палочка при аденоидите
В статье представлен обзор клинических исследований по изучению воспалительной патологии лимфоглоточного кольца Вальдейра–Пирогова, а именно хронического аденоидита, в педиатрической практике. Значительную роль в формировании персистенции данных патогенов
The article covers the review of clinical studies on inflammatory pathology of lymphoepithelial ring of pharynx, that is, chronic adenoiditis in pediatric practice. Significant role in formation of these pathogen persistence in nasopharynx in chronic adenoiditis belongs to the ability of the bacteria to form biofilms. Bacterial biofilms, as well as the fact of discovery of large number of bacteria inside the tissue of pharyngeal tonsil condition a lot of questions on necessity of rational therapy. Early diagnostics of the pathology and timely prescribed therapy condition prevention of complication formation and chronization of the process.
Пациенты с воспалительной патологией верхних дыхательных путей ежедневно попадают на прием к педиатрам и детским оториноларингологам. Одной из причин роста инфекционной заболеваемости верхних дыхательных путей может быть неблагоприятная эпидемиологическая ситуация по острым респираторным вирусным инфекциям (ОРВИ). Такая высокая заболеваемость ОРВИ обусловлена многообразием этиологических факторов. В настоящее время известно более 200 штаммов вирусов возбудителей гриппа и ОРВИ: аденовирусы, риновирусы, гриппа, парагриппа, реовирусы, бокавирусы, респираторно-синцитиальный вирус (РСВ) и др. Ведущее место по распространенности в детском возрасте среди всех заболеваний верхних дыхательных путей занимают воспалительные заболевания органов лимфоглоточного кольца Вальдейра–Пирогова. Особое внимание уделяется глоточной миндалине, при этом хронический аденоидит занимает ведущее место в структуре ЛОР-патологии в дошкольном возрасте и составляет 20–50% патологии верхних дыхательных путей (ВДП) [1].
Характерные для детского возраста морфофункциональная незрезлость дыхательного тракта, формирование микробиоценоза слизистых оболочек ВДП, а также становление иммунных механизмов определяют склонность к воспалительным заболеваниям ВДП [2]. Анатомо-физиологические особенности и незрелость иммунной системы, а именно низкий уровень синтеза секреторного иммуноглобулина А и низкий синтез провоспалительных цитокинов Th1, предрасполагают к развитию острой и хронической ЛОР-патологии.
Глоточная миндалина имеет большое значение в создании защитного барьера ВДП, а также в становлении местного и системного иммунитета ребенка. Гипертрофия лимфоидных органов глотки и носоглотки в детском возрасте рассматривается как ответ на респираторную антигенную вирусно-бактериальную нагрузку, а длительное сохранение патогенных микроорганизмов на лимфоидных органах характерно для персистирующих вирусных инфекций [3–6].
Гипертрофия аденоидных вегетаций — это стойкое увеличение размера глоточной миндалины, приводящее к стойкой или повторяющимся эпизодам затяжной назофарингеальной обструкции, которая помимо затруднения носового дыхания нередко сопровождается другими осложнениями. В зависимости от доли, занимаемой глоточной миндалиной в полости носоглотки, выделяют три степени:
- I степень — аденоидная ткань занимает не более 1/3 просвета носоглотки, при отсутствии воспалительных изменений у детей клинического значения не имеет и является нормальным состоянием глоточной миндалины.
- II степень — аденоидная ткань занимает более 1/3, но менее 2/3 просвета носоглотки; имеет клинические проявления при пролабировании ткани глоточной миндалины в просвет хоан (хоанальный синдром), что приводит к умеренному, но стойкому затруднению носового дыхания, или при выраженном латеральном варианте роста с блоком носоглоточного устья слуховой трубы, что может проявляться рецидивирующей или хронической патологией среднего уха.
- III степень — аденоидная ткань занимает более 2/3 просвета носоглотки; имеет основное клиническое значение.
Необходимо отметить, что размер глоточной миндалины напрямую не имеет прямой корреляции с наличием воспалительных изменений в носоглотке. Так, выраженные клинические проявления хронического аденоидита часто отмечаются у детей с аденоидами I степени. И наоборот, часто аденоиды II, а иногда III степени не имеют клинических проявлений и при отсутствии хронического воспаления сохраняют свои физиологические функции [7].
Хронический аденоидит — это хроническое полиэтиологическое заболевание с преобладающей симптоматикой постназального синдрома, в основе которого лежит нарушение физиологических иммунных процессов глоточной миндалины. При этом нет единого мнения о длительности воспалительного процесса, при котором данные изменения можно считать хроническими. Учитывая, что во всем мире оториноларингологи не рассматривают хронический аденоидит как отдельную нозологическую форму, а выделяют лишь гипертрофию аденоидных вегетаций или при наличии воспалительных изменений в носоглотке хронический риносинусит, то, согласно W. Fokkens, V. Lund, J. Mullol и соавт., наиболее корректно говорить о хроническом аденоидите при сохранении клинических проявлений заболевания более 12 недель.
Другой ответ на патогенную нагрузку организма — активация мукоцилиарного клиренса, гиперсекреция слизи, вырабатываемой клетками слизистой оболочки, в состав которой входят иммуноглобулины и ферменты (лизоцим, лактоферрин). Стараясь уничтожить патогенный микроорганизм, в слизистой оболочке развивается воспалительный процесс, изменяется состав секрета, увеличивается фракция геля, что обеспечивает формирование вязкости экссудата [7]. Более того, длительное присутствие внутриклеточных патогенов и персистирующих вирусных инфекций на слизистой оболочке полости носа, а затем носоглотки предрасполагает к развитию вторичной бактериальной микрофлоры, формируя сочетанную вирусно-бактериальную патогенную флору, которая поднимается по слуховой трубе в полость среднего уха, что способствует переходу воспалительного процесса на слизистую оболочку полости среднего уха, а также к формированию того самого хронического аденоидита с хроническим экссудативным средним отитом (ЭСО), сопровождающихся гипертрофией глоточной миндалины [8–12].
Хронический аденоидит с гипертрофией глоточной миндалины напрямую связан с повышенным отрицательным давлением в полости среднего уха и возникновением обструкции глоточного устья слуховой трубы, что нарушает физиологические пути транспорта отделяемого слизистой оболочки околоносовых пазух и полости носа, обеспечивает скопление назофарингеального секрета непосредственно в устье слуховой трубы. Перечисленные изменения сопровождаются уменьшением циркуляции воздуха в полостях среднего уха, быстрым снижением интратимпанального давления, парциального давления кислорода в барабанной полости, что в дальнейшем предрасполагает к формированию экссудативного среднего отита [13].
Полость среднего уха выстлана цилиндрическим ресничным эпителием респираторного типа, к которому у многих вирусов также существует тропизм, а инфицирование происходит прямым путем через слуховую трубу из полости носа и/или носоглотки [11, 14–16]. Некоторые авторы рассматривают развитие экссудативного среднего отита в связи с наличием инфекционного очага в глоточной миндалине и дальнейшим распространением на слуховую трубу [15–17].
Согласно некоторым авторам, вирусные агенты либо поражают полость среднего уха с развитием воспалительного процесса и последующим формированием экссудата, либо приводят к дисфункции слуховых труб, снижению внутритимпанального давления, а в дальнейшем к образованию выпота [19]. Из вирусных патогенов наиболее часто идентифицируются: аденовирус и РСВ, также вирус гриппа А, В и С, парагриппа и риновирусы, энтеровирусы, обладающие высокой тропностью к слизистой оболочке ВДП, в экссудате среднего уха у больных ЭСО [20, 21]. Цитопатогенное действие вирусов на мукоцилиарную систему способствует развитию дисфункции слуховой трубы и нарушению эвакуации слизи. Согласно исследованию, у 60% исследуемых пациентов с ЭСО идентифицированы вирусные нуклеиновые кислоты в экссудате среднего уха методом полимеразной цепной реакции, при этом РСВ у 3%, ЦМВ у 10%, а также сочетание аденовируса с РСВ у 10% и ЦМВ с РСВ у 7%, что подтверждает важность вирусов как этиологических патогенных факторов в развитии ЭСО [20]. Также изучена роль сочетанной вирусно-бактериальной флоры в формировании ЭСО, характеризующая длительное, рецидивирующее течение заболевания и способствующая хронизации воспалительного процесса [22].
Из бактериальных возбудителей наиболее часто идентифицируются при воспалительных патологиях ВДП: Hemophilus influenza, Streptococcus pneumoniae, Moraxella catarrhalis и др. Важным вопросом на сегодняшний день остается роль ведущего бактериального патогена при хроническом аденоидите у детей. По мнению одних исследователей, ведущим в развитии хронического воспаления в носоглотке считают Streptococcus pneumoniae (В. К. Таточенко, 2008). По данным I. Brook и соавт. (2001) c поверхности глоточной миндалины наиболее часто получали Hemophilus influenzae (64,4%), Moraxella catarrhalis (35,6%) и Staphylococcus aureus (33,3%). В другом исследовании у детей с хроническим аденоидитом Streptococcus pneumoniae обнаружен в 50% случаев, гемофильная палочка — в 66,7% [23].
По данным исследования C. D. Lin и соавт. (2011) Staphylococcus aureus был самым часто выделяемым патогеном (21,2%) из носоглотки у детей с хроническим аденоидитом.
Ряд исследований описывают возможность большинства патогенных и условно-патогенных микроорганизмов к образованию биопленок. По современным представлениям, в этиологии хронического аденоидита большое значение придают хронической бактериальной инфекции, одним из маркеров которой являются именно бактериальные биопленки. Это форма существования микроорганизмов в сообществах, характеризующихся клетками, которые прикреплены к поверхности или друг к другу и покрыты неким экзополисахаридным матриксом (гликокаликс), вырабатываемым самими микробами. Биопленки, включающие множество видов микроорганизмов, составляют комплексы с высокоорганизованной структурой. По данным современной литературы, именно биопленки являются причиной рецидивирующего и хронического течения инфекционно-воспалительных процессов [23, 24].
Рост устойчивости микроорганизмов к антибактериальным препаратам, развитие иммуносупрессии и дисбиоза являются одной из актуальных проблем современной медицины [25].
Одним из путей решения вышеописанных проблем является клиническое применение иммуномодулирующих препаратов, обладающих способностью стимулировать системный (врожденный и приобретенный) иммунитет.
Эта группа препаратов воздействует на клеточное и гуморальное звенья иммунитета, формируя специфический иммунный ответ, активируя факторы неспецифической защиты (лизоцим, муцин, лактоферрин, мукоцилиарный клиренс). Доказано, что иммуномодулирующие препараты снижают частоту острых респираторных инфекций и рецидивов хронических заболеваний, обеспечивают эрадикацию возбудителя, быстрое и полное выздоровление, повышают эффективность этиотропного медикаментозного лечения, способствуют уменьшению антибиотикорезистентности.
Бактериальные лизаты — наиболее изученная и эффективная группа иммуномодулирующих препаратов. Лизаты представляют смесь антигенов инактивированных бактерий — наиболее распространенных возбудителей инфекционных заболеваний ВДП.
Системный препарат бактериальных лизатов ОМ-85 (Бронхо-Мунал, Бронхо-Ваксом), содержит лизаты 21 штамма 8 видов бактерий, наиболее часто вызывающих воспалительные процессы в дыхательных путях: Streptococcus pyogenes, Streptococcus pneumoniae, Streptococcus viridans, Staphylococcus aureus, Haemophilus influenzae, Klebsiella pneumoniae, Klebsiella ozaenae, Moraxella catarrhalis. ОМ-85 может применяться в составе комплексной терапии при острой респираторной инфекции с целью увеличения сопротивляемости организма к вирусным и бактериальным инфекциям дыхательных путей, уменьшения частоты острых инфекций дыхательных путей, и, как следствие, снижения риска развития бактериальных осложнений. Противопоказано применение препарата в случае индивидуальной чувствительности к компонентам препарата, беременности и в периоде лактации. Детские формы препаратов ОМ-85 применяются у детей с 6 месяцев до 12 лет, взрослые формы — у детей с 12 лет и взрослых. Схема приема препарата: один раз в сутки утром натощак. В случае детского возраста, когда пациент испытывает трудности при глотании целой капсулы, врачи допускают и рекомендуют высыпать ее содержимое в емкость с небольшим количеством воды комнатной температуры. Для профилактики инфекционных заболеваний верхних и нижних дыхательных путей препарат ОМ-85 применяют тремя десятидневными курсами, соблюдая межкурсовые интервалы в 20 дней. Полный курс профилактики занимает 3 месяца. Следует отметить, что препарат совместим с другими лекарственными средствами, в том числе разрешено применение совместно с антибактериальной терапией.
Существует ряд научных работ, свидетельствующих об оправданном применении и его эффективности [26–28]. Согласно исследованию D. Gomez Barreto, препарат безопасен в детском возрасте, а также ускоряет лечение в комплексной терапии с антибиотиками и улучшает процесс выздоровления подострого синусита, способствует снижению частоты респираторных инфекций в последующем [26]. Более современное ретроспективное исследование, изучающее профилактику рецидивирующего тонзиллита в детском возрасте, описывает уменьшение частоты рецидивов патологического процесса и снижение риска проведения тонзилэктомии. 131 пациент — претенденты на тонзилэктомию по показателю частоты возникновения острого тонзиллита — получали ОМ-85 в течение 10 дней в месяц в течение 3 последовательных месяцев, 80% из них получали профилактический курс антибиотика в течение первого месяца приема ОМ-85. Пациенты находились под наблюдением в течение 6 месяцев, включая период приема ОМ-85. В результате у 75,6% пациентов был получен положительный ответ на терапию ОМ-85: 51,2% полный ответ (снижение частоты заболевания более, чем на 50%) и 24,4% частичный ответ (снижение частоты заболевания менее, чем на 50%). Различия в группах были достоверны (р
Е. П. Карпова 1 , доктор медицинских наук, профессор
К. Ю. Бурлакова
ГБОУ ДПО РМАНПО МЗ РФ, Москва
Д.А. Тулупов, Е.П. Карпова
Российская медицинская академия последипломного образования, Москва, Российская Федерация Представлен обзор результатов клинических исследований по изучению роли патогенной бактериальной флоры в этиологии хронического аденоидита у детей. Согласно литературным данным, основной причиной развития хронической патологии носоглотки у детей является вирусная инфекция. При этом роль бактериальной микрофлоры в развитии хронического аденоидита вторична, но весьма существенна. Основными бактериальными патогенами, выделяемыми из носоглотки детей с хроническим аденоидитом, являются Staphylococcus aureus, Haemophilus influenzae и Streptococcus pneumoniae, однако существует выраженная диссоциация в частоте выделения данных бактериальных патогенов по данным разных исследователей. Значительную роль в формировании персистенции данных патогенов в носоглотке при хроническом аденоидите играет способность бактерий к образованию биопленок. Бактериальные биопленки, а также факт обнаружения большого количества бактерий внутри ткани глоточной миндалины, обусловливают возникновение дискуссии о возможностях системной и топической антибактериальной терапии.
Ключевые слова: хронический аденоидит, бактериальная микрофлора, Staphylococcus aureus, Haemophilus influenzae, Streptococcus pneumoniae.
Хронический аденоидит (ХА) — полиэтиологическое заболевание с преобладающей симптоматикой постназального синдрома (post-nasal drip). В его основе лежит нарушение иммунных процессов глоточной миндалины. При этом отсутствует единое мнение о длительности воспалительного процесса, при котором указанные изменения можно считать хроническими. С учетом того, что оториноларингологи не рассматривают ХА как отдельную нозологическую форму, а выделяют лишь гипертрофию аденоидных вегетаций или, при наличии воспалительных изменений в носоглотке, хронический риносинусит, наиболее корректно говорить о ХА в случае сохранения клинической симптоматики заболевания более 12 нед [1].
По современным представлениям, несмотря на главенствующую роль вирусов, в этиологии ХА достаточно большое значение придают хронической бактериальной инфекции. Согласно результатам последних исследований, одним из маркеров хронической бактериальной инфекции являются бактериальные биопленки. Биопленка (от англ. biofilm) представляет собой микробное сообщество, состоящее из клеток, которые прикреплены к поверхности или друг к другу и покрыты экзополисахаридным слоем (гликокаликсом), вырабатываемым самими микробами. По данным B. Winther и соавт., на поверхности удаленных аденоидов бактериальные биопленки были обнаружены в 8 из 9 случаев [5]. В работе итальянских оториноларингологов при исследовании 16 образцов небных миндалин и аденоидов и 24 образцов слизистой оболочки, взятой при вскрытии клеток решетчатого лабиринта у пациентов с хроническим риносинуситом, биопленки были обнаружены в 57,5 и 41,7% случаев, соответственно [6]. В отличие от ХА роль бактерий в гипертрофии аденоидных вегетаций дискутабельна. В частности, по данным J. Coticchia и соавт., у пациентов с ХА биопленки были обнаружены в 94,9% случаев, тогда как на образцах ткани глоточной миндалины, удаленной у пациентов с синдромом обструктивного апноэ сна, — только в 1,9% [7]. Способность бактериальных патогенов к образованию биопленок во многом обусловливает неэффективность антибактериальной терапии при попытке плановой санации носоглотки. При этом считают, что клинические признаки обострения хронического процесса связаны с увеличением количества планктонных форм бактерий, подавление роста которых можно считать обоснованием применению антибактериальных средств [8, 9].
Важным вопросом в настоящее время остается вид основного бактериального патогена при ХА у детей. По мнению одних исследователей, им является Streptococcus pneumoniae (пневмококк) [10, 11]. Согласно другим, главенствующие бактериальные патогены при ХА — это представители грамотрицательной флоры Haemophilus influenzae и Moraxella catarrhalis. По данным I. Brook и соавт., при исследовании материала c поверхности глоточной миндалины наиболее часто обнаруживали H. influenzae (64,4%), M. catarrhalis (35,6%) [12]. В другом исследовании у детей с ХА гемофильная палочка обнаружена в 66,7% случаев [13]. Однако наибольшее число авторов указывают на ведущую роль Staphylococcus aureus в развитии ХА у детей. К примеру, по данным C. D. Lin и соавт., S. aureus был наиболее часто выделяемым патогеном (21,2%) из носоглотки у детей с ХА [14]. По данным M. Emaneini и соавт. [15], частота идентификации S. aureus составила 23%. Согласно результатам отечественных исследований, частота обнаружения S. aureus при исследовании материала с поверхности глоточной миндалины составляет 32%, из ткани — 45%, что уступает только частоте выделения пневмококка [10].
По нашим данным, основным бактериальным патогеном при ХА является золотистый стафилококк, выделяемый с поверхности глоточной миндалины почти у 50% детей. В группе детей с гастроэзофагеальной рефлюксной болезнью частота высевания S. aureus с поверхности глоточной миндалины находится на уровне 70–75% [16]. Регулярный заброс кислого химуса в носоглотку при гастроэзофагеальной рефлюксной болезни приводит к нарушению работы механизмов местного иммунитета (в первую очередь мукоцилиарной системы), что создает благоприятные условия для колонизации и роста патогенной бактериальной микрофлоры (рис.).
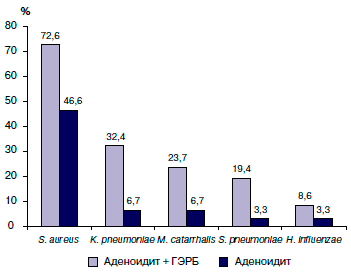
Рис. Частота высеваемости высокопатогенной микрофлоры с поверхности глоточной миндалины у детей с хроническим аденоидитом, ассоциированным и не ассоциированным с гастроэзофагеальной рефлюксной болезнью
Примечание. ГЭРБ — гастроэзофагеальная рефлюксная болезнь.
Согласно последним сведениям, роль грибковой микрофлоры в развитии хронической патологии носоглотки не подтверждена [17]. В отечественной литературе встречаются единичные работы, результаты которых свидетельствуют о вкладе микотической инфекции в развитие ХА. Так, по данным А. И. Мачулина, в 33,3% случаев у детей с ХА имеет место грибково-бактериальная ассоциация [18].
Убедительные фактические данные о значимой роли атипичных возбудителей (Chlamydophila pneumoniae, Mycoplasma pneumoniae) в развитии ХА в настоящее время отсутствуют [17]. Мнения зарубежных исследователей по этому вопросу достаточно противоречивы. Например, в работе G. P. Pintucci и соавт. при исследовании 55 образцов ткани глоточной и небных миндалин M. pneumoniae обнаружены в 10,9% случаев, C. pneumoniae — в 18,2% [19], а в исследовании L. Drago и соавт. в 44 образцах ткани аденоидов C. pneumoniae обнаружены только в 4,8% случаев, тогда как M. pneumoniae не обнаружены вовсе [20].
Вопрос о консервативном лечении ХА достаточно сложен, поскольку не существует каких-либо жестких стандартов его терапии. Лечение ХА, как и любого хронического заболевания, должно быть комплексным, с учетом этиопатогенеза воспалительного процесса [21].
Основным направлением современной фармакотерапии ринологической патологии в настоящее время принято считать противовоспалительную терапию. Наиболее эффективными из существующих средств с противовоспалительным эффектом являются глюкокортикоидные препараты. Так, накоплен клинический опыт применения мометазона фуроата в лечении неаллергической воспалительной ринологической патологии у детей и взрослых [1]. Однако патология носоглотки (гипертрофия аденоидных вегетаций и аденоидит) не входит в официально зарегистрированные показания к применению назального спрея мометазона фуроата.
Вторым по значимости при обсуждении схемы терапии обострений ХА является вопрос об этиотропном лечении. Учитывая главенствующую роль вирусов в развитии ХА, логичным решением было бы активное применение противовирусных средств в лечении и профилактике острых респираторных инфекций. Однако последний анализ рандомизированных клинических исследований показал сомнительную эффективность подавляющего большинства противовирусных препаратов в лечении, и особенно в профилактике острых респираторных инфекций [22].
Учитывая значимую роль патогенной бактериальной микрофлоры при обострении ХА (в особенности при гнойных его формах), необходимо обсудить вопрос о применении антибактериальных средств. При неосложненной форме аденоидита (и даже при гнойной форме, по мнению отечественных авторов) назначение системных антибактериальных лекарственных препаратов не является целесообразным [9, 23, 24]. По нашему мнению, показаниями к проведению системной антибактериальной терапии при ХА можно считать:
- осложненные формы гнойных аденоидитов (острый средний отит, острый бактериальный риносинусит);
- гнойный аденоидит с выраженным снижением качества жизни ребенка (нарушение сна) при неэффективности топической противовоспалительной терапии.
Таким образом, проблема хронических форм патологии носоглотки у детей является одной из наиболее актуальных в современной оториноларингологии и педиатрии, требующей дальнейшего изучения с целью определения единой клинически обоснованной тактики лечения. Вопрос о роли антибактериальных препаратов, как топических, так и системных, также требует дальнейших клинических исследований для разработки единых общепринятых стандартов с формулированием показаний к применению и схемы антибактериальной терапии при обострении хронического аденоидита у детей.
Здравствуйте!
Ребёнок 2-ой год ходит в сад!
в первый год она болела не значительно-в этот год стали болеть очень часто-болезнь горла и насморк(без температуры)
поставили диагноз-Хронический тонзилит
взяли мазок из носа и зева
ВЫДЕЛЕНА-Haemophilus influenza-(обильный рост!)
педиатр прописала КИП-курс 5 дней!
если ребёнок заболевает-назначила "Супракс"
Подскажите,пожалуйста-как от этой палочки избавится??
Что нужно делать?(прочитала в интернете,что она плохо поддаётся лечению даже антибиотиками-так ли это?)
спасибо большое за ответ!очень буду ждать его!
спасибо за ответ большое.
а подскажите ,пожалуйста снижает ли эта палочка местный иммунитет.
и если не трудно,подскажите. чем можно поднять иммунитет ребёнку в этом возрасте?
ликопид
анаферон
бронхоммунал
нам не помог
болеем часто.
вот опять пропили КИП-как нам прописал педиатр-опять заболели.
2. наличии заболеваний со стороны ЛОР-органов. У ребенка хронический тонзиллит и Вам необходимо регулярно посещать ЛОР-врача и выполнять его назначения.
3. наличии заболеваний со стороны желудочно-кишечного тракта. Есть ли у ребенка жалобы со стороны желудочно-кишечного тракта - боли в животе, наличие отрыжки, изжоги, повышенного газообразования? Какой характер стула? Какой аппетит? Если есть какие-то изменения со стороны желудочно-кишечного тракта, то советую обратиться к детскому гастроэнтерологу.
Вы дали информацию о медикаментозном лечении ребенка. Но кроме медикаментозного лечения очень важно правильное питание ребенка, достаточное питье, окружающая ребенка обстановка, правильный режим дня, достаточный сон, прогулки.
Очень важно для снижения заболеваемости окружающая ребенка обстановка. В помещении, где находится ребенок необходимо регулярно проводить влажную уборку. Температура воздуха должна быть не выше 22 и не ниже 18 градусов. Сухой жаркий воздух в квартире способствует высушиванию слизистой дыхательных путей и это приводит к частой заболеваемости. При сухости воздуха необходимо пользоваться увлажнителями воздуха.
Проанализируйте, где находится детская кроватка. Детская кроватка не должна стоять рядом с батареей, рядом с окном и на линии, соединяющей окно и дверь, где обязательно присутствуют сквозняки. Если в квартире есть сквозняки, то бороться с ними необходимо, заделывая щели в окнах и дверях, а не кутая ребенка. Сквозняк воздействует на дыхательные пути, а не на кожу.
Может быть у кого-то из членов семьи есть хронические заболевания носоглотки и этот человек постоянно заражает ребенка.Необходимо предпринять меры для уменьшения заболеваемости членов семьи. Если в семье кто-то заболел-принимать меры профилактики для ребенка и для здоровых членов семьи.
Подумайте, может ребенок раскрывается ночью и замерзает.
В данном возрасте дети еще не приучены к соблюдению правил гигиены и, поэтому, частая проблема -глисты. Продукты жизнедеятельности глистов аллергизируют организм, снижают иммунитет. Необходимо приучать ребенка к соблюдению правил гигиены и постоянно контролировать соблюдение этих правил. Советую обследовать ребенка на наличие глистов.
Не следует с часто болеющим ребенком ходить в общественные места (по магазинам, в кинотеатры, в гости, на выставки, на массовые гуляния и т.д.).
Гулять на улице регулярно, но не катать ребенка в коляске или на санках.
Для повышения иммунитета очень важное значение имеет правильное вскармливание. Питание должно быть разнообразным и обязательно включать молочные продукты (молоко, творог, сыр, кисломолочные продукты). Особенно полезны для повышения иммунитета кисломолочные напитки. Они обладают способностью подавлять рост возбудителей кишечных инфекций, нормализуют состав полезных микробов в кишечнике, стимулируют местный иммунитет.
Необходимо ежедневно включать в рацион ребенка кисломолочные напитки -йогурт Био Баланс, Эрмигурт с пребиотиками, Активия, Актимель, Иммунеле, ацидофилин, йогурт Агуша с омега-3 жирными кислотами. В аптеках продается закваска Нарине. Можно самим сделать кисломолочный продукт.
Мясо является источником полноценного белка, а также богато солями железа, фосфора, магния, витаминами группы В. Субпродукты (печень, сердце, язык) особенно богаты железом и другими минеральными веществами. Их рекомендуется широко использовать в питании часто болеющих детей для профилактики такого заболевания как анемия (снижение гемоглобина).
Для повышения иммунитета очень полезна в питании детей рыба нежирных сортов (треска, минтай, хек, навага) и среднежирных сортов (горбуша, карп, сельдь, лосось). Рыба содержит омега-3 жирные кислоты, необходимые для нормального функционирования иммунной системы. Специально, для повышения иммунитета у детей старше года выпускается молочная смесь "Нутрилак 12+", содержащая жирные кислоты омега-3 и омега-6. А, кроме того, в состав этой смеси входят пребиотики-олигосахариды, способствующие росту полезных бактерий в кишечнике и профилактике дисбактериоза. Смесь Нутрилак 12+включает широкий комплекс витаминов и микроэлементов и полностью обеспечивает ребенка всеми питательными веществами, необходимыми для правильного роста и развития.
Овощи, фрукты, ягоды, зелень-ценнейшие источники многих витаминов. Особенно важен для повышения иммунитета витамин С, которым богаты черная смородина, шиповник, облепиха, рябина, цитрусовые, капуста, картофель, сладкий перец (особенно красный), томаты, зелень. Каротин, из которого в отганизме образуется витамин А, содержится в моркови, томатах, тыкве, абрикосах, хурме, облепихе, морошке.
В некоторых овощах, фруктах, ягодах содержатся вещества, обладающие противомикробным и противовоспалительным действием. Ими богата черника, рябина, кизил, айва, груши, гранаты, баклажаны. А фитонциды, содержащиеся в чесноке, зеленом луке, зелени петрушки, укропе, сельдерее, кинзе оказывают выраженное противомикробное действие. Большинство фруктов и овощей богато клетчаткой, которая нормализует моторику кишечника.
Очень важен питьевой режим ребенка. Пить необходимо побольше -чай с лимоном, медом, клюквенный морс, травяные чаи (ромашка, мята, зверобой), зеленый чай, компоты из сухофруктов и свежих фруктов, соки. Необходимо исключить из рациона ребенка Пепси-Колу, Кока-Колу, фруктовые воды, Швепс, Фанту, Спрайт и другие газированные напитки, кофе.
При необходимости можно обратиться в консультативно-диагностический центр при Научном центре здоровья детей (институт педиатрии). Адрес Научного центра здоровья детей- г Москва, Ломоносовский проспект, дом 2\62. Тел регистратуры 8-499-134-03-64.
или в детский центр диагностики и лечения им Н. А. Семашко. М. Фрунзенская, ул 2-я Фрунзенская, дом 9, тел 8-499-242-00-05
Выздоравливайте. Желаю удачи.
Читайте также:


