Где лечат парапротезную инфекцию
Аннотация научной статьи по клинической медицине, автор научной работы — Гольник Вадим Николаевич, Прохоренко Валерий Михайлович, Павлов Виталий Викторович
Проведен анализ результатов лечения больных с ранней парапротезной инфекцией после эндопротезирования тазобедренного сустава с использованием тактики, направленной на сохранение имплантата и функции оперированного сустава, основанной на многоэтапной хирургической санации и клинико-лабораторном мониторинге раневого процесса. Показана эффективность выбранной тактики в 83 % случаев. На основе полученных данных предложен алгоритм лечения ранней парапротезной. инфекции при эндопротезировании тазобедренного сустава, который может быть рекомендован к широкому использованию в клинической практике.
Похожие темы научных работ по клинической медицине , автор научной работы — Гольник Вадим Николаевич, Прохоренко Валерий Михайлович, Павлов Виталий Викторович
TREATMENT OF EARLY PERIPROSTHETIC INFECTION AT HIP REPLACEMENT
We carried out the analysis of results of treatment of patients with early periprosthetic infection after total hip replacement with use of tactics aimed at the preservation of an implant and function of the operated joint, based on a multi-stage surgical rehabilitation, clinical and. laboratory monitoring of the wound healing process. The efficiency of chosen tactics in 83 % of cases was shown. Based on these results an algorithm for treatment of early periprosthetic infection at the hip replacement that can be recommended for widespread use in clinical practice was offered.
В.Н. Гольник, В.М. Прохоренко, В.В. Павлов
лечение ранней парапротезной инфекции при эндопротезировании тазобедренного сустава
Минздравсоцразвития РФ (Новосибирск)
Проведен анализ результатов лечения больных с ранней парапротезной инфекцией после эндопротезирования, тазобедренного сустава с использованием, тактики, направленной на сохранение имплантата и функции оперированного сустава, основанной на многоэтапной хирургической санации и клинико-лабораторном, мониторинге раневого процесса. Показана эффективность выбранной тактики в 83 % случаев. На основе полученных данных предложен алгоритм, лечения ранней парапротезной инфекции при эндопротезировании тазобедренного сустава, который может быть рекомендован к широкому использованию в клинической, практике.
Ключевые слова: эндопротезирование, парапротезная инфекция, имплантант-ассоциированная инфекция, инфекция области хирургического вмешательства
TREATMENT oF EARLY pERipRosTHETiC iNFECTioN AT Hip REpLACEMENT
V.N. Golnik, V.M. Prokhorenko, V.V. Pavlov
We carried out the analysis of results of treatment of patients with early periprosthetic infection after total hip replacement with use of tactics aimed, at the preservation of an implant and function of the operated, joint, based on a multi-stage surgical rehabilitation, clinical and laboratory monitoring of the wound, healing process. The efficiency of chosen tactics in 83 % of cases was shown. Based on these results an algorithm, for treatment of early periprosthetic infection at the hip replacement that can be recommended, for widespread use in clinical practice was offered.
Key words: endoprosthesis replacement, periprosthetic infection, implant-associated infection, surgical site infection
Инфекционные осложнения в ортопедии являются одними из самых грозных осложнений, которые обусловливают увеличение сроков госпитализации пациентов, приводят к инвалидизации пациентов или ее усугублению, увеличивают экономические затраты на лечение данных пациентов [2, 7, 10]. В особо тяжелых случаях данное осложнение может приводить и к летальным исходам [13].
Несмотря на относительно постоянный процент осложнений (0,5 — 6 %), наблюдаемое повышение общего числа артропластик привело к более высокому общему количеству инфекций [1]. Основные сложности по-прежнему обусловлены трудностью идентификации возбудителя, сложностью лечения и тяжестью последствий хирургической инфекции. В основе патогенеза парапротез-ной инфекции лежит способность возбудителей формировать биопленки как на имплантате, так и на поверхности раны, что является одной из основных причин неудовлетворительных результатов лечения пациентов с имплантат-ассоциированной инфекцией [4, 5, 9].
фективность хирургической санации при острой парапротезной инфекции, по данным разных авторов значительно варьирует в пределах 18 — 83 % случаев [2, 3]. Ряд авторов подчеркивает важность динамического мониторинга раневого процесса и контроля санации путем этапных санационных мероприятий, позволяющих отследить динамику раневого процесса и определить тактику лечения. При этом необходимо обеспечить действие активного антимикробного агента между этапами хирургической санации [2, 3, 6].
Цель работы: Улучшить результаты лечения пациентов с ранней парапротезной инфекцией после эндопротезирования тазобедренного сустава на основе разработанного алгоритма.
материалы и методы
Исследование основано на ретро- и проспективном анализах группы пациентов, пролеченных за период 2007 — 2010 гг., общей численностью 2516 человек, из них группа пациентов с ранней парапротезной инфекцией, развившейся после первичного и ревизионного эндопротезирования тазобедренного сустава, составила 50 человек (1,6 %).
К ранней парапротезной инфекции отнесены случаи развития инфекционного процесса в сроки до 3 месяцев с момента операции [3]. Для клинической картины было характерно острое начало, с локальными признаками воспаления в виде отёка, гиперемии, локального повышения температуры, усиления болевого синдрома в раннем послеоперационном периоде.
По локализации выделяли поверхностные и глубокие формы инфекции, разделение осуществляли по анатомическому признаку, границей служила широкая фасция бедра.
Поверхностная парапротезная инфекция отмечена у 15 (0,59 %) пациентов (проявлялась в виде лигатурных свищей, некроза кожных покровов и расхождением краев раны, подкожной гематомы).
Глубокая парапротезная инфекция зарегистрирована у 35 (1,15 %) больных (проявлялась в свищевой форме, в виде инфицированной субфас-циальной гематомы, в форме некроза парапротез-ных тканей).
Лечение группы пациентов с глубокой пара-протезной инфекцией проводили согласно разработанной в отделении методике, направленной на сохранение стабильного имплантата.
При отсутствии признаков нестабильности компонентов эндопротеза действовали в зависимости от состояния местных тканей. При невыраженных местных воспалительных явлениях, отсутствии патологических грануляций, очагов некроза, налета фибрина выполнялась одномоментная вторичная хирургическая обработка раны с последующим ушиванием. В случае выраженных воспалитель-
Последующие этапы хирургической санации также выполнялись в условиях операционной под наркозом с интервалом 1—2 дня. Края раны разводили, удаляли сорбент, производили ревизию раны. При этом оценивалась клинически динамика раневого процесса: наличие и характер раневого экссудата, наличие патологического отделяемого, состояние тканей, распространенность некрозов, наличие и выраженность грануляций. Также производился забор биоптатов для бактериологического исследования. Хирургическая санация и тампонада раны сорбентом выполнялась по принципу, описанному выше.
Продолжительность лечения и количество санаций определялось эффективностью проводимых мероприятий. Клиническим критерием эффективности служили снижение температуры, уменьшение отека тканей. В ране такими критериями являлись появление ярких, отчетливо выраженных грануляций, отсутствие очагов некроза, фибрина. Бактериологическим критерием служил отрицательный результат микробиологического исследования. В оценке динамики раневого процесса критерием эффективности являлось появление воспалительно-регенераторного и регенераторно-воспалительного типа цитограмм в мазках-отпечатках. В лабораторных показателях крови оценивали динамику снижения маркеров воспаления: лейкоцитоз, скорость оседания эритроцитов, С-реактивный белок, фибриноген. Устойчивое снижение описанных показателей являлось показанием для заключительного этапа, на котором производили замену модульных компонентов эндопротеза, дренирование раны, выполнялся отсроченный вторичный шов раны.
Всем пациентам проводилась этиотропная антибактериальная терапия согласно чувствительности возбудителя, нутритивная поддержка сбалансированными питательными смесями, гемотрансфузия и инфузионная терапия производились по показаниям.
результаты и обсуждение
По данным бактериологического исследования наиболее частым возбудителем являлся стафи-
лококк, выделенный в 15 случаях: метициллин-резистентный S. Aureus (MRSA) — 5; метициллин-чувствительный S. Aureus — 4; метициллин-чувствительный S. Epidermidis — 4; S. saprophyti-cus — 1; Enterococcus — 7; E. Coli — 4; Aeruginosa — 4; Proteus — 1; Alcoligenes — 1; Acinetobacter — 1. В 4 случаях отмечалась смешанная флора или смена возбудителя. В 14 случаях при наличии клинической картины раневой инфекции возбудитель не выявлен.
Из 35 пациентов с глубокой парапротезной инфекцией этапная хирургическая санация применялась у 30 человек, при этом у 2 пациентов в качестве подготовительного этапа для хирургического закрытия раны и санации после удаления эндопротеза в связи с выраженными воспалительными изменениями в тканях, их деструкцией и бесперспективностью сохранения имплантата. В 28 случаях глубокой парапротезной инфекции этапная хирургическая санация применена с целью сохранения эндопротеза при отсутствии признаков не-
стабильности. Вторичная хирургическая обработка раны с одномоментным закрытием раны при отсутствии признаков нестабильности эндопротеза использована в 4 случаях. В 1 случае ранней глубокой парапротезной инфекции тазобедренного сустава произведено удаление нестабильного эндопротеза с одномоментным закрытием раны. Применение методики многоэтапной хирургической санации с использованием сорбционного перевязочного материала на основе полиакрилата при глубокой форме ранней парапротезной инфекции со стабильным эндопротезом позволило в 21 случае из 28 купировать признаки инфекционного процесса и достичь стойкой ремиссии, что составило 75 % (сроки наблюдения — от 18 месяцев до 5 лет). В 7 случаях имел место рецидив инфекции, в результате чего было произведено удаление эндопротеза.
При поверхностной форме парапротрезной инфекции после эндопротезирования тазобедренного сустава из 15 пациентов этапная хирургическая санация проводилась у 13 пациентов, в 2 случаях
Рис. 1. Алгоритм лечения ранней парапротезной инфекции.
выполнена вторичная хирургическая обработка раны одномоментно. Во всех случаях хирургического лечения поверхностной парапротезной инфекции получена стойкая ремиссия. Таким образом, многоэтапная хирургическая санация использована у 41 пациента с ранней парапротезной инфекцией в условиях стабильного имплантата и оказалась эффективной в 34 случаях (83 %).
При анализе 11 случаев удаления эндопротеза при ранней парапротезной инфекции установлено, что основными возбудителями инфекции являлись MRSA и грамотрицательная микрофлора, в 5 случаях исходно имелся высокий риск инфекционных осложнений в связи с выраженным рубцовым перерождением тканей после перенесенных оперативных вмешательств и травм области тазобедренного сустава.
Анализ полученных результатов позволил разработать алгоритм лечения парапротезной инфекции при эндопротезировании тазобедренного сустава, согласно которому применение тактики, направленной на сохранение эндопротеза оправдано при: 1) манифестации инфекции не позднее 12 недель с момента эндопротезирования сустава; 2) высокой чувствительности возбудителя к антибиотику; 3) отсутствии признаков нестабильности эндопротеза (рис. 1). Использование методики этапной хирургической санации показало свою эффективность в 83 % случаев лечения ранней парапротезной инфекции и позволило сохранить имплантат.
1. Ахтямов И.Ф., Кузьмин И.И. Ошибки и осложнения эндопротезирования тазобедренного сустава: руководство для врачей. — Казань, 2006. - 328 с.
2. Ключевский В.В. Хирургические методы лечения инфекционных осложнений после эндопротезирования тазобедренного сустава: автореф. дис. . канд. мед. наук. — М., 2007. — 22 с.
3. Прохоренко В.М., Павлов В.В. Инфекционные осложнения при эндопротезировании тазобедренного сустава. — Новосибирск: Наука, 2010. - 179 с.
4. Сидоренко С.В. Роль бактериальных биопленок в патологии человека // Инфекции в хирургии. - 2004. - Т. 2, № 3. - С. 16-20.
5. Donlan R.M., Costerton J.W. Biofilms: Survival mechanisms of clinically relevant microorganisms // Clinical Microbiology Reviews. - 2002. - Vol. 15, N 2. - P. 167-193.
6. Estes C.S., Beauchamp C.P., Clarke H.D., Spangehl M.J. A two-stage retention debridement protocol for acute periprosthetic joint infections // Clin. Orthop. Relat. Res. - 2010. - Vol. 468 (8). - P. 2029-2038.
7. Everts R.J., Chambers S.T., Murdoch D.R. et al. Successful antimicrobial therapy and implant retention for streptococcal infection of prosthetic joints // ANZ J. Surg. - 2004. - Vol. 74, N 4. - P. 210-214.
8. Forsberg J.A., Potter B.K., Cierny G. et al. Diagnosis and management of chronic infection // J. Am. Acad. Orthop. Surg. - 2011. - Vol. 19, Suppl. 1. -P. S8-S19.
9. James G.A., Swogger E., Wolcott R. et al. Biofilms in chronic wounds // Wound Repair Regen. -2008. - Vol. 16 (1). - P. 37-44.
10. Kienapfel H., Kuhn K.-D. The infected implant. - Springer, 2009, Springer Medizin Verlag Heidelberg, 2009.
11. Parvizi J., Azzam K., Ghanem E., Valle C.D. et al. Periprosthetic infection: A new prognostic classification // 27th Annual Meeting of the EBJIS. -Barcelona, 2008.
12. Pignatti G., Nitta S., Rani N. et al. Two stage revision in periprosthetic infection: results of 41 cases // Open Orthop. J. - 2010. - Vol. 4. - P. 193-200.
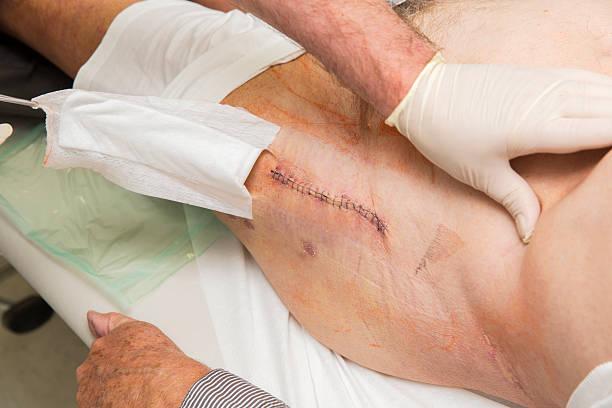
Гной в послеоперационной ране говорит о развитии инфекционных осложнений. В ортопедии и травматологии они тяжело поддаются лечению и приводят к инвалидизации пациентов. Парапротезные инфекции обусловливают увеличение срока пребывания в стационаре и требуют затрат на борьбу с ними.

Выделения из ТБС.
Инфекции после эндопротезирования бывают поверхностными или глубокими, острыми или хроническими, развиваться в раннем или позднем послеоперационном периоде. Воспалительный процесс может затрагивать только мягкие ткани нижней конечности или распространяться на прооперированный сустав.
Если после эндопротезирования у вас появился гной в шраме, повысилась температура и возникли боли в ноге – немедленно идите к врачу. Тот осмотрит вас, назначит нужные исследования и выяснит, насколько тяжелое у вас состояние. Вам придется лечь в стационар и пройти курс лечения.
Актуальность проблемы
По разным данным, частота развития ранней парапротезной инфекции после первичной замены крупных суставов составляет 0,3-0,5%, после ревизионной – 9%. Воспалительные процессы выявляют в течение первых трех недель после хирургического вмешательства.
Если говорить о частоте развития поздних инфекционных осложнений, то чаще всего они возникают в первые два года после эндопротезирования (1,63% пациентов). Реже (у 0,59% прооперированных) глубокие парапротезные инфекции развиваются в последующие 8 лет после операции.
Частота инфекционных осложнений на протяжении нескольких десятилетий остается неизменной. Однако заметно увеличилось общее количество артропластик, выросло и общее число осложнений. Поэтому становится все более актуальной их профилактика, ранняя диагностика и лечение.
Факт! Как показали научные исследования, риск развития инфекционных осложнений зависит от вида эндопротеза. Выяснилось, что в общей сумме имплантация отечественных моделей приводит к воспалению чаще (3-10% случаев), чем установка импортных (0,3-4,8%).
Что такое инфекция в области хирургического вмешательства
ИОХВ – это острое или хроническое воспаление, развивающееся в месте разреза или в области, которая подвергалась ятрогенному воздействию в ходе хирургического вмешательства. В 67% случаев инфекция затрагивает только зону операционного разреза, в 33% – распространяется на имплантированный сустав.
Факторы развития ИОХВ:
- длительность операции более 3 часов;
- технические трудности во время хирургического вмешательства;
- интраоперационная кровопотеря более 1 литра;
- нестабильность установленного эндопротеза;
- использование дополнительных синтетических и биологических материалов в ходе операции;
- наличие тяжелых хронических заболеваний.

Воспалительные процессы, которые не распространяются на прооперированный сустав, можно победить без ревизионного эндопротезирования. Если же инфекция затрагивает костную ткань, компоненты эндопротеза, остатки суставной капсулы или другие части коленного или тазобедренного сустава – лечить ее будет крайне тяжело. В этом случае больному скорее всего потребуется повторное эндопротезирование.
Существует ряд факторов, которые отягощают состояние пациента, замедляют выздоровление и ухудшают прогноз: снижение иммунитета, перенесенные операции, частое лечение антибиотиками. Стойкость обнаруженной микрофлоры к антибактериальным средствам, плохое кровообращение в области сустава, массивные гнойные очаги тоже осложняют терапию.
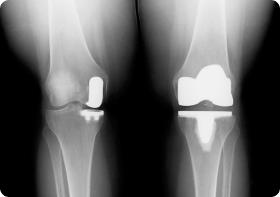
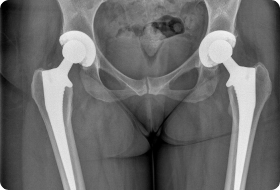
Виды парапротезной инфекции
В ортопедии и травматологии используют несколько классификаций ИОХВ. Систематизация и отнесение инфекции к конкретному виду помогает врачам оценить тяжесть состояния пациента. Классификация Coventry-Fitzgerald-Tsukayama самая распространенная.
Таблица 1. Типы глубокой парапротезной инфекции по Coventry-Fitzgerald-Tsukayama.
| Тип | Время развития | Тактика лечения | |
| I | Острая послеоперационная | 1-й месяц | Ревизия послеоперационной раны, удаление некротизированных тканей, при необходимости – замена некоторых частей эндопротеза при сохранении его основных компонентов. |
| II | Поздняя хроническая | От 1 месяца до 1 года | Обязательное ревизионное эндопротезирование. |
| III | Острая гематогенная | После 1 года | Вполне оправданной является попытка сохранить установленный протез. |
| IV | Положительные интраоперационные культуры | Бессимптомная бактериальная колонизация поверхности импланта | Консервативное лечение, заключающееся в парентеральной антибиотикотерапии на протяжении 6 недель. |
В классификации, созданной Новосибирским НИИТО, ИОХВ делят на ранние острые, поздние острые и хронические. Первые развиваются на протяжении трех месяцев после эндопротезирования, вторые – на 3-12 месяце, третьи – после 1 года. Инфекционные осложнения могут протекать в латентной, свищевой, флегмоноподобной или атипичной форме.
По распространенности инфекции бывают эпифасциальными (поверхностными) и субфасциальными (глубокими). Могут сопровождаться тотальной, бедренной или тибиальной нестабильностью.
Поверхностные и глубокие инфекции
Возникают в первый месяц после эндопротезирования. Характеризуются развитием воспаления в мягких тканях нижней конечности. Сам бедренный или коленный сустав остается интактным, то есть не вовлекается в патологический процесс. Причиной осложнения чаще всего является занесение в рану патогенных микроорганизмов во время хирургического вмешательства или в послеоперационном периоде.
- некроз кожных покровов;
- лигатурные свищи;
- расхождение краев раны;
- подкожная гематома.
- некроз парапротезных тканей;
- глубокие свищи;
- инфицированная субфасциальная гематома.
Факт! Незначительная болезненность, локальная припухлость, покраснение и гипертермия кожи в области шрама обычно указывают на поверхностную инфекцию, которая поддается лечению. Появление лихорадки, спонтанное расхождение швов и сильные боли в ноге позволяют заподозрить воспаление глубоких тканей. В этом случае прогноз менее благоприятный.
Инфекции протезированного сустава
При патологии воспаление распространяется на полости и оболочки прооперированного сустава, остатки синовиальной оболочки, кости в месте фиксации эндопротеза и прилегающие мягкие ткани. Причиной осложнения является колонизация поверхностей сустава патогенной микрофлорой. Бактерии могут попадать из внешней среды или заноситься гематогенным путем.
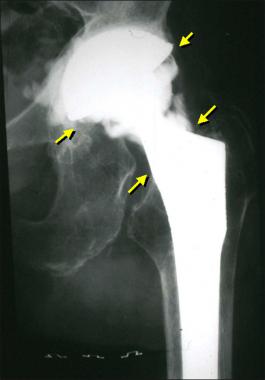
Так выглядит инфекция на рентгене.
Инфекции протезированного сустава самое грозное осложнение среди всех ИОХВ. Они не поддаются консервативной терапии, поэтому лечить их приходится хирургическим путем. Врачи заменяют эндопротез, однако иногда им все же удается сохранить его.
Существует три метода лечения инфекций протезированного сустава: ревизия раны без удаления импланта, ревизионное одноэтапное и двухэтапное эндопротезировение. Выбор методики зависит от состояния пациента, время манифестации инфекции, стабильности компонентов протеза и характера патогенной микрофлоры.
Методы диагностики ИОХВ
На наличие инфекционного процесса в области послеоперационной раны указывают гнойные выделения, боль, припухлость и локальное повышение температуры. Все эти симптомы появляются как при глубоких, так и при поверхностных инфекциях.
Рентгенологические исследования
Большую роль в дифференциальной диагностике свищевых форм инфекции играет рентгенофистулография. С ее помощью можно определить размер, форму и расположение свищей, выявить гнойные затеки и их связь с очагами костной деструкции. Это позволяет отличить поверхностные ИОХВ от глубоких.
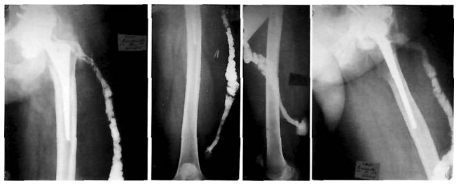
Фото: Рентгенофистулография, свищ в нижней трети бедра.
Для диагностики инфекции протезированного сустава чаще всего используют рентгенографию. Метод на дает 100% верных результатов, однако позволяет заподозрить патологию. На наличие парапротезной инфекции указывает внезапное появление периостальной реакции и остеолиза. Если эти признаки возникают внезапно, вскоре после успешно проведенной операции, – есть повод заподозрить неладное.
Любопытно! МРТ, УЗИ и радиоизотопное сканирование в диагностических целях используют редко из-за их низкой информативности. К примеру, установленный эндопротез создает помехи при магнитно-резонансной томографии, что делает изображение размытым и нечетким.
Лабораторные анализы
Сдача анализов помогает выявить острые и хронические воспалительные процессы в организме. Повышение показателей не является достоверным признаком ИОХВ. Для постановки диагноза нужно учитывать наличие определенных клинических симптомом, данных рентгенографии и других методов исследования.
Клинически значимые лабораторные показатели:
- Количество лейкоцитов. Имеет значение в диагностике острой парапротезной инфекции. Ярким признаком воспаления является повышение общего количества лейкоцитов и нейтрофилов, сдвиг лейкоцитарной формулы влево.
- СОЭ. Является неспецифическим показателем. Нормальная скорость оседания эритроцитов говорит об отсутствии воспалительных процессов, повышенная – об их наличии.
- С-реактивный белок. СРБ является белком острой фазы воспаления и высокочувствительным маркером ИОХВ для людей, которым выполнили эндопротезирование. При диагностике парапротезных инфекций нужно обращать внимание именно на этот показатель.


Микробиологические исследования
Бактериоскопическое и бактериологическое исследования позволяют выявить и идентифицировать возбудителя инфекции, а также определить его чувствительность к антибиотикам. Количественные исследования дают возможность установить число микробных тел в гнойном отделяемом.
Для исследования могут использоваться такие материалы:
- отделяемое из раны;
- образцы ткани;
- жидкость из суставной полости;
- протезный материал.
При имплант-ассоциированной инфекции выявить бактерии в биологических жидкостях и тканях практически невозможно. Патогенные микроорганизмы обнаруживают на самих поверхностях эндопротезов. Они покрывают импланты в виде адгезивной пленки.
Факт! Кроме бактериологического исследования для диагностики могут использовать ПЦР – полимеразную цепную реакцию. Метод имеет высокую чувствительность, но низкую специфичность. Из-за этого он нередко дает ложноположительные результаты.
Лечение
Прежде чем решить, как бороться с инфекцией, врачи тщательно обследуют пациента. Лишь установив диагноз и определив чувствительность патогенной микрофлоры к антибиотикам, они принимают окончательное решение.
Таблица 2. Методы лечения парапротезных инфекций:
| Метод | Показания | Результаты |
| Санация раны с сохранением эндопротеза | Проводится в том случае, когда ИОХВ возникла в первые 3 месяца после операции. Сохранить эндопротез можно лишь при отсутствии гнойных затеков и тяжелых сопутствующих заболеваний. При этом имплант должен быть стабильным, а микрофлора – высокочувствительной к антибиотикам. | Является наименее травматичным методом лечения. По разным данным, эффективность хирургической санации составляет 18-83%. |
| Ревизионное (повторное) эндопротезирование | Одномоментная или двухмоментная замена импланта выполняется в том случае, когда сохранить сустав не представляется возможным. Подобная ситуация наблюдается при нестабильности компонентов эндопротеза, позднем развитии инфекции, низкой чувствительности микрофлоры к антибиотикам, наличии тяжелых соматических заболеваний. | Позволяет полностью справиться с проблемой в 73-94% случаев. К сожалению, в ходе лечения больному приходится полностью менять установленный эндопротез. |
| Артродез с чрезкостным остеосинтезом | Глубокая рецидивирующая парапротезная инфекция, нечувствительная к антибиотикам микрофлора, наличие тяжелой сопутствующей патологии. | В 85% случаев позволяет устранить воспалительный процесс и восстановить опороспособность нижней конечности. |
| Экзартикуляция в тазобедренном суставе | Хроническое рецидивирующее воспаление, угрожающее жизни больного, или полная потеря функции нижней конечности. | Человек безвозвратно теряет ногу. Отсекают ее на уровне тазобедренного сустава. |
Имплант-сохраняющая тактика
Ее главная цель – устранение инфекционного процесса при одновременном сохранении эндопротеза. Больному проводят хирургическую обработку раны, в ходе которой удаляют гной и некротизированные ткани. При вовлечении в патологический процесс самого сустава выполняют артроскопический дебридмент. Больному назначают массивную антибактериальную терапию.
Любопытно! Научные исследования доказали эффективность безоперационного лечения ранних глубоких инфекций. Как выяснилось, комбинация антибиотиков и ферментных препаратов помогает ликвидировать воспаление за 5-7 дней.
Ревизионные операции
Выполняются в тех случаях, когда врачам не удается сохранить сустав. Хирурги полностью удаляют эндопротез, а на его место ставят новый. Риск повторного развития инфекции после ревизионного эндопротезирования выше, чем после первичного.
Инфекция – одна из самых частых осложнений при эндопротезировании. При ревизионном вмешательстве цифры пострадавших от инфекции увеличиваются до 40%. И эти цифры возрастают с каждым годом, так как растет количество людей, прибегнувших к эндопротезированию. Раньше это были пожилые пациенты, а сейчас ставят имплантаты и молодежь. Поэтому в 21 веке эндопротезирование поставлено буквально на поток. Причины возникновения парапротезной инфекции разные и полностью до конца неизученные. В последнее время всё чаще появляются публикации о связи возбудителя и материала, из которого сделан протез, так как есть данные о способности к адгезии некоторых микроорганизмов к определенным видам имплантатов.
Выраженность симптомов инфицирования после эндопротезирования зависит от вирулентности возбудителя, источника заражения, состояния пациента и его возраста. В первые несколько дней после имплантации коленного протеза клинические данные все еще не позволяют четко различать послеоперационную тканевую реакцию и начальную инфекцию. Классические признаки воспаления (гипертермия, покраснение, отек, боль и нарушение функции) могут первоначально существовать и без наличия инфекции, а их отсутствие или сильная задержка в течение первой недели должны стать весомым основанием для осуществления дальнейшего контроля.
Парапротезное воспаление проявляется после постановки эндопротеза в течение нескольких месяцев, в зависимости от времени возникновения его различают:
- если симптоматика появилась в течение 30 дней после вмешательства, говорят об острой форме;
- если признаки инфекции проявились спустя 30 дней после постановки имплантат или в течение года после нее, то речь идет о хронической форме;
- если жалобы появились через 12 месяцев после операции, то врачи говорят об острой гематогенной инфекции
Фебрильная температура тела, как указание на инфекцию, обычно возникает через три-шесть дней после эндопротезирования, в большей степени, в случае (супер-) инфицированной послеоперационной гематомы. Однако, наличие персистирующей (суб-) фебрильной температуры тела, по крайней мере, следует рассматривать как сигнал тревоги, нуждающийся в усиленном наблюдении. Если возникают системные параметры сепсиса, то следует исключить послеоперационную раневую инфекцию.
Иногда болезнь протекает латентно без явных признаков. Наличие выпота без локальных или системных признаков инфекции обычно является неспецифическим параметром. Его можно пунктировать в стерильных условиях, чтобы пунктат был в дальнейшем исследован микробиологически. Для свищевой формы характерно появление свища в виде патологического хода от протеза до эпидермиса, через который выделяется гной.
Диагноз основывается на данных осмотра, анамнеза, жалоб больного и дополнительного обследования. Из-за стертости симптомов и отсутствии специфических результатов обследования постановка диагноза параинфекции является довольно сложным делом и в, первую очередь, зависит от опыта и квалификации врача.
К врачу приходят обычно с жалобами на отечность сустава, ограничение его функциональности, субфебрильную температуру (а иногда и лихорадку), покраснение и припухлость в области колена.
Но классические признаки воспаления могут отсутствовать, а основным симптомом инфицирования и жалобой пациента будет являться постоянная боль в колене, нечетко связанная с движением и усиливающаяся ночью. Боль может быть ноющей или пульсирующей, локальной или иррадиирующей.
Если парапротезный процесс глубокий, поражаются мышцы рядом с имплантатом. Интоксикация распространяется по всему организму, общее состояние ухудшается, температура держится высокой, больного знобит, отмечается слабость, возможна рвота.
Врач уточняет у пациента характер боли, ее начало, динамику процесса, выясняет проводилось ли лечение (если жалобы появились вне клиники)
Если инфекция латентная, выраженных жалоб может не быть, пациент отмечает усталость, ноющую боль, легкую припухлость в области сустава.
Любая жалоба на боль в области эндопротеза особенно в течение первых трех лет после операции должна рассматриваться как инфекционное осложнение. Помимо жалоб врач собирает тщательный анамнез, выясняя:
- есть ли болезни суставов;
- страдает ли пациент ревматизмом;
- принимал ли длительный курс лекарственных препаратов;
- были ли после операции травмы и падения;
- в каком состоянии находятся сосуды;
- есть ли сахарный диабет;
- есть ли остеопороз;
- какой тип протеза и были ли проблемы с послеоперационной раной;
- есть ли сердечно-сосудистая недостаточность;
- есть ли боли в области протеза, и когда они появились
При клиническом осмотре обращается внимание на увеличенное в объеме колено или ограниченная припухлость, изменение цвета кожи вокруг сустава. Врач выявляет, отмечается ли ограничение движения. Однозначным подтверждением парапротезной инфекции являются свищевые ходы. Края раны могут расходиться, появляется отделяемое из нее, иногда формируются участки омертвения.
При пальпации – увеличение паховых лимфоузлов, повышение локальной температуры, болезненность в области проекции суставной щели. Отмечается тахикардия (учащенный ритм сердца) и частое дыхание.
Обычно берут кровь на клинический и биохимический анализ, сдают кровь на посев. Лабораторные исследования включают, в частности, определение сывороточного CRP [C-реактивный протеин], который в настоящее время представляет собой наиболее важный контрольный параметр в дополнение к показателю количества лейкоцитов в картине крови. Однако, здесь абсолютные значения соответствующих показателей имеют меньшую значимость, по сравнению с течением заболевания. Сразу после проведения операции значения CRP (C-реактивного протеина) практически всегда увеличиваются, а затем, в последующие дни, начинают падать. Отсутствие понижения CRP или его продолжающийся рост, в сочетании с клиническими признаками инфекции говорят о наличии инфекции до тех пор, пока не будет доказано обратное. В этом контексте, скорость оседания эритроцитов (СОЭ) в современной клинической картине вряд ли играет определенную роль, за исключением осуществления косвенного контроля над долгосрочным течением заболевания и определения хронической инфекции.
Что касается лабораторных параметров, то следует отметить, что, например, такая инфекция, как эпидермальный стафилококк (Staphylococcus epidermidis), обыкновенно не вызывает значительного увеличения CRP и клинические параметры часто оказываются очень неспецифическими.
Так, например, может наблюдаться изменение количества лейкоцитов, но информативность этого параметра параэндопротезной инфекции не имеет существенного значения. Если посевы синовии стерильны, это еще не говорит об отсутствии параинфекции, надо повторить исследования тканей на посев из разных областей коленного сочленения.
Абсолютно никаких сомнений не существует в случае больших дефектов мягких тканей с визуально различимыми компонентами протеза, выявленных при инструментальном обследовании.
Сонографическое исследование играет важную роль при подозрении на наличие ранней инфекции, поскольку его можно использовать для визуализации перипротезного выпота или гематомы и, при необходимости, для выполнения сонографически контролируемой пункции. Основанием для постановки диагноза могут быть обнаруженные участки гипоэхогенности.
Обычное рентгеновское изображение едва ли сможет передать целевую информацию при ранней параинфекции, так как специфических рентгенологических признаков существует очень мало. В отличие от этого, при поздней форме существует другая ситуация: в этом случае перипротезные признаки ослабления на рентгеновском снимке можно наблюдать в двух уровнях. Предположить наличие инфекционного воспаления может выявленная на снимке периостальная реакция и признаки остеолиза. Обязательным является регулярный рентген-контроль, чтобы видеть динамику процесса. Если существует свищ, то с помощью рентгенфистулографии может быть получено доказательство вовлечения протеза в патологический процесс. Рентгеновское изображение свища уточняет его локализацию, разветвление его ходов, соединение с органами и тканями, находит гнойные скопления (затеки). Кроме того, при наличии свища берется мазок для проведения бактериологического исследования, включая резистограмму.
Вследствие наслаивания протеза при имплантировании, в большинстве случаев, стальных компонентов, компьютерная томография (КТ) и магнитно-резонансная томография (МРТ) практически не играют здесь никакой роли (исключение составляют титановые протезы).
В случае длительного течения заболевания, может быть также использована (трехэтапная) сцинтиграфия, с помощью которой может быть доказана патологическая метаболическая активность мягких тканей и/или кости в околопротезной области.
Пункция тканей в области коленного сочленения с целью получения пунктата проводится под контролем ультразвука. Полученное содержимое изучается в лаборатории, где проводится посев на идентификацию возбудителя.
Только после интерпретации полученных данных врач может выработать оптимальную стратегию лечения.
Правильная диагностика поможет ответить на многие врачебные вопросы, выяснить вовлечение окружающих тканей и конструкции эндопротеза в воспалительный процесс, узнать распространенность его, понять на какой стадии нарушено кровообращение и, самое главное, разработать оптимальную и эффективную тактику лечения. Лечение парапротезной инфекции длительное, с применением дорогостоящих лекарств и материалов. Продолжаются дебаты о выборе оптимальных технологий, способных восстановить функции сустава с минимальным риском повторной инфекции, поэтому очень важно найти врача с большим опытом эндопротезирования и специализированную клинику с современным оборудованием.
Читайте также:


