Энтеробактер как внутрибольничная инфекция
Условно-патогенные представители семейства Enterobacteriaceae могут вызывать разнообразные клинические синдромы, воспалительные процессы различной локализации и сепсис.
Из всех клинически значимых бактерий энтеробактерии составляют около 50%, из грамотрицательных - примерно 80%. На долю энтеробактерий приходиться около 50% всех возбудителей септицемий, до 70% возбудителей инфекций мочевого тракта.
Кроме представителей рода Shigella, многие энтеробактерии вызывают внекишечные инфекции (мочевые, особенно циститы, респираторные, раневые, кровяные, инфекции ЦНС). Их чаще вызывают представители семи видов: E. сoli, K. pneumonia, K. oxytoca, P. mirabilis, E. aerogenes, E.сloacae, S. Marcescens [Инфекционные болезни…, 2007].
Род Escherichia включает большое количество микроорганизмов, обладающих рядом общих свойств, но отличающихся по биохимическим, антигенным и патогенным свойствам.
В состав вида Escherichia coli наряду с непатогенными кишечными палочками входят патогенные варианты:
- ЭГКП (энтерогеморрагические кишечные палочки) - возбудители энтерогеморрагического эшерихиоза с гемолитико-уремическим синдромом.
- ЭИКП (энтероинвазивные), вызывающие дизентериеподобные заболевания.
- ЭТКП (энтеротоксигенные), вызывающие холероподобный эшерихиоз.
- ЭПКП (энтеропатогенные), возбудители детских энтеритов и другие возбудители кишечных инфекций, а также уропатогенные эшерихии - возбудители инфекций мочевых путей [Воробьёв, Кривошеин, Широбоков, 2003].
Патогенные эшерихии подразделяются на две большие группы: первую, вызывающую развитие патологических процессов внекишечной локализации, и вторую, обусловливающую развитие острых кишечных инфекций. Эшерихии, вызывающие инфекционный процесс внекишечной локализации, подразделяют на 3 патогруппы: менингеальные (MENEC - meningitis E. сoli), септицемические (SEPES - septicemia E. coli) и урологические (UPEC - uropathogenic E. coli) [Генетические детерминанты…, 2004].
Другие эшерихии, являясь условно-патогенными, могут вызывать оппортунистические инфекции: пневмонии, нагноения ран и полостей, менингиты, сепсис. Помимо Escherichia coli, такими свойствами могут обладать другие представители рода: Escherichia hermanii, Escherichia vulneris. При накоплении в пищевых продуктах эшерихии могут стать причиной пищевого отравления [Воробьёв, 2003].
Эшерихиозы (коли-инфекции) - острые инфекционные заболевания с фекально-оральным механизмом передачи; характерно преимущественное поражение ЖКТ с развитием энтерита или энтероколита, в редких случаях - генерализованных форм с внекишечными проявлениями.
Механизм передачи - фекально-оральный, пути передачи - пищевой, водный и бытовой. По данным ВОЗ, заражение ЭТКП и ЭИКП чаще происходит пищевым путём, а ЭПКП - бытовым. Среди пищевых продуктов преобладают молочные изделия (нередко творог), готовые мясные блюда, напитки (компот, квас и др.), салаты из варёных овощей. В детских коллективах, а также в больничных условиях возбудитель может распространяться через предметы ухода, игрушки, руки матерей и персонала. При энтерогеморрагических эшерихиозах заражение людей происходит при употреблении в пищу недостаточно термически обработанного мяса, а также сырого молока. Описаны вспышки заболеваний, связанные с употреблением гамбургеров. Водный путь передачи эшерихиозов наблюдают реже; опасно интенсивное загрязнение открытых водоёмов в результате сброса необезвреженных хозяйственно-бытовых и сточных вод, особенно из инфекционных больниц.
Естественная восприимчивость к эшерихиозам достаточно высокая, однако она варьирует в разных возрастных группах населения. Перенесённое заболевание оставляет нестойкий группоспецифический иммунитет [Инфекционные болезни…, 2007].
Род Klebsiella относится к семейству Enterobacteriaceae. К роду Klebsiella относится несколько видов. Основную роль в патологии человека из них играет вид Klebsiella pneumonia, которая подразделяется на три подвида: K. pneumonia subsp. pneumonia, K. pneumonia subsp. ozaenae и K. pneumonia subsp. rhinoscleromatis. Клебсиеллы постоянно обнаруживают на коже и слизистых оболочках человека и животных. K. pneumonia - частый возбудитель внутрибольничных инфекций, в том числе смешанных. Источником служит больной человек и бактерионоситель. Возможно как экзогенное, так и эндогенное заражение. Наиболее частые пути передачи - пищевой, воздушно-капельный и контактно-бытовой. Факторами передачи чаще всего являются пищевые продукты, вода, воздух. В последние годы частота клебсиеллезов возросла, одна из причин этого - повышение патогенности возбудителя в связи со снижением резистентности организма человека. Этому способствует также широкое использование антибиотиков, изменяющих нормальное соотношение микроорганизмов в естественном биоценозе, иммунодепрессантов и т. д [Коротяев, Бабичев, 2008].
Наиболее известные поражения вызывает K. pneumonia, как правило, у лиц с поражением дыхательных путей. Клебсиеллы пневмонии вызывают у человека воспаление лёгких, а также бронхиты и бронхопневмонии. Пневмония характеризуется поражением одной или нескольких долей лёгкого. Иногда возбудители пневмонии вызывают менингит, цистит; у детей - септицемию и другие заболевания [Прозоркина, Рубашкина, 2008].
K. ozaenae поражает слизистую оболочку носа и его придаточных пазух, вызывает их атрофию, воспаление сопровождается выделением вязкого зловонного секрета.
K. rhinoscleromatic поражает не только слизистую оболочку носа, но и трахею, бронхи, глотку, гортань, при этом в поражённой ткани развиваются специфические гранулемы с последующим склерозированием и развитием хрящевидных инфильтратов. Течение заболевания хроническое, смерть может наступить на фоне обтурации трахеи или гортани [Тимаков, Левашев, Борисов, 1983].
Выделяют два вида сальмонелл: Salmonella enterica и Salmonella bongori. Вид Salmonella enterica включает подвиды: enterica, salamae, arizonae, diarizonae, houtenae. Наиболее патогенны для человека и других теплокровных животных серовары подвида enterica.
Сальмонеллёз. Сальмонеллы хорошо приспособлены к обитанию в организме различных животных. У человека инфекция обычно не выходит за пределы кишечника. Заболевание характеризуется саморазрешающейся диареей. В некоторых случаях микроорганизмы могут вызывать инвазивные, угрожающие жизни человека заболевания, сопровождающиеся бактериемией, септицемией и остеомиелитом.
Сальмонелл обнаруживают в организме большинства домашних животных. Важными источниками инфекции считают больных людей и реконвалесцентных носителей. Механизм передачи заболевания — фекально-оральный (при употреблении контаминированных продуктов питания). Самые тяжёлые случаи сальмонеллёза наблюдают у пациентов со сниженным иммунитетом и сниженной секрецией желудочного сока, а также у лиц, перенёсших спленэктомию. В некоторых случаях заболевание осложняется реактивным артритом или развивается хроническое носительство.
Брюшной тиф. Возбудители брюшного тифа — серовары typhi и paratyphi подвида Salmonella enterica. Заболевание характеризуется поражением стенки кишечника, затем регионарных лимфатических узлов, сопровождается первичной бактериемией и инфекцией ретикулоэндотелиальной системы. В последующем бактерии попадают в кишечник из жёлчного пузыря, размножаются в пейеровых бляшках (развивается вторичная бактериемия), вызывают изъязвление стенки кишечника, которое может привести к кровотечению или перфорации. Пациенты предъявляют жалобы на высокую температуру, нарушение функций кишечника (диарею или запор) и сыпь (розеолёзные элементы на передней брюшной стенке). Наблюдают гепатоспленомегалию. Иногда брюшной тиф осложняется остеомиелитом и реже менингитом.
Инфекции мочевыводящих путей и пиелонефрит. Большинство инфекций мочевыводящих путей вызвают определённые серотипы Escherichia coli. Они способны к повышенному образованию К-антигена и гемолизина и прикреплению к эпителию мочевыводящих путей посредством пилей (последнее свойство характерно и для некоторых видов протея). При наличии у возбудителя маннозоустойчивых пилей развивается пиелонефрит. Важный фактор вирулентности бактерий рода Proteus — уреаза, снижающая рН и стимулирующая процесс образования камней.
Менингит и абсцессы мозга. Важной причиной менингита у новорождённых (характеризуется высокой смертностью) является Escherichia coli, штаммы которой в большом количестве продуцируют капсульный Kl-антиген. Кроме того, заболевание может быть следствием нейрохирургических вмешательств, операций по протезированию. Следует отметить, что энтеробактерии очень часто присутствуют в патогенной микрофлоре, сопровождающей абсцессы головного мозга.
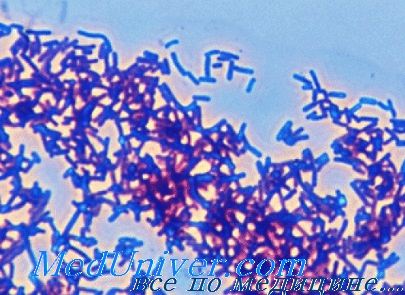
Возбудитель сальмонеллеза - Salmonella enterica
Остеомиелит и септический артрит. Тяжелейшее осложнение у пациентов с серповидно-клеточной анемией и ВИЧ-инфекцией — остеомиелит или септический артрит, вызванные сальмонеллами. Кроме того, сальмонеллы и другие энтеробактерии часто вызывают инфекции костей и суставов у пожилых пациентов. Иногда эти заболевания возникают вследствие проникающего ранения. Для лечения обычно применяют фторхинолоны, так как они обладают способностью проникать в костную ткань (например, ципрофлоксацин).
Инфекции, вызванные представителями рода Klebsiella. Микроорганизмы рода Klebsiella обычно вызывают внутрибольничные инфекции. Кроме того, они могут быть причиной развития пневмонии (особенно у пациентов, находящихся на искусственной вентиляции лёгких), инфекций мочевыводящих путей, раневых инфекций и бактериемии. У высоковосприимчивых пациентов известны случаи заболеваний, сопровождающихся септицемией и заканчивающихся летальным исходом. Первичная пневмония, вызванная подвидом Pneumoniae вида К. pneumoniae, — редкое и крайне тяжёлое внебольничное заболевание, характеризующееся неблагоприятным исходом. Возбудитель прогрессирующей гранулематозной инфекции слизистой оболочки полости носа — Klebsiella rhinoscleromatis. Большинство случаев заболевания регистрируют в тропических регионах мира. Другой вид — Klebsiella ozanae — возбудитель хронической бронхо-эктатической болезни.
Инфекции, вызванные бактериями родов Enterobacter, Serratia и Citrobacter. Представители этих родов обитают в окружающей среде и могут поражать пациентов лечебных учреждений, вызывая раневые инфекции, бактериемию и внутрибольничную пневмонию. Выбор антибактериального препарата осложняется тем, что большинство возбудителей устойчиво к действию антибиотиков.
Диагностика энтеробактерий:
• Бактериологическое исследование крови или костного мозга (особенно в диагностике брюшного тифа).
• Изучение биохимических свойств возбудителя (например, способности расщеплять углеводы).
• Серотипирование (серотипы различают по липополисахаридному (О) и жгутиковому (Н) антигену) и фаготипирование применяют при эпидемиологических исследованиях.
• Колицинотипирование.
• Современные молекулярно-генетические исследования.
Большинство грамотрицательных энтеробактерии чувствительны к действию аминогликозидов, цефалоспоринов широкого спектра действия, фторхинолонов, бета-лактамов и карбапенемов (например, меропенем). Лечение назначают только после определения чувствительности возбудителя к антимикробным средствам, так как некоторые микроорганизмы способны вырабатывать бета-лактамазу и ферменты, разрушающие аминогликозидные препараты. Возросшая в последнее время устойчивость энтеробактерии к антибиотикам широкого спектра действия обусловлена появлением штаммов, обладающих бета-лактамазами широкого спектра действия.
Препараты выбора при инфекциях мочевыводящих путей — цефалексин, ампициллин, нитрофурантоин или триметоприм.
Для профилактики заболеваний, сопровождающихся диареей, необходимо соблюдать правила личной гигиены, приготовления пищи, а также использовать безопасные источники водоснабжения. Основной метод лечения — пероральная регидратация организма.
Препарат выбора при брюшном тифе — ципрофлоксацин, альтернативные средства — триметоприм или цефалоспорины третьего поколения. В некоторых странах инфекционисты сталкиваются с заболеваниями, вызванными мультирезистентными штаммами возбудителя. Для профилактики заболевания людям, посещающим эти регионы, рекомендуют использовать живую аттенуированную (Ту21А) или бесклеточную (содержит Vi-антиген) вакцины, но вакцинация лишь частично защищает от инфекции.
Нозокомиальные (внутрибольничные) инфекции отличаются от внебольничных как спектром возбудителей, так и их устойчивостью к противомикробным средствам. К ним относят инфекции, развившиеся через 48 часов и более после поступления в стационар (если больной не находился в инкубационном периоде), и возникшие в течение 72 часов после выписки из стационара. К нозокомиальным относят и инфекции, возникшие в закрытых медицинских учреждениях, а также возникшие в связи с лечением больного на дому.
Анаэробные возбудители
Анаэробные возбудители в большинстве своем являются представителями нормальной флоры человека, вызывая патологические процессы при снижении иммунной реактивности (анаэробная ангина) и/или барьерных функций (пупочная ранка, повреждение слизистых, операции, занос в легкое при аспирации или бронхоскопии), чаще всего как сопутствующая другим возбудителям нозокомиальная инфекция. Анаэробные посевы оправданы у истощенных детей с пролежнями, нейтропенией, при абдоминальной патологии, низкой гигиене рта, обширной травме и т.д.
Бактероиды. Bacteroides — грам-отрицательиые факультативно анаэробные неспорообразующие палочки. Prevotella melaninogenicus и P. oralis (ранее относившиеся к бактероидам) обитают в ротовой полости, представители группы В. fragilis — в толстом кишечнике, являясь основой его бактериальной популяции (10 10 особей в 1 г кала); они также обитают во влагалище. Вызванные этими возбудителями процессы практически всегда полимикробны. При инфекции легких они сочетаются с гемолитическим стрептококком группы А, стафилококком, реже — с гемофильной палочкой типа b. Инкубационный период 1-5 дней, больной не заразен.
Лекарственная чувствительность бактероидов практически 100%-ная к клиндамиципу, а также к метронидазолу, хлорамфениколу, карбапенемам, фторхинолонам. Превотеллы ротовой полости обычно чувствительны к амино- и уреидопенициллинам, но с учетом возможности выработки лактамаз препаратами выбора являются ингибитор-защищенные пенициллины и цсфалоспорины.
Клинические проявления. Обитая в десневых карманах и зубных бляшках, превотеллы могут вызывать их инфекцию, а также хронические синусит, средний отит, перитонзиллярный абсцесс, а при заносе или аспирации — абсцесс и гангрену легкого. Анаэробы кишечника выявляются при перитоните, абсцессах брюшной полости и органов малого таза, при перианальных и вагинальных воспалительных процессах. Инфекции пупочной ранки и кожи (под датчиками) нередки у новорожденных. В качестве возбудителей бактериемии анаэробы составляют не более 5%, но их всегда следует иметь в виду при гематогенных абсцессах.
Терапия. Препарат выбора — клиндамицин, эффективны ингибитор-защищенные амино- и уреидопенициллины, цефоперазон/сульбактам. В терапию вероятно анаэробных процессов (в т.ч. бактериемии) часто эмпирически включают метроиидазол.
Clostridium difficile. С. difficile — спорообразующий облигатный грам-положительная анаэроб, выделяющий токсины А и В. Обитает в почве и часто колонизирует кишечник, особенно у детей 1-го года жизни. Основной фактор риска — нарушение нормальной микрофлоры кишечника при массивной антибактеральной терапии (особенно, но не исключительно пенициллинами, цефалоспоринами, клиндамицином), что создает условия для размножения возбудителя и продукции им токсинов. Играет роль и госпитализация при наличиии в отделении носителя клостридий. Инкубационный период не известен.
Лекарственная чувствительность к метронидазолу и ванкомицину.
Клинические проявления. Псевдомембранозный колит — обычно развивается в стационаре на фоне антибиотика, но иногда — через несколько недель после выписки.
Диагностические тесты. Высев возбудителя диагностического значения не имеет. Поскольку клинические проявления связаны с воздействием токсинов, их выявление в кале (есть ИФА- системы) — основной метод. К сожалению, у здоровых носителей клостридий в возрасте до 1 года также можно выявить токсины, так что важно исключить другие инфекции. Характерные изменения выявляются при эндоскопии.
Лечение. Внутрь или в/в метронидазол (30 мг/кг/сут на 4 приема — макс. 2 г/сут), при неэффективности — внутрь ванкомицин (40 мг/кг/сут на 4 приема, макс. 500 мг/сут).
Пептострептококки. Peptostreptococcus spp. — наиболее важная в клиническом отношении группа анаэробных кокков ротовой полости, желудочно-кишечного тракта, влагалища. Часто высевается из анаэробных абсцессов, обычно вместе с бактероидами.
Лекарственная чувствительность к природным и полусиптетическим пенициллинам, цефалоспоринам, карбапенемам, клиндамицину, хлорамфениколу, на 80-90% — к фторхинолонам.
Клинические проявления. Специфическую роль пептострептококков, выявляемых обычно вместе с другими анаэробами, установить трудно.
Терапия. Выбор препаратов для лечения инфекции бактероидами бывает обычно эффективным и в отношении пептострептококков.
Enterobacteriaceae spp.
Эта группа микроорганизмов обитает в кишечнике человека, представляя серьезную опасность для новорожденных с еще не установившейся флорой кишечника. У старших детей и взрослых эти возбудители вызывают инфекции мочевых путей, являясь, в то же время, важнейшей причиной нозокомиальных инфекций.
Представители этой группы при нозокомиальной инфекции обычно полирезистентны, часто за счет выработки бета-лактамаз расширенного спектра (БЛРС). Поэтому основная тактика при их выявлении — базировать выбор препаратов на данных о чувствительности выделенных штаммов.
Кишечная палочка. Esherichia coli является основным возбудителем инфекций мочевых путей (см. Главу 4), у новорожденных является важной причиной менингита и септицемии (особенно штаммы, содержащие К-1 полисахарид), а у старших детей нередко вызывает нозокомиальные инфекции. Вызывающие энтерит кишечные палочки — см. Главу 3.
Лекарственная чувствительность к ампициллину снижается, особенно при ИМП, но чувствительность к аминогликозидам обычно сохраняется. БЛРС-отрицательными штаммы чувствительны к цефалоспоринам 2-4 поколения, ингибитор-защищенным пенициллинам, фторхинолонам.
Клинические проявления: менингит и септицемия новорожденных, инфекция мочевых путей у старших детей, внутрибольничная (нозокомиальная) пневмония.
Терапия. При септицимии новорожденных эмпирически используют ампициллин + гентамицин. При нозокомиальных инфекциях, вызванных БЛРС-отрицательными штаммами, используют цефалоспорины и амоксицшлин/клавуланат, в т.ч. с аминогликозидами. Для БЛРС-положительных штаммов рекомендуется использовать карбапенемы, фторхинолоны, цефоперазон/сульбактам, также с аминогликозидами.
Клебсиеллы. Klebsiella pneumoniae — представитель многочисленного вида Klebsiella, патогенна для человека также К. oxitoca. Эти грам-отрицательные возбудители продуцируют эндотоксин, вызывающий ДВС-синдром и другие признаки септического процесса. Заражение возможно через загрязненные предметы: мы наблюдали случаи клебсиеллезной пневмонии у детей, помещенных в палату, где незадолго до этого был аналогичный больной.
Лекарственная чувствительность практически 100% штаммов чувствительны к карбапенемам, 70% — к амикацину, цефоперазопу/сулъбактаму и фторхинолонам. Нозокомиальные штаммы в России высоко резистентны к пенициллинам (86-100% устойчивых штаммов), в т.ч. ингибитор-защищенным (42-85%), цефалоспоринам 3-4 поколений 57-76%), что указывает на широкое распространение (81%) штаммов с БЛРС в отделениях интенсивной терапии, где проводилось исследование. В целом, доля штаммов с БЛPC превышала 60%, причем в стационарах, где эта инфекция наблюдалась часто, отмечалась более высокая частота продукции этой лактамазы. К ко-тримоксазолу устойчивы 62% штаммов, к гентамицину — 75%.
Клинические проявления: лобарная пневмония у госпитализированных (редко вне больницы у истощенных больных, при ИДС), раневая инфекция, ИМП, ИЖП.
Терапия. Эмпирически для БЛРС-отрицательных штаммов: цефалоспорины 3-4 поколения, ингибитор-защищенные пенициллины, в т. ч. с аминогликозидами, фторхинолоны. Для БЛРС-положительных штаммов: карбапенемы, фторхинолоны, цефоперазон/сульбактам, в т.ч. с аминогликозидами (лучше — с амикацином).
Провиденция. Providencia spp. распространены в окружающей среде, колонизируют желудочно-кишечный тракт. Внутрибольничную (нозокомиальную) инфекцию человека чаще вызывает P. stuartii.
Лекарственная чувствительность природная — к пенициллинам, цефалоспоринам 2-3 поколения, карбапеиемам, фторхинолонам и аминогликозидам, ко-тримоксазолу. В связи с учащающейся резистентностью важно проведение антибиоти-кограммы.
Клинические проявления: нозокомиальная инфекция мочевого тракта, реже пневмония, септицемия.
Терапия. Эмпирически используют цефалоспорины 3 поколения, карбапенемы, в т.ч. в комбинации с аминогликозидами.
Протей. Proteus vulgaris (индол-отрицательный) и Proteus mirabilis (индол-положительный) — грам-отрицательные обитатели кишечника человека, вызывающие инфекции мочевых путей (благодаря наличию фимбрий и жгутика, а также способности разлагать мочевину) и 10-15% нозокомиальных инфекций. Протей, как и другие возбудители этой группы, вызывает вспышки в отделениях для новорожденных детей, часто с развитием менингита.
Лекарственная чувствительность природная бета-лактамная — выражена в большей степени в отношении уреидопенициллинов и цефалоспоринов 2-4 поколений, но нозокомиальные штаммы протея теряют чувствительность к бета-лактамам, а также к аминогликозидам; это в большей степени относится к штаммам P. vulgaris.
Клинические проявления: ИМП, пневмония, раневая инфекция, хроническая некротическая инфекция среднего уха.
Терапия. Эмпирическая для БЛРС-отрицательных штаммов: цефалоспорины 3-4 поколения, ингибитор-защищенные пенициллины, фторхинолоны, в т.ч. в комбинации с аминогликозидами. Для БЛРС-положительных штаммов: карбапенемы, фторхинолоны, цефоперазон/сульбактам, в т.ч. с аминогликозидами.
Серрация. Serratia marcescens колонизирует кишечник и вызывает нозокомиальные инфекции, в основном, в отделениях интенсивной терапии.
Лекарственная чувствительность. Показано, что применение цефалоспоринов 3-4 поколения ведет к отбору устойчивых штаммов серраций, так что подбор препаратов должен основываться на данных антибиотикограммы.
Клинические проявления: нозокомиальная пневмония, ИМП, бактериемия.
Терапия. Эмпирически используют защищенные пенициллины широкого спектра, цефепим, карбапенемы, в т.ч. в комбинации с аминогликозидами.
Цитробактер. Citrobacter divcrsus и ряд других представителей вида обитает в кишечнике и могут колонизировать мочевые пути, респираторный тракт, раны. Вырабатывает эндотоксин, сходный с таковым клебсиелл.
Лекарственная чувствительность , как и других эитеробактерий во многом определяется наличием лактамаз.
Клинические проявления: септицемия и менингит новорожденных, нозокомиальная пневмония, инфекция мочевых путей, бактериемия.
Терапия. Эмпирически используют карбапенемы, цефепим.
Энтеробактер. Enterobacter — грам-отрицательный обитатель кишечника, на 50% (по ДНК) родственный клебсиеллам. Продуцирует эндотоксин (липополисахарид), вызывающий ДВС-синдром, лейкоцитоз или лейкопению, падение АД и другие септические проявления.
Лекарственная чувствительность. Нозокомиальные штаммы часто БЛРС+.
Клинические проявления: бактериемия, пневмония, инфекция ожогов.
Терапия. Эмпирически: защищенные уреидопенициллины, меропенем, цефепим.
Неферментирующие микроорганизмы
В эту группу входят возбудители нозокомиальных инфекций, не ферментирующие, в отличие от большинства других возбудителей, глюкозу.
Alcaligenes spp. Широко распространенные во внешней среде грам-отрицательные бактерии, некоторые из них — A. fecalis, A. xyloxidans (также известный как Achromobacter xyloxidans) колонизируют кишечник человека. Источником может быть загрязнение растворов, больничного оборудования, вентиляционных систем. Особо восприимчивы истощенные больные, в т.ч. на иммуносупрессии, инфицированные ВИЧ лица.
Лекарственная чувствительность к цефалоспоринам 3 поколения, уреидопени-инллинам, карбапенемам, но быстро вырабатывается устойчивость. Чувствительность к иминогликозидам и фторхинолонам непостоянна.
Клинические проявления: бактериемия, пневмония, послеоперационная инфекция рай, нервной системы.
Терапия. Меропенем, цефалоспорины 3-4 поколения, в т.ч. с аминогликозидами.
Acinetobacter spp. A. baumannii, A. cacoaceticus и ряд других представителей вида — грам-отрицательные каталозо-положительные коккобациллы, не ферментирующие лактозу, родственные Neisseria и Moraxella, распространены в воде и почве, они колонизируют кожу (25% взрослых), респираторный тракт (5%), мочевые пути. Частота колонизации возрастает у грахеостомированных и больных на ИВЛ; среди заболевших до половины дети с онкологической патологией, почти все — с центральным венозным катетером. Обнаруживается в местах высокой влажности — вентиляционных системах, увлажнителях, ингаляторах. Внебольничная инфекция крайне редка.
Лекарственная чувствительность больничных штаммов набольшая к амикацину п чмитнему, в последние 2 десятилетия она снижается из-за выработки лактамаз, в т.ч. металлл-бета-лактамазы (МБЛ). Нарастает устойчивость и к аминогликозидам (в России — 68-89%), цефалоспоринам 3-4 поколений (64-98%) и фторхинолонам (62-74%).
Клинические проявления: ИВЛ-ассоциированная пневмония, бактериемия, менингит, ИМИ, абдоминальный сепсис, инфекция мягких тканей.
Терапия. Ими не нем, меропенем, цефоперазон/сульбактам, в т.ч. с аминогликозидами.
Лекарственная чувствительность изначальная к аминопенициллинам, цефалоспоринам 3 поколения, карбапенемам, хлорамфениколу, тобрамицину, ко-тримоксазолу, фторхинолонам, однако у большинства штаммов, выделенных у больных муковисцидозом, наблюдается множественная лекарственная устойчивость.
Клинические проявления. У иммунокомпетентных лиц возбудитель вызывает но-юкомиальные ИМП, пневмонии, сепсис, протекающие без особой тяжести. У больных муковисцидозом и хронической гранулематозной болезнью развиваются тяжелые пневмонии, при инфицировании пересаженного легкого летальность достигает 80%.
Терапия. Эмпирически: тобрамицин или ципрофлоксацин + цефтазидим или защищенный уреидопенициллин. Альтернативы: карбапенем, хлорамфеникол.
Псевдомонады. Pseudomonas aeruginosa (из-за выработки синего пигмента известен как сине-гнойная палочка) — широко распространенный микроорганизм, обитающий в сырых местах — сливах раковины, ванн, душевых поддонов, увлажнителях, аэрозольных аппаратах. Колонизация наблюдается часто, выделение их из клинических проб в отсутствие проявлений диагностического значения пе имеет. Заболевание развивается, в основном, у лиц с нарушенными барьерами (трахеостомия, ИВЛ, муковисцидоз, нейтропения, ожоги), а также при манипуляциях (катетеризация, пункции и т.д.).
Клинические проявления практически неотличимы от вызванных энтеробакте-риями, при плеврите, ожоговом нагноении; характерен синеватый вид гноя.
Терапия. Эмпирически: карбапенемы, цефепим, цефтазидим, ципрофлоксацин, в т.ч. с аминогликозидами.
Stenotrophomonas. S. maltophilia — грам-отрицательиая аэробная палочка, широко распространенная во внешней среде, нередко выделяется из кала. Инфицирует больных на иммуносу-прессии, длительно получающих антибиотики, имеющих внутривенные катетеры.
Лекарственная чувствительность к ко-тримоксазолу. Металло-бета-лактамазы (МБЛ) делают его устойчивым ко всем (3-лактамам, в т.ч. карбапенемам.
Клинические проявления: септицемия, раневая инфекция, пневмония, ИМИ.
Терапия. Ко-тримоксазол в комбинации с защищенными пенициллинами и фторхинолоном. Используют и доксициклин или ципрофлоксацин + тикарциллин/клавуланат.
Стафилококки
Нозокомиальная стафилококковая инфекция распространена повсеместно, ее вызывает, в основном, S. aureus: коагулазо-отрицательный (белый, КоаНС) стафилококк представляет собой серьезную угрозу для новорожденных детей.
Лекарственная чувствительность. Среди больничных штаммов S. aureus в России 50% (0-87%) составляют метициллинорезистентные (МРЗС), но чувствительные на 100% к ванкомицииу, линезолиду, мупироцин, а также (на 97-99%) к фузидиевой кислоте и ко-тримоксазолу. 46-75% стафилококков были устойчивы к остальным препаратам. В США в ОРИТ доля МРЗС в 2003 г. достигла 60%. Среди КоаНС встречаются как чувствительные к метициллииу штаммы (МЧЭС), так и резистентные (МРЭС).
Клинические проявления. Внутрибольничная (нозокомиальная) инфекция, вызванная стафилококком как МЧЗС, так и МРЗС) проявляется в форме бактериемии, сепсиса, остеомиелита, артрита, эндокардита (особенно частого при длительной катетеризации магистральной вены), в виде органного поражения (чаще всего пневмонии), а также как раневая инфекция и инфекция мягких тканей.
Терапия. Практически все случаи нозокомиальной стафилококковой инфекции следует расценивать как МРЗС и эмпирически использовать ванкомицин (в т.ч. в комбинации с аминогликозидами или рифампицином). Препарат резерва — линезолид. Местные процессы, вызванные МРЗС, поддаются лечению мупироцином.
При лечении инфекции, вызванной КоаНС, используют те же правила, что и в отношении золотистого стафилококка соответствующей чувствительности; но и в этом случае эмпирически оправдано применение ванкомицина.
Профилактика. Для борьбы с носительством стафилококков персоналом применяется обработка входа в нос мупироцином (Бактробан) в течение 5 дней.
Энтерококки
Enterococcus spp. — ранее относимые к стрептококкам группы D — каталазо-отрицательные, обитающие в кишечнике, нередко также в уретре, влагалище, реже во рту. Близок к ним S. bovis, обитающий в кишечнике и вызывающий бактериемию и эндокардит у лиц с патологией толстого кишечника. Обладая умеренной патогенностью, энтерококки рассматриваются как оппортунистические возбудители внутрибольничных инфекций, особенно у лиц, получающих много антибиотиков. Ко-патогенами чаще всего становятся грам-отрицательные бактерии.
Лекарственная чувствительность к линезолиду (100%), ванкомицину (98% — только Е. fecium). К ампициллину чувствителен Е. fecalis, но не Е. fecium (97% и 8% соответственно). Оба штамма устойчивы к тетрациклинам (Е. fecalis 69%, Е. fecium 53%), хлорамфениколу (45% и 58%), ципрофлоксацину (70% и 100%), гентамицину (41% и 82%), стретомицину (34% и 74%). Энтерококки изначально устойчивы к бета-лактамам (кроме ампициллина), клиндамицину, ко-тримоксазолу. В целом, частота выявления устойчивых штаммов Е. fecalis намного ниже, чем Е. fecium.
В США в 2003 г. доля устойчивых к ванкомицину энтерококков (ВРЭ) в ОРИТ составила 28%5; для лечения вызванных ими инфекций у взрослых там лицензированы квинупристин-дальфопристин, даптомицин. Доля МРЗС и ВРЭ в педиатрических ОРИТ США намного ниже чем во взрослых ( Клинические проявления. Помимо бактериемии, энтерококки вызывают инфекцию мочевых путей, эндокардит, внутриабдоминальную инфекцию. Часто осложняет использование эндопротезов, шунтов и в/в катетеров.
Диагностические тесты. Достоверным является высев из стерильных в норме жидкостей. Обнаружение возбудителей в крови в 85-90% указывает на инфекцию.
Терапия. Стандартом лечения энтерококковой инфекции является ампициллин, амоксищиишн или ванкомицин в комбинации с аминогликозидом; с учетом высокой устойчивости к гентамицину в России, следует использовать другой препарат этой группы. При выделении резистентных к ванкомицину штаммов используют линезолид, доксициклин, хлорамфеникол (не у новорожденных!), даптомицин; терапия эндокардита требует 4-6 недель, другие инфекции лечат более короткими курсами.
Читайте также:


