Что такое рецидивирующие инфекции дыхательных путей
В последнее время отмечается активное включение иммуномодуляторов со свойствами вакцин в лечение детей с патологией ЛОР-органов
В последнее десятилетие устойчиво сохраняется тенденция к росту числа часто и длительно болеющих детей. На сегодня выявлены следующие особенности данной патологии:
- заболеванию подвержены дети младшего возраста (3-5 лет);
- начало связано, как правило, с вирусной инфекцией, течение которой часто осложняется бактериальной инфекцией ЛОР-органов (отитами, синуситами, тонзиллофарингитами);
- характерно длительное рецидивирующее течение;
- недостаточная эффективность традиционных видов консервативной терапии (включая антибактериальную);
- раннее формирование хронических форм заболеваний ЛОР-органов.
С другой стороны, в детских дошкольных учреждениях создаются благоприятные условия для массивного инфицирования верхних дыхательных путей, в первую очередь лимфоглоточного кольца, условно-патогенной флорой, что вызывает чрезмерное напряжение иммунной системы, ведущее к ее истощению.
Дети с иммунологической недостаточностью составляют группу повышенного риска при острых респираторных заболеваниях, так как особенно тяжело болеют, многократно получают самые разнообразные антибиотики, однако заметного снижения заболеваемости, в первую очередь связанной с бактериальными возбудителями, у них не отмечается. Обусловлено это в числе прочего и ростом резистентности основных возбудителей инфекций верхних дыхательных путей даже к относительно новым антибактериальным препаратам, усилением роли условно-патогенной микробной флоры, внутриклеточных возбудителей в этиологии данных заболеваний у детей. При обследовании посещающих детские дошкольные учреждения детей в возрасте 4-6 лет, 24% из которых, по нашим данным, можно отнести к часто болеющим (67% имеют хроническую патологию ЛОР-органов), были выявлены следующие закономерности: в микробиоценозе миндалин и носоглотки преобладали стафилококки (77,9%), из них золотистый стафилококк высевался в 61,7% случаев, стрептококк высевался в 16,2% (Strept. pyogenus — в 8,8%); Corinebacter (flaver, xerosis, renale, minitiss, psevdotuberculosis) — в 10,3%; Candida albicans — в 11,8%. Рост монокультуры обнаружился в 60,3% случаев, в 16,1% высевались две культуры бактерий. В подавляющем большинстве случаев Сandida albicans обнаруживалась в сочетании с бактериальной флорой (чаще в ассоциации со стафилококком). В 86% посевов степень обсемененности высокая. Роста бактерий не обнаружено в 8,7% случаев.
Штаммы стафилококка были чувствительны: к рифампицину в 88,7% случаев, к кефзолу в 73,6%, к азитромицину в 69,8%, к ципрофлоксацину в 64,1%, к доксициклину в 62,3%; обладали устойчивостью: к бисептолу в 83%, к ванкомицину в 75,5%, к пенициллину в 69,8%, к клиндамицину в 56,6%, к цефтазидиму в 52,8%. Штаммы стрептококка обладали чувствительностью: к пенициллину в 63,6%, к рифампицину в 62%, к азитромицину в 45,5% случаев. Стрептококк показал устойчивость к клиндамицину в 63,8%, к ванкомицину, бисептолу, цефтазидиму, ципрофлоксацину, доксициклину в 45-46% случаев.
Данные результаты заставили медиков обратить пристальное внимание на вакцины против ведущих патогенов верхних дыхательных путей — Hemophilis influenza, Str. pneumonia, с которыми связывают и развитие внутричерепных, орбитальных осложнений, септических процессов. Достижения в области иммунологии обусловили активное включение бактериальных иммуномодуляторов со свойствами вакцин в процесс лечения больных с разнообразной патологией ЛОР-органов.
Комплексная иммунотерапия у детей может осуществляться несколькими способами: 1) активная иммунизация, 2) пассивная, заместительная иммунотерапия, 3) иммунотерапия растительными препаратами и др.
Среди средств активной иммунизации в середине 80-х годов использовалось парентеральное введение нативного анатоксина, антифагина, стрептостафилококковой, синегнойной вакцины.
В настоящее время особый интерес представляет возможность введения иммунокорригирующих препаратов более простыми и удобными для пациента и его родителей способами — капли, свечи и пр. Стоит обратить внимание на препарат ИРС 19, выпускаемый в виде спрея для интраназального применения.
Нами проведено исследование, в ходе которого оценивался лечебный и профилактический эффект препарата ИРС 19 (амбулаторно и в условиях стационара).
В амбулаторных условиях препарат ИРС 19 применялся у 20 детей с острыми синуситами (катаральными — 15, гнойными — 5). Все пациенты относились к категории часто болеющих и состояли на учете у ЛОР-врача с патологией лимфоглоточного кольца (гипертрофия аденоидных вегетаций, небных миндалин различной степени выраженности); у 50% их них заболевание, а следовательно, и прием ИРС 19, совпали с началом посещения массовых детских учреждений.
Средний возраст детей — 5 лет 3 мес. (от 1 года до 13 лет). Из них 9 мальчиков (45%) и 11 девочек (55%).
Препарат включали в базовую схему лечения основного заболевания: по одному впрыскиванию в обе ноздри 1-2 раза в день.
Эффективность действия оценивалась по срокам нормализации риноскопической картины, а также по результатам следующих анализов:
- оценка иммунологического статуса (определение иммуноглобулинов слюны, а в ряде случаев и носового секрета);
- посев отделяемого из носа и зева на флору и чувствительность к антибиотикам
- анализ крови клинический
- анализ мочи общий
- рентгеновский снимок придаточных пазух носа (ППН), в ряде случаев — УЗИ ППН.
Средние значения иммуноглобулинов слюны детей до и после приема препарата представлены в табл. 1.
Результаты микробиологического исследования показали, что в 45% случаев патогенной микрофлоры в отделяемом из носа высеяно не было; у 55% определялась патогенная микрофлора (Staph. aureus — 85%, Str. viridens — 15%). После курса лечения непатогенная микрофлора определялась в 55% случаев, в 45% случаев штамм остался тот же, уменьшилась степень обсемененности.
В условиях стационара ИРС 19 применялся у 35 детей с острыми синуситами. Средний возраст больных 10,6 лет (от 7 до 14 лет). Среди них — 20 мальчиков (57%) и 15 девочек (43%). В зависимости от формы воспаления была выделена группа с катаральными синуситами (I группа) — 13 детей (37%) и гнойными синуситами (II группа) — 22 (63%). Оценка эффективности препарата проводилась по динамике общего состояния, риноскопической картине, данным пункции верхнечелюстных пазух, результатам клинических анализов крови, по срокам выздоровления (по сравнению с контрольной группой). По окончании исследования было отмечено, что у детей, получавших препарат ИРС 19, сократилось время болезни по сравнению с контрольной группой: на три-пять дней раньше наступало выздоровление (оценивали по данным ЛОР-осмотра и результатам пункций гайморовых пазух), уменьшилось среднее количество пункций верхнечелюстных пазух, повысился процент выздоровления по отношению к улучшению течения заболевания (рис. 1).
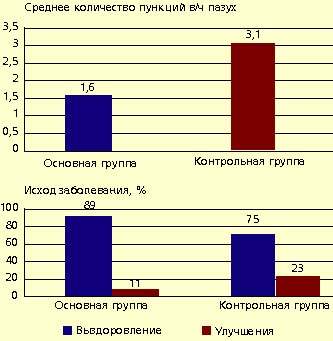 |
| Рисунок 1. Показатели эффективности препарата ИРС 19 у больных с острыми синуситами |
Результаты микробиологического исследования полости носа у больных с острыми синуситами основной и контрольной групп представлены в табл. 2.
Оценивая профилактические возможности препарата ИРС 19 в группе детей с рецидивирующей инфекцией верхних дыхательных путей, мы проанализировали среднюю продолжительность периода обострения, среднюю частоту обострения, интенсивность применения сосудосуживающих и антигистаминных средств после трехнедельного приема препарата, сравнив соответствующие результаты у тех же самых детей за аналогичный период предыдущего (1999) года. В качестве контрольных показателей служили данные о заболеваемости часто болеющих детей, не получавших препарат ИРС 19 за текущий и предыдущий сезоны.
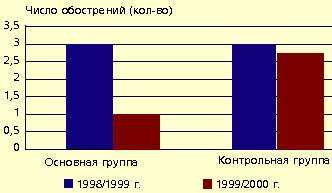 |
| Рисунок 2. Динамика средней частоты обострений инфекций верхних дыхательных путей в основной и контрольной группах |
Рис. 2 и 3 показывают динамику средней частоты и длительности обострений инфекций верхних дыхательных путей. Отмечено также существенное снижение потребности в сосудосуживающих и антигистаминных средствах (соответственно в 5 и 9 раз).
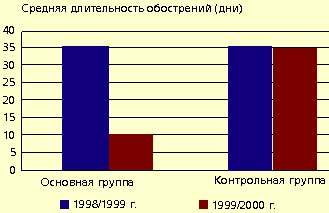 |
| Рисунок 3. Динамика средней длительности обострений инфекций верхних дыхательных путей в основной и контрольной группах |
Говоря о переносимости препарата, хочется отметить практически стопроцентное отсутствие побочных эффектов. Детям младшего возраста рекомендуется индивидуальный подбор дозы, чтобы избежать возможного повышения отделяемого из носовых ходов, приступов чихания после приема препарата. После индивидуального подбора дозы препарата никаких побочных эффектов от приема препарата не отмечено.
Обобщая вышеизложенное, отметим, что ИРС 19 имеет выраженный лечебный и профилактический эффект и очень хорошо переносится. Это позволяет рекомендовать его к более широкому использованию в амбулаторных условиях (детские поликлиники) для профилактики сезонной заболеваемости, а также включать в план лечения острых синуситов, затяжных ринитов для профилактики развития осложнений и для скорейшего выздоровления.

По крайней мере в первые годы жизни вполне нормально переносить несколько респираторных инфекций. Эти инфекции (как и другие ранние инфекции) способствуют структурированию и тренировке иммунной системы. Определение характера патологии может происходить только в связи с тяжестью инфекции и средней частотой установленной в процессе наблюдения за когортой. Так от шести до десяти эпизодов ринофарингита является правилом в первые годы жизни с пиком частоты, приходящимся в периоде между шестью и 18 месяцами. Также и в отношении отитов, эпидемиологические исследования из Pittsburgh убедительно показали, что более двух третей детей, обратившихся к врачу в первые три года жизни, имели, по крайней мере, один эпизод отита и, что треть детей перенесла три эпизода или более.
Респираторные рецидивирующие инфекции часто плохо воспринимаются семьями и пугают практических врачей. Для многих пациентов эти рецидивирующие инфекции не представляют ничего иного как последовательность вирусных инфекций в значительной степени, определяемой возрастом, созреванием иммунной системы, факторами окружения (братья и сестры, ясли, недостаток железа и пр.) Для других они являются свидетельством первого проявления атопии. Связь между аллергией и респираторными инфекциями очень трудно установить. Обе патологии часты, совокупность пациентов и аллергична, и обращается с рецидивирующими инфекциями, а известно, что при респираторной аллергии вирусы являются наиболее частой причиной обострения заболевания; и, наоборот, атопи-ческая область объясняет тяжесть вирусных инфекций. Кроме того, если нет сомнений в отношении того, что недостаток железа увеличивают предрасположенность к инфекциям, то и рецидивирующие инфекции способны нарушать на поступление железа. Для некоторых пациентов инфекции могут оказаться первыми признаками сопутствующего более тяжелого заболевания (локального или иногда иммунного). Чрезвычайно редко, чтобы иммунный дефицит единственно проявился бы респираторными рецидивирующими инфекциями без ассоциации с другими инфекциями различной локализации. В то же время, у некоторых пациентов описаны более тонкие иммунные дефициты. Prellner et al. показали, что у детей с рецидивирующими отитами имелись более низкие уровни антител к определенным серотипам пневмококка, чем у здоровых детей контрольной группы того же возраста. Такие же результаты были получены Yamanaka et Faden в отношении протеина Р6 H. Influenzae, не поддающихся типированию. Факторы окружающей среды, очевидно, играют определенную более значимую роль, чем фактический иммунный дефицит.
Ведение таких детей никогда не должно скрывать тот факт, что само естественное течение ведет к излечению в преобладающем большинстве случаев. Также Alho et al. в Финляндии сообщили о наблюдении в течение двух лет за когортой из 222 детей соответствующих международно принятому определению рецидивирующего отита и не получавших никакого специфического лечения; только у 4% из них развился хронический отит и у 12% продолжали проявляться рецидивирующие острые средние отиты. Также и в отношении респираторных инфекций нижних дыхательных путей на сегодня известно, что у значительного большинства грудных детей с эпизодами рецидивирующего свистящего дыхания, связанного с вирусами, эволюция не происходит в сторону астматического заболевания.
Определения
Наиболее распространенное международное определение рецидивирующего отита: три эпизода в течение шести месяцев или четыре эпизода за год. Для формирования группы определение четыре раз за год не достаточно дискриминациионное, в частности, в отношении маленьких детей, находящихся в коллективе. Фактически эти определения надо интепретировать в зависимости от уверенности диагностики предшествующих эпизодов , возраста, контекста (ясли, наличие братье и сестер . . . ), от локального состояния между эпизодами.
Определение рецидивирующих ангин, принятое международно - это семь или более эпизодов в течение одного года или десять в течение двух трех последних лет. Кроме того, соответствие диагностики предшествующих случаев может представить проблему. Распространенность во Франции быстрых диагностических тестов на стрептококк группы А (TDR) вероятно станет прогрессом, позволяющим проводить различие между стрептококковыми инфекциями и другими.
Для ринофарингитов не существует международно принятых определений, но для создания группы кажется приемлемым "более шести эпизодов фебрильного ринофарингита в год, начиная с возраста три года".
Синуситы создают еще более сложную проблему. Если определение рецидива синусита и существу-ет (повторное возникновение симптомов спустя свободный интервал два дня), то трудность диагностики каждого эпизода общепризнанна и нет консенсусного определения рецидиврующего синусита. Единственный обнаруженный в литературе является дериватом отита (три за шесть или четыре за год).
В отношении пневмоний нет международно принятого определения; два эпизода за год или три эпизода за неизвестно какой срок должны рассматриваться как входящие в рамки рецидиврующих пневмоний при условии, что рентгенография была нормальна между эпизодами. Рецидив паренхиматозной инфекции в той же области должен обязательно заставить заняться поиском локальной причины.
В отношении бронхиолитов три эпизода за два первых года жизни заставляют говорить об астме грудного ребенка ; фактически это должно интепретироваться в зависимости от атопического личного и семейного контекста. Что касается ларингитов и бронхитов, то международно принятых определений не существует.
Что же для практики?
Итоги высказываемые в этой главе является отражением консенсусной группы экспертов. Вероятно, они будут применяться все целиком для всех пациентов, но они должны интегрирововаться поэтапно дополнительно к проведению лечения.
Почти все обследования должны включать общую формулу крови, аллергологическое обследование, то есть выявление атопии при этих заболеваниях:
· Суть общей формулы крови состоит в выявлении нейтропении или лимфопении, определении недостатка железа (уровень гемоглобина и средний объем эритроцитов);
· Алллергологическое обследование предлагается проводить в зависимости от анамнеза, возмож-ностей и привычек различных врачей; схематически в зависимости от возраста пациентов и контекста:
· До трех лет: общий IgE, специфичные или целенаправленно выявляемые IgE распределенные по наборам (Trophatop, Phadiatop, например);
· После трех лет: кожные тесты (prick тест) или поиск специфических IgE (Phadiatop).
Другие обследования показаны при различных рецидивирующих респираторных инфекциях:
· Назофаринегеальная фиброскопия: в ней нет необходимости, если имеются клинические признаки обструкции или перманенетный серозный отит между эпизодами среднего острого отита (ОМА), так как при этом показана аденоидектомия. Если таковая требуется, то ее цель состоит в уточнении состояния вегетаций и выявлении опосредованных признаков гастро-эзофагального рефлюкса ;
· PH-метрия имеет своей целью выявление гастро-эзофагального рефлюкса (RGO) внешне не проявляющегося;
· Дозировку иммуноглобулинов (IgG, IgA в частности) часто трудно интерпретировать на первом году жизни;
· Оценка реакции на вакцинальные антигены (тетанус, дифтерия, Hib) могут оказаться более полезными;
· Дозировка подклассов IgG (IgG2) не должна назначаться до достижения возраста двух лет и в случае нормальных результатов предшествующих исследований.
В отношении рецидивирующих отитов изначально обследование включает полную формулу крови и аллергологическое обследование. Уже затем можно обсуждать проведение назофарингеальной фиброскопии. РН-метрия и иммунологический анализ должны рассматриваться только в качестве третьего этапа, если предшествующие обследования окажутся негативными и, если существует инфекция. В отношении рецидивирующих ринофарингитов может быть проведен тот же тип обследования, завершаемый рентгенографией грудной клетки.
В отношении рецидивирующих ангин никакие обследования не оказываются полезными. Фактически исключительно редко, чтобы эта ситуация могла бы привести к выявлению дополнительной причины.
При риносинуситах индивидуальное обследование включает кроме общей формулы крови и аллергологического обследования, рентгенографию грудной клетки и тест на пот. Затем может быть проведен иммунологическое обследование, рН-метрия и сканирование на выявление костных пороков или минимального полипоза. И наконец, негативные предшествующие обследования и непреходящий характер риносинуситов должны привести к проведению чистке щеткой (brossage) или биопсии слизистой носовой полости в целях исключения цилиарной примитивной дискинезии.
Для рецидивирующих респираторных инфекций нижних дыхательных путей выявление причины оказывается фундаментальным. Схемы 1,2 и 3 предлагают для пневмоний, бронхиолитов и рецидивирующих бронхитов древо принятия решений, включающего ведение и проведение различных обсле-дований. Нередко обследование приводит к выявлению множественных причин или различных фак-торов риска возникновения рецидивирующих респираторных инфекций.
Какое лечение?
Всякий раз как только устанавливается терапевтическая или хирургическая причина должна начи-наться специфическое лечение : специфическое лечение респираторной аллергии, гастро-эзофагального рефлюкса (RGO), иммунного дефицита с инъекцией поливалентных иммуноглобулинов … Также во всех случаях родителям должен быть предложен контроль за всеми факторами ок-ружающей среды благоприятствующие рецидиву (табак, ясли, аллергическое окружение …). Олигоэлементы, иммунностимуляторы и другие иммуномодуляторы были предложены для лечения инфекций верхних респираторных путей. Ни одно контролированное исследование, сравнивающее достаточное количество больных, не выявило их пользы.
Польза введения en spray бета-гемолитических стрептококков для стимуляции тренировки барьерного эффекта между инфекционными эпизодами была подтверждена многими клиническими исследованиями проведенными шведскими группами в отношении ангин и OMA. Эти продукты отсутствуют во Франции и не состоят на данный момент в профилактическом терапевтическом арсенале ни одной из стран. Также анти-адгезивные молекулы (препараты) (олигосахариды такие как xylitol) были предложены с противоречивыми результатами.
Для рецидивирующих ORL инфекций медицинское или хирургическое лечение были предложены да-же независимо от причины.
В отношении ангин тесты на диагностику стрептококков группы А (TDR) должны в ближайшем буду-щем провести различие между рецидивирующими ангинами, таковыми вызванными стрептококками группы А, и другими. Для первых лечение антибиотиками в частности доказало свою эффективность благоприятствуя лучшей эрадикации или снижению рецидивов (цефалоспорины второго поколения и третьего поколения amoxillin-acide clavunique, клиндамицин, рифампицин).
Кроме детей поступающих с обструктивными феноменами или осложнениями по типу аденофлегмоны, амигдалектомия должна оставаться исключением, и терпение, как основное оружие, должно вдалбливаться в головы родителей. Действительно, недавнее исследование подтвердило, что та скромная польза отмечаемая после амигдалектомии у умеренно пораженных детей не оправдывает такого типа вмешательства в сравнении с риском заболеваемости вызываемым самим хирургическим вмешательством.
При рецидивирующих ОМА наиболее широко были изучены неспецифические типы лечения: профилактическая антибиотикотерапия длительными курсами, аденоидэктомия, транстимпаническая аэра-ция, вакцины.
· Профилактическая ежедневная антибиотикотерапия малыми дозами показала в контролированных исследованиях двойных слепых versus плацебо (en double insu versus placebo) свою эффективность в предупреждении рецидивов ОМА. Эффективность скромная (снижение на 0,12 эпизода ОМА в месяц и на ребенка), но существенная. Наиболее часто применяемым препаратом был амоксицил-лин. Эволюция бактериальной резистентности, а именно, пневмококков говорит о меньшей эффективности и, прежде всего, о неблагоприятном экологическом воздействии. Поэтому поборники этого метода или отказались или ограничили показания для наиболее тяжелых случаях.
· Хирургия (аденоидектомия с или без аэраторов) показывает эффективность в случае обструкции носа или серозного перманентного отита между эпизодами OMA. При отсутствии серозного выраженного отита между ОИА, польза хирургии ограничена. Фактически, ни аденоидектомия/амигдалектомия, ни аэраторы не уменьшают существенно количество острых эпизодов в группе получавшей лечение по сравнению с контрольными группами. И наоборот, аэраторы снижают количество дней с ОМА. Скромная польза должна взвешиваться в отношении недостатков присущих этому методу: общая анестезия, кровотечение (аденоидектомия/амигдалектомия), тимпанические рубцы (аэраторы) и наконец стоимость.
· Анти-гриппозные вакцины, речь идет о инактивированных вакцинах для инъекций и живой аттенюированной (ослабленной) вакцине способны снизить частоту ОМА. Три исследования продемонстрирвоали снижение на одну треть частоты ОМА в вакцинированных группах у детей без особого антецедента ОМА, посещающих ясли или другие учреждения. И наоборот, недавнее исследование ран-домизированное en double insu включавшее почти 800 пациентов в возрасте от шести до 24 месяцев не обнаружило снижения ОМА в вакцинированной группе. В то же время следует отметить, что в течение двух последних лет проведения исследования величина поаржений гриппом была особенно низкой у детей получавших плацебо : 15,9% первый год и 3,3% второй. Итальянское исследование с использованием виросомальной (отсутствующей во Франции) вакцины обнаружило ту же эффективность у детей соответствующих критериям рецидивирующих отитов. Хотя дети, страдающие рецидивирующими отитами, не входят в популяцию детей, в отношении которых противогриппозная вакцинация рекомендована во Франции комитетом вакцинации, однако эта иммунизация является вероят-но одним из видов профилактического лечения показывающего наилучшие соотношения польза/риск/стоимость в предупреждении ОМА.
· Коньюгированная пневмококковая вакцина в теоретическом плане является одним из наиболее обещающих видов лечения детей, страдающих рецидивирующими отитами; она рекомендована для этих пациентов Американской Академией Педиатрии США. Действительно, у этих детей часто определяются антитела (типа IgA, IgG2) антипневмококковые против серотипов часто присутствующих при ОМА, на более низких уровня чем у контроля. Более того, синтез у них антител после введения анти-пневмококковой полисахаридной вакцины чувствительно менее хорош, чем у нормальных детей группы контроля. Многие крупные исследования двойного слепого контроля, где практиковалось введение коньюгированной вакцины здоровым грудным детям с возраста двух месяцев, показали существенное снижение количества пациентов страдающих рецидивирующими ОМА в группе получавшей коньюгированную вакцину (10% снижение рецидивирующих отитов и более 20% снижение установик транстимпанических аэраторов). Также многие исследования продемонстрировали, что у детей с рецидивирующими отитами, не реагирующими на полисарадные вакцины, коньюгированные вакцины оказались иммуногенными. Естественно, что иммуногеннсть была менее хорошей чем у здоровых без отита детей, но этого оказалось достаточным для большинства пациентов и совокупности серотипов (уровни антител после вакцинации возрастали в 4 или выше от 1 mgr/ml).
Недавно проведенное двойное слепое контролированное исследование у пациентов с антецедентами ОМА и вакцинированных спустя в среднем 18 месяцев (Prevenar при примовакцинации, затем для напоминания полисахаридная вакцина) не показали никакого снижения количества отитов в группе вакцинированной антипневмококковыми вакцинами. Выдвигались различные гипотезы в попытке объяснить вводящие в заблуждение результаты. Наиболее вероятно, что у этих ослабленных пациентов происходило замещение в ринофаринксе серотипов пневмококков содержащихся в вакцине другими бактериями (другими серотипами пневомококка или другими видами). Даже, если антипневмококковые вакцины не уменьшали частоты эпизодов ОМА у детей соответствующих критериям ре-циливирующих ОМА, тем не менее, можно обозначить два благотворных эффекта : снижение риска системных инфекций и снижение резистентности к антибиотикам имеющихся бактерий. Фактически серотипы содержащиеся в антипневмококковой коньюгированной вакцине во Франции представляют преобладающее большинство видов резистентных к антибиотикам. Снижая носительство и величину участия этих видов в ОМА это уменьшает риск наличия резистентного вида.
Польза от антигриппозных вакцин и антипневмококковых коньюгированых вакцин не должна ограничиваться рецидивами ОМА, но должна переносится и на детей с рецидиврующими пневмопатиями.
Заключение
Респираторыне рецидивирующие инфекции представляют собой часто встречающуюся в педиатрии проблему. Задача состоит в выявлении детей с сопутствующим заболеванием, не преумножая величину и лечения "нормальных" детей : незаменимую пользу приносят опрос, клиническое обследование и несколько дополнительных обследований. Отношения польза/риск/затраты медицинских и предлагаемых хирургических методов лечения должны сопоставляться с перспективами предоставляемыми вакцинами, а именно антигриппозными и коньгированными антипневомкокковыми.
Инфекции верхних дыхательных путей могут быть причиной следующих состояний:
• затруднения вскармливания детей грудного возраста, поскольку нос у них заложен, это затрудняет дыхание;
• фебрильных судорог;
• обострения бронхиальной астмы.
Детям грудного возраста может быть необходима госпитализация для исключения более серьёзной инфекции, при недостаточности питания или для утешения родителей.
Обычная простуда (насморк). Это наиболее распространённая инфекция в детском возрасте. Классические признаки включают прозрачные или слизисто-гнойные выделения из носа и заложенность носа. Наиболее распространёнными возбудителями бывают вирусы — риновирусы (существует более 100 их различных серотипов), коронавирус и РСВ.
В качестве санитарного просвещения следует сообщить родителям, что такая простуда — самоограничивающееся заболевание и не существует его специфического лечения; это может уменьшить тревогу родителей и предотвратить ненужные визиты к врачу. Лихорадку и боль лучше всего лечить парацетамолом или ибупрофеном. Антибиотики бесполезны, поскольку обычная простуда имеет вирусное происхождение, а вторичная бактериальная природа встречается очень редко.

Боль в горле (фарингит). Боль в горле обычно развивается вследствие инфицирования респираторными вирусами (главным образом аденовирусами, энтеровирусами и риновирусами). У более старших детей очень распространённым возбудителем бывает b-гемолитический стрептококк группы А. Глотка и мягкое нёбо воспалены, а локальные лимфатические узлы увеличены и болезненны.
Тонзиллит. Это форма фарингита, при которой отмечают значительное воспаление миндалин, часто с гнойным экссудатом. Наиболее распространённые возбудители — b-гемолитический стрептококк группы А и ЭБВ.
Хотя наиболее частой причиной фарингита и тонзиллита бывают вирусы, особенно у детей дошкольного возраста, клинически различить вирусную и бактериальную причины невозможно. Ярко выраженные органические расстройства, такие как головная боль, апатия, боль в животе, экссудат на миндалинах и лимфаденопатия шейных лимфатических узлов, чаще встречают при бактериальной инфекции.
Антибиотики (в основном бензилпенициллин или эритромицин, если существует аллергия на бензилпенициллин) часто назначают при тяжёлом фарингите и тонзиллите, несмотря на то, что только треть из них вызвана бактериями. Они могут ускорить выздоровление от стрептококковой инфекции, но необходимо 10 дней лечения, чтобы уничтожить возбудителей и предотвратить развитие ревматизма (в настоящее время это чрезвычайно редко происходит в Западной Европе).
Лучше избегать назначения амоксициллина, поскольку он может вызвать распространённую пятнисто-папулёзную сыпь, если причиной тонзиллита стал инфекционный мононуклеоз.
Невозможно клинически различить вирусный и бактериальный тонзиллит.
Синусит. Инфицирование околоносовых пазух может возникнуть при вирусных инфекциях верхних дыхательных путей. Иногда это вторичная бактериальная инфекция с болью, опуханием и болезненностью щеки из-за инфицирования верхнечелюстной пазухи. Поскольку лобные пазухи не развиты до подросткового возраста, лобный синусит редко встречают в первые 10 лет жизни. Для лечения острого синусита используют антибиотики и обезболивающие препараты.
Детей с рецидивирующими инфекциями верхних дыхательных путей часто направляют для удаления миндалин и аденоидов, это наиболее частые операции, проводимые у детей. У многих детей отмечают большие миндалины, но это само по себе не считают показанием к тонзилэктомии, поскольку миндалины самопроизвольно уменьшаются в подростковом возрасте.
Показания к тонзилэктомии спорны, но включают следующие состояния:
• рецидивирующий тонзиллит (в противоположность рецидивирующим инфекциям верхних дыхательных путей) — тонзилэктомия уменьшает количество эпизодов тонзиллита на треть, например, с трёх до двух в год;
• паратонзиллярный абсцесс (острый гнойный тонзиллит);
• обструктивное апноэ во время сна.
Как и миндалины, аденоиды увеличиваются в размерах приблизительно до 8 лет жизни, а затем постепенно уменьшаются. У детей раннего возраста аденоиды растут относительно быстрее, чем дыхательные пути, поэтому такое их влияние, как сужение просвета воздухоносных путей, наиболее выражено в возрасте между 2 и 8 годами. Они могут сузить заднее носовое пространство настолько, что аденоидэктомия будет оправданна. Показания для удаления как миндалин, так и аденоидов спорны, но включают следующие состояния:
• средний отит с выпотом и потерей слуха, когда это даёт небольшое дополнительное преимущество для введения отоскопа (продувание труб);
• обструктивное апноэ во время сна (абсолютное показание).
Читайте также:


