Что такое инфекционная энцефалопатия
Энцефалопатия — это обобщающее название разнообразных по своему генезу патологических процессов, основу которых составляет дегенерация нейронов головного мозга вследствие нарушения их метаболизма. Энцефалопатия проявляется полиморфными неврологическими расстройствами, нарушениями в интеллектуально-мнестической и эмоционально-волевой сфере. Диагностический поиск состоит из комплексного неврологического обследования и установления причинной патологии. Лечение энцефалопатии сводится к устранению вызвавшего ее патологического состояния, терапии причинного заболевания и поддержанию оптимального метаболизма церебральных нейронов.
МКБ-10
Общие сведения
Понятие перинатальная энцефалопатия было введено в 1976 г. и подразумевает церебральные поражения, возникающие в период с 28-й недели беременности до 7-го дней жизни. Перинатальная энцефалопатия манифестирует у детей первых месяцев жизни. Приобретенная энцефалопатия имеет вторичный характер и отмечается преимущественно у взрослых, чаще у лиц среднего и пожилого возраста, при наличии тяжелых хронических заболеваний, после перенесенных травм, интоксикаций и т. п. Энцефалопатия является междисциплинарной патологией, в соответствии с этиологией требующей внимания со стороны специалистов в области неврологии, педиатрии, травматологии, наркологии, токсикологии, урологии.

Причины энцефалопатии
К триггерным факторам, в результате воздействия которых может возникнуть перинатальная энцефалопатия, относятся:
Риск перинатальной патологии возрастает при аномалиях родовой деятельности, крупном плоде, преждевременных родах и недоношенности новорожденного, узком тазе, обвитии пуповиной.
Приобретенная форма патологии может развиваться вследствие:
- перенесенной черепно-мозговой травмы;
- воздействия ионизирующего излучения;
- интоксикации нейротропными химическими (этиловым спиртом, свинцом, хлороформом, наркотиками, барбитуратами) и бактериальными (при дифтерии, столбняке, ботулизме и др.) токсинами;
- сосудистых нарушений: атеросклероза, артериальной гипертензии, венозной дисциркуляции, ангиопатии церебральных сосудов при амиломидозе, приводящих к хронической ишемии головного мозга;
- осложнения различных заболеваний внутренних органов: острого панкреатита, острой и хронической почечной недостаточности, цирроза печени и печеночной недостаточности;
- болезней легких, приводящих к расстройству легочной вентиляции (туберкулез легких, абсцесс легкого, бронхоэктатическая болезнь, ТЭЛА). Аналогичный гипоксический генез имеет энцефалопатия, наблюдаемая у ряда пациентов после проведения реанимационных мероприятий;
- метаболических расстройств: энцефалопатия может развиться как при понижении уровня глюкозы (гипогликемии), так и при его повышении (гипергликемии), что часто наблюдается при сахарном диабете. Причиной метаболических церебральных расстройств бывает гиповитаминоз (в первую очередь недостаток витаминов гр. В);
- падения осмотического давления и гипонатриемии, возникших из-за задержки воды при гиперсекреции антидиуретического гормона (при гипотиреозе, надпочечниковой недостаточности, опухолевых процессах и пр.);
- к редко встречающимся относится лейкоэнцефалопатия, имеющая вирусную этиологию и отмечающаяся у иммунокомпрометированных пациентов.
Патогенез
Энцефалопатия любого генеза является диффузным, т. е. затрагивающим различные церебральные структуры, процессом. В ее основе лежит кислородная недостаточность (гипоксия) и обменные нарушения нейронов. Последние могут быть обусловлены самой гипоксией (при дисциркцуляторных и гипоксических энцефалопатиях), дефицитом отдельных метаболитов и воздействием токсинов (при метаболических и токсических энцефалопатиях). Указанные нарушения приводят к дегенерации и гибели церебральных нейронов.
К морфологическим признакам, которыми характеризуется энцефалопатия, относятся: дегенерация и уменьшение количества нейронов в мозговом веществе, а значит его диффузная атрофия; очаги демиелинизации и некроза, а также глиальные разрастания, локализующиеся в белом веществе; микрогеморрагии и отечность церебральных тканей; полнокровие церебральных оболочек. Преимущественная локализация указанных изменений и степень их выраженности может варьировать в зависимости от вида энцефалопатии.
Классификация
В соответствии с этиологическим фактором, энцефалопатия классифицируется на посттравматическую, токсическую, метаболическую, сосудистую (дисциркуляторную), лучевую.
- Посттравматическая энцефалопатия относится к отдаленным последствиям ЧМТ и может развиваться через несколько лет после нее.
- Токсические варианты включают алкогольную энцефалопатию, наблюдающуюся при хроническом алкоголизме, а также церебральные нарушения, возникающие у наркоманов.
- Метаболические варианты: печеночная (портосистемная, билирубиновая), уремическая (азотемическая), диабетическая, панкреатическая, гипогликемическая, гипоксическая, аноксическая энцефалопатии и синдром Гайе-Вернике.
- Дисциркуляторная энцефалопатия подразделяется на атеросклеротическую, гипертоническую, венозную. Отдельной формой гипертонической энцефалопатии выступает болезнь Бинсвангера.
В клинической практике используют градацию энцефалопатии по тяжести, однако это разграничение весьма условно:
- I степень тяжести подразумевает субклиническое течение, т. е. отсутствие проявлений при наличии церебральных изменений, фиксируемых инструментальными методами диагностики. В этой стадии патология может диагностироваться при проведении диспансерного обследования пациентов с хроническими, в первую очередь сосудистыми, заболеваниями.
- II степень тяжести характеризуется наличием легкой или умеренной неврологической симптоматики, зачастую имеющей преходящий характер.
- При III степени наблюдаются тяжелые неврологические расстройства, в большинстве случаев выступающие причиной инвалидизации пациента.
Симптомы энцефалопатии
Более распространена хроническая энцефалопатия, отличающаяся малосимптомным началом и постепенным развитием. Наиболее часто она имеет дисдиркуляторный и посттравматический характер. Острая энцефалопатия характеризуется внезапным дебютом и быстрым усугублением состояния пациента, наличием нарушений сознания. Она может возникнуть при интоксикациях и дисметаболических расстройствах. Примерами являются острая панкреатическая, уремическая, печеночная энцефалопатия, синдром Гайе-Вернике, гипоксическая энцефалопатия при ТЭЛА.
На ранних стадиях проявляется затруднениями при попытке вспомнить недавние события или недавно полученную информацию, снижением внимательности и умственной работоспособности, утомляемостью, нарушением сна, недостаточной гибкостью при перемене вида деятельности, психоэмоциональной лабильностью. Пациенты могут отмечать повышенную раздражительность, дневную сонливость, шум в голове, головную боль, не имеющую определенной локализации.
Симптомы могут варьировать у разных больных. В неврологическом статусе возможен нистагм, умеренная гиперрефлексия и мышечная гипертония, наличие рефлексов орального автоматизма и стопных знаков, неустойчивость в позе Ромберга, дискоординация, недостаточность ЧМН (понижение зрения, тугоухость, легкий птоз, парез взора), признаки вегетативной дисфункции.
Прогрессирование энцефалопатии сопровождается усугублением симптомов с формированием того или иного четко доминирующего неврологического синдрома: вестибуло-атактического, паркинсонического, гиперкинетического, псевдобульбарного. Нарастание нарушений интеллектуальной и эмоционально-волевой сферы приводит к формированию деменции. Возможны психические расстройства.
Дебютирует внезапным психомоторным возбуждением с интенсивной головной болью, зрительными нарушениями, тошнотой и рвотой, шаткостью, в некоторых случаях — онемением языка, дистальных отделов кистей и стоп, психическими расстройствами. Достаточно быстро возбуждение сменяется апатией, зачастую происходит нарушение сознания различной глубины: оглушенность, дезориентация, сопор и кома. Могут наблюдаться различные виды эпиприступов. Острая энцефалопатия относится к ургентным состояниям и без оказания срочной медицинской помощи может привести к смертельному исходу вследствие отека мозга, нарушения функции жизненно важных церебральных центров.
Диагностика
Первичная диагностика энцефалопатии осуществляется неврологом по результатам опроса и неврологического осмотра. Дополнительно проводится комплексное инструментальное неврологическое обследование:
- Электроэнцефалография. ЭЭГ, как правило, выявляет диффузную дезорганизацию биоэлектрической активности мозга с появлением медленных волн. Возможно выявление эпи-активности.
- Эхоэнцефалография. Эхо-ЭГ позволяет оценить внутричерепное давление.
- Сосудистые исследования.Реоэнцефалография или УЗДГ сосудов головы дают информацию о состоянии церебрального кровообращения.
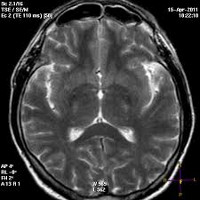
- Томография. Проанализировать степень морфологических изменений можно при помощи МРТ головного мозга. Этот метод также позволяет дифференцировать энцефалопатию от других церебральных заболеваний: болезни Альцгеймера, внутримозговой опухоли, энцефалита, рассеянного энцефаломиелита, инсульта, кортикобазальной дегенерации, болезни Крейтцфельдта — Якоба и пр.
Важнейшее значение в понимании этиологии энцефалопатии имеет сбор анамнеза, обследование соматических органов и консультации смежных специалистов: кардиолога, нефролога, гастроэнтеролога, эндокринолога, пульмонолога, нарколога. По показаниям проводятся гормональные исследования, определение уровня холестерина и сахара крови, анализ мочи, биохимия крови и мочи, УЗИ печени, УЗИ поджелудочной железы, экскреторная урография, УЗИ мочевыделительной системы, КТ почек, рентгенография грудной клетки, КТ легких и т. п.
Лечение энцефалопатии
Острая энцефалопатия является показанием к срочной госпитализации и ургентной терапии. Она может потребовать таких мер, как ИВЛ, гемодиализ, парентеральное питание. В лечении как острой, так и хронической энцефалопатии, ведущее место принадлежит терапии причинного заболевания.
При интоксикациях производится дезинтоксикация, в т. ч. введение инфузионных растворов; при дисметаболических нарушениях — коррекция метаболизма (подбор дозы сахароснижающих препаратов или инсулина, введение р-ра глюкозы, в/в введение тиамина). Осуществляется лечение гепатита, цирроза, панкреатита, нефрита, заболеваний легких, гипертонической болезни, атеросклероза. Рекомендуется соблюдение диеты, соответствующей основной патологии, и режима, адекватного состоянию пациента.
Наличие ишемического компонента в патогенезе энцефалопатии является показанием к назначению сосудистой терапии: пентоксифиллина, тиклопидина, винпоцетина, ницерголина. Атеросклеротическая энцефалопатия требует включения в схему лечения гиполипидемических фармпрепаратов (например, симвастатина, гемфиброзила). Терапия гипертонической энцефалопатии проводится с назначением гипотензивных средств и мониторированием цифр АД.
В обязательном порядке проводится нейропротекторная и метаболическая терапия. В нее входят ноотропы (к-та гопантеновая, пирацетам, пиритинол, луцетам), аминокислоты (глицин, глутаминовая кислота), витамины (В1, В6, С, Е), препараты ГАМК (пикамилон, фенибут). При психических расстройствах необходимы психотропные средства: диазепам, бромиды, дроперидол, фенозепам. При судорогах проводится антиконвульсантная терапия, ноотропы противопоказаны.
Фармакотерапия осуществляется повторными курсами 2-3 раза в год. В качестве вспомогательного лечения используются методы физиотерапии: рефлексотерапия, электрофорез, магнитотерапия.
Прогноз и профилактика
Во многих случаях прогноз вторичной энцефалопатии определяет то, насколько эффективно можно лечить причинную патологию. Исход терапии также зависит от степени произошедших церебральных изменений. В ряде случаев положительным эффектом считается стабилизация энцефалопатии. При дальнейшем прогрессировании энцефалопатия достигает III степени и приводит к тяжелым неврологическим и эмоционально-психическим нарушениям, инвалидизирующим пациента. В случае перинатальной или острой энцефалопатии исход зависит от массивности и тяжести поражения мозговых тканей. Зачастую острые токсические энцефалопатии сопровождаются глубоким и необратимым поражением мозга.
Профилактика перинатальной энцефалопатии — это вопрос корректного выбора способа родоразрешения, адекватного ведения беременности, соблюдения правил ухода за новорожденным. Профилактика вторичной энцефалопатии заключается в своевременном выявлении и адекватном лечении сосудистых, урологических, гастроэнтерологических заболеваний, легочной патологии, эндокринных и метаболических нарушений. В качестве профилактических мер можно рассматривать правильное питание, активный образ жизни, отказ от курения, наркотиков и алкоголя.

Токсическая энцефалопатия возникает вследствие негативного воздействия на головной мозг различных токсинов, как правило, экзогенного происхождения, которые способны проникать через гематоэнцефалический барьер в нейроны и вызывать их структурные изменения.
Токсическое повреждение нервной ткани может протекать как остро, так и хронически, но эту патологию нельзя назвать редкой главным образом потому, что в числе ядов — алкоголь и наркотические вещества, которыми злоупотребляет значительное число людей, причем чаще — молодого возраста.
Негативное влияние нейротропных ядов проявляется разнообразными психоневрологическими нарушениями, нередко процесс носит необратимый прогрессирующий характер, способствуя стойкой инвалидизации, а в тяжелых случаях — смерти больных.
Головной мозг чрезвычайно чувствителен к неблагоприятным внешним воздействиям. Его клетки страдают от недостатка кислорода, действия самых разных химических веществ, попадающих в кровь через органы дыхания, пищеварения, инъекционным путем. Даже небольшие количества сильных нейротропных ядов могут вызвать тяжелейшие деструктивные изменения, бороться с которыми подчас невозможно.
Постоянное поступление небольших доз токсинов на производстве или в быту влечет развитие хронической энцефалопатии, первые признаки которой неспецифичны или и вовсе незаметны, что затрудняет своевременную диагностику и откладывает время начало лечения до развернутой стадии страдания мозга.
По мере накопления в мозге токсических продуктов, нарастают дистрофические и некротические процессы в его клетках, появляются очажки микроинфарктов вследствие нарушения микроциркуляции, усугубляется гипоксия. Процесс носит диффузный характер, однако первыми страдают наиболее уязвимые отделы центральной нервной системы — подкорковые узлы, ствол мозга, мозжечок, чем объясняется тяжесть симптоматики и серьезный риск для жизни пациента.
Особенности симптоматики и скорость прогрессирования мозгового поражения обычно связаны с характером токсина, путем его проникновения и дозой. В ряде случаев имеются специфические симптомы, характерные для того или иного вида токсической энцефалопатии, позволяющие проводить целенаправленные исследования состава крови для определения причинного фактора.
Причины и виды токсической энцефалопатии

Токсическая энцефалопатия бывает:
В случае острой патологии симптоматика нарастает быстро, через короткое время после поступления нейротропного яда, при этом доза — не всегда имеет решающее значение. К примеру, острая алкогольная энцефалопатия может возникнуть после употребления довольно большого объема этанола, в то время как количество метилового спирта или этиленгликоля может быть относительно небольшим.
Хроническая энцефалопатия нарастает неделями и месяцами и связана чаще всего с постоянным употреблением ядовитых веществ в тех количествах, которые не вызывают острой интоксикации, однако способствуют кумуляции яда в нейронах и их диффузной деструкции.
Вещества, провоцирующие токсическую энцефалопатию, проникают из внешней среды или образуются в ходе метаболизма в организме больного при патологии печени, эндокринной системы, почек. Яды могут попадать в организм при контакте с ними на производстве, к примеру, на объектах химической промышленности. В быту самым частым нейротропным ядом становится этиловый спирт.
Хроническую энцефалопатию токсического генеза (код по МКБ 10 – G92) могут спровоцировать неблагоприятные экологические условия, когда крупные промышленные предприятия выбрасывают в атмосферу большое количество ядовитых веществ и отходов производства. В таких неблагополучных регионах жители чаще сталкиваются с хронической головной болью, ранними признаками сосудистого поражения мозга, симптомами кислородного голодания. Определенный риск создают и техногенные катастрофы, сопровождающиеся попаданием в атмосферу и воду нейротропных ядов.
Потенциально опасными нейротропными ядами считаются:
- Этиловый спирт;
- Наркотические вещества, особенно — произведенные в кустарных условиях;
- Метанол;
- Продукты нефтеперегонки, углеводороды;
- Угарный газ;
- Пестициды, использующиеся в сельском хозяйстве;
- Некоторые тяжелые металлы (свинец, ртуть и др.) и их соединения;
- Марганец;
- Отдельные лекарственные средства;
- Эндогенные продукты обмена — кетоновые тела, соли мочевой кислоты, билирубин.
Марганцевая (как и алкогольная) энцефалопатия выделена в отдельную группу ввиду особенностей симптоматики. Этот элемент может попасть в организм вместе с наркотиками, изготовленными кустарно, реже — на производстве (металлургическая промышленность, добыча руды). Проявления марганцевого отравления напоминают болезнь Паркинсона.
Нейротропными могут быть и яды биологического происхождения. К примеру, токсическая энцефалопатия способна развиться при таких инфекционных заболеваниях как ботулизм, дифтерия, корь.
Симптоматика токсической энцефалопатии

Энцефалопатия токсического генеза имеет довольно разнообразную симптоматику, часть проявлений может указывать на конкретный токсический агент, но есть и общие признаки повреждения нервной ткани, возникающие вне зависимости от типа действующего яда. Таковыми считаются:
- Возбуждение, беспокойное поведение, чувство страха;
- Эйфоричность или агрессия;
- Судорожный синдром;
- Расстройство координации движений (больше характерны для хронической формы с поражением мозжечковых структур);
- Онемение частей тела;
- Головокружения, головные боли;
- Явления паркисонизма;
- Вегетативная дистония с нарушением терморегуляции, сердечного ритма, мочеиспускания.
Часто действие нейротоксина начинается симптомами возбуждения, пациент может стать агрессивным и неадекватным в поступках и речи. По мере увеличения концентрации яда в нейронах деятельность мозга угнетается, появляется сонливость, наступают состояние оглушенности и кома. Рефлексы и подвижность снижаются, при сопутствующих поражениях спинного мозга присоединяются также расстройства чувствительности и работы тазовых органов.
Алкогольная энцефалопатия
Одной из самых частых причин токсического поражения нейронов считается отравление этанолом. Специалисты такую форму энцефалопатии определили в самостоятельное заболевание — алкогольная энцефалопатия. Хроническое течение патология приобретает при систематическом длительном злоупотреблении спиртным, а первые симптомы становятся заметны уже примерно через три года после регулярного приема алкогольных напитков.

Этанол способен вызывать повреждение нейронов и утрату ими взаимосвязей не только сам по себе, но и благодаря таким токсичным продуктам метаболизма, как уксусный альдегид. Кроме непосредственного токсического действия, алкоголь может вызывать расстройства микроциркуляции и тромбообразование, необратимые изменения сосудистых стенок, множественные кровоизлияния.
При употреблении чрезмерных доз этанола или отравлении его суррогатами развивается острая алкогольная энцефалопатия, которая может протекать в виде синдрома Гайе-Вернике, алкогольного псевдопаралича и других форм патологии.
Симптоматика токсической энцефалопатии при алкоголизме включает:
- Нарастающую слабость, постоянное чувство усталости;
- Потерю веса;
- Головокружения и краниалгии;
- Расстройства пищеварения в виде неустойчивого стула, рвоты;
- Бессонницу, кошмарные сновидения;
- Потливость, тахикардию и другие расстройства ритма.
Пациенты худеют, кожа становится бледной, а затем синюшной, с выраженной сосудистой сеточкой на лице, характерна отечность, одутловатость лица. Неврологическая симптоматика складывается из нарушений координации, неустойчивости, тремора конечностей, губ, парестезий.
Психические изменения очень характерны для алкогольной энцефалопатии. Пациенты могут быть агрессивны или апатичны, склонны к депрессии, эмоционально лабильны. Галлюцинации носят угрожающий характер, прогрессирует нарушение сна. Значительно снижается интеллект и способность выполнять умственную работу.
Тяжелейшей формой алкогольного поражения мозга считается энцефалопатия Гайе-Вернике, когда от первых признаков патологии до гибели больного проходит всего 2 недели. Она проявляется делирием с галлюцинациями, который сменяется полной заторможенностью и обездвиживанием.
Пациенты неадекватны и недоступны контакту, истощены, отечны, выражена неврологическая симптоматика в виде парезов и параличей, гиперкинезов. Характерны повышение температуры тела, учащенные пульс и дыхание, гипотония. Нередки судорожные припадки генерализованного характера.
Кома вызвана прогрессирующим отеком мозга и распространенными геморрагиями в среднем и промежуточном отделах мозга, при этом полностью утрачивается сознание и серьезно нарушается работа жизненно важных органов. Присоединение вторичных инфекций увеличивает риск смерти.
Исходом острой энцефалопатии алкогольного происхождения может стать стойкий психоорганический синдром с необратимой мозговой дисфункцией, утратой трудоспособности и навыков самообслуживания.

изменения мозга при алкогольной токсической энцефалопатии
Отравление марганцем
Марганец оказывает токсическое действие преимущественно на подкорковые нервные центры, сосудистую сеть мозга, а отравления чаще регистрируются при добыче руды и ее переработке, при производстве сплавов и электродов. Симптомами отравления считаются:

- Вялость, сонливость;
- Снижение тонуса мышц;
- Неясные боли в конечностях;
- Снижение интеллектуальных способностей — расстройства памяти, письма;
- Апатия, депрессия.
В тяжелых случаях прослеживается расширение глазных щелей, тремор языка и признаки паркинсонизма, неадекватные эмоциональные реакции в виде смеха или плаксивости. Эти изменения носят органический характер и необратимы, поэтому уже при первых признаках отравления марганцем пациент изолируется от контакта с металлом.
В клинике выделяют три степени (стадии) марганцевой энцефалопатии. На первой наблюдаются астенизация, слабость, чувство сонливости, повышение артериального давления, снижение тонуса мышц, боли и парестезии в ногах и руках. На второй стадии перечисленные симптомы усиливаются, нарушается интеллект, нарастает полинейропатия. Для третьей стадии характерны нарушения двигательной сферы, походки, речи. Больной теряет самокритику, появляется эмоциональная нестабильность, насильственный смех либо плач.
Отравления тяжелыми металлами, медикаментами и парами токсических веществ
При ртутной энцефалопатии четко проявляются гиперкинезы, прогрессируют психические нарушения. При попадании ртути в органы пищеварения появляются сильные боли в животе, рвота, диарея с кровью. Начальная степень отравления протекает наподобие вегетативной дисфункции и неврастенического расстройства. Пациенты жалуются на раздражительность, плохой сон, головные боли, учащенный пульс, повышенное потоотделение. Характерны расстройства функции эндокринных органов.
При острой ртутной интоксикации усиливается боль в голове, пропадает сон, нарастает вегетативная симптоматика — кардиалгии, тахикардия, колебания давления. Прогрессирование отравления влечет психические нарушения.

При действии свинца на нейроны появляются характерный металлический сладкий привкус во рту, слюнотечение, рвота, абдоминальные боли, запоры, метеоризм. Бывают также краниалгии, психические нарушения, патология дыхания и сердцебиения. Осложнениями интоксикации свинцом считаются полиневриты токсического генеза, параличи и парезы.
Отравления сероуглеродом встречаются на химических и текстильных производствах, в сельском хозяйстве при применении инсектицидов. Это соединение вызывает вегетативные расстройства и нарушения нервной регуляции. В клинике возможны психические нарушения, вегетативная дисфункция, полинейропатии, мозговая астения. В тяжелых случаях наступает кома.
При хроническом длительном воздействии яда развивается органическое поражение мозга, появляются разнообразные галлюцинации, теряется интеллект, нарастает депрессия, паркинсонизм, становится постоянной гипертония.
Пары бензина при вдыхании вызывают отравление и признаки энцефалопатии. Характерен психоорганический синдром, повышенная судорожная готовность, сосудистая дистония, эмоциональная лабильность, беспокойство, нарушения сна.
Попадание мышьяка провоцирует диффузную дистрофию нейронов как в мозге, так и в периферических нервных стволах, при этом полинейропатии выходят на первый план в клинике заболевания. Характерны жгучие боли и слабость в конечностях, трофические нарушения в коже, атрофические изменения мышц.
Лекарственная энцефалопатия возникает при передозировке аспиринсодержащих препаратов, брома, нейролептиков, снотворных и даже нестероидных противовоспалительных средств. Она проявляется слабостью, головной болью, расстройствами зрения, речи, дыхания, рвотой, психическими нарушениями — возбужденность, агрессия или апатия, сонливость.
Эндогенные интоксикации

Еще одной причиной токсической энцефалопатии способна стать патология внутренних органов — печени и почек. Такие пациенты также имеют разнообразную психоневрологическую симптоматику — меняется поведение (агрессивность, апатия, депрессия и др.), снижается интеллект, появляются неопрятность и трудности с самообслуживанием, парестезии, расстройства двигательной сферы и функции тазовых органов. Тяжелые степени сопровождаются комой и церебральным отеком.
На специфическую причину токсической энцефалопатии могут указывать данные о поражении конкретного органа — увеличение печени, желтуха, кровоточивость, характерный печеночный или уремический запах, отеки и бледность, скопление жидкости в полостях, эрозивные поражения слизистых пищеварительной и дыхательной системы.
Ввиду особенностей патогенеза, течения и терапии указанные виды токсической энцефалопатии отнесены к патологии соответствующих органов и имеют отдельные рубрики в Международной классификации болезней — печеночная или другие неуточненные энцефалопатии (К72, G93.4).
Лечение и последствия токсической энцефалопатии
Органическое поражение мозговой ткани при действии нейротропных ядов не проходит бесследно. Восстановить утраченные нейроны вряд ли возможно, поэтому изменения психики и неврологического статуса зачастую носят стойкий характер, приводя к инвалидности. Опасными последствиями считаются:
- Психоорганический синдром с потерей интеллектуальных способностей;
- Кома и смерть;
- Кровоизлияние в головной мозг;
- Необратимые психические расстройства — галлюцинации, депрессия, астеноневротический синдром;
- Судорожный синдром;
- Параличи и полинейропатии.
Лечение токсической энцефалопатии должно быть начато как можно раньше, при самых первых симптомах неблагополучия. Кроме того, важен комплексный подход, учитывающий характер токсина, степень мозговой дисфункции, состояние других органов больного.
При тяжелой энцефалопатии тактика направлена на стабилизацию состояния, во всех случаях показана инфузионная терапия и быстрейшее ограничение контакта с ядовитым веществом. Пациенты наблюдаются в условиях токсикологических или реанимационных отделений, где есть все возможности для осуществления интенсивной терапии.
Первое действие, которое должно быт предпринято, – прекращение контакта с нейротропным ядом (для экзогенных токсинов). В случае энцефалопатии на фоне поражения печени или почек прекратить действие токсических агентов сразу невозможно, поэтому начинается активная детоксикационная терапия.

Основными принципами лечения тяжелых поражений мозга при интоксикации являются:
- Консервативные или хирургические способы дезинтоксикации, введение специфических антидотов;
- Инфузия растворов и форсирование диуреза (имеет ограничения при почечной недостаточности);
- Применение средств, усиливающих распад ядовитых веществ — глюкоза, витамин С, кислородные смеси, гипохлорид натрия);
- Переливание альбумина, свежезамороженной плазмы для нормализации реологических свойств крови и гемостаза;
- Введение глюкокортикоидов и диуретиков для борьбы с отеком мозга;
- Использование препаратов, улучшающих обменные процессы в мозге — церебролизин, ноотропил, АТФ, никотиновая кислота, витамины С и группы В;
- Противосудорожное лечение — диазепам, магнезия, гексенал;
Выведение нейротропного яда производится путем назначения солевых растворов в вену, глюкозы, ускорения выделения мочи мочегонными препаратами. Показаны очистительные клизмы и промывание желудка, чтобы прекратить дальнейшее всасывание токсина. При необходимости проводится гемодиализ, гемосорбция и плазмаферез.
Симптоматическая терапия включает применение противосудорожных средств (клоназепам, диазепам), транквилизаторов, нейролептиков при психозах. Для восстановления кровотока в мозге показаны сосудистые средства и антигипоксанты (кавинтон, ноотропил, актовегин, витамины группы В и др.). В случае необходимости назначаются гипотензивные средства, антиаритмики, специфические антидоты при их наличии.
Среди консервативных методов лечения важное значение придается психотерапии. Особенно показана она при алкогольном поражении и злоупотреблении наркотическими средствами, а также депрессивных расстройствах. Кроме того, используются методы физиотерапии (массаж, дарсонваль, лечебные ванны).
На протяжении всего реабилитационного периода пациент принимает поливитаминные комплексы, антиоксиданты, препараты на основе омега-3, нооторопы. По показаниям продолжаются прием антидепрессантов и работа с психотерапевтом.
Прогноз при энцефалопатии токсического генеза очень серьезный вне зависимости от того, какой яд ее вызвал, так как повреждения носят необратимый характер. Риск развития отека мозга, комы, стойкого психоорганического синдрома требует предельно раннего начала лечения и динамического наблюдения за пациентом после стабилизации состояния.
Видео: о токсической энцефалопатии после приема наркотиков
Читайте также:


