Анаэробная инфекция в кале
Комплексное молекулярно-генетическое исследование, которое позволяет выявить генетический материал наиболее вероятных возбудителей острых кишечных инфекций в кале и установить этиологию заболевания.
Синонимы английские
Acute intestinal infection screening; Bacterial and viral diarrhea screening, PCR, fecal samples.
Полимеразная цепная реакция в режиме реального времени.
Какой биоматериал можно использовать для исследования?
Как правильно подготовиться к исследованию?
- Исследование рекомендуется проводить до начала приема антибиотиков и других антибактериальных химиотерапевтических препаратов.
- Исключить прием слабительных препаратов, введение ректальных свечей, масел, ограничить прием медикаментов, влияющих на перистальтику кишечника (белладонна, пилокарпин и др.) и на окраску кала (железо, висмут, сернокислый барий), в течение 72 часов до сбора кала.
Общая информация об исследовании
Острые кишечные инфекции (ОКИ) – группа заболеваний, обусловленных вирусами, бактериями или паразитами, для которых характерен фекально-оральный механизм передачи. Общими для данных инфекций являются факторы передачи: пищевые продукты, вода, инфицированные бытовые предметы и грязные руки. Первые симптомы возникают через несколько часов или дней после инфицирования, начало резкое, с появлением частого жидкого стула, рвоты, боли в животе, признаков интоксикации (лихорадки, озноба, тошноты). Заболевание может носить групповой характер и проявиться у нескольких человек, употреблявших инфицированную пищу или воду.
Согласно официальной статистике, в России до 65-67% заболеваний этой группы составляют ОКИ неуточненной этиологии. Если возбудитель инфекции неизвестен, эффективность противоэпидемических мероприятий ограничивается. Соотношение частоты выявления вирусных и бактериальных патогенов варьируется в разных возрастах: у детей до 3 лет на долю вирусных агентов приходится 80-90% заболеваний, на долю бактериальных – 10-20%; среди взрослых пациентов доля вирусных возбудителей снижается до 30%.
Shigella species и Esherichia coli – грамотрицательные палочковидные микроорганизмы из семейства энтеробактерий. К роду Shigella относятся патогенные бактерии S. dysenteriae, S. flexneri, S. boydii и S. sonnei, которые являются возбудителями шигеллеза (бактериальной дизентерии). Энтероинвазивные E. coli (EIEC) очень близки с шигеллами, синтезируют и выделяют шигеллоподобный токсин, способны проникать в клетки слизистой кишечника и разрушать энтероциты, что приводит к образованию язвенных дефектов в слизистой кишечника. За значительную часть случаев "бактериологически неподтвержденной дизентерии", особенно у детей, ответственен энтероинвазивный эшерихиоз.
Бактерии рода Salmonella относятся к семейству энтеробактерий. S. typhi и S. parathyphi являются возбудителями брюшного тифа и паратифа. Существует множество серовариантов Salmonella species, способных вызвать у человека инфекцию по типу гастроэнтероколита, а также стать причиной внутрибольничных инфекций. Сальмонеллез может протекать в форме острой кишечной инфекции, тяжелой генерализированной инфекции или бессимптомного носительства. Окончательный диагноз ставится только после выделения возбудителя или обнаружения его ДНК.
Кампилобактерии являются одними из наиболее сложных для культивирования (которое требуется в ходе анализа) микроорганизмов. Это объясняется их микроаэрофильностью и возможностью подавления их роста сопутствующей флорой. Род кампилобактерий объединяет как возбудителей ОКИ (термофильные виды), так и сапрофитные и условно-патогенные виды, о чем необходимо помнить при выявлении этих микроорганизмов в клиническом материале. Применение наборов на основе ПЦР для определения термофильной группы кампилобактерий позволяет не только избежать трудоемкой и высокозатратной бактериологической работы, но и четко ограничить детекцию тех видов кампилобактерий, которые имеют этиологическую связь с острой кишечной инфекцией (С. jejuni, C. coli, C. lari, C. upsaliensis).
В соответствии с данными зарубежной литературы, норовирус – наиболее частый возбудитель вспышек ОКИ небактериальной этиологии. Эта особенность связана с низкой инфицирующей дозой и высокой устойчивостью в окружающей среде. ПЦР является "золотым стандартом" в клинической диагностике норовирусных инфекций.
Несмотря на несколько меньшую в сравнении с рота- и норовирусами распространенность, астровирусы составляют значительный пласт кишечных инфекций, у трети пациентов протекающий с явлениями колита. Ротавирусы группы А являются наиболее частой причиной спорадических заболеваний ОКИ у детей, а ДНК-содержащий аденовирус F (серотипы 40 и 41) нередко вызывает вспышки гастроэнтеритов у детей младшего возраста.
Для выявления и дифференциальной диагностики кишечных инфекций используются культуральные и молекулярно-генетические методы исследования генетического материала возбудителя в кале и определение концентрации специфических иммуноглобулинов в крови. ПЦР обладает преимуществом перед культуральными методами благодаря быстрому получению результатов, высокой специфичности и чувствительности исследования. Данный анализ позволяет со 100-процентной точностью определить возбудителя кишечного заболевания, а быстрая диагностика острых кишечных инфекций помогает избежать лишних процедур и оперативных вмешательств, своевременно начать лечение и ограничить очаг распространения инфекции.
Для чего используется исследование?
- Для установления этиологического фактора острой кишечной инфекции;
- для дифференциальной диагностики причин острого гастроэнтероколита (воспаления ЖКТ).
Когда назначается исследование?
- При симптомах острого гастроэнтерита, вероятно, инфекционной этиологии (жидкий частый стул, рвота, лихорадка, боли в животе);
- при одновременном или последовательном развитии ОКИ у нескольких членов семьи, у детей в детском учреждении или пациентов в стационаре;
- при подозрении на развитие внутрибольничной кишечной инфекции (при обострении симптомов энтероколита у пациента, находящегося на лечении по поводу ОКИ).
Что означают результаты?
Референсные значения: отрицательно.
Причины положительного результата:
- присутствие ДНК или РНК возбудителя ОКИ; этиология в зависимости от выявленного вида возбудителя (Shigella spp., E. coli (EIEC), Salmonella spp., Campylobacter spp., Adenovirus F, Rotavirus A, Norovirus (2-й генотип), Astrovirus).
Причины отрицательного результата:
- отсутствие инфицирования Shigella spp., E. coli (EIEC), Salmonella spp., Campylobacter spp., Adenovirus F, Rotavirus A, Norovirus (2-й генотип), Astrovirus.
- Рекомендуется проводить исследование в первые 3 суток с начала заболевания, у госпитализированных пациентов – в первый день госпитализации.
- Важно помнить, что острый энтероколит может быть обусловлен и другими инфекциями (например, амебами, лямблиями, иерсиниями, клостридиями, протеями и др.) или неинфекционными причинами (токсинами, ядовитыми веществами, острой непроходимостью кишечника, тромбозом сосудов брыжейки, воспалительными заболеваниями кишечника, острым панкреатитом, аппендицитом, целиакией, острым гепатитом, мальабсорбцией, дивертикулитом).
Кто назначает исследование?
Инфекционист, гастроэнтеролог, терапевт, педиатр.
Литература
- Борисов Л. Б. Медицинская микробиология, вирусология, иммунология. М.: МИА, 2005. – 736 с.
- Gómez-Duarte O., Bai J., Newel E. Detection of E. coli, Salmonella spp., Shigella spp., Yersinia enterocolitica, Vibrio cholerae, and Campylobacter spp. enteropathogens by Three-reaction Multiplex PCR. Diagn Microbiol Infect Dis. 2009 January; 63(1): 1-9. PMCID: PMC2701628.
Кишечные инфекции – большая группа заболеваний, вызываемых патогенными или условно-патогенными бактериями, вирусами и простейшими. Ведущим симптомом таких патологий является диарея. Такие заболевания очень широко распространены в мире, включая развитые страны.
Все кишечные инфекции лечатся одинаково, поэтому выявление конкретного возбудителя важно не лечащему врачу, а ученым-эпидемиологам, изучающим пути распространения, способы передачи, проявления болезни в каждом новом случае, эффективность лечения и другие характеристики бактерии или вируса-возбудителя. Эта информация крайне важна, учитывая широкое распространение кишечных инфекций на планете и их высокую заразность, поскольку бактерии и вирусы изменяются. Кроме того, возбудителя устанавливают для понимания, какие профилактические мероприятия нужно провести, чтобы предотвратить заражение других людей.
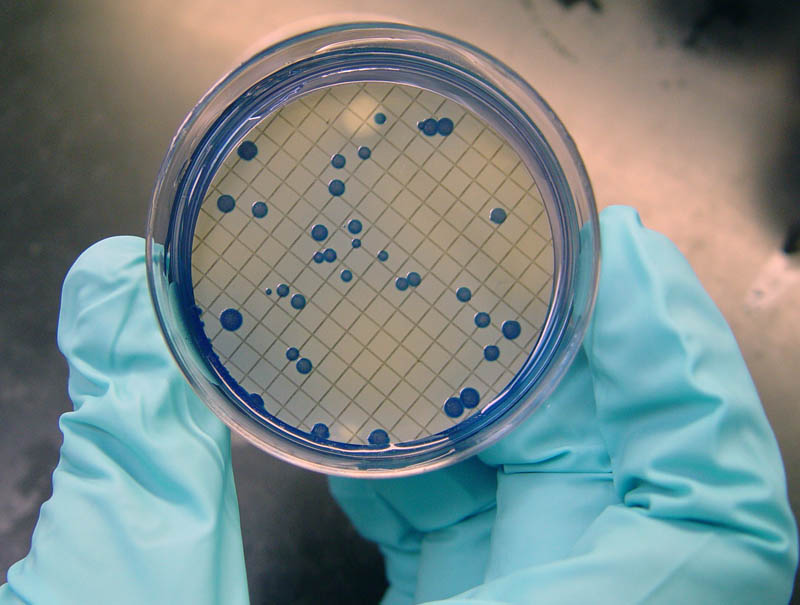
Одним из способов выявления инфекционного агента является бактериологический анализ кала. Он проводится при любых обращениях к врачу с жалобами на диарею. Это самый универсальный способ выявления причины кишечной инфекции, не требующий сложной аппаратуры.
Бактериологический анализ кала основан на изучении физиологических свойств возбудителя, выявленного в биоматериале. Он включает культивирование, выделение чистых культур, идентификацию и типирование возбудителей.
Классификация кишечных инфекций
Перечислим заболевания, которые относятся к группе кишечных инфекций.
1. Вызванные бактериями:
- Холера.
- Ботулизм.
- Брюшной тиф и паратиф (сальмонеллез).
- Шигиллез (дизентерия).
- Эшерихиозы (колиинфекция).
- Другие бактериальные инфекции – кампилобактериоз, иерсиниоз.
2. Вызванные простейшими:
- Амебиаз.
- Лямблиоз и др.
3. Вызванные вирусами:
- Ротавирусом.
- Аденовирусом.
- Норовирусом и др.
4. Вызванные условно-патогенными микроорганизмами:
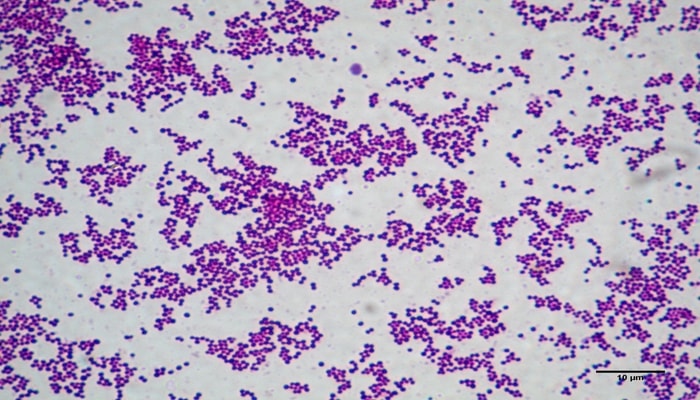
- Стафилококки (есть условно патогенные и патогенные, например, золотистый стафилококк).
- Клебсиеллы.
- Цитробактер (есть патогенные и условно-патогенные штаммы).
- Кишечная палочка.
- Протей и др.
5. Кишечные инфекции невыясненной этиологии.
6. Смешанные кишечные инфекции.
В 40% случаев возбудителем кишечной инфекции являются вирусы, в 20% - бактерии, в 40% возбудитель не удается установить.
По данным ВОЗ острые кишечные инфекции являются причиной 30 % смертельных случаев у детей до 5 лет.
Как правильно сдать анализ
Подготовка к анализу кала на бактериологическое исследование включает особые правила:
- Использование специального контейнера для сбора кала. Врач может выдать специальную пробирку с питательной средой и стерильную ректальную петлю.
- Подготовка судна – обработать его дезинфицирующим раствором, несколько раз сполоснуть проточной водой, обдать кипятком.
- Нельзя касаться ложечки, внутренних стенок контейнера и крышки.
- Нельзя сдавать анализ после приема антибиотиков.
- Проведение тщательного туалета анального отверстия.
Проба должна попасть в лабораторию в максимально короткие сроки. Допускается хранение материала 2 часа при комнатной температуре и 3 часа при температуре 2-8 °С. Для выявления некоторых возбудителей необходим посев на питательную среду сразу же после взятия биоматериала.
Этапы бактериологического анализа кала
1 день. Посев материала на дифференциально-диагностические среды.
Это специальные питательные среды, применяемые для выявления групп бактерий, отличающихся по способности утилизировать то или иное вещество. Например, часто для выращивания возбудителей кишечных инфекций в питательную среду добавляют лактозу. Некоторые бактерии (кишечная палочка) ее расщепляют. Тогда на поверхности среды вырастают окрашенные колонии микроорганизмов. Некоторые микроорганизмы лактозу не расщепляют (сальмонеллы). Тогда вырастают неокрашенные колонии.
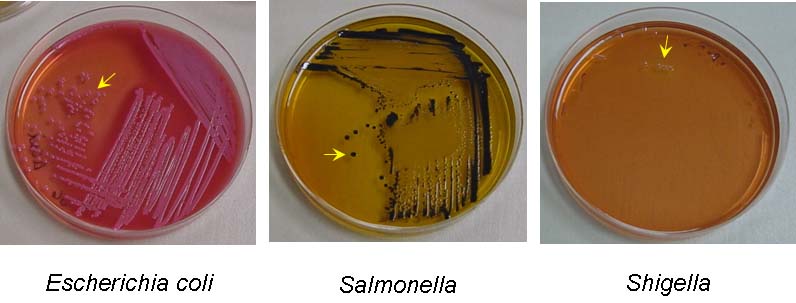
2 день. Выросшие колонии просматривают под микроскопом и описывают. Окрашивают по Граму и пересевают на другие специфические среды для накопления чистой культуры возбудителя.
3 день. С бактериями чистых культур проводят реакции агглютинации. Пересевают культуры на другие среды (Гисса) для выяснения ферментативной активности.
4 день. Оценивают результаты реакции агглютинации, рост на средах Гисса. На основании полученной информации дают окончательный ответ о виде возбудителя, присутствующего в кале.
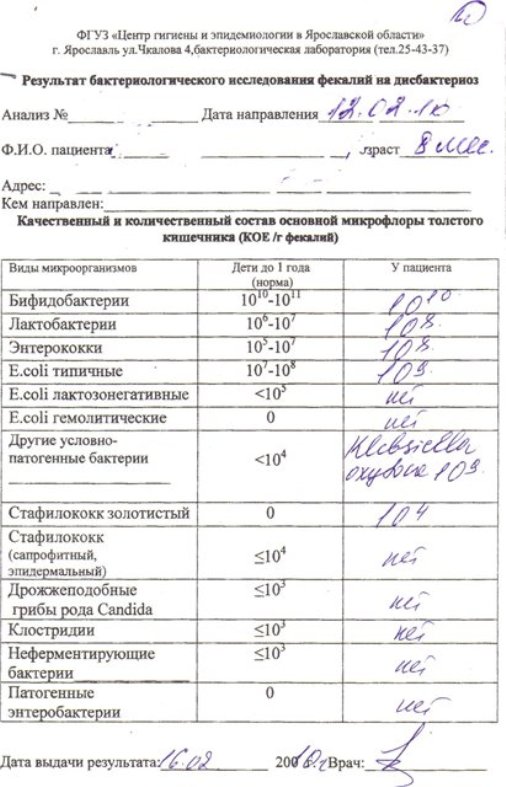
Расшифровка результата
Стандартный анализ кала на бактериологическое исследование включает выявление нескольких групп бактерий. Особое внимание уделяется кишечной палочке – отдельно сообщается о ее колониях с разными ферментативными свойствами. Большинство этих бактерий относится к группе условно-патогенных. То есть они обитают в кишечнике в качестве сапрофитов, но при определенных условиях становятся патогенными. Стандартное исследование включает и бактериологический анализ кала на дисбактериоз. Какие бактерии могут быть обнаружены в пробе? Об этом можно узнать из приведенного ниже (для примера) результата анализа.
Кишечная палочка, или Escherichia coli (E. coli)
Эти микроорганизмы заселяют толстый кишечник ребенка сразу после рождения. Здесь они преобладают среди факультативно-анаэробных бактерий. Кишечные палочки выполняют множество полезных функций в организме человека. Они способствуют выработке иммунитета к патогенным разновидностям бактерии, а также вырабатывают вещества, сдерживающие рост других микроорганизмов.
Бактерии вида E. coli бывают патогенные и условно-патогенные. Под микроскопом одни и другие выглядят одинаково. Их различают по строению антигенов, расположенных на поверхности бактерий. Для этого проводят серологическое исследование. Условно-патогенные кишечные палочки обитают в толстом кишечнике, но на фоне иммунодефицита могут вызвать воспаления и в других органах, например, в мочевыводящих. Патогенные представители E. coli называют диареегенными. Они относятся к транзиторным бактериям, то есть не локализуются постоянно в организме. При попадании в кишечный тракт они вызывают болезни под общим названием эшерихиозы, главным проявлением которых является диарея.
Расшифровка результатов определения количества кишечной палочки
Стандартный бактериологический анализ кала на кишечную группу инфекций включает такие подсчеты количества кишечных палочек:
- Общее количество E. coli.
- Палочек типичных.
- Со слабовыраженными ферментативными свойствами.
- Лактозонегативных.
- Гемолитических.
Общее количество эшерихии коли в 1 г кала у детей колеблется в пределах от 400 млн до 1 млрд, а у взрослых – 300-400 млн. Чрезмерное размножение бактерий в кишечнике приводит к дисбактериозу.
Типичные (классические) кишечные палочки полезны для организма. Их нормальное количество в кале должно быть в интервале 10 7 -10 8 . Снижение свидетельствует об интоксикации, приводящей к гибели полезной микрофлоры в толстом кишечнике, а также о заселении кишечника паразитами – глистами или простейшими. Другие причины – высокая чувствительность к аллергенам, поражение печени, почек, поджелудочной и щитовидной желез.
Высокое содержание в кале этих бактерий говорит об их чрезмерном размножении, что может привести к появлению гнойных воспалений разной локализации.
Разновидности кишечной палочки, не ферментирующие лактозу (лактозонегативные), являются патогенными. Они поражают клетки толстого кишечника, вызывая диарею. Количество данных бактерий в кале не должно превышать 10 5 . Если у больного с диареей их обнаружено больше, например 10 6 или 10 7 , значит, именно эти микроорганизмы явились причиной болезни. Неспособность использовать лактозу и некоторые другие свойства роднят их с шигеллами – возбудителями дизентерии.
Гемолитические кишечные палочки являются патогенными, локализуются, в основном, в слепой кишке. Вызывают геморрагический колит с симптомами общей интоксикации (тошнота, рвота). В норме в кале отсутствуют.
Условно-патогенные микроорганизмы, способные вызвать кишечную инфекцию
Все чаще бактерии, постоянно обитающие в толстом кишечнике человека, вызывают инфекции различной локализации – пищеварительного тракта, дыхательной или мочеполовой системы. К этому приводят ухудшающаяся экологическая обстановка, бесконтрольный прием антибиотиков и других препаратов, постоянное присутствие бактерий в окружении человека. Заболевают, как правило, новорожденные и дети первых 6 месяцев жизни.
Можно выполнить бактериологический анализ кала в "Инвитро". Это сеть лабораторий, филиалы которых есть во всех крупных городах. Пациентам нравится то, что результаты анализа можно получить онлайн, то есть не нужно за ними ехать в лабораторию.
Стафилококки
Существует три вида бактерий рода Staphylococcus, которые способны вызвать кишечную инфекцию:
- Золотистый стафилококк (Staphylococcus aureus).
- Эпидермальный.
- Сапрофитный.

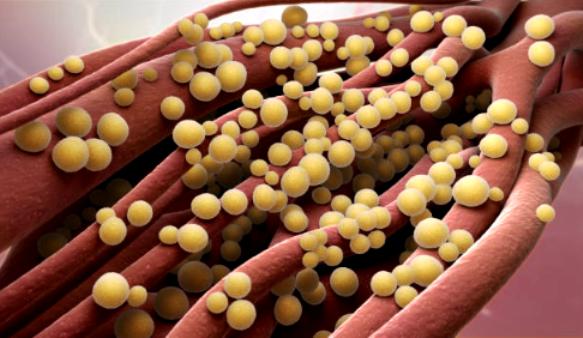
Золотистый стафилококк является самым патогенным из них, то есть при попадании в организм всегда вызывает развитие болезни. Поэтому в результатах анализа он обычно прописывается отельной строкой. В норме золотистого стафилококка в кале быть не должно. На картинке представлен вид чистой культуры золотистого стафилококка под микроскопом.
Эпидермальный вид также является патогенным, но он менее агрессивен, чем золотистый, то есть может присутствовать в организме, не повреждая его. Сапрофитный вид является обычным обитателем толстого кишечника. Суммарно количество эпидермального и сапрофитного стафилококков не должно превышать 10 4 .
Патогенные микроорганизмы, вызывающие кишечные инфекции
Бактериологический анализ кала на патогенную кишечную группу включает определение бактерий рода Salmonella и рода Shigella. Они являются патогенными, то есть в случае попадания в кишечник вызывают патологии – сальмонеллез, брюшной тиф, дизентерию. В норме отсутствуют в организме, поэтому не выделяются с калом.
Реже в анализах кала обнаруживают другие патогенные микроорганизмы, способные вызвать кишечные инфекции.
Вирусы при анализе кала
У детей первого года жизни возбудителями кишечных инфекций могут быть различные вирусы. При анализе кала микроскопическими и бактериологическими методами вирусы не выявляются.
Обнаружение в кале возбудителей любых кишечных инфекций требует госпитализации детей до 3-месячного возраста. Желательна госпитализация и детей до года.
При установлении дизентерии, сальмонеллеза, стафилококковой инфекции, пищевых токсикоинфекций, эшерихиоза у взрослых и детей старше года назначают лечение на дому. Если течение болезни тяжелое или существует высокая степень риска распространения болезни, больных госпитализируют в инфекционную больницу.
Диагностика и дифференциальная диагностика диарейных инфекций, гельминтозов и протозойных инвазий, оценка тяжести осложнений.
Всем пациентам инфекционного стационара производят бактериологическое исследование кала. Для диагностики нарушения микробиоценоза толстой кишки исследуют состав микрофлоры кала.
Копрологическое исследование у больных инфекционными болезнями производят:
- для выявления воспалительного процесса;
- для выявления кишечного кровотечения;
- для диагностики нарушений переваривания и всасывания пищи;
- для диагностики гельминтозов и протозойных инфекций.
Противопоказаний для исследования нет.
При отсутствии срочных показаний в течение 3–5 дней больной получает стандартизованную диету (Певзнера, Шмидта), при подозрении на микрокровотечение в течение 2–3 сут — диету, не содержащую мясо, рыбу, птицу, зеленые овощи, помидоры, а также препараты железа.
Специального оборудования не требуется.
Для сбора кала используют горшок или судно, тщательно вымытые без применения дезинфектантов.
Макроскопическое (визуальное) исследование включает оценку количества, консистенции, цвета, запаха, наличия видимых примесей. Осмотр кала проводят у всех больных кишечными инфекциями ежедневно до нормализации стула.
Микроскопическое исследование включает просмотр нативных и окрашенных мазков для выявления мышечных волокон, нейтрального жира и жирных кислот,крахмала, клетчатки, форменных элементов крови, простейших и яиц глистов.
Химическое исследование включает определение pH, скрытой крови, жёлчных пигментов.
Нормальные показатели копрограммы
• Количество — 150–200 г/сут.
• Консистенция и форма — оформленный, плотный.
• Цвет — коричневый (меняется в зависимости от характера пищи и приёма лекарств).
• Видимые примеси — отсутствуют.
- реакция — нейтральная или слабощелочная;
- скрытая кровь — реакция отрицательная (может быть положительной при употреблении мяса, рыбы, препаратов гемоглобина);
- стеркобилин — реакция положительная;
- растворимый белок — отсутствует.
- пищевые остатки: мышечные волокна, соединительная ткань, нейтральный жир и жирные кислоты, крахмал, клетчатка — отсутствуют или выявляются в небольшом количестве;
- лейкоциты — единичные в препарате;
- кристаллические образования — оксалаты кальция, кристаллы холестерина;
- бактерии и грибы — в большом количестве;
- простейшие — непатогенные формы (кишечные трихомонада, лямблия, амёба);
Увеличение объёма каловых масс характерно для всех инфекционных болезней, протекающих с синдромом энтерита (холера, сальмонеллёз, ПТИ, вирусные диареи и др.); объём каловых масс следует учитывать для определения потерь жидкости и оценки степени дегидратации.
Кал может быть оформленным, полуоформленным, кашицеобразным, жидким.
Примесь слизи и крови обнаруживают при остром шигеллёзе, энтероинвазивном эшерихиозе, колитическом варианте сальмонеллёза, клостридиозе, протеозе, иерсиниозе, амёбиазе, при злокачественных новообразованиях толстой кишки.
Чёрный (дёгтеобразный) стул появляется при кровотечении из язв тонкой кишки на 2–3-й нед брюшного тифа. Возможна положительная реакция на скрытую кровь при туберкулёзе кишечника, НЯК, гельминтозах, исходах вирусных гепатитов (цирроз печени). У больных брюшным тифом положительная реакция на скрытую кровь может предшествовать макроскопическому кровотечению.
Гной в испражнениях свидетельствует о выраженном воспалительном процессе в левом отделе толстой кишки, что характерно для хронического амёбиаза, болезни Крона, парапроктитов, дивертикулёза толстой кишки.
Увеличение количества мышечных волокон (креаторея) и появление непереваренных мышечных волокон происходит при ахилии, ускоренном пассаже пищевых масс по ЖКТ (шигеллёз, сальмонеллёз, эшерихиоз, кампилобактериоз и др.), при нарушении функции желудка и поджелудочной железы, гнилостной диспепсии.
Увеличение в кале содержания клетчатки (китаринорея) возникает при ахилии, энтеритах, энтероколитах. Появление крахмала наблюдают при энтеритах, бродильной диспепсии.
Стеаторея (увеличение содержания жира) возникает при нарушении внешнесекреторной функции поджелудочной железы при паротитной инфекции и острых кишечных инфекциях.
Увеличение жёлчных кислот и мыл — при уменьшении поступления жёлчи в кишечник при вирусных гепатитах, нарушении всасывания в тонкой кишке при туберкулёзе кишечника.
В кале могут быть обнаружены патогенные и непатогенные простейшие в двух формах: вегетативной (трофозоит) — активной, подвижной, неустойчивой к внешним воздействиям (охлаждение) — и в виде устойчивых к внешним воздействиям цист (ооцист). В оформленном кале можно выявить лишь ооцисты, для выявления вегетативных форм следует исследовать тёплый кал. Выявляют 20 видов простейших (8 патогенных и условно-патогенных и 12 комменсалов). Простейшие обитают на протяжении всего кишечника, их относят к одной из четырёх групп: амёб, жгутиковых, реснитчатых и кокцидий.
Приводим некоторые свойства испражнений при протозоозах.
При балантидиазе — жидкий стул (до 20–30 раз в сут) с гнилостным запахом, примесью слизи и крови. Обнаружение балантидий возможно в нативном кале (не позднее 20 мин после дефекации), лучший результат — при исследовании мазков и соскобов, взятых при ректороманоскопии. Возможно носительство у здоровых людей.
При лямблиозе — стул разжиженный с неприятным запахом, на поверхности примесь жира. Лямблии паразитируют преимущественно в двенадцатиперстной кишке и жёлчном пузыре (жидкая среда). Выделение паразита происходит с 5–7-го дня болезни: вегетативные формы можно обнаружить в жидких испражнениях или после приёма слабительных, а цисты (незрелые двуядерные, зрелые четырёхъядерные) — при повторных исследованиях оформленного кала.
При криптоспоридиозе — стул водянистый с отвратительным кислым запахом.
Ооцисты обнаруживают в первые 4–5 дней болезни в испражнениях, реже — в биоптате слизистой оболочки тонкой кишки при синдроме водянистой диареи.
Особенность течения криптоспоридиоза у ВИЧ-инфицированных пациентов — массивность поражения ЖКТ (от ротоглотки до прямой кишки).
При аспергиллёзе (генерализованная форма у больных СПИДом) — стул жидкий, пенистый, содержит большое количество аспергилл.
При кандидозах (гематогенно-диссеминированные формы с поражением ЖКТ) — выделение культуры грибка из испражнений при исследовании мазков и соскобов.
Приводим некоторые свойства испражнений при гельминтозах.
При энтеробиозе — у некоторых больных учащённый кашицеобразный стул с примесью слизи. На поверхности свежевыделенных фекалий можно видеть взрослые подвижные особи (самки остриц). Яйца остриц легче обнаружить при микроскопии с кожи перианальной области, чем в кале.
При кишечном шистосомозе — учащённый стул с примесью слизи и крови. Яйца шистосом в кале можно обнаружить только при интенсивной инвазии и в первой порции кала, личинки шистосом — используя специальные методы, основанные на их фототропизме. В биоптате слизистой оболочки, взятой при ректороманоскопии, обнаруживают яйца шистосом в каплях глицерина.
При клонорхозе — яйца клонорхисов можно обнаружить через 2–4 нед после стихания острых явлений. При описторхозе — яйца гельминта можно обнаружить через месяц после заражения. При дифиллоботриозе — в кале яйца гельминта и отрывки стробилы, что отличает этот гельминтоз от инвазии свиным и бычьим цепнями. При тениархозе — отхождение члеников цепня возможно вне акта дефекации. При тениозе видны зрелые членики свиного цепня, отделяющиеся группами по 5–6 (реже поодиночке). При гименолепидозе характерен длительно неустойчивый или жидкий стул; в кале яйца цепня (при исследовании нативного мазка с параллельным использованием метода флотации).
Охлаждение, высыхание пробы, хранение при комнатной температуре.
Анаэробная инфекция – инфекционный процесс, вызываемый спорообразующими или неспорообразующими микроорганизмами в условиях, благоприятных для их жизнедеятельности. Характерными клиническими признаками анаэробной инфекции служат преобладание симптомов эндогенной интоксикации над местными проявлениями, гнилостный характер экссудата, газообразующие процессы в ране, быстро прогрессирующий некроз тканей. Анаэробная инфекция распознается на основании клинической картины, подтвержденной результатами микробиологической диагностики, газожидкостной хроматографии, масс-спектрометрии, иммуноэлектрофореза, ПЦР, ИФА и др. Лечение анаэробной инфекции предполагает радикальную хирургическую обработку гнойного очага, интенсивную дезинтоксикационную и антибактериальную терапию.
Общие сведения
Анаэробная инфекция – патологический процесс, возбудителями которого выступают анаэробные бактерии, развивающиеся в условиях аноксии (отсутствия кислорода) или гипоксии (низкого напряжения кислорода). Анаэробная инфекция представляет собой тяжелую форму инфекционного процесса, сопровождающуюся поражением жизненно важных органов и высоким процентом летальности. В клинической практике с анаэробной инфекцией приходится сталкиваться специалистам в области хирургии, травматологии, педиатрии, нейрохиругии, отоларингологии, стоматологии, пульмонологии, гинекологии и других медицинских направлений. Анаэробная инфекция может возникнуть у пациентов любого возраста. Доля заболеваний, вызываемых анаэробной инфекцией, точно не известна; из гнойных очагов в мягких тканях, костях или суставах анаэробы высеваются примерно в 30% случаев; анаэробная бактериемия подтверждается в 2-5% случаев.

Причины анаэробной инфекции
Анаэробы входят в состав нормальной микрофлоры кожи, слизистых оболочек, желудочно-кишечного тракта, органов мочеполовой системы и по своим вирулентным свойствам являются условно-патогенными. При определенных условиях они становятся возбудителями эндогенной анаэробной инфекции. Экзогенные анаэробы присутствуют в почве и разлагающихся органических массах и вызывают патологический процесс при попадании в рану извне. Анаэробные микроорганизмы делятся на облигатные и факультативные: развитие и размножение облигатных анаэробов осуществляется в бескислородной среде; факультативные анаэробы способны выживать как в отсутствии, так и в присутствии кислорода. К факультативным анаэробными бактериями принадлежат кишечная палочка, шигеллы, иерсинии, стрептококки, стафилококки и др.
Облигатные возбудители анаэробной инфекции делятся на две группы: спорообразующие (клостридии) и неспорообразующие (неклостридиальные) анаэробы (фузобактерии, бактероиды, вейллонеллы, пропионибактерии, пептострептококки и др.). Спорообразующие анаэробы являются возбудителями клостридиозов экзогенного происхождения (столбняка, газовой гангрены, ботулизма, пищевых токсикоинфекций и др.). Неклостридиальные анаэробы в большинстве случаев вызывают гнойно-воспалительные процессы эндогенной природы (абсцессы внутренних органов, перитонит, пневмонию, флегмоны челюстно-лицевой области, отит, сепсис и др.).
Основными факторами патогенности анаэробных микроорганизмов служат их количество в патологическом очаге, биологические свойства возбудителей, наличие бактерий-ассоциантов. В патогенезе анаэробной инфекции ведущая роль принадлежит продуцируемым микроорганизмами ферментам, эндо- и экзотоксинам, неспецифическим факторам метаболизма. Так, ферменты (гепариназа, гиалуронидаза, коллагеназа, дезоксирибонуклеаза) способны усиливать вирулентность анаэробов, деструкцию мышечной и соединительной тканей. Эндо- и экзотоксины вызывают повреждение эндотелия сосудов, внутрисосудистый гемолиз и тромбоз. Кроме этого, некоторые клостридиальные токисины обладают нефротропным, нейротропным, кардиотропным действием. Также токсическое влияние на организм оказывают и неспецифические факторы метаболизма анаэробов - индол, жирные кислоты, сероводород, аммиак.
Условиями, благоприятствующими развитию анаэробной инфекции, являются повреждение анатомических барьеров с проникновением анаэробов в ткани и кровеносное русло, а также снижение окислительно-восстановительного потенциала тканей (ишемия, кровотечение, некроз). Попадание анаэробов в ткани может происходить при оперативных вмешательствах, инвазивных манипуляциях (пункциях, биопсии, экстракции зуба и др.), перфорации внутренних органов, открытых травмах, ранениях, ожогах, укусах животных, синдроме длительного сдавления, криминальных абортах и т. д. Факторами, способствующими возникновению анаэробной инфекции, выступают массивное загрязнение ран землей, наличие инородных тел в ране, гиповолемический и травматический шок, сопутствующие заболевания (коллагенозы, сахарный диабет, опухоли), иммунодефицит. Кроме этого, большое значение имеет нерациональная антибиотикотерапия, направленная на подавление сопутствующей аэробной микрофлоры.
В зависимости от локализации различают анаэробную инфекцию:
- центральной нервной системы (абсцесс мозга, менингит, субдуральная эмпиема и др.)
- головы и шеи (пародонтальный абсцесс, ангина Людвига, средний отит, синусит, флегмона шеи и т. д.)
- дыхательных путей и плевры (аспирационная пневмония, абсцесс легкого, эмпиема плевры и пр.)
- женской половой системы (сальпингит, аднексит, эндометрит, пельвиоперитонит)
- брюшной полости (абсцесс брюшной полости, перитонит)
- кожи и мягких тканей (клостридиальный целлюлит, газовая гангрена, некротизирующий фасциит, абсцессы и др.)
- костей и суставов (остеомиелит, гнойный артрит)
- бактериемию.
Симптомы анаэробной инфекции
Независимо от вида возбудителя и локализации очага анаэробной инфекции, различным клиническим формам свойственны некоторые общие черты. В большинстве случаев анаэробная инфекция имеет острое начало и характеризуется сочетанием местных и общих симптомов. Инкубационный период может составлять от нескольких часов до нескольких суток (в среднем около 3-х дней).
Типичным признаком анаэробной инфекции служит преобладание симптомов общей интоксикации над местными воспалительными явлениями. Резкое ухудшение общего состояния больного обычно наступает еще до возникновения локальных симптомов. Проявлением тяжелого эндотоксикоза служит высокая лихорадка с ознобами, выраженная слабость, тошнота, головная боль, заторможенность. Характерны артериальная гипотония, тахипноэ, тахикардия, гемолитическая анемия, иктеричность кожи и склер, акроцианоз.
При раневой анаэробной инфекции ранним местным симптомом выступает сильная, нарастающая боль распирающего характера, эмфизема и крепитация мягких тканей, обусловленные газообразующими процессами в ране. К числу постоянных признаков относится зловонный ихорозный запах экссудата, связанный с выделением азота, водорода и метана при анаэробном окислении белкового субстрата. Экссудат имеет жидкую консистенцию, серозно-геморрагический, гнойно-геморрагический или гнойный характер, неоднородную окраску с вкраплениями жира и наличием пузырьков газа. На гнилостный характер воспаления также указывает внешний вид раны, содержащей ткани серо-зеленого или серо-коричневого цвета, иногда струпы черного цвета.
Течение анаэробной инфекции может быть молниеносным (в течение 1 суток с момента операции или травмы), острым (в течение 3-4 суток), подострым (более 4 суток). Анаэробная инфекция часто сопровождается развитием полиорганной недостаточности (почечной, печеночной, сердечно-легочной), инфекционно-токсического шока, тяжелого сепсиса, являющихся причиной летального исхода.
Диагностика
Для своевременной диагностики анаэробной инфекции большое значение имеет правильная оценка клинических симптомов, позволяющая своевременно оказать необходимую медицинскую помощь. В зависимости от локализации инфекционного очага диагностикой и лечением анаэробной инфекции могут заниматься клиницисты различных специальностей – общие хирурги, травматологи, нейрохирурги, гинекологи, отоларингологи, челюстно-лицевые и торакальные хирурги.
Методы экспресс-диагностики анаэробной инфекции включают бактериоскопию раневого отделяемого с окраской мазка по Грамму и газожидкостную хроматографию. В верификации возбудителя ведущая роль принадлежит бактериологическому посеву отделяемого раны или содержимого абсцесса, анализу плевральной жидкости, посеву крови на аэробные и анаэробные бактерии, иммуноферментному анализу, ПЦР. В биохимических показателях крови при анаэробной инфекции обнаруживается снижение концентрации белков, увеличение уровня креатинина, мочевины, билирубина, активности трансаминаз и щелочной фосфатазы. Наряду с клиническими и лабораторными исследования, выполняется рентгенография, при которой обнаруживается скопление газа в пораженных тканях или полостях.
Анаэробную инфекцию необходимо дифференцировать от рожистого воспаления мягких тканей, полиморфной экссудативной эритемы, тромбоза глубоких вен, пневмоторакса, пневмоперитонеума, перфорации полых органов брюшной полости.
Лечение анаэробной инфекции
Комплексный подход к лечению анаэробной инфекции предполагает проведение радикальной хирургической обработки гнойного очага, интенсивной дезинтоксикационной и антибактериальной терапии. Хирургический этап должен быть выполнен как можно раньше – от этого зависит жизнь больного. Как правило, он заключается в широком рассечении очага поражения с удалением некротизированных тканей, декомпрессии окружающих тканей, открытом дренировании с промыванием полостей и ран растворами антисептиков. Особенности течения анаэробной инфекции нередко требуют проведения повторных некрэктомий, раскрытия гнойных карманов, обработки ран ультразвуком и лазером, озонотерапии и т. д. При обширной деструкции тканей может быть показана ампутация или экзартикуляция конечности.
Важнейшими составляющими лечения анаэробной инфекции являются интенсивная инфузионная терапия и антибиотикотерапия препаратами широкого спектра действия, высокотропными к анаэробам. В рамках комплексного лечения анаэробной инфекции находят свое применение гипербарическая оксигенация, УФОК, экстракорпоральная гемокоррекция (гемосорбция, плазмаферез и др.). При необходимости пациенту вводится антитоксическая противогангренозная сыворотка.
Прогноз и профилактика
Исход анаэробной инфекции во многом зависит от клинической формы патологического процесса, преморбидного фона, своевременности установления диагноза и начала лечения. Уровень летальности при некоторых формах анаэробной инфекции превышает 20%. Профилактика анаэробной инфекции заключается в своевременной и адекватной ПХО ран, удалении инородных тел мягких тканей, соблюдении требований асептики и антисептики при проведении операций. При обширных раневых повреждениях и высоком риске развития анаэробной инфекции необходимо проведение специфической иммунизации и противомикробной профилактики.
Читайте также:


