Выход вирусов из клетки характеристика
Лекция 6
РЕПЛИКАЦИЯ
Репликация ДНК осуществляется ДНК-полимеразами. Для начала репликации необходим предварительный синтез короткого участка РНК на матрице ДНК, который называется затравкой. С затравки начинается синтез нити ДНК, после чего РНК быстро удаляется с растущего участка.
Репликация вирусных ДНК. Репликация генома ДНК-содержащих вирусов в основном катализируется клеточными фрагментами и механизм ее сходен с механизмом репликации клеточной ДНК.
Каждая вновь синтезированная молекула ДНК состоит из одной родительской и одной вновь синтезированной нити. Такой механизм репликации называется полуконсервативным.
У вирусов, содержащих кольцевые двунитчатые ДНК (паповавирусы), разрезается одна из нитей ДНК, что ведёт к раскручиванию и снятию супервитков на определенном участке молекулы.
При репликации однонитчатых ДНК (семейство парвовирусов) происходит образование двунитчатых форм, которые представляют собой промежуточные репликативные формы.
Репликация вирусных РНК. В клетке нет ферментов, способных осуществить репликацию РНК. Поэтому ферменты, участвующие в репликации, всегда вирусспецифические. Репликацию осуществляет тот же фермент, что и транскрипцию; репликаза является либо модифицированной транскриптазой, либо при репликации соответствующим образом модифицируется матрица.
Репликативные комплексы ассоциированы с клеточными структурами либо с предсуществующими, либо вирусиндуцируемыми. Например, репликативные комплексы пикорнавирусов ассоциированы с мембранами эндоплазматической сети, вирусов оспы — с цитоплазматическим матриксом, репликативные комплексы аденовирусов и вирусов герпеса в ядрах находятся в ассоциации со вновь сформированными волокнистыми структурами и связаны с ядерными мембранами. В зараженных клетках может происходить усиленная пролиферация клеточных структур, с которыми связаны репликативные комплексы, или их формирование из предсуществующего материала. Например, в клетках, зараженных пикорнавирусами, происходит пролиферация гладких мембран. В клетках, зараженных реовирусами, наблюдается скопление микротрубочек; в клетках, зараженных вирусами оспы, происходит формирование цитоплазматического матрикса.
В репликативных комплексах одновременно с синтезом геномных молекул осуществляется транскрипция и происходит сборка нуклеокапсидов и сердцевин, а при некоторых инфекциях — и вирусных частиц. О сложной структуре репликативных комплексов говорит, например, такой состав репликативного комплекса аденовирусов: реплицирующиеся ДНК, однонитчатые ДНК, однонитчатые РНК, ферменты репликации и транскрипции, структурные и неструктурные вирусные белки и ряд клеточных белков.
СБОРКА ВИРУСНЫХ ЧАСТИЦ
Синтез компонентов вирусных частиц в клетке разобщен и может протекать в разных структурах ядра и цитоплазмы. Вирусы, репликация которых проходит в ядрах, условно называют ядерными. В основном это ДНК-содержащие вирусы: аденовирусы, паповавирусы, парвовирусы, вирусы герпеса. Вирусы, реплицирующиеся в цитоплазме, называют цитоплазматическими. К ним относятся из ДНК-содержащих вирус оспы и большинство РНК-содержащих вирусов, за исключением ортомиксовирусов и ретровирусов. Однако это разделение весьма относительно, потому что в репродукции тех и других вирусов есть стадии, протекающие соответственно в цитоплазме и ядре.
Внутри ядра и цитоплазмы синтез вирусспецифических молекул также может быть разобщен. Так, например, синтез одних белков осуществляется на свободных полисомах, а других — на полисомах, связанных с мембранами. Вирусные нуклеиновые кислоты синтезируются в ассоциации с клеточными структурами вдали от полисом, которые синтезируют вирусные белки. При таком дисъюнктивном способе репродукции образование вирусной частицы возможно лишь в том случае, если вирусные нуклеиновые кислоты и белки обладают способностью при достаточной концентрации узнавать друг друга в многообразии клеточных белков и нуклеиновых кислот и самопроизвольно соединяться друг с другом, т. е. способны к самосборке.
В основе самосборки лежит специфическое белок-нуклеиновое и белок-белковое узнавание, которое может происходить в результате гидрофобных, солевых и водородных связей, а также стерического соответствия. Белок-нуклеиновое узнавание ограничено небольшим участком молекулы нуклеиновой кислоты и определяется уникальными последовательностями нуклеотидов в некодирующей части вирусного генома. С этого узнавания участка генома вирусными капсидными белками начинается процесс сборки вирусной частицы. Присоединение остальных белковых молекул осуществляется за счет специфичеческих белокбелковых взаимодействий или неспецифических белокнуклеиновых взаимодействий.
В связи с разнообразием структуры вирусов животных разнообразны и способы формирования вирионов, однако можно сформулировать следующие общие принципы сборки.
1. У просто устроенных вирусов формируются провирионы, которые затем в результате модификаций белков превращаются в вирионы. У сложно устроенных вирусов сборка осуществляется многоступенчато. Сначала формируются нуклеокапсиды или сердцевины, с которыми взаимодействуют белки наружных оболочек.
2. Сборка сложно устроенных вирусов (за исключением сборки вирусов оспы и реовирусов) осуществляется на клеточных мембранах. Сборка ядерных вирусов происходит с участием ядерных мембран, сборка цитоплазматических вирусов — с участием мембран эндоплазматической сети или плазматической мембраны, куда независимо друг от друга прибывают все компоненты вирусной частицы.
5. Сложно устроенные вирусы для построения своих частиц используют ряд элементов клетки-хозяина, например липиды, некоторые ферменты, у ДНК-геномного SV40 — гистоны, у оболочечных РНК-геномных вирусов — актин, а в составе ареновирусов обнаружены даже рибосомы. Клеточные молекулы несут определенные функции в вирусной частице, однако включение их в вирион может явиться и следствием случайной контаминации, как, например, включение ряда ферментов клеточных оболочек или клеточных нуклеиновых кислот.
Сборка РНК-содержащих вирусов. Сборка просто устроенных РНК-содержащих вирусов заключается в ассоциации вирусного генома с вирусными капсидными белками с образованием нуклеокапсида.
Все вирусные компоненты — нуклеокапсиды и суперкапсидные белки прибывают к месту сборки независимо друг от друга. Первыми к месту сборки прибывают суперкапсидные белки. Обычно этими белками являются гликопротеиды, которые синтезируются в полисомах, связанных с мембранами, и через шероховатые, а затем гладкие мембраны в результате слияния с ними везикул комплекса Гольджи транспортируются на наружную поверхность плазматических мембран или остаются в составе везикул.
Включение М-белка в клеточные мембраны является сигналом для сборки вирусной частицы: вслед за включением немедленно следует связывание нуклеокапсидов с мембранами и почкование вирусной частицы. Тем самым М-белок обладает функцией лимитирующего сборку фактора.
В результате связывания ДНК с капсидами появляется новый класс промежуточных форм, которые называются неполными формами. Помимо неполных форм с разным содержанием ДНК, существует другая промежуточная форма в морфогенезе — незрелые вирионы, отличающиеся от зрелых тем, что содержат ненарезанные предшественники полипептидов. Таким образом, морфогенез вирусов тесно связан с модификацией (процессингом) белков.
Сборка ядерных вирусов начинается в ядре, обычно — с ассоциации с ядерной мембраной. Формирующиеся в ядре промежуточные формы вируса герпеса почкуются в перинуклеарное пространство через внутреннюю ядерную мембрану, и вирус приобретает таким путем оболочку, которая является дериватом ядерной мембраны. Дальнейшая достройка и созревание вирионов происходит в мембранах эндоплазматической сети и в аппарате Гольджи, откуда вирус в составе цитоплазматических везикул транспортируется на клеточную поверхность.
ВЫХОД ВИРУСНЫХ ЧАСТИЦ ИЗ КЛЕТКИ
Выход из клетки путем взрыва связан с деструкцией клетки, нарушением ее целостности, в результате чего находящиеся внутри клетки зрелые вирусные частицы оказываются в окружающей среде. Такой способ выхода из клетки присущ вирусам, не содержащим липопротеидной оболочки (пикорна-, рео-, парво-, папова-, аденовирусы). Однако некоторые из этих вирусов могут транспортироваться на клеточную поверхность до гибели клетки.
Выход из клеток путем почкования присущ вирусам, содержащим липопротеидную мембрану, которая является дериватом клеточных мембран. При этом способе клетка может длительное время сохранять жизнеспособность и продуцировать вирусное потомство, пока не произойдет полное истощение ее ресурсов.

Вирусы — это микроскопические патогены, заражающие клетки живых организмов для самовоспроизводства. Они состоят из одного вида нуклеиновой кислоты (или ДНК или РНК, но не обе вместе), которая защищена оболочкой, содержащей белки, липиды, углеводы или их комбинацию. Размер типичного вируса варьируется от 15 до 350 нм, поэтому его можно увидеть только с помощью электронного микроскопа.
В 1892 году русский ученый Д.И. Ивановский впервые доказал существование ранее неизвестного типа возбудителя болезней, это был вирус мозаичной болезни табака. А в 1898 году Фридрих Лоффлер и Пол Фрош нашли доказательства того, что причиной ящура у домашнего скота была инфекционная частица, которая меньше, чем любая бактерия. Это были первые шаги к изучению природы вирусов, генетических образований, которые лежат где-то в серой зоне между живыми и неживыми состояниями материи. На текущий момент описано около 6 тыс. вирусов, но их существует несколько миллионов.
Строение вирусов
Вне клеток-хозяев вирусы существуют в виде белковой оболочки (капсида), иногда заключенного в белково-липидную мембрану. Капсид обволакивает собой либо ДНК, либо РНК, которая кодирует элементы вируса. Находясь в такой форме вне клетки, вирус метаболически инертен и называется вирионом.
Простая структура, отсутствие органелл и собственного метаболизма позволяет некоторым вирусам кристаллизоваться, т.е. они могут вести себя подобно химическим веществам. С появлением электронных микроскопов было установлено, что их кристаллы состоят из тесно прижатых друг к другу нескольких сотен миллиардов частиц. В одном кристалле вируса полиомиелита столько частиц, что ими можно заразить не по одному разу всех жителей Земли.
Формы вирусов
Вирусы встречаются в трех основных формах. Они бывают:
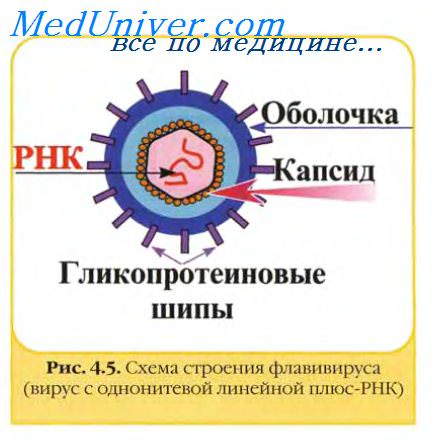
- Сферическими (кубическими или полигидральными). Вирусы герпеса, типулы, полиомы и т.д.
- Спиральными (цилиндрическими или стержнеобразными). Вирусы табачной мозаики, гриппа, эпидемического паротита и др.
- Сложными. Например, бактериофаги.
Проникновение вирусов в клетку-хозяина
Капсид в основном защищает нуклеиновую кислоту от действия клеточного нуклеазного фермента. Но некоторые белки капсида способствуют связыванию вируса с поверхностью клеток-хозяев, и работают, как ключики, вставляемые в нужные замочки. Другие поверхностные белки действуют как ферменты, они растворяют поверхностный слой клетки-хозяина и таким образом помогают проникновению нуклеиновой кислоты вируса в клетку-хозяина.
Жизненный цикл вирусов сильно отличается у разных видов, но существует шесть основных этапов жизненного цикла вирусов:
Присоединение к клетке-хозяину представляет собой специфическое связывание между вирусными капсидными белками и рецепторами на клеточной поверхности. Эта специфика определяет хозяина вируса.
Проникновение следует за прикреплением: вирионы проникают в клетку-хозяина через рецептор-опосредованный эндоцитоз или слияние мембран. Это часто называют вирусной записью.
Проникновение вирусов в клетку достигается за счет:
Размножение вирусов
После того, как вирусный геном освобождается от капсида, начинается его транскрипция или трансляция. Именно эта стадия вирусной репликации сильно различается между ДНК- и РНК-вирусами и вирусами с противоположной полярностью нуклеиновой кислоты. Этот процесс завершается синтезом новых вирусных белков и генома (точных копий внедрённых).
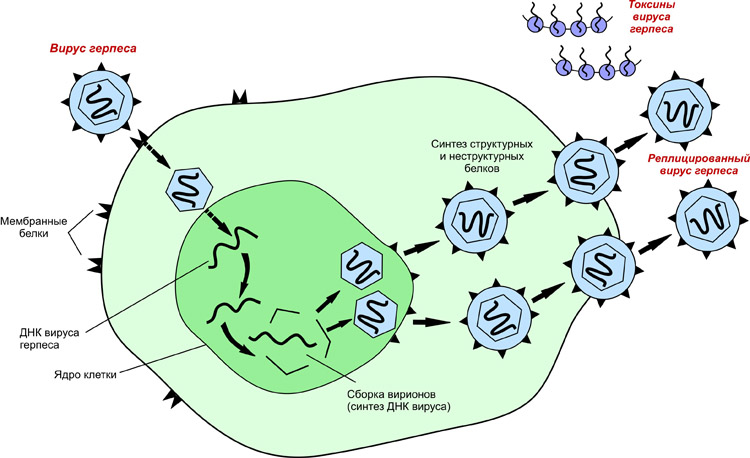
Механизм репликации зависит от вирусного генома.
- ДНК-вирусы обычно используют белки и ферменты клетки-хозяина для получения дополнительной ДНК, она транскрибируется в РНК-мессенджер (мРНК), которая затем используется для управления синтезом белка.
- РНК-вирусы обычно используют ядро РНК в качестве матрицы для синтеза вирусной геномной РНК и мРНК. Вирусная мРНК направляет клетку-хозяина на синтез вирусных ферментов и капсидных белков и сборку новых вирионов. Конечно, есть исключения из этого шаблона. Если клетка-хозяин не обеспечивает ферменты, необходимые для репликации вируса, вирусные гены предоставляют информацию для прямого синтеза отсутствующих белков.
Чтобы преобразовать РНК в ДНК, вирусы должны содержать гены, которые кодируют вирус-специфический фермент обратной транскриптазы. Она транскрибирует матрицу РНК в ДНК. Обратная транскрипция никогда не происходит в неинфицированных клетках. Необходимый фермент, обратная транскриптаза, происходит только от экспрессии вирусных генов в инфицированных клетках.
Вироиды
Вироиды заражают только растения. Одни вызывают экономически важные заболевания сельскохозяйственных культур, в то время как другие являются доброкачественными. Двумя примерами экономически важных вироидов являются кокосный cadang-cadang (он вызывает массовую гибель кокосовых пальм) и вироид рубцовой кожицы яблок, который безнадежно портит товарный вид яблок.
30 известных вироидов были классифицированы в две семьи.
- Члены семейства Pospiviroidae, названные по имени вироида клубневого веретена картофеля, имеют палочковидную вторичную структуру с небольшими одноцепочечными областями, имеет центральную консервативную область, и реплицируются в ядре клетки.
- Avsunviroidae, названный в честь вироида авокадо, имеет как палочковидную, так и разветвленную области, но не имеет центральной консервативной области и реплицируется в хлоропластах растительной клетки.
В отличие от вирусов, которые являются паразитами механизма трансляции хозяина, вироиды являются паразитами клеточных транскрипционных белков.
Бактериофаги

Существуют тысячи разновидностей фагов, каждый из которых может заразить только один тип или несколько близких типов бактерий или архей. Фаги классифицируются по ряду семейств вирусов; например:
Как и все вирусы, фаги являются простыми организмами, которые состоят из ядра генетического материала (нуклеиновой кислоты), окруженного капсидом белка. Нуклеиновая кислота может представлять собой либо ДНК, либо РНК, и может быть двухцепочечной или одноцепочечной.
Существует три основных структурных формы фага:
- Икосаэдрическая (20-сторонняя) головка с хвостом
- Икосаэдрическая головка без хвоста
- Нитевидная форма
Во время заражения фаг прикрепляется к бактерии и вставляет в нее свой генетический материал. После этого фаг обычно следует одному из двух жизненных циклов: литическому (вирулентному) или лизогенному (умеренному).
Литические, или вирулентные, фаги захватывают механизм клетки, чтобы скопировать компоненты фага. Затем они разрушают или лизируют клетку, высвобождая новые частицы фага.
Лизогенные, или умеренные, фаги включают свою нуклеиновую кислоту в хромосому клетки-хозяина и реплицируются с ней как единое целое, не разрушая клетку. При определенных условиях лизогенные фаги могут индуцироваться в соответствии с литическим циклом.
Существуют и другие жизненные циклы, в т.ч. псевдолизогенез и хроническая инфекция. При псевдолизогении бактериофаг проникает в клетку, но не использует механизм репликации клеток и не интегрируется в геном хозяина, просто как бы прячется внутри бактерии, не нанося ей никакого вреда. Псевдолизогенез возникает, когда клетка-хозяин сталкивается с неблагоприятными условиями роста и, по-видимому, играет важную роль в выживании фага, обеспечивая сохранение генома фага до тех пор, пока условия роста хозяина снова не станут благоприятными.
При хронической инфекции новые фаговые частицы образуются непрерывно и длительно, но без явного уничтожения клеток.
Вскоре после открытия фаги начали использовать для лечения бактериальных заболеваний человека, таких как бубонная чума и холера. Но фаговая терапия тогда не была успешной, и после открытия антибиотиков в 1940-х годах она была практически заброшена. Однако с появлением устойчивых к антибиотикам бактерий терапевтическому потенциалу фагов уделяется все больше внимания.
Наше время с антибиотиками заканчивается. В 2016 году женщина в штате Невада умерла от бактериальной инфекции, вызванной Klebsiella pneumoniae, которая была устойчивой ко всем известным антибиотикам. Бактерии, устойчивые к колистину, антибиотику последней инстанции, были обнаружены на свинофермах в Китае. В настоящее время бактерии приспосабливаются к антибиотикам быстрее, чем когда-либо.
Покажите ножницы которыми вирусы разрезают молекулу РНК что бы встроиться для мутации.Может что нибудь придумаете другое.К примеру деление цепочка аминокислот получив энергию из вне как одноименные заряды распадается на две. К каждой соединятся только те какие были ранее (другие проскочат мимо),казалось бы копии,но внутренняя энергия разная(уменьшается увеличивается) поэтому распад и создание. Вся химия углерода на этом построена 1000 орган соединений создает у других хим элементов этого свойства нет. Иммунная система делает накладку(интерференция)с помощью энергии интерферонов пытаясь разрушить цепочку РНК вируса.Надо помочь организму но не вакциной(вирус быстро мутирует)
Синтез компонентов вирусных частиц в клетке разобщен и может протекать в разных структурах ядра и цитоплазмы. Вирусы, репликация которых проходит в ядрах, условно называют ядерными. В основном это ДНК-содержащие вирусы: адено-, папова-, парвовирусы, вирусы герпеса. Вирусы, реплицирующиеся в цитоплазме, называют цитоплазмэтическими. К ним относятся из ДНК-содержащих вирус оспы и большинство РНК-содержащих вирусов, за исключением ортомиксо- и ретровирусов. Однако это разделение весьма относительно, потому что в репродукции тех и других вирусов есть стадии, протекающие соответственно в цитоплазме и ядре.
Внутри ядра и цитоплазмы синтез вирусспецифических молекул также может быть разобщен. Так, например, синтез одних белков осуществляется на свободных полисомах, а других--на полисомах, связанных с мембранами. Вирусные нуклеиновые кислоты синтезируются в ассоциации с клеточными структурами вдали от полисом, которые синтезируют вирусные белки. При таком дизъюнктивном способе репродукции образование вирусной частицы возможно лишь в том случае, если вирусные нуклеиновые кислоты и белки обладают способностью при достаточной концентрации узнавать друг друга в многообразии клеточных белков и нуклеиновых кислот и самопроизвольно соединяться друг с другом, т. е. способны к самосборке.
В основе самосборки лежит специфическое белок-нуклеиновое и белок-белковое узнавание, которое может происходить в результате гидрофобных ионных и водородных связей, а также стерического соответствия. Белок-нуклеиновое узнавание ограничено небольшим участком молекулы нуклеиновой кислоты и определяется уникальными последовательностями нуклеотидов в некодирующей части вирусного генома. С этого узнавания участка генома вирусными капсидными белками начинается процесс сборки вирусной частицы. Присоединение остальных белковых молекул осуществляется за счет специфических белок-белковых взаимодействий или неспецифических белок-нуклеиновых взаимодействий.
Объединение белка с вирусными нуклеиновыми кислотами в клетке происходит спонтанно как чисто физико-химическая реакция агрегации, требующая участия дополнительных факторов (рН, ионной силы, ионов металлов, осмоса и т.п.). После того как концентрация вирусных РНК и белка достигает критического уровня; у сложно устроенных вирусов принципы самосборки обеспечивает от начала до конца морфогенез вирионов.
Для того чтобы представить этап созревания дочерних вирусных частиц у парамиксовирусов, необходимо выяснить, каким образом молекула 50S РНК, около 10 тыс. молекул белков, липидов и сахара собираются в зараженной клетке и образуют морфологически и биологически полноценную частицу. Созревание можно разделить на три этапа: 1) образование внутриклеточных нуклеокапсидов; 2) организация вирусной мембраны; 3) выход зрелой вирусной частицы из клетки с помощью так называемого почкования.
Организация вирусной мембраны. Структурной основой вирусных и цитоплазматических мембран является двойной липидный слой. Последний у вирусной мембраны почти без изменений повторяет липидный слой плазматической мембраны клетки-хозяина. Мембраны вирусных частиц содержат наружный (гликопротеиды HN и F) и внутренний белковый слой (белок М).
В построении вирусной мембраны участвуют предсуществующие липиды клеточных мембран. Гликопротеиды вируса включаются в мембраны зараженных клеток, поэтому вскоре после их заражения в наружных мембранах клеток выявляется поверхностный вирусный антиген (гликопротеид HN, являющийся одновременно гемагглютинином, нейраминидазой и рецепторным белком).
В плазматических мембранах клеток, зараженных вирусом гриппа, обнаружены все белки липопротеидной оболочки вируса: НА (либо НА1 + НА2); NA (нейраминидаза) и М (внутренний белок вирусной мембраны). Гликопротеиды НА (гемагглютинина) и NA синтезируются в так называемых шероховатых мембранах, т.е. в мембранах, с которыми связаны синтезирующие белки рибосомы. После синтеза полипептиды транспортируются по гладким плазматическим мембранам в комплекс Гольджи, где происходит тримминг углеводных цепей. Из комплекса Гольджи гликопротеиды поступают в наружные мембраны. Происходит сборка структур, состоящих из 6 молекул гемагглютинина, вокруг одной молекулы нейраминидазы. Белок М синтезируется там же, где и гликопротеиды, но транспортируется иначе и накапливается на внутреннем листке плазмалеммы.
Главная роль в организации липопротеидной мембраны вируса, равно как и во включении нуклеокапсида в участок почкования, видимо, принадлежит белку М.
В связи с разнообразием структуры вирусов животных разнообразны и способы формирования вирионов, однако можно сформулировать следующие общие принципы сборки
1) у просто устроенных вирусов формируются провирионы, которые затем в результате модификаций белков превращаются в вирионы. У сложно устроенных вирусов сборка осуществляется многоступенчато -- сначала формируются нуклеокапсиды или сердцевины, с которыми взаимодействуют белки наружных оболочек;
2) сборка сложно устроенных вирусов (за исключением сборки вирусов оспы и реовирусов) осуществляется на клеточных мембранах. Сборка ядерных вирусов происходит с участием ядерных мембран, сборка цитоплазматических вирусов -- с участием мембран эндоплазматической сети или плазматической мембраны, куда независимо друг от друга прибывают все компоненты вирусной частицы; 3) у ряда сложно устроенных вирусов существуют специальные гидрофобные белки, выполняющие функции посредников между сформированными нуклеокапсидами и вирусными гликопротеидами. Такими белками являются матриксные белки у ряда минус-нитевых вирусов (ортомиксо-, парамиксо-, рабдовирусов);
5) сложно устроенные вирусы для построения своих частиц используют ряд элементов клетки-хозяина, например липиды, некоторые ферменты, у ДНК-геномного SV40 -- гистоны, у оболочечных РНК-геномных вирусов -- актин, а в составе арена-вирусов обнаружены даже рибосомы. Клеточные молекулы несут определенные функции в вирусной частице, однако включение их в вирион может явиться и следствием случайной контаминации, как, например, включение ряда ферментов клеточных оболочек или клеточных нуклеиновых кислот.
В результате связывания ДНК с капсидами появляется новый класс промежуточных форм, которые называются неполными формами. Помимо неполных форм с разным содержанием ДНК, существует другая промежуточная форма в морфогенезе -- незрелые вирионы, отличающиеся от зрелых тем, что содержат ненарезанные предшественники полипептидов. Таким образом, морфогенез вирусов тесно связан с модификацией (процессингом) белков.
Сборка ядерных вирусов начинается в ядре, обычно -- в ассоциации с ядерной мембраной. Формирующиеся в ядре Промежуточные формы вируса герпеса почкуются в перинукле-арное пространство через внутреннюю ядерную мембрану, и вирус приобретает таким путем оболочку, которая является дериватом ядерной мембраны. Дальнейшая достройка и созревание вирионов происходят в мембранах эндоплазм этической сети и в аппарате Гольджи, откуда вирус в составе цитоплазматических везикул транспортируется на клеточную поверхность.
Выход вирусных частиц из клетки
Существует два способа выхода вирусного потомства из клетки: путем взрыва и путем почкования. Выход из клетки путем взрыва связан с деструкцией клетки, нарушением ее целостности, в результате чего находящиеся внутри клетки зрелые вирусные частицы оказываются в окружающей среде. Такой способ выхода из клетки присущ вирусам, не содержащим липопротеидной оболочки (пикорна-, рео-, парво-, папова-, аденовирусы). Однако некоторые из этих вирусов могут транспортироваться на клеточную поверхность до гибели клетки.
Выход из клетки путем почкования присущ вирусам, содержащим липопротеидную мембрану, которая является дериватом клеточных мембран. При этом способе клетка может длительное время сохранять жизнеспособность и продуцировать вирусное потомство, пока не произойдет полное истощение ее ресурсов.
Процесс репродукции вируса завершается формированием и освобождением вирионов из клетки. Зрелые вирионы образуются из синтезированных в клетке вирусных компонентов: нуклеиновой кислоты и белков. Как только их концентрация достигнет определенного уровня, начинается процесс самосборки вирионов, в основе которого лежит специфическое узнавание-взаимодействие вирионных компонентов.
В инфицированных клетках вирусные нуклеиновые кислоты и вирусспецифические белки синтезируются в значительно большем количестве, чем включаются в вирусные частицы. Синтез вирусных нуклеиновых кислот и вирусспецифических белков происходит почти одновременно и не менее чем на 1 ч опережает начало созревания вирусных частиц.
Разнообразие структуры вирусов отражается на способе их формирования и выходе из клетки. У просто устроенных вирусов формируются провирионы, которые затем в результате модификаций белков превращаются в вирионы.
Все безоболочечные вирусы позвоночных имеют кубическую симметрию. Структурные белки просто устроенных вирусов связываются спонтанно, образуя капсомеры, которые благодаря самосборке образуют капсиды, в которые упаковывается вирусная нуклеиновая кислота.
В процессе морфогенеза пикорнавирусов образуются различные вирусные структуры с последовательно возрастающими коэффициентами седиментации. Комплектование вириона часто связано с протеолитическим расщеплением одного или более капсидных белков, что хорошо изучено на примере полиовируса и вируса ящура.
Перед образованием зрелых вирионов из трех структурных полипептидов VPO, VP1 и VP3 (по 60 копий каждого) формируется прокапсид. Затем белок VPO расщепляется на два структурных белка (VP2 и VP4), и образуются зрелые частицы пикорнавирусов.
Механизм укладки вирусной нуклеиновой кислоты в переформированный прокапсид был выяснен у аденовирусов. Особый белок, прикрепленный к нуклеотидной последовательности на одном конце вирусной ДНК-известный как упаковывающая последовательность, помогает ДНК входить в прокапсид, прикрепляясь к базовым белкам ядра, после чего некоторые капсидные белки расщепляются и вирион становится зрелым. Большинство безоболочечных вирусов накапливается в цитоплазме или ядре и их можно обнаружить, как внутриклеточные инфекционные вирионы перед освобождением путем цитолиза.
Вирионы могут освобождаться из клетки при ее разрушении в результате лизиса или медленного, контролируемого процесса. По первому типу выходят из клетки вирусы, лишенные оболочки. Второй тип выхода из клетки характерен для оболочечных вирусов.
У оболочечных вирусов сначала формируются нуклеокапсиды, или сердцевины, которые затем покрываются белками наружных оболочек. Вирусы, имеющие оболочку (кроме вирусов оспы и реовирусов), формируются на клеточных мембранах.
Все оболочечные вирусы млекопитающих со спиральным нуклеокапсидом, так же как некоторые вирусы с икосаэдрическим нуклеокапсидом (герпесвирусы, тогавирусы и ретровирусы), созревают при почковании через плазматическую мембрану, через внутреннюю цитоплазматическую мембрану или через мембрану ядра.
Выход этих вирусов из клетки является одновременно и завершающей стадией формирования зрелого вириона. Образование зрелых вирионов у оболочечных вирусов осуществляется при почковании их нуклеопротеинов через модифицированные участки цитоплазматических или ядерных (герпесвирусы) мембран, в которых клеточные белки заменены вирусспедифическими.
Внутриклеточные и внеклеточные (полные) вирионы вируса оспы различаются между собой в антигенном отношении. Вирус выходит из ядра только через те участки мембраны, которые образовались после заражения. Именно этим и объясняется наличие вирусспецифических белков в вирусной оболочке.
Включение вирусных гликопротеинов в липидную двуслойную оболочку зараженной клетки происходит в результате замещения клеточных белков. Вирусные гликопротеины, объединенные в олигомеры, образуют типичные палочкообразные или булавообразные пепломеры с гидрофильными участками, экспонируемые над наружной поверхностью мембраны, а гидрофобный трансмембранный якорный домен и короткий гидрофильный цитоплазматический домен проецируется слабо в цитоплазме. В случае с икосаэдрическими вирусами, каждая молекула белка нуклеокапсида соединена непосредственно с цитоплазматическим доменом олигомера мембранного гликопротеина, окружающего нуклеокапсид.
Вирусы со спиральными нуклеокапсидами в большинстве случаев имеют матриксный белок, который прикрепляется к цитоплазматическому участку гликопротеинового пепломера; а противоположным концом к матриксному белку и это инициирует почкование. Освобождение отдельного вириона и массы вирионов не сопровождается образованием бреши в плазматической мембране и ее заметным повреждением. Многие, но не все вирусы, которые почкуются через плазматическую мембрану, являются цитопатогенными и могут быть связаны с персистентной инфекцией.
Флавивирусы, коронавирусы, артеривирусы и буньявирусы созревают, почкуясь через мембрану комплекса Гольджи или гладкой эндоплазматической сети; везикулы, содержащие вирус, затем мигрируют к плазматической мембране, с которой они сливаются, освобождая вирионы экзоцитозом. Уникальным для герпесвирусов является то, что их оболочка формируется при почковании через внутренний слой ядерной мембраны. Такие вирионы выходят из клетки через каналы цитоплазматического ретикулума, соединяющие ядерную оболочку с наружной мембраной клетки.
Благодаря такому механизму выделения, эти вирусы могут передаваться от клетки к клетке, несмотря на наличие антител в экстрацеллюлярном пространстве. Таким образом, возможна передача вируса от клетки к клетке без выхода во внешнюю среду.
Особую проблему представляет механизм формирования зрелых вирусных частиц, содержащих несколько различных молекул РНК (ортомиксо-, рео-, бир-на- и аренавирусы). Трудно представить, каким образом из пула нуклеиновых кислот в данный вирион попадает строго определенный комплект молекул РНК. Вероятно, важную роль в отборе нужных молекул играет специфическое взаимодействие нуклеиновой кислоты с определенными структурными белками вирионов.
- Вернуться в оглавление раздела "Микробиология."
Читайте также:


