Вирусная нагрузка при цитомегаловирусе
В статье проанализированы опубликованные данные по вопросам адекватной диагностики антенатальной и постнатальной цитомегаловирусной инфекции (ЦМВИ), а также лечению острых ЦМВИ у беременной, плода и новорожденного. Представлены отечественные клинические р
The article gives analysis of the data on the issues of relevance of diagnostics of antenatal and postnatal cytomegaloviral infection (CMVI), as well as treatment of acute CMVI in the pregnant, fetus and newborns. National clinical guidelines on diagnostics and treatment of congenital CMVI developed by the Russian Association of antenatal medicine in 2016, were presented; as well as the first unofficial international guidelines on the issues of diagnostics and treatment of congenital CMVI.
Цитомегаловирус (ЦМВ) — чрезвычайно распространенный вирус, поражающий людей всех возрастов и формирующий пожизненную персистенцию в организме инфицированного человека. Считается, что в большинстве случаев персистенция начинается в ранние годы жизни и протекает латентно, не оказывая выраженного патологического влияния на состояние здоровья инфицированного. С другой стороны, доказано, что персистенция вируса может сопровождаться хроническим воспалением, формировать разнообразные многочисленные иммунные дисфункции и определять развитие вторичных иммунных, аутоиммунных и дегенеративных нарушений. Различного рода иммунокомпрометации могут приводить к рецидивам размножения вируса и многообразным клиническим проявлениям с поражением любых органов и систем в любом возрасте.
Особое значение имеют врожденные инфекции детей, которые отличаются высоким риском развития тяжелых генерализованных форм и инвалидизирующих исходов заболевания, таких как потеря слуха, зрения, умственная отсталость, микроцефалия, судорожный синдром и пр. Такие пожизненные проблемы со здоровьем развиваются примерно у каждого пятого ребенка с врожденной цитомегаловирусной инфекцией (ЦМВИ), что определяет потребность в своевременном пренатальном выявлении беременных и плодов с высоким риском развития врожденной ЦМВИ и ранней диагностике и лечении инфекций у новорожденных.
Теоретические дискуссии по вопросам адекватной диагностики антенатальной и постнатальной ЦМВИ, а также лечению острых ЦМВИ у беременной, плода и новорожденного продолжаются с 1990-х гг., но отсутствие единых руководящих принципов затрудняет практическую работу врачей. Российской ассоциацией специалистов перинатальной медицины в 2016 г. выработаны отечественные клинические рекомендации по диагностике и лечению врожденной ЦМВИ. Созданная в рамках 5-й Международной конференции по ЦМВИ (Брисбен, Австралия, 19 апреля 2015) международная группа экспертов на основе консенсусных дискуссий и обзора литературы выработала первые неофициальные международные рекомендации по вопросам диагностики и лечения врожденной ЦМВИ, которые опубликованы в Lancet Infect Dis в марте 2017. Все эти рекомендации будут нуждаться в постоянном обновлении по мере поступления дополнительных данных.
ЦМВ — двухцепочечный ДНК-вирус, член семейства герпес-вирусов (β-герпесвирус человека). Синтез вирусного генома ДНК происходит в ядре клетки-хозяина. Исследования последних лет подтверждают гипотезу о том, что штаммы ЦМВ могут варьировать в их вирулентности, тропизме и патогенном потенциале, который, в свою очередь, вероятно, связан с генетической изменчивостью ключевых для патогенеза генов. Внешняя оболочка вируса содержит множественные гликопротеины, кодируемые вирусом. Гликопротеин B и гликопротеин H, по-видимому, являются основными факторами для формирования гуморального иммунитета — антитела к ним способны нейтрализовать вирус. Эти гликопротеины используют сегодня при разработке анти-ЦМВ-вакцин [3].
Вирус распространяется различными способами: через продукты крови (переливание, трансплантация органов), грудное вскармливание, пролиферацию в местах контактов (кожа, любые слизистые оболочки), перинатально и половым путем. ЦМВИ может протекать в виде первичной инфекции ранее неинфицированных (серонегативных) пациентов, реинфекции или реактивации у инфицированных (серопозитивных) людей; может вызывать острое, латентное и хроническое течение врожденных или приобретенных форм болезни [4].
При острой ЦМВ-инфекции могут поражаться практически все типы клеток человеческого организма — эндотелиальные клетки, эпителиальные клетки, клетки гладкой мускулатуры, фибробласты, нейронные клетки, гепатоциты, трофобласты, моноциты/макрофаги, дендритные клетки и пр. Все типы клеток поражаются и в мозге: нейроны, астроциты, клетки эпендимы, выстилающие желудочки, макроглия, эндотелий капилляров, оболочек, микроглия, сплетения сосудистой оболочки, дендриты и аксоны — т. е. вирус в мозге не имеет избирательной клеточной цели, что объясняет многообразие клинических форм поражения нервной системы у больных [5].
Считается, что ЦМВ реплицируется в эндотелиальных клетках с низкой скоростью, вызывая преимущественно подострые инфекции, однако истинная скорость репликации вируса в клетках определяется эффективностью цитотоксического Т-клеточного иммунитета и степенью иммуносупрессии хозяина. Так, например, на моделях ЦМВИ у животных продемонстрировано, что отсутствие CD4 Т-клеток сопровождалось более тяжелым и стремительным заболеванием ЦМВИ. Известно также, что ВИЧ-инфицированные новорожденные имеют очень высокую частоту врожденной ЦМВИ с высоким риском смерти, неврологических дефектов и прогрессии ВИЧ-инфекции [6–7].
Особое свойство ЦМВИ — способность вызывать депрессию практически всех звеньев иммунитета, резко угнетать продукцию интерферонов (ИНФ), в первую очередь ИНФ-α. Внедрение ЦМВ приводит к иммунной перестройке в виде снижения реакции лимфоцитов на вирусы в связи с угнетением экспрессии антигена макрофагами, подавлением пролиферативной активности лимфоцитов (что коррелирует с тяжестью болезни), угнетением фагоцитарной активности и завершенности фагоцитоза [7].
Доказано, что и первичные и латентные ЦМВИ сами могут индуцировать хронические воспалительные системные реакции с устойчивой иммунной активацией, запускать и поддерживать аутоиммунные процессы, усиливать аллореактивность Т-клеток после трансплантации и, возможно, участвовать в комплексе причин повышения частоты нейродегенеративных состояний с возрастом человека (Jones R. P. The debility cascade in neurological degenerative disease). Установлено также, что ЦМВ-индуцированные иммунные изменения в пожилом возрасте могут отвечать, например, за замедленную элиминацию вируса гриппа из легких, сниженный поствакцинальный иммунитет на гриппозные вакцины, измененную реакцию организма на терапию интерферонами [8].
Многие годы риск развития врожденных инфекций плода ассоциировали преимущественно с первичной инфекцией матери, однако к настоящему моменту не вызывает сомнения, что большая доля врожденных ЦМВИ (до 75%) встречается в условиях рецидивирующей во время беременности материнской инфекции. Допускаются также и экзогенные реинфекции с новыми штаммами ЦМВ — доказательства основываются на молекулярных данных, подтверждающих получение нового штамма вируса.
Вместе с тем степень риска вертикального инфицирования плода в условиях первичной инфекции матери рассматривают по-прежнему как чрезвычайно высокую — в 30–50% случаев острой первичной инфекции беременной развивается врожденная инфекция ребенка. Показано, что ранее существовавший материнский иммунитет хоть и не гарантирует полной защиты, тем не менее обеспечивает снижение риска врожденной ЦМВИ при следующих беременностях на 69% [9].
Недавними исследованиями установлено, что ЦМВ может поражать амниотическую мембрану, ухудшая цитотрофобласт-индуцированный лимфангиогенез и ремоделирование сосудов в плаценте и задерживая правильное развитие клеток — предшественников трофобласта, одновременно вызывает врожденную провоспалительную иммунную реакцию. Это приводит к гипоксии плода, задержке внутриутробного развития и возможным последующим гипоксическим повреждениям головного мозга. Степень поражения плода определяется сроками антенатального инфицирования и вирусной нагрузкой в размножающихся клетках — чем меньше гестационный возраст, тем более выражена альтерация (разрушение) тканей с формированием пороков развития [10]. Особенно быстро ЦМВ достигает максимума в астроцитарных и глиальных клетках, при этом максимальная экспрессия вируса найдена в глиальных клетках развивающегося мозга мышат (что объясняет микрогирию, микроцефалию и другие пороки ЦМВ-инфицированного мозга детей). По мере увеличения срока гестации в клинической картине инфекционного заболевания плода преобладают симптомы системного воспаления с выраженной пролиферацией и экссудацией. У 1/3 умерших от ЦМВИ новорожденных (из них 60% — недоношенные) при морфологическом исследовании выявляют различные пороки развития. У 43% — признаки генерализованной внутриутробной инфекции с геморрагическими и ишемическими инфарктами (в том числе в головном и спинном мозге) [11].
Способность вируса реплицироваться в любых клетках человеческого организма определяет многообразие клинических форм болезни; ЦМВ может вызывать как генерализованные инфекции, так и поражения отдельных органов: печени, головного мозга, сердца, легких, мочеполовых органов, желудочно-кишечного тракта и др.
У беременных острая первичная ЦМВИ протекает чаще бессимптомно (25–50%) или малосимптомно — с неспецифическими проявлениями (обычно лихорадка, астения и головная боль).
Как первичная, так и рецидивирующая ЦМВИ матери может стать причиной антенатальных ультразвуковых признаков поражения плода в результате трансплацентарной инфекции. Самые частые УЗИ-признаки: задержка роста плода, вентрикуломегалия, микроцефалия, перивентрикулярная гиперэхогенность, кальцификаты в мозге, плевральный выпот или асцит, гепатоспленомегалия, гиперэхогенный кишечник и мекониальный илеус и др. Эти УЗИ-аномалии эмбриона прогнозируют тяжелую генерализованную манифестную врожденную ЦМВИ новорожденного с высоким риском формирования инвалидизирующих исходов болезни и смерти. Поэтому первичная острая ЦМВИ во время беременности может являться показанием к ее искусственному прерыванию. Установлено, что около 4% детей с антенатальной ЦМВИ умрут в утробе матери или вскоре после рождения, среди остальных около 60% будут иметь когнитивные дефекты, нейросенсорную потерю слуха и другие неврологические и прочие проблемы [11–12].
Сегодня установлено также, что нейросенсорная тугоухость является прогрессирующим заболеванием и может формироваться в течение 5–6 лет жизни даже у детей, родившихся с бессимптомной ЦМВИ (это связывают с многолетней репликацией ЦМВ в перилимфе), что требует соответствующей длительности наблюдения ребенка.
При инфицировании в поздние сроки гестации ЦМВИ у новорожденного может проявляться и как генерализованная инфекция, и как поражение отдельных органов с нетяжелыми транзиторными симптомами болезни, например, умеренной гепатомегалией, изолированным снижением количества тромбоцитов или повышенным уровнем аланинаминотрансферазы. Возможна и клинически бессимптомная ЦМВИ с изолированной нейросенсорной тугоухостью.
У 10% всех новорожденных в течение первого месяца жизни возникают инфекционные заболевания в результате в основном семейных контактов, в том числе грудного вскармливания. Экскреция ЦМВ с грудным молоком в течение первых недель после родов бывает низкой, достигает максимума к 4–8 неделям, завершается к 9–12 неделям. Считается, что риск трансмиссии вируса коррелирует с вирусной нагрузкой в молоке, передача максимальна при высокой экскреции. У доношенных детей в результате инфицирования ЦМВ через молоко матери формируется, как правило, субклиническое течение инфекции без остаточных явлений; в клинической картине более вероятно развитие энтероколита и транзиторного холестатического гепатита с минимальным цитолизом. Недоношенные дети (вес
И. Я. Извекова 1 , доктор медицинских наук, профессор
М. А. Михайленко
Е. И. Краснова, доктор медицинских наук, профессор
ФГБОУ ВО НГМУ МЗ РФ, Новосибирск
Цитомегаловирусная инфекция в практике врача: современный алгоритм диагностики и лечения/ И. Я. Извекова, М. А. Михайленко, Е. И. Краснова
Для цитирования: Лечащий врач № 4/2018; Номера страниц в выпуске: 90-95
Теги: новорожденные, беременность, инфекция, персистирование
Цитомегаловирус (ЦМВ) или вирус герпеса 5 типа, – ДНК-содержащий вирус Cytomegalovirus hominis семейства Herpesviridae подсемейства Betaherpesvirinae. Цитомегаловирусная инфекция (ЦМВИ) человека – хроническая антропонозная болезнь вирусной этиологии, характеризующаяся многообразием форм патологического процесса и клинических проявлений – от латентной инфекции до клинически выраженного генерализованного заболевания. Заболевание ЦМВИ классифицируют в зависимости от сроков и механизмов заражения (врожденная и приобретенная инфекция, пренатальная, интранатальная и постнатальная), степени активности вируса (латентная, персистирующая и реактивированная инфекция), первичного или повторного заражения (острая инфекция, реактивация вируса и реинфекция).
Отличительными особенностями инфекции являются возможность ЦМВ персистировать во многих органах и способность его к инфицированию практически всех клеток организма человека, что предопределяет многообразие клинических проявлений, как при врожденной, так и приобретенной формах инфекции. ЦМВ рассматривается в качестве основного возбудителя внутриутробной инфекции, имеющей самые различные исходы: от инфицирования без реализации инфекции, формирования пороков развития и заболевания новорожденных до гибели плода и мертворождения.
ЦМВИ – типичный антропоноз. Источником инфекции является больной человек либо вирусоноситель. Пути передачи: вертикальный, половой, воздушнокапельный, фекально-оральный, артифициальный (парентеральный). Факторами передачи являются кровь, цервикальный и вагинальный секреты, сперма, женское молоко. Вирус выделяется с мочой, фекалиями, слюной, мокротой, в меньшей степени – со слезной жидкостью. Заражение может происходить также при переливании крови, трансплантации органов и тканей. Цитомегалия — широко распространенная инфекция, среди взрослого населения РФ у 73–98% обнаружены АТ-ЦМВ.
ЦМВИ относится к оппортунистическим инфекциям, особую опасность представляет для больных с иммунодефицитами различной природы. Иммуносупрессия приводит к реактивации латентной инфекции и развитию манифестных вариантов болезни с поражением различных органов и систем, способных привести к летальному исходу. Манифестная ЦМВИ занимает одно из первых мест в структуре оппортунистических заболеваний у ВИЧ-инфицированных пациентов. Данная патология встречается у 20–40% больных СПИДом, не получающих антиретровирусной терапии. Клинически выраженная ЦМВИ — одно из серьезных инфекционных осложнений при трансплантации органов, инфекция обостряет процессы, приводящие к реакции отторжения трансплантата.
При персистенции ЦМВ в организме человека выделяют две стадии, которые сменяют друг друга – продуктивную (с репликацией вируса) и латентную. Выход вируса из латентной стадии означает реактивацию, что может быть предопределено снижением иммунорезистентности либо появлением иных факторов, способствующих его репродукции. Выявление прямых маркеров репликации вируса (виремия, ДНК или АГ) свидетельствует о наличии инфекции.
При первичном заражении на 5–7 день вырабатываются АТ IgM, через 10–14 дней – низкоавидные АТ IgG, затем постепенно авидность этих АТ увеличивается, они становятся высокоавидными. АТ IgM исчезают через один месяц, низкоавидные АТ IgG – через 1–3 месяца, высокоавидные АТ IgG циркулируют в крови носителя пожизненно. При первичном инфицировании в стадии “серологического окна”, до начала синтеза АТ, происходит активная репликация вируса, в этот период единственным маркером инфекции является ДНК вируса в крови. При реактивации возможно появление АТ IgM и/или IgA, а также низкоавидных АТ IgG; в пик реактивации выявляются ДНК либо АГ ЦМВ в плазме крови.
Решающим условием антенатальной ЦМВИ является виремия у матери вследствие первичного или повторного заражением вирусом или его реактивации. ЦМВ способен преодолевать плацентарный барьер и поражать плод в различные сроки беременности, вызывая врожденную инфекцию. По данным различных авторов, активная форма ЦМВИ выявляется у женщин с отягощенным акушерским анамнезом в 35–60% случаев. Входными воротами для вируса в антенатальном и интранатальном периодах течения беременности могут быть плацента и плодные оболочки, в неонатальном периоде и позже – дыхательные пути и пищеварительный тракт, возможно заражение и через кровь.
ЦМВ обладает преимущественно нейротропным, эпителиотропным, гепатотропным и кардиотропным действием на плод. Его воздействие может быть и опосредованным, приводящим к различным нарушениям в плаценте: расстройству маточно- плацентарного кровообращения, отклонению в эволюционном формировании плаценты. Клиническим эквивалентом этих расстройств могут быть сокращение продолжительности беременности и преждевременное родоразрешение, рождение детей с симптомами перенесенной гипоксии или признаками внутриутробной гипотрофии, общая задержка внутриутробного развития.
Наибольшее значение для развития ранних перинатальных поражений плода имеет гематогенный путь инфицирования. Кроме того, для интранатальных и более поздних поражений характерными являются вертикальный и контактный пути передачи ЦМВ, нередки также случаи смешанного инфицирования. Острая ЦМВИ может протекать в виде генерализованной формы с присоединением вторичных инфекций и иметь летальный исход уже в первые недели жизни ребенка. При инфицировании плода во время реактивации латентной ЦМВИ чаще имеют место поздние проявления инфекции в виде нарушений зрения, слуха, задержки психического развития, двигательных нарушений. При отсутствии выраженных иммунологических нарушений острая ЦМВИ переходит в латентную с пожизненным присутствием вируса в организме человека. Развитие иммуносупрессии, в частности связанной с ВИЧ-инфекцией, ведет к возобновлению репликации ЦМВ, появлению вируса в крови и манифестации заболевания. Летальность больных ВИЧ-инфекцией, страдающих ЦМВИ, составляет 25–27%.
Клинический диагноз ЦМВ-инфекции требует обязательного лабораторного подтверждения. Выявление в крови пациента АТ-ЦМВ IgМ и/или IgG недостаточно ни для установления факта активной репликации ЦМВ, ни для подтверждения манифестной формы заболевания.
Показания к обследованию
- Женщины, планирующие беременность;
- женщины с отягощенным акушерским анамнезом (перинатальные потери, рождение ребенка с врожденными пороками развития);
- беременные женщины (в первую очередь имеющие УЗИ-признаки внутриутробной инфекции, лимфоаденопатии, лихорадку, гепатит и гепатоспленомегалию неясного генеза);
- беременные женщины с иммунодефицитом, в т. ч. с ВИЧ-инфекцией;
- матери, родившие ребенка с признаками внутриутробной инфекцией или врожденными пороками развития;
- дети, имеющие симптоматику врожденной инфекции, пороки развития или рожденные женщинами из группы риска по внутриутробной передаче ЦМВ;
- пациенты (в первую очередь новорожденные) с сепсисом, гепатитами, менингоэнцефалитом, пневмонией, поражением ЖКТ;
- пациенты с наличием иммунодефицита с клинической картиной органных или генерализованных поражений.
- Врожденная ЦМВИ – краснуха, токсоплазмоз, неонатальный герпес, сифилис, бактериальная инфекция, гемолитическая болезнь новорожденных, родовая травма, наследственные синдромы;
- мононуклеозоподобное заболевание – инфекции, вызываемые вирусом Эпштейна-Барр, герпес-вирусами 6 и 7 типов, острая ВИЧ-инфекция, стрептококковый тонзиллит, дебют острого лейкоза;
- заболевание органов дыхания у детей раннего возраста – коклюш, бактериальный трахеит или трахеобронхит, РС-вирусной инфекция, герпетический трахеобронхит;
- у больных с иммунодефицитом – пневмоцистная пневмония, туберкулез, токсоплазмоз, микоплазменная пневмония, грибковые и герпетические инфекции, бактериальный сепсис, лимфопролиферативные заболевания, ВИЧ-энцефалит, нейросифилис, прогрессирующая многоочаговая лейкоэнцефалопатия;
- полинейропатия и полирадикулопатия – полирадикулопатия, вызванная герпесвирусами 2 и 6 типов, синдром Гийена-Барре, токсическая полинейропатия, связанная с приемом лекарственных средств, алкоголя, наркотических психотропных веществ.
Этиологическая лабораторная диагностика включает микроскопические исследования, выявление возбудителя в культуре клеток, обнаружение АГ или ДНК, определение АТ IgM, IgА, IgG, авидности АТ IgG.
Материал для исследования
- Кровь (сыворотка, плазма), лейкоциты крови, моча, слюна, СМЖ – культуральные исследования, выявление ДНК;
- пуповинная кровь, амниотическая жидкость – выявление ДНК;
- слюна, моча – выявление АГ;
- сыворотка/плазма крови – определение АТ.
Для обнаружения АГ вируса в слюне и моче используют метод РИФ, по количеству светящихся клеток можно приблизительно оценить интенсивность выделения вируса. В связи с персистенцией ЦМВ обнаружение АГ не указывает на активность инфекционного процесса, для ее оценки требуются дополнительные исследования – выявление отдельных АГ вируса (р55, рр65 и др.).
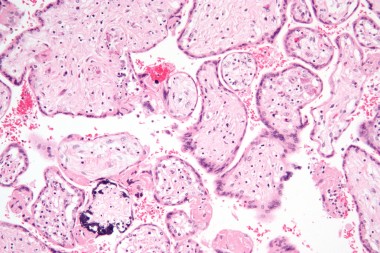
При проведении микроскопического исследования (световая микроскопия) основными морфологическими признаками ЦМВИ являются гигантские клетки с внутриядерными включениями (цитомегалы). Их можно обнаружить в эпителии почечных канальцев, желчных протоках, выводных протоках слюнных желез, поджелудочной железы, ткани легких, клетках глии, нейронах, эндотелиоцитах. Наличие таких клеток указывает на репродукцию вируса, однако они обнаруживаются не во всех случаях активной инфекции. Диагностическая чувствительность метода не превышает 50%.
Определение специфических АТ к вирусу помогает в распознавании заражения человека ЦМВ, но ввиду длительного периода нарастания титра АТ от момента инфицирования, последующего долгого сохранения их в крови, трансплацентарного перехода АТ IgG от матери к плоду (выявляются у ребенка до 1,5 лет) диагностическая ценность исследования ограничена. При наблюдении в динамике (2–4 недели) повышение титра АТ IgG в 4 раза указывает на активную ЦМВИ. Однако необходимость длительного периода наблюдения (до 4 недель) и возможность сохранения повышенного титра АТ на протяжении ряда лет лимитирует использование такого подхода к диагностике.
Дополнительным исследованием при поражении мозга, вызванного ЦМВ, может быть параллельное обнаружение АТ IgG в периферической крови и СМЖ методом ИФА с последующим расчетом их соотношения. Значение соотношения позволяет выявить интратекальную продукцию АТ и соответственно вовлечение в инфекционный процесс ЦНС.
Иммуноблот позволяет детектировать АТ IgM и IgG к отдельным белкам ЦМВ, подтвердить специфичность исследования, следить в динамике за появлением и исчезновением отдельных белков, что имеет высокое диагностическое и прогностическое значение. Наличие АТ к отдельным АГ вируса подтверждает формирование иммунного ответа к ЦМВ.
Показания к применению различных лабораторных исследований и интерпретация их результатов у разных категорий обследуемых
Диагностика первичного заражения, в т. ч. в период беременности, возможна только у пациентов, в крови которых отсутствуют АТ-ЦМВ. Независимо от клинических вариантов заболевания, при первичной ЦМВИ выявляются прямые (присутствие вируса, его ДНК или АГ) и косвенные (АТ-ЦМВ) лабораторные маркеры активной репликации ЦМВ. При обследовании больных при подозрении на активную ЦМВИ и манифестную форму заболевания (ЦМВ-болезнь) необходимо количественное определение содержания ДНК ЦМВ в крови. Определение ДНК ЦМВ в ликворе, плевральной жидкости, БАЛЖ, биоптатах бронхов, биоптатов органов выполняют при наличии соответствующей органной патологии.
Выявление прямых маркеров репликации вируса (виремия, ДНК или АГ) свидетельствует о наличии инфекции. Выявление ДНК ЦМВ или АГ вируса в крови беременной женщины – основной маркер высокого риска заражения плода и развития врожденной ЦМВИ.
Отсутствие АТ-ЦМВ IgM, IgА и IgG означает отсутствие ЦМВ в организме. Однако у лиц с выраженным иммунодефицитом при активной репликации ЦМВ продукция специфических АТ может быть снижена до неопределяемого уровня.
Выявление АТ-ЦМВ разных классов позволяет определить фазы инфекционного процесса (репликативная или латентная). АТ IgM чаще оценивают как маркер первичной герпес-вирусной инфекции. При выявлении АТ IgM для подтверждения инфицирования ЦМВ рекомендуются дополнительные исследования: определение АТ IgА или авидности АТ IgG, выявление АТ к отдельным белкам с использованием иммуноблота; повторное обследование женщины или ребенка через 2 недели. Выявление АТ IgА и(или) низкоавидных АТ IgG подтверждает наличие инфекции. При повторном выявлении АТ IgM и отсутствии IgА и(или) низкоавидных IgG результат выявления АТ IgM считают ложноположительным.
Выявление АТ IgM и IgG к предранним белкам-антигенам и низкоавидных АТ IgG свидетельствует о первичном инфекционном процессе.
Обнаружение только АТ IgG не позволяет охарактеризовать период заболевания. При наличии иммуносупрессии классического (4-х кратного) увеличения АТ IgG во время рецидива не наблюдают.
Установление факта инфицирования плода осуществляется на основании обнаружения ДНК ЦМВ. Выбор биологического материала определяется с учетом срока гестации, обусловливающего возможность проведения того или иного метода инвазивной пренатальной диагностики: амниотическая жидкость – 16–23 недели, пуповинная кровь – 20–24 недели. Косвенным подтверждением факта инфицирования плода является обнаружение АТ IgM и/или АТ IgА в пуповинной крови (проведение исследования возможно с 22 недели беременности).
Лабораторная диагностика врожденной ЦМВИ основана на обнаружении ЦМВ, его ДНК или АГ в различном биологическом материале (периферическая кровь, моча, слюна, смывы и мазки от ротоглотки, СМЖ) и выявлении в сыворотке или плазме крови АТ IgМ и IgА в течение первых 7 дней после рождения. Проведение исследования в более поздние сроки не позволяет дифференцировать врожденную и приобретенную инфекцию. Выявление ДНК ЦМВ или АГ вируса в крови, моче, соскобах со слизистой ротовой полости через 4–6 недель жизни ребенка при отсутствии вируса в первые 2 недели говорит об интранатальном или раннем постанатальном заражении. Подтверждением манифестной ЦМВИ у детей первых месяцев жизни является наличие ДНК ЦМВ в крови.
При сомнительных результатах дополнительную диагностическую информацию может дать выявление АТ IgМ к отдельным белкам-антигенам вируса методом иммуноблота. Отсутствие АТ-ЦМВ у детей с врожденной ЦМВИ может быть связано с развитием иммунологической толерантности к АГ вируса цитомегалии (инфицирование ЦМВ не сопровождается эффективным синтезом АТ-ЦМВ).
Выявление АТ IgG в сыворотке крови новорожденного без сопоставления с уровнем АТ в крови матери не является диагностически значимым вследствие возможности их трансплацентарного переноса из материнского организма. Только при динамическом (с интервалом в 14–21 день) сравнении уровня АТ IgG новорожденного ребенка с уровнем АТ IgG в крови матери можно судить об их природе. Если титры АТ IgG у ребенка при рождении равны материнским, а при повторном исследовании через 3–4 недели снижаются приблизительно в 1,5–2 раза, то АТ, выявленные у ребенка, являются материнскими.
Скрининг беременных женщин – выявление АТ IgМ и низкоавидных АТ IgG. Для исключения реактивации целесообразно определение АТ IgА и низкоавидных АТ IgG.
Обследование больных с наличием иммунодефицита при подозрении на активную ЦМВИ и манифестную форму заболевания (ЦМВ-болезнь) включает гистологическое исследование биопсийных материалов для выявление цитомегалов (окраска гематоксилином и эозином), обнаружение ДНК ЦМВ в ликворе, плевральной жидкости, БАЛ, биоптатах бронхов, биоптатов внутренних органов при наличии соответствующей органной патологии; выявление АГ ЦМВ в крови, определение концентрации ДНК ЦМВ в крови методом ПЦР. В диагностике ЦМВИ у ВИЧинфицированных наиболее информативно наличие в крови ДНК ЦМВ в высокой концентрации (в плазме крови >10000 копий/мл, в лейкоцитах > 1000 копий/ 105 лейкоцитов).
Продолжая использовать наш сайт, вы даете согласие на обработку файлов cookie, пользовательских данных (сведения о местоположении; тип и версия ОС; тип и версия Браузера; тип устройства и разрешение его экрана; источник откуда пришел на сайт пользователь; с какого сайта или по какой рекламе; язык ОС и Браузера; какие страницы открывает и на какие кнопки нажимает пользователь; ip-адрес) в целях функционирования сайта, проведения ретаргетинга и проведения статистических исследований и обзоров. Если вы не хотите, чтобы ваши данные обрабатывались, покиньте сайт.
Copyright ФБУН Центральный НИИ Эпидемиологии Роспотребнадзора, 1998 - 2020

! Продолжая использовать наш сайт, вы даете согласие на обработку файлов cookie, пользовательских данных (сведения о местоположении; тип и версия ОС; тип и версия Браузера; тип устройства и разрешение его экрана; источник откуда пришел на сайт пользователь; с какого сайта или по какой рекламе; язык ОС и Браузера; какие страницы открывает и на какие кнопки нажимает пользователь; ip-адрес) в целях функционирования сайта, проведения ретаргетинга и проведения статистических исследований и обзоров. Если вы не хотите, чтобы ваши данные обрабатывались, покиньте сайт.

Есть ещё один представитель семейства герпесвирусов - цитомегаловирус (ЦМВ, лат. Cytomegalovirus, CMV) — вирус герпеса человека 5 типа.
Своё название (от греч. цитос - клетка и мегас - большой) этот вирус, открытый в середине 20-го века, получил за способность проникать в клетки организма , вызывая их мегалию (патологическую увеличенность, например, клеток крови). Он повреждает цитоскелет клеток, после чего последний раздувается. О том, какое это имеет значение поговорим в этой статье, но позже.
Данный вирус, как и ВЭБ широко распространён среди всей человеческой популяции, во всех расовых группах и точках земного шара. Около 60% детей старше 6 лет и всех взрослых имеют антитела к нему, обеспечивающие защиту. Теоретически возможен воздушно-капельный путь передачи, но как правило доминирует путь тесного контакта с заражённым. Вирус лимфотропен, хотя и способен проникать в кровь, минуя лимфу. Кроме того, может поражать железы (особенно слюнные), мышечные волокна и очень многие внутренние органы (при слабом контроле над ним со стороны иммунной системы). Основной источник заражения - биологические жидкости заражённого: сперма, вагинальный секрет, кровь, слюна. Особенную опасность для плода представляет заражение матери ЦМВ во время беременности или его активация у беременной женщины (правда, во втором случае риск заражения ребёнка ниже, чем при первичном инфицировании матери). Способен вызывать серьёзные пороки развития у плода в случае его заражения: врождённые пороки сердца, поражения ЦНС, гепатиты и врождённые циррозы печени. Как правила данные изменения необратимы и имеют неблагоприятный прогноз.
После попадания в организм, инкубационный период длится от трёх недель до двух месяцев, после чего наступает острая фаза заболевания, которая длится от 2 до 6 недель. При этом появляются: повышение температуры тела, признаки общей интоксикации, слабость, ознобы, головные боли, боли в мышцах и бронхит. Может возникать мононуклеозоподобный синдром с сыпью, но все серологические тесты (поиск специфических антител) на ВЭБ отрицательны. Далее, иммунная система готовится к отражению атаки и старается обуздать названного гостя (чаще всего, успешно. Во всяком случае ранее, когда причин для снижения иммунитета было меньше, это было так. Сейчас же ситуация несколько поменялась в силу факторов, рассматриваемых в статье о ВЭБ). В случае нехватки сил организма острая фаза переходит в более спокойную форму (стёртое либо подострое течение) которая проявляется вегето-сосудистыми расстройствами и постепенными поражениями внутренних органов. В данном случае возможны три сценария проявления заболевания, разворачивающиеся в долговременной перспективе.
1)ОРВИ-сценарий (острая респираторная вирусная инфекция) — представлены все симптомы ОРВИ — слабость, общее недомогание, быстрая утомляемость, повышение температуры тела носит субфебрильный характер (37,2 - 37,5), головные боли, насморк, увеличение и воспаление слюнных желез, белесоватые налеты на языке и деснах; иногда возможно наличие воспаленных миндалин, симптомы чем-то напоминают тонзиллит, но антибиотики не эффективны. ОРВИ сценарий может длится долго, периодически затихать и возникать вновь. Человек может при этом думать, что постоянно “подхватывает” простуду. Эта форма может со временем пройти, либо привести к более серьёзному течению и/или осложнениям.
2)Форма генерализованной инфекции (самая тяжёлая, потенциально летальная) — поражение ЦМВ внутренних органов (воспаление печеночной ткани - ЦМВ-гепатит, надпочечников, почек, селезенки, поджелудочной железы, сосудов, сердца, лёгких). ЦМВ в этом случае может стать причиной бронхита, пневмонии, что ещё более ухудшает состояние и ещё сильнее повышает нагрузку на (и без того) ослабленную иммунную систему. При этом лечение антибиотиками оказывается менее эффективным, нежели при обычном протекании бронхита и/или пневмонии, чаще и вовсе неэффективным. Снижая противовирусный иммунитет и местные иммунные функции, антибиотики могут даже способствовать ухудшению состояния! Вместе с тем может наблюдаться уменьшение тромбоцитов в периферической крови, поражение стенок кишечника, сосудов глазного яблока, головного мозга и нервной системы (энцефалиты, менингиты с риском ослабления мозговых функций и расстройств умственной деятельности - цмв-энцефалопатия у взрослых. Заболевание способно прогрессировать до состояния деменции). Вирус способен поражать эндотелиальные клетки сосудов, способствуя их дисфункции и в конечном итоге - развитию атеросклероза. Кроме того, находясь в клетках почек он способствует выделению ими излишков гормона ренина, что в сочетании с повреждением сосудистой выстилки и дисфункцией сосудистого тонуса может приводить к артериальной гипертензии. Но сердечно-сосудистые эффекты ЦМВИ имеют отдалённый и постепенный характер (то-то В.Покровский и Ко пытались “вич” прицепить к повышенному риску ССЗ в перспективе!).
Внешне генерализованная форма проявляется, в дополнении к увеличенным слюнным железам, кожной сыпью, возможны присоединения других кожных расстройств. Чем не развёрнутая клиника СПИДа?? Повсеместно в медицинских источниках говорится о том, что такая форма ЦМВИ (цитомегаловирусной инфекции) возможна только при сильном ослаблении иммунной системы. Перечисляются такие факторы риска как: возрастной - недоношенность и грудничковый возраст (когда иммунная система ещё не окрепла), старость (когда защитные функции слабеют и угасают); образ жизни - частое употребление алкоголя; регулярное недоедание, постоянное несбалансированное питание (об этом, правда, речь идёт всегда реже всего, ибо согласно политике двойных стандартов, уровень жизни нормальный и с питанием у людей проблем нет. Реалии прохимиченных и лишённых всякой пользы продуктов со счетов сбрасываются и умалчиваются); химический фактор: терапия цитостатиками, иммуносупрессорами, глюкокортикостероидами, употребление наркотиков; фактор анамнеза - наличие других ослабляющих иммунитет заболеваний, операции, пересадка органов и конечно же (угадали. ) – ВИЧ-инфекция! Куда же без неё то родимой, никуда ж теперь ведь. Причём по значимости, её ставят чаще на первое место. Ведь это просто клондайк для мошенничества - антибиотики не работают, иммунитет больного ослаблен и продолжает слабеть из-за деятельности ЦМВ. А если раскинуть мозгами, то изначальные причины ослабления иммунного ответа, изменения в цитокиновой обстановке, делающие иммунный ответ вялым, запаздывающим и неполноценным рассмотрены в предыдущей статье и других моих статьях.
Посему - повторяться не буду. Снова ситуация как у “Миши” и снова её последствия. И что самое то главное, ведь будет же ИФА и иммуноблот плюсовать, т.е давать положительную реакцию в тесте на вич. И никто, никак и нигде не заподозрит фальсификации. Тяжёлое течение ЦМВ приобретает у лиц с ослабленным иммунитетом? Да. Тесты на ВИЧ дают +? Дают. Состояние прогрессирует? А как же! Снова шито-крыто. Конечно, зная наперёд эти варианты, можно в одну из вариаций развернувшегося СПИДа внести описание клиники генерализованной ЦМВИ. Тем более, что он способен ещё и приводить к снижению уровня тромбоцитов, ослабленность организма приводит со временем к анемии. А это выдают за действие вируса иммунодефицита на костный мозг и всё. Примечательно и то, что при изначально ослабленном иммунитете и генерализованной форме ЦМВИ на этом фоне, присоединившиеся бактериальные инфекции ведут себя не так, как у лиц с изначально сильной иммунной системой. В частности, общеизвестен факт, что все вирусные инфекции открывают как бы “входные ворота” бактериям. На этом фоне развиваются бактериальные осложнения после гриппа и ОРВИ, например. Так вот, при генерализованной форме вирусной инфекции, попытки лечить вторичные бакт. инфекции почти не приносят результата: антибиотики глушат бактерии, но снижают противовирусный иммунитет ещё больше, вирус реплицируется и умножается, открывая входные ворота следующим бактериям и неизбежен рецидив только что перенесённой бактериальной инфекции или присоединение ещё одной. А силы организма ведь не бесконечны. Эта потенциально фатальная ситуация на фоне положительных тестов на ВИЧ приписывается ВИЧ и СПИДу, а на деле всё совсем иначе. Для того, чтобы обман был удобен, есть целая проторенная калея. Заключается она вот в чём.

Согласно постановлению ВОЗ, чтобы получить диагноз “вич-инфекция” нужно, чтобы в иммуноблоте была реакция антител с двумя либо тремя из так называемых “белков оболочки ВИЧ”. Если такая реакция есть - то независимо от наличия положительной или отрицательной реакции с другими антигенами вич, человек признаётся вич-позитивным. Если реакция только с одним из “белков оболочки”, то тогда результат сомнительный (и надо проверяться каждые 3 мес,чтобы когда организм ослабнет и появится более сильный аутоиммуный процесс, получить-таки свой “подарочек” в виде вич-позитивности). Если же к “белкам оболочки вич” антитела не найдены, то будь они найдены хоть ко ВСЕМ остальным антигенам вич, человек признаётся вич-негативным. Представляете. Чудеса да и только. Вспомним о белках оболочки вич, что они из себя представляют: gp160, gp120 и gp41 - где g сокр. от “глико-” , а р- протеин. Гликопротеин (гликопротеид) это белок с включением сахара (уровень сахара в крови еще называют гликемией, от такого же “глико”) в своей молекуле, это если по простому. Эти gp нам известны как компоненты актина. Мы говорили в начале статьи о цитоскелете, пришло время остановиться на этом понятии подробнее.
Цитоскелет — это клеточный каркас или скелет, находящийся в цитоплазме каждой живой клетки. Это динамичная, изменяющаяся структура, в функции которой входит поддержание и адаптация формы клетки к внешним воздействиям, обеспечение движения клетки как целой единицы, внутриклеточный транспорт веществ и клеточное деление. Цитоскелет образован белками, несколько основных его систем называют либо по основным структурным элементам, заметным при электронно-микроскопических исследованиях (микрофиламенты, промежуточные филаменты, микротрубочки), либо по основным белкам, входящим в их состав (актин-миозиновая система, кератины, тубулин-динеиновая система).
Микрофиламенты это две цепочки из белка актина, закрученные спиралью. В основном они сконцентрированы у внешней мембраны клетки, так как отвечают за форму клетки и способны образовывать выступы на поверхности клетки (микроворсинки). Также они участвуют в межклеточном взаимодействии (образовании адгезивных контактов - слипаний клетки с чем-либо), передаче сигналов и, вместе с миозином — в мышечном сокращении (как скелетной поперечно-полосатой мускулатуры, так и гладкой мускулатуры сосудов, кишечника, дых.путей и других органов с гладкомышечными клетками). Как мы помним, ЦМВ повреждает цитоскелет клеток, встраиваясь в них. Суть аутоиммунной реакции (после того, как иммунные барьеры пропустили много вирионов вируса внутрь организма) состоит в том, что вместе с антителами к антигенам вируса, синтезируются антитела и к пораженным компонентам клеток, к тем же микрофиламентам! Иммунная система старается уничтожить как можно больше пораженных клеток и антител к микрофиламентам становится много. Т.е для того, чтобы стать вич-позитивным, достаточно просто иметь снижение иммунитета и на его фоне заразиться тем же ЦМВ, вынужденно впустив много его вирионов в свой организм, или же получить реактивацию уже имеющегося в организме (он ведь у многих есть), а дальше, возникает аутоиммунная реакция и вич-положительность обеспечена. Чем больше вирионов было внедрено в организм, тем больше клеток они повредили и тем больше будет антител к их компонентам, в частности, актину. Когда иммунная система изначально сильна, то вирионы вторгнутся в меньшее кол-во клеток и аутоиммунная реакция (уничтожение инфицированных клеток иммунной системой) будет не такой масштабной.
Ещё один, третий сценарий течения ЦМВИ при сниженном иммунитете -поражение органов мочеполовой/мочевыводящей системы — проявляется в виде неспецифического и периодического воспаления (пиелонефрит, цистит). При этом, как и в случае бронхита и пневмонии, воспаления плохо поддаются лечению традиционными для данных заболеваний антибиотиками. У мужчин могут возникать уретриты (воспаление мочеиспускательного канала, сопровождается острой сильной болью при мочеиспускании) и орхиты (воспаления яичка); у женщин цервициты (воспаления и эрозии шейки матки), эндометрит, воспаления яичников.
Как поёт Елена Ваенга “а я узнала интересный момент, что и Ван Гог и Матис и Дали…” - антигены ЦМВ снова похожи с некоторыми антигенами ВИЧ в иммуноблоте! Как и больной ВЭБ-инфекцией на фоне снижения иммунитета из-за нарушения цитокинового ответа, больной ЦМВИ будет иметь антитела и к актиновым гликопротеидам и к некоторым другим антигенам, якобы вич, в иммуноблоте. Больные же ВЭБ и/или ЦМВИ без нарушения цитокинового ответа этих нарушений (антител к актину) иметь не будут, и вич-положительными по результатам блота не станут. При том их диагностировать гораздо легче, всё типично для мононуклеоза ВЭБ или для ЦМВИ. А те больные, что имеют неспецифические супрессии иммунитета, сниженную или изменённую продукцию цитокинов, редко бывают диагностированы как больные ВЭБ или ЦМВИ (диагностика их представляет огромные сложности - поражения внутренних органов нередко протекает под маской иных заболеваний [изначально вызванных ЦМВИ, например] и все диагностические и лечебные мероприятия сконцентрированы вокруг этих вторичных заболеваний. Выявленные при этом антитела igG класса интерпретируются как неактивное носительство, коим могут “похвастаться” очень многие, а анализы на igM к ЦМВ могут зачастую и вовсе не назначаться. Ещё одна сложность, что при ЦМВ поражении внутренних органов наиболее точной диагностической процедурой является взятие биопсии [кусочка ткани] из органа, что тоже не делается, т.к ЦМВ поражение не является обычно “главным подозреваемым”. Альтернатива биопсии - тщательный и скрупулёзный сбор анамнеза и детальное рассмотрение очень многих анализов - в рутинном конвейерном обследовании этого не делается, в формате рутинных обследований оцениваются лишь следствия, а положительные результаты антител на ЦМВ, если и приходят, то снова бывают оценены в качестве “имеющихся у всех”) но вот протестированы на ВИЧ все эти больные очень даже бывают…
Вот антигены ЦМВ

Хочу обратить внимание читателя на то, что цифра в обозначении антигена означает его молекулярную массу в килодальтонах (кДа). кДа = 1000 дальтонов или масса 1000 атомов водорода. При использовании разных тестовых систем и методик один и тот же белок может быть идентифицирован по своей мол.массе с погрешностью в 5000 атомов водорода или 5кДа. Т.е скажем, антиген р70, может быть обозначен в другой тест-системе как р66 или р72. Это касается всех вирусных антигенов.
Углубление в полиорганное поражение
Поражение внутренних органов при ЦМВИ включает в себя сочетание таких составляющих, как прямое поражение клеток самим вирусом, уничтожение иммунными клетками заражённых клеток (аутоиммунный процесс), присоединение бактериальной инфекции. Вариации доминирующей составляющей из этих трёх компонентов, обуславливают разное течение заболевания. В вариабельность вносятся ещё большие коррективы тем, что цитокиновый ответ, его скорость у всех людей различна (но одинаково не адекватна при дефиците важнейших веществ; длительных изматывающих болезнях; химических отравлениях хронического характера, как у лиц, злоупотребляющих спиртным и наркопотребителей, а также у всех , кто питается прохимиченными продуктами из магазина, особенно полуфабрикатами).
Так, у одного человека поражение почек при ЦМВИ приведёт к трудноподдающемуся лечению пиелонефриту , а у другого будет доминировать аутоиммунный комплекс и сформируется гломерулонефрит. У одного будет мягкий гепатит , у другого дойдёт до цирроза и печеночной недостаточности.
У одного разовьётся цмв-пневмония, у другого на этом фоне альвеолит, лёгочный фиброз и тд.
Наиболее частые поражения НЕ аутоиммунного характера при ЦМВИ это:
Цитомегаловирусный гепатит;
Цитомегаловирусный ретинит (воспаление сетчатки глаза) - способен привести к полной потере зрения;
Цитомегаловирусный колит (воспаление толстой кишки. Часто с перианальными язвами, в некоторых случаях с кровавыми включениями);
Цитомегаловирусный пневмонит (воспаление сосудов в альвеолах лёгких с развитием лёгочного фиброза и дыхательной недостаточности);
Цитомегаловирусный эзофагит (боль при глотании, мучительное чувство “комка в горле”, вплоть до потери возможности принимать пищу);
Полирадикулопатия (корешковый синдром, разновидность радикулита), поперечный миелит, и подострый энцефалит (в ряде случаев приводящий к медленно-прогрессирующей деменции).
Аутоиммунные:
Формирование реакции, которую затем идентифицируют в качестве гепатитов В и С;
Тяжёлая бронхиальная астма, ХОБЛ, лёгочный фиброз;
Неспецифический язвенный колит (НЯК) и болезнь Крона (б.К).
Читайте также:
- Aclon программа гепатита с
- Вирус z connect что это такое
- Ячмень это вирус герпеса
- Что действует на вирус папилломы человека
- Дайджин тест вирус папилломы человека что это
 Пожалуйста, не занимайтесь самолечением!При симпотмах заболевания - обратитесь к врачу.
Пожалуйста, не занимайтесь самолечением!При симпотмах заболевания - обратитесь к врачу.

