Тест системы для ифа диагностики гепатитов
Иммуносорбент – смесь синтетических и рекомбинантных HCV-антигенов, сорбированных в лунках планшета для ИФА 96-луночные разборные или цельные планшеты для ИФА из прозрачного бесцветного полистирола, сорбированные HCV-антигенами
Конъюгат (х51 концентрат) - моноклональные антитела мыши против IgG человека, меченные пероксидазой хрена Прозрачная жидкость сине-зелёного цвета
К+ - контрольный положительный образец инактивированный Прозрачная жидкость красного цвета
К- - контрольный отрицательный образец инактивированный Прозрачная жидкость жёлтого цвета
РИП - разбавитель исследуемых проб Прозрачная жидкость сине-фиолетового цвета
ФСР-Т (х25 концентрат) - фосфатно-солевой буферный раствор с твином-80 Прозрачная или опалесцирующая жидкость бесцветная или жёлтоватого цвета, допускается выпадение бесцветного кристаллического осадка
ЦБ – цитратный буферный раствор, содержащий Н2О2 Прозрачная бесцветная жидкость
ТМБ (х5 концентрат) – раствор 3,3',5,5'-тетраметилбензидина в димексиде
Стоп-реагент – 1 М раствор кислоты серной
Набор №1 рассчитан на проведение 192 определений, набор №2 рассчитан на проведение 96 определений, включая контрольные.
Набор реагентов предназначен для выявления антител к вирусу гепатита С в сыворотке (плазме) крови человека и препаратах крови.
Принцип метода
В основе метода лежит принцип непрямого твердофазного иммуноферментного анализа (ИФА) для выявления антител класса IgG к антигенам вируса гепатита С.
При внесении исследуемых или контрольных образцов в лунки планшета, антитела к вирусу гепатита С (анти-ВГС), в случае их наличия в образце, связываются с антигенами, иммобилизованными на твердой фазе, образуя иммунный комплекс антиген-антитело. Не связавшиеся антитела удаляют промыванием лунок. Внесение пероксидазного конъюгата моноклональных антител к IgG человека приводит к образованию комплекса антиген-антитело-конъюгат, на поверхности лунок планшета. Избыток конъюгата удаляют промыванием. Для выявления образовавшегося комплекса в лунки добавляют бесцветный субстратный раствор, в состав которого входит водорода перекись и хромоген (ТМБ). В результате
ферментативной реакции из водорода перекиси выделяется кислород, который переводит хромоген в окрашенную форму. Ферментативную реакцию останавливают внесением раствора кислоты серной. Измеряют оптическую плотность (ОП), величина которой зависит от концентрации анти-ВГС в образце.
Подготовка реагентов для ИФА
Все компоненты перед использованием выдержать не менее 30 мин при температуре от 18 до 25 °C. В случае выпадения кристаллов солей в ФСР-Т (х25 концентрат), прогреть его при температуре 37 °C до полного растворения осадка. Растворы готовить в зависимости от количества используемых стрипов иммуносорбента в соответствии с таблицей.
Рабочий раствор ФСР-Т хранить при температуре от 2 до 8 °C не более 3 сут. Рабочий раствор конъюгата и субстратный раствор готовить непосредственно перед применением. Не хранить. К+, К-, РИП и Стоп-реагент готовы к использованию.
После отбора необходимого количества оставшиеся концентраты реагентов и неиспользованные стрипы хранить плотно закрытыми в пакете в течение срока годности при температуре от 2 до 8 °C.
Подготовка к исследованию препаратов крови
Лиофилизированные препараты крови перед исследованием растворить в дистиллированной воде (если иное не указано в ФСП на препарат) и довести объем до номинального.
Все препараты иммуноглобулинов перед исследованием дополнительно развести рабочим раствором ФСР-Т до конечной концентрации белка:
- 10+1 мг/мл (для иммуноглобулинов внутривенного введения),
- 5+0,25 мг/мл (для иммуноглобулинов внутримышечного введения),
- 5+0,4 мг/мл (для иммуноглобулинов энтерального применения).
Растворенные препараты крови хранению не подлежат.
Проведение ИФА
Иммуносорбент перед использованием промыть 2 раза рабочим раствором ФСР-Т, заполняя лунки до краёв и удаляя промывающий раствор в ёмкость с дезинфицирующим раствором.
Во все лунки внести по 100 мкл РИП, добавить по 20 мкл контрольных или исследуемых образцов и перемешать пипетированием. При этом цвет раствора в лунках (за исключением К+) должен измениться с сине-фиолетового на сине-зеленый. При использовании 1 стрипа иммуносорбента контрольные образцы вносить каждый в 1 лунку. При использовании большего количества стрипов контрольные образцы внести не менее чем в 2 лунки каждый.
Планшет закрыть липкой лентой или крышкой и инкубировать при температуре 37 °C в течение 30-40 мин, затем промыть 5 раз как описано выше.
Во все лунки внести по 100 мкл рабочего раствора конъюгата, планшет закрыть липкой лентой или крышкой и инкубировать при температуре 37 °C в течение 30-40 мин, затем промыть 5 раз как описано выше.
Во все лунки внести по 100 мкл субстратного раствора, выдержать в течение 10-15 мин при температуре от 18 до 25 °C в защищённом от света месте, затем добавить по 50 мкл стоп-реагента и не позднее чем через 5 мин учесть результаты ИФА.
Учет и интерпретация результатов
Провести измерение оптической плотности (ОП) раствора в лунках иммуносорбента с помощью анализатора иммуноферментного при двух длинах волн. Тест-фильтр – 450 нм, референс-фильтр – 620-680 нм. Допускается одноволновое измерение при 450 нм.
Результаты оценивать, если среднее значение ОП в лунках с К- (ОПср.К-) не превышает 0,150, в лунках с К+ - не менее 1,000.
Исследуемые образцы, ОП которых не выше критического значения ОПкрит., оценивать как отрицательные. Образцы, ОП которых выше ОПкрит., оценивать как положительные. Значение ОПкрит. вычислять по формуле:
ОПкрит. = ОПср.К- + 0,150
Входящие в набор реагентов контрольные образцы инактивированы. Однако исследуемая сыворотка и плазма крови людей, а также растворы, оборудование и материалы, находящиеся с ними в контакте представляют собой потенциально инфекционный материал, и обращаться с ним следует осторожно: при работе использовать резиновые перчатки; оборудование, находившееся в контакте с биологическими образцами и реагентами, дезинфицировать до и после работы спирта этилового раствором 70 %; все использованные материалы обеззараживать водорода перекиси раствором 6 % или хлорамина Б раствором 3 % в течение 2 ч, или автоклавированием при (2,0±0,1) кгс/см2 ((0,20±0,01)МПа), температуре (132±2) °C в течение 60 мин; при работе с растворами ТМБ и кислоты серной не использовать пипетки с металлическими частями и избегать попадания этих растворов на кожный покров. Загрязненные участки кожи и слизистые оболочки обильно промывать водой.









Основные ссылки
Вы здесь
Кальво А., Дробченко С.Н., Сэмюэльс Ф. Бесприборные ИФА тест-системы для дифференциации гепатитов А, В, С. Инфекционные болезни: актуальные вопросы в клинике и эксперименте. Сборник научных трудов 13 Российской научно-практической конференции.- Махачкала, 2008. – С. 273 — 276.
БЕСПРИБОРНЫЕ ИФА ТЕСТ-СИСТЕМЫ ДЛЯ ДИФФЕРЕНЦИАЦИИ ГЕПАТИТОВ А, В, С
Дробченко С.Н., Кальво А., Сэмюэльс Ф.
При подозрении на вирусный гепатит на первом этапе лечащему врачу необходимо исключить острые вирусные гепатиты А, В, С. В случае подтверждения вирусного гепатита следующим этапом является определение соотношения маркеров вирусного гепатита с целью выявления стадии заболевания.
Для точной диагностики вирусных гепатитов крайне важно наиболее полное определение всего спектра серологических маркеров. Достижения в области молекулярной биологии, биотехнологии в последнее десятилетие ХХ века позволили создать новое поколение иммуноферментных бесприборных тест-систем ИммуноКомб, что значительно расширило возможности в диагностике вирусных гепатитов.
ИммуноКомб позволяет определить вид вирусного гепатита, перенес ли пациент гепатит в прошлом, силу иммунитета после перенесенной инфекции, есть ли инфекция в настоящее время, стадию гепатита, была ли сделана прививка против гепатита, силу прививочного иммунитета.
Типовой набор реагентов ИммуноКомб позволяет проводить анализ по единому плану, варьируя количество исследуемого образца, длительность и температуру инкубации в зависимости от типа набора. Единая схема проведения анализа для всех тест-систем ИммуноКомб упрощает процесс подготовки персонала и позволяет избежать ошибок.
Выявление IgM-антител к HBc указывает на острую фазу вирусного гепатита В, при этом HBs Ag может не определяться на самых ранних стадиях заболевания, т.к. его концентрация в крови незначительна. Определение HBs Ag и IgG-антител к HBc подтверждает хроническую фазу ВГВ. HBc IgG является единственным маркером во время, так называемого, серологического окна острого гепатита В - периода после исчезновения специфических IgM и до образования анти-HBs. Выявление антител к поверхностному антигену вируса гепатита В свидетельствует о развитии иммунитета к вирусу гепатита В.
В тест-системе ИммуноКомб HCV на разные точки одного зубца гребня нанесены высокоочищенные антигены HCV: отдельно core и неструктурные NS3, NS4, NS5. Благодаря этому решению ИммуноКомб HCV позволяет определять ранние анти-NS3, NS4, NS5 антитела так же хорошо, как и анти-коровые антитела, которые вынесены на отдельную точку на гребне, что играет значительную роль в правильном обнаружении ранней стадии гепатита С.
Дифференцированное выявление антител к структурным и неструктурным антигенам вируса гепатита С позволяет прогнозировать течение заболевания и определять более раннюю стадию заболевания. Обнаружение антител только к core-антигену свидетельствует об острой фазе заболевания. При хронизации процесса обнаруживаются антитела как к core-антигену, так и к неструктурным белкам.
Проведенные ВОЗ сравнительные испытания 10 быстрых простых тестов на HBsAg (Determine HBsAg, DoubleCheck HBs Antigen, ImmunoComb (ИммуноКомб) II HBs Ag 90’, Serodia-HBs.PA, Genelabs Diagnostics Rapid HBsAg, Hepacard, Advanced Quality One Step HBsAg Test, Uni-Gold HBsAg, Genedia HBsAg, Hep B Stat-Pack) показали, что чувствительность и специфичность этих тестов не уступает характеристикам ELISA тестов на HBsAg. ИммуноКомб II HBs Ag 90’ определял HBsAg на более ранних стадиях и в более низких концентрациях, чем другие тесты, участвовавшие в испытаниях. ИммуноКомб II HBs Ag 90’ выявлял антиген в образцах сероконверсионной панели в среднем на 1 сутки раньше, чем референс-тест Monolisa Ag HBs Plus. Все остальные тесты обнаруживали HBsAg, отставая от референс-теста, по крайней мере, на двое суток. Количество образцов низкотитражной панели, идентифицированных тестом ИммуноКомб, как содержащие HBsAg, совпадало с количеством образцов, выявленных референс-тестом Hepanostika HBsAg.
Проведенные во Франции международные испытания показали, что чувствительность и специфичность ИммуноКомб II HCV соответствует уровню наиболее высокочувствительных тестов Abbot, Ortho и составляет 100% и 99,5% соответственно. При исследовании сероконверсионных панелей было показано, что БПТ ИммуноКомб первым выявлял образцы более ранних стадий сероконверсий, превосходя показатели референс-теста (Био-Рад).
Современный период борьбы с вирусными гепатитами характеризуется началом массового применения вакцин против гепатитов В и А. При этом необходимо осуществлять как пред, так и пост-вакцинальный скрининг. ИммуноКомб HAV Ab и ИммуноКомб аnti-HВs позволяют количественно оценивать уровень антител в крови оперативно решать вопросы о необходимости вакцинации и ее результативности.
В Российской Федерации ИФА БПТ ИммуноКомб разрешены и успешно используется для скрининга и обследования доноров с 1992 года. Типовой набор реагентов ИммуноКомб (от 1 до 36 тестов) позволяет проводить анализ по единому плану, варьируя количество исследуемого образца и продолжительность инкубации в зависимости от типа тест-системы. Возможен как визуальный, так и автоматизированный учет количественных результатов. Такой унифицированный подход к диагностике вирусных гепатитов намного упрощает подготовку персонала и работу лаборатории в целом.
ИФА БПТ ИммуноКомб сертифицированы СЕ и широко используются более чем в ста странах мира. Как достоверные, высокочувствительные и специфичные тесты ИммуноКомб отобраны для программ ВОЗ, UNAIDS, Красного Креста. Минздравсоцразвития рекомендует ИФА БПТ ИммуноКомб для обследования доноров крови, органов и тканей человека, скрининговых исследований; для подтверждения результатов скрининговых исследований (приказ № 292 от 30.07.2001г., № 322 от 21.10.2002г., № 336 от 07.09.2000г.).
МИНИСТЕРСТВО ЗДРАВООХРАНЕНИЯ РОССИЙСКОЙ ФЕДЕРАЦИИ
от 31 декабря 1997 года N 392
О проведении сравнительных испытани1
диагностических иммуноферментных тест-систем
для диагностики гепатита В и С
В настоящее время для диагностики гепатита В и С широко применяются тест-системы отечественного производства для массового скрининга на наличие НВsАg и анти-ВГС.
Вместе с тем с 1994 года отмечены признаки значительного ухудшения эпидемической обстановки по гепатиту В и С. Рост числа регистрируемых случаев острого гепатита В и С в большинстве регионов России определяется прежде всего за счет вовлечения в эпидемический процесс возрастных групп 15-29 лет. Обеспечение максимально полного выявления лиц с наличием НВsАg и анти-ВГС позволит предотвратить передачу гепатита В и С через донорскую кровь, другие биологические жидкости и ткани.
Сложившаяся ситуация требует проведения оценки применяемых в здравоохранении диагностических тест-систем, предназначенных для выявления НВsАg и анти-ВГС.
В целях повышения эффективности диагностики гепатита В и С
приказываю:
1. Провести в 1 квартале 1998 года сравнительные испытания диагностических иммуноферментных тест-систем для выявления НВsАg и анти-ВГС в сыворотке крови человека, включенных в перечень иммуноферментных тест-систем для выявления НВsАg и анти-ВГС, выпускаемых предприятиями, участвующими в проведении испытаний (Приложение 1).
2. Испытание диагностических иммуноферментных тест-систем провести в соответствии с инструкцией (Приложение 2).
3. Назначить базой для проведения испытания НИИ эпидемиологии и микробиологии им. Н.Ф.Гамалеи РАМН и Санкт-Петербургский НИИ эпидемиологии и микробиологии им. Л.Пастера.
4. Государственному НИИ стандартизации и контроля медицинских иммунобиологических препаратов им. Л.А.Тарасевича, НИИ эпидемиологии и микробиологии им. Н.Ф.Гамалеи РАМН и Санкт-Петербургскому НИИ эпидемиологии и микробиологии им. Л.Пастера сформировать и предоставить для проведения испытаний стандартные контрольные панели в необходимом количестве.
5. Финансирование работ, связанных с проведением испытаний диагностических иммуноферментных тест-систем, обеспечить за счет производителей диагностических иммуноферментных тест-систем, участвующих в сравнительном испытании.
6. Комиссии по организации и проведению сравнительных испытаний диагностических иммуноферментных тест-систем для выявления НВsАg и анти-ВГС в сыворотке крови человека (Приложение 3) по результатам испытаний представить в Минздрав России отчет и рекомендации по дальнейшему использованию испытанных тест-систем в диагностической практике к 01.04.97.
7. Контроль за выполнением настоящего приказа возложить на руководителя Департамента Госсанэпиднадзора Минздрава России Монисова А.А.
Первый заместитель Министра
Г.Г.Онищенко
Приложение 1
к приказу Минздрава России
от 31 декабря 1997 года N 392
Перечень
предприятий и производимых ими наборов иммуноферментных тест-систем
для выявления НВsАg и анти-ВГС*, участвующих в проведении испытаний
* Подтверждающий тест при его наличии должен быть представлен в Комиссию.
1. "Аквапаст" Санкт-Петербург
2. "Диагностические препараты" Нижний Новгород
3. "Имбио" Нижний Новгород
4. "Мультитест" Москва
5. "Ниармедик" Москва
6. "Биосервис" Калужская область
7. "Вектор Бест" Новосибирск
8. "Алкор Био" Санкт-Петербург
9. "Предприятие по производству бактерийных препаратов Санкт-Петербург"
10. "Эколаб" Московская область
11. "Брынцалов" Москва
12. Отдел новых технологий НИИ эпидемиологии и микробиологии им. Л. Пастера, Санкт-Петербург
13. "Авиценна" Москва
14. "Диаплюс" Москва
2. Роше -Диагностика Швейцария
3. Диагностик Пастер Франция
4. Органон Техника Голландия
5. Лабсистем Финляндия
7. Кайрон США (Орто)
8. Берингер Манхейм Германия
9. Мюрекс Великобритания
10. Дженелабс Диагностик Швейцария
11. Ордженикс Израиль
Руководитель Департамента
госсанэпиднадзора
А.А.Монисов
Приложение 2
к приказу Минздрава России
от 31 декабря 1997 года N 392
Инструкция
по проведению испытаний диагностических
иммуноферментных тест-систем для выявления НВsАg
и Анти-ВГС в сыворотке крови человека
1. Изучаемые препараты: наборы иммуноферментных тест-систем предприятий, зарегистрированных в качестве участников данных испытаний.
В испытании должны быть изучены по 2 набора одной серии тест-систем:
N 1 - прошедший контроль в государственном НИИ стандартизации и контроля медицинских иммунобиологических препаратов им.Л.А.Тарасевича:
N 2 - поступивший с мест применения (из диагностических лабораторий различного уровня).
При проведении испытаний используются тест-системы отечественного и зарубежного производства, имеющие разрешение на применение в Российской Федерации.
Все тест-системы должны быть испытаны в пределах срока годности, указанного на наборе.
Условия хранения наборов: +2 + 8° С.
2. Материалы для исследования:
2.1. Контроль диагностических препаратов для выявления НВsАg:
- стандартный препарат высокоочищенного антигена (ОСО, сер. N) должен быть представлен в Государственный НИИ стандартизации и контроля медицинских иммунобиологических препаратов им. Л.А.Тарасевича;
- панель сывороток с низкой концентрацией НВsАg фирмы ВВJ N АF (15 образцов);
- панель сывороток для оценки чувствительности при выявлении НВsАg фирмы ВВJ N АF (21 образец);
- сыворотки крови больных острым гепатитом В (подтвержденные выявлением НВsАg при постановке диагноза) на 30-40-й день после госпитализации в инфекционный стационар должны быть представлены 1-й инфекционной больницей г.Москвы и больницей им. С.П.Боткина г.Санкт-Петербурга;
- сыворотки крови больных, находящихся на лечении в отделении хронического гемодиализа, должны быть представлены клинической больницей им. Боткина г.Москвы и клинической больницей им. Эрисмана г.Санкт-Петербурга;
- сыворотки крови здоровых доноров, не содержащие НВsАg.
2.2. Контроль диагностических препаратов для выявления анти-ВГС:
- стандартная панель сывороток крови человека, содержащая антитела к ВГС (ОСО, сер. N), должна быть представлена Государственным НИИ стандартизации и контроля медицинских иммунобиологических препаратов им. Л.А.Тарасевича;
- серо-конверсионная панель ВГС-позитивных сывороток производства фирмы В ВJ N АF (9 образцов);
- панель сывороток с низкой концентрацией антител к анти-ВГС фирмы ВВJ N АF (15 образцов);
- стандартная панель сывороток крови человека, не содержащая антитела к ВГС, должна быть представлена Государственным НИИ стандартизации и контроля медицинских иммунобиологических препаратов им. Л.А.Тарасевича;
- сыворотки крови больных хроническим гепатитом С, позитивных по РНК-ВГС, должны быть представлены 1-й инфекционной больницей г.Москвы и больницей им. С.П.Боткина г.Санкт-Петербурга;
- сыворотки крови больных, находящихся на лечении в отделении хронического гемодиализа, должны быть представлены клинической больницей им. Боткина г.Москвы и клинической больницей им. Эрисмана г.Санкт-Петербурга;
- сыворотки крови здоровых доноров, не содержащие антител к ВГС.
Все вышеперечисленные сыворотки должны быть предварительно паспортизированы, иметь полную характеристику по ИФА и иммунному блоттингу.
3. Условия проведения испытания:
Все сыворотки, кроме ОСО Государственного НИИ стандартизации и контроля медицинских иммунобиологических препаратов им. Л.А.Тарасевича, должны быть зашифрованы. Информация по шифрам хранится в отделе профилактики ВИЧ/СПИД департамента Госсанэпиднадзора Минздрава России.
Испытания должны проводиться на двух планшетах каждого набора:
- по одному планшету наборов N 1 и N 2 необходимо использовать для проведения контроля с помощью стандартных панелей Государственного НИИ стандартизации и контроля медицинских иммунобиологических препаратов им. Л.А.Тарасовича (сер.N и сер. N), постановка контрольного опыта должна проводиться в соответствии с инструкциями по применению тест-системы и стандартных панелей;
- по результатам испытаний определяются основные показатели качества тест-систем: чувствительность и специфичность;
- вторые планшеты наборов N 1 и N 2 необходимо использовать для постановок шифрованных сывороток, постановку опыта и учет результатов проводить в соответствии с инструкцией по применению тест-систем;
- после расшифровки полученных результатов испытуемые тест-системы оцениваются по способности выявления сывороток в соответствии с их паспортными характеристиками.
Наборы N 1 и N 2 каждой тест-системы должны быть исследованы параллельно в НИИ эпидемиологии и микробиологии им. Н.Ф.Гамалеи РАМН и НИИ эпидемиологии и микробиологии им. Л.Пастера.
По каждому опыту испытаний должен быть составлен протокол, к которому прилагается распечатка со спектрофотометра.
Анализ полученных результатов проводится комиссией. По результатам испытаний составляется отчет, разрабатываются рекомендации по качеству каждой тест-системы и возможности ее использования для выявления НВsАg и анти-ВГС.
Испытания должны быть проведены на базе лаборатории индикации НИИ эпидемиологии и микробиологии им. Н.Ф.Гамалеи РАМН и НИИ эпидемиологии и микробиологии им. Л.Пастера, Санкт-Петербург.
Исполнители работ - сотрудники этих учреждений.
Руководитель Департамента
госсанэпиднадзора
А.А.Монисов
Приложение 3
к приказу Минздрава России
от 31 декабря 1997 года N 392
Состав
комиссии и рабочей группы по организации и проведению сравнительного испытания диагностических иммуноферментных тест-систем для выявления поверхностного антигена вируса гепатита В (НВsАg) и антител к вирусу гепатита С (анти-ВГС) в сыворотке или плазме крови человека

Иммуноферментный анализ (ИФА) — метод лабораторной диагностики, позволяющий обнаруживать специфические антитела и антигены при самых разных патологиях.
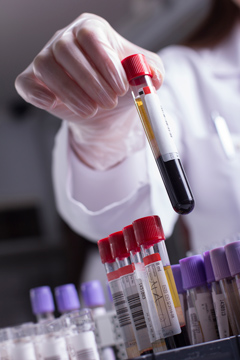
ИФА — один из самых распространенных и точных методов для выявления инфекций, передающихся половым путем, в частности ВИЧ, ВПЧ, гепатита В.

Для того чтобы результаты анализов были максимально достоверными, необходимо правильно подготовиться к их сдаче.

Спецпредложения, скидки и акции помогут существенно сэкономить на медицинском обследовании.
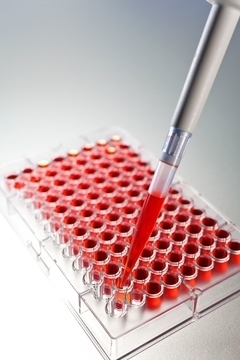
Контроль качества лабораторных исследований, осуществляемый по международным стандартам, — дополнительная гарантия точности результатов анализов.
Современная диагностика в медицине немыслима без высокочувствительных лабораторных анализов. Прежде для установления причин тех или иных симптомов врачи были вынуждены ориентироваться на косвенные признаки болезни, а также проводить многоступенчатые микроскопические исследования в попытке обнаружить возбудителя инфекции. Сегодня достаточно одного-единственного теста — такого как иммуноферментный анализ — чтобы подтвердить или опровергнуть первоначальный диагноз.
Основные понятия и принцип метода иммуноферментного анализа
Существует несколько разновидностей антител, каждая из которых вступает в действие на определенном этапе иммунного ответа. Так, первыми в ответ на проникновение антигена в организм синтезируются иммуноглобулины класса М (IgM). Содержание этих антител наиболее высоко в первые дни инфекционного процесса.
Следом за ними иммунная система выбрасывает в кровь иммуноглобулины класса G (IgG), которые помогают уничтожать антигены до полной победы над инфекцией, а также продолжают циркулировать по сосудам в дальнейшем, обеспечивая иммунитет к повторному заражению. На этом явлении основана вакцинация: благодаря прививкам, содержащим ослабленные антигены микробов и вирусов, в нашей крови появляется большое количество IgG, которые при контакте с реальной угрозой быстро подавляют инфекцию — до того, как она нанесет вред здоровью.
Как узнать, какие именно антигены или антитела присутствуют в организме человека? Когда врач предполагает, что причиной заболевания является определенная инфекция, или желает измерить концентрацию определенного гормона, он назначает пациенту иммуноферментный анализ.
ИФА бывает качественным и количественным. В первом случае подразумевается однозначный ответ: искомое вещество или найдено, или не найдено в образце. В случае с количественным анализом более сложная цепь реакций дает возможность оценить концентрацию антител в крови человека, что в сравнении с результатами предыдущих тестов даст ответ на вопрос о том, как развивается инфекционный процесс.
Бесспорные преимущества ИФА — высокая чувствительность и специфичность метода. Чувствительность — это возможность распознать искомое вещество, даже если его концентрация в образце невысока. Специфичность же подразумевает безошибочность диагностики: если результат положительный, значит, найдены именно те антитело или антиген, которые предполагались, а не какие-то другие.
Высокая степень технологичности проведения иммуноферментного анализа минимизирует влияние человеческого фактора, что снижает вероятность ошибки. Большинство используемых в современных лабораториях тест-систем и реактивов для ИФА выпускаются в промышленных условиях, что гарантирует точный результат.
В случае диагностики инфекционных заболеваний иммуноферментный анализ не может найти возбудителя и определить его специфичные свойства: он лишь указывает на наличие антител в крови у больного, косвенно свидетельствующих о присутствии чужеродного микроорганизма в теле человека.
ИФА — крайне точный, но не дешевый метод, поэтому обращаться к нему нужно с умом, а интерпретацией результатов должен заниматься квалифицированный врач.
Невозможно охватить полный список показаний к проведению ИФА. Вот наиболее распространенные цели анализа:
- Диагностика острых и хронических инфекционных заболеваний:
- IgM и IgG к вирусным гепатитам А, B, C, E, а также антигенов гепатитов В и С;
- IgG к ВИЧ;
- Ig M и IgG к цитомегаловирусной инфекции;
- Ig M и IgG к вирусу Эпштейна-Барр;
- Ig M и IgG к герпетическим инфекциям;
- Ig M и IgG к токсоплазмозу;
- Ig M и IgG к кори, краснухе, сальмонеллезу, дизентерии, клещевому энцефалиту и другим заболеваниям;
- IgG к паразитарным заболеваниям;
- Ig M и IgG к инфекциям, передающимся половым путем;
- IgG к хеликобактерной инфекции.
- Общая оценка показателей иммунитета человека и маркёров некоторых аутоиммунных заболеваний.
- Выявление онкологических маркёров (фактора некроза опухоли, простатспецифического антигена, раково-эмбрионального антигена и других).
- Определение содержания гормонов в сыворотке крови (прогестерона, пролактина, тестостерона, тиреотропного гормона и других).
Основной биоматериал для проведения ИФА — это сыворотка крови: в лаборатории у пациента берут образец крови из вены, из которого в дальнейшем удаляют форменные элементы, затрудняющие проведение анализа. В некоторых других случаях для анализа используется спинномозговая жидкость, околоплодные воды, мазки слизистых оболочек и т.д.
Для того чтобы избежать искажений в результатах, рекомендуется сдавать кровь натощак, а за две недели до исследования (если целью является диагностика хронических, скрыто протекающих инфекционных заболеваний) необходимо отказаться от приема антибиотиков и противовирусных препаратов.
При наличии необходимых реактивов и хорошей организации работы лаборатории результат анализа вы получите в течение 1–2 суток после забора крови. В некоторых случаях, при необходимости получения экстренного ответа, этот срок может быть сокращен до 2–3 часов.
- IgM — наличие этого класса иммуноглобулинов говорит об остром инфекционном процессе в организме. Отсутствие IgM может говорить как об отсутствии конкретного возбудителя в организме, так и о переходе инфекции в хроническую стадию.
- IgA при отрицательном результате теста на IgM чаще всего свидетельствует о хронической или скрыто протекающей инфекции.
- IgM и IgA (совместное присутствие) — два положительных результата говорят о разгаре острой фазы заболевания.
- IgG говорит либо о хронизации заболевания либо о выздоровлении и выработке иммунитета к инфекционному агенту.
В зависимости от содержания анализа в бланке могут быть представлены данные в виде таблицы с перечислением всех антител или антигенов с пометками об отрицательной или положительной реакции, либо будет указано количественное значение результата (отрицательный, слабоположительный, положительный или резко положительный). Последний вариант определяет, сколько антител содержится в анализируемом образце.
Еще один количественный показатель — индекс авидности антител, выраженный в процентах. Он указывает, сколько времени прошло от начала инфекционного процесса (чем выше индекс — тем больше).
Сегодня выпускаются тысячи видов тест-систем ИФА, позволяющих обнаруживать специфические антитела и антигены при самых разных патологиях. Поэтому этот анализ используется практически во всех медицинских отраслях. Диагноз, поставленный с помощью ИФА, — это гарантия назначения адекватной терапии и эффективного лечения заболевания.
Информативность ИФА делает этот анализ важным инструментом в работе многих медицинских центров. Но можно ли доверять такую диагностику государственным лабораториям или лучше самим выбрать, где провести такое исследование?
Читайте также:



