При цитомегаловирусе может быть эпилепсия или нет
*Импакт фактор за 2018 г. по данным РИНЦ
Журнал входит в Перечень рецензируемых научных изданий ВАК.

Читайте в новом номере
Цитомегаловирусная инфекция (ЦМВИ) характеризуется широким распространением в популяции и разнообразием клинических форм. Если при постнатальном инфицировании тяжелое течение заболевания отмечается только на фоне выраженных дисфункций иммунитета, то при врожденной ЦМВИ существует высокий риск повреждений плода с возможным развитием неблагоприятных исходов, а у выживших — различных нарушений состояния здоровья. Врожденная ЦМВИ является одной из наиболее частых внутриутробных инфекций в мире. Источником инфекции для плода практически всегда является мать, переносящая во время беременности ЦМВИ. В статье представлены литературные данные, свидетельствующие о безопасности, эффективности и высокой профилактической результативности гипериммунного антицитомегаловирусного иммуноглобулина для внутривенного введения (анти-ЦМВ-ИГВВ) при его использовании в лечении беременных женщин с ЦМВИ. В России данный препарат зарегистрирован под торговым названием НеоЦитотект. Применение гипериммунного анти-ЦМВ-ИГВВ при активной ЦМВИ у беременных позволяет существенно снизить трансплацентарную трансмиссию ЦМВ и развитие врожденной ЦМВИ. Также возможно применение анти-ЦМВ-ИГВВ в качестве этиотропного препарата для лечения врожденной ЦМВИ у детей раннего возраста, что позволяет существенно снизить вероятность осложнений, особенно при использовании в комбинации с противовирусными препаратами.
Ключевые слова: цитомегаловирус, цитомегаловирусная инфекция, внутриутробная инфекция, антицитомегаловирусный иммуноглобулин, НеоЦитотект, антенатальная профилактика.
Для цитирования: Заплатников А.Л., Шахгильдян В.И., Подзолкова Н.М., Ефимов М.С., Шипулина О.Ю., Карасева Л.Н., Подкопаев В.Н., Домонова Э.А., Дементьев А.А., Чабаидзе Ж.Л. Возможно ли предупредить последствия врожденной цитомегаловирусной инфекции? (взгляд акушера-гинеколога, инфекциониста и неонатолога). РМЖ. Медицинское обозрение. 2018;10:45-50.
Is it possible to prevent the consequences of congenital cytomegalovirus infection? (the opinion of the obstetrician-gynecologist, neonatologist and infectiologist)
A.L. Zaplatnikov 1,2 , V.I. Shakhgildyan 3 , N.M. Podzolkova 1 , M.S. Efimov 1 , O.Yu. Shipulina 3 , L.N. Karaseva 2 , V. N. Podkopaev 1,2 , E.A. Domonova 3 , A.A. Dementiev 1 , Zh.L. Chabaidze 1
1 Russian Medical Academy of Continious Professional Training
2 Bashlyaeva Children’s Municipal Clinical Hospital, Moscow
3 Central Research Institute of Epidemiology, Moscow
Cytomegalovirus infection (CMVi) is characterized by a wide distribution in the population and a variety of clinical forms.
If during postnatal infection a severe course of the disease is observed only against the background of pronounced immunity dysfunctions, then with congenital CMVi there is a high risk of fetal damage with possible adverse events, and in survived there are various health disorders. Congenital CMVi is one of the most frequent intrauterine infections in the world. A source of infection for the fetus is almost always a mother who carries CMVi during pregnancy. The article presents literature data indicating the safety, efficacy, and high prophylactic performance of a hyperimmune anti-cytomegalovirus immunoglobulin for intravenous administration (anti-CMV-IGIV) when used in the treatment of pregnant women with CMVi. In Russia, this drug is registered under the trade name NeoCytotect. An application of hyperimmune anti-CMV-IGIV with active CMVi in pregnant women can significantly reduce the transplacental transmission of CMV and the development of congenital CMVi (antenatal prophylaxis). It is also possible to use anti-CMV-IGIV as an etiotropic drug for treating congenital CMVi in young children, which can significantly reduce the likelihood of complications, especially when used in combination with antiviral drugs.
Key words: cytomegalovirus, cytomegalovirus infection, intrauterine infection, anti-cytomegalovirus immunoglobulin, NeoCytotect, antenatal prophylaxis.
For citation: Zaplatnikov A.L., Shakhgildyan V.I., Podzolkova N.M. et al. Is it possible to prevent the consequences of congenital cytomegalovirus infection? (the opinion of the obstetrician-gynecologist, neonatologist and infectiologist) // RMJ. Medical Review. 2018. № 10. P. 45–50.
В статье представлены литературные данные, свидетельствующие о безопасности, эффективности и высокой профилактической результативности гипериммунного антицитомегаловирусного иммуноглобулина для внутривенного введения при его использовании в лечении беременных женщин с цитомегаловирусной инфекцией.

Учитывая изложенное выше, следует сделать вывод, что перенесенная женщиной в период беременности ЦМВИ (как первичная, так и вторичная) характеризуется высоким риском неблагоприятного воздействия на плод и последующее развитие ребенка. Особо при этом необходимо отметить, что в подавляющем большинстве случаев ЦМВИ в период беременности остается нераспознанной, т. к. нередко протекает субклинически [18, 19, 21–24]. В связи с этим активно обсуждается необходимость проведения скрининга беременных женщин для раннего выявления у них ЦМВИ [18, 25]. При этом в ряде стран Европы, а также в Австралии, Израиле и в некоторых штатах США скрининг, проводимый в рамках популяционных исследований или локальных протоколов, показал высокую эффективность [18, 26–28]. В то же время существует мнение экспертов о необязательности рутинного обследования женщин на ЦМВИ в период беременности [29]. При этом в качестве аргумента указанной рекомендации представлен факт отсутствия общепризнанных способов эффективного и безопасного лечения ЦМВИ во время беременности, однако имеющиеся в литературе данные свидетельствуют о безопасности, эффективности и высокой профилактической результативности гипериммунного антицитомегаловирусного иммуноглобулина для внутривенного введения (анти-ЦМВ-ИГВВ) при его использовании в лечении беременных женщин с ЦМВИ [30–34]. Во всех указанных случаях был использован гипериммунный анти-ЦМВ-ИГВВ, который в нашей стране зарегистрирован под торговым названием НеоЦитотект [35].
НеоЦитотект является гипериммунным анти-ЦМВ-ИГВВ, который изготовлен из плазмы доноров с высоким титром антител против возбудителя ЦМВИ. В 1 мл препарата содержится 50 мг белков плазмы человека, которые не менее чем на 96% представлены IgG. При этом распределение подклассов IgG соответствует их распределению в плазме здоровых доноров. Антицитомегаловирусная активность 1 мл препарата соответствует 100 анти-ЦМВ единиц (определено по эталонному препарату Института Пауля Эрлиха, Германия) [36]. Высокая эффективность гипериммунного анти-ЦМВ-ИГВВ отмечена как при профилактическом его назначении (у пациентов после трансплантации органов, с подавленным иммунитетом и др.), так и при лечении активной ЦМВИ. При этом было отмечено, что для достижения аналогичного эффекта доза стандартного иммуноглобулина должна превышать дозу НеоЦитотекта более чем в 11 раз [37].
Установлено, что применение гипериммунного анти-ЦМВ-ИГВВ в случаях выявления активной ЦМВИ у женщин во время беременности позволяет существенно снизить трансплацентарную трансмиссию ЦМВ и развитие врожденной ЦМВИ [30–34]. Особый интерес представляют результаты исследований G. Nigro et al. (2005) и К.О. Kagan et al. (2018) [30, 34]. Так, G. Nigro et al. (2005) наблюдали за 181 беременной женщиной с верифицированной первичной ЦМВИ, которым для снижения риска внутриутробного инфицирования плода и развития врожденной ЦМВИ была предложена терапия гипериммунным анти-ЦМВ-ИГВВ [30]. Добровольное информированное согласие на лечение было получено у 68 женщин, которые составили основную группу. В группу сравнения вошли беременные женщины с первичной ЦМВИ, отказавшиеся от терапии (n=58) (рис. 1). 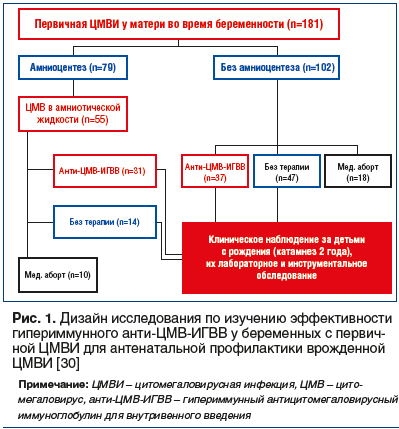
Анализ эффективности гипериммунного анти-ЦМВ-ИГВВ проводили на основании результатов сравнения частоты внутриутробной ЦМВИ у детей, рожденных в исследуемых группах. Катамнез наблюдения за детьми составил 2 года. Оказалось, что применение гипериммунного анти-ЦМВ-ИГВВ позволило в целом более чем в 5 раз снизить частоту врожденной ЦМВИ (p Литература
Только для зарегистрированных пользователей
ЦИТОМЕГАЛОВИРУС
Что надо знать о ЦМВ инфекции.
ЦИТОМЕГАЛОВИРУС
Цитомегаловирус – представитель семейства герпесвирусов,которое включает вирусы простого герпеса,вируса ветряной оспы и вирус Эпштейна-Бара (возбудителя инфекционного мононуклеоза).Вирус цитомегаловируса широко распространен во всем мире во всех социально-экономических группах,но более часто встречается в развивающихся странах в областях с низким уровнем социально-экономического развития.
Вирус обнаруживают в различных биологических жидкостях организма человека,включая мочу,слюну,грудное молоко,кровь,слезы,сперму и влагалищное отделяемое.
Однажды попав в организм вирус в большинстве случаев остается там на всю жизнь.
Наиболее часто инфицрование вирусом никак не проявляется.
Цитомегаловирус может вызвать смерть и заболевание у плода и новорожденных,заболевания у людей с ослабленной иммунной системой (у людей подвергшихся трансплантации(пересадки) органов,больных СПИДом и онкологических больных)
Около 80% взрослого населения моложе 40 лет инфицированы вирусом цитомегалии.
Приблизительно 1из 150 детей рождается с врожденной цитомегаловирусной инфекцией.
Приблизительно 1 из 750 детей рождается с заболеваниям,связанными с инфицированием цитомегаловирусом.
ПЕРЕДАЧА И УСЛОВИЯ ЗАРАЖЕНИЯ
Передача цитомегаловируса происходит от человека к человеку через контакт с инфицированной биологической жидкостью (моча, слюна (слюна), грудное молоко, кровь, слезы, сперма, и влагалищое отделяемое) но вероятность инфицирования при однократном случайном контакте ничтожна мала.
Приблизительно от 1% до 4 % беременных женщин инфицируются цитомегаловирусом во время беременности,у одной трети из них происхождит внутриутробное заражение плода.
Никакие меры не могут полностью исключить риск внутриутробного заражения,но простые правила (о них ниже) могут существенно снизить его риск.
СИМПТОМЫ ЦИТОМЕГАЛОВИРУСНОЙ ИНФЕКЦИИ
Большинство здоровых детей и взрослых,инфицированных ЦМВ не имеют никаких симптомов инфекции и даже не подозревают что они заражены.
Симптомы могут проявлятся в виде повышения температуры,усталости,воспаления глотки,увелечением небных миндалин,но эти симптомы присущи и многим другим инфекционным болезням, поэтому большинство людей не может вспомнить, когда они заразились цитомегаловирусом.
У большинства новорожденных с врожденной цитомегаловирусной инфекцией никогда не развиваются симптомы ЦМВ,у некоторых отмечаются так называемые временные проявления,которые со временем бесследно исчезают,а у незначительного количества признаки врожденной ЦМВ выражены и остаются на всю жизнь.
Временные симптомы ЦМВ у новорожденных:
1. Поражение печени
2. Поражение селезенки
3. Желтуха (кожа и слизистая глаз)
4. Пятнистая сыпь на коже (синюшно-фиолетового цвета)
5. Поражение легких
6. Низкий вес
Постоянные симптомы ЦМВ у новрожденных
1. Потеря слуха
2. Потеря зрения
3. Умственная отсталость
4. Маленькая голова
5. Нарушение координации
6. Смерть
У некоторых детей постоянные признаки ЦМВ не проявляются сразу после рождения,а возникают через несколько месяцев и даже лет.Наиболее часто это потеря слуха и зрения.
Поэтому важно знать произошло ли инфицирование новорожденного цитомегаловирусом для того чтобы в первые месяцы и годы его жизни проводить регулярное исследование его слуха и зрения.
ЦМВ и беременность.
ДИАГНОСТИКА ЦМВ У БЕРЕМЕННЫХ И НОВОРОЖДЕННЫХ
В настоящее время в мире не рекомендуется проверка всех беременных женщин на наличие ЦМВ (в России по приказу№50 она обязательна). Исследование может помочь вам узнать заражались ли вы когда - нибудь эти вирусом. Исследование на так называемые антитела IgG покажет,выработались ли в вашем организме антитела против цитомегаловируса.Если вы беременная и имеете положительные антитела IgG против цитомегаловируса то шанс передачи вируса от вас плоду является ничтожным малым,если вы не заразились ЦМВ за предшествующие беременности несколько месяцев.Другие исследования - на антитела IgM и авидные IgG могут помочь определить давность заражения вирусом.
Если у беременной не выявлены антитела IgG против цитомегаловируса и нет других видов антител (IgM и авидных IgG) то ребенок имеет высокий шанс заразиться во время беременности, если произойдет инфицирование матери. Поэтому беременные с отсутствием (отрицательными результатами) антител против цитомегаловируса должны проявлять осторожность при контакте с маленькими детьми,так как у них часто (до 40%) обнаруживают цитомегаловирус в слюне и моче. Самые простые правила – не целовать детей в губы и после контакта с ними тщательно вымыть руки.
Если наблюдающий беременную врач решит,что она заразилась цитомегаловирусом во время беременности,это совсем не означает,что будущий ребенок будет заражен.В этих случаях возможно проведение более тщательных обследований (амниоцентез) для того, чтобы узнать заражен ли плод или нет.В подавляющем большинстве случаев дети, рожденные с ЦМВ, развиваются обычно.По этим причинам исследование на ЦМВ как обязательное не рекомендуется.
Исследование на ЦМВ при планировании беременности
Если вы планируете беременность,то исследование на ЦМВ поможет вам в оценить насколько надо быть осторожной во время беременности в отношении ЦМВ.
Если у вас положительный тест на IgG,то вы будете знать,что есть ничтожный шанс внутриутробной цитомегаловирусной инфекции,если тест на IgG отрицательный,то тщательно следуйте изложенным в этой статье рекомендациям.
Если вы узнали,что инфицированы ЦМВ впервые в течении вашей беременности, вы должны удостовериться инфицирован ли ребенок после родов. Диагноз врожденной цитомегаловирусной инфекции новорожденному ставиться в том случае, когда у него из мочи,крови,слюны непосредственно выделен цитомегаловирус (методом ПЦР или культуральным методом) в течении 3 недель после рождения. Исследование на антитела (IgM,IgG) для постановки диагноза не применяется. Наиболее часто дети,инфицированные во время беременности развиваются как нормальные дети, но в течении первых лет жизни вы должны регулярно проверять его зрение и слух.
В настоящее время нет никаких лекарств и вакцин способных предотвратить внутриутробное заражение плода цитомегаловирусом.
Есть данные,что применение препарата ганцикловир может предотвратить потерю слуха у детей с врожденным ЦМВ, но этот препарат имеет серьезные побочные действия и должен назначаться при угрожающих жизни состояниях.
ЦМВ и беременность.
ЧАСТЫЕ ВОПРОСЫ И ОТВЕТЫ
--Как я могу узнать,заражалась ли я когда нибудь ЦМВ ?
Исследование на атитела IgG в случае положительного результата может определить что вы заражались когда нибудь цитомегаловирусной инфекцией,но оно не покажет инфицированы вы в течении беременности и не определит заражен ли ЦМВ плод.
При отрицательных результатах исследования на антитела IgG против цитомегаловируса вы должны проявлять осторожность для предотвращения инфицированием ЦМВ во время беременности.
--Как я могу узнать,инфицирована ли я ЦМВ во время беременности ?
Об этом можно узнать,проводя исследование на антитела IgG через определенный промежуток времени.Если первое обследование показало отрицательный результат,а второе положительный то вы инфицировались вирусом во время беременности.Есть исследование,которое может определить заражение во время беременности с помощью однократного обследование (определение авидных IgG).Другим способом является определение антител IgM, которые существуют в крови в течении 30-60 дней после первичного заражения вирусом,а затем исчезают.Исследование необходимо проводить совместно с определением антител IgG/
--Как я могу узнать инфицирован ли плод ?
Так как в настоящее время нет никаких эффективных препаратов для лечения инфицированных ЦМВ беременных женщин ,то нет никакого смысла проводить исследования для определения заражен ли плод.Обследования иногда проводятся у беременных женщин с первичным заражением ЦМВ во время беременности,так как они с высоким риском (33 %) могут передать вирус плоду .Исследование амниотической жидкости или крови эмбриона совместно с ультразвуковым обследованием часто может выявить заражен ли плод ЦМВ или нет.Однако эти обследования опасны и не всегда точны.
--Как я могу узнать, имеет ли новорожденный врожденную цитомегаловирусную инфекцию?
Диагноз врожденной цитомегаловирусной инфекции новорожденному ставиться в том случая когда у него из мочи,крови,слюны непосредственно выделен цитомегаловирус (методами ПЦР или культуральным методом) в течении 3 недель после рождения. Исследование на антитела (IgM,IgG) для постановки диагноза не применяется.
Если вашему ребенку установлен диагноз врожденной ЦМВ вы регулярно должны проводить обследование его слуха и зрения,но в большинстве случае дети с врожденным ЦМВ развиваются нормально.
Врожденная цитомегаловирусная инфекция не может быть установлена и в том случае,если исследование на непосредственное определение цитомегаловируса проводилось у новорожденного позже чем через 3 недели после рождения.
--Должна ли я проверятся на ЦМВ,если я планирую беременность ?
Если вы планируете беременность,то исследование на ЦМВ поможет вам в оценить насколько надо быть осторожной во время беременности в отношении ЦМВ.
Если у вас положительный тест на IgG,то вы будете знать,что есть ничтожный шанс внутриутробной цитомегаловирусной инфекции,если тест на IgG отрицательный,то тщательно следуйте изложенным в этой статье рекомендациям.
--Как можно предотвратить заражение цитомегаловирусом во время беременности?
Наибольшая вероятность заражения во время беременности имеется у женщин с отрицательными результатами на тест с IgG (серонегативных).Никакие меры не могут полностью исключить риск заражения,но соблюдение этих правил уменьшит вероятность инфицирования ЦМВ.
1.Тщательно мойте руки с мылом в течении 15-20 минут,особенно после смены подгузников (памперсов) у грудных детей
2.Никогда не целуйте детей младше 5 лет в губы
3.Выделите для себя и маленьких детей отдельную посуду и столовые приборы
4.Если вы работаете в детских учреждениях (яслях,дет.садах) на время беременности возьмите отпуск или резко ограничьте контакты с детьми.
--Если у меня есть уже ребенок с врожденным ЦМВ,мой следующий ребенок будет также инфицирован?
Почти все женщины,которые имеют одного ребенка с врожденным ЦМВ защищены от цитомегаловирусной инфекции так как у них уже сформировался иммунитет к ЦМВ.
— Мало того, что вы один из лучших пульмонологов Европы, вы ещё и в главной группе риска сейчас по коронавирусу. Дайте, пожалуйста, рекомендации для людей вашего поколения и чуть помладше, то есть для тех, кто, как мы видим, действительно подвержен высокой летальности — и в Китае, и в Италии, и в Иране.
— Для того чтобы понять группы риска при этом заболевании: в первую очередь это люди, которые контактируют с животными, представляющими биологический резервуар. Скажем, 2002 год — это были африканские кошечки, в 2012 году это были верблюды, а сейчас немножко путается наука, до конца не установлено. Больше данных, что это определённый сорт летучей мыши — тот, который китайцы употребляют в пищу.
Вот эта летучая мышь распространяет коронавирус через испражнения. Поэтому идёт обсеменение. Допустим, рынок — морепродукты или какие-то другие продукты и так далее. Но когда мы говорим об эпидемии, то человек заражает человека. Поэтому эта фаза уже пройдена. Сейчас человек заражает человека.
Коронавирусы — очень-очень распространённая вирусная инфекция, и человек с ней встречается в жизни много-много раз. Ребёнок в течение года до десяти раз переносит заболевания, которые мы называем острой простудой. А за этой острой простудой стоят определённые вирусы.
И второе место по своей распространённости занимает как раз коронавирус. Проблема в том, что от этих вроде бы безобидных возбудителей отмахивались, никогда не могли понять причинно-следственных отношений. Если, скажем, ребёнок простыл, у него насморк, что за этим пойдёт? И так далее. Где-то в течение двух недель малыш или взрослый болеет — и всё это бесследно исчезало.
А вот в 2002-м, 2012-м и теперь уже в 2020 году ситуация качественно изменилась. Потому что те серотипы, которые стали циркулировать… они поражают эпителиальные клетки.

Эпителиальные клетки — клетки, которые выстилают дыхательные пути, желудочно-кишечный тракт и мочевыводящую систему. Поэтому у человека симптомы лёгочные, симптомы кишечные. И при исследовании анализов мочи тоже выделяют… такую нагрузку.
Но эти новые штаммы, о которых мы сейчас с вами ведём беседу, у них есть такие свойства — вступить в контакт с рецептором второго типа, ангиотензин-превращающего фермента. А с этим рецептором связано такое серьёзное проявление, как кашель.
Поэтому у больного, у которого появляются симптомы поражения нижнего отдела дыхательных путей, характерный признак — кашель. Это поражаются эпителиальные клетки самых-самых дистальных отделов дыхательных путей. Эти дыхательные трубочки очень маленькие.
— Дистальных — дальних, вы имеете в виду?
— Дальних. Маленького диаметра.
— Значит, это то, что рядом с бронхами находится у нас?
— Это бронхи, потом уже бронхиолы, респираторные бронхиолы. И когда воздух, диффузия газов идёт на поверхности альвеол, то они проходят как раз этот участок дыхательных путей.
— То есть первичный. Первое — это кашель.
— Нет, первое — это насморк, першение в горле.
— Вот говорят, что насморка как раз нет.
— Нет, это проблемы больших данных. Обработаны 74 тыс. историй болезни, и у всех ринорея (насморк. — RT) была. Когда вам так говорят — там действительно есть некоторые нюансы. Биология такая. Биологическая мишень вируса — эпителиальные клетки. Нос, орофарингеальная область, трахея, и потом мелкие бронхиолы, которые являются особенно опасными для человека. А оказалось, что, имея этот механизм, они приводят к резкому срыву иммунитета.
— Почему?
— Объяснение, которое сегодня даёт наука, — вовлекается в процесс белок, который называется интерферониндуцированный протеин-10. Вот именно с этим белком связана регуляция врождённого иммунитета и приобретённого иммунитета. Как это увидеть? Это очень глубокое поражение лимфоцитов.
— То есть у вас падают лимфоциты сразу на общем анализе?
— Да. И если там лейкоциты повысятся, тромбоциты повысятся, а более устойчивой является именно лимфопения, то есть лимфотоксический эффект самих вирусов. Поэтому сама болезнь имеет как минимум четыре очерченных этапа. Первый этап — это вирусемия. Безобидная простуда, ничего особого нет. Семь дней, девять — приблизительно в этом интервале.
А вот начиная с девятого дня по 14-й ситуация качественно меняется, потому что именно в этот период формируется вирусно-бактериальная пневмония. После поражения эпителиальных клеток в анатомическом пространстве дыхательных путей происходит колонизация микроорганизмов, в первую очередь тех, которые населяют у человека орофарингеальную область.
— То есть уже бактерии?
— Бактерии, да. Поэтому эти пневмонии всегда вирусно-бактериальные.
— Значит, вирус, так сказать, наполняет альвеолы, где всё время живут какие-то бактерии? И они сами по себе где-то живут, в каком-то количестве?
— Вообще, мы считаем, что нижний отдел дыхательных путей стерилен. Вот так устроен механизм защиты, что именно нижний отдел дыхательных путей.
— Там ничего нет.
— Не заселён. Когда вирус внедрился и он нарушил этот барьер, там, где была стерильная среда в лёгких, начинают колонизироваться, размножаться микроорганизмы.
— То есть не вирус вызывает пневмонию? Всё равно пневмонию вызывают бактерии, конечно.
— Ассоциации: вирус — бактерии.
— Да.
— Окно, где врач должен проявить своё искусство. Потому что часто вирусемический период — как лёгкое заболевание, как лёгкая простуда, недомогание, насморк, лёгкая температура небольшая, субфебрильная. А вот период, когда кашель усилился и когда появилась одышка, — это два признака, которые говорят: стоп, это уже качественно другой пациент.
Если эта ситуация не контролируется и болезнь прогрессирует, то наступают уже более серьёзные осложнения. Мы называем это респираторным дистресс-синдромом, шоком. Человек дышать самостоятельно не может.

— Отёк лёгких?
— Понимаете, отёков лёгкого много, на самом деле, бывает. Если быть точными, мы это называем некардиогенный отёк лёгкого. Если, скажем, кардиогенный отёк лёгкого мы можем лечить с помощью определённых лекарственных препаратов, то этот отёк лёгкого можно лечить только с помощью машины механической вентиляции лёгких или продвинутых методов, таких как экстракорпоральная гемоксигенация.
Если человек переносит эту фазу, то иммуносупрессия, вызванная поражением приобретённого и врождённого иммунитета, становится губительной и у больного присоединяются такие агрессивные возбудители, как синегнойная палочка, грибы. И те случаи смерти, которые произошли, — у 50%, которые длительно находились на искусственной вентиляции лёгких, альвеолы все заполнены грибами.
Грибы появляются тогда, когда глубокая иммуносупрессия. Какая же судьба человека, который перенес всё это? То есть он перенёс вирусемию, он перенёс вирусно-бактериальную пневмонию, он перенёс респираторный дистресс-синдром, некардиогенный отёк лёгкого и он перенёс септическую пневмонию. Он будет здоров или нет? И вот, собственно говоря, сегодня мир озабочен именно этим: какая судьба у человека, у тех вот 90 тыс. китайцев, которые перенесли коронавирусную инфекцию?

— 90 тыс. — они сами по себе перенесли, они на ИВЛ не лежали, грибов у них не было. ОРЗ и ОРЗ.
— Но сама проблема — она очень важна. Потому что практическая медицина стоит перед фактом резкого роста так называемых лёгочных фиброзов. И вот у этой группы лиц, перенёсших коронарную инфекцию, в течение года формируется фиброз лёгкого.
— То есть когда лёгочная ткань уплотняется?
— Да. Как жжёная резина. Лёгкое становится как жжёная резина, если аналогию проводить.
— К вам попадает пожилой человек, у него точно диагностирован коронавирус. И он ещё не на девятом дне, то есть его ещё не надо на ИВЛ класть. Как вы его будете лечить?
— Вы знаете, в чём дело: мы таких больных пока не лечим, потому что нет лекарственных препаратов, лекарственных средств, которые надо применять в этой фазе. Панацеи нет. Потому что лекарство, которое бы действовало на вирусемию, на вирусно-бактериальную фазу, на некардиогенный отёк лёгкого, на сепсис, — панацея, такого не может быть.
Потому что, если вернуться к опыту 2002 года, когда увидели уязвимость медицинского персонала, врачам, сёстрам рекомендовали применять тамифлю и озельтамивир — антигриппозный препарат. И при определённых серотипах коронавируса, действительно, механизм внедрения в клетку тот же, как при вирусах гриппа. Поэтому показали, что эти препараты могут защитить лиц, где высокий риск развития этого заболевания.
Или же у него выявляется носительство вируса, ему дают эти препараты и так далее. Но это, я ещё раз хочу сказать, серьёзной доказательной базы не имеет. Ситуация, которая наиболее грозная, потому что она определяет судьбу человека. Простудное состояние — одно дело. А другое дело — когда вирусно-бактериальная пневмония, это принципиально другая вещь.
И здесь очень важно подчеркнуть, что только антибиотиками помочь такому больному проблематично. Здесь должна быть обязательно комбинированная терапия, которая включает средства, стимулирующие иммунитет. Это очень важный момент.
— А что вы имеете в виду? То есть, условно говоря, вы ему пропишете амоксиклав с каким-то иммуномодулятором?
— Да, обычно назначают цефалоспорины четвёртого поколения, не амоксиклав, в комбинации с ванкомицином. Такая комбинация — широкая, потому что очень быстро идёт смена грамположительной и грамотрицательной флоры. А вот какой иммуномодулирующий препарат назначить — это вопрос для научного исследования.
Итак, мы понимаем, что резко пострадает иммунитет. Мы понимаем высокую уязвимость человека к той инфекции, которая у него начинает колонизироваться в дыхательных путях. Поэтому, к сожалению, мы как бы чёткой линии не имеем. Но то, что реально может помогать таким больным в такой ситуации, — это иммуноглобулины. Потому что это заместительная терапия.
И поэтому таким больным, чтобы не разыгрался сепсис, по крайней мере, они не вошли в фазу сепсиса, назначают высокие иммуноглобулины. Американские врачи применили средство у своего больного, которое применяют при лихорадке Эбола. Это препарат группы, аналог нуклеозидов. Это группа препаратов, которые применяют при герпесе, при цитомегаловирусе и так далее.
— То есть это противовирусная или поддерживающая антивирусную терапию, да?
— Нет, это препарат, который действует всё-таки на те механизмы в клетке, которые противостоят репликации вируса. Вот у меня в руках (фотография президента США Дональда Трампа. — RT). Он собрал всю верхушку, которая могла бы высказаться по препаратам перспективным. Два вопроса, которые он поставил, он готовился к этой конференции. Первый вопрос: насколько учёные Соединенных Штатов Америки готовы к внедрению вакцины?
— Полтора года.
— Да, совершенно точно. Это два года. Он говорит: что в таком случае? Есть ли у страны препараты, которые могли бы защитить? И, собственно говоря, они сказали: да, такой препарат есть.
— Что?
— Что это за препарат? Он называется ремдесивир.

— Давайте посмотрим его.
— Вот учёные сказали, учитывая тот опыт, который есть, и обсуждения и так далее. Хотя, конечно, есть другие препараты, которые активно изучаются. Вообще, это направление очень интересное: что, собственно говоря, считается перспективным. Перспективным считается применение стволовых мезенхимальных клеток. Но в какой стадии?
— Слушайте, вот вы, как человек, который много лет этим занимается, от астмы до пневмонии, можете как-то попытаться спрогнозировать развитие этой эпидемии, например, в России?
— Вы знаете, в чём дело? Я хочу сказать, что, если Россию сравнивать с окружающим миром и брать коронавирус 2002 года, там ни одного больного не было.
— Может, мы просто не диагностировали?
— Он у нас вообще единственный сертифицированный, да?
— Вирус уже в России, как бы санэпидемслужба ни старалась. Как вы считаете, как он будет развиваться? Закончится ли он весной, например, с приходом лета?
— Знаете, мне кажется, картинка повторяет то, что было тогда. Это, если вы помните.
— Тогда — в 2002 году? То есть когда был SARS?
— Он отличается на 16, по-моему, нуклеозидов.
— Если пойдёт по этому сценарию, то нужно сказать, что где-то в апреле-мае эта проблема уже остро, по крайней мере, стоять не будет.
— Просто из-за сезонного прекращения респираторных инфекций?
— Да. Климатический фактор, целый ряд других факторов. Сейчас, когда беда, конечно, к нам приходит не из Китая, а из Европы. Те, кто возвращается из этих стран, в первую очередь из Италии, сегодня, запомните: Урбани. Это он сделал очень многое. Я считаю, это просто подвиг врача, который так много сделал. Это был вирусолог из Милана.

— Тогда, в 2002 году?
— Он эксперт ВОЗ, я с ним встречался по линии Всемирной организации здравоохранения. Он в списке был эксперт по коронавирусам. И тогда его направили в Ханой. Они распределились, ему достался Вьетнам. И во Вьетнаме, когда он приехал, была паника. Врачи перестали выходить на работу. Медицинский персонал тоже. Больные есть, а врачебного и медицинского персонала нет.
Он оценил ситуацию. С трудом ему удалось переломить её, снять эту паническую ситуацию, которая была тогда в госпитале. Ну а самое главное — он стал общаться с правительством и сказал: закрыть страну на карантин. Вот откуда всё это пошло. Это пошло от Урбани. Они начали артачиться.
— Вьетнамцы?
— Да, Вьетнам. Что это экономика, туризм и так далее. В общем, он нашёл эти слова, он убедил. И Вьетнам — первая страна, которая вышла из этого. И он посчитал, что его работа закончена. Он набрал материал для вирусологического обследования и сел в самолёт, который летел в Бангкок.
Там американские вирусологи, они должны были встретиться. А когда уже полетел, понял, что заболел. Заболел так же, как эти несчастные вьетнамцы в том госпитале. И он стал всё записывать, описывать. Вот время такое-то — моё самочувствие такое-то.
— Лететь три часа?
— Какие рекомендации вы можете дать человеку, который обнаруживает у себя… Ну то есть мы уже договорились, что вирус в общей популяции. Мы уже не можем, на самом деле, его контролировать.
— Да. Значит, такие обывательские рекомендации?
— Да, именно так.
— В первую очередь — это всё-таки хороший уход за слизистой носа и орофарингеальной областью.
— То есть покупаешь морскую воду и себе…
— Да, и промываешь тщательно. Но лоры — они очень хорошо показывают эффективный лаваж. То есть должно прийти всё-таки ощущение свободного дыхания. Второе место — это орофарингеальная область за увулой. И там тоже нужно хорошо сделать лаваж орофарингеальной области.
— То есть надо прыскать не только в нос, но и глубоко в гортань?
— Да, и прополаскивать. И не лениться делать до тех пор, пока не придёт чувство чистых, хороших дыхательных путей. Из всех путей это средство самое эффективное. Я бы посоветовал тем людям, которые могут себе позволить, приобрести небулайзер или.
— То есть такой аэрозольный, да? С ультразвуком?
— Да. И он позволяет гигиену именно верхней части дыхательных путей доводить до хорошего состояния. Когда присоединяется кашель — желательно всё-таки применить те лекарства, которые мы прописываем больным бронхиальной астмой. Это или беродуал, или вентолин, или сальбутамол. Потому что именно эти препараты улучшают мукоцилиарный клиренс, снимают спазм.
— То есть отхаркивающий? АЦЦ?
— Да, АЦЦ и флуимуцил. И чего нельзя делать — это применять глюкокортикостероиды. Этот вирус, его репликация резко нарастает.
— Что это значит?
— Глюкокортикостероиды — это преднизолон, метилпреднизолон, дексаметазон, метаметазон.
— То есть не надо колоть гормоны, условно говоря, если у вас вирусная инфекция?
— Есть ингаляционные стероиды. Но есть больные с астмой, которые заболели, находятся на этой терапии. Это уже как бы индивидуальные решения. Конечно, 2020-й войдёт в историю медицины как новая болезнь. Мы должны это признать, что мы поняли новую болезнь. Две новые пневмонии пришли. Это пневмония, которая вызывается электронными сигаретами, вейпами, и сейчас в Соединённых Штатах от этого умерли.
— . несколько тысяч подростков. Да, это известный факт, и чем лечить — непонятно. Сажаешь на ИВЛ — они умирают сразу.
— Да. Вы понимаете, в чём проблема-то? Вот у них развиваются те изменения в лёгких, которые возникают при этом. Они вроде бы схожие. Это респираторный дистресс-синдром, о котором мы с вами ведём разговор. В литературе поднимаются очень серьёзные вопросы: роль коронавирусов в трансплантологии. Одна из проблем — это облитерирующий бронхиолит, который возникает особенно при пересадке.
— Пересадке лёгких?
— Да, лёгких и костного мозга. Стволовых клеток. Вот, собственно говоря, всё хорошо сделано, всё нормально, человек ответил на эту терапию, а начинает нарастать проблема дыхательной недостаточности. И причину этих бронхиолитов поймали — это коронавирус. То есть новое знание пришло.
Читайте также:


